-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Transplantace jater pro hepatocelulární karcinom, dlouhodobé přežití a faktory ovlivňující rekurenci tumoru (zkušenosti jednoho centra)
Liver transplantation for hepatocellular carcinoma, long-term outcomes and risk factors of tumour recurrence (single-centre experience)
Background and aims:
Liver transplantation (OLT) is currently the treatment of choice for hepatocellular carcinoma (HCC) in cirrhotic liver, because it removes the tumour as well as the cirrhotic tissue with malignant potential. However, OLT improves survival especially in patients with a small tumour, who have a low risk of tumour recurrence after OLT. The aim of our study was to retrospectively analyse survival of patients who underwent liver transplantation for HCC in our centre and to identify the risk factors of tumour recurrence after OLT.Patient characteristics:
Eighty-one adult patients who underwent liver transplantation in our centre for HCC (HCC group) were enrolled into the study. They all complied with the extended indication criteria (HCC < 6.5 cm) and 61/81 also met the Milan criteria (HCC < 5 cm). The control group consisted of 606 patients transplanted for end-stage liver disease without evidence of tumour (Ci group) within the same period.Results:
1-, 3 - and 5-year overall survival was worse in HCC patients compared with the Ci group (HCC 77%, 70% and 66% vs Ci 93%, 90% and 87%, p < 0.001). Long-term survival is comparable with foreign transplant centres in the Metroticket Group (5-year survival 71.2% and 10-year survival 58.4% if the extended criteria are met). 13/81 (16%) patients experienced HCC recurrence, and the median time to recurrence after OLT was 182 days (101–2322).Conclusions:
Higher AFP value before OLT, the largest node size and proved angioinvasion represented the independent predictive factors of tumour recurrence. To achieve even better results, regular screening of risk groups of cirrhotic patients resulting in detection of small tumours and their early referral to OLT is crucial.Key words:
liver transplantation – hepatocellular carcinoma – recurrence – survival – cirrhosis
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
6. 3. 2014Accepted:
7. 4. 2014
Autoři: R. Šenkeříková 1; S. Fraňková 1
; J. Šperl 1
; M. Oliverius 2; J. Froněk 2; E. Kieslichová 3
; H. Filipová 4; D. Kautznerová 4; E. Honsová 5; P. Trunečka 6; J. Špičák 1
Působiště autorů: Klinika hepatogastroenterologie, IKEM, Praha 1; Klinika transplantační chirurgie, IKEM, Praha 2; Klinika anesteziologie, resuscitace a intenzivní péče, IKEM, Praha 3; Pracoviště radiodiagnostiky a intervenční radiologie, IKEM, Praha 4; Pracoviště klinické a transplantační patologie, IKEM, Praha 5; Transplantcentrum, IKEM, Praha 6
Vyšlo v časopise: Gastroent Hepatol 2014; 68(2): 139-145
Kategorie: Hepatologie: původní práce
Souhrn
Úvod a cíle:
Transplantace jater (OLT) pro hepatocelulární karcinom (HCC) v cirhotických játrech je ideální léčebnou metodou, která odstraňuje tumor i cirhotická játra s dalším maligním potenciálem. Významné zlepšení přežití přináší transplantační léčba zejména pacientům s malým tumorem a s nízkým rizikem rekurence po OLT. Cílem práce bylo retrospektivně zhodnotit přežití pacientů, kteří v našem centru podstoupili OLT pro HCC a identifikovat rizikové faktory podporující rekurenci tumoru po OLT.Soubor pacientů:
Do studie bylo zařazeno 81 dospělých pacientů transplantovaných v našem centru pro HCC (skupina HCC). Všichni splnili tzv. extendovaná indikační kritéria (HCC < 6,5 cm) a 61/81 i tzv. Milánská kritéria (HCC < 5 cm). Kontrolní skupinu tvořilo 606 pacientů, kteří ve stejném období podstoupili OLT pro jaterní cirhózu bez tumoru (skupina Ci).Výsledky:
Celkové jedno-, tří - a pětileté přežití bylo u pacientů s HCC horší ve srovnání s Ci skupinou (HCC 77 %, 70 % a 66 % vs Ci 93 %, 90 % a 87 %; p < 0,001). Dlouhodobé přežití našich HCC pacientů bylo srovnatelné se zahraničními centry zařazenými do tzv. Metroticket Group (přežití pět let 71,2 % a 10 let 58,4 % při splnění extendovaných indikačních kritérií). K rekurenci HCC po OLT došlo u 13/81 pacientů (16 %). Medián doby mezi OLT a rekurencí byl 182 dnů (101–2 322).Závěr:
Vyšší hodnota AFP před OLT, velikost největšího ložiska a přítomnost angioinvaze byly nezávislými prediktivními faktory rekurence. Pro další zlepšení výsledků je zásadní pravidelný screening rizikových skupin cirhotiků detekující malé tumory a jejich časné odeslání k OLT.Klíčová slova:
transplantace jater – hepatocelulární karcinom – rekurence – přežití – cirhóza
Hepatocelulární karcinom (HCC) je nejčastějším primárním tumorem jater. Hlavním a společným rizikovým faktorem vzniku HCC je cirhotická přeměna jaterního parenchymu, přičemž největší riziko představuje cirhóza, která vznikla na podkladě chronické infekce virem hepatitidy B či C nebo na podkladě alkoholické choroby jater či nonalkoholické steatohepatitidy [1,2]. V posledních desetiletích incidence HCC celosvětově vzrůstá, což je dáno vysokou prevalencí chronické hepatitidy B v rozvojových zemích, v rozvinutých zemích se naopak na vzestupu incidence HCC podílí zejména chronická hepatitida C a nonalkoholická steatohepatitida [1]. V ČR se HCC diagnostikuje přibližně u 500 obyvatel za rok [3]. Radikální léčbou časného HCC v jaterní cirhóze může být chirurgická resekce nebo transplantace jater. Resekce je možná jen u pacientů s plně kompenzovanou jaterní cirhózou bez významné portální hypertenze. Transplantace jater představuje optimální řešení, neboť odstraňuje samotný nádor i nemocnou tkáň s potenciálem další maligní přeměny a zároveň řeší i problémy dysfunkce jater a portální hypertenze [4,5].
V době rychlého rozvoje transplantace jater v 80. letech tvořila nádorová onemocnění nejvýznamnější indikační skupinu. Pacienti s tumorem v málo pokročilé cirhóze bez významné portální hypertenze a bez koagulopatie představovali ideální kandidáty s nízkou operační mortalitou. Dlouhodobé přežití po transplantaci však nebylo uspokojivé pro vysoký počet rekurencí tumoru po transplantaci. Zásadní zlom nastal poté, co Bismuth et al navrhli první indikační kritéria transplantace jater pro HCC [6], která byla naopak velmi restriktivní. Za vhodné kandidáty byli považováni jen pacienti s tumorem do 3 cm. V dalších letech se indikační kritéria znovu rozšiřovala, v roce 1996 Mazzaferro et al publikoval retrospektivní analýzu souboru pacientů indikovaných k transplantaci jater pro HCC [7]. Ve zmíněné publikaci byli identifikováni podle nálezu v explantovaných játrech pacienti s dobrou prognózou a nízkým rizikem rekurence HCC po transplantaci. Studie prokázala, že dobrou prognózu po transplantaci jater mají pouze pacienti s malým HCC. Kritéria určující pojem malý HCC posléze vstoupila do obecného povědomí jako tzv. Milánská kritéria. Milánská kritéria byla definována jako jedno ložisko do velikosti 5 cm nebo maximálně tři tumory menší než 3 cm, bez známek vaskulární invaze a s vyloučením generalizace onemocnění. U takto definovaných nádorů je přežití pacientů podobné jako přežití pacientů indikovaných k transplantaci pro cirhózu bez HCC [7]. Kritéria byla však stále výrazně restriktivní a splnila je jen malá část pacientů odeslaných k transplantaci jater pro HCC, většině referovaných pacientů s HCC byl přístup k transplantaci jater odmítnut. Uplatnění Milánských kritérií vedlo k odmítnutí transplantační léčby i u pacientů, kterým by transplantace jater přinesla zlepšení přežití ve srovnání s konzervativní léčbou. Další rozšíření Milánských kritérií za podmínky přesné radiologické diagnostiky vedlo v několika monocentrických studiích jen k mírnému a ještě přijatelnému zhoršení dlouhodobého přežití po transplantaci. V současné době se indikace k transplantaci jater nejčastěji posuzuje dle tzv. kritérií UCSF (University of California, San Francisco), která jsou založena na sestavě publikované Yao et al [8]. UCSF kritéria (někdy nazývaná též jako extendovaná kritéria) dovolují indikovat k transplantaci jater nemocné s jedním uzlem HCC do 6,5 cm nebo s maximálně třemi uzly, z nichž největší ložisko má velikost do 4,5 cm a součet velikostí všech uzlů je menší než 8 cm, podmínkou je nepřítomnost vaskulární invaze. Ve studii publikované Duffy et al [9] měli pacienti splňující UCSF kritéria srovnatelné pětileté přežití s pacienty splňujícími Milánská kritéria (64 % vs 79 %; p = 0,06) při hodnocení splnění kritérií jen dle velikosti a počtu ložisek na zobrazovacích metodách (71 % vs 86 %; p = 0,057) a při hodnocení splnění kritérií dle velikosti ložisek i přítomnosti angioinvaze dle histologického nálezu v explantovaných játrech.
Při hledání vztahu mezi velikostí a počtem ložisek na jedné straně a pravděpodobností rekurence nádoru, resp. přežitím pacientů po transplantaci na straně druhé se užívá pojem „Metro-ticket koncept“ – čím dále jedete, tím vyšší cenu zaplatíte, tedy čím rozsáhlejší nádor léčíte transplantací jater, tím je vyšší riziko rekurence tumoru po transplantaci [4]. S rostoucí velikostí největšího tumoru stoupá riziko přítomnosti vaskulární invaze a nízké diferenciace, které byly identifikovány jako nezávislé rizikové faktory rekurence HCC po transplantaci jater [10].
Cílem naší studie bylo zhodnotit výsledky transplantace jater u pacientů se známým HCC v našem centru a identifikovat rizikové faktory rekurence tumoru po transplantaci.
Metodika
Retrospektivně jsme zhodnotili klinická a laboratorní data a parametry tumoru u 81 dospělých pacientů, kteří podstoupili v našem centru transplantaci jater pro HCC (skupina HCC). U 80 pacientů se jednalo o HCC v cirhóze a jeden pacient měl HCC v necirhotických játrech. Kontrolní skupinu tvořilo 606 dospělých pacientů, kteří ve stejném období podstoupili transplantaci jater pro nevratné selhání jater při jaterní cirhóze různé etiologie (skupina Ci). Hodnocené skupiny pacientů byly vybrány z celkového počtu 868 pacientů, kteří v době od ledna 1995 do srpna 2012 podstoupili v našem centru ortotopickou transplantaci jater (OLT). Z retrospektivního hodnocení bylo vyřazeno 181 pacientů transplantovaných pro akutní jaterní selhání, metabolická onemocnění bez cirhotické přestavby jaterního parenchymu, pro polycystózu jater či pro tumory jiné než HCC, děti mladší 18 let a pacienti s jaterní cirhózou, kterým byl HCC nalezen náhodně až po transplantaci (tzv. incidentální HCC) při histologickém vyšetření explantovaných jater.
Diagnóza HCC před transplantací jater byla stanovena pomocí dvou zobrazovacích metod (sonografie břicha a kontrastní CT jater nebo MR jater) a dalšího kritéria: vysoké hodnoty alfa-fetoproteinu (AFP) a/nebo potvrzena cílenou biopsií z ložiska u pacientů s nejednoznačným nálezem zobrazovacích metod. Cílená biopsie ložiska nebyla prováděna standardně u všech pacientů před zařazením do čekací listiny, ale dle indikačního protokolu měla být provedena u pacientů, kteří velikostí tumoru nebo počtem ložisek přesahovali Milánská kritéria. Generalizace onemocnění byla vyloučena pomocí CT hrudníku, CT mozku a scintigrafie skeletu. V průběhu let se vyvíjela indikační kritéria k transplantaci jater pro HCC. Před rokem 2008 byli k OLT pro HCC indikováni v našem centru jen pacienti splňující velikostí a počtem ložisek Milánská kritéria a od roku 2008 byli indikováni i pacienti přesahující Milánská kritéria, ale splňující kritéria UCSF. Splnění Milánských i UCSF kritérií bylo hodnoceno v době zařazení do čekací listiny dle velikosti a počtu ložisek HCC při kontrastním CT vyšetření a v explantovaných játrech následně na základě velikosti a počtu tumorů a přítomnosti angioinvaze.
Statistika
Výsledky jsou prezentovány jako průměry a směrodatné odchylky, mediány a rozsahy hodnot nebo jako četnosti. T-test nebo Mann-Whitney test byl použit pro srovnání průměrů, chí-kvadrát test pro porovnání četností. Významné rizikové faktory z jednorozměrné analýzy byly dále hodnoceny pomocí logistické regresní analýzy. Cut-off points pro spojité veličiny byly získány z Receiver Operating Characteristic (ROC) křivek. Analýza přežití byla hodnocena pomocí Kaplan-Meier křivek, které pak byly porovnány pomocí log-rank testu. Porovnání významnosti křivek v jednotlivých bodech bylo testováno pomocí konfidenčních intervalů. Hodnota p < 0,05 byla považována za statisticky významnou. Statistická analýza byla provedena pomocí JMP 10.0.0.
Výsledky
Pacienti indikovaní k transplantaci jater pro HCC se statisticky významně lišili od pacientů indikovaných pro jaterní cirhózu bez HCC v zastoupení pohlaví a věku (p < 0,001). Charakteristika a srovnání obou skupin v době zařazení do čekací listiny (waiting list; WL) je uvedena v tab. 1. Pokročilost jaterního onemocnění podle Child-Pugh klasifikace (CPS) a MELD skóre (Model for End-stage Liver Disease) byla signifikantně nižší u pacientů s HCC v době zařazení na čekací listinu ve srovnání s Ci skupinou (CPS: 8 ± 2 vs 9 ± 2; p < 0,001; MELD: 12 ± 5 vs 16 ± 5; p < 0,001). Medián AFP byl ve skupině HCC 17 µg/l (3–1 750) vs 4 µg/l (0,5–474) v Ci skupině (p < 0,001). Pacienti s HCC strávili kratší dobu na čekací listině, medián 55 dnů (rozpětí 2–583) než pacienti Ci skupiny, medián 84 dnů, (rozpětí 0–1 331), rozdíl ale nebyl signifikantní (p = 0,075). Nejvíce HCC bylo diagnostikováno v jaterní cirhóze na podkladě chronické infekce virem hepatitidy C a B a v alkoholické jaterní cirhóze, žádný HCC nebyl nalezen u cholestatických cirhóz (tab. 1).
Tab. 1. Charakteristika pacientů v době zařazení na čekací listinu k transplantaci jater. Tab. 1. Patient characteristics at the time of enlistment for liver transplantation. 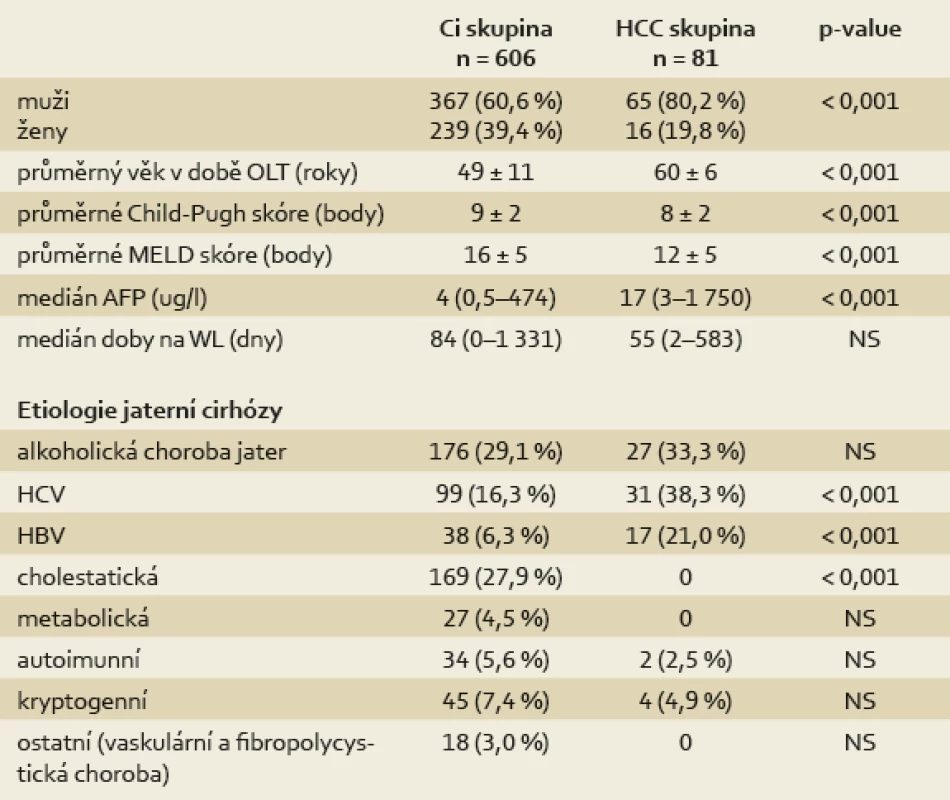
Na základě velikosti a počtu ložisek HCC dle kontrastního CT zobrazení splnili všichni pacienti v HCC skupině UCSF kritéria v době zařazení na WL a 61 pacientů z 81 (75,3 %) i Milánská kritéria (tab. 2). U 55 % (11/20) pacientů s HCC, který přesahoval Milánská kritéria, ale splňoval UCSF kritéria, byla provedena cílená biopsie z ložiska, u sedmi z nich byl potvrzen dobře nebo středně diferencovaný HCC (grade 1 nebo 2) bez přítomnosti mikroangioinvaze a u čtyř pacientů nebyly v získaném vzorku zachyceny nádorové struktury. U zbylých 9/20 pacientů bylo od provedení biopsie upuštěno pro vysoké riziko výkonu (riziko poranění velkých cév či subkapsulární uložení tumoru). Podle nálezu v explantátu (tab. 3) splnilo UCSF kritéria jen 42 pacientů z 81 (51,9 %) a Milánská kritéria jen 31 z 81 pacientů (38,3 %). Důvodem nesplnění UCSF kritérií v explantátu byl nález angioinvaze ve 32 případech, překročení počtu ložisek v pěti případech a ve dvou případech byla kritéria nesplněna z důvodu překročení velikosti ložisek.
Tab. 2. Charakteristika tumorů podle nálezu při dynamickém CT zobrazení před transplantací jater. Tab. 2. Tumour characteristics according to dynamic CT finding before liver transplantation. 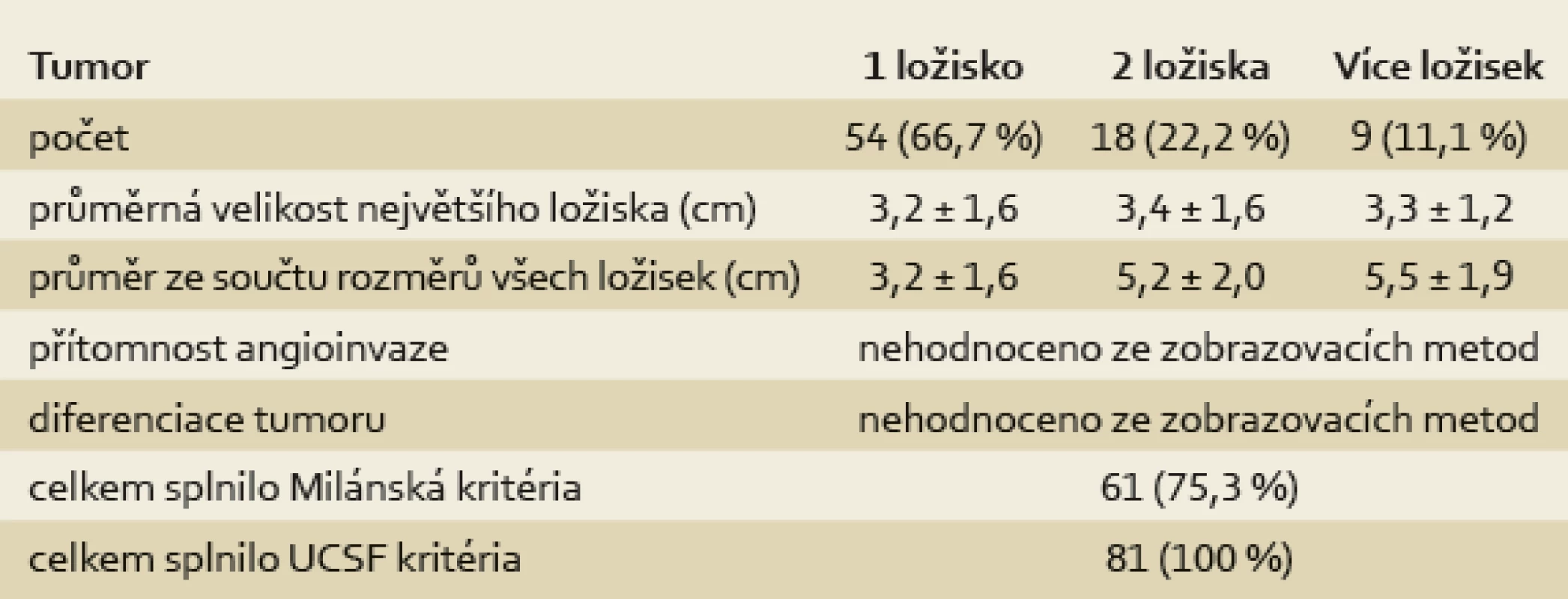
Tab. 3. Charakteristika tumorů podle nálezu v explantovaných játrech. Tab. 3. Tumour characteristics according to the finding in the explanted liver. 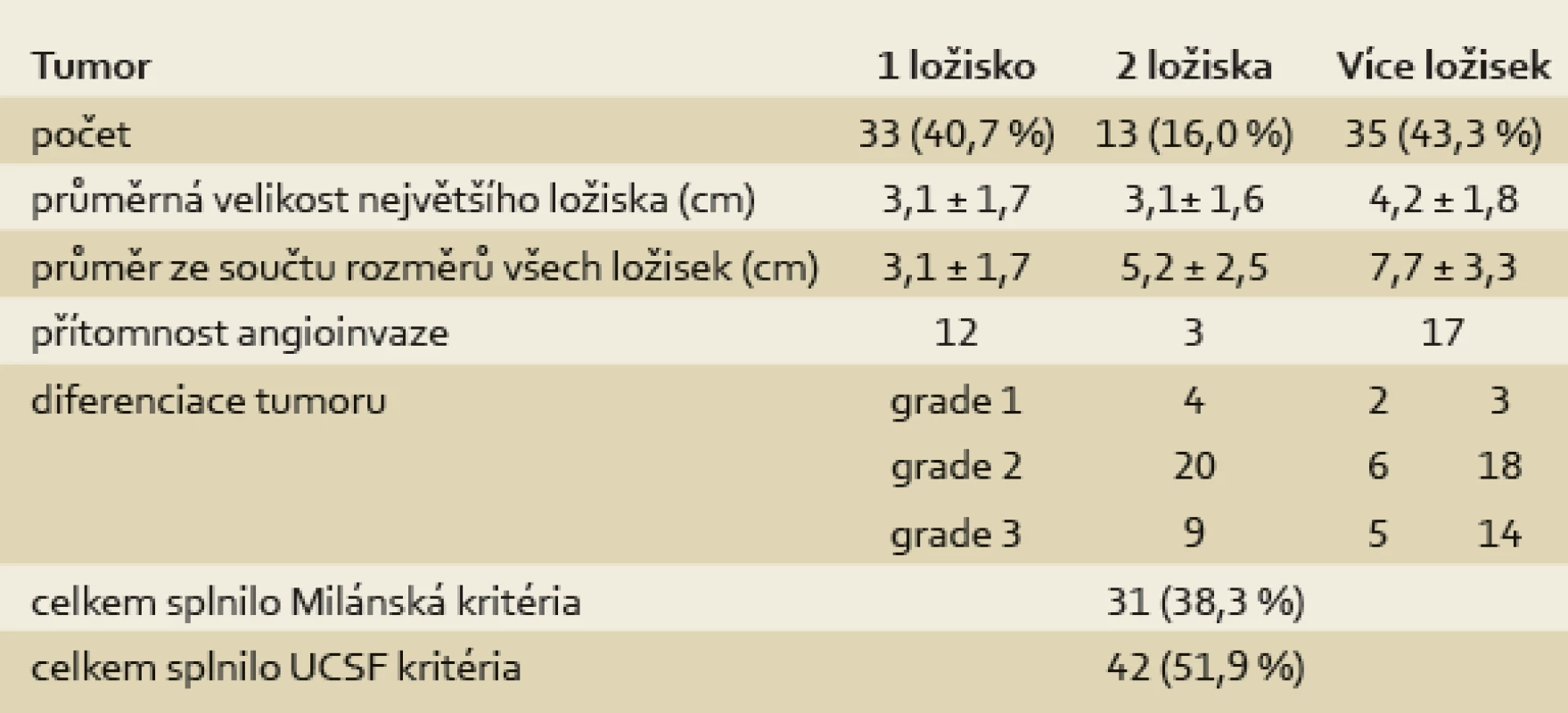
Celkové jedno-, tří - a pětileté přežití bylo u pacientů s HCC horší ve srovnání s Ci skupinou (HCC: 77 %, 70 % a 66 % vs Ci pacienti: 93 %, 90 % a 87 %; p < 0,001) (graf 1). Rozdíl byl statisticky významný ve všech výše zmíněných letech i v celkových křivkách hodnocených log-rank testem (tab. 4). Obě skupiny se lišily v přežití i po adjustaci na věk pomoci Coxova regresního modelu na hladině významnosti p = 0,0008. Jedno-, tří - a pětileté přežití pacientů s HCC bez nálezu rekurence tumoru (recurrence-free survival – RFS) bylo 74 %, 69 % a 62 %.
Graf 1. Celkové přežití pacientů transplantovaných pro HCC a pacientů s jaterní cirhózou bez tumoru (Ci skupina). Graph 1. Overall survival in patients transplanted for HCC vs those with liver cirrhosis without tumor (Ci group). 
Tab. 4. Celkové přežití pacientů transplantovaných pro HCC a pacientů s jaterní cirhózou bez tumoru (Ci skupina). Tab. 4. Overall survival in patients transplanted for HCC vs. those with liver cirrhosis without tumour (Ci group). 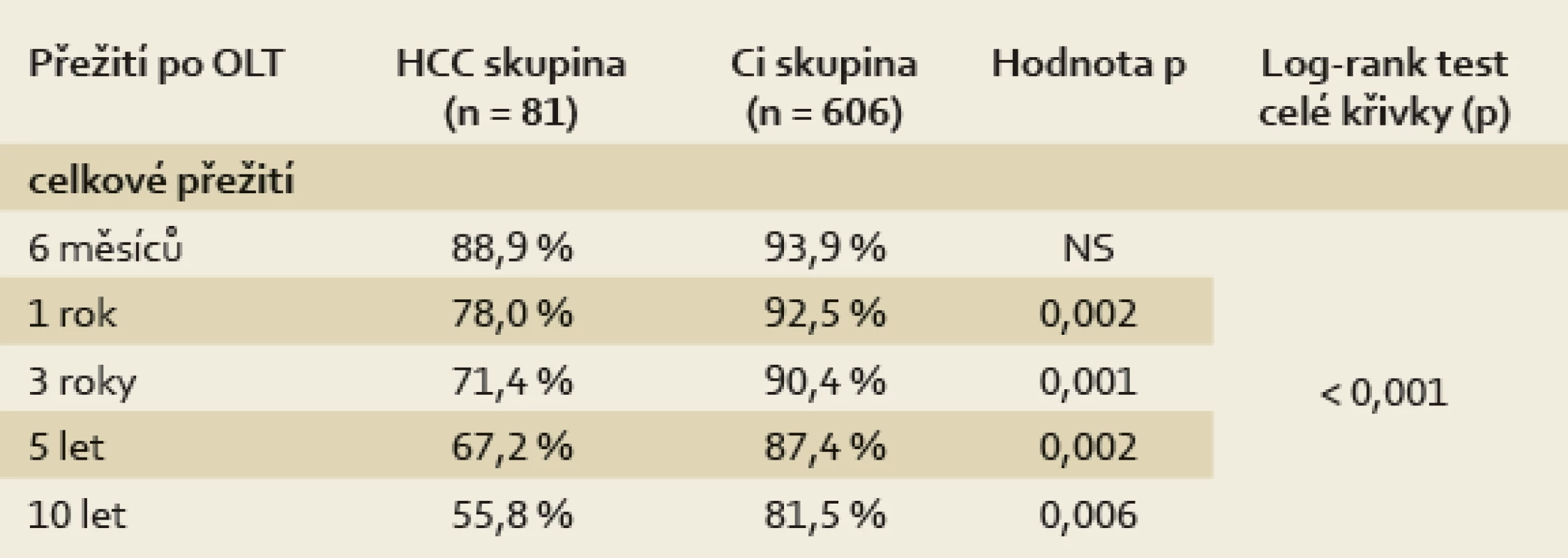
Z analyzovaných veličin (pohlaví, věk, Child-Pugh skóre, MELD skóre, doba na WL, hodnota AFP, etiologie jaterního onemocnění, počet ložisek, velikost největšího ložiska, součet průměrů všech ložisek, přítomnost angioinvaze, diferenciace tumoru, splnění Milánských kritérií) byla prokázána negativním prognostickým faktorem celkového přežití pouze nízká diferenciace tumoru dle nálezu v explantátu (grade 3 vs grade 1 a 2; p = 0,03).
U třinácti pacientů (13/81, 16 %) došlo k rekurenci HCC po transplantaci jater. Jedenáct ze třinácti pacientů s rekurencí HCC nesplnilo dle nálezu v explantátu UCSF kritéria. Medián doby mezi zjištěním rekurence a transplantací jater byl 182 dnů (101–2 322). Z výše uvedených analyzovaných veličin byla logistickou regresní analýzou potvrzena velikost největšího ložiska (OR 1,92, 95 % IS 1,17–3,15; p = 0,009) a přítomnost mikroangioinvaze (OR 5,56, 95 % IS 1,23–25,1; p = 0,024) nezávislými prediktivními faktory rekurence HCC po transplantaci jater. Na hranici statistické významnosti byla v univariantní analýze i průměrná vyšší hodnota AFP před transplantací jater (386 vs 204 µg/l; p = 0,048) a špatná diferenciace tumoru (grade 3 vs grade 1 a 2; p = 0,056).
Diskuze
Předložené výsledky dlouhodobého přežití pacientů po transplantaci dokládají, že program transplantace jater pro HCC v našem centru dosahuje výsledků srovnatelných se zahraničními centry.
Mazzaferro et al v multicentrické retrospektivní studii tzv. „Metro-ticket Group“ zhodnotili výsledky transplantace jater pro HCC ve 36 především evropských centrech. Do studie bylo zařazeno celkem 1 556 pacientů s HCC, 444 (28,5 %) pacientů splňovalo Milánská kritéria a jejich pětileté a desetileté přežití bylo 73,3 % a 69,6 %. Dalších 283 (18,2 %) pacientů mělo tumor větší než požadují Milánská kritéria, ale splňovalo kritéria extendovaná, a jejich pěti - i desetileté přežití po transplantaci jater bylo 71,2 % a 58,4 %, tj. srovnatelné s první skupinou [10]. Dlouhodobé přežití pacientů indikovaných k transplantaci jater pro HCC je vždy horší než přežití pacientů indikovaných pro jaterní cirhózu bez tumoru kvůli rekurencím HCC. Na druhou stranu transplantace jater poskytuje pacientům s HCC vynikající naději na delší přežití ve srovnání s konzervativní léčbou. Při konzervativní léčbě nepřesahuje obvyklé přežití pacientů s HCC jeden rok [11]. Výsledky transplantace jater pro HCC nelze plně srovnávat s výsledky radikálních resekcí jater. Při rozhodování mezi resekcí a transplantací naše centrum dodržuje tzv. Barcelonskou klasifikaci HCC [12], kdy pacienti indikovaní k léčbě resekcí jater nemají známky jaterní dysfunkce a portální hypertenze.
Narůstající podíl transplantací jater pro HCC vyvolává ve světě diskusi o nejvhodnější alokaci štěpu. V centrech, kde je pořadí pacientů v čekací listině určeno výhradně hodnotou MELD skóre, se pacientům s HCC při zařazení do čekací listiny MELD skóre arbitrárně navyšuje dle velikosti nádoru a následně dle délky čekání, jinak by neměli šanci na získání štěpu v kompetici s pacienty s více pokročilou cirhózou bez tumoru. Léčba pacientů s HCC transplantací jater významně vyčerpává dostupné zdroje dárcovských orgánů a doba strávená na čekací listině ve skupině cirhotiků bez tumoru se neúměrně prodlužuje. Zvýhodněni tak jsou pacienti s horší dlouhodobou prognózou po transplantaci a prodloužení čekací doby ve skupině kandidátů bez HCC zhoršuje i přežívání v této skupině. Vzhledem k limitovaným zdrojům a zvyšujícím se nárokům na čekací listinu nemá problém alokací ideální řešení. V našem centru je pro potřeby alokace štěpu dysfunkce jater klasifikována dle závažnosti komplikací do čtyř stupňů (1: pacient čekající doma, 2: na standardním lůžku v nemocnici, 3: na lůžku intenzivní péče, 4: fulminantní selhání, urgentní příjemce). Pacientům s HCC se stupeň dysfunkce navyšuje o jeden stupeň až po šesti měsících čekání. Náš systém vystihuje situaci našeho centra, tj. kratší čekací doba a menší čekací listina. Doba strávená na čekací listině je u našich pacientů s HCC také kratší než u pacientů s cirhózou bez tumoru, rozdíl ale není signifikantní.
Pacienti s HCC byli v našem centru do konce roku 2008 zařazováni do čekací listiny k transplantaci jater podle Milánských kritérií a od roku 2009 jsou zařazováni i podle extendovaných UCSF kritérií. Při zařazování do čekací listiny je rozhodující velikost tumoru, nepřítomnost makroangioinvaze a nepřítomnost vzdálených metastáz, u pacientů splňujících pouze UCSF kritéria pak dobrá nebo střední diferenciace tumoru a nepřítomnost angioinvaze prokázaná biopsií z největšího z ložisek.
Pacienti jsou do čekací listiny standardně zařazováni podle nálezu na zobrazovacích metodách (ultrasonografie a čtyřfázové CT břicha nebo dynamická MR břicha) provedených během protokolárního předtransplantačního vyšetření. Podle současných doporučení České hepatologické společnosti [13] není ke stanovení diagnózy HCC nutné provádět jaterní biopsii, výkon je u pokročilých cirhotiků navíc zatížen značným rizikem komplikací. U většiny pacientů proto není doložena nepřítomnost mikroangioinvaze a stupeň diferenciace nádoru před transplantací jater. V našem souboru jsme byli schopni provést biopsii u necelé poloviny pacientů, u ostatních bylo riziko komplikací příliš vysoké. Vyloučení mikroangioinvaze a špatné diferenciace tumoru (grade 3) cílenou biopsií ložiska bylo v našem indikačním protokolu požadováno u pacientů, jejichž tumor velikostí či počtem ložisek přesahoval Milánská kritéria a měli být indikováni k transplantaci díky splnění UCSF kritérií. Takových pacientů bylo v hodnoceném souboru celkem 20, cílená biopsie byla však proveditelná pouze u 11 z nich. Devět pacientů indikovaných dle UCSF kritérií tak bylo zařazeno bez provedení cílené biopsie. Odmítnout léčbu transplantací pacientům, u kterých nebyla cílená biopsie proveditelná pro vysoké riziko výkonu, jsme nepovažovali za racionální a zdůvodnitelné. Toto rozhodnutí se ukázalo později být správným, neboť v explantátu byla prokázána mikroangioinvaze jen u jednoho z devíti pacientů, kteří biopsii nepodstoupili. Na druhou stranu stále trváme na protokolu, který cílenou biopsii ložiska u pacientů přesahujících velikostí tumoru Milánská kritéria požaduje. Nemožnost získat vzorek však nemůže paušálně vést k odmítnutí transplantační léčby. Tento postup nám současná dynamika čekací listiny umožňuje, případné prodlužování čekací doby v budoucnosti by vedlo k více restriktivnímu indikačnímu postupu.
Dle údajů uvedených v tab. 2 sice všichni pacienti před zařazením do čekací listiny splnili UCSF kritéria z hlediska velikosti tumoru, celá jedna třetina pacientů však měla velikost tumoru těsně pod akceptovanou hranicí. Dle nálezu v explantátu splnila UCSF kritéria jen polovina pacientů. Nejčastějším důvodem nesplnění byla přítomnost angioinvaze. Při srovnávání nálezů v době zařazení do čekací listiny a nálezů v explantátu je nutno brát v úvahu, že mezi oběma hodnoceními je doba strávená na čekací listině. Není zde proto možno hovořit o neshodě mezi nálezy zobrazovacích metod a nálezem patologa, neboť za dobu čekání na transplantaci je nutno počítat s progresí tumoru. Velikost tumoru a nepřítomnost generalizace se v době čekání na transplantaci kontroluje každé tři měsíce; pokud velikost tumoru naroste a přesáhne UCSF kritéria, je pacient z čekací listiny vyřazen. Jediným postupem, který by vedl ke snížení počtu pacientů přesahujících UCSF nálezem v explantátu, by bylo časnější zařazování pacientů s HCC do čekací listiny. Zařazování pacientů s menším tumorem lze dosáhnout pouze pečlivým screeningem HCC u rizikových cirhotiků. Zlepšení screeningu ale není v možnostech transplantačního centra, nýbrž je věcí odesílajících lékařů. Z literatury vyplývá, že regulérnímu screeningu je v zahraničí podrobena jen čtvrtina cirhotiků. V letos prezentované práci ze Slovenska bylo ukázáno, že podíl správně screenovaných cirhotiků se zvyšuje až na polovinu, pokud je screening jednoznačně doporučen ambulantnímu lékaři ve zprávě z hospitalizace [14].
V literatuře je uváděným hlavním problémem po transplantaci jater pro HCC recidiva onemocnění, která se vyskytuje u 11–18 % nemocných [15,16]. K rekurenci HCC dochází nejčastěji během prvních dvou let po transplantaci jater, rekurence je spojena s mediánem přežití cca jeden rok od doby jejího zjištění [15]. V našem souboru jsme zaznamenali recidivu u 16 % pacientů, z nichž 76,9 % (10/13) mělo přítomnou mikrovaskulární invazi v explantátu jater, která významně ovlivňuje prognózu pacienta. Nezávislé prediktivní faktory rekurence HCC v potransplantačním období našeho souboru byly tedy podobné faktorům uveřejněným v metaanalýze Sotiropoulose et al [17].
Závěr
Transplantace jater se v průběhu své existence vyvinula ve standardní metodu léčby hepatocelulárního karcinomu nabízející vynikající dlouhodobé přežití. Výsledky transplantace jater pro HCC jsou v našem centru srovnatelné s výsledky z jiných zahraničních center. Pro další zlepšení dlouhodobého přežití po transplantaci jater pro HCC je podstatné, aby pacienti byli do čekací listiny zařazováni časně. To je však úkol přesahující možnosti transplantačního centra, neboť toho lze dosáhnout pouze pravidelným screeningem rizikových skupin cirhotiků jejich ošetřujícími lékaři a následnou spoluprací s transplantačním centrem.
Autoři děkují paní RNDr. Věře Lánské, CSc. za statické zhodnocení klinických dat a paní Lucii Janečkové za pomoc s analýzou zdrojových dat.
Podpořeno MZ ČR – RVO (Institut klinické a experimentální medicíny – IKEM, IČ 00023001).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 6. 3. 2014
Přijato: 7. 4. 2014
MUDr. Renáta Šenkeříková
Klinika hepatogastroenterologie, IKEM
Vídeňská 1958/9, 140 21 Praha 4
renata.senkerikova@ikem.cz
Zdroje
1. Jemal A, Bray F, Center MM et al. Global cancer statistics. CA Cancer J Clin 2011; 61(2): 69–90. doi: 10.3322/caac.20107.
2. Sangiovanni A, Prati GM, Fasani P et al. The natural history of compensated cirrhosis due to hepatitis C virus: A 17-year cohort study of 214 patients. Hepatology 2006; 43(6): 1303–1310.
3. Ústav zdravotnických informací a statistiky ČR. [online]. Dostupné z: http://www.uzis.cz/registry-nzis/nor.
4. Llovet JM, Schwartz M, Mazzaferro V. Resection and liver transplantation for hepatocellular carcinoma. Semin Liver Dis 2005; 25(2): 181–200.
5. Mazzaferro V, Bhoori S, Sposito C et al. Milan criteria in liver transplantation for hepatocellular carcinoma: an evidence-based analysis of 15 years of experience. Liver Transpl 2011; 17 (Suppl 2): S44–S57. doi: 10.1002/lt.22365.
6. Bismuth H, Chiche L, Adam R et al. Liver resection versus transplantation for hepatocellular carcinoma in cirrhotic patients. Ann Surg 1993; 218(2): 145–151.
7. Mazzaferro V, Regalia E, Doci R et al. Liver transplantation for the treatment of small hepatocellular carcinomas in patients with cirrhosis. N Engl J Med 1996; 334(11): 693–699.
8. Yao FY, Ferrell L, Bass NM et al. Liver transplantation for hepatocellular carcinoma: comparison of the proposed UCSF criteria with the Milan criteria and the Pittsburgh modified TNM criteria. Liver Transpl 2002; 8(9): 765–774.
9. Duffy JP, Vardanian A, Benjamin E et al. Liver transplantation criteria for hepatocellular carcinoma should be expanded: a 22-year experience with 467 patients at UCLA. Ann Surg 2007; 246(3): 502–509; discussion: 509–511.
10. Mazzaferro V, Llovet JM, Miceli R et al. Predicting survival after liver transplantation in patients with hepatocellular carcinoma beyond the Milan criteria: a retrospective, exploratory analysis. Lancet Oncol 2009; 10(1): 35–43. doi: 10.1016/S1470-2045(08)70284-5.
11. Llovet JM, Ricci S, Mazzaferro V et al. Sorafenib in advanced hepatocellular carcinoma. N Engl J Med 2008; 359(4): 378–390. doi: 10.1056/NEJMoa0708857.
12. Bruix J, Sherman M. Management of hepatocellular carcinoma: an update. Hepatology 2011; 53(3): 1020–1022. doi: 10.1002/hep.24199.
13. Brůha R, Šperl J, Urbánek P et al. Doporučený postup pro léčbu a diagnostiku hepatocelulárního karcinomu. Gastroent Hepatol 2012; 66(2): 83–92.
14. Adamcová-Selčanová S, Badinková J, Skladaný Ľ. Hepatocelulárny karcinóm (HCC). Gastroent Hepatol 2013; 67 (Suppl 3): S17.
15. Roayaie S, Schwartz JD, Sung MW et al. Recurrence of hepatocellular carcinoma after liver transplant: patterns and prognosis. Liver Transpl 2004; 10(4): 534–540.
16. Regalia E, Fassati LR, Valente U et al. Pattern and management of recurrent hepatocellular carcinoma after liver transplantation. J Hepatobiliary Pancreat Surg 1998; 5(1): 29–34.
17. Sotiropoulos GC, Molmenti EP, Lösch C et al. Meta-analysis of tumor recurrence after liver transplantation for hepatocellular carcinoma based on 1,198 cases. Eur J Med Res 2007; 12(10): 527–534.
Štítky
Detská gastroenterológia Gastroenterológia a hepatológia Chirurgia všeobecná
Článek Správná odpověď na kvízČlánek Projekt RISING STARSČlánek MUDr. Boris Pekárek (1978)Článek OznámeníČlánek OmluvaČlánek Kvíz
Článok vyšiel v časopiseGastroenterologie a hepatologie
Najčítanejšie tento týždeň
2014 Číslo 2- Těhotenství a idiopatické střevní záněty – terapie zlepšuje stav a je bezpečná
- Vliv těhotenství na klinickou aktivitu Crohnovy nemoci
- Medikace u IBD v těhotenství
- Adherence a kvalita života adolescentních pacientů s IBD
- Adherence pacientů se střevním zánětlivým onemocněním
-
Všetky články tohto čísla
- Léčba portální hypertenze pomocí transjugulární intrahepatální portosystémové spojky – prvních 1 000 výkonů ve FN Hradec Králové
- 1 000 TIPS ve FN Hradec Králové: indikace a přežívání nemocných
- Budd-Chiari syndrom a TIPS – 21 let zkušeností
- Transjugulární intrahepatální portosytémová spojka v terapii refrakterního ascitu: současný pohled jednoho pracoviště
- Dispenzarizace nemocných po zavedení transjugulární intrahepatální portosystémové spojky – diagnostika dysfunkce zkratu a možnosti intervence
- Transplantace jater pro hepatocelulární karcinom, dlouhodobé přežití a faktory ovlivňující rekurenci tumoru (zkušenosti jednoho centra)
- Využití EUS navigované choledochoduodenostomie v léčbě biliární obstrukce
- Hereditárny angioedém ako príčina bolestí brucha
- Malígny melanóm konečníka – zriedkavá kazuistika a prehľad literatúry
- Moderní diagnostika Lynchova syndromu
- Správná odpověď na kvíz
- Diskusia k príspevku „Moderní diagnostika Lynchova syndromu“
- Projekt RISING STARS
- doc. MUDr. Jan Martínek, Ph.D., AGAF (1969)
- MUDr. Ondřej Ryska, Ph.D. (1981)
- MUDr. Sylvia Dražilová (1972)
- MUDr. Boris Pekárek (1978)
- EUS workshop v Jablonci nad Nisou
- 13th Czech-Slovak IBD symposium
- 9th Congress of ECCO, Copenhagen, Denmark
- Oznámení
- Omluva
- Nový člen výkonné redakční rady
- Remsima™ – první biosimilární infliximab
- Autodidaktický test: hepatologie
- Hepatologie nejen z Hradce Králové
- Kvíz
- Gastroenterologie a hepatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- doc. MUDr. Jan Martínek, Ph.D., AGAF (1969)
- MUDr. Sylvia Dražilová (1972)
- MUDr. Ondřej Ryska, Ph.D. (1981)
- Budd-Chiari syndrom a TIPS – 21 let zkušeností
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



