-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Použití chemoterapie v kombinaci s cílenou biologickou léčbou u diseminovaného kolorektálního karcinomu: kazuistika dlouhodobé a výrazné klinické odpovědi
The Role of Chemotherapy and Targeted antiVEGF - and antiEGFR-Therapy in Metastatic Colorectal Cancer: a Case Report of Long-Term and Intensive Response
Backgrounds:
Colorectal cancer (CRC) is the second most frequent malignancy in the Czech Republic. Treatment of a metastatic disease is based on application of palliative chemotherapy (fluorouracil, leucovorin, irinotecan, oxaliplatin). When combined with targeted agents against vascular endothelial growth factor (VEGF) and epidermal growth factor receptor (EGFR), it can result in significant and long-term response.Case:
We present a case of a 34-years old man with adenocarcinoma of sigmoid colon (Dukes C) with 5 years disease-free survival (DFS) after primary surgery (in 2002) and adjuvant chemotherapy with FOLFIRI (12 cycles). A solitary relapse in retroperitoneal lymph nodes in November 2007 was treated with retroperiotoneal dissection followed by adjuvant chemotherapy with FOLFOX 4 (12 cycles) and targeted radiotherapy of retroperitoneal area (completed in May 2008). An early relapse occurred one month later (June 2008 – infraclavicular area, thoracic wall and retroperitoneal lymph nodes), patient underwent first line palliative chemotherapy with XELIRI + bevacizumab leading to partial remission (PR) after 3 months and complete remission (CR) after 6 months of treatment. Bevacizumab monotherapy was continued for the next 8 months up to March 2010, when a progression in the lung occurred. After wild-type status was confirmed, KRAS treatment was changed to the second line combination of irinotecan and cetuximab that resulted in nearly complete remission after 6 months and preservation of this remission after the next 6 months of cetuximab monotherapy. All treatments were well tolerated with good quality of life.Conclusion:
Our case demonstrates the current options in the treatment of metastatic CRC. There is a trend to gradually use all the above listed cytostatics in combination with anti-VEGF and anti-EGFR monoclonal antibodies. When administered early, it may provide a significant and long-term treatment response.Key words:
colorectal cancer – bevacizumab – cetuximab
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.Submitted:
25. 3. 2011Accepted:
27. 10. 2011
Autori: R. Němeček
; R. Vyzula
Pôsobisko autorov: Klinika komplexní onkologické péče, Masarykův onkologický ústav, Brno
Vyšlo v časopise: Klin Onkol 2011; 24(6): 465-469
Kategória: Kazuistiky
Súhrn
Východiska:
Kolorektální karcinom je v České republice druhou nejčastější malignitou. Základní léčebnou metodou diseminovaného onemocnění je systémová paliativní chemoterapie založená na aplikaci 5-fluorouracilu s leukovorinem a irinotekanem, event. oxaliplatinou. Kombinací s cílenou biologickou léčbou monoklonálními protilátkami proti vaskulárnímu endotelovému růstovému faktoru (VEGF) a receptoru pro epidermální růstový faktor (EGFR) lze při včasné indikaci docílit výrazných a dlouhodobých klinických odpovědí.Případ:
Kazuistika demonstruje průběh onemocnění 34letého pacienta s adenokarcinomem sigmatu (stadium Dukes C), který byl po primární operaci v roce 2002 a po zajištění adjuvantní chemoterapií režimem FOLFIRI (12 sérií) po dobu 5 let bez známek nádorového onemocnění. V listopadu roku 2007 došlo k solitárnímu relapsu v retroperitoneu, následovala neradikální operace (pozitivní okraje), adjuvantní chemoterapie režimem FOLFOX 4 (12 sérií) a cílená radioterapie na oblast retroperitonea (do května roku 2008). Vzhledem k časnému relapsu onemocnění v červnu roku 2008 (podklíček, hrudní stěna, retroperitoneum) byla zahájena I. linie paliativní chemoterapie režimem XELIRI + bevacizumab s efektem parciální remise (PR) po 3 měsících a dosažení kompletní remise onemocnění (CR) po 6 měsících léčby. V léčbě bevacizumabem v monoterapii pokračováno dalších 8 měsíců do března roku 2010, kdy došlo k progresi na plicích. Po vyloučení mutace genu KRAS byla zahájena II. linie paliativní bio-chemoterapie režimem irinotekan + cetuximab, která vykázala rovněž velmi dobrý efekt – dosažení téměř kompletní remise po necelých 6 měsících léčby a udržení této remise po dalších 6 měsíců při monoterapii cetuximabem. To vše při minimální toxicitě léčby a velmi dobré kvalitě života prezentovaného pacienta.Závěr:
Uvedená kazuistika demonstruje dnešní možnosti systémové léčby diseminovaného kolorektálního karcinomu se snahou o postupné využití všech používaných cytostatik v kombinaci s biologickou léčbou. Je-li cílená léčba monoklonálními protilátkami proti VEGF a EGFR v kombinaci s chemoterapií podána včas, může vést k dlouhodobým a výrazným klinickým výsledkům.Klíčová slova:
kolorektální karcinom – bevacizumab – cetuximabÚvod
Zhoubné nádory tlustého střeva a konečníku představují v České republice druhou nejčastější malignitu; jejich incidence i mortalita po dlouhodobém kontinuálním nárůstu v posledních 5 letech stagnuje [1,2]. Základní léčebnou modalitou diseminovaného onemocnění je systémová paliativní chemoterapie založená na aplikaci 5-fluorouracilu s leukovorinem a irinotekanem, eventuálně oxaliplatinou [3–5]. Kombinace chemoterapie s cílenou biologickou léčbou monoklonálními protilátkami zaměřenými proti vaskulárnímu endotelovému růstovému faktoru (VEGF) a receptoru pro epidermální růstový faktor (EGFR) zlepšuje léčebné výsledky [6–8], posunuje medián celkového přežití pacientů za hranici 24 měsíců [9,10] a ve vybraných případech představuje díky konverzi původně inoperabilního nálezu na operabilní šanci na „vyléčení“ pacientů [11].
Popis případu
34letý pacient, dosud bez vážnějších onemocnění, pozoroval od konce května roku 2001 občasnou příměs krve ve stolici. Potížím nevěnoval pozornost. V květnu roku 2002 navštívil lékaře – byla provedena kolonoskopie a zjištěna stenozující infiltrace sigmatu neprůchodná pro kolonoskop. Při následném došetření nebyly prokázány vzdálené metastázy ani elevace nádorových markerů. Dne 28. 5. 2002 byla v Masarykově onkologickém ústavu v Brně provedena radikální resekce sigmatu, histologicky potvrzen středně diferencovaný adenokarcinom (s metastázami do 6 kolických uzlin z 27 vyšetřených). Uzavřeno jako stadium Dukes C (pT3 pN2 MO) a po onkologické rozvaze byla vzhledem k rozsahu onemocnění a velmi dobrému stavu pacienta indikována pooperační chemoterapie režimem FOLFIRI. 1. série byla podávána od 17. 6. 2002 (po předchozím zavedení i.v. portu), celkově bylo aplikováno 12 sérií, poslední zahájena od 19. 11. 2002. Léčba byla pacientem dobře tolerována, nebyly zaznamenány žádné nežádoucí účinky grade 3–4 (dle NCI-CTC kritérií). Na přelomu ledna a února roku 2003 byl pacient přešetřen, potvrzena kompletní remise onemocnění (CR), dále indikováno sledování. V dubnu 2003 provedena polypektomie suspektního polypu colon transversum, histologicky verifikován benigní nález.
Remise onemocnění trvala do listopadu roku 2007 (tedy celkem 5 let), kdy se na PET objevila patologická uzlina v retroperitoneu (paraaortálně vlevo v úrovni dolního okraje levé ledviny), doprovázená elevací nádorových markerů (CEA 13,1 µg/l, CA 19–9 43,4 kU/l). Pacient byl indikován k operační revizi, která byla provedena v MOÚ dne 27. 11. 2007. Patologická uzlina v retroperitoneu byla odstraněna a její okolí bylo označeno klipy pro pozdější cílenou radioterapii. Histologicky z resekátu potvrzena retroperitoneální metastáza kolorektálního adenokarcinomu s pozitivními okraji, proto byla indikována pooperační léčba – chemoterapie režimem FOLFOX 4 a cílená radioterapie. Chemoterapie probíhala od 17. 12. 2007 do 20. 5. 2008, celkem bylo aplikováno 12 sérií. Léčba byla pacientem opět velmi dobře tolerována, z nežádoucích účinků se objevila pouze postupně progredující periferní neuropatie (klasifikovaná v závěru léčby jako grade 2 dle NCI-CTC kritérií).
Při následném přešetření 6. 6. 2008 nebyly shledány známky recidivy základního onemocnění v dutině břišní, v pooperační léčbě bylo tedy pokračováno plánovanou cílenou radioterapií na oblast lůžka patologické uzliny v retroperitoneu. Tato probíhala ve dnech 10. 6.–14. 7. 2008, celkově byla aplikována dávka 46 Gy ve 23 frakcích. Léčba byla provázena poradiační dermatitidou grade 1, jinak tolerance výborná. Pooperační léčba byla radioterapií plánovaně ukončena.
Přešetření pomocí metody PET/CT v říjnu 2008 (obr. 1) prokázalo časný relaps onemocnění – několik drobných ložisek s metabolizmem vitálních nádorových buněk v retroperitoneu (obr. 2), v levém podklíčku (obr. 3) a v hrudní stěně vlevo (obr. 4), které na CT odpovídaly většinou nezvětšeným lymfatickým uzlinám; v plicích pak dle CT několik drobných nodulů pod rozlišovací schopností PET, k jejichž etiologii se nelze jednoznačně vyjádřit.
Obr. 1. PET + CT – říjen 2008. 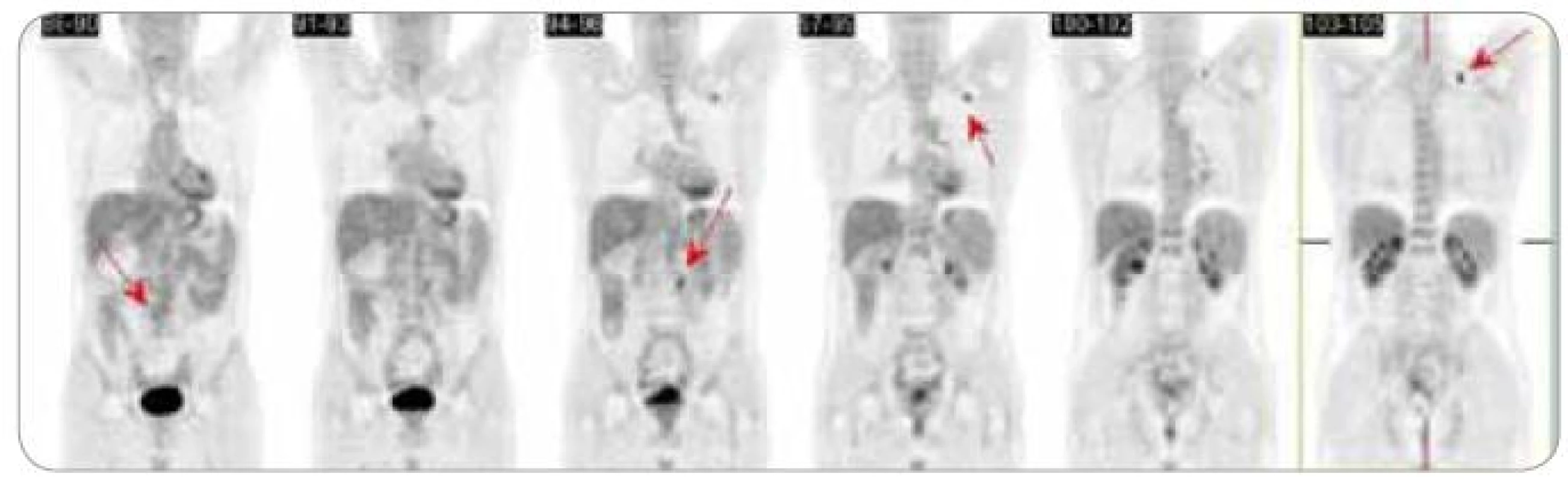
Obr. 2. PET + CT – patologické ložisko v retroperitoneu. 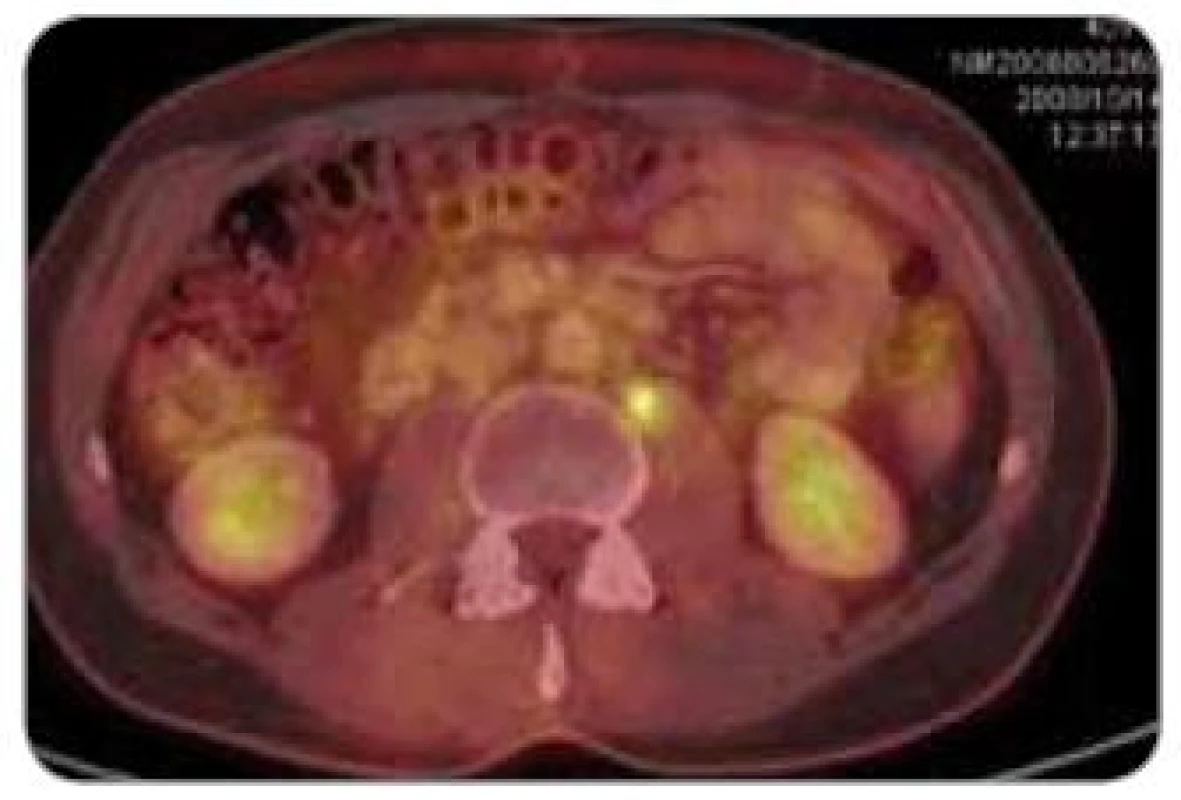
Obr. 3. PET + CT – patologické ložisko infraklavikulárně vlevo. 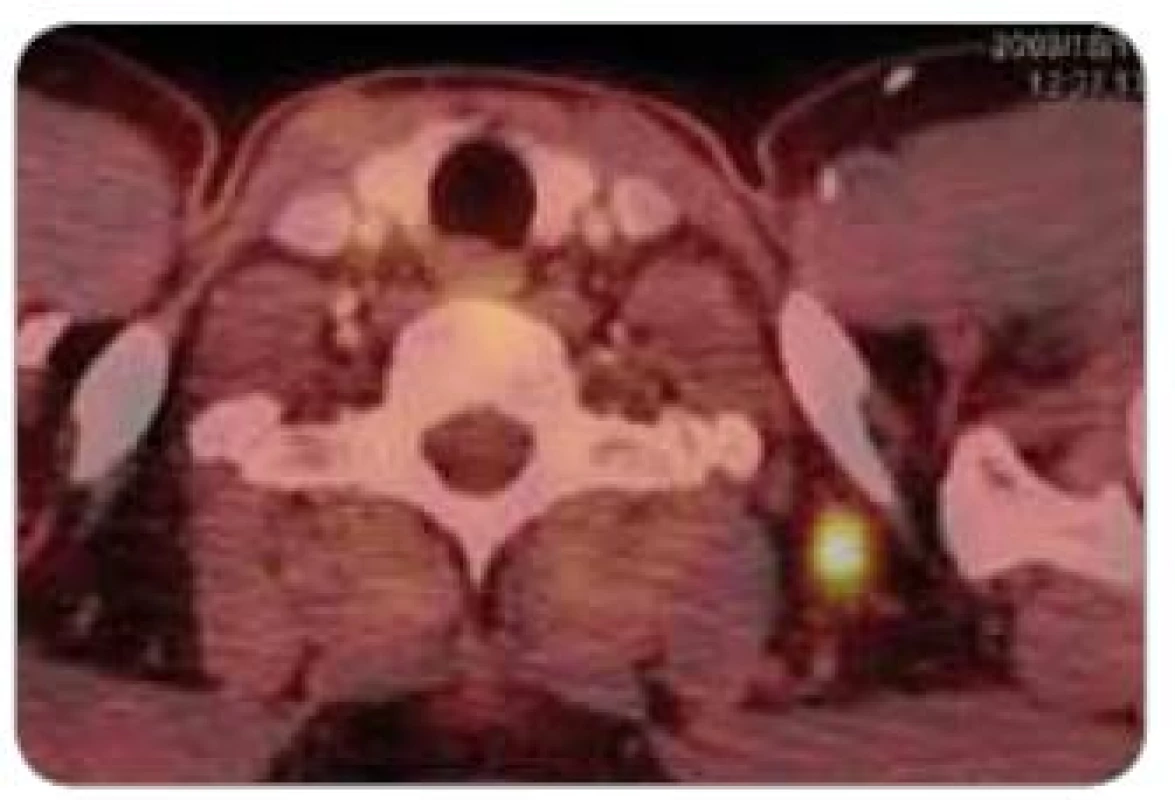
Obr. 4. PET + CT – patologické ložisko v hrudní stěně vlevo. 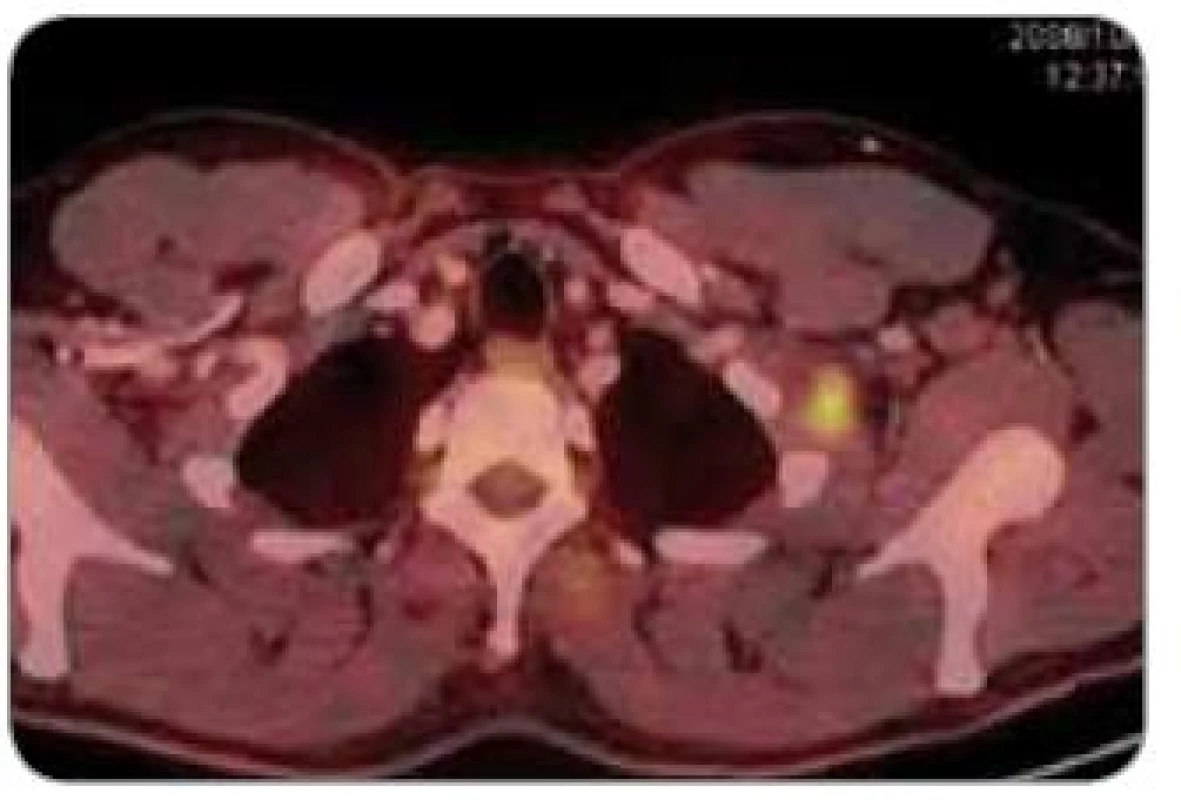
Od 24. 10. 2008 byla zahájena I. linie paliativní chemoterapie režimem XELIRI + bevacizumab. Po 6 sériích byla dle CT potvrzena parciální remise onemocnění (v oblasti hrudní stěny vlevo a levostranné nadklíčkové lymfatické uzliny), v léčbě pokračováno do 12. série, která byla aplikována od 9. 7. 2009. Následné přešetření pomocí PET/CT (obr. 5) potvrdilo negativní nález, taktéž nádorové markery byly v normálním rozmezí. Byla tedy konstatována kompletní remise onemocnění a od 30. 7. 2009 se pokračovalo v udržovací léčbě bevacizumabem. Z nežádoucích účinků kombinované léčby XELIRI + bevacizumab byla zaznamenána ojedinělá asymptomatická myelotoxicita charakteru leuko-neutropenie grade 2–3, jinak byla léčba pacientem velmi dobře tolerována.
Obr. 5. PET + CT červenec 2009. 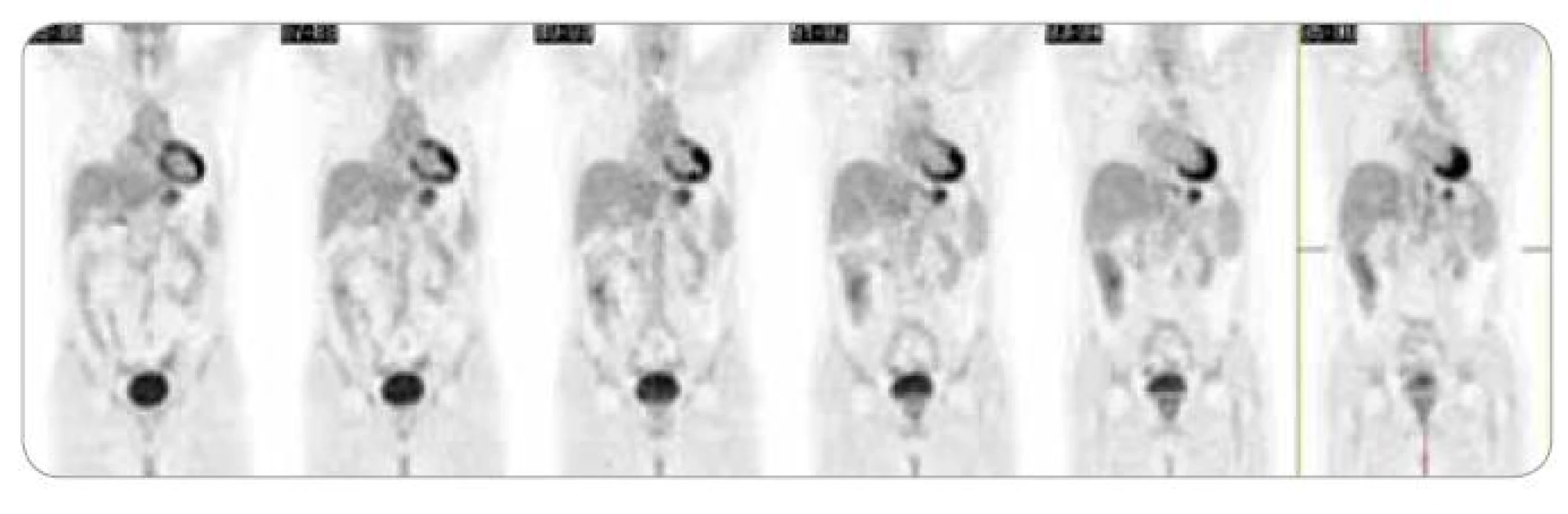
Léčba bevacizumabem v monoterapii pokračovala až do března roku 2010. Od podzimu roku 2009 byl patrný pozvolný nárůst CEA (6 … 8 … 9,5 … 10 µg/l), proto bylo v lednu 2010 provedeno přešetření – dle PET/CT nález drobné patologické uzliny v pánvi vlevo a nález několika drobných nodulů v plicích (největší 9 mm vlevo bazálně, dva menší vpravo), které byly oproti vyšetření ze srpna roku 2009 označeny za nové nebo progredující. Nález byl nejednoznačný, hodnoceno jako stabilizace onemocnění (SD) a v léčbě bevacizumabem pokračováno.
Dne 4. 3. 2010 byla dle CT (obr. 6) progrese onemocnění potvrzena (přibližně 40% zvětšení velikosti několika plicních ložisek bilaterálně), léčba bevacizumabem po 14 měsících ukončena.
Obr. 6. CT březen 2010 – plicní metastáza. 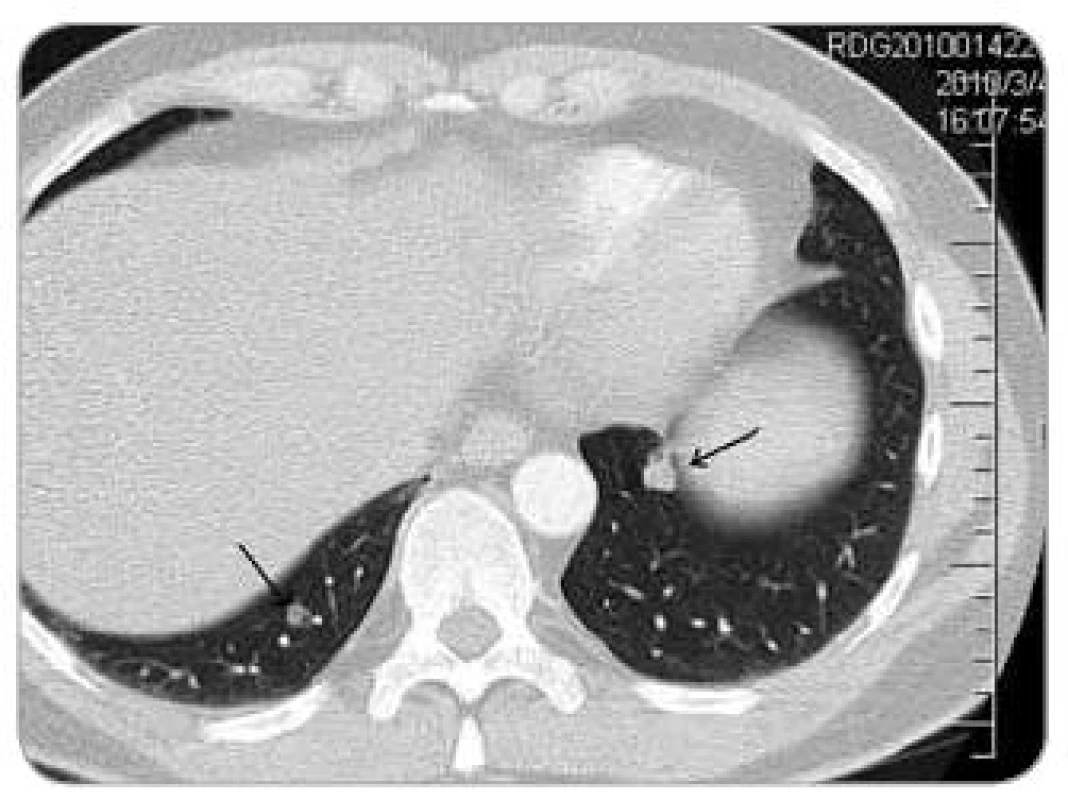
V histologických preparátech z operace primárního nádoru byl potvrzen wild-type status genu KRAS a pozitivní exprese EGFR (2+). Vzhledem k předléčenosti a celkově dobrému stavu pacienta byla indikována paliativní bio-chemoterapie II. linie režimem irinotekan + cetuximab, která byla zahájena od 18. 3. 2010. Již během prvního měsíce léčby došlo k normalizaci nádorových markerů (CEA 12,7 … 4,5 μg/l). Léčba byla pacientem veskrze velmi dobře tolerována, z nežádoucích účinků se objevila pouze očekávaná kožní toxicita (akneiformní exantém grade 2), mírná gastrointestinální toxicita (nauzea grade 1 + diarrhea grade 1–2) a intermitentně i mírná hematotoxicita irinotekanu (asymptomatická neutropenie grade 2), a to i přesto, že irinotekan byl podáván po celou dobu v plné dávce, tj. 350 mg/m2 (tedy v celkové dávce 700 mg à 3 týdny).
Po 7 sériích léčby bylo provedeno přešetření – dle PET/CT z 3. 8. 2010 (obr. 7 a 8) minimální nález (dle CT regrese nálezu na plicích, dle PET stacionární aktivita drobných uzlin v pravé axille, retroperitoneu a malé pánvi vlevo – SUV do 3,1 svědčí spíše jen pro reparační změny), pacient požádal o přerušení chemoterapie irinotekanem, dále pokračováno pouze v biologické léčbě cetuximabem v monoterapii.
Obr. 7. CT srpen 2010 – regrese plicní metastázy. 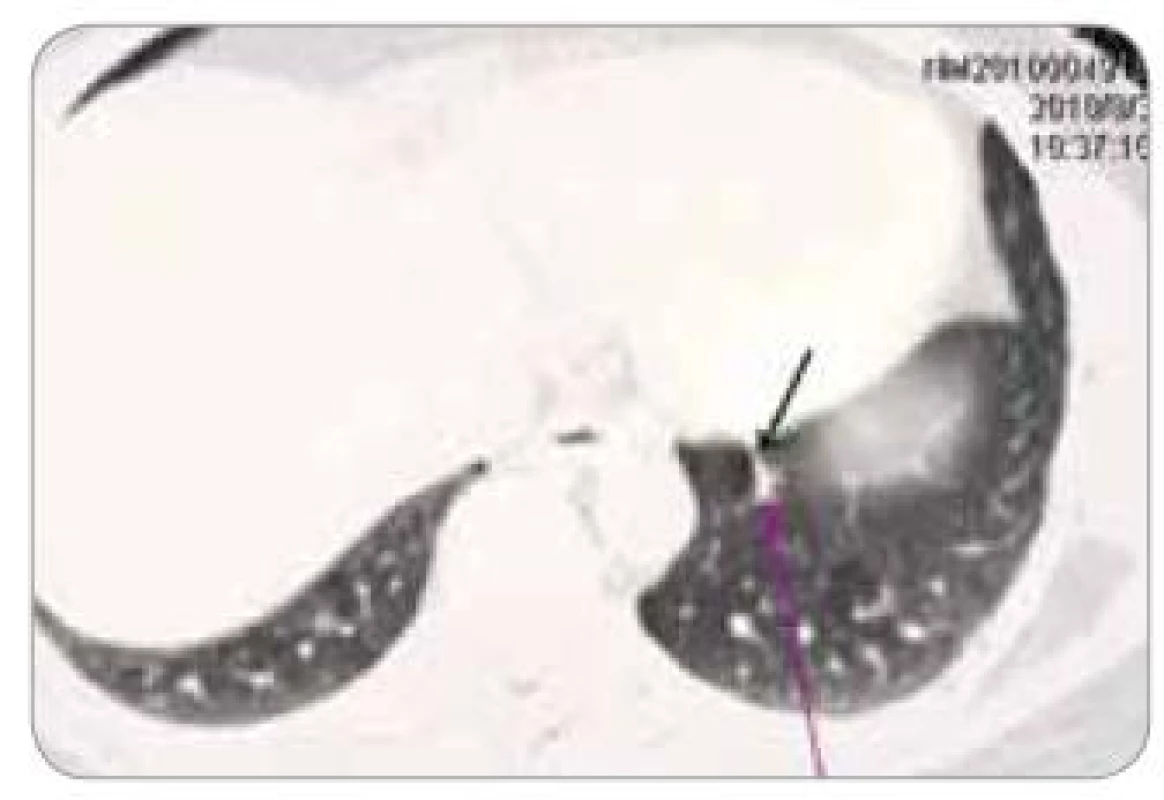
Tato probíhá bez přerušení až dosud (únor 2011) – z nežádoucích účinků přetrvává pouze akneiformní exantém grade 1–2, ostatní po ukončení aplikace irinotekanu ustoupily. Dne 3. 2. 2011 byl pro obtížnou průchodnost portu proveden nástřik RTG-kontrastní látkou a vysloveno podezření na trombózu portu, proto byla zavedena antikoagulační terapie LMWH. Pacient je aktuálně ve velmi dobrém celkovém stavu (PS 1).
Diskuze
Uvedená kazuistika téměř ideálně demonstruje dnešní možnosti systémové léčby diseminovaného kolorektálního karcinomu se snahou o postupné využití všech používaných cytostatik v kombinaci s biologickou léčbou [9,10].
Pokud se vrátíme do období diagnózy, trvalo období bez progrese onemocnění – i přes stadium Dukes C (pT3pN2M0) po zaléčení adjuvantní chemoterapií posílenou o irinotekan – po dobu celých pěti let. Nutno podotknout, že v roce 2002 nebyly k dispozici aktuální výsledky studií potvrzujících minimální benefit irinotekanu v adjuvantním podání [12]. Pacient byl při stadiu pT3pN2 a primárně obturujícím nádoru evidentně výrazně rizikový, snaha o účinnější kombinovanou chemoterapii posílením o cytostatikum nové generace byla tedy na místě.
Vzhledem k solitárnímu nálezu nádorové aktivity v retroperitoneu, potvrzené nejmodernějšími zobrazovacími metodami, byla operace retroperitonea správným řešením. I když bohužel nemohla vést ke zcela radikálnímu odstranění metastáz, ozřejmila lokoregionální nález v retroperitoneu a lokalizovala jej pro plánovanou radioterapii. Vzhledem k systémovému charakteru onemocnění bylo pokračováno kombinovanou „pseudoadjuvantní“ chemoterapií s oxaliplatinou, následovanou po standardním podání 12 sérií a negativním přešetření aplikací plánované radioterapie na oblast retroperitonea. Zde lze samozřejmě diskutovat nad načasováním radioterapie (zda tato měla v rámci snahy o lokální kontrolu a zabránění lokoregionálnímu relapsu předcházet podání systémové chemoterapie, či být „vložena“ sandwichově mezi jednotlivé chemoterapeutické cykly) a nad indikací radioterapie jako takové (která je ověřena při léčbě karcinomu rekta, u nádorů colon své jednoznačné místo však zatím nemá). Na druhou stranu ovšem nutno podotknout, že se jednalo o pacienta s negativním nálezem při přešetření (po ukončení systémové léčby), kde bylo na výběr buď cílené ozáření místa v retroperitoneu (vyznačeného peroperačně klipy), nebo pouhé sledování.
I přes tuto relativně intenzivní léčbu došlo k relapsu již v průběhu prvního měsíce od ukončení radioterapie, a proto byla zahájena systémová paliativní chemoterapie I. linie v kombinaci s biologickou antiangiogenní léčbou bevacizumabem. Tato demonstrovala velmi dobrý efekt – parciální remisi po 3 měsících a dosažení kompletní remise onemocnění po 6 měsících léčby. Ve snaze o udržení remise bylo pokračováno v antiangiogenní terapii po dobu dalších 8 měsíců, tedy celkově byla kombinovaná léčba s bevacizumabem účinná po dobu 14 měsíců.
Při další progresi onemocnění byla zvolena biologická léčba cílená na EGFR, neboť její efektivitu bylo možno predikovat s ohledem na vyloučení mutace v genu KRAS. Léčba touto monoklonální protilátkou v kombinaci s irinotekanem byla opět evidentně efektivní, což potvrzuje dosažení téměř kompletní remise po necelých 6 měsících léčby a udržení této remise po dalších 6 měsíců při monoterapii cetuximabem. To vše při relativně diskrétní toxicitě léčby, a tedy velmi dobré kvalitě života našeho pacienta.
Další vývoj onemocnění ukáže čas. Nicméně již teď se celkové přežití pacienta pohybuje na hranici 9 let od stanovení diagnózy, respektive 40 měsíců od potvrzení generalizace onemocnění, což mnohonásobně převyšuje statisticky udávané mediány přežití u tohoto onemocnění.
Závěr
Z uvedené kazuistiky vyplývá, že biologická léčba monoklonálními protilátkami proti VEGF a EGFR v kombinaci s chemoterapií je účinná, a pokud je správně indikována a především je-li podána včas, může vést k dlouhodobým a výrazným klinickým výsledkům.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
MUDr. Radim Němeček
Klinika komplexní onkologické péče
Masarykův onkologický ústav
Žlutý kopec 7
656 53 Brno
e-mail: nemecek@mou.cz
Obdrženo: 25. 3. 2011
Přijato: 27. 10. 2011
Zdroje
1. Ústav zdravotnických informací a statistiky ČR, Národní zdravotnický informační systém (NZIS), Národní onkologický registr (NOR), [20.12.2007]. Dostupné z: http://www.uzis.cz/info.php?article=368&mnu_id=7300.
2. Dušek L, Mužík J, Kubásek M et al. Epidemiologie zhoubných nádorů v České republice [online]. Masarykova univerzita 2005 [cit. 2008-12-15]. Dostupný z: http://www.svod.cz.
3. de Gramont A, Bosset JF, Milan C et al. Randomized trial comparing monthly low-dose leucovorin and fluorouracil bolus with bimonthly high-dose leucovorin and fluorouracil bolus plus continuous infusion for advanced colorectal cancer: a French intergroup study. J Clin Oncol 1997; 15(2): 808–815.
4. Douillard JY, Cunningham D, Roth AD et al. Irinotecan combined with fluorouracil compared with fluorouracil alone as first-line treatment for metastatic colorectal cancer: a multicentre randomised trial. Lancet 2000; 355(9209): 1041–1047.
5. de Gramont A, Figer A, Seymour M et al. Leucovorin and fluorouracil with or without oxaliplatin as first-line treatment in advanced colorectal cancer. J Clin Oncol 2000; 18(16): 2938–2947.
6. Hurwitz HI, Fehrenbacher L, Hainsworth JD, et al. Bevacizumab in combination with fluorouracil and leucovorin: an active regimen for first-line metastatic colorectal cancer. J Clin Oncol 2005; 23(15): 3502–3508.
7. Saltz LB, Clarke S, Díaz-Rubio E et al. Bevacizumab in combination with oxaliplatin-based chemotherapy as first-line therapy in metastatic colorectal cancer: a randomized phase III study. J Clin Oncol 2008; 26(12): 2013–2019.
8. Cunningham D, Humblet Y, Siena S et al. Cetuximab monotherapy and cetuximab plus irinotecan in irinotecan-refractory metastatic colorectal cancer. N Engl J Med 2004; 351(4): 337–345.
9. Tol J, Koopman M, Cats A et al. Chemotherapy, bevacizumab, and cetuximab in metastatic colorectal cancer. N Engl J Med 2009; 360(6): 563–572.
10. Köhne CH, Lenz HJ. Chemotherapy with targeted agents for the treatment of metastatic colorectal cancer. Oncologist 2009; 14(5): 478–488.
11. Gruenberger B, Tamandl D, Schueller J et al. Bevacizumab, capecitabine, and oxaliplatin as neoadjuvant therapy for patients with potentially curable metastatic colorectal cancer. J Clin Oncol 2008; 26(11): 1830–1835.
12. Chau I, Cunningham D. Adjuvant therapy in colon cancer – what, when and how? Ann Oncol 2006; 17(9): 1347–1359.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2011 Číslo 6- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Fixní kombinace tramadol/paracetamol je doporučenou volbou v léčbě chronické bolesti v ordinaci praktického lékaře
-
Všetky články tohto čísla
- Pozitronová emisní tomografie v diagnostice a sledování pacientů s neseminomovými germinálními nádory
- Plazminogen aktivátor systém a jeho klinický význam u pacientů s nádorovým onemocněním
- Castlemanova choroba
- Prediktivní hodnota ultrazvukových parametrů, CA-125 a indexu rizika malignity u pacientek s karcinomem ovarií
- Naše päťročné výsledky in vitro testovania chemorezistencie u onkologických pacientov
- Aktuálne charakteristiky deskriptívnej epidemiológie nádorov žalúdka v Slovenskej republike v kontexte medzinárodného porovnania
- Neskoré následky u pacientov liečených alogénnou transplantáciou kmeňových krvotvorných buniek
- Dlouhodobé sledování pacienta s eozinofilním granulomem žebra
- Použití chemoterapie v kombinaci s cílenou biologickou léčbou u diseminovaného kolorektálního karcinomu: kazuistika dlouhodobé a výrazné klinické odpovědi
- Erratum
- Lékový registr – trabectedin
- Srovnání pegylovaného lipozomálního doxorubicinu a karboplatiny s paklitaxelem a karboplatinou v léčbě pacientek s pozdním relapsem platina-senzitivního karcinomu ovaria
- HER2 pozitivní T1N0M0 tumor: Čas pro změnu?
- Nový způsob smýšlení o rakovině (Poznámky k ESMO 2011)
- Zápis ze schůze výboru České onkologické společnosti ČLS JEP dne 18. 10. 2011 ve Fakultní Thomayerově nemocnici v Praze
- Zápis videokonference a schůze výboru České onkologické společnosti dne 4. 11. 2011 na MOÚ v Brně
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Castlemanova choroba
- Dlouhodobé sledování pacienta s eozinofilním granulomem žebra
- Lékový registr – trabectedin
- Prediktivní hodnota ultrazvukových parametrů, CA-125 a indexu rizika malignity u pacientek s karcinomem ovarií
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy