-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Lékový registr – trabectedin
Trabectedin Registry
Backgrounds:
The Yondelis® (trabectedin) project was initiated in January 2011 with the aim to obtain basic epidemiological information on patients with soft tissue sarcomas, standard treatment procedures, and results of trabectedin therapy in routine clinical practice. Expert patronage is provided by the Czech Society for Oncology, CzMA JEP. The project covers a representative sample of Comprehensive Cancer Care centres established to provide systematic treatment to patients with soft tissue sarcoma.Patients and Methods:
45 patients diagnosed with soft tissue sarcoma were retrospectively included in the database. Median age at the initiation of trabectedin therapy was 51 years (23–72 years). Leiomyosarcoma was the most frequent tumour (35.6%), synovial sarcoma occurred in 13.3% of patients; liposarcoma, peripheral nerve sheath tumours and unspecified sarcomas contributed 6.7% each. 62.2% of sarcomas were larger than 5 cm. Trabectedin was administered in a dose of 1.5 mg/m2 once in 3 weeks. 40% of patients received trabectedin as the 2nd line treatment, 35.6% as the 3rd line, and 34.4% as the 4th line. Results: Median number of administered cycles was 4 (1–10 cycles). Neutropenia (28.9% of patients) and elevated liver enzymes (26.7% of patients) were the most frequent adverse affects. 73.8% of patients terminated the therapy due to disease progression. Treatment response was recorded in 6.6% of patients (complete and partial remission), stable disease in 26.7%, and progression in 53.3%. Median overall survival (95% CI) was 11.7 months (9.6; 13.8), median progression-free survival (95% CI) was 3 months (2.4; 3.6).Conclusion:
Expert cancer societies have recently recommended trabectedin as the 2nd line palliative treatment for soft tissue sarcomas with documented effectiveness, particularly in liposarcomas and leiomyosarcomas, and good safety profile.Key words:
soft tissue sarcoma – chemotherapy – trabectedin – treatmentSubmitted:
18. 7. 2011Accepted:
8. 11. 2011
Autoři: K. Kubáčková 1; J. Fínek 2; R. Vyzula 3; M. Zvaríková 3; M. Vočka 4; S. Batko 1; J. Dreslerová 2; P. P. Lazarov 5; M. Lysý 6; Z. Ptáčková 7; V. Benešová 8; Z. Bortlíček 9; V. Kandrnal 9
Působiště autorů: Fakultní nemocnice v Motole, Praha 1; Fakultní nemocnice Plzeň 2; Masarykův onkologický ústav, Brno 3; Všeobecná fakultní nemocnice, Praha 4; Krajská nemocnice Liberec 5; Masarykova nemocnice Ústí nad Labem 6; Fakultní nemocnice Hradec Králové 7; Nemocnice Jihlava 8; Institut biostatistiky a analýz, MU Brno 9
Vyšlo v časopise: Klin Onkol 2011; 24(6): 470-474
Kategorie: Aktuality z registrů
Souhrn
Východiska:
Projekt Yondelis® (trabectedin) byl zahájen v lednu 2011 s cílem získat základní epidemiologické informace o pacientech se sarkomy měkkých tkání, o standardních postupech léčby a výsledcích léčby přípravkem trabectedin v běžné klinické praxi. Odbornou garanci nad projektem převzala Česká onkologická společnost ČSL JEP. Projekt reprezentativně pokrývá síť komplexních onkologických center, která se systematicky zabývají léčbou sarkomů měkkých tkání.Soubor pacientů a metody:
Do databáze bylo retrospektivně zařazeno 45 nemocných s diagnózou sarkomu měkkých tkání. Medián věku při zahájení terapie trabectedinem byl 51 let (23–72 let). V databázi se nejčastěji vyskytovali nemocní s leiomyosarkomem (35,6 %), synoviální sarkom se vyskytl u 13,3 % pacientů, liposarkom, maligní tumor periferních nervových pochev a blíže nespecifikované sarkomy byly zastoupeny každý u 6,7 % nemocných. Velikost větší než 5 cm dosáhlo 62,2 % sarkomů. Trabectedin byl podáván v dávce 1,5 mg/m2 1krát za 3 týdny. U 40 % nemocných byl podáván v II. linii léčby, u 35,6 % ve III. linii a u 24,4 % v linii IV. Výsledky: Medián podaných cyklů byl 4 (1–10 cyklů). Nejčastěji se vyskytujícím nežádoucím účinkem byla neutropenie u 28,9 % nemocných a elevace jaterních enzymů u 26,7 %. Celkem 73,8 % nemocných ukončilo léčbu pro progresi onemocnění. Léčebné odpovědi bylo dosaženo u 6,6 % nemocných (kompletní remise a parciální remise), u 26,7 % pacientů došlo ke stabilizaci onemocnění a u 53,3 % k progresi choroby. Medián celkového přežití (95% IS) je 11,7 měsíce (9,6; 13,8), medián přežití bez známek progrese (95% IS) 3 měsíce.Závěr:
Trabectedin je v současnosti doporučován onkologickými odbornými společnostmi jako druhá linie paliativní léčby u sarkomů měkkých tkání s prokázanou efektivitou především u liposarkomů a leiomyosarkomů s dobrým toxickým profilem.Klíčová slova:
sarkomy měkkých tkání – chemoterapie – trabectedin – léčbaVýchodiska
Cílem retrospektivního přehledu bylo získat základní epidemiologická data o pacientech se sarkomy měkkých tkání léčených trabectedinem v komplexních onkologických centrech v období 2008–2010 v podmínkách běžné klinické praxe. Trabectedin je látka původně izolovaná z mořského živočicha Ecteinascidia turbinata. Patří mezi alkylační činidla; mechanizmus jeho antiproliferačního účinku spočívá ve vazbě na DNA a interferenci s jejími reparačními procesy [1–4].
Soubor pacientů a metody
Údaje byly získány z databáze, do které byla anonymně konsekutivně ukládána data. Léčba i frekvence sledování byly v kompetenci zadávajícího lékaře, který do databáze zaznamenával informace o výsledcích a nežádoucích účincích léčby. Do databáze bylo zařazeno 45 nemocných léčených v období 2008–2010, z toho bylo 55,6 % žen a 44,4 % mužů. Medián věku při stanovení diagnózy byl 47 let (21–70 let) a 51 let (23–72 let) při zahájení terapie trabectedinem. Věkové rozložení při stanovení diagnózy a při zahájení léčby udává obr. 1. Dva nemocní před stanovením diagnózy sarkomu podstoupili radioterapii, u ostatních pacientů nebyl zaznamenán žádný rizikový faktor pro vznik sarkomů měkkých tkání, jako jsou známé genetické mutace, expozice k chemickým karcinogenům, chronický lymfedém či jiný známý rizikový faktor. Funkční stav pacienta byl hodnocen dle Karnofského indexu (KI). U 62,2 % nemocných byl KI 90–100 % a 26,7 % pacientů mělo KI 70–80 %. U 5 nemocných nebyl funkční stav uveden. Nejčastějším histologickým typem sarkomů v souboru byl leiomyosarkom u 35,6 % pacientů a synoviální sarkom u 13,3 %; liposarkom, maligní tumor periferních nervových pochev a blíže nespecifikované sarkomy byly zastoupeny u stejného počtu pacientů – 6,7 %. Výskyt dalších typů tumoru ukazuje tab. 1. U všech typů sarkomů byla diagnóza potvrzena histopatologicky, u 77,8 % byla doplněna imunohistochemickým vyšetřením a u 3,6 % sarkomů bylo provedeno molekulárně-genetické vyšetření.
Obr. 1. Věková struktura pacientů. 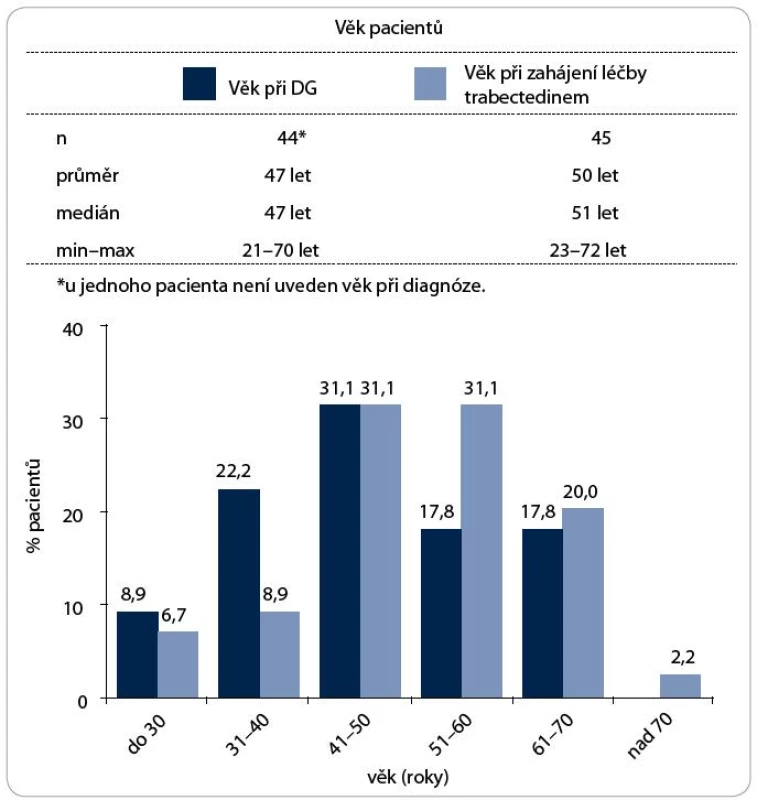
Tab. 1. Histologický typ nádoru. 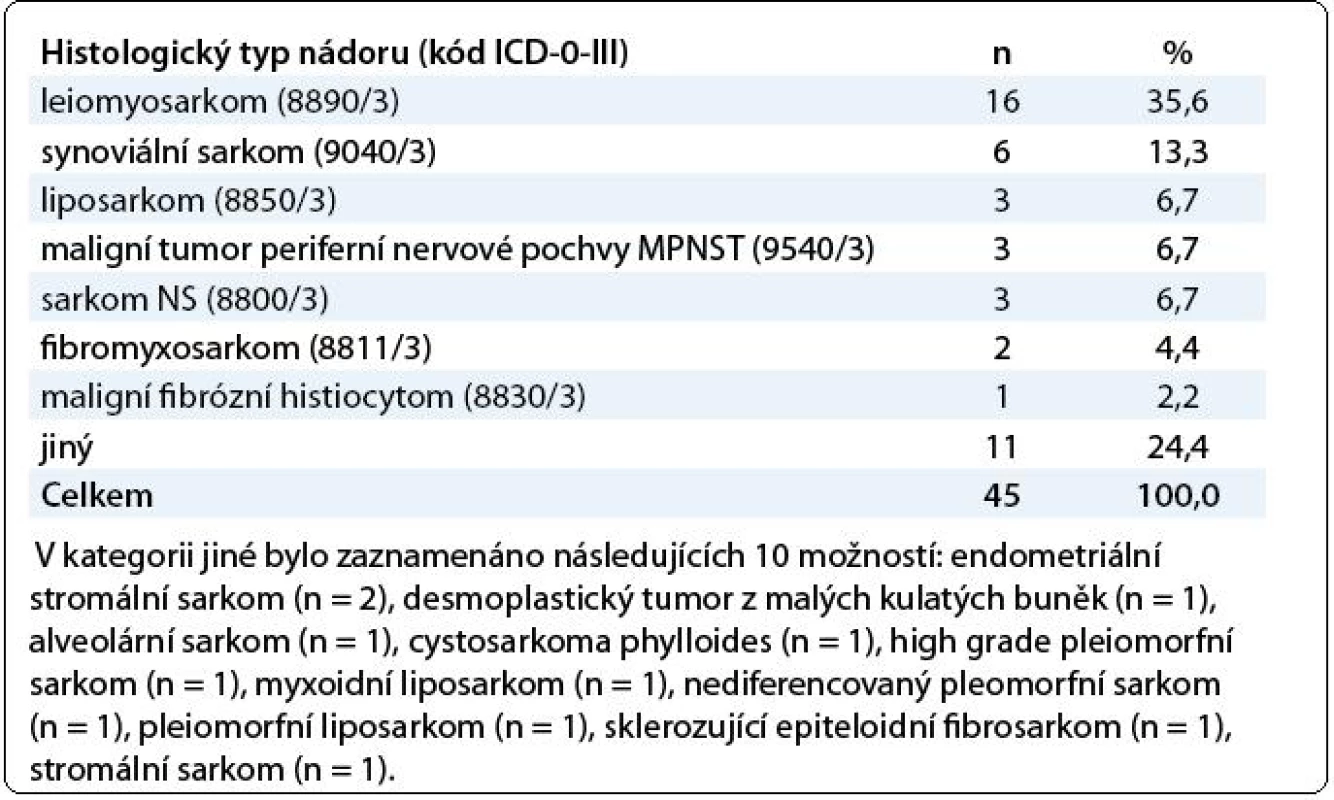
Téměř polovina sarkomů (48,9 %) byla diagnostikována s nádorovým grade 3, u 20 % byl stanoven nádorový grade 2, u 6,7 % grade 4 a u 4,4 % tumorů grade 1. U 26,7 % nemocných byl sarkom lokalizován na dolních končetinách, v 15,6 % se jednalo o sarkom dělohy, u 11,5 % byl tumor lokalizován v dutině břišní, u 6,7 % se nádor nacházel v retroperitoneu a u stejného počtu v oblasti hlavy a krku. V době primární diagnózy bylo 17,8 % nádorů uloženo povrchově nad superficiální facií, v hloubce bylo lokalizováno 48,9 % tumorů a u 33,3 % nemocných nebyla informace o uložení relevantní. U 13,3 % nemocných byl primárně diagnostikován tumor o velikosti 2–5 cm, u 37,8 % nemocných byl tumor velikosti 6–10 cm, 24,4 % nemocných bylo diagnostikováno s tumorózní rezistencí přesahující 10 cm a u stejného procenta nemocných nebyla velikost primárního tumoru určena. S klinickými projevy onemocnění zahájilo léčbu 80 % nemocných, 20 % nemocných bylo asymptomatických. 63,9 % nemocných bylo prezentováno s klinicky manifestní progredující tumorózní rezistencí, u 33,3 % nemocných se tumorózní proces projevoval tlakem na lokální struktury, u 3 nemocných bylo jediným příznakem gynekologické krvácení, u dvou dušnost a ulcerace.
U 53,7 % pacientů byla provedena kompletní resekce tumoru v době diagnózy, u 46,4 % nebyl radikální chirurgický výkon možný. V databázi sledovaných pacientů byla léčba trabectedinem zahájena u 40 % nemocných ve II. linii paliativní chemoterapie, u 35,6 % ve III. linii a u 24,4 % v linii IV. Trabectedin byl podáván v dávce 1,5 mg/m2 ve 24hodinové kontinuální infuzi do centrálního žilního řečiště v 3týdenním intervalu. Medián podaných cyklů byl 4 (rozmezí 1–10) a medián délky léčby byl 10 týdnů (rozmezí 1–38 týdnů) – viz obr. 2. Léčba trabectedinem byla zahájena u 37,8 % pacientů s KI 90–100 %, 48,9 % nemocných mělo KI 70–80 %, 13,3 % nemocných mělo KI 50–60 %. V době zahájení léčby trabectedinem bylo 95,6 % nemocných ve IV. stadiu onemocnění, pouze 4,4 % mělo stadium III. Přežití pacientů bylo hodnoceno metodikou podle Kaplana a Meiera.
Obr. 2. Počet cyklů léčby a celková délka léčby. 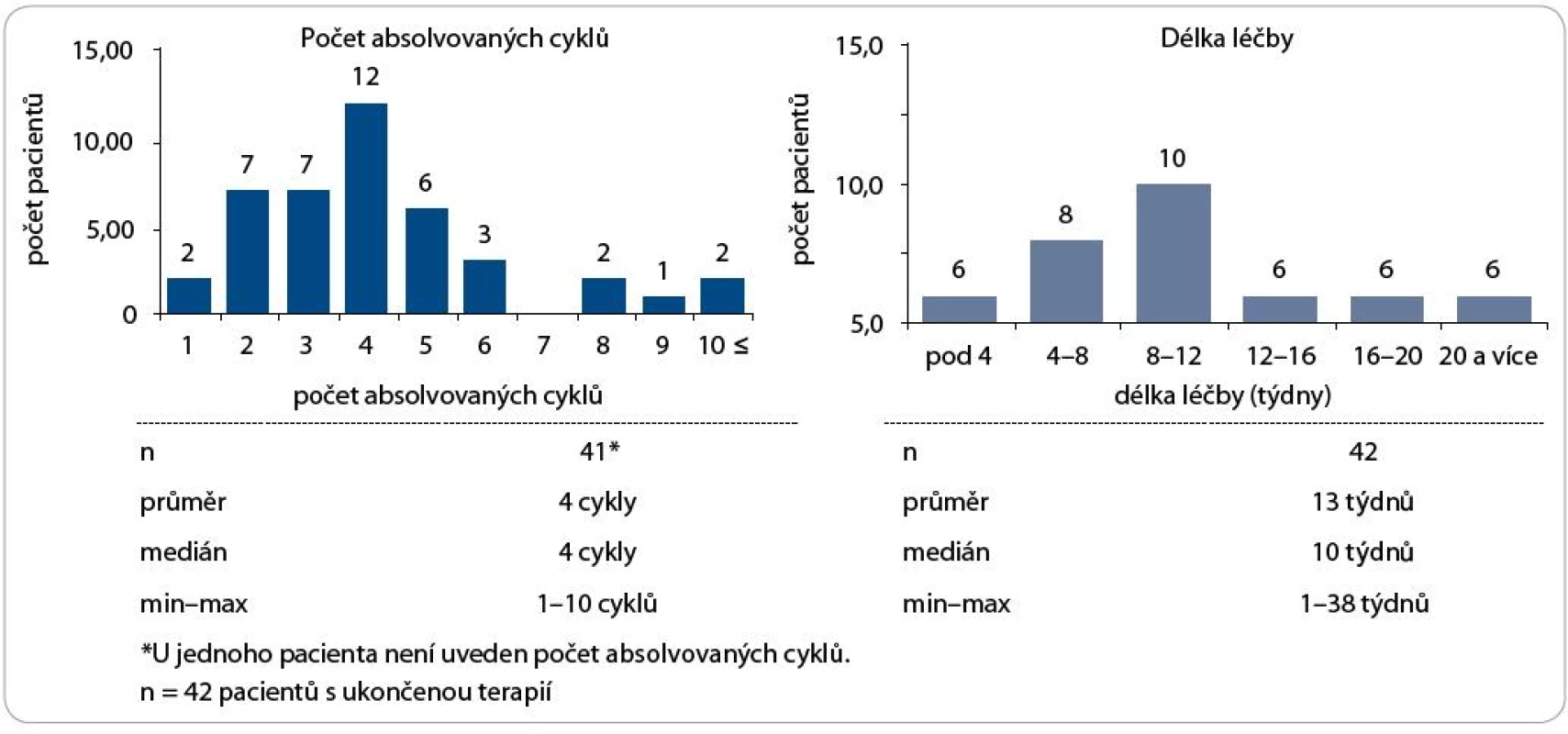
Výsledky léčby trabectedinem
Léčebné odpovědi bylo dosaženo u 6,6 % nemocných (kompletní remise a parciální remise), u 26,7 % nemocných byla zaznamenána stabilizace onemocnění (tab. 2). Medián celkového přežití (95% IS) byl 11,7 měsíce (9,6; 13,8) a medián doby do progrese (95% IS) 3 měsíce (2,4; 3,6). Celkové přežití v jednom roce (95% IS) bylo 49,4 % (31,7; 67,1), v 18 měsících (95% IS) přežívalo 32,3 % (14,1; 50,4). Ve 3 měsících bylo bez progrese onemocnění 48,4 % (32,9; 63,9) nemocných, v 6 měsících bez progrese onemocnění přežívalo 19,2 % (6,1; 32,3) nemocných (obr. 3). V době analýzy dat byla u 73,8 % nemocných léčba ukončena pro progresi onemocnění, u 6,7 % léčba pokračovala, 48,9 % nemocných zemřelo a 40 % žilo, u 5 nemocných nebyl stav znám.
Tab. 2. Nejlepší dosažená léčebná odpověď na léčbu trabectedinem. 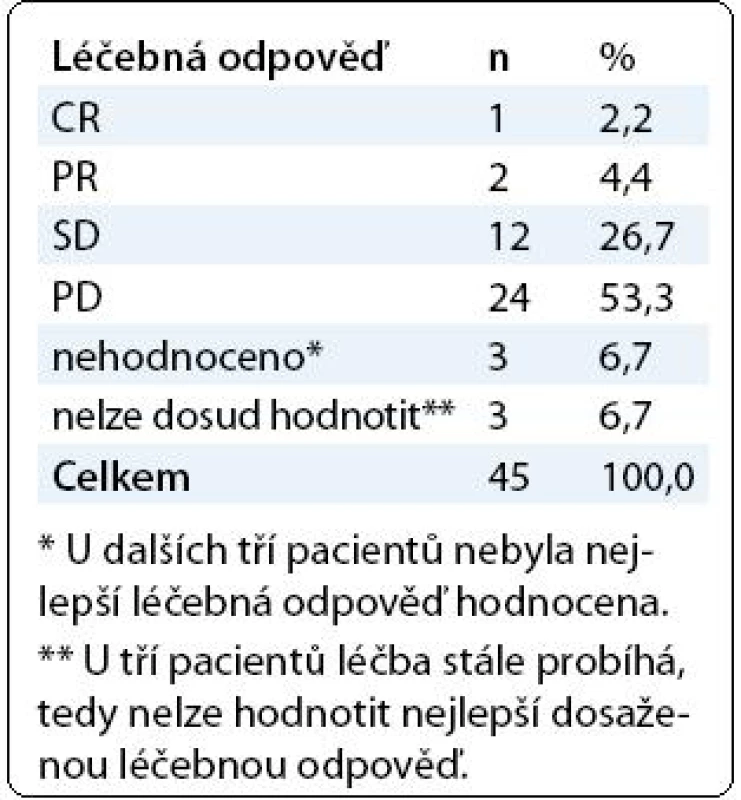
Obr. 3. Celkové přežití a přežití bez známek progrese. 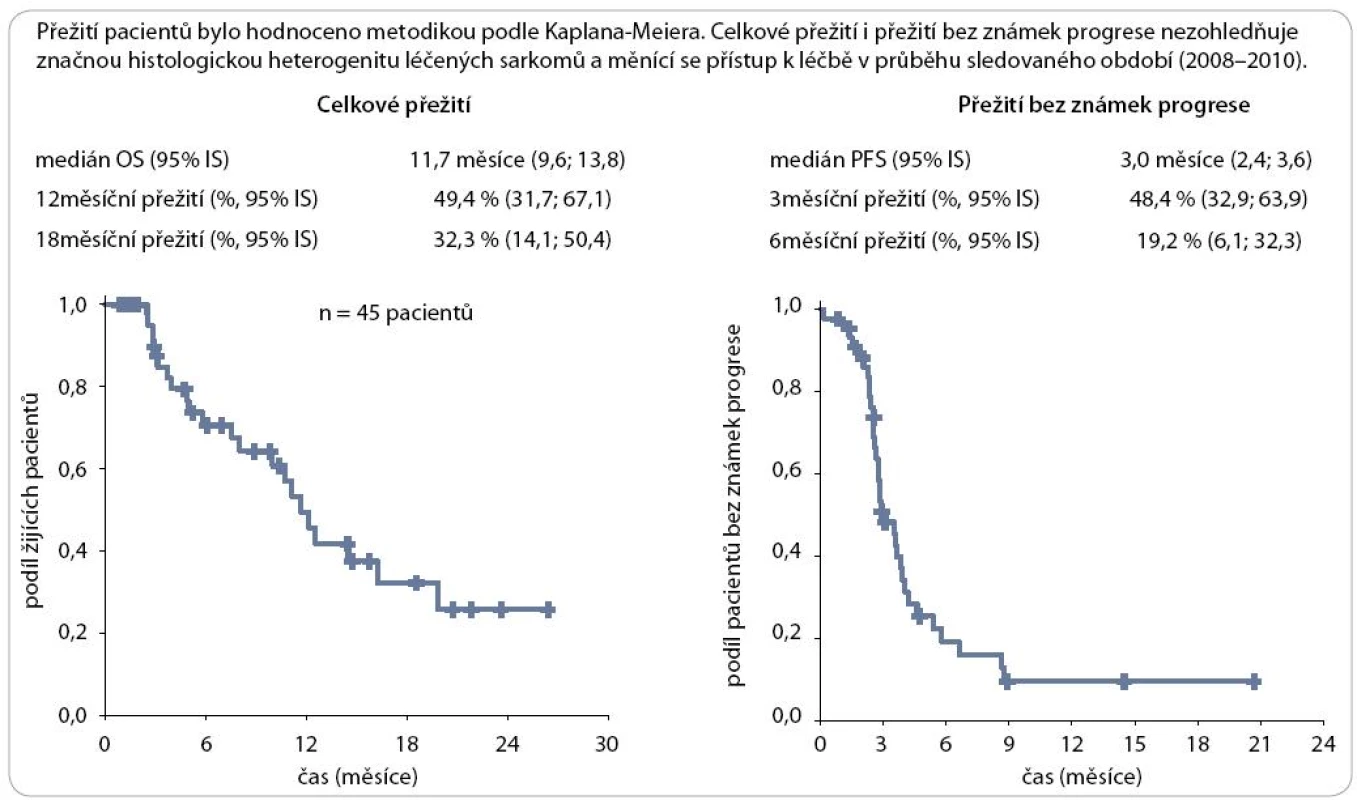
Nejčastěji se vyskytujícím nežádoucím účinkem byla neutropenie u 28,9 % nemocných, elevace jaterních enzymů u 26,7 %, snížení renálních testů u 4,4 % a anémie a trombocytopenie u 2,2 % nemocných.
Diskuze
Sarkomy měkkých tkání představují značně heterogenní skupinu vzácných maligních onemocnění. Určení histologického typu nádoru je jednou z klíčových podmínek pro správnou volbu léčebného algoritmu. Řada autorů doporučuje doplnění histologického a imunohistochemického vyšetření ke zpřesnění diagnostiky dalšími metodikami, jako jsou například molekulárně-genetická vyšetření [5–8]. Doporučováno je též druhé čtení na specializovaných pracovištích, která se systematicky věnují diagnostice sarkomů. Dle údajů Národního onkologického registru se incidence sarkomů měkkých tkání v České republice pohybovala v letech 2000–2008 v rozmezí 3,26–3,59 případu na 100 000 obyvatel za rok [9]. Z hlediska incidence není rozdíl v populaci mužů a žen. V databázi trabectedinu mírně převažovaly ženy (55,6 %) nad muži (44,4 %). V České republice se sarkomy měkkých tkání vyskytují nejčastěji mezi 50. a 70. rokem věku. Medián věku pacientů při stanovení diagnózy v našem souboru byl 47 let, v době zahájení terapie trabectedinem byl 51 let, tedy odpovídající věkovému rozmezí výskytu sarkomů. Léčba generalizovaných sarkomů měkkých tkání je paliativní, jejím základním cílem je zpomalení růstu nádoru, zmírnění symptomů onemocnění a zlepšení kvality života. Medián přežívání v době diagnózy metastatického onemocnění je 12 měsíců, pouze 20–25 % nemocných přežívá 2 roky. Zlatým standardem první linie paliativní chemoterapie je doxorubicin. U vybrané skupiny nemocných v dobrém klinickém stavu, kde chceme dosáhnout rychlého efektu léčby, je možná kombinovaná terapie doxorubicinu s ifosfamidem. Trabectedin byl v roce 2007 schválen agenturou EMA pro léčbu pokročilých sarkomů měkkých tkání u nemocných, u nichž selhala léčba antracykliny či ifosfamidem, nebo pro pacienty, kteří nejsou vhodní pro tuto terapii [10]. Data o jeho účinnosti byla doložena pro leiomyosarkomy a liposarkomy na základě randomizované studie fáze II srovnávající účinnost a bezpečnost dvou různých léčebných schémat u pacientů po selhání předchozí terapie antracykliny a ifosfamidem [11]. Leiomyosarkom byl v našem souboru nemocných léčených trabectedinem nejčastějším typem sarkomu. Výsledky léčby trabectedinem u všech typů sarkomů v databázi jsou srovnatelné s výsledky v registrační studii – přežití bez známek progrese onemocnění 3 měsíce, v registrační studii 3,7 měsíce, medián celkového přežití 11,7 měsíce ve srovnání s 13,9 měsíce v randomizované registrační studii. Výskyt nežádoucích účinků byl zaznamenán u 46,7 % nemocných a pouze u dvou nemocných se jednalo o závažné nežádoucí účinky. Nežádoucí účinky nebyly důvodem k ukončení terapie trabectedinem. Ve shodě se známým toxickým profilem trabectedinu byla nejčastěji zaznamenaným nežádoucím účinkem neutropenie a elevace jaterních enzymů. Žádný pacient neukončil léčbu pro toxicitu. Dle doporučení České onkologické společnosti je trabectedin indikován k léčbě liposarkomů, leiomyosarkomů a synovialosarkomů po selhání terapie doxorubicinem v kombinaci či bez předléčení ifosfamidem [12]. Dle doporučení ESMO (European Society of Medical Oncology) je trabectedin možnou volbou pro II. linii léčby u leiomyosarkomů a liposarkomů, s pozorovanou léčebnou odpovědí u myxoidních liposarkomů a synoviálních sarkomů [13]. Během našeho tříletého sledování je patrný měnící se trend zahájení léčby trabectedinem. Zatímco v roce 2008, kdy získal registraci a jeho dostupnost byla omezená, byl trabectedin nasazován převážně ve třetí či další linii; v roce 2010 již byla léčba trabectedinem zahájena u 55,6 % pacientů v rámci druhé linie léčby. Tato skutečnost značně komplikuje provedenou analýzu přežití a determinuje dosažitelnost výsledků. Při indikaci léčby trabectedinem bychom měli zvažovat histologický typ sarkomu a celkový stav nemocného s jeho komorbiditami tak, aby mohlo být dosaženo maximálního efektu [14–16].
Závěr
Trabectedin je registrován pro léčbu sarkomů měkkých tkání po selhání doxorubicinu a ifosfamidu či pro nemocné, kteří nejsou indikováni k této léčbě. Lékový registr trabectedinu zahrnuje 45 nemocných. Výsledky léčby i toxický profil trabectedinu jsou srovnatelné s výsledky registrační studie. Snahou ČOS je koncentrovat léčbu pacientů se sarkomy měkkých tkání do komplexních onkologických center, která mají s léčbou tohoto onemocnění zkušenosti a jsou schopna zajistit multidisciplinární přístup, který léčba těchto vzácných nádorů vyžaduje. Jenom tak může být zaručena správná indikace léčby.
MUDr. Vít Kandrnal
Institut biostatistiky a analýz
MU Brnoa
Kotlářská 2
611 37 Brno
e-mail: kandrnal@iba.muni.cz
Obdrženo: 18. 7. 2011
Přijato: 8. 11. 2011
Zdroje
1. Carter NJ, Keam SJ. Trabectidin: a review of its use in soft tissue sarcoma and ovarian cancer. Drugs 2010; 70(3): 355–376.
2. Chuk MK, Balis FM, Fox E. Trabectedin. Oncologist 2009; 14(8): 794–799.
3. Schöffski P, Dumez H, Wolter P et al. Clinical impact of trabectedin (ecteinascidin-743) in advanced/metastatic soft tissue sarcoma. Expert Opin Pharmacother 2008; 9(9): 1609–1618.
4. Blay JY, von Mehren M, Samuels BK et al. Phase I combination study of trabectidin and doxorubicin in patients with soft-tissue sarcoma. Clin Cancer Res 2008; 14(20): 6656–6662.
5. Clark MA, Fisher C, Judson I et al. Soft-tissue sarcomas in adults. N Engl J Med 2005; 353(7): 701–711.
6. Hogendoorn PC, Collin F, Daugaard S et al. Changing concepts in the pathological basis of soft tissue and bone sarcoma treatment. Eur J Cancer 2004; 40(11): 1644–1654.
7. Veselý K. Histopatologická diagnostika nádorů měkkých tkání. Onkologie 2010; 4(5): 293–296.
8. Cormier JN, Pollock RE. Soft tissue sarcomas. CA Cancer J Clin 2004; 54(2): 94–109.
9. Dušek L, Mužík J, Kubásek M et al. Epidemiologie zhoubných nádorů v České republice [online]. Masarykova univerzita 2005 [cit. 2011-4-27]. Dostupný z http://www.svod.cz.
10. Yondelis Summary of Product Characteristics SPC. EMA 2010. Available from: http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_Product_Information/human/000773/WC500045832.pdf.
11. Demetri GD, Chawla SP, von Mehren M et al. Efficacy and safety of trabectedin in patients with advanced or metastatic liposarcoma or leiomyosarcoma after failure of prior anthracyclines and ifosfamide: results of a randomized phase II study of two different schedules. J Clin Oncol 2009; 27(25): 4188–4196.
12. Vyzula R et al. Zásady cytostatické léčby maligních onkologických onemocnění. 13. vydání. Brno: Masarykův onkologický ústav 2011.
13. Casali PG, Blay JY. ESMO/CONTICANET/EUROBONET Consensus Panel of Experts. Soft tissue sarcomas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2010; 21 (Suppl 5): v198–v203.
14. Schöffski P, Taron M, Jimeno J et al. Predictive impact of DNA repair functionality on clinical outcome of advanced sarcoma patients treated with trabectedin: a retrospective multicentric study. Eur J Cancer 2011; 47(7): 1006–1012.
15. Ray-Coquard I. An increasing role for trabectidin in gynecological cancers: efficacy in uterine sarcomas. Int J Gynecol Cancer 2011; 21 (10 Suppl 1): S3–S5.
16. Scurr M. Histology-driven chemotherapy in soft tissue sarcomas. Curr Treat Options Oncol 2011; 12(1): 32–45.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2011 Číslo 6- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Fixní kombinace tramadol/paracetamol je doporučenou volbou v léčbě chronické bolesti v ordinaci praktického lékaře
-
Všetky články tohto čísla
- Pozitronová emisní tomografie v diagnostice a sledování pacientů s neseminomovými germinálními nádory
- Plazminogen aktivátor systém a jeho klinický význam u pacientů s nádorovým onemocněním
- Castlemanova choroba
- Prediktivní hodnota ultrazvukových parametrů, CA-125 a indexu rizika malignity u pacientek s karcinomem ovarií
- Naše päťročné výsledky in vitro testovania chemorezistencie u onkologických pacientov
- Aktuálne charakteristiky deskriptívnej epidemiológie nádorov žalúdka v Slovenskej republike v kontexte medzinárodného porovnania
- Neskoré následky u pacientov liečených alogénnou transplantáciou kmeňových krvotvorných buniek
- Dlouhodobé sledování pacienta s eozinofilním granulomem žebra
- Použití chemoterapie v kombinaci s cílenou biologickou léčbou u diseminovaného kolorektálního karcinomu: kazuistika dlouhodobé a výrazné klinické odpovědi
- Erratum
- Lékový registr – trabectedin
- Srovnání pegylovaného lipozomálního doxorubicinu a karboplatiny s paklitaxelem a karboplatinou v léčbě pacientek s pozdním relapsem platina-senzitivního karcinomu ovaria
- HER2 pozitivní T1N0M0 tumor: Čas pro změnu?
- Nový způsob smýšlení o rakovině (Poznámky k ESMO 2011)
- Zápis ze schůze výboru České onkologické společnosti ČLS JEP dne 18. 10. 2011 ve Fakultní Thomayerově nemocnici v Praze
- Zápis videokonference a schůze výboru České onkologické společnosti dne 4. 11. 2011 na MOÚ v Brně
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Castlemanova choroba
- Dlouhodobé sledování pacienta s eozinofilním granulomem žebra
- Lékový registr – trabectedin
- Prediktivní hodnota ultrazvukových parametrů, CA-125 a indexu rizika malignity u pacientek s karcinomem ovarií
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



