-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Doporučení pro diagnostiku a léčbu onemocnění štítné žlázy v těhotenství a pro ženy s poruchou fertility
Vyšlo v časopise: Klin. Biochem. Metab., 21 (42), 2013, No. 1, p. 41-64
Kategorie: Doporučení
Obsah
Souhrn
- Obecný úvod
- 1.1 Proč Guidelines upravujeme pro ČR?
- 1.2 Úvod do problematiky funkčních tyreopatií a těhotenství
- 1.3 Choroby štítné žlázy v graviditě – stručný přehled
- Funkční tyreoidální testy v graviditě
- 2.1 Změny hladin hormonů v těhotenství
- 2.1.1 Tyreotropin (TSH)
- 2.1.2 Volný tyroxin (FT4)
- 2.1.3 Autoprotilátky
- 2.1.4 Jodurie
- 2.2 Stanovení referenčních intervalů
- 2.2.1 Referenční intervaly pro TSH a FT4
- 2.2.2 Rozhodovací meze – cut off pro Anti-TPO
- 2.1 Změny hladin hormonů v těhotenství
- Hypotyreóza
- 3.1 Definice hypotyreózy
- 3.2 Horní mez TSH v těhotenství
- 3.3 Rizika hypotyreózy v těhotenství
- 3.3.1 Manifestní (overt) hypotyreóza
- 3.3.2 Subklinická hypotyreóza
- 3.4 Prevence a léčba hypotyreózy v těhotenství a po porodu
- 3.4.1 Prevence, informovanost
- 3.4.2 Léčba hypotyreózy v těhotenství
- 3.5 Eufunkční ženy s průkazem protilátek v těhotenství
- 3.5.1 Riziko rozvoje hypotyreózy v průběhu těhotenství u (dosud) eutyroidních žen s pozitivními Anti-TPO
- 3.5.2 Riziko porodnických komplikací u (dosud) eutyroidních žen s pozitivními Anti-TPO
- 3.5.3 Rizika po porodu, poporodní tyreoiditida (PPT)
- Význam jodu v graviditě
- 4.1 Význam jodu pro lidský organizmus a jeho zdroje
- 4.2 Mění těhotenství potřebu jodu?
- 4.3 Jaké jsou důsledky nedostatku jodu v těhotenství?
- 4.4 Jak lze hodnotit zásobení jodem v těhotenství?
- 4.5 Jak řešit optimalizaci přívodu jodu v těhotenství?
- Tyreotoxikóza, tranzientní gestační hypertyreóza
- 5.1 Úvod
- 5.2 Hypertyreóza (Tx) v graviditě
- 5.2.1 Klinický obraz
- 5.2.2 Laboratorní nálezy u Tx v graviditě
- 5.2.3 Léčba Tx v graviditě
- 5.2.4 Prekoncepční odhalení rizika Tx a preventivní opatření
- 5.3 Tranzientní gestační hypertyreóza (TGH)
- 5.3.1 Klinický, laboratorní a sonografický obraz TGH
- 5.3.2 Léčba TGH
- 5.4 Endokrinní orbitopatie v graviditě
- Ženy s infertilitou, po potratu a po předčasném porodu
- 6.1 Úvod
- 6.2 Ženy se zvýšeným rizikem infertility, potratů a předčasných porodů z důvodu tyreopatií
- 6.3 Léčba tyreopatií u žen s infertilitou, po potratu či předčasném porodu
- 6.4 Faktory, které u žen s infertilitou, po potratu či předčasném porodu podporují zahájení léčby hraničních stavů levotyroxinem
- Struma, uzlová přestavba ve štítné žláze
- 7.1 Struma difúzní
- 7.2 Struma uzlová, uzly ve štítné žláze
- 7.2.1 Gravidita a uzlová přestavba
- 7.2.2 Vyšetření uzlů v graviditě
- 7.2.3 Postup při nálezu (benigního) uzlu
- 7.2.4 Malignita na základě FNAB u gravidních žen
- 7.2.5 Nejistý – hraniční suspektní výsledek FNAB
- Karcinom štítné žlázy v graviditě
- 8.1 Výskyt
- 8.2 Ovlivňuje gravidita růst karcinomu tyreoidey?
- 8.3 Jak řešit průkaz (podezření) papilárního karcinomu?
- 8.4 Gravidita u ženy, již dříve léčené pro diferencovaný karcinom tyreoidey
- 8.5 Hladiny TSH u ženy, která prodělala léčbu pro diferencovaný karcinom tyreoidey, při plánování gravidity a v jejím průběhu
- 8.6 Zvyšuje gravidita riziko rekurence diferencovaného tyreoidálního karcinomu?
- 8.7 Operace štítné žlázy v graviditě u eufunkční ženy
- Screening tyreopatií v graviditě
- 9.1 Úvod
- 9.2 Rozsah screeningu – univerzální nebo cílený?
- 9.3 Načasování screeningu
- 9.3.1 Těhotenský screening
- 9.3.2 Prekoncepční screening
- 9.4 Co v rámci screeningu vyšetřovat?
- 9.5 Jak postupovat při pozitivním screeningu?
- 9.6 Finanční zajištění screeningu
Seznam zkratek
Souhrn
Vzhledem ke specifičnosti tyreoidálních onemocnění považuje Česká endokrinologická společnost ČLS JEP za nezbytné se k doporučením vydaným ATA, ETA a Endocrine Society [1-4] stručně vyjádřit a připojit některé připomínky ohledně diagnostiky a léčby v České republice při respektování obecných principů zmíněných doporučení.
- Tyreoidální laboratorní parametry v graviditě (kapitola 2)
Pro základní zhodnocení stavu štítné žlázy v těhotenství se doporučuje vyšetření tří parametrů: TSH, FT4 a Anti -TPO protilátek. Tyreotropní aktivita choriového gonadotropinu (hCG) vede ke snížení hladiny TSH na začátku těhotenství a horní hranice pro TSH v graviditě je tedy nižší než pro běžnou populaci. Normy pro TSH jsou specifické pro každý trimestr.
Stanovení FT4 umožňuje zjistit množství biologicky dostupného tyroxinu pro těhotnou ženu i její plod, nicméně výsledky vyšetření FT4 jsou ovlivněny použitou metodou a jsou nejméně spolehlivým tyreoidálním markerem v těhotenství.
Vyšetření Anti-TPO protilátek je nezbytným podkladem pro hodnocení stavu štítné žlázy - u žen s jejich pozitivitou se může v těhotenství rozvinout některá z poruch štítné žlázy a také naznačuje nebezpečí výskytu poporodní tyreoiditidy. Jejich přítomnost může být i bez poruchy funkce štítné žlázy asociována s neplodností, opakovaným potrácením, selháním metod asistované reprodukce a snad i dalšími dopady na plod.
Vyšetření protilátek proti TSH receptoru (TRAK) slouží k diferenciální diagnóze hypertyreózy a posouzení dynamiky GB-toxikózy; tyto protilátky přecházejí transplacentárně.
- Hypotyreóza (kapitola 3)
Pro vstupní diagnózu hypotyreózy v těhotenství využíváme stanovení TSH a FT4. Horní mez normálního rozmezí TSH je závislá na trimestru, populaci a metodě. Jako zjevnou (overt) hypotyreózu označíme zvýšení TSH nad horní mez spolu se snížením FT4 , jako subklinickou hypotyreózu označíme zvýšení TSH při normálním FT4. Vyšetření Anti-TPO je neoddělitelnou součástí vyšetření k určení etiologie i perspektivy choroby. Ženy v reprodukčním věku, ať již léčené pro hypotyreózu nebo pouze sledované pro chronickou lymfocytární tyreoiditidu, mají být poučeny o vyšších nárocích na tyreoidální hormony v těhotenství. Mají vyhledat svého endokrinologa před plánovaným otěhotněním nebo co nejdříve po zjištění těhotenství. Žena, již léčená pro hypotyreózu, má po zjištění těhotenství zvýšit dávku levotyroxinu průměrně asi o 30 % a navštívit ihned endokrinologa, který má stávající nebo zahájenou dávku levotyroxinu upravovat na cílový TSH: před graviditou na TSH méně 2,5 mIU/l, v graviditě na TSH pro příslušnou metodu a trimestr. U žen s nově diagnostikovanou hypotyreózou v graviditě a žen se subklinickou hypotyreózou a pozitivními Anti-TPO protilátkami a/nebo UZ nálezem postupujeme obdobně. Je-li pouze mírná elevace TSH (negativní protilátky a normální nález na UZ tyreoidey), není chybou zahájit léčbu podle výše uvedených zásad (potenciální benefit a nevýznamné riziko) ani léčbu nezahajovat a pouze sledovat vývoj; rozhodnutí bude záviset na preferenci endokrinologa. Síla tohoto doporučení je menší pro absenci jednoznačných důkazů. Pro léčbu izolované hypotyroxinémie (TSH v normě, protilátky negativní) nejsou důkazy a tedy léčba není indikována, pokud však pacientka trpí nedostatkem jodu, je nutné zajistit doporučené denní dávky. Sledování těhotných žen s hypotyreózou (zjevnou i subklinickou, léčené i neléčené) má být do 20. gestačního týdne každé cca 4 týdny (např. 5. - 6., 10., 14. a 20. týden ± 1 týden) vyšetřením TSH v krvi, případně mezi 28. a 32. gestačním týdnem. Tento termín může být při stabilizaci stavu vynechán. Nutné je vyšetření TSH 4-6 týdnů po porodu a dále 3, 6, 12 a 24 měsíců po porodu., aby se zachytil případný rozvoj poporodní tyreoiditidy u žen s chronickou lymfocytární tyreoiditidou či aktivita Gravesovy-Basedowovy choroby, a aby se upravila dávka substituční léčby. Substituce se po porodu obvykle vrací na dávku před otěhotněním.
- Eufunkční ženy s průkazem protilátek (kapitola 3)
Léčba eufunkčních žen s průkazem protilátek a s normálním vstupním TSH je spíše doporučena, a to malou dávkou levotyroxinu (50 µg/den). Léčba má zabránit rozvoji hypotyreózy během těhotenství, cílové hodnoty TSH jsou jako u žen s prokázanou hypotyreózou. Kontroly, obdobně jako péče po porodu, jsou stejné jako u žen s hypotyreózou. Asi polovina eufunkčních žen s průkazem protilátek a s normálním vstupním TSH progreduje po porodu do trvalé hypotyreózy.
- Zásobení jodem v graviditě (kapitola 4)
Stavům zásobení jodem u gravidních žen v české populaci bude nutno věnovat i v budoucnosti zvýšenou pozornost vzhledem k tomu, že nedostatečný přívod jodu v těhotenství ohrožuje dvě generace – těhotnou ženu i vyvíjející se plod. Nepříznivé důsledky pro plod by znamenaly snížení kvality budoucích generací. U všech těhotných a kojících žen se doporučuje plošná suplementace jodem v dávce 100 µg elementárního jodu denně nad rámec běžného příjmu v potravě.
- Tyreotoxikóza (kapitola 5)
Tyreotoxikóza v graviditě se vyskytuje nejvýše u 0,5 % těhotných žen. Klinické projevy se v podstatě neliší od běžné populace, vzhledem k věku převažuje výskyt autoimunitních forem (GB choroba) nad jinými etiologiemi. Onemocnění je nutno odlišit od přechodné gestační suprese TSH v 1. trimestru gravidity (tranzientní gestační hypertyreóza netyreoidálního původu), která je vyvolána zvýšenou produkcí tyreostimulačních látek (hCG) v placentě. Diagnostika tyreotoxikózy se opírá o vyšetření TSH a FT4 (eventuálně FT3) a TRAK, případně ultrazvuk štítné žlázy. Základem léčby je podávání tyreostatik, v 1. trimestru propylthiouracylu (CAVE hepatální léze) a pak methimazolu. Aktivita tyreotoxikózy v graviditě obvykle při léčbě spontánně klesá, po porodu často stoupá. Podávání nízkých a středních dávek tyreostatik neovlivňuje nepříznivě průběh gravidity, vývoj plodu ani nitroděložně ani po porodu v rámci kojení. V budoucnosti bude optimálním postupem v rámci plánovaného rodičovství odhalit tyreotoxikózu již před početím a účinně jí zaléčit. Uvedené zásady odpovídají doporučení ATA + ETA, v detailech se postupy doporučené různými experty mohou lišit. Není plné shody na podávání jodu u těhotných žen s tyreotoxikózou, v ČR ho doporučujeme vzhledem k nutnosti zajistit dostatek jodu pro optimální vývoj plodu. Endokrinní orbitopatie v graviditě je vzácná a léčebné postupy se příliš neliší od běžné populace. Jde-li o aktivní zrak ohrožující EO je na místě podání vysokých dávek kortikoidů (methylprednisolon) v intravenózních pulsech. Kumulativní dávka by měla být co nejmenší při zachování účinnosti. Obvykle je snaha podávat dávky menší než u netěhotných - kumulativně do 2-3 g během 6 týdnů. Vzácně, není-li patrný efekt, je třeba přistoupit i k chirurgické dekompresi orbity.
- Postup u žen s infertilitou, po potratu a po předčasném porodu (kapitola 6)
Vyšetření TSH a Anti-TPO v krvi by mělo být provedeno u všech žen s infertilitou, po potratu, předčasném porodu či u žen s jinak komplikovaným těhotenstvím, které plánují nebo usilují o další graviditu. Podrobný diagnostický a léčebný postup je uveden v textu kapitoly 6.
- Struma a tyreoidální uzly (kapitola 7)
Péče o ženy se strumou a uzly ve štítné žláze v graviditě je obdobná jako u žen netěhotných, s tou výjimkou, že s určením etiologie spěcháme až urgentně, dle charakteru uzlu. V oblastech s mírným jodovým deficitem nebo hraničním jodovým zásobením mají již preexistující uzly v průběhu gravidity tendenci ke zvětšení, a nový uzel se objeví asi u 15 % žen. Léčba vychází z etiologie, snažíme se respektovat přání nemocné, supresní léčba v graviditě není vhodná. Při nejistém nálezu (Bethesda III. a lV.) je možné operaci odložit po porodu, obdobně jako při FNAB nálezu mikrokarcinomu. Hladina TSH má být spíše na dolní hranici normálu. Pokud si žena přeje řešení dříve, je operace možná ke konci 2. trimestru. Substituci je nutné zahájit ihned po operaci.
- Karcinom štítné žlázy (kapitola 8)
Při silném podezření či průkazu karcinomu ve štítné žlázce je léčba gravidních stejná jako u netěhotných – operace. Léčba radiojodem následuje po porodu, případně po ukončení kojení. Většina studií nepovažuje graviditu za zhoršující riziko, a tudíž operace může být odložena. Autoři doporučení pro ČR však spíše podporují radikálnější variantu. Doporučení ATA 2011 se opírají pouze o studie retrospektivní, nikoliv randomizované. Operace by se určitě měla ještě v graviditě uskutečnit u medulárního karcinomu a tumoru s metastázami. Operace štítné žlázy ve 2. trimestru v rukou zkušeného chirurga není spojena se zvýšeným rizikem matky či plodu, nicméně indikace k operaci musí být opřena o jasný nález. Operaci mikrokarcinomu je možné odložit po porodu.
- Screening (kapitola 9)
Screening tyreopatií by měl být proveden u všech žen v prvním trimestru gravidity a/nebo u žen plánujících graviditu. Za současných podmínek, dle doporučení ATA, ETA a ve shodě s doporučením ČES ČLS JEP v České republice by měl registrující gynekolog u všech těhotných žen zhodnotit rizikové faktory a při pozitivitě kteréhokoliv údaje provést vyšetření TSH a Anti-TPO. Rizikové faktory jsou následující: pozitivní údaje z rodinné či osobní anamnézy (prodělané nebo aktuální tyreopatie, autoimunitní choroby - především DM 1. typu), příznaky tyreoidální dysfunkce, struma, potrat nebo předčasný porod v anamnéze, infertilita, prodělané ozáření hlavy a/nebo krku, současné i dřívější užívání amiodaronu, lithia, aplikace cytokinů, nedávná aplikace jodového RTG kontrastu, známá pozitivita Anti-TPO, obezita s BMI ≥ 40 kg/m2, informace o tom, zda žena nežije v oblasti se středním či těžkým jodovým deficitem a věk nad 30 let [2-4]. Nicméně při cíleném screeningu unikne 30-50 % žen diagnóze. Proto ČES ČLS JEP dává přednost zavedení univerzálního laboratorního screeningu (TSH a Anti-TPO), který se však dosud nepodařilo dojednat. Pokud není prokazatelný rizikový ukazatel, je možné požádat o vyšetření v rámci nadstandardu. Ženy by měly být o možnosti screeningu informovány u svého gynekologa a praktického lékaře. Screening by měl být realizován ideálně v 5.-6. týdnu, eventuelně kdykoli později, pokud není proveden v této časné fázi těhotenství, nejpozději však v rámci screeningu vrozených vývojových vad a HBsAg v 1. trimestru (9.-11. týden gravidity).
1. Obecný úvod
Límanová Z.
Hormony štítné žlázy zasahují do fertility ženy, průběhu gravidity, vývoje plodu i do vývoje dítěte v pozdějším období. Je nepopiratelnou skutečností, že tyroxin (T4) a trijodotyronin (T3) jsou nezbytné jak pro období prekoncepční (jejich syntéza je závislá na přísunu jodu), tak pro oplodnění (u hypotyreózy dochází vlivem zvýšené hladiny prolaktinu – PRL k poruchám fertility), a dále po celé období gravidity až po několik měsíců po porodu. Plod je zcela závislý na produkci tyroxinu matkou především do 12.-16. týdne, poté začínají tyreocyty plodu vlastní syntézu T4, ale matčina dodávka T4 je důležitá po celé období gravidity.
Poznatky o vztazích štítné žlázy a gravidity se v posledních 20 letech výrazně rozšířily. Důsledkem snahy o sjednocení diagnostiky a léčby jednotlivých onemocnění v graviditě byly pod záštitou The Endocrine Society publikovány v r. 2007 v JCEM [1]. Tato obsáhlá práce byla společným dílem expertů z prestižních světových pracovišť. V r. 2011 publikovala ATA svoje guidelines [2, 3], které v některých detailech rozšiřují či zpřesňují doporučení z r. 2007, další aktualizovaná doporučení byla publikována v r. 2012 [4].
1.1 Proč Guidelines upravujeme pro ČR?
Vzhledem ke specifičnosti tyreoidálních onemocnění považuje Česká endokrinologická společnost ČLS JEP za nezbytné se k těmto doporučením stručně vyjádřit a připojit některé připomínky ohledně diagnostiky a léčby v České republice při respektování obecných principů doporučení ETA, ATA a Endocrine Society.
Vznik onemocnění štítné žlázy i jeho průběh je závislý především na několika zásadních okolnostech: genetické výbavě včetně imunologických vlastností jedince, stavu zásobení jodem, a na dalších zevních faktorech. Tyto okolnosti jsou natolik specifické, že nelze jednotné postupy akceptovat všeobecně bez znalosti a respektování regionálních specifik, do kterých patří i zvyklosti zdravotnictví, možnosti prevence i přístupu jedince k jeho zdraví. Významnou roli hrají i tradice v mateřství, zvyklosti při péči o těhotnou ženu, a v neposlední řadě i mezioborová spolupráce zdravotníků. V ČR (ale i v Evropě) zaznamenáváme v posledních 20 letech výrazné změny v přístupu ke zdravotnickým zvyklostem: mizí paternalistický přístup zdravotníků, občané se více zajímají o své zdraví a chtějí více rozhodovat o diagnostice i léčbě, díky všeobecné komunikaci a sdělovacím prostředkům se občané více vzdělávají v otázce zdraví a nemoci. Věk těhotných se posunul na nynějších v průměru 32 let, těhotenství je většinou plánované, a je umožněno nejen ženám vyšších věkových skupin, ale i ženám se zdravotními riziky (po onkologické léčbě, po transplantaci orgánů). Na druhé straně však se snižuje fertilita nejen žen, ale i mužů, a umělé oplodnění podstupuje každým rokem vyšší počet žen - nyní cca 6-8 % ze všech těhotenství. Mezi těmito ženami je 10-20 % žen s tyreopatiemi. Zpřesnily se normy pro laboratorní ukazatele v jednotlivých trimestrech gravidity, rozšiřují se poznatky o rizikových faktorech, které negativně dopadají na vztah tyreoidey a gravidity. Do této skupiny patří i důsledky autoimunity štítné žlázy. V graviditě a po porodu je žena vystavena významným změnám nejen hormonálním, ale i imunologickým, metabolickým a hemodynamickým. Je tedy zřejmé, že jde o mezioborovou spolupráci, proto se do péče o těhotnou ženu zapojují vedle gynekologů, porodních asistentek a gynekologických sester nejen praktičtí lékaři, ale i další odborníci. Důležité místo samozřejmě patří endokrinologům. Na základě jejich široké diskuze, s ohledem na velmi složitou problematiku těhotenství a nedostatek randomizovaných kontrolovaných studií (RCT) - nebude v argumentaci léčby hraničních stavů bezvýhradně splněn požadavek „evidence-based“.
1.2 Úvod do problematiky funkčních tyreopatií a těhotenství
Úzký vztah gravidity a činnosti tyreoidey je po staletí znám. Dříve se zájem soustředil především na otázku příjmu jodu - tento problém přetrvává na zeměkouli dosud pro více než 2 miliardy lidí. Česká republika patří do oblastí spíše s přiměřeným zásobením jodu [5] a struma z nedostatku jodu je dnes ojedinělým nálezem, nicméně význam jodu v graviditě je nadále nutné připomínat a suplementace jodem po celou dobu gravidity je žádoucí. V prvních týdnech po početí se potřeba jodu zvyšuje, zvyšuje se i průtok krve tyreoideou, jod se více vychytává a je k dispozici pro zvýšenou syntézu tyroxinu. Pokud je zásobení jodem dostatečné, tyreoidea se zvětšuje jen mírně. V oblastech s mírným nedostatkem jodu se tyreo-idea zvětšuje o 10-20 % a v oblastech s deficitem jodu až o 40 % svého objemu. Přesto, že v ČR není závažnější deficit jodu, je vyšší potřebu jodu v graviditě nutné pokrýt zvýšením jeho příjmu. Vlivem elevace estrogenů se v játrech zvyšuje syntéza thyroxine binding globulinu (TBG) a zvyšuje se hladina celkového T4, hladina volného T4 (FT4) má tendenci přechodně klesat. Placenta uplatňuje svůj vliv na štítnou žlázu prostřednictvím choriového gonadotropinu (hCG ), který má významnou synergickou TSH aktivitu, tím se přechodně TSH zpětnovazebně v 1. trimestru snižuje. Zdravá žláza zvyšuje produkci T4 a nastává nová rovnováha. Pokud není tyreoidea plně funkční (je např. postižena autoimunitou) a není schopná přiměřeně na požadavky reagovat zvýšením produkce T4, vzniká subklinická až plně rozvinutá hypotyreóza [1-3, 6, 7]. Diskuze o aktivním vyhledávání těhotných žen s poruchou funkce tyreoidey byla v ČR zahájena již v r. 2004 [8]. Na základě zkušeností s vyšetřením tisíců těhotných žen v 1. trimestru gravidity v několika centrech v ČR, při kterém bylo diagnostikováno nejméně 5 % žen s elevací TSH a 8-15 % s pozitivními protilátkami [9,10], jsou nyní předkládána doporučení, vedoucí k řešení onemocnění štítné žlázy v graviditě. Diskuze o zavedení univerzálního screeningu je uvedena v kapitole 11. Následující doporučení může být podnětem k další mezioborové diskuzi.
1.3 Choroby štítné žlázy v graviditě - stručný přehled
Nejčastějším endokrinním onemocněním žen, a to i v graviditě, je autoimunitní postižení štítné žlázy. Do této skupiny patří především chronická lymfocytární tyreoiditida (CLT) a choroba Gravesova-Basedowova (GB). Zatímco obávaná komplikace v graviditě tyreo-toxikóza nejčastěji GB typu postihuje asi 0,1-0,4 % žen, CLT je diagnostikována při cíleném vyhledávání u 10-15 % většinou asymptomatických žen. CLT nemusí být primárně provázena funkční poruchou, ale při zátěži – v graviditě – se subklinická až klinická hypotyreóza často rozvine (u více než 20 %). Následky u těchto žen se mohou manifestovat i po porodu v podobě poporodní tyreoiditidy (PPT). Jak zvýšená, tak snížená funkce štítné žlázy může způsobit těhotné ženě i dítěti (plodu) značné komplikace. Je prokázáno, že důsledkem snížené činnosti tyreoidey, tj. jak rozvinuté, tak subklinické hypotyreózy, jsou častější potraty, předčasné porody, abrupce placenty, malá porodní váha, častější neonatální respirační distress. Negativní dopad na IQ a psychomotorický vývoj dětí, narozeným matkám s hypotyreózou, byl jednoznačně prokázán [1-3], negativní důsledky u dětí matek se subklinickou hypotyreózou (SH) nebo s prokázanými Anti-TPO sice prokázány nebyly jednoznačně [11], ale některé publikace tuto skutečnost podporují [12]. O závěrech Lazarusovy práce se nyní živě diskutuje [13,14]. Problematika psychomotorického vývoje dětí je totiž nejen multifaktoriální, ale velice složitá z metodologického a etického hlediska, proto vyžaduje další seriozní studie, na kterých se musejí podílet odborníci z různých oborů. Význam tyroxinu pro vývoj nervové soustavy plodu je nepochybný [15,16]. Gynekologické komplikace u žen s AITD nezávisle na funkci štítné žlázy, především častější potrácení, je ověřeno v řadě studií (viz kapitola 7).
2. Funkční tyreoidální testy v graviditě
Springer D.
Vzhledem ke zvýšené potřebě tyreoidálních hormonů v těhotenství a adaptaci štítné žlázy na tyto nároky, nastávají změny v hladinách tyreoidálních markerů. To vyvolává potřebu určení specifických referenčních intervalů především pro TSH a FT4, a to ideálně pro každý trimestr těhotenství zvlášť. Pro základní zhodnocení stavu štítné žlázy v těhotenství se doporučuje vyšetření tří parametrů: TSH, protilátek proti tyreoidální peroxidáze (Anti-TPO ) a FT4 . Výsledky jsou obvykle k dispozici během několika hodin, u méně frekventovaných metod (Anti-TPO - protilátky proti TSH receptoru neboli TRAK neboli Anti-TSH-R) maximálně do několika dnů.
Při hodnocení laboratoře se za velmi významné považuje zajištění kvality vyšetření a mezilaboratorní srovnatelnosti, uvádění ověřených referenčních intervalů i rozhodovacích mezí pro těhotenství a z interpretačního hlediska potom znalost možných analytických a biologických interferencí [17].
2.1 Změny hladin hormonů v těhotenství
Choriový gonadotropin (hCG) je ve vysoké koncentraci stimulátorem tvorby tyreoidálních hormonů prostřednictvím receptorů pro TSH. Zvýšení hladiny hCG vede ke zvyšování produkce mateřského T4 a T3 v době kritického vývoje mozkové kůry v prvních týdnech vývoje plodu. Hladina T3 se může v průběhu třetího trimestru zvyšovat asi na 1,5 násobek normálních hodnot. Pro základní dia-gnostiku toto vyšetření není nutné. V prvním týdnu po porodu klesají hladiny T3 opět k normálu. Stanovení FT4 umožňuje zjistit množství biologicky dostupného tyroxinu pro těhotnou ženu i její plod. Hladina FT4 je ovlivněna především dostatečným množstvím jodu a týdnem těhotenství. Nicméně laboratorní výsledek může být ovlivněn i použitou vyšetřovací metodou a závisí také na tom, zda poměr vázané a volné frakce tyroxinu in vivo zůstane zachován i během analýzy. Vyšetření FT4 v těhotenství je považováno v současné době za nejméně spolehlivý tyreoidální parametr (pokud se nepoužije dysekvilibrační dia-lýza, což je metoda, která se u nás nepoužívá vzhledem k její náročnosti a ceně). Výsledek vyšetření celkového T4 v graviditě je ovlivněn vazebnými bílkovinami (TBG), proto doporučujeme posuzovat FT4, pokud informaci o jeho hladině potřebujeme. Stanovení celkového tyroxinu a v graviditě následné násobení koeficientem 1,5 tak, jak používají některé země [4], nepovažujeme v ČR v běžné praxi za přínosné. O významu nálezu izolovaného snížení FT4 se diskutuje a je tomu věnována zvláštní kapitola 3.6. Zvýšení FT4 v graviditě (spolu se supresí TSH) jednoznačně podpoří diagnózu hypertyreózy.
2.1.1 Tyreotropin (TSH)
Stanovení TSH má při diagnostice poruch funkce štítné žlázy klíčovou úlohu. Tyreotropní aktivita hCG vede na začátku těhotenství ke snížení hladiny TSH. K největšímu poklesu TSH dochází v prvním trimestru, kdy je hladina hCG nejvyšší. Během těhotenství se sice TSH zvyšuje, ale přesto zůstává jeho referenční interval po celé těhotenství nižší než pro běžnou populaci. Vzhledem k tomu, že hladina hCG je u vícenásobné gravidity vyšší, je i snížení TSH u vícenásobných gravidit výraznější. Malé procento žen může mít v 1. trimestru velmi nízké hladiny TSH (< 0,01 mIU/l), zvláště při hyperemesis gravidarum, a přesto jde o zdravé těhotenství. Izolovaná suprese TSH není spojená se zhoršeným výsledkem těhotenství a není považována za nebezpečnou (viz kapitola 6).
Stanovení TSH se považuje za nejpřesnější obraz stavu štítné žlázy v těhotenství. Existují signifikantní etnické rozdíly v hladinách TSH. Černošky a Asiatky mají v průměru o 0,4 mIU/L nižší TSH než bělošky, a to i v těhotenství. TSH má diurnální variabilitu s pulzní sekrecí, maximum je mezi půlnocí a 4. hodinou ranní, minimum mezi 7.-13. hodinou. Odběry krve je vhodné provádět mezi 7.-13. hodinou. Denní hodnoty mohou být až poloviční proti nejvyšší noční koncentraci. Referenční intervaly pro TSH se mohou lišit podle používané analytické metody (viz Tabulka 1).
Tab. 1. Srovnání referenčních intervalů pro TSH a FT4 pro běžnou populaci a pro těhotné v 1. trimestru – hodnoty podle doporučení jednotlivých výrobců imunodiagnostik a stanovené ve studii VFN a 1. LF UK v Praze* 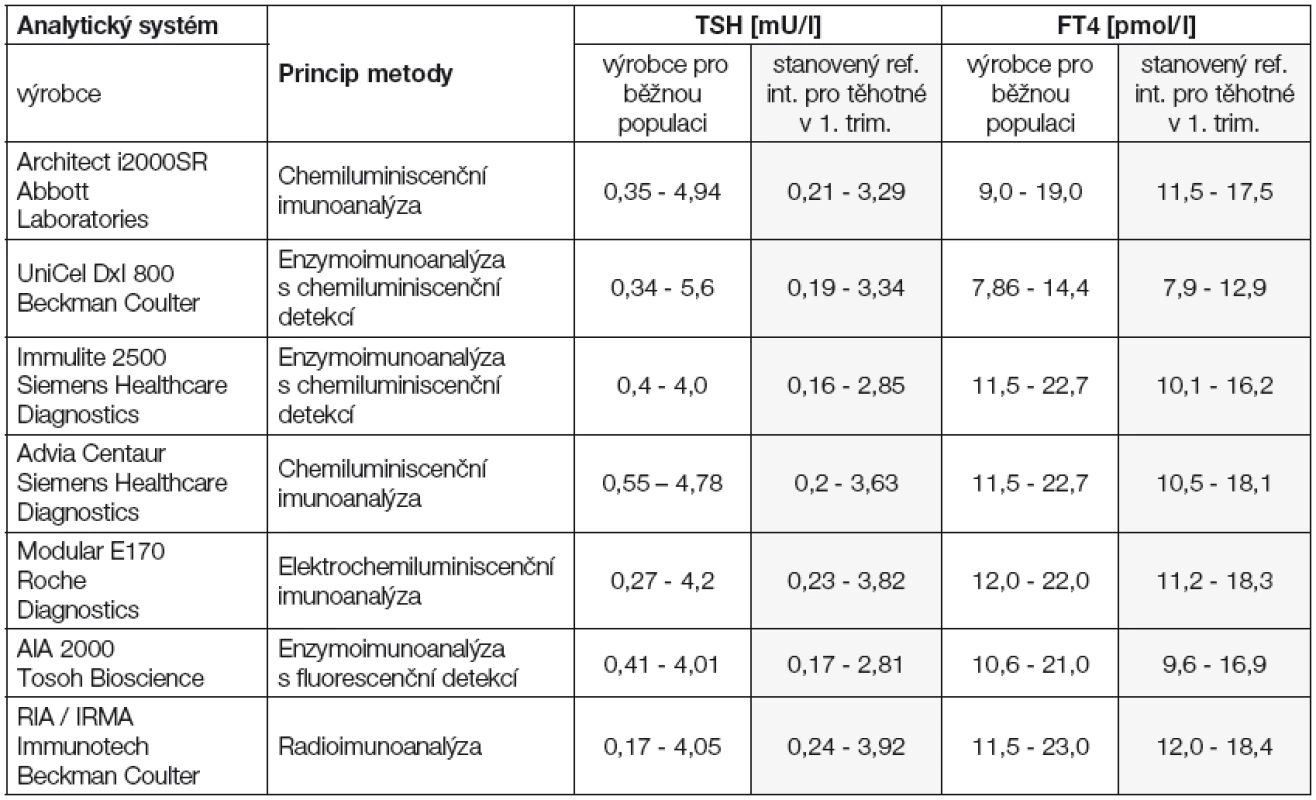
*nepublikovaná studie Springer 2012 2.1.2 Volný tyroxin (FT4)
Hladina celkového tyroxinu je v graviditě výrazně ovlivňována koncentrací sérových proteinů, proto se dává přednost stanovení FT4, jehož hladina nejlépe odráží skutečný funkční stav tyreoidálního metabolizmu. Během 4-6 týdnů po otěhotnění se zvyšuje TBG – asi o 50 %, a tím i celkový tyroxin. Hladina FT4 v séru se během těhotenství mírně snižuje.
Zvýšená hladina vazebných proteinů v těhotenství může přinést problém s imunoanalytickým stanovením FT4. Jako nejvhodnější metoda se pro stanovení sérového FT4 v těhotenství považuje stanovení tyroxinu v dialyzátu nebo ultrafiltrátu s využitím on-line extrakce a LC/MS/MS). Tyto postupy jsou ale zatím velmi drahé a časově náročné. Pro stanovení FT4 se proto používají imunoanalytické techniky, které má laboratoř k dispozici a které jsou pro běžnou diagnostiku v těhotenství dostačující. Nicméně hodnocení samotné hladiny FT4 v graviditě, pokud je v referenčním intervalu, se ukázalo jako mírně problematické (viz kapitola 7). Pro FT4 jsou vyžadovány trimestr specifické referenční intervaly. U žen, léčených levotyroxinem, je doporučen odběr před užitím léku (falešně zvýšené hodnoty FT4 až 4 hod po užití).
2.1.3 Autoprotilátky
Protilátky proti tyreoidální peroxidáze a tyreoglobulinu
Protilátky proti tyreoglobulinu (Anti-Tg) se v těhotenství běžně nevyšetřují, využívají se pouze při sledování nádorového markeru - tyreoglobulinu. Doporučení ATA [1] tyto protilátky pro diagnostiku v těhotenství nevyzdvihuje.
Naproti tomu stanovení Anti-TPO protilátek v těhotenství je velmi důležité, protože tyto protilátky jsou markerem autoimunitního procesu probíhajícího ve štítné žláze. Přítomnost Anti-TPO protilátek v těhotenství informuje o riziku dalších komplikací během těhotenství i po porodu (viz kapitoly 4 a 7).
Autoprotilátky jsou heterogenní, v graviditě mohou přechodně klesat a při poporodní tyreoiditidě se naopak mohou zvyšovat. Jednotlivé typy produkovaných protilátek mají různou vazebnou schopnost s antigeny používanými v imunoanalytických metodách. Mezi výsledky, získanými různými metodami u konkrétních pacientů můžeme nalézt velké rozdíly, a to v řádech desítek až stovek procent. Je proto vhodnější posuzovat jejich hladinu spíš semikvantitativně – negativní, mírně pozitivní, vysoce pozitivní apod.
Eutyreoidní ženy s pozitivními Anti-TPO protilátkami by měly být během těhotenství rovněž sledovány, zda nedochází k rozvoji hypotyreózy (viz kapitoly 4 a 7).
Protilátky proti TSH receptoru (TRAK, Anti-TSH, TRAb)
Autoimunitní protilátky proti TSH receptorům obsaženým v buněčných membránách buněk štítné žlázy, označované souhrnně TRAK, mohou podle účinku na TSH receptor blokovat nebo stimulovat činnost štítné žlázy. S vysokou citlivostí (95 %) a specificitou (98 %) poskytují informaci o etiologii tyreotoxikózy, jejich hladiny korelují s aktivitou i tíží onemocnění. Stanovení TRAK se indikuje při diferenciální diagnostice hypertyreózy (autoimunitního a neautoimunitního původu, rezistence vůči tyreoidálním hormonům) a sledování jejich léčby. Jsou hlavním markerem GB tyreotoxikózy. Remise je provázena poklesem a opětný vzestup těchto protilátek ukazuje na relaps choroby. Hladina TRAK není ovlivněna graviditou, ale aktivitou choroby, která se během těhotenství obvykle zklidňuje. Vzestup hladiny TRAK po porodu odráží reaktivaci GB choroby. U fertilních žen s GB tyreotoxikózou se mohou nacházet cirkulující TRAK i po totální tyreoidektomii a mohou přecházet transplacentárně a velmi vzácně mohou vyvolat dysfunkce štítné žlázy jak postnatálně, tak in utero [18].
U těhotných, které mají v anamnéze dřívější nebo současný výskyt GB tyreotoxikózy, se doporučuje vyšetřit TRAK i během těhotenství, a to mezi 20. a 24. týdnem těhotenství.
2.1.4 Jodurie
Jod je nezbytný pro tvorbu hormonů štítné žlázy a jeho potřeba se během těhotenství zvyšuje. Pro stanovení saturace jedince jodem je možné vyšetřit koncentraci jodidového aniontu v moči (jodurii). Nejužívanější laboratorní metodou pro stanovení jodurie je Sandell Kolthoffova metoda založená na fotometrickém stanovení Ce3+ iontů, které vznikají v redox systému Ce4+/As3+ katalytickým působením jodidových aniontů. Fotometrickému stanovení předchází mineralizace vzorku v alkalickém prostředí (lze použít i kyselou mineralizaci). Metoda je časově náročná, nepříliš vhodná do současných klinických laboratoří, nově byla vypracována s elektrochemickou detekcí jodidového aniontu. Vyšetření je vzhledem k analytické náročnosti využíváno méně, než by bylo potřebné (viz kapitola 6).
2.2 Stanovení referenčních intervalů
Realizace doporučení IFCC je v případě těhotenských referenčních intervalů nemožná vzhledem k popsané referenční populaci. Přesto je možně držet se alespoň základních požadavků. Jednoznačně se doporučuje uvádět referenční interval jako hodnotu 2,5–97,5 percentilu ve skupině zdravých dobrovolníků, kteří nemají v rodinné ani osobní anamnéze onemocnění štítné žlázy a kteří nemají pozitivní protilátky proti štítné žláze. Obě krajní hodnoty intervalu – referenční limity – se vyjadřují s 90 % intervalem spolehlivosti. Těhotné ženy jsou významnou podskupinou, kterou lze definovat při tvorbě referenčních intervalů, jak je popsáno v doporučeních IFCC.
Je nutné počítat s významnými rozdíly mezi produkty různých výrobců IVD (in vitro diagnostika) pro stanovení parametrů funkce štítné žlázy i protilátek, ale může být dosaženo srovnatelnosti číselných hodnot v rámci identických měřících systémů, pokud jsou dodrženy výrobcem předepsané měřící postupy. Norma ISO 15189, podle které je akreditována většina českých laboratoří, ukládá klinickým laboratořím periodicky prověřovat referenční intervaly.
2.2.1 Referenční intervaly pro TSH a FT4
Hladina TSH v prvním trimestru je fyziologicky snížená (vliv hCG). Pro těhotné v jodově dobře zásobených oblastech byly stanoveny pro TSH zvláštní referenční intervaly, které se však liší podle užívané metodiky stanovení. V Tabulce 2 jsou data z doporučení ATA.
Tab. 2. Orientační referenční intervaly pro jednotlivé trimestry v těhotenství podle doporučení ATA 2011 [1] ![Orientační referenční intervaly pro jednotlivé trimestry v těhotenství podle doporučení ATA 2011 [1]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/e9e52fdabf8f29faee91311ba7b1c36b.png)
Pro FT4 vychází v prvním trimestru rozmezí hladin podobně jako pro běžnou populaci. Ve 2. a 3. trimestru jsou hodnoty nižší. Referenční interval pro FT4 se opět liší podle metod, ale interpretace vyžaduje zvláštní referenční intervaly pro těhotenství. Počítá se jako 95% interval.
Je třeba počítat s tím, že imunoanalytické vyšetření FT4 je v těhotenství nejméně spolehlivým tyreoidálním parametrem a výsledek může ovlivnit i změna vazebných proteinů v graviditě. Rámcově lze říci, že dolní hranice referenčního intervalu pro TSH je v 1. trimestru nižší minimálně o 0,15 mIU/l a horní hranice přibližně o 1,5 mIU/l, pokud se uvažuje obvyklý referenční interval udávaný výrobci pro běžnou populaci 0,4-4,0-5,0 mIU/l. O přesné hranice pro různé trimestry se vedou nadále diskuze.
Pro českou populaci těhotných žen v 1. trimestru byl na základě vyšetření asi 5000 zdravých těhotných žen stanoven referenční interval pro TSH na 0,062–3,67 mIU/l [17]. Další studie, která se podrobně zabývala stanovením referenčních intervalů pro TSH a FT4 různými analytickými systémy, potvrdila jejich vzájemnou odlišnost. Výsledky pro českou populaci těhotných žen v 1. trimestru jsou uvedeny v Tabulce 1.
2.2.2 Rozhodovací meze - cut off pro Anti-TPO
Referenční intervaly pro testy stanovující tyreoidální protilátky by měly být stanoveny na základě vyšetření 120 „normálních” jedinců, kteří mají TSH v normě, nemají v rodinné ani osobní anamnéze onemocnění štítné žlázy nebo některé autoimunitní onemocnění; osoby s predispozicí k AITD mají být vyloučeny. Optimální je vyšetřit u nich i UZ štítné žlázy. V oficiálním doporučení se předpokládá vyšetření zdravých mladých mužů, pro těhotné by se cut-off pozitivity měl určit ze séra těhotných žen bez viditelné či hmatné strumy s koncentracemi TSH v séru v rozmezí 0,5 – 2,5 mIU/l, bez zátěže autoimunitními chorobami v rodinné a osobní anamnéze (tyreopatie, diabetes mellitus 1. typu, lupus apod.) a pokud možno i s normálním UZ nálezem tyreoidey.
Stanovení rozhodovacího limitu u protilátek je stále metodicky závislé a nelze je plně sjednotit. Pro případ posouzení pozitivity protilátek je možné použít rozhodovací mez používanou pro běžnou populaci. Avšak za klinicky významné lze považovat zvýšení na minimálně dvojnásobek horní hranice normy. Zvýšení menší než dvojnásobek je potřeba zvažovat individuálně a případně dovyšetřit – opakovat odběr, UZ. Absolutní hodnoty Anti-TPO, stanovené různý metodikami, nelze srovnávat, praktičtější je hodnocení semikvantitativní. O významu změn hladin Anti-TPO v průběhu gravidity chybí dostatečné informace (viz kapitoly 4 a 7).
3. Hypotyreóza
Horáček J.
3.1 Definice hypotyreózy
Hypotyreóza v těhotenství je prakticky vždy periferní a její nejčastější příčiny v graviditě jsou chronická lymfocytární tyreoiditida (CLT), nezvýšení substituční dávky v době zvýšených nároků a relativní nedostatek jodu. Centrální hypotyreóza je v graviditě velice vzácná.
Klasickým laboratorním nálezem je vzestup TSH v séru jako kompenzační reakce na klesající koncentrace periferních hormonů (zpravidla se hodnotí pomocí volného T4, hladina T3 klesá až u těžké hypotyreózy). Subklinická (mírná, latentní) hypotyreóza je charakterizována vyšším TSH při normálních periferních hormonech. V těhotenství je normální rozmezí TSH posunuto níže, navíc existují rozdíly mezi jednotlivými trimestry a populacemi a především mezi různými metodami -viz kapitola 2, tato problematika je též přehledně shrnuta v doporučeních ATA [2]. Diagnóza hypotyreózy v těhotenství se opírá o stanovení TSH. Současné vyšetření Anti-TPO přispěje k určení etiologie onemocnění, v hraničních případech k rozhodnutí o léčbě, a pomůže vyhledat osoby se zvýšeným rizikem poporodní tyreoiditidy (PPT). Pokud je TSH mimo normální rozmezí, je vyšetření volného T4 důležité pro určení hloubky poruchy (plně rozvinutá/subklinická hypotyreóza).
3.2 Horní mez TSH v těhotenství
Stanovení horní hranice „těhotenské normy“ TSH je z praktického hlediska jak pro screening, tak pro diagnózu hypotyreózy v těhotenství kritické. Vyšší hodnoty jsou spojeny s nízkou senzitivitou, a tedy s rizikem nezachycení části reálných případů hypotyreózy (falešná negativita). Naopak nižší hodnoty horní hranice „cut-off“ vedou k falešné pozitivitě (snižují specificitu) a vystavují některé pacientky (bez skutečné hypofunkce) zbytečnému dalšímu vyšetřování i psychickému stresu a nadměrně zatěžují příslušné endokrinologické pracoviště. Pro TSH v 1. trimestru byl již podán důkaz, že i „vyšší normální“ hodnoty (s mediánem 1,48 mIU/l) jsou spojeny se zvýšeným rizikem potratu a úmrtí plodu či novorozence [19]. Horní mez normálního rozmezí TSH je závislá na trimestru, populaci a metodě. Není-li (na základě lokální normativní studie) definována jinak, zdá se na základě publikovaných studií i vlastních zkušeností užitečné aproximovat horní mez TSH v těhotenství jako hodnotu horní hranice normy obvyklé metody pro netěhotné zmenšenou o 1,5 mIU/l. Tzn. pro metody s horní mezí 5,0 mIU/l nastavit „těhotenskou“ normu na 3,5 mIU/l a pro metody s horní mezí 4,0 mIU/l na 2,5 mIU/l (ve shodě s doporučeními ATA [2]).
3.3 Rizika hypotyreózy v těhotenství
3.3.1 Manifestní (overt) hypotyreóza
Manifestní hypotyreóza je spojena se zvýšeným rizikem potratu, předčasného porodu, nízké porodní hmotnosti, gestační arteriální hypertenze a porušeného neuropsychického vývoje dítěte (podrobně v doporučeních ATA [2]).
3.3.2 Subklinická hypotyreóza
Pro subklinickou (mírnou) hypotyreózu byla obdobná rizika rovněž publikována (a jsou koneckonců biologicky plausibilní), ale asociace rizik je méně jednoznačná a zřejmě kvantitativně méně významná [2]. Patrně záleží nejen na vzestupu TSH, ale také na přítomnosti CLT, obvykle dokumentované pozitivitou antityreoidálních protilátek (viz kapitola 4).
3.4 Prevence a léčba hypotyreózy v těhotenství a po porodu
3.4.1 Prevence, informovanost
Jak ženy v reprodukčním věku již léčené pro hypotyreózu levotyroxinem, tak ženy s CLT a dosud normální funkcí štítné žlázy mimo těhotenství (a tedy dosud neléčené), mají být poučeny o vyšších nárocích na tyreo-idální hormony v těhotenství (nejlépe slovně i tištěným materiálem) a také o nutnosti zvýšit po dobu gravidity a kojení příjem jodu (bez ohledu na přítomnost CLT a i u žen substituovaných levotyroxinem).
Před plánovaným otěhotněním má endokrinolog upravit TSH na cílové hodnoty < 2,5 mIU/l buď zvýšením dávky, nebo zahájením léčby. Žena má být informována o možném rozvoji poporodní tyreoiditidy (PPT).
3.4.2 Léčba hypotyreózy v těhotenství
Substituční léčba hypotyreózy levotyroxinem je poměrně snadná, levná a bezpečná. Řídíme se hodnotou TSH a v těhotenství se snažíme vyhnout především poddávkování, protože i mírně vyšší TSH je spojeno se zvýšeným rizikem [19] a naopak hodnoty TSH v dolní části rozmezí či mírně pod ním jsou z hlediska vývoje těhotenství bezpečné [20]. Všechna doporučení jsou založena na konsensu odborných společností a vycházejí jednak z asociačních studií, jednak z biologické plausibility vztahu mezi hypotyreózou a některými riziky. Podobně tomu je také u doporučení naší společnosti. Jednoznačná shoda panuje u manifestní hypotyreózy, kde je substituční léčba jasně indikovaná [2]. U subklinické (mírné) hypotyreózy je situace složitější. Bylo prokázáno snížení incidence některých porodnických komplikací léčbou na úroveň eutyroidních žen [21,22] (viz kapitola 7) a u subklinické hypotyreózy na podkladě CLT je tedy příznivý vliv léčby pravděpodobný. Naopak v jediné dosud publikované intervenční studii nebyl potvrzen příznivý vliv léčby na psychomotorický vliv dítěte [11], jakkoli jsou vysloveny pochybnosti o metodice hodnocení [13,14], a pro spolehlivé závěry bude nutné vyčkat ověření na jiné populaci jinými metodami.
Úprava dávky u žen léčených již před otěhotněním
Činnost normální štítné žlázy se zvyšuje v graviditě přiměřeně zvýšeným nárokům již asi ve 4.-6. gestačním týdnu a stoupá asi do 16.-20. týdne; poté zůstává činnost žlázy poměrně stabilní (plateau) až do porodu [23]. Hypotyreózní ženy léčené již před otěhotněním proto vyžadují asi v 50-85 % zvýšení dávky levotyroxinu od 5.-6. týdne gravidity. Zvýšení je individuální v závislosti na etiologii hypotyreózy (vyšší je obvykle u žen po totální tyreoidektomii než u žen s CLT) a upravuje se podle kontrol TSH v uvedených termínech (viz kapitola 3.5.1.). Kontroly jsou nejdůležitější v první polovině těhotenství.
Otěhotní-li léčená žena neplánovaně, pak má vědět, že co nejdříve po zjištění těhotenství má zvýšit dávku levotyroxinu průměrně asi o 30 % (např. za týden vzít 2 denní dávky navíc, tedy 9 dávek místo 7) a co nejdříve vyhledat svého endokrinologa, který má upravit dávku na cílový TSH. Potřeba zvýšení dávky je individuální v závislosti na příčině hypotyreózy a množství zbytkové funkční tyreoidální tkáně (25-50 %). Cílové hodnoty TSH jsou při léčbě levotyroxinem 0,1-2,5 mIU/l pro 1. trimestr, 0,2-3,0 mIU/l pro 2. trimestr a 0,3-3,0 mIU/l pro 3. trimestr (bez ohledu na metodu) ve shodě doporučeními ATA [2].
Postup u žen se sníženou funkční rezervou štítné žlázy (CLT) dosud neléčených
Tyreoidea žen s dosud neléčenou eufunkční CLT se zvýšeným nárokům v těhotenství nedokáže přizpůsobit, jak dokládá např. studie Yassa et al. [24], kde u 92 % neléčených žen byly po 4 týdnech zachyceny abnormální hodnoty TSH. Otěhotní-li dosud neléčená žena s CLT neplánovaně, má navštívit endokrinologa, který při této návštěvě po zvážení individuálních okolností zahájí léčbu levotyroxinem, obvykle ve vstupní dávce 50 µg denně a dávku směruje na cílový TSH. Léčba se zahajuje vždy u žen s TSH v pásmu subklinické/manifestní hypotyreózy pro těhotné ženy (horní hranice normy pro netěhotné ponížená o 1,5 mIU/l). U žen s normálním TSH (normy pro těhotné ženy) a pozitivními Anti-TPO se zahajuje léčba individuálně - obvykle u žen anamnesticky rizikových (potraty/předčasné porody, jiné autoimunitní choroby), u žen s pozitivním nálezem na ultrazvuku či u žen se sníženým volným T4 v krvi. Předpokladem pro správné hodnocení mírných odchylek TSH a racionální indikaci léčby levotyroxinem je dostatečná suplementace jodem (mírná elevace TSH může být způsobena jodovým deficitem).
Léčba nově zachycené manifestní hypotyreózy
Pokud zjistíme v těhotenství manifestní hypotyreózu, je nutné zahájit substituční léčbu levotyroxinem v dávce 75-100 µg (event. 1,5 µg/kg) denně neprodleně s cílem dosáhnout normy TSH pro příslušný trimestr co nejdříve (viz kapitola 3.2).
Kontroly v průběhu gravidity
Těhotná žena s hypotyreózou (manifestní i subklinickou) i eufunkční s přítomností protilátek, má být sledována vyšetřením TSH časně po potvrzení těhotenství (5.-6. týden) a dále v 10.,14. a 20. týdnu (± 1 týden). Koncentrace TSH mají být udržovány v normě pro těhotné ženy. Poté při stabilizaci stavu stačí další vyšetření TSH po šestinedělí, event. může být v případě pochybnosti provedeno ještě 1x mezi 28. a 32. gestačním týdnem (viz dále).
Kontroly po porodu
Po porodu je vhodné snížit substituční dávku levotyroxinu na hodnotu před otěhotněním, suplementace jodem se ponechává ve stejné dávce po celou dobu kojení. Kontroly musí být častější, aby se zachytila případná hyper i hypo fáze PPT nebo aktivita GB choroby. Optimální je naplánovat první kontrolu TSH 6 týdnů po porodu a další kontroly za 3, 6 a 12 měsíců po porodu, při patologických nálezech příslušně častěji. Je vhodné poučit ženu, že při příznacích hypertyreózy má vyhledat kontrolu dříve. Je skutečností, že ženy si obtíže jak při fázi hyperfunkce tak při fázi hypotyreózy příliš neuvědomují.
Izolovaná hypotyroxinémie a její význam pro těhotenství
Jako izolovanou hypotyroxinémii označujeme nález sníženého volného tyroxinu spolu s normálním TSH v krvi, protilátky by měly být negativní. Observační studie [25] ukazují asociaci takového stavu s horším psychomotorickým vývojem dítěte. To má plausibilní biologické zdůvodnění, neboť před zahájením tvorby hormonů ve fetální štítné žláze (asi ve 12. týdnu) je vývoj mozku plodu závislý na mateřském tyroxinu [15]. Vysvětlení izolované hypotyroxinémie při existenci zpětné vazby mezi periferními hormony a TSH není jednoduché a spekuluje se především o deficitu jodu s relativně vyšší tvorbou T3 než T4. Tomu by mohla odpovídat bimodální distribuce abnormalit ve studii CATS [11]: 5 % žen mělo zjevnou hypotyreózu, asi 47 % subklinickou hypotyreózu a asi 48 % mělo izolovanou hypotyroxinémii. Taková distribuce naznačuje, že se jedná o etiologicky různé poruchy. V našich podmínkách je izolovaná hypotyroxinémie vzácnější [17,26], což může odrážet lepší saturaci populace jodem [5]. Důležitý praktický problém pro interpretaci izolované hypotyroxinémie navíc představuje malá spolehlivost běžně užívaných metod pro stanovení volného T4 v těhotenství [27] (viz kapitola 2.1.2), a také naprostá absence norem pro volný T4 v těhotenství. Jediná dosud publikovaná intervenční studie CATS neprokázala příznivý účinek substituce levotyroxinem na IQ potomků žen s izolovanou hypotyroxinémií [11], ale složitosti s vyšetřováním volného tyroxinu ve studii byly zjevné [28]. Izolovaná hypotyroxinémie má dosud nejistý význam pro těhotenství a není prokázán příznivý účinek substituce levotyroxinem; ta proto dle ATA [2] není indikována. Je vhodné zvážit, zda pacientka netrpí nedostatkem jodu, a zajistit doporučené denní dávky. Některé z uvedených studií ale nevyšetřovaly tyreoidální protilátky. Je tedy možné, že minimálně část žen s tzv. izolovanou hypotyroxinémií má i pozitivní protilátky. V těchto případech lze léčbu levotyroxinem považovat za oprávněnou (viz kapitola 3.4.2).
3.5 Eufunkční ženy s průkazem protilátek v těhotenství
3.5.1 Riziko rozvoje hypotyreózy v průběhu těhotenství u (dosud) eutyroidních žen s pozitivními Anti-TPO
Vzhledem ke zvyšujícím se nárokům na produkci tyreoidálních hormonů v těhotenství a často omezené funkční rezervě při pomalu progredující CLT dochází u části žen během těhotenství k vzestupu TSH i při jeho normální vstupní hladině. Ve skupině neléčených žen s CLT zvýšilo TSH nad normu asi 20 % dosud eutyroidních žen s pozitivitou Anti-TPO [29] a podobné riziko (19 %) bylo dokumentováno v další studii u Anti-TPO pozitivních žen, u nichž hodnota TSH ve 12. týdnu byla normální [30,31]. Stanovení Anti-TPO je přinejmenším stejně významnou součástí screeningového vyšetření těhotné ženy jako TSH (možná kvantitativně významnější). U Anti-TPO pozitivních žen se vstupním TSH nižším 2,5 mIU/l je možné individuálně zahájit léčbu malou dávkou levotyroxinu (50 µg/d) i v případě normálního vstupního TSH a dávku upravovat podle kontrol jako u žen se vstupní hypotyreózou. Léčba má zabránit rozvoji hypotyreózy během těhotenství (cca u 20 %) a redukovat riziko porodnických komplikací (cca 3x). Léčba se obvykle zahajuje u žen anamnesticky rizikových (potraty/předčasné porody, jiné autoimunitní choroby), u žen s pozitivním nálezem na ultrazvuku či u žen se sníženým volným T4 v krvi. Je nutno poznamenat, že cut-off pro pozitivní Anti-TPO v těhotenství neodpovídá hodnotě udávané výrobcem pro běžnou populaci (např. ve studii Springer et al. 2009 byla pro metodu s „cut-off“ 60 kIU/l pro běžnou populaci stanovena norma pro těhotné ženy s normálním TSH na 143 kIU/l). Proto je při rozhodování o léčbě Anti-TPO pozitivních těhotných žen s normálním TSH třeba brát v úvahu i výši titru Anti-TPO a případně i nález na ultrazvuku štítné žlázy.
TPO-pozitivní ženy je nutné kontrolovat častěji v poporodním období (stejně jako ženy s hypotyreózou, viz kapitola 4.3). Cílem je včas zachytit a léčit jak PPT, tak i event. aktivaci GB choroby. Je třeba počítat s tím, že jejich podstatná část (asi polovina) žen s PPT bude progredovat do trvalé hypotyreózy a neléčená pak nepříznivě ovlivní jejich další těhotenství.
3.5.2 Riziko porodnických komplikací u (dosud) eutyroidních žen s pozitivními Anti-TPO
Nedávná metaanalýza 31 převážně observačních studií [32] ukázala, že u těchto žen je asi 3x vyšší riziko spontánního potratu (v kohortových studiích asi 3,9x, v case-control studiích asi 1,8x) a asi 2x vyšší riziko předčasného porodu. Naproti tomu intervenční studie je pouze z jednoho pracoviště [30]. Ačkoli podporuje příznivý efekt léčby levotyroxinem na porodnické komplikace, její autor (Roberto Negro) v editorialu k uvedené metaanalýze [31] připomíná, že asociace je jasná, ale účinnost léčby je dosud nejistá pro více možných činitelů ve hře. Léčbu malou dávkou levotyroxinu takovým ženám můžeme s přihlédnutím ke konkrétnímu případu podávat (viz kapitoly 4.1 a 7), protože potenciální přínos je zjevný a rizika minimální (pokud není žena předávkována). Také cena je nízká, takže analýza cost-efektivity vyznívá pro léčbu, a dokonce i pro univerzální screening [33]. Spolehlivější odpověď můžeme očekávat od dalších studií, např. od probíhající multicentrické studie TABLET.
3.5.3 Rizika po porodu, poporodní tyreoiditida (PPT)
Po porodu se opět sníží nároky na tyreoidální hormony na úroveň před otěhotněním. Logické by proto bylo rovněž substituční dávku snížit na původní hodnotu a u předtím neléčených žen substituci vysadit. Protože však po porodu změnou imunologického vyladění dochází k akcentaci autoimunitních procesů, není vhodné takto postupovat automaticky, ale vždy individuálně. V praxi se jeví jako vhodný postup, aby se ženy léčené již před těhotenstvím vrátily k dávce jako před graviditou a u žen s léčbou nově nasazenou v těhotenství byla léčba ponechána a úprava byla provedena podle kontroly TSH 6 týdnů po porodu. Další kontrola TSH by měla být za 3, 6 a 12 měsíců po porodu a při patologických nálezech příslušně častěji. Je důležité kontrolovat častěji zejména ženy se známým autoimunitním onemocněním (nejen) štítné žlázy. Je-li proto přítomna CLT, pak se tato akcentace v prvním poporodním období (asi do 3. měsíce) může projevit zvýšeným vyplavováním hormonů z poškozené žlázy (hyper fáze PPT), které je v dalším období od 3.-6. měsíce následováno sníženou sekrecí (hypo fáze PPT); ta pak může zůstat snížená (a případně progredovat) nebo se vrátit k hodnotám před otěhotněním.
U žen s pozitivními Anti-TPO, které byly před otěhotněním eutyroidní, je riziko PPT asi 40 % [3] a asi u 20 % eutyroidních žen s pozitivními Anti-TPO přetrvává hypotyreóza i po roce od porodu a přechází v klasickou CLT a obdobně mohou po porodu reagovat ženy s již dříve léčenou CLT. Hyperfunkční fáze se může projevit nutností snížit dávku levotyroxinu nebo i přechodně léčbu vysadit. Tyreostatika se samozřejmě nepodávají, pouze v případě obtíží indikujeme v malých dávkách a krátkodobě betablokátory. Kojení není nutno přerušovat. Podle nedávné studie [34] více než 50 % žen s CLT potřebuje v poporodním období substituční dávku vyšší než původní. Podobně může dojít k aktivaci Gravesovy nemoci (relaps nebo méně často první ataka), vyžadující ovšem příslušnou tyreostatickou terapii (viz kapitola 6).
4. Význam jodu v graviditě
Zamrazil V.
4.1 Význam jodu pro lidský organizmus a jeho zdroje
Jod je nezbytnou součástí hormonů štítné žlázy trijodtyroninu (T3) a tyroxinu (T4). Do lidského organizmu se jod dostává ze zevního prostředí potravou, možným zdrojem jsou v některých oblastech i minerální vody, jinak obsah jodu v pitné vodě obvykle nestačí zajistit dostačující přívod do organizmu. Je obtížné stanovit optimální přívod jodu, obvykle se určuje nejnižší přívod, který ještě dlouhodobě zajistí normální funkci štítné žlázy, a nadměrně zvýšený přívod, který je spojen s riziky nepříznivých účinků.
4.2 Mění těhotenství potřebu jodu?
Dostačující přívod jodu se uvádí pro oběžnou dospělou populaci hodnotou 150 µg/den. Těhotenství (a také kojení) mění situaci v tom smyslu, že je nutno zajistit dva organizmy (těhotnou ženu a vyvíjející se plod). Samo těhotenství zvyšuje potřebu jodu u gravidní ženy vlivem na zvýšenou potřebu tyreoidálních hormonů, změnami koncentrace přenosových vazebných proteinů (především TBG), zvýšeným vylučováním jodu močí při zvýšené glomerulární filtraci. K nedostatku jodu může přispět i změna životosprávy těhotné ženy, zejména doporučované omezení solení (jodovaná sůl je u nás a ve většině zemí převažujícím a nejdůležitějším zdrojem jodu). Na zvýšené potřebě jodu v těhotenství se podílí vyvíjející se plod dvěma základními mechanizmy: 1. spotřebovává hormony štítné žlázy, které získává z organizmu matky cestou placentárního oběhu, 2. štítná žláza plodu začíná zhruba od 12. – 14. týdne gravidity produkovat hormony štítné žlázy. K tomu samozřejmě potřebuje dostatek jodu, který získává rovněž z mateřského oběhu [35,36]. Problematice jodového deficitu se věnuje řada organizací od WHO (Světová zdravotnická organizace) přes UNICEF, až po k tomu účelu zřízené ICCIDD (International Council for Control of Iodine Deficiency Disorders), která organizuje, provádí a kontroluje programy optimalizace přísunu jodu. Tato organizace rovněž vypracovala kriteria pro hodnocení saturace jodem v populaci (Tabulka 3) a hodnocení rizik z nedostatečného a zvýšeného přísunu jodu.
Tab. 3. Hodnocení zásobení jodem dle ICCIDD (hodnoceno pomocí jodurie) 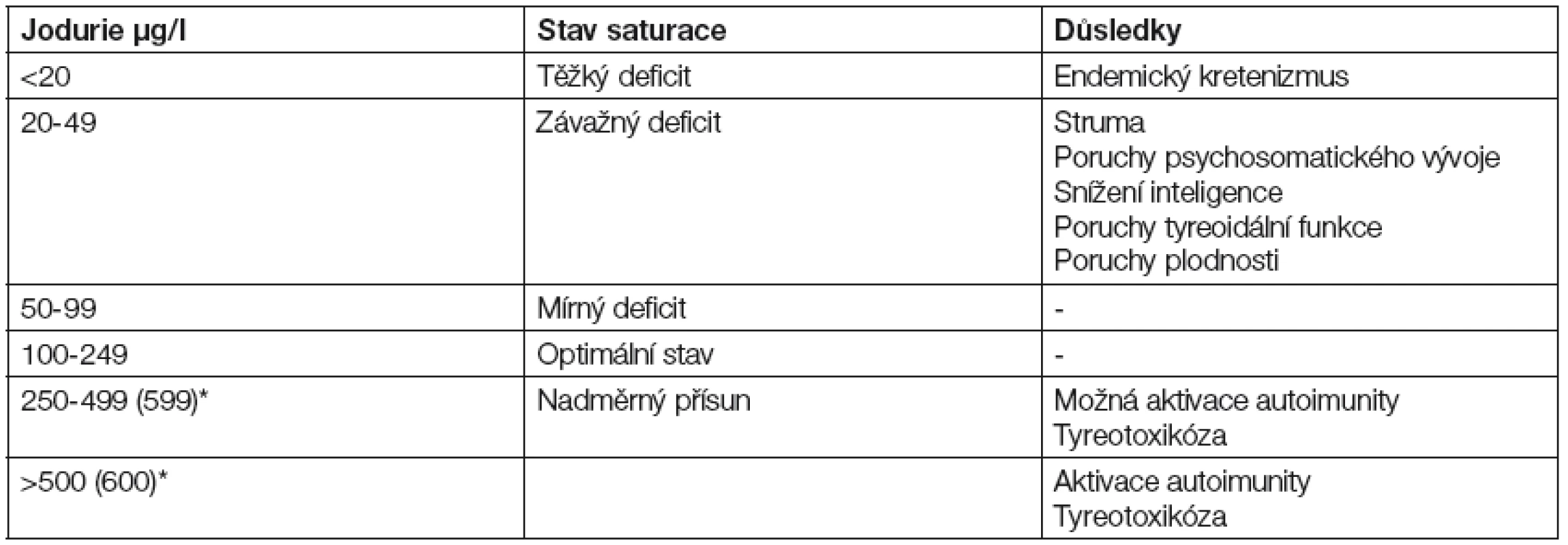
* odlišné hranice podle doporučení různých expertů Základními kriterii hodnocení zásobení jodem je jodurie (obvykle vyšetřovaná jako koncentrace jodu v prvním ranním vzorku moči), výskyt zvětšené štítné žlázy (strumy) a u novorozenců vyšetření TSH krvi. Výsledky našeho epidemiologického průzkumu prokázaly, že v České republice je celopopulační průměrný přísun jodu hodnocený pomocí jodurie v referenčních mezích. Jodurie byla průměrně 120-130 µg/l (při dolní hranici 100 µg/l) [5]. To odpovídá příjmu asi 150 µg jodu denně. V těhotenství vzhledem ke zvýšené potřebě jodu stoupá hranice minimálního přívodu na 250 µg denně. Jak vyplývá z uvedených čísel, průměrný přívod jodu v naší populaci však této hodnoty spíše nedosahuje [37].
4.3 Jaké jsou důsledky nedostatku jodu v těhotenství?
Stručně řečeno jsou významné jak z hlediska matky, tak i plodu a jsou přehledně uvedeny v Tabulce 4. Nejdůležitější jsou poruchy vývoje centrálního nervového systému plodu, ke kterým dochází při závažném nedostatku jodu, a z toho vyplývajícího z nedostatku tyreoidálních hormonů v oběhu matky a druhotně i plodu v časných fázích těhotenství. V extrémních případech vede porucha vývoje CNS a dalších vývojových poruch např. změn vývoje skeletu ke vzniku těžce defektního jedince. Tento stav se označuje jako endemický kretenizmus a je ireparabilní. U nás se již nevyskytuje. V našich podmínkách se však může vyskytnout u části těhotných žen lehčí nedostatek jodu. Ten může vést k mírným změnám psychosomatického vývoje, a ke změnám chování dítěte – hyperaktivní těžko zvládnutelný jedinec je postrachem pedagogů i rodičů.
Tab. 4. Jod v graviditě a nepříznivé důsledky jodopenie 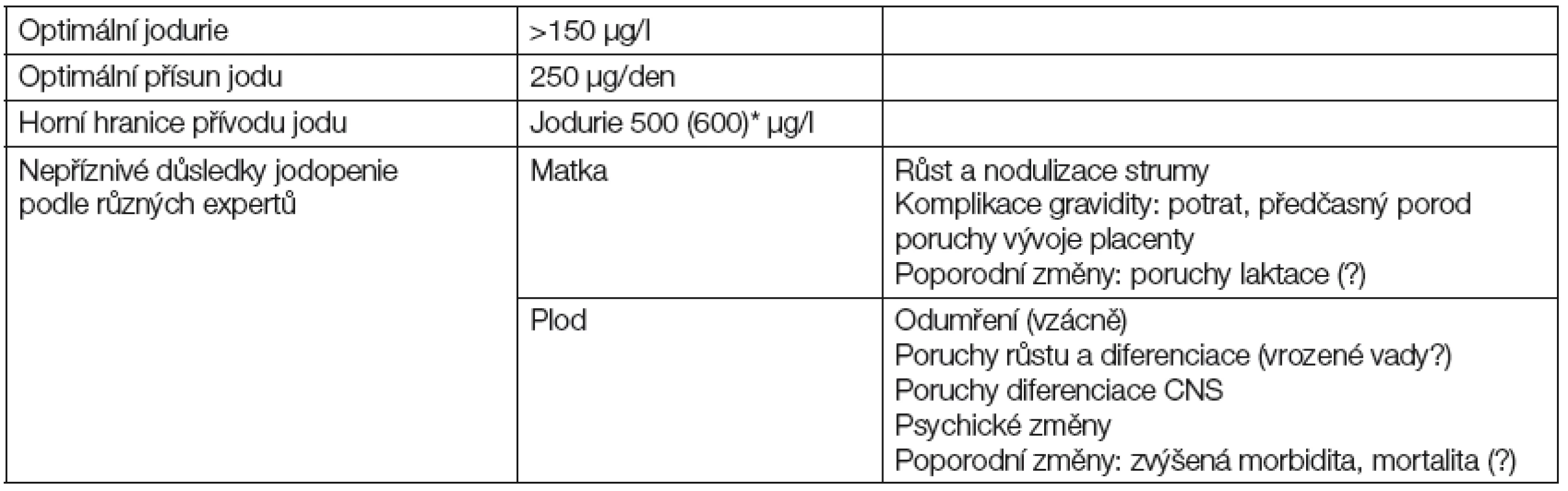
* odlišné hranice podle doporučení různých expertů 4.4 Jak lze hodnotit zásobení jodem v těhotenství?
Ve skutečnosti je velice obtížné vyšetřovat obsah jodu v přijímané potravě. Vzhledem k tomu, že asi 80 % jodu se vylučuje močí, slouží i v těhotenství ke zhodnocení přívodu jodu stanovení jodurie. Ta by podle doporučení ICCIDD měla v těhotenství dosáhnout nejméně 150 µg/l. Vyšetření jodurie však není obecně tak dostupné jako je vyšetření tyreoidálních hormonů nebo protilátek, takže si je rezervujeme pouze pro nejasné případy. Klinické známky nedostatečného přívodu jodu u matky, a tím spíše u plodu prakticky neexistují. Může na něj upozornit růst štítné žlázy či vznik strumy a její nodulizace.
4.5 Jak řešit optimalizaci přívodu jodu v těhotenství?
Základem je zajištění dostatečného přívodu jodu v celé populaci. To je u nás uskutečňováno jodovanou solí, která v ČR obsahuje 27 + 7 mg jodu ve formě KI v 1 kg soli. Je nutno zdůraznit, že obsah jodu v soli propagované zastánci zdravé výživy (např. mořská sůl a alpská sůl) zdaleka nedosahuje uvedených hodnot, obvykle se pohybuje v koncentracích do 10 mg jodu v 1 kg soli. Proto doporučujeme těhotným ženám, aby používaly jodovanou sůl. Dalšími zdroji jodu jsou mořské produkty (které nejsou u nás příliš populární a mohou obsahovat rtuť) a mléko, v nich ale koncentrace jodu značně kolísá.
Proto Česká endokrinologická společnost ČLS JEP a Česká pediatrická společnost ČLS JEP doporučují celoplošně saturovat těhotné a kojící ženy dávkou 100 µg jodu navíc ve formě tablet kalium jodidu (Jodid) nebo ve vitaminových přípravcích, doporučovaných v graviditě. Recentní revidovaná guidelines Endocrine Society doporučují dokonce dávky o něco vyšší (150-200 µg denně) [4]. Nadměrný přívod jodu sice může aktivovat autoimunitní tyreoidální procesy, při imunotoleranci v graviditě je však toto riziko minimální. Vzhledem k trvalým nepříznivým důsledkům jodopenie u plodu je zvýšený přívod jodu nutný i u žen s autoimunitními tyreopatiemi, ovšem za pečlivé odborné endokrinologické kontroly. Pokud matka kojí, je dítě rovněž závislé výhradně na přísunu jodu mateřským mlékem. Je proto nutno zachovávat zvýšený přívod i po dobu kojení.
5. Tyreotoxikóza, tranzientní gestační hypertyreóza
Zamrazil V.
5.1 Úvod
Hypertyreóza (Tx) je stav, kdy produkce hormonů štítné žlázy přesahuje aktuální potřeby organizmu. Kromě manifestní formy existuje vzácně tzv. subklinická hypertyreóza. Jde o nepoměr mezi sníženými hladinami TSH a normálními hodnotami tyreoidálních hormonů FT4, FT3 . Přitom není rozhodující přítomnost klinických známek Tx.
5.2 Hypertyreóza (Tx) v graviditě
Tx v graviditě představuje důležitou, i když méně častou poruchu funkce štítné žlázy. Její nejdůležitější formy jsou uvedeny v Tabulce 5. Nejčastější je autoimunitní forma – GB tyreotoxikóza.
Tab. 5. Nejdůležitější formy tyreotoxikózy v graviditě 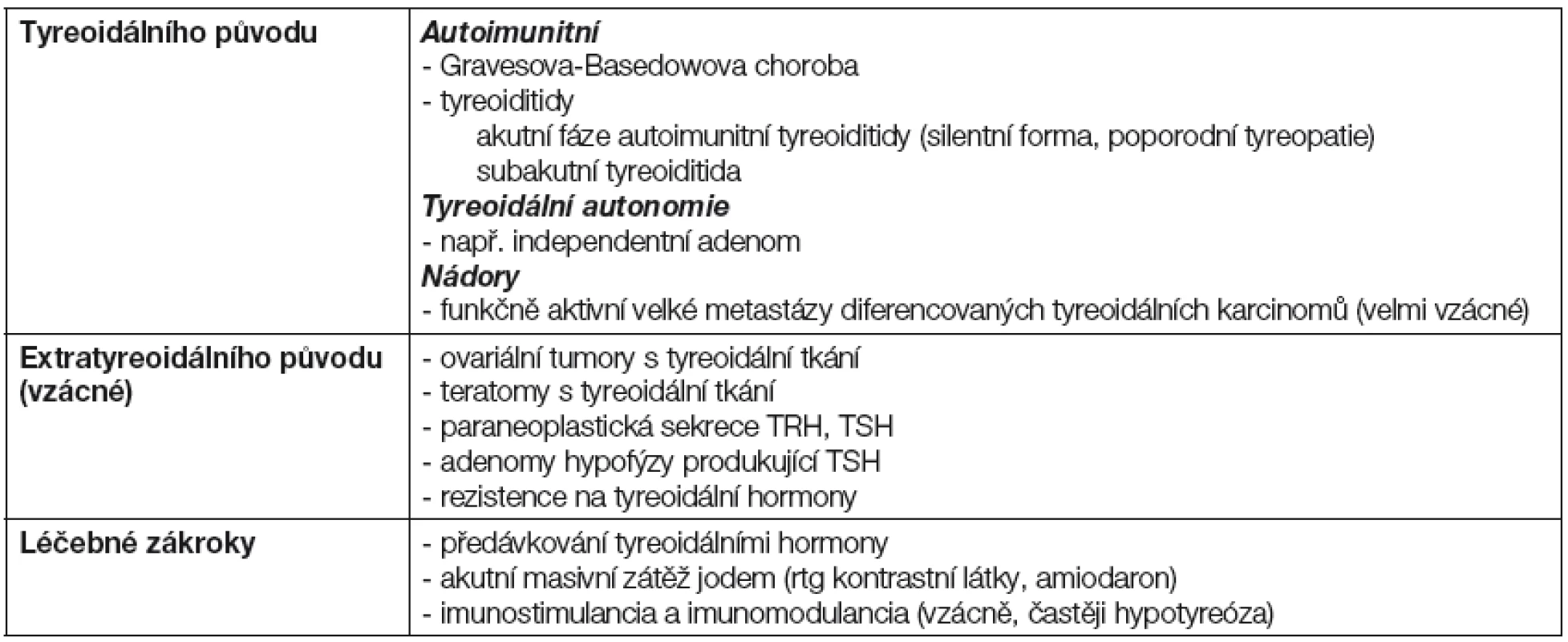
Význam Tx v graviditě je komplexní a může nepříznivě ovlivnit:
- Samotný průběh těhotenství: sklon k abortům, předčasným porodům, poruchám vývoje placenty.
- Vývoj plodu: nepříznivě působí na rychlost růstu a zrání plodu, problematická je souvislost se zvýšeným výskytem vrozených vad, zejména kardiovaskulárního systému.
- Průběh porodu: snížená schopnost kontraktility dělohy, porod může vyvolat závažné zhoršení klinického obrazu Tx až do vzniku tyreotoxické krize.
- Vývoj novorozence a kojence: zvýšená hladina tyreo-idálních hormonů v graviditě se přenáší do plodu, takže po porodu má novorozenec klinické známky Tx, která je obvykle přechodná. U autoimunitní Tx vyvolané tvorbou protilátek stimulujících TSH receptor se tyto protilátky přenášejí do plodu [38,39].
5.2.1 Klinický obraz
Klasický obraz Tx může být v graviditě zastřen, převažují pocity horka a pocení, bušení srdce (spíše výjimečně s pocity nepravidelnosti). Změny chutí k jídlu mohou být ovlivněny obecně se vyskytujícími gastrointestinálními potížemi v graviditě, a mohou vést k poklesu hmotnosti. Vzácně může být přítomen pocit diskomfortu na krku. Oční potíže mohou být přítomny, nejčastěji jde o pálení očí, zvýšené slzení, ale typická endokrinní orbitopatie je v graviditě vzácná.
5.2.2 Laboratorní nálezy u Tx v graviditě
Neliší od laboratorní diagnostiky u negravidních osob: jde o supresi TSH a zvýšené hodnoty FT4 a FT3 tyreoidální etiologie.
Problémem může být suprese TSH v 1. trimestru, která je způsobena zvýšenou tvorbou stimulujících proteinů v placentě (tranzientní gestační hypertyreóza), proto suprese TSH v 1. trimestru není spolehlivou známkou tyreotoxikózy [40,41]. Hodnoty FT4 se fyziologicky v graviditě nezvyšují, takže hodnoty nad normu svědčí pro Tx. Totéž platí v menší míře i pro hodnoty FT3.
Zvýšené hodnoty TSH stimulujících protilátek (TRAK neboli Anti-TSH ) svědčí pro přítomnost GB Tx. Vzhledem k imunotoleranci spojené s graviditou jejich hodnota v průběhu gravidity při léčbě obvykle klesá a sleduje remisi choroby. Sonografické změny štítné žlázy ve smyslu hypoechogenity a zvýšeného krevního průtoku jsou stejně spolehlivou známkou autoimunitní Tx jako u negravidních žen.
5.2.3 Léčba Tx v graviditě
Neliší se zásadně od běžných doporučovaných postupů. V současné době se mění názor na podávání tyreostatik propylthiouracylového (PTU) a imidazolového (MMI) typu (thiamazol). Novější nálezy svědčí pro výrazný hepatotoxický vliv PTU. Proto původní doporučení podávat PTU v průběhu gravidity a kojení (důvodem byl údajný snížený průnik PTU placentou) se mění na doporučení podávat PTU pouze v 1. trimestru gravidity, dále pak přejít na MMI. Obecně je však u autoimunitních forem vliv gravidity na aktivitu Tx příznivý, takže dávku tyreostatik je možno výrazně snížit, výjimečně i vysadit. Po porodu obvykle dochází ke zvýšení aktivity Tx.
Iniciální farmakoterapie
Dříve diskutovaná otázka bezpečnosti tyreostatické léčby v graviditě je v současné době vyřešena v tom smyslu, že nižší dávky (např. 10–20 mg thiamazolu) neovlivňují nepříznivě průběh gravidity a vývoj plodu mohou ovlivnit jen velmi vzácně (pokud dojde k předávkování). Při této dávce je možné i kojení.
V léčebném postupu je nutno odlišit dvě situace:
A) Tx je diagnostikována na začátku gravidity:
Na základě recentních údajů je doporučeno zahájit léčbu propylthiouracylem v dávkách do 200 mg denně a ve 2. a 3. trimestru použít thiamazol (do 20 mg denně). Tyreotoxikóza má obvykle tendenci ke zklidnění ve 2. trimestru a výjimečně jsou nutné dávky vyšší (propylthiouracyl max. 300 mg denně a thiamazol max. 30 mg denně). Vždy je nutné kon-trolovat klinický stav a hladinu FT4 a eventuelně FT3, a to zpočátku po 2-4 týdnech a dbát na to, aby hladina FT4 neklesla pod 12 pmol/l, optimální je udržovat hladinu v rozmezí 15 – 20 pmol/l (přiměřeně dle norem daných výrobcem). Menším zlem je hodnota hraničně vyšší než hodnota FT4 iatrogenně snížená. Monitorování hodnot TSH nemá v průběhu léčby Tx zásadní význam, hodnota může být suprimovaná po zklidnění Tx řadu měsíců. Při riziku předávkování TSH upozorní na rozvoj iatrogenní hypotyreózy. Po porodu obvykle dochází ke zvýšení aktivity Tx.
B) Tx je léčena již před koncepcí:
Těhotenství je možné, ale je nutné věnovat ženě během těhotenství zvýšenou pozornost. Ideální by bylo dosáhnout plného zklidnění již před těhotenstvím ve formě přípravy na plánované těhotenství. Důležité je, aby před otěhotněním byla tyreotoxikóza skutečně zklidněná, takže je nutné ženu před koncepcí vyšetřit klinicky i laboratorně (stanovením TSH, FT4, TRAK), eventuelně provést UZ tyreoidey. U zklidněné tyreotoxikózy v remisi není důvod nepodávat suplementaci jodem v běžných dávkách, tj. 100-150 µg jodu/den.
Těhotenství je možné při nižších a středních dávkách tyreostatik, tj. do cca 150–200 µg propylthio-uracylu v 1. trimestru a 15–20 µg thiamazolu v dalším průběhu těhotenství. Po zklidnění metabolické aktivity Tx a poklesu FT4 (FT3) je nezbytné snižovat dávku tyreostatik k dosažení optimální hladiny FT4 a jsou nutné častější klinické a laboratorní kontroly (cca 1x za měsíc) se sledováním klinického stavu a hodnot FT4. Hodnoty TSH jsou méně spolehlivým indikátorem, ale upozorní na případné předávkování tyreostatika a rozvoj iatrogenní hypotyreózy. Iatrogenní hypotyreóza je nepříznivá pro plod, mimo jiné může vyvolat fetální strumu.
Operace štítné žlázy v graviditě, radiojod
Pokud je špatná spolupráce s těhotnou ženou, objevují se známky intolerance (alergické reakce, leukopenie, poruchy jaterní funkce), Tx vyžaduje trvale vysoké dávky tyreostatika, případně těhotná žena preferuje sama operaci, je možno provést tyreoidektomii na konci 2. a začátku 3. trimestru gravidity. V České republice doporučujeme totální tyreoidektomii. Ve výše uvedené době tento výkon nemá negativní dopad na průběh gravidity ani na vývoj plodu. Žena musí být k operaci připravena, tj. mít normální hladinu FT4. Po operaci ihned podáváme plnou substituční dávku tyroxinu. Léčba radiojodem je v těhotenství kontraindikována.
Léčba relabující Tx po porodu
U autoimunitních forem Tx dochází obvykle po porodu k relapsu Tx. Projevuje se to běžnými klinickými projevy a často i poruchami laktace. Po porodu je nutná klinická a laboratorní kontrola nejen po 4-6 týdnech, ale i v dalším období. Podávání tyreostatik podle současných názorů není kontraindikací kojení při dávkách thiamazolu do 20 mg/den.
Pokud je nutné pro aktualizaci tyreotoxikózy podat po porodu vyšší dávky, je vhodné kojení přerušit. Doporučuje se užití thiamazolu vždy po nakojení. Thiamazol i betablokátory přecházejí do mateřského mléka.
Subklinická Tx v graviditě
Na rozdíl od subklinické hypotyreózy nepředstavuje v graviditě subklinická Tx obvykle závažný zdravotní problém. Odlišení od fyziologického poklesu TSH v 1. trimestru gravidity se opírá především o vyšetření protilátek (TRAK) a nález na UZ štítné žlázy. Jediným možným rizikem je přechod subklinické Tx do manifestní formy. To je ovšem v graviditě zcela výjimečné. Rozhodně by bylo chybou ovlivňovat sníženou hladinu TSH bez zvýšené hladiny FT4 a/nebo FT3 a bez klinických známek Tx v graviditě podáváním tyreostatik [42].
Vedlejší účinky léků používaných k léčbě tyreotoxikózy na plod
- Methimazol
Při léčbě methimazolem byly ojediněle popsány negativní dopady na plod: choanální nebo esofageální atrézie a dysmorfie obličeje, aplasia cutis, hypoty-reóza plodu, struma plodu [43-47].
- Betablokátory
Dlouhodobé podávání (déle než 6 týdnů) je spojeno s intrauterinní růstovou retardací, bradykardií plodu a hypoglykémií novorozence [47]. Po betablokátorech byly popsány i častější spontánní potraty [48].
5.2.4 Prekoncepční odhalení rizika Tx a preventivní opatření
V současné době stoupá význam odhalení tyreotoxikózy u žen před početím. V rámci plánovaného rodičovství (prekoncepční péče) je možné odhalit některé faktory, které znamenají zvýšené riziko vzniku Tx v graviditě. Na tyto osoby by se měla zaměřit zvýšená péče ve smyslu prekoncepčního vyšetření tyreoidálního stavu (TSH, Anti-TPO, eventuelně UZ štítné žlázy, FT4). Týká se to především žen tzv. rizikových (viz kapitola 7). Optimální by bylo i vyšetření jodurie. Pak je možno prekoncepčně léčit zjištěné odchylky.
5.3 Tranzientní gestační hypertyreóza (TGH)
5.3.1 Klinický, laboratorní a sonografický obraz TGH
Při hyperfunkci štítné žlázy vyvolané stimulací placentárními hormony (tranzientní gestační hypertyreóza - TGH) je přítomná suprese TSH, protilátky TRAK (proti TSH receptoru) nejsou zvýšené a chybějí další známky přítomnosti autoimunitního procesu (další tyreoidální protilátky, hypoechogenita štítné žlázy při sonografickém vyšetření). Tyreoidální hormony (FT4 a FT3) v krvi bývají normální, ale mohou být i mírně zvýšené. Klinické příznaky většinou nejsou žádné, někdy tyto změny provází hyperemesis gravidarum a někdy mohou být i mírné klinické příznaky hypertyreózy.
5.3.2 Léčba TGH
Tento stav není indikací k podávání tyreostatik. Pokud jsou potíže výrazné, je možno v 1. trimestru gravidity se zvážením potenciálních rizik podávat betablokátory, které jsou však v pozdní fázi gravidity kontraindikované. Stav spontánně odeznívá koncem 1. trimestru.
5.4 Endokrinní orbitopatie v graviditě (Jiskra J.)
Endokrinní orbitopatie (EO) v graviditě je velmi vzácná, může se však vyskytnout a byla popsána dokonce i u eutyreózních žen [49]. Guidelines pro léčbu tyreopatií v těhotenství ani pro léčbu EO tuto problematiku nezmiňují. Důvodem je naprostá absence jakýchkoliv systematických studií z důvodu nízké incidence onemocnění. Léčba je tudíž zcela empirická a poznatky lze získat pouze z ojedinělých publikovaných kazuistik. Základními předpoklady léčby jsou co nejrychlejší dosažení eutyreózního stavu, zanechání kouření a správná klasifikace aktivity a závažnosti onemocnění. Žena by měla být odeslána do specializovaného centra vždy, když jde o střední až těžkou či zrak ohrožující EO. Léčebný postup u lehké aktivní EO se v graviditě neliší od běžné populace. Jde o lokální léčbu (umělé slzy, sluneční brýle apod.) a lze vyzkoušet efekt tablet se selenem v dávce 2x200 µg denně. U střední až těžké se vždy postupuje individuálně. Je-li ohrožen zrak ženy, je na místě podání vysokých dávek kortikoidů (methylprednisolon) i.v. v pulsech podobně jako u běžné populace. Kumulativní dávka by měla být co nejmenší při zachování účinnosti. Obvykle je snaha podávat dávky menší než u netěhotných - kumulativně do 2-3 g během 6 týdnů v závislosti na efektu léčby a stupni těhotenství (raději menší dávky v 1. trimestru) a není-li patrný efekt, je třeba přistoupit k chirurgické dekompresi orbity. Tato léčba měla v publikovaném případě dobrý efekt [49]. Methylprednisolon nebyl z důvodu nedostatku dat dosud FDA stran potenciálních rizik v těhotenství kategorizován, nežádoucí účinky na vývoj plodu jsou tedy možné (zejména v 1. trimestru), ale kontrolovaná data u lidí nejsou k dispozici. Dosud dostupná data jsou rozporuplná – bylo publikováno riziko rozštěpu rtu u dětí při podání steroidů v 1. trimestru [50], na druhou stranu se ukázalo, že steroidy jsou z velké části metabolizovány přímo v placentě a k plodu se dostane jen nepatrná část [51]. V publikovaných případech byl perorální prednison podáván z indikace EO bez negativního vlivu na plod již od konce 1. trimestru [52]. Alternativou k i. v. pulzům methylprednisolonu se jeví aplikace i. v. pulzů imunoglobulinů (IVIG), které nejsou teratogenní [53], a které se používají v graviditě při léčbě roztroušené sklerózy [54]. U těhotných žen s EO však s nimi nejsou dosud žádné zkušenosti. Radioterapie je v těhotenství kontraindikovaná.
6. Ženy s infertilitou, po potratu a po předčasném porodu
Jiskra J.
6.1 Úvod
Je prokázáno, že nejen plně vyjádřená (manifestní) tyreoidální dysfunkce, ale i subklinická hypotyreóza či pouhá pozitivita tyreoidálních protilátek (ThAb) - proti tyreoidální peroxidáze (Anti-TPO) a/nebo proti tyreoglobulinu (Anti-Tg) - je spojena s vyšší prevalencí infertility, potratů, předčasných porodů a dalších komplikací gravidity [32].
6.2 Ženy se zvýšeným rizikem infertility, potratů a předčasných porodů z důvodu tyreopatií
Nejvíce rizikových žen je ve skupině s manifestní nebo subklinickou hypotyreózou a ve skupině žen s normální tyreoidální funkcí a pozitivními Anti-TPO, protože těch je nejvíce (10-15 % žen ve fertilním věku). Tyto ženy jsou ve valné většině asymptomatické a nejsou diagnostikovány, pokud není vyšetření provedeno záměrně. Subklinická hypertyreóza tyreoidální etiologie je u žen ve fertilním věku mnohem vzácnější (viz kapitola 6). Vyšetření TSH a Anti-TPO v krvi by proto mělo být provedeno u všech žen s infertilitou, po potratu, předčasném porodu či u žen s jinak komplikovaným těhotenstvím, které plánují další graviditu.
6.3 Léčba tyreopatií u žen s infertilitou, po potratu či předčasném porodu
Názor na léčbu žen s manifestními tyreoidálními dysfunkcemi je jednoznačný – měla by se ihned zahájit a strategie léčby se neliší od běžné populace. Podobně se doporučuje léčit ženy se subklinickou hypotyreózou a současně pozitivními Anti-TPO. Cílové hodnoty TSH při léčbě jsou 0,5-2,5 mIU/l [2,3] (viz kapitola 4).
Nejasnosti stran léčby levotyroxinem však stále přetrvávají především u žen s normální tyreoidální funkcí a pozitivními Anti-TPO, u žen se subklinickou hypotyreózou, ale negativními Anti-TPO a žen s izolovanou hypotyroxinémií (to se týká jak těhotných žen, tak žen s infertilitou a žen po spontánních potratech). Máme zatím jen omezené množství informací z randomizovaných kontrolovaných studií (RCT), proto nelze jednoznačně říci, že léčba levotyroxinem v těchto případech snižuje incidenci potratů, předčasných porodů, či jiných komplikací těhotenství, zlepšuje fertilitu či zlepšuje psychomotorický vývoj narozených dětí. Ve studii Negro et al. [21] byla při podávání levotyroxinu eutyreózním Anti-TPO-pozitivním ženám redukce incidence potratů o 36 % a předčasných porodů o 69 %. V další studii bylo podáváním levotyroxinu eutyreózním Anti-TPO-pozitivním ženám při IVF dosaženo redukce incidence potratů o 75 % [55]. Obě studie jsou ze stejného pracoviště, a to je jeden z argumentů, proč některé autority nepovažují tyto důkazy za dostatečné, a výsledky těchto studií se nepromítly do nejnovějších doporučení z r. 2011 [2,3]. Proto je postup v těchto situacích zatím individuální.
6.4 Faktory, které u žen s infertilitou, po potratu či předčasném porodu podporují zahájení léčby hraničních stavů levotyroxinem
V rozhodování zda léčit nebo neléčit hraniční stavy (subklinická hypotyreóza s negativními Anti-TPO, pozitivní Anti-TPO s normální tyreoidální funkcí, izolovaná hypotyroxinémie) levotyroxinem může být prospěšné zvážení následujících ukazatelů: přítomnost dalších rizikových faktorů (tyreopatie či autoimunitní onemocnění v rodinné či osobní anamnéze), počet potratů, počet předchozích neúspěšných cyklů IVF, komplikace v předchozích těhotenstvích, výše titru Anti-TPO [17], sérové koncentrace FT4, nález na sonografii štítné žlázy [56] a také preference vyšetřované ženy. Faktem je, že u žen s infertilitou, před plánovaným cyklem IVF a u žen s potraty v anamnéze přistupujeme k léčbě hraničních stavů častěji než u jinak zdravých těhotných žen, i když tento postup není „evidence-based“. Je nezbytné si uvědomit, že příprava IVF vyvolá “hormonální bouři“, na kterou tyreoidea postižená autoimunitním zánětem může reagovat přiměřeně (obr. 1).
Obr. 1. Diagnostický a léčebný postup u žen s infertilitou, po potratu, předčasném porodu či jinak komplikovaném těhotenství, které plánují další graviditu 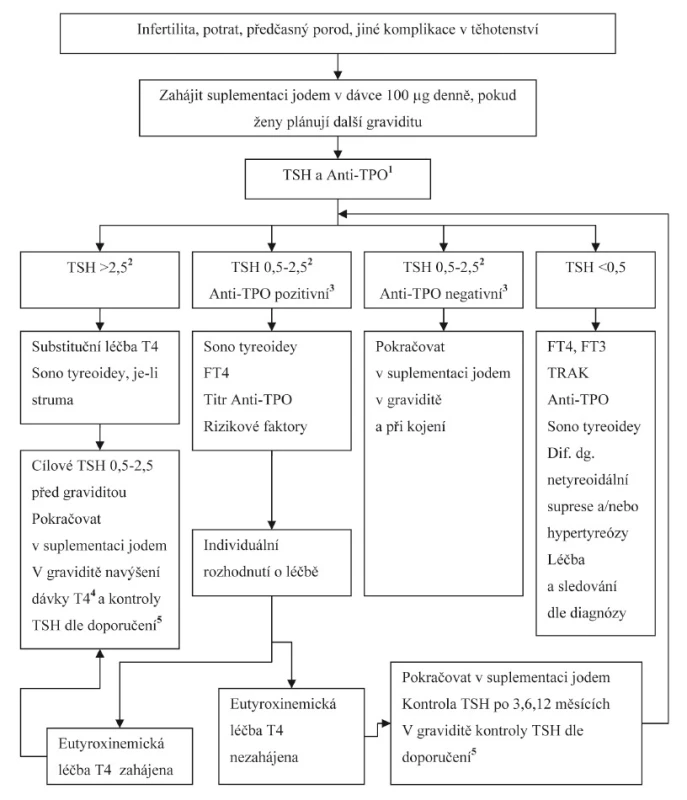
T4: levotyroxin, TSH: sérové koncentrace tyreoidálního stimulačního hormonu (mIU/l), Anti-TPO: sérové koncentrace protilátek proti tyreoidální peroxidáze (kIU/l), FT4: sérové koncentrace volného tyroxinu (pmol/l) 1 ne dříve než 6 týdnů po zahájení suplementace jodem, abychom minimalizovali podíl jodového deficitu na elevaci TSH 2 hodnota 2,5 mIU/l platí pro metody s horním limitem 4,0 mIU/l, přesněji jde o horní limit konkrétní metody snížený o 1,5 mIU/l, nejlépe horní limit TSH pro těhotné ženy konkrétní laboratoře, pokud je k dispozici 3 dle norem konkrétní laboratoře; za klinicky významné se v těhotenství považuje zvýšení na minimálně dvojnásobek normy uváděné výrobcem [17] 4 navýšení dávky levotyroxinu průměrně asi o 30 % [potřeba zvýšení dávky je individuální (25-50 %) v závislosti na příčině hypotyreózy a množství zbytkové funkční tyreoidální tkáně] 5 v graviditě kontroly TSH v 5.-6., 10.,14. a 20. týdnu (± 1 týden), dále po šestinedělí a každé 3 měsíce 1. rok po porodu a každých 6 měsíců 2. rok po porodu. Doporučení ATA 2011 uvádějí ještě kontrolu TSH mezi 28.-30. týdnem těhotenství, podle našich zkušeností je však tato kontrola při dobrém klinickém průběhu málokdy důvodem ke změně terapie, proto ji považujeme za nadbytečnou. Dle doporučení ATA 2001 by však ženy plánující graviditu měly mít TSH do 2,5 mIU/l [2,3], nebo přesněji dle našich doporučení ne vyšší než je horní hranice normy dané metody snížená o 1,5 mIU/l, což implikuje zahájení léčby u všech žen se subklinickou hypotyreózou bez ohledu na Anti-TPO. Naopak léčbu izolované hypotyroxinémie levotyroxinem ATA rutinně nedoporučuje. Domníváme, že v našich podmínkách by měla být izolovaná hypotyroxinémie (FT4 méně než dolní hranice normální hodnoty pro běžnou populaci) léčena pouze tehdy, pokud se vyskytne za podmínek dostatečného příjmu jodu a současně nejde o interferenci z důvodu změny poměru volné a vázané frakce při vzestupu vazebných bílkovin v těhotenství. Všechny ženy, usilující o graviditu, by měly být suplementovány jodem v dávce 100 µg denně, recentní revidovaná guidelines Endocrine society doporučují dokonce dávky o něco vyšší (150-200 µg denně) [4].
7. Struma, uzlová přestavba ve štítné žláze
Límanová Z.
7.1 Struma difúzní
Problematika difúzní zvětšené tyreoidey není v Doporučení ATA [2,3] zmiňována, pro ČR se stručně o difúzních strumách zmíníme:
S objemnými strumami se u mladších žen v ČR již nesetkáváme, pokud taková situace v graviditě nastane (většinou imigrantky), léčíme dle etiologie, operační postup je nezbytný v případě mechanických příznaků. Při nálezu difúzní strumy neodkladně zjistíme etiologii (základní laboratoř), UZ krku včetně posouzení uzlin, a řešení se řídí její příčinou. V našich podmínkách jde nejčastěji o důsledek choroby GB nebo o strumu Hashimotovu (na podkladě CLT). Klinické vyšetření s podrobnou anamnézou, příznaky poruchy funkce, výsledky laboratoře - FT4, TSH, protilátky včetně TRAK a UZ nasměrují snadno k léčbě. Zjistíme-li poruchu funkce (viz kapitoly 3 a 6). U rychle rostoucího většinou jednostranného postižení může být příčinou i malignita netyreoidálního původu (viz dále).
7.2 Struma uzlová, uzly ve štítné žláze
Pokud je štítná žláza změněna uzlovou přestavbou, ať jde o uzel, zjištěný již před graviditou nebo v graviditě, nebo náhodný nález odhalený při UZ v nezvětšené žláze, postupujeme v graviditě obdobně jako u netěhotných pouze s tou výjimkou, že s určením etiologie spěcháme až urgentně, dle charakteru uzlu [57]. Klademe důraz na vyšetření protilátek Anti-TPO, protože v ČR jsou uzly v terénu CLT poměrně časté a standardně protilátky doplňujeme – příčinou uzlu často bývá CLT. Uvážíme vyšetření kalcitoninu, především při klinickém podezření na medulární karcinom (anamnéza, výsledek FNAB). Ke standardním postupům vyšetření kalcitoninu nepatří.
7.2.1 Gravidita a uzlová přestavba
Opakovanými graviditami má tyreoidea tendenci k uzlovatění, jak dokládají studie z oblastí s mírným až středním deficitem. Prevalence uzlů ve štítné žláze před graviditou je uváděna u 3-21% žen a počet uzlů stoupá s počtem parity [58,59]. Ve studii z r. 1993 [58] byl před graviditou zachycen uzel u 9 % žen a výskyt stoupal na 20,7% resp. 33,7% po druhém a třetím těhotenství. Vyšší věk je spojen taktéž s vyšším počtem uzlů - 11-20 % žen s 1 uzlem mělo po 2. graviditě druhý uzel. Uzly se patrně těhotenstvími i zvětšují, 60 % uzlů velikosti 5-12 mm zdvojnásobilo v graviditě velikost. Uváděné studie jsou staršího data a pocházejí z oblastí s mírným až středním nedostatkem jodu. Pro ČR nemáme pro graviditu recentní ani relevantní studie.
7.2.2 Vyšetření uzlů v graviditě
Postup je obdobný jako v běžné populaci, je však nutné vyšetření uskutečnit bezodkladně s ohledem na psychiku těhotné. Výtěžek FNAB může díky překrvení žlázy v těhotenství být pod limitem hodnotitelnosti, lepší buněčný zisk je možný při punkci bez aspirace. Sama gravidita cytologické hodnocení nekomplikuje. Akcentujeme rodinnou anamnézu - mimo obvyklé choroby cílíme dotaz na výskyt medulárního karcinomu (MEN 2), familiární polypózu - Gardnerův syndrom, karcinom tyreoidey. V osobní anamnéze opět mimo obvyklé dotazy nás zajímá záření krku, léčba pro jakoukoliv malignitu (možná metastáza), rychlost růstu uzlu. Palpace včetně vyhledávání zvětšených uzlin je samozřejmostí.
Vyšetření má být neodkladné a kvalitní – např. při UZ se musí vyšetřující v závěru vyjádřit i k charakteristice uzlu. Suspekci vyvolávají nepravidelné okraje, uzel výrazně hypoechogenní, je-li osa delší než širší, přítomnost chaotických cévních spotů a/nebo i mikrokalcifikací. Při přítomností 1 a více z uvedených kritérií je oprávněné podezření z malignity. Prorůstání uzlu do okolí a /nebo zvětšené uzliny jsou pro malignitu typické. Na rozdíl od doporučení ATA, ve kterých u nesuspektních uzlů lze FNAB uskutečnit až po porodu a menší uzly než 10 mm nevyžadují FNAB, v ČR doporučujeme FNAB vždy u uzlů nad 10 mm a/nebo u uzlů sonograficky či klinicky suspektních (např. RA, rizikové faktory) provést vždy. Rychlým růstem uzlu se projevuje karcinom anaplastický, dále lymfom, příčinou může i metastáza (plíce, ledviny, prs), stav vyžaduje rychlé vyšetření opět s využitím UZ a FNAB. Další postup opět dle etiologie.
Laboratorní vyšetření: obvyklé TSH a FT4 většinou k diagnóze nepřispěje, na druhé straně však doporučujeme Anti-TPO (podpoří diagnózu CLT, což je důležitá informace pro cytopatologa), a při podezření z medulárního karcinomu nebo MEN (klinika, RA) je vyšetření kalcitoninu nezbytné. Prospektivní studie prokázaly, že rutinní vyšetření sérového kalcitoninu u neselektované populace s uzlem ve štítné žláze detekuje medulární karcinom pouze asi u 1 z 200-300 vyšetření [60,61].
7.2.3 Postup při nálezu (benigního) uzlu
Gravidita je rizikovým faktorem pro uzlovatění ve štítné žláze, ale rozhodně v této době není indikována supresní léčba. Je-li uzel benigní dle UZ a FNAB (Bethesda II), lze rozhodnutí o operaci snadno odložit po porodu. Výjimku tvoří benigní uzly, vyvolávající mechanický syndrom (útlak trachey), v těch případech je operace indikována ke konci 2. trimestru, obdobně přistupujeme k uzlu rychle rostoucímu – na rozdíl od Doporučení ATA [1], který připouští i postup rezervovanější – odklad operace po porodu.
7.2.4 Malignita na základě FNAB u gravidních žen
Jak často je ve vyšetřovaném uzlu odhalena malignita, rozdílně uvádějí tři starší nevelké studie: v selektované populaci gravidních žen na exklusivních pracovištích byl pozitivní histologický u 6/40 - [62], 7/57 [63] a 7/16 [64]. Naopak v Číně byl sice diagnostikován uzel u 15,3 % ze souboru 221 (nález především z UZ, jen minimum bylo palpovatelných) vyšetřovaných těhotných, ale nebyla prokázána žádná malignita hodnocením z klinického průběhu. Jen u minima však byl nález ověřen FNAB [52]. Vesměs jde o starší studie a menší soubory. Postup při záchytu malignity či podezření na malignitu ve FNAB (Bethesda V-VI) je v kapitole 8.3.
7.2.5 Nejistý – hraniční suspektní výsledek FNAB
Svědčí-li cytologické hodnocení pro folikulární či onkocytární neoplazii nejisté biologické povahy (Bethesda III-IV), doporučuje se další klinická rozvaha s opakováním UZ a punkce za 3 měsíce. Jsou-li jakékoliv diagnostické pochybnosti či klinické podezření na malignitu, je možná operace v graviditě (ke konci 2. trimestru), která umožní klidný porod a kojení. V úvahu je nutné vzít i přání těhotné ženy.
8. Karcinom štítné žlázy v graviditě
Límanová Z.
8.1 Výskyt
Karcinom tyreoidey tvoří asi 1% ze všech malignit a při vyšetřování v neselektované populaci se uvádí pozitivní nález asi v 5% uzlů. V graviditě je tato diagnóza závažným, nikoliv neřešitelným zjištěním. Výskyt karcinomu štítné žlázy v graviditě je většinou uváděn jako obdobný s běžnou populací, ale dosavadní studie zahrnují malé počty a často selektovanou populaci. Početný soubor pochází z registru 4,846.505 těhotných žen, které porodily v Kalifornii. Bylo zachyceno 14,4/100.000 žen s karcinomem tyreoidey a dle očekávání převažoval karcinom papilární. U 75% případů byl karcinom odhalen do 1 roku po porodu, u 24 % před porodem a u cca 1% v době porodu [65].
8.2 Ovlivňuje gravidita růst karcinomu tyreoidey?
Důležitá je úvaha, zda gravidita prognózu karcinomu zhoršuje. Odpověď není jednoznačná: ze 7 publikací, ve kterých byla diagnóza karcinomu stanovena v graviditě nebo do 1 roku po porodu, výsledky 6 studií podporují domněnku, že gravidita prognózu nezhoršila, a k této domněnce se přiklání i ATA r. 2011 [66]. Nicméně jedna studie 15 žen [67] považuje situaci za prognosticky horší a opírá se o nález estrogenních receptorů ve tkáni karcinomu tyreoidey, ale k potvrzení závěrů je nutné získat více informací. Recentní studie připomínají, že mimo estrogenové receptory mohou hrát v graviditě roli i růstové faktory - vše je však v oblasti úvah a výzkumu. Dopad gravidity na medulární a anaplastický karcinom není znám.
8.3 Jak řešit průkaz (podezření) papilárního karcinomu?
Je-li dle FNAB uzel maligní nebo je podezření na malignitu (Bethesda V-VI), měl by se tumor odstranit raději v graviditě, obdobně by se měl řešit uzel, je-li choroba pokročilá, je uzel objemný, nebo uzel v graviditě roste o 50 % objemu a 20 % nejméně v jednom rozměru. Pokud se ve 2. polovině gravidity uzel nemění, může se operovat po porodu, ale je vhodné udržet TSH mezi 0,1-1,5 mIU/l, což někdy vyžaduje podání T4. Kontrola uzlu, monitorování růstu a případných uzlin a vyšetření UZ se doporučuje uskutečnit každý trimestr. Případné opakovaní FNAB a řešení dle etiologie je možné ke konci 2. trimestru. V ČR je zvyklostí postupovat radikálněji, spíše doporučujeme operaci ještě v graviditě, zvláště při podezření na diferencovaný karcinom. Substituce je nezbytná ihned po operaci a udržení TSH v graviditě pod 0,1 mIU/l. Doléčení radiojodem se uskuteční až po ukončení kojení. Nicméně se názor na indikaci k operaci tyreoidey i při průkazu karcinomu tyreoidey různí. S ohledem na vlastnosti nádoru (pomalý růst a skutečnost, že negativní vliv gravidity na růst karcinomu nebyl jednoznačně prokázán), je možné akceptovat dva postupy. První postup, který je uváděn v Doporučení 2011 [2,3] uvažuje o odložení chirurgického výkonu po porodu a bere v úvahu možné i operační riziko pro matku a dítě. Druhý postup, který podporujeme my, je uskutečnění operace ke konci 2. trimestru, s okamžitě zahájenou plnou substitucí a dosažením TSH k hodnotě 0,1 mIU/l co nejdříve. Je-li léčba radiojodem následně indikována, je možné ji odložit až po ukončení kojení. Druhý postup se opírá o následující argumenty: pro matku je představa odkladu plánované operace nepochybně stresem, naopak operace před porodem umožní klidný poporodní průběh a kojení. V rukou zkušeného chirurga není totální tyreoidektomie výkonem delším než 60-90 minut. U žen, které jsme indikovali, jsme nezaznamenali žádnou komplikaci ze strany matky či dítěte. Není však jednoznačný závěr a je tedy možné respektovat přání budoucí matky. Výjimku tvoří mikrokarcinomy, které jsou většinou po určitou dobu stacionární a nízkorizikové, a odložení operace po porodu je tedy možné.
8.4 Gravidita u ženy, již dříve léčené pro diferencovaný karcinom tyreoidey
Po prodělané léčbě radiojodem by žena neměla otěhotnět dříve než za 6 měsíců, důvodem je především ustálení supresní dávky levotyroxinu. Při dodržení tohoto postupu nebyl prokázán negativní vliv léčby radiojodem na fertilitu, průběh gravidity, potrácení či na vývoj dítěte. Je vhodné připomenout, že jedna studie, vycházející z početného souboru 483 žen prokázala vyšší riziko potrácení za 6-12 měsíců po léčbě radiojodem [68], další [69] upozorňuje na přechodné poruchy cyklu po léčbě radiojodem a možný nepatrně časnější nástup menopauzy. Graviditu tyto ženy tedy bezpečně mohou podstoupit po uplynutí nejméně 6, raději však 12 měsíců [68].
Pokud těhotná žena obdržela léčebnou dávku radiojodu a nevěděla, že je těhotná, je namístě úvaha o přerušení těhotenství, pokud gravidita pokračuje, je nutné sledování plodu a včasná léčba případně vzniklé hypotyreózy. Tyto situace jsou zřejmě vzácné.
Muž, který byl léčen radiojodem, by neměl ženu oplodnit dříve než 3-4 měsíce po aplikaci radiojodu.
8.5 Hladiny TSH u ženy, která prodělala léčbu pro diferencovaný karcinom tyreoidey, při plánování gravidity a v jejím průběhu
U žen, které prodělaly léčbu pro karcinom tyreoidey, cílová hodnota TSH v graviditě záleží na nálezech v prekoncepčním období. Před koncepcí je doporučena raději suprese TSH pod 0,1 mIU/l. V průběhu gravidity pak u žen bez známek choroby a s nízkým rizikem může být TSH v normálním pásmu 0,3-1,5 m IU/l. Je-li persistence choroby, ale žena je bez známek choroby, TSH má být pod 0,1 mIU/l. Pokud žena patří do skupiny s vysokým rizikem, má být TSH 0,1-0,5 IU/l. Kontrola hladiny TSH jsou nutné, obvykle na počátku gravidity ihned po jejím potvrzení je nezbytné malé zvýšení dávky, uvádí se o 9 % v 1. trimestru, o 21 % ve druhém a o 26 % ve třetím trimestru, ale řešení je vždy individuální [70]. Kontroly po 4 týdnech do 20. týdne v té samé laboratoři jsou potřebné, a jedna kontrola mezi 26.-32. týdnem. Některé ženy potřebují adjustaci dávky i ve 2. trimestru [68]. Hladina Tg by měla být vyšetřena před graviditou a po porodu. Doporučuje se sledování UZ v každém trimestru u žen, které měly vysoký Tg ještě před graviditou nebo byly známky persistence choroby.
8.6 Zvyšuje gravidita riziko rekurence diferencovaného tyreoidálního karcinomu?
Odpověď není jednoznačná, zvýšené riziko však prokázáno nebylo. Jiná situace však je u žen s persistencí choroby. O stimulaci tkáně karcinomu graviditou (estrogeny, růstovými faktory) uvažuje Hirsch [67]. Uvádí, že progrese choroby je možná, i když nemusí být jednoznačně důsledkem gravidit. Je-li žena bez známé choroby („disease free“), není v graviditě nutné sledovat UZ ani hladinu Tg. Jiná je situace u žen s vysokým Tg nebo známkami aktivity choroby – u nich jsou doporučeny kontroly UZ a hladiny Tg každý trimestr. Řešení je individuální - situace jsou vzácné. U žen bez známek aktivity choroby se riziko nezvyšuje, ale stimulace růstu karcinomu u osob se známými strukturálními nebo biochemickými známkami je graviditou možná [65,67]. Těhotenství v těchto případech není indikací k přerušení gravidity.
8.7 Operace štítné žlázy v graviditě u eufunkční ženy
Pokud indikujeme operaci štítné žlázy v graviditě pro podezření z malignity, je samozřejmě nutné vážit možné komplikace pro matku a dítě. Operace ke konci druhého trimestru je však dobře snášena: Studie 113 operací za 22 let většinou ve 2. trimestru nezaznamenala žádné komplikace [62], další studie srovnávající operaci 201 gravidních žen zaznamenala mateřské komplikace ve 4,5 % a fetální v 5,5 %, ale chybělo srovnání s kontrolním souborem. Okamžitá substituce po operaci je samozřejmostí. U žen s mikrokarcinomem, který je považován za nízkorizikový, je možné vyčkat s operací až po porodu.
9. Screening tyreopatií v graviditě
Jiskra J.
9.1 Úvod
Přestože panuje shoda, že neléčené manifestní i subklinické tyreopatie a dokonce i pozitivní tyreoidální protilátky s normální funkcí mají negativní vliv na průběh gravidity a vývoj plodu, zůstává screening tyreopatií v těhotenství stále kontroverzním tématem. Obecné podmínky univerzálního screeningu a jejich naplnění jsou uvedeny v Tabulce 6 [71]. Světové odborné, především endokrinologické společnosti, dosáhly konsensu v tom, že screening je potřebný, není ale dosud jednotný názor na jeho konkrétní podobu. Posun nastal v tom, že za rizikový faktor je považován věk nad 30 let [2, 3].
Tab. 6. Obecné podmínky pro zavedení univerzálního systematického screeningu, které jsou/nejsou splněny (upraveno podle [71]) ![Obecné podmínky pro zavedení univerzálního systematického screeningu, které jsou/nejsou splněny (upraveno podle [71])](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/e36869cadb3a3a28b8d81bd6c37e36a1.png)
Hlavní rozpory jsou v rozsahu screeningu (univerzální nebo cílený na rizikové skupiny), ve vyšetřovaných parametrech, v otázce kdy a kým má být screening realizován, jak má být financován, kdo se na něm má podílet, a částečně také, jak se mají ženy s pozitivním výsledkem screeningu léčit. V průběhu pokračujících diskuzí se odborníci k univerzálnímu screeningu stále častěji přiklánějí [4].
9.2 Rozsah screeningu - univerzální nebo cílený?
Celosvětově dosud nebylo dosaženo konsenzu, zda má být screening univerzální (celoplošný) nebo má být cílený na rizikové skupiny žen („case-finding screening“) [2, 3] (Tabulka 7).
Tab. 7. Přehled doporučení světových společností v otázce screeningu tyreopatií v graviditě a vývoj názorů v posledních letech (upraveno podle [71]) ![Přehled doporučení světových společností v otázce screeningu tyreopatií v graviditě a vývoj názorů v posledních letech (upraveno podle [71])](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/f9ab16f4ad1aecb10d65881e6d15a18e.png)
Hlavními argumenty odpůrců univerzálního screeningu jsou nedostatek randomizovaných kontrolovaných studií (RCT), které by prokázaly, že léčba subklinické hypotyreózy a žen s pozitivními tyreoidálními protilátkami a normální funkcí redukuje komplikace v těhotenství či pozitivně ovlivňuje vývoj dětí. Randomizovaných studií, o které se opírají jak zastánci, tak odpůrci univerzálního screeningu, je málo a mají často závažné limitace [4, 21,22, 55, 71-73]. Další studie dále probíhají, na jejich výsledky však budeme muset ještě několik let počkat („A Randomized Trial of Thyroxine Therapy for Subclinical Hypothyroidism or Hypothyroxinemia Diagnosed During Pregnancy“, „The Effect of Thyroid Hormone Levels in Pregnant Women on the Intelligence Quotient (IQ) of Their Children“).
Skutečností je, že při realizaci case-finding screeningu (cíleného na rizikové skupiny), který podporují poslední světová doporučení [1], nejméně 25-50 % žen s abnormalitami v tyreoidálních laboratorních testech uniká diagnóze (obr. 2). Rozšíření dosavadních rizikových faktorů o věk nad 30 let dle doporučení ATA 2011 ([2, 3], Tabulka 8) významně zvýší procento těhotných žen, které budou ve screeningu laboratorně vyšetřeny, což je sice pozitivní, avšak racionální základ toto doporučení nemá a je zjevně kompromisem. Ukázalo se totiž, že věk nad 30 let není významným rizikovým faktorem pro záchyt tyreopatií v těhotenství a že věk riziko tyreopatií u těhotných žen nijak významně neovlivňuje [74].
Obr. 2. Únik ze screeningu v případě strategie case-finding 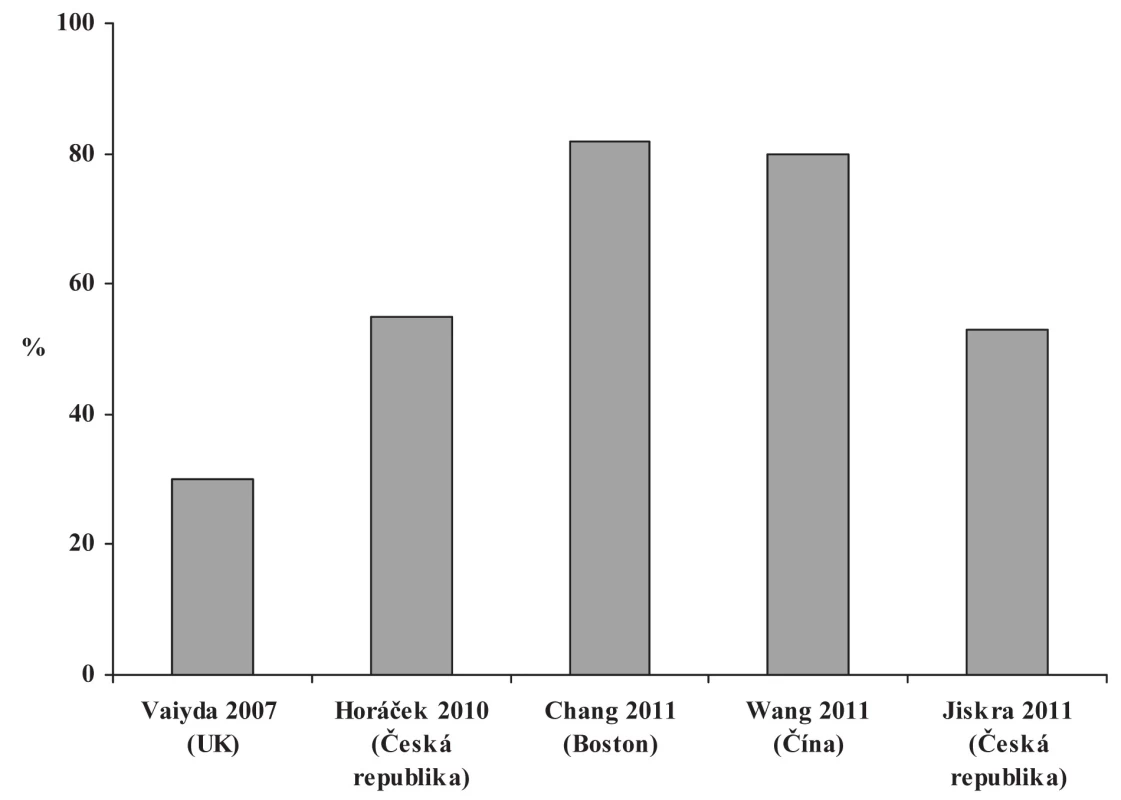
Vaiyda et al. 2007[75], Chang et al. 2011 [76], Wang et al. 2011 [77]: hypotyreóza; Horáček et al. 2010 [26], Jiskra et al. 2011 [78]: hypotyreóza a/nebo pozitivní Anti-TPO Tab. 8. Ženy, které mají zvýšené riziko tyreopatie v těhotenství [3] ![Ženy, které mají zvýšené riziko tyreopatie v těhotenství [3]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/dda0c741f0ae44f7aab85b234fb416ed.png)
Efektivitu cíleného screeningu by nepochybně zlepšila forma dotazníku, který by všechny těhotné ženy při první návštěvě u gynekologa vyplnily. Informace, které ČES JEP ČLS poskytuje praktickým (rodinným) lékařům pro ženy ve fertilním věku nepochybně prospějí lepšímu chápání celé složité problematiky. Spolupráce s nimi se slibně rozvíjí.
9.3 Načasování screeningu
Závažnou a diskutovanou otázkou je načasování screeningu. Štítná žláza plodu začíná tvořit tyreoidální hormony od 12. gestačního týdne, nicméně až do 18.-20. týdne je sekrece nedostatečná a plod je závislý na mateřském tyroxinu. Mateřský tyroxin je zřejmě v určitém množství nutný i v dalších fázích těhotenství. Kritické období vývoje CNS spojené s radiální migrací neuronů do mozkové kůry začíná již v 11. gestačním týdnu [79], možná i dříve. Plod je tedy do 12. týdne zcela a později minimálně částečně závislý na sekreci tyroxinu matkou. Podle doporučení ATA 2011 je vhodné, aby žena plánující graviditu neměla TSH v krvi vyšší než 2,5 mIU/l [2, 3]; přesněji řečeno by TSH nemělo být vyšší než je horní limit dané metody snížený o 1,5 mIU/l, nebo nejlépe horní limit normálního rozmezí pro 1. trimestr gravidity, pokud jsou normy pro danou metodu pro těhotné ženy k dispozici.
9.3.1 Těhotenský screening
V případě těhotenského screeningu je optimální odběr v 5.-6. týdnu gravidity a má zahrnout kromě TSH vždy i Anti-TPO. TSH (a rovněž FT4) může být v této časné fázi těhotenství i falešně negativní. Druhou možností je využít prvního krevního odběru v těhotenství v rámci screeningu vrozených vývojových vad a HBsAg v 1. trimestru (9.-11. týdnu gravidity). Pokud screening v 1. trimestru není proveden, pak je vhodné jej realizovat alespoň při vyšetření v 16. týdnu gravidity při odběru na klasický „triple test“, tento odběr však nezachytí důležité období pro vývoj plodu v prvním trimestru. Využití spolupráce s praktickými lékaři je v začátcích. O obecných problémech s časnými krevními odběry v graviditě svědčí i práce Lazaruse [11].
9.3.2 Prekoncepční screening
Screening prekoncepční je zřejmě optimální. Toho lze reálně dosáhnout u žen, které se již s tyreopatiemi léčí, nebo byly vyšetřeny a jsou sledovány, anebo u žen, které o svém zvýšeném riziku vědí a které se o svůj zdravotní stav zajímají. Úloha praktických lékařů, praktických lékařů dětí a dorostu, endokrinologů, pe-diatrů či gynekologů je v těchto případech jednoznačná. Organizovaný univerzální prekoncepční screening nelze v současné době považovat za reálný, a není ani jasná doba, po kterou by vyšetření bylo možné považovat za validní. Celosvětové diskuze se na prekoncepční screening nezaměřují.
9.4 Co v rámci screeningu vyšetřovat?
Každý z navrhovaných ukazatelů (TSH/Anti-TPO/FT4) přináší jiné informace. Pozitivní Anti-TPO přinášejí důležitou informaci o možném snížení tyreoidální rezervy v průběhu gravidity (i když vstupní TSH i FT4 mohou být normální), rozvoji poporodní tyreoiditidy a vzniku porodnických komplikací (potraty, předčasné porody apod.) (viz kapitola 7). Vyšetření Anti-TPO by mělo být provedeno vždy, tj. jak ve screeningu prekoncepčním tak v časné fázi gravidity (5.-6. týden), kdy se možná snížená funkční tyreoidální rezerva nemusí ještě projevit změnami TSH a/nebo FT4. TSH je nejspolehlivější a nejstandardizovanější parametr k posouzení periferní poruchy tyreoidální funkce. Za určitých okolností však může být TSH ještě normální a jediným patologickým nálezem může být snížený FT4 (např. u jodového deficitu, reakce na vyšší potřebu sekrece tyreoidálních hormonů v těhotenství při vzestupu TBG, vzácně i při snížené reaktivitě tyreotropů hypofýzy). V současné době však nejsou pro FT4 v graviditě (navíc vyšetřovaného různými metodami), jednotné normy, což činí hodnocení FT4 v graviditě poněkud problematickým.
Za předpokladu suplementace všech těhotných žen jodem (100 µg denně) a s přihlédnutím k ekonomickým aspektům se pro těhotenský screening jeví v podmínkách České republiky jako nejvýhodnější kombinace TSH a Anti-TPO.
9.5 Jak postupovat při pozitivním screeningu?
V případě pozitivního screeningu, tj. kteréhokoliv z vyšetřených ukazatelů, musí definitivní diagnózu a rozhodnutí o event. léčbě určit endokrinolog. Farmakologická léčba by měla být zahájena u všech žen s manifestní hypertyreózou a se subklinickou hypotyreó-zou s pozitivními Anti-TPO. Přístup k léčbě žen s mírnou elevací TSH a negativními Anti-TPO a eutyreózních žen s pozitivními Anti-TPO není dosud přesně vymezen: měl by být individuální s ohledem RA a OA, na nález na ultrazvuku štítné žlázy, titry Anti-TPO, sérové koncentrace TSH a FT4 a další okolnosti (viz kapitola 3). Není chybou zahájit léčbu podle výše uvedených zásad (potenciální benefit a nevýznamné riziko) ani léčbu nezahajovat a pouze sledovat vývoj; rozhodnutí bude záviset na preferenci endokrinologa. Síla tohoto doporučení je menší pro absenci jednoznačných důkazů. Léčbu izolované hypotyroxinémie levotyroxinem v graviditě ATA 2011 rutinně nedoporučuje. Podrobně pojednávají o léčbě a sledování žen s tyreopatiemi v graviditě (viz kapitoly 4, 6, 7).
9.6 Finanční zajištění screeningu
V odborné literatuře byly dosud publikovány 2 „cost-effectiveness“ analýzy, které obě ukázaly, že univerzální screening je - přes všechny rozpory a trvající diskuze - nákladově efektivní [33,72,73]. Analýza nákladové efektivity je závislá na konkrétních socioekonomických podmínkách země. V České republice dosud žádná „cost-effectiveness“ či „cost-benefit“ analýza provedena nebyla. Orientační analýza nákladů na univerzální screening u skupiny 5520 náhodně vybraných těhotných žen ukázala, že v podmínkách České republiky byly náklady na 1 pozitivní výsledek screeningu (patologické TSH a/nebo pozitivní Anti-TPO) 3546 Kč, na záchyt jedné hypotyreózy 2685 Kč a na záchyt 1 ženy s pozitivními Anti-TPO 3850 Kč [80].
Univerzální screening je zřejmě nejefektivnější strategií k záchytu klinicky významných tyreopatií v těhotenství, přesto se ho nepodařilo ve většině světových zemí dosud prosadit. V současné době je v České republice možné a doporučené u všech těhotných žen uskutečnit cílené-„case-finding“-vyhledávání při vstupním gynekologickém vyšetření zhodnocením rizikových faktorů podle Tabulky 8 (ústně nebo formou dotazníku). Pokud je alespoň jeden z nich pozitivní, je vhodné realizovat laboratorní screening TSH a Anti-TPO, a pak jsou tyto ukazatele plně hrazeny ze zdravotního pojištění. Reálnou možností je zahrnout univerzální screening tyreopatií (stanovení TSH a Anti-TPO) u všech těhotných žen v 1. trimestru gravidity (ideálně v rámci prenatálního gynekologického screeningu), a u žen plánujících graviditu mezi nadstandardní vyšetření za přímou úhradu. Podmínkou je, že ženy budou o této možnosti přiměřeně informovány u svého gynekologa a praktického lékaře. ČES ČLS JEP bude nadále jednat s pojišťovnami o zařazení screeningu tyreopatií v těhotenství do hrazených výkonů.
Seznam použitých zkratek
ATA The American Thyroid Association
ETA The European Thyroid Association
TSH Tyreoideu stimulující hormon
T4 celkový tyroxin
FT4 volný tyroxin
T3 trijodtyronin
FT3 volný trijodtyronin
HCG choriový gonadotropin
TBG thyroxine binding globulin
CLT chronická lymfocytární tyreoiditida
GB Graves-Basedowova choroba
Tx hypertyreóza
PPT poporodní tyreoiditida
ThAb tyreoidální protilátky
Anti-TPO protilátky proti tyroidální peroxidáze
Anti-Tg protilátky proti tyreoglobulinu
SH subklinická hypotyreóza
TRAK protilátky proti TSH receptoru (Anti-TSH-R)
ICCIDD International Committee for Control of Iodine Deficiency Disorders
IFCC International Federation of Clinical Chemistry and Laboratory Medicine
IVF in vitro fertilizace
IVD in vitro diagnostika
FNAB biopsie tenkou jehlou
RCT randomizované kontrolované studie
UZ ultrazvuk štítné žlázy
Doporučení vzniklo ve spolupráci odborníků České endokrinologické společnosti ČLS JEP a České společnosti klinické biochemie ČLS JEP; výborem ČSKB ČLS JEP bylo schváleno 10. 12. 2012.
Doporučení bylo zveřejněno v časopise Diabetologie, metabolismus, endokrinologie, výživa (DMEV, ročník 16, č. 1, 2013), vychází se souhlasem redakce i vydavatele časopisu.
Zdroje
1. Abalovich, M., Nobuyuki, A., Barbour, L. A. et al. Clinical Practice Guideline. Management of thyroid dysfunction during pregnancy and postpartum: An Endocrine Society Clinical Practice Guideline. J Clin. Endocrinol. Metab., 2007, Aug 92 (8 Suppl), S1-47.
2. Stagnaro-Green, A., Abalovich, M., Alexander, E., Azizi, F., Mestman, J., Negro, R., Nixon, A., Pearce, E. N., Soldin, O. P., Sullivan, S., Wiersinga, W. Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum. Thyroid, 2011a, 21, p. 1-45.
3. Stagnaro-Green, A., Schwartz, A., Gismondi, R., Tinelli, A., Mangieri, T., Negro, R. High rate of persistent hypothyroidism in a large-scale prospective study of postpartum thyroidits in southern Italy. J Clin. Endocrinol. Metab., 2011b, 96, p. 652–657.
4. DeGroot, L., Abalovich, M., Alexander, E. K. et al. Management of thyroid dysfunction during pregnancy and postpartum: An Endocrine Society practice guidelines. J Clin. Endocrinol. Metab., 2012, 97, p. 2543-2565.
5. Zamrazil, V., Bilek, R., Cerovska, J., Delange, F. The elimination of iodine deficiency in the Czech Republic: the steps toward success. Thyroid, 2004, 14, p. 49-56.
6. Glinoer, D., Soto, M. F., Bourdoux, P. et al. Pregnancy in patients with mild thyroid abnormalities: maternal and neonatal repercussions. J Clin. Endocrinol. Metab., 1991, 73, p. 421-427.
7. Krassas, G. E., Poppe, K., Glinoer, G. Thyroid function and human reproductive health. Endocr. Rev., 2010, 31, 5, p. 702-55.
8. Límanová, Z., Zamrazil, V. Má být zaveden screening funkčních tyreoidálních onemocnění u dospělých v České republice? DMEV, 2004, 7, 3, p. 124-130.
9. Springer, D., Horáček, J., Hauerová, D. et al. Poruchy štítné žlázy v těhotenství - souhrn výsledků nezávislých studií. Čes. Gynek., 2007, 72, 6, p. 375-381.
10. Límanová, Z., Springer, D. Současné zkušenosti s vyšetřováním tyreopatií v graviditě - výsledky pilotního projektu. Čas. Lék. Čes., 2011, 150, p. 389-393.
11. Lazarus, J. H., Betswick, J. P., Channon, S., Paradice, R., Maina, A., Ries, R., Chiusano, E., John, R., Guaraldo, V., George, L. M., Perona, M., Dall’Amico, D., Parkes, A. B., Joomun, M., Wald, N. J. Antenatal thyroid screening and childhood cognitive function. New Engl. J Med., 2012, 366, p. 493-501.
12. Ghassabian, A., Bongers-Schokking, J. J., De Rijke, Y. B. et al. Maternal thyroid autoimmunity during pregnancy and the the risk of attention deficit/hyperactivity problems in children: the Generation R Study. Thyroid, 2012, 22, 2, p. 178-186.
13. Brent, G. A. The debate over thyroid –function screening in pregnancy. New Engl. J Med., 2012, 366, 6, p. 562-563.
14. Osorio, J. Thyroid screening in pregnancy - no effect on child cognition? Nature Reviews Endocrinology, 2012, 8, p. 193.
15. Morreale de Escobar, G., Obregon, M. J., Escobar del Rey, F. Maternal thyroid hormones early in pregnancy and fetal brain development. Best Pract. Res. Clin. Endocrinol. Metab., 2004, 18, p. 225-248.
16. Wiliams, G. R. Neurodevelopment and neurophysiological actions of thyroid hormone. Journal of Neuroendocrinology, 2008, 20, 6, p. 784-794.
17. Springer, D., Zima, T., Limanova, Z. Reference intervals in evaluation of maternal thyroid function during the first trimester of pregnancy. Eur. J Endocrinol., 2009, 160, p. 791–797.
18. McKenzie, J. M., Zakarija, M. Fetal and neonatal hyperthyroidism and hypothyroidism due to maternal TSH receptorantibodies. Thyroid, 1992, 2, p. 155–159.
19. Benhadi, N., Wiersinga, W. M., Reitsma, J. B., Vrijkotte, T. G. M., Bonsel, G. J. Higher maternal TSH levels in pregnancy are associated with increased risk for miscarriage, fetal and neonatal death. Eur. J Endocrinol., 2009, 160, p. 985–991.
20. Casey, B. M., Dashe, J. S., Wells, C. E., McIntire, D. D., Leveno, K. J., Cunningham, F. G. Subclinical hyperthyroidism and pregnancy outcomes. Obstet. Gynecol., 2006, 107 (2 Pt 1), p. 337-341.
21. Negro, R., Formoso, G., Mangieri, T., Pezzarossa, A., Dazzi, D., Hassan, H. Levothyroxine treatment in euthyroid pregnant women with autoimmune thyroid disease: effects on obstetrical complications. J Clin. Endocrinol. Metab., 2006, 91, p. 2587-2591.
22. Negro, R., Schwartz, A., Gismondi, R., Tinelli, A., Mangieri, T., Stagnaro-Green, A. Universal screening versus case finding for detection and treatment of thyroid hormonal dysfunction during pregnancy. J Clin. Endocrinol. Metab., 2010, 95, p. 1699-1707.
23. Alexander, E. K., Marqusee, E., Lawrence, J., Jarolim, P., Fischer, G. A., Larsen, R. Timing and magnitude of increases in levothyroxine requirements during pregnancy in women with hypothyroidism. New Engl. J Med., 2004, 351, p. 349-353.
24. Yassa, L., Marqusee, E., Fawcett, R., Alexander, E. K. Thyroid hormone early adjustment in pregnancy (the THERAPY trial). J Clin. Endocrinol. Metab., 2010, 95, p. 3234-3241.
25. Pop, V., Brouwers, E. P., Vader, H. L., Vulsma, T., Van Baar, A. L., De Vijlder, J. J. Maternal hypothyroxinaemia during early pregnancy and subsequent child development: a 3-year follow-up study. Clin. Endocrinol., 2003, 59, 282-288.
26. Horáček, J., Špitálníková, S., Dlabalová, B. et al. Universal screening detects two-times more thyroid disorders in early pregnancy than targeted high-risk case finding. Eur. J Endocrinol., 2010, 163, p. 645-650.
27. Negro, R., Soldin, O. P., Obregon, M. J., Stagnaro-Green, A. Hypothyroxinemia and pregnancy. Endocr. Pract. 2011a, 17, p. 422-429.
28. Bath, S. C., Rayman, M. P. Antenatal thyroid screening and childhood cognitive function New Engl. J Med., 2012, 366, 17, p. 1640-1.
29. Glinoer, D., Riahi, M., Grun, J. P., Kinthaert, J. Risk of subclinical hypothyroidism in pregnant women with asymptomatic autoimmune thyroid disorders. J Clin. Endocrinol. Metab., 1994, 79, p. 197–204.
30. Negro, R., Schwartz, A., Gismondi, R., Tinelli, A., Mangieri, T., Stagnaro-Green, A. Thyroid antibody positivity in the first trimester of pregnancy is associated with negative pregnancy outcomes. J Clin. Endocrinol. Metab., 2011b, 96, E920-E924.
31. Negro, R., Stagnaro-Green, A. Thyroid antibodies, preterm birth, and miscarriage. The association is clear, but the effects of levothyroxine treatment are uncertain. Brit. Med. J 2011c, 342, d2260.
32. Thangaratinam, S., Tan, A., Knox, E., Kilby, M. D., Franklyn, J., Coomarasamy, A. Association between thyroid autoantibodies and miscarriage and preterm birth: meta-analysis of evidence. Brit. Med. J, 2011, 342, d2616.
33. Dosiou, C., Barnes, J., Schwartz, A., Negro, R., Crapo, L., Stagnaro-Green, A. Cost-effectiveness of universal and risk-based screening for autoimmune thyroid disease in pregnant women. J Clin. Endocrinol. Metab., 2012, 97, p. 1536-1546.
34. Galofre, J. C., Haber, R. S., Mitchell, A. A., Pessah, R., Davies, T. F. Increased postpartum thyroxine replacement in Hashimoto’s thyroiditis. Thyroid, 2010, 20, p. 901-908.
35. Delange, F. Optimal iodine nutrition during pregnancy, lactation and the neonatal period. J Clin. Endocr. Metab., 2004, 2, p. 1-12.
36. Zimmermann, M., Delange, F. Iodine supplementation of pregnant women in Europe. A review and recomendation. Eur. J Clin. Nutr., 2004, 58, p. 979-84.
37. Zamrazil, V., Bílek, R., Čeřovská, J., Dvořáková, M., Němeček, J. Jodový deficit ve světě i v České republice - současný stav a perspektivy. Vnitř. Lék. 2010, 56(12), p. 1310-1315
38. Braverman, L. E., Utiger, R. D. Introduction to thyrotoxicosis., 2005 In: Braverman LE, Utiger RD (eds) Werner and Ingbar’s The Thyroid: A Fundamental and Clinical Text, 9th edition. Lippincott, Williams and Wilkins, Philadelphia, p. 453–455.
39. Patil-Sisodia, K., Mestman, J. H. Graves hyperthyroidism and pregnancy: a clinical update. Endocr. Pract., 2010, 16, p. 118–129.
40. Tan, J. Y., Loh, K. C., Yeo, G. S., Chee, Y. C. Transient hyperthyroidism of hyperemesis gravidarum. BJOG, 2002, 109, p. 683–688.
41. Niebyl, J. R. Clinical practice. Nausea an pregnancy. N. Engl. J. Med., 2010, 363, p. 1544–1550.
42. Russo, M. W., Galanko, J. A., Shrestha, R., Fried, M. W. Subclinical hyperthyroidism and pregnancy outcomes. Obstet. Gynecol., 2006, 107 (2 Pt 1), p. 337-341.
43. Clementi, M., Di Gianantonio, E., Pelo, E. et al. Methimazole embryopathy: delineation of the phenotype. Am. J Med. Genet., 1999, 83, p. 43–46.
44. Barbero, P., Valdez, R., Rodriguez, H. et al. Choanal atresia associated with maternal hyperthyroidism treated with methimazole: a case-control study. Am. J Med. Genet., 2008 A, 146A, p. 2390–2395.
45. Clementi, M., Di Gianantonio, E., Cassina, M. et al. Treatment of hyperthyroidism in pregnancy and birth defects. J Clin. Endocrinol. Metab., 2010, 95, E337–341.
46. Cassina, M., Dona, M., Di Gianantonio, E. et al. Pharmacologic treatment of hyperthyroidism during pregnancy. Birth Defects Res. Clin. Mol. teratol., 2012, 94, 8, p. 612-619.
47. Yoshira, A., Noh, J., Yamaguchi, T. et al. Treatment of Grave’s disease with antithyroid drugs in the first trimestr of pregnancy and the prevalence of congenital malformation. J Clin. Endocrinol. Metab., 2012, 97, 7, p. 2396-2403.
48. Rubin, P. C. Current concepts: beta-blockers in pregnancy. N. Engl. J Med., 1981 305, p. 1323–1326.
49. Stafford, I. P., Dildy, G. A. 3rd, Miller, J. M. Jr. Severe Graves‘ ophthalmopathy in pregnancy. Obstet. Gynecol., 2005 May,105 (5 Pt 2), p. 1221-1223.
50. Carmichael, S. L., Shaw, G. M., Ma, C., Werler, M. M., Rasmussen, S. A., Lammer, E. J. National Birth Defects Prevention Study. Maternal corticosteroid use and orofacial clefts. Am. J Obstet. Gynecol., 2007, 197(6), 585. e1–7, discussion 683–684, e1–7.
51. Lee, M., O’Brien, P. Pregnancy and multiple sclerosis. Journal of Neurology, Neurosurgery, and Psychiatry, 2008, 79, p. 1308–1311.
52. Nüssgens, Z., Roggenkämper, P., Schweikert, H. U. Development of endocrine orbitopathy in pregnancy. Klin. Monbl. Augenheilkd., 1993, Feb 202(2), p. 130-133.
53. Achiron, A., Kishner, I., Dolev, M., Stern, Y., Dulitzky, M., Schiff, E., Achiron, R. Effect of intravenous immunoglobulin treatment on pregnancy and postpartum-related relapses in multiple sclerosis. J Neurol., 2004, 251(9), p. 1133–1137.
54. Haas, J. High dose IVIG in the post partum period for prevention of exacerbations in MS. Mult. Scler., 2000, 6 Suppl 2, 18–20; discussion S33.
55. Negro, R., Mangieri, T., Coppola, L., Presicce, G., Casavola, E. C., Gismondi, R. Levothyroxine treatment in thyroid peroxidase antibody-positive women undergoing assisted reproduction technologies: a prospective study. Hum. Reprod., 2005, 20, p. 1529-33.
56. Jiskra, J., Bartáková, J., Holinka, S., Límanová, Z., Springer, D., Fait, T., Antošová, M., Telička, Z., Potluková, E. Low concordance between positive antibodies to thyroperoxidase and thyroid ultrasound autoimmune pattern in pregnant women. Endocr. J., 2011, Oct 29, 58(10), p. 849-59. Epub 2011 Aug 27.
57. Hartl, D. M., Travagli, J. P. The Updated American Thyroid Association Guidelines for Management of Thyroid Nodules and Differentiated thyroid cancer. A surgical perspective Thyroid, 2009, 19, 11, p. 1149-1151.
58. Struve, C. V., Haupt, S., Ohlen, S. Influence in frequency of previous pregnancies on the prevalence of thyroid nodules in women without clinical evidence of thyroid disease. Thyroid, 1993, 3, p. 7-9.
59. Kung, A. V., Chau, M. T., Lao, T. T. et al. The effect of pregnancy on thyroid nodule formation. J Clin. Endocrinol. Metab., 2002, 87, p. 1010-1014.
60. Hegedus, L., Bonnema, S. J., Bennedbaek, F. N. Management of simple nodular goiter: current status and future perspectives. Endocr. Rev., 2003, 24, p. 102–132.
61. Costante, G., Meringolo, D., Durante, C. et al. Predictive value of serum calcitonin levels for preoperative diagnosis of medullary thyroid carcinoma in a cohort of 5817 consecutive patients with thyroid nodules. J Clin. Endocrinol. Metab., 2007, 92, p. 450–455.
62. Tan, G. H., Gharib, H., Goellner, G. H. et al. Management of thyroid nodules in pregnancy. Arch. Intern. Med., 1996, 156, p. 122-125.
63. Marley, F., Oertel, Y. C. Fine needle aspiration of thyroid lesions in 57 pregnant and Postpartum women. Diagn. Cytopathol., 1997,16, p. 122-125.
64. Rosen, I. B., Walfish, P. G. Pregnancy as a predisposing factor in thyroid neoplasia. Arch. Surg., 1986, 121, p. 1287–1290.
65. Smith, L. H., Danielsen, B., Allen, M. E. et al. Cancer associated with obstetric delivery: results of linkage with the California cancer registry. Am. J Obstet. Gynecol., 2003, 189, p. 1128–1135.
66. Gibelli, B., Zamperini, P., Tradati, N. Pregnancy and thyroid cancer. Recent Results Cancer Res., 2008, 178, p. 123-136.
67. Hirsch, D., Levy, S., Tsvetov, G. et al. Impact of pregnancy on outcome and prognosis of survivors of papillary thyroid cancer. Thyroid, 2010, 20, p. 1179-1185.
68. Garsi, J. P., Schlumberger, M., Rubino, C. et al. Therapeutic administration of 1311 for differentiated thyroid cancer: radiation dose to ovaries and outcome of pregnancies. 2008 J Nucl. Med., 2008, 49, p. 845-852.
69. Sawka, A. M., Lakra, D. C., Lea, J. et al. A systematic review examining the effect of therapeutic radioactive iodine on ovarian function and future pregnancy in female thyroid cancer survivors. Clin. Endocrinol., (Oxf) 2008, 69, p. 479-490.
70. Pacini, F., Schlumberger, M., Dralle, H. et al. European Thyroid Cancer Taskforce 2006 European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium. Eur. J Endocrinol., 2006, 154, p. 787-803.
71. Lazarus, J. H. Thyroid screening in pregnancy. In: Lazarus, J. H., Pirags, V., Butz, S. The thyroid and reproduction. Merck European Thyroid Symposium, Georg Tieme Verlag, Stuttgart, 2008, p. 105-113.
72. Dosiou, C., Sanders, G. D., Araki, S. S., Crapo, L. M. Screening pregnant women for autoimmune thyroid disease: a cost-effectiveness analysis. Eur. J Endocrinol., 2008, Jun, 158(6), p. 841-51.
73. Thung, S. F., Funai, E. F., Grobman, W. A. The cost-effectiveness of universal screening in pregnancy for subclinical hypothyroidism. Am. J Obstet. Gynecol., 2009, Mar (3), 267.e1-7. Epub 2008 Dec 27.
74. Potlukova, E., Potluka, O., Jiskra, J., Limanova, Z., Telicka, Z., Bartakova, J., Springer, D. Is Age a Risk Factor for Hypothyroidism in Pregnancy? An Analysis of 5223 Pregnant Women. J Clin. Endocrinol. Metab., 2012, Mar 21, [Epub ahead of print]
75. Vaiyda, B., Anthony, S., Bilous, M. et al. Detection of thyroid dysfunction in early pregnancy: Universal screening or targeted high risk case finding? J Clin. Endocrinol. Metab., 2007, 92, p. 203–207.
76. Chang, D. L., Leung, A. M., Braverman, L. E. et al. Pearce EN. Thyroid testing during pregnancy at an academic Boston Area Medical Center. J Clin. Endocrinol. Metab. 2011, Sep, 96(9), E1452-6. Epub 2011 Jun 29.
77. Wang, W., Teng, W., Shan, Z., Wang, S., Li, J., Zhu, L., Zhou, J., Mao, J., Yu, X., Li, J., Chen, Y., Xue, H., Fan, C., Wang, H., Zhang, H., Li, C., Zhou, W., Gao, B., Shang, T., Zhou, J., Ding, B., Ma, Y., Wu, Y., Xu, H., Liu, W. The prevalence of thyroid disorders during early pregnancy in China: the benefits of universal screening in the first trimester of pregnancy. Eur. J Endocrinol., 2011, Feb, 164(2), p. 263-268. Epub 2010 Nov 8.
78. Jiskra, J., Bartáková, J., Holinka, Š., Límanová, Z., Springer, D., Antošová, M., Telička, Z., Potluková, E. Low prevalence of clinically high-risk women and pathological thyroid ultrasound among pregnant women positive in universal screening for thyroid disorders. Exp. Clin. Endocrinol. Diabetes., 2011 Oct, 119(9), p. 530-535. Epub 2011 Aug 2.
79. Auso, E., Lavado-Autric, R., Cuevas, E. et al. A moderate and transient deficiency of maternal thyroid function at the beginning of fetal neocorticogenesis alters neuronal migration. Endocrinology, 2004, 145, p. 4037-4044.
80. Telička, Z., Jiskra, J., Springer, D. Simple Method of Economical Analysis of Diagnosis Procedure (Used in Screening of Thyroid Gland Diseases in Pregnant Women) during the first trimester of pregnancy. European Journal for Biomedical Informatics, Prague 2010; online: http://ejbi.cz/articles/201012/59/1.html
Štítky
Biochémia Nukleárna medicína Nutričný terapeut
Článok vyšiel v časopiseKlinická biochemie a metabolismus
Najčítanejšie tento týždeň
2013 Číslo 1
-
Všetky články tohto čísla
- Význam a možnosti vyšetřování metabolismu mozku pomocí mikrodialýzy v neurointenzivní péči
- Stanovení sérových markerů v diferenciální diagnostice časného karcinomu prostaty (pilotní studie)
- Prevalence míry snížení glomelurální filtrace u pacientů s monoklonální gamapatií neurčeného významu
- Stanovení odhadu glomerulární filtrace eGFR - vývoj pokračuje
- Nové regulační hormony mateřského mléka
- Smuteční oznámení - Prof. Dr. Hermann Wisser
- Doporučení pro diagnostiku a léčbu onemocnění štítné žlázy v těhotenství a pro ženy s poruchou fertility
- Buněčnost likvoru, energetické poměry v likvorovém kompartmentu a intenzita zánětlivé odpovědi v centrálním nervovém systému
- Klinická biochemie a metabolismus
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Doporučení pro diagnostiku a léčbu onemocnění štítné žlázy v těhotenství a pro ženy s poruchou fertility
- Stanovení odhadu glomerulární filtrace eGFR - vývoj pokračuje
- Význam a možnosti vyšetřování metabolismu mozku pomocí mikrodialýzy v neurointenzivní péči
- Buněčnost likvoru, energetické poměry v likvorovém kompartmentu a intenzita zánětlivé odpovědi v centrálním nervovém systému
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



