-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Preserflo MicroShunt verzus trabekulektómia: klinické výsledky 6-mesačnej retrospektívnej štúdie
Clinical Outcomes of Preserflo MicroShunt versus Trabeculectomy: A Retrospective 6-Month Study
Objective: To characterize and compare the efficacy and safety of trabeculectomy and Preserflo microshunt (PMS) implantation in patients with openangle glaucoma. Material and Methods: This retrospective 6-month study included 100 eyes (100 patients). The 100 patients were divided into two groups of 50 patients, who were randomly assigned to either trabeculectomy or PMS implantation with mmC (0.4 mg/ml) applied using saturated sponges. The patients attended follow-up checks at 1, 8, 30, and 90 days postoperatively and at 6 months postoperatively. Endothelial cells were assessed at 3 and 6 months respectively. The main observed parameters were intraocular pressure (IOP), best corrected visual acuity (BCVA), anterior chamber depth (ACD), corneal hysteresis (CH), corneal endothelial cell density (CECD), coefficient of variation (CV), and antiglaucoma treatment. Results: In patients after trabeculectomy and after PMS implantation a comparable reduction in mean IOP values of 40.2% and 45.8% respectively was recorded for both surgical approaches in comparison with the preoperative mean IOP values. In all the studied patients, regardless of the type of surgical procedure, a significant reduction of CECD values was recorded 6 months after surgery. However, PMS implantation led to a greater reduction in antiglaucoma treatment postoperatively compared to trabeculectomy. Qualified success was almost identical in the case of both operations throughout the entire course, complete success was higher in favor of PMS at the beginning of the observation, but their values converged or met from approximately day 90 to month 6. Conclusion: The performed clinical evaluation of the efficacy and safety of PMS implantation compared to the classical surgical approach using trabeculectomy showed positive results related primarily to the reduction of postoperative complications, while maintaining the effectiveness of the surgical procedure. However, further clinical studies with a longer follow-up period are needed in order to provide long-term evidence of clinical efficacy.
Keywords:
trabeculectomy – glaucoma – Preserflo MicroShunt – antiglaucoma drugs
Autori: Nora Majtánová 1,2; Adriana Takáčová 1; Lucia Herdová 1; Veronika Kurilová 1,2; Juraj Majtán 3,4; Zlatica Fellner 1,2; Dalibor Cholevík 1,2; Petr Kolář 1,2
Pôsobisko autorov: Očná klinika Slovenskej zdravotníckej univerzity a Univerzitnej nemocnice Bratislava 1; Lekárska fakulta, Slovenská zdravotnícka univerzita, Bratislava 2; Ústav molekulárnej biológie, Slovenská akadémia vied, Bratislava 3; Ústav mikrobiológie, Lekárska fakulta, Slovenská zdravotnícka univerzita, Bratislava 4
Vyšlo v časopise: Čes. a slov. Oftal., 82, 2026, No. 2, p. 83-93
Kategória: Původní práce
doi: https://doi.org/10.31348/2025/35Súhrn
Cieľ: Charakterizovať a porovnať účinnosť a bezpečnosť trabekulektómie a implantácie Preserflo microshuntu (PMS) u pacientov s glaukómom s otvoreným uhlom. Materiál a metódy: Do retrospektívnej 6 mesačnej štúdie bolo zaradených 100 očí (100 pacientov). Z celkového počtu 100 pacientov boli pacienti prerozdelení do dvoch skupín po 50 pacientov, ktorí podstúpili trabekulektómiu alebo implantáciu PMS s mitomycínom C (MMC) (0,4 mg/ml) aplikovaným prostredníctvom nasiaknutých špongií. Pacienti boli sledovaní po 1., 8., 30. a 90. dni po operácii a 6. mesiaci po operácii. Endotelové bunky boli stanovené po 3, resp. 6 mesiacoch. Hlavné sledované parametre boli vnútroočný tlak (IOT), najlepšie korigovaná zraková ostrosť (BCVA), hĺbka prednej komory (ACD), rohovková hysteréza (CH), počet endotelových buniek rohovky (CECD), koeficient variability endotelových buniek (CV) a antiglaukomová liečba. Výsledky: U pacientov po trabekulektómii a po implantácii PMS bol pri oboch metódach zaznamenaný porovnateľný pokles priemerných hodnôt IOT o 40,2 %, resp. 45,8 % oproti predoperačným priemerným hodnotám IOT. U všetkých pacientov v súbore, bez ohľadu na typ operačného výkonu, bol zaznamenaný signifikantný pokles hodnôt CECD po 6 mesiacoch od operácie. Avšak implantácia PMS viedla k väčšiemu zníženiu antiglaukómovej liečby pooperačne oproti trabekulektómii. Kvalifikovaný úspech bol pri oboch operáciách takmer identický v celom priebehu, úplný úspech bol na začiatku pozorovania vyšší v prospech Preserflo Microshuntu, no ich hodnoty sa priblížili alebo stretli od približne 90. dňa po 6. mesiac. Záver: Prevedené klinické hodnotenie účinnosti a bezpečnosti implantácie PMS oproti klasickému operačnému prístupu pomocou trabekulektómie preukázalo pozitívne výsledky súvisiace predovšetkým s redukciou pooperačných komplikácií pri zachovaní účinnosti operačného výkonu. Na preukázanie dlhodobej klinickej účinnosti sú však potrebné ďalšie klinické štúdie s dlhším obdobím sledovania.
Klíčová slova:
glaukom – Preserflo MicroShunt – trabekulektómia – antiglaukomatíka
ÚVOD
Glaukóm je jedno z najčastejších ochorení vedúcich až k slepote [1]. Neliečené alebo nedostatočne liečené glaukómové ochorenie predstavuje celospoločenský problém, ktorý vedie k invalidizácii pacienta [2]. Veľký dôraz je preto nevyhnutné klásť nielen na správnu liečbu, ale aj na skorú detekciu glaukómového ochorenia. Operačné riešenie spolu s lokálnou a prípadne aj celkovou antiglaukómovou liečbou predchádza funkčným a štrukturálnym zmenám v zornom poli a na zrakovom nerve.
Hlavným cieľom antiglaukómovej liečby je zníženie a kontrola vnútroočného tlaku (IOT) za účelom zabránenia vzniku alebo zhoršovania poškodenia zrakového nervu a výpadom v zornom poli. Trabekulektómia ako hlavný predstaviteľ incíznej glaukómovej chirurgie je stále zlatým štandardom [3] a predstavuje optimálne riešenie u určitých skupín pacientov s glaukómom [4]. Spolu s operačnými technikami s drenážnými implantátmi však prináša vyššiu pravdepodobnosť vzniku komplikácií. Toto viedlo k vývoju nových operačných metód, ktorých cieľom bola obdobná úspešnosť v zmysle redukcie IOT pri nižšom riziku vzniku peri - a pooperačných komplikácií. Tieto postupy sa nazývajú minimálne invazívne (MIGS) alebo menej invazívne (LIGS) a využívajú fyziologické odtokové cesty vnútroočnej tekutiny [5]. Väčšinou však vyžadujú náročnejšie a drahšie technické vybavenie a zdĺhavejšie vyučenie personálu na rozdiel od trabekulektómie, ktorá je finančne výhodná a relatívne nenáročná čo sa týka operačného vybavenia [6], avšak niekedy omnoho ťažšia na správnu realizáciu a vyžaduje si skúsenosť chirurga.
Základným princípom MIGS výkonov je ab interno minimálne traumatizujúci mikroincízny prístup cez veľmi malú operačnú ranu, ktorá šetrí spojovku a skléru. V posledných rokoch bola vyvinutá široká škála implantátov MIGS, pričom ako nová kategória sa objavila minimálne invazívna chirurgia blebov (MIBS) [6]. Jedným z takýchto zariadení MIBS je PreserFlo MicroShunt (PMS), ktorý je vyrobený z termoplastického a elastomérneho biomateriálu (poly[styrén-blok-izobutylén-blok-styrén]) [7]. PMS je schválený a certifikovaný v Európe, ale zatiaľ nie je schválený americkým Úradom pre kontrolu potravín a liečiv.
PMS je ab-externo subkonjunktiválne zariadenie, ktoré je možné použiť ako náhradu trabekulektómie pri glaukómoch s otvoreným uhlom. Shunt má dĺžku 8,5 mm a na jeho tele sa nachádza rebro. Je umiestnené 4,5 mm od proximálneho hrotu skosenia microshuntu a má lúmen 70 µm. Je vyrobený z blokového kopolyméru styrénu a izobutylénu. Je flexibilný a vysoko biokompatibilný. PMS ponúka nový prístup k filtračnej operácii kombináciou minimálne invazívneho zariadenia s výrazným znížením IOT a vyžaduje starostlivú disekciu a umiestnenie tkaniva.
Nedávno vykonaná meta-analýza porovnávala PMS s trabekulektómiou u viac ako 1800 pacientov s nekontrolovaným glaukómom [8]. Meta-analýza ukázala, že trabekulektómia je účinnejšia u pacientov s nekontrolovaným glaukómom do 2 rokov, najmä ak sa zvažujú nižšie cieľové hodnoty IOT. Naviac, analýza uvádza vyššie riziko re-intervencie u PMS. Na druhej strane, iná nedávna meta-analýza [9] ukázala, že PMS vykazuje nižšiu mieru re-intervencie. Vzhľadom na tieto diskrepancie medzi vykonanými meta-analýzami, je potrebné vykonanie ďalších komparatívnych klinických štúdií. Preto cieľom predloženej retrospektívnej 6-mesačnej klinickej štúdii bolo charakterizovať účinnosť a bezpečnosť dvoch rôznych filtračných operačných prístupov: trabekulektómie a implantácie PMS s použitím mitomycínu C (MMC) aplikovaného pomocou špongie.
MATERIÁL A METÓDY
Nábor pacientov
Operačné výkony boli realizované na pracovisku Očnej kliniky SZU a UNB v Bratislave na súbore 100 pacientov (100 očí). Nábor a sledovanie pacientov indikovaných na operačný zákrok s trabekulektómiou prebiehalo od januára 2020 do mája 2022 a pacientov s implantovaným Preserflo microshuntom od júna 2022 do decembra 2023 na Očnej klinike SZU a UNB v Bratislave. Sledovanie bolo v súlade so zásadami Helsinskej deklarácie, pacienti boli riadne poučení a predoperačne podpísali informovaný súhlas. Pacientov sme vyberali podľa nasledujúcich inklúznych kritérií: glaukóm s otvoreným uhlom, nekontrolovaný IOT (viac ako 21 mmHg), zhoršovanie zorného poľa a/alebo štrukturálne zmeny na terči zrakového nervu, neabsolvovali žiaden predchádzajúci antiglaukómový operačný výkon, vek nad 20 rokov a bez alergie na mmC.
Pacienti, ktorí už absolvovali predchádzajúci antiglaukómový výkon, alebo im bola diagnostikovaná chronická alebo rekurentná uveitída, patologická myopia, neovaskularizácia dúhovky, neboli zaradení do štúdie. Neochota alebo neschopnosť súhlasiť s výkonom predstavovalo exklúzne kritérium. U jednotlivých pacientov sme vždy zahrnuli do štúdie len jedno oko. Pacienti mali glaukóm s otvoreným uhlom, a to buď primárny alebo sekundárny typ (pseudoexfoliatívny a pigmentový glaukóm).
Z celkového počtu 100 pacientov boli pacienti prerozdelení do dvoch skupín po 50 pacientov, ktorí podstúpili trabekulektómiu alebo implantáciu PMS. Pretože trabekulektómia predstavuje tradičný a zaužívaný operačný prístup, prvých 50 očí podstúpilo trabekulektómiu s MMC (0,4 mg/ml) aplikovaným prostredníctvom nasiaknutých špongií. Zvyšných 50 očí sa podrobilo implantácii PMS s MMC (0,4 mg/ml) aplikovaným prostredníctvom nasiaknutých špongií.
Všetci zahrnutí pacienti boli kaukazskej etnicity. Demografické charakteristiky, operované oko a typ glaukómu u pacientov z jednotlivých súborov sú zobrazené v Tabuľke 1.
Obr. 1. Demografické charakteristiky, operované oko a typ glaukómu u pacientov podľa zaradenia do jednotlivých terapeutických skupín 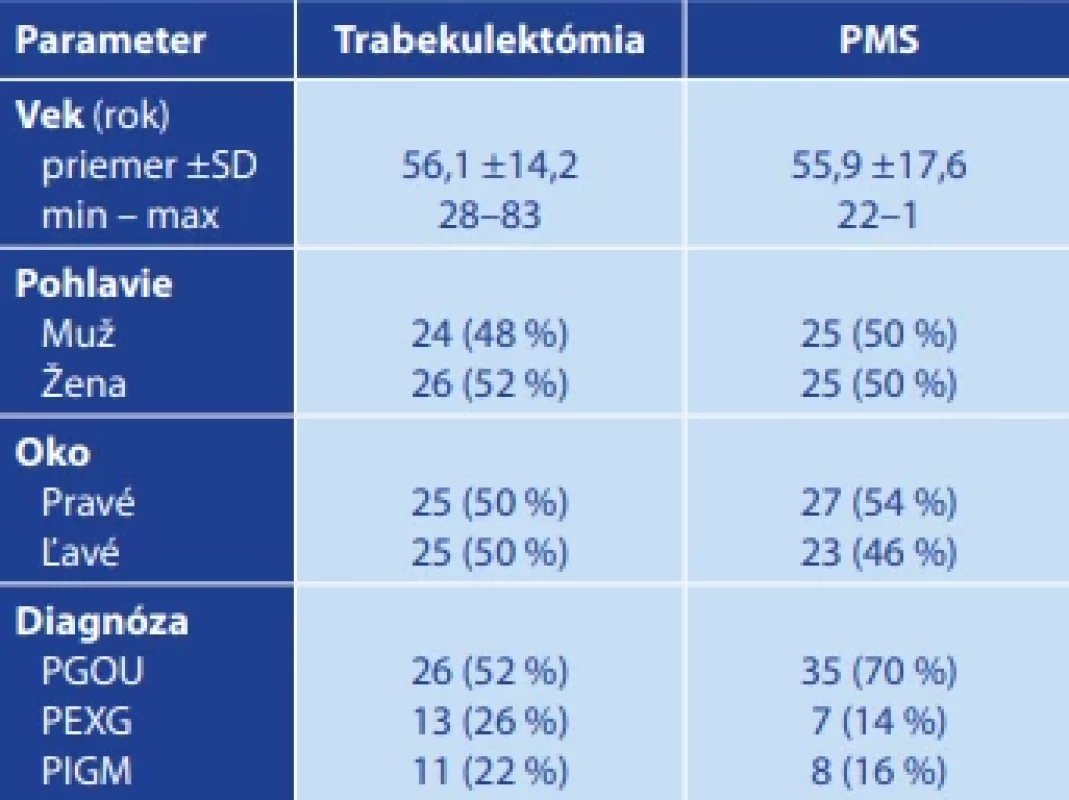
PGOU – primárny glaukóm s otvoreným uhlom, PEXG – pseudoexfoliatívny glaukóm, PIGM – pigmentový glaukóm, SD – smerodajná odchýlka Predoperačné vyšetrenie
Všetci pacienti zahrnutí do štúdie absolvovali kompletné očné vyšetrenie zahŕňajúce meranie IOT pomocou Goldmannovho aplanačného tonometra (Keeler Ltd, Windsor, UK) a korneálnu hysterézu pomocou prístroja Ocular Response Analyser (ORA, Reichert Inc., NZ, USA). Následne bolo vykonané vyšetrenie najlepšej korigovanej zrakovej ostrosti (BCVA) pomocou ETDRS optotypov, meranie hĺbky prednej komory (ACD) pomocou Casia2 (Tomey, Nemecko), počet a koeficient variability endotelových buniek (CECD a CV) pomocou nekontaktného spekulárneho mikroskopu Perseus (CSO, Taliansko). Meranie IOT a korneálna hysteréza (CH) boli realizované pred podaním lokálnej liečby a vždy v čase od 8 : 00 do 11 : 00, aby sa vylúčil vplyv diurnálnej fluktuácie IOT. Bol zaznamenaný aj počet antiglaukómových medikácií, ktoré pacienti užívali.
Dôležitými parametrami pre hodnotenie rizika straty endotelových buniek pri antiglaukomových operáciách s pouźitím implnatátu sú CECD a CV, ktorých hodnoty je nevyhnutné sledovať v čase a vyhnúť sa tak riziku endoteliálnej dekompenzácie. Hodnoty týchto parametrov sú vypočítavané automaticky pomocou špecifickeho softvéru, ktorý umožnuje zobrazenie endotelovej vrstvy rohovky s presnou špecifikáciou tvaru a veľkosti endotelových buniek. Pri komparatívnej analýze je možné porovnať stav endotelovej vrstvy rohovky pacienta s časovým odstupom. Časové horizonty v našom sledovaní boli 1, 3 a 6 mesiacov od operácie.
Operačný výkon
Trabekulektómia
Anestézia pri operačnom výkone bola celková alebo lokálna parabulbárna pomocou 2 ml 4% supracaínu, ktorý sa vyznačuje rýchlym nástupom účinku s efektom trvajúcim približne 45 minút od aplikácie. Anestézia bola aplikovaná v nazálnom hornom kvadrante orbity z dôvodu, aby bola zachovaná hybnosť bulbu smerom nadol a nemuseli sme použiť trakčný steh na rotáciu bulbu smerom nadol a uľahčenie prístupu k operačnému poľu.
Všetky operačné výkony boli vykonané jedným operatérom (NM). Na zvlhčovanie povrchu oka počas výkonu bol použitý izotonický fyziologický roztok, ktorý bol aplikovaný do injekčnej striekačky s tupou kanylou.
Po príprave a zarúškovaní oka sa vykonala limbálna konjunktiválna peritómia v hornom kvadrante a následne tupá disekcia Tenonskej kapsuly. Z dôvodu zabránenia možného krvácania a nutnosti hemostázy počas operačného výkonu sa episklerálne vény skoagulovali pomocou bipolárnej diatermie. Pomocou plytkých incízií bol označený korneosklerálny lalok, ohraničujúc tak tri strany 5 mm štvorca s voľnými ukončeniami pokračujúcimi radiálne od limbu. Na ohraničené miesto bol aplikovaný mmC (0,4 mg/ml) aplikovaný prostredníctvom nasiaknutých špongií po dobu 2 minút, ktoré nasledovalo výplachom prúdom Ringerovho roztoku. Pomocou kreščendového noža sa preparoval korneosklerálny lalok s hrúbkou 2/3 skléry, nasledovala excízia časti trámčiny a Schlemmovho kanála, a tým vzniklo vytnutie trabekulárneho okienka pod sklerálnym lalokom. Do prednej komory pod sklerálny lalok sme prenikli pomocou preparácie 30° nožom.
Periférna iridektómia bola realizovaná pomocou Vannasových nožníc. Nasledovala sutura sklerálneho laloka dvomi 10-0 nylonovými jednotlivými stehmi na okrajové časti štvorca vytvoreného laloka. Spojovka bola suturovaná 10-0 nylonovým pokračujúcim stehom smerom k limbu, aby rana bola hermeticky uzatvorená, čo bolo potvrdené v závere kontrolou tesnosti uzáveru operačnej rany.
Implantácia Preserflo microshuntu
Drenážna operácia pomocou implantátu Preserflo bola zavedená do praxe so snahou vyvinúť operačný postup, ktorý by bol bezpečnejší ako trabekulektómia a súčasne by dosahoval podobný hypotonizujúci efekt.
Po štandardnej príprave operačného poľa sa odpreparovala spojovka pri limbe a tupou disekciou sa vytvoril dostatočne široký a hlboký priestor pre následné miesto implantácie. Hemostáza bola uskutočnená podľa štandardných postupov.
Ideálna poloha na implantáciu je v superotemporálnom alebo superonazálnom kvadrante. Na prevenciu jazvenia sa aplikovali špongie s MMC (0,4 mg/ml) na 2 min na sklerálne lôžko za plánovaným miestom zavedenia implantátu. Po vybratí špongií bol nevyhnutný výplach daného miesta, ako aj okolitých tkanív väčším množstvom vyváženého soľného roztoku. Miesto plánovanej incízie sa označil s použitím 3 mm markeru vo vzdialenosti 3 mm za limbom a následne s využitím 1 mm zahnutého noža sa vytvoril plytký 2 mm sklerálny tunel paralelne so sklérou bez vstupu do prednej komory. Vstup do prednej komory sa vytvoril pomocou 25G zahnutej ihly, kde pri vstupe do prednej komory sa menil smer vstupu na úrovnitrámčiny, a to do paralelného smeru s dúhovkou.
Koniec ihly bol zreteľne viditeľný v prednej komore. Implantát sa vložil pomocou uzliacich pinziet s otvorom nahor, s krídelkami zanorenými v sklerálnom tuneli a lúmenom viditeľným v prednej komore. Implantát sa posúval novovytvoreným kanálom smerom do prednej komory a dbalo sa na to, aby sa proximálny hrot udržal v skosenej polohe. Miernym tlakom na rohovku sa skontrolovala účinnosť filtrácie. Ak sa nepotvrdíla filtrácia, je nutný preplach implantátu kanylou. Na našom pracovisku sa to realizuje pomocou aplikácie intrakamerálnych antibiotík cefuroxim v dávke 0,1 ml do prednej komory. Pokiaľ je poloha implantátu správna, čiže 2–3 mm proximálneho konca implantátu sa nachádza v strednej časti hĺbky prednej komory, bez dotyku s endotelom alebo dúhovkou, bez obštrukcie, odtok komorovej tekutiny musí byť verifikovaný. Na záver sa spojovku saturovala pomocou 10-0 nylonového pokračujúceho stehu, pričom distálny lúmen implantátu sa nachádzal voľne v subtenonskom priestore paralelne so sklérou s obmedzením možnej obštrukcie distálneho konca implantátu. Tenonská fascia mohla byť suturovaná aj samostatne. Následne sa skontrolovala tesnosť operačnej rany. Nad implantátom sa po suture rany začal formovať filtračný vankúšik.
Aplikácia mmC
Aplikácia mmC pomocou špongie predstavuje štandardný a najčastejšie používaný spôsob aplikácie mmC. V súbore pacientov v tejto štúdii bolo perioperačné podanie riedeného roztoku mmC v koncentrácii 0,4 mg/ml na špongii s dobou expozície 2 minúty a následným oplachovaním fyziologickým roztokom v množstve aspoň 20 ml. V prípade aplikácie mmC pri trabekulektómii sa špongia aplikovala priamo na miesto budúceho sklerálneho laloka ešte pred jeho vytvorením. Naopak, pri implantácii Preserflo microshuntu bola špongia s MMC aplikovaná do subtenonského priestoru v mieste vytvorenej kapsy za plánovanou implantáciou Preserflo microshuntu.
Pooperačný manažment pacienta
Všetci pacienti mali pooperačne podávané lokálne antibiotikum 0,5% levofloxacín a lokálny kortikosteroid 1% prednizolón acetát vo frekvencii 5-krát denne. Pacienti boli sledovaní po 1., 8., 30. a 90. dni po operácii a 6. mesiaci po operácii. Endotelové bunky boli stanovené po 3, resp. 6 mesiacoch.
V rámci hodnotenia úspešnosti operačného riešenia bol sledovaný aj tzv. „úplný úspech“, kedy bol IOT pooperačne 21 mmHg alebo menej s redukciou jeho hodnoty o aspoň 20% oproti jeho pôvodnej hodnote bez použitia akejkoľvek antiglaukómovej liečby a bez nutnosti ďalšej antiglaukómovej operácie. „Kvalifikovaný úspech“ bol definovaný podobne ako úplný úspech, ale bez potreby navýšenia antiglaukómovej liečby v porovnaní s obdobím pred operáciou a bez potreby ďalšej antiglaukómovej chirurgie. Ako „kompletné zlyhanie“ sme si stanovili stav, keď bola potrebná ďalšia antiglaukómová chirurgia (okrem revíznych výkonov).
Štatistická analýza
Štatistická analýza prebiehala v programovacom jazyku Python a vizualizácia štatistických výsledkov pomocou programu Microsoft Excel a GraphPad Prism. Na stanovenie distribúcie dát bol použitý Shapirov-Wilkov test normality. Pre normálne distribuované dáta bol použitý t-test a na dáta bez normálnej distribúcie párový Wilcoxonov test. Pri hodnotení dát sa hodnota P menšia ako 0,05 považovala za štatisticky signifikantnú. Na hodnotenie úspešnosti operácií sa použila Kaplan-Meierova analýza. Na vyhodnotenie testov pre korelačný koeficient bola použitá Fisherova Z premenná a metóda založená na t-premennej za predpokladu, že korelácia je rovná nule.
VÝSLEDKY
Trabekulektómia s aplikáciou antimetabolitu mmC pomocou špongie patrí medzi klasickú a najčastejšiu formu operačného výkonu u pacientov s glaukómom. Priemerná hodnota IOT predoperačne v súbore 50 pacientov bola 33,1 ±6,7 mmHg, pričom hodnoty boli v rozmedzí od 24 do 51 mmHg. Prvý pooperačný deň bola priemerná hodnota IOT 11,1 ±3,6 mmHg, 8. deň 15,2 ±3,3, na 90. deň 19.0 ±3,2 a po 6. mesiacoch 19,8 ±2,4 mmHg (pokles o 40 %) (Graf 1A). V závislosti od jednotlivých typov glaukómu, najväčší pokles hodnôt IOT zaznamenaný u PEX glaukómu, nasledovaný PGOU a pigmentovým glaukómom, ale bez štatisticky významných zmien.
Graf 1. Kaplan-Meierova analýza prežitia úplnej alebo kvalifikovanej úspešnosti kontroly IOT u pacientov po trabekulektómii s aplikovaním mmC pomocou špongie u pacientov po (A) trabekulektómii alebo po (B) implantácii Preserflo microshuntu IOT – vnútroočný tlak, mmC – mitomycín C 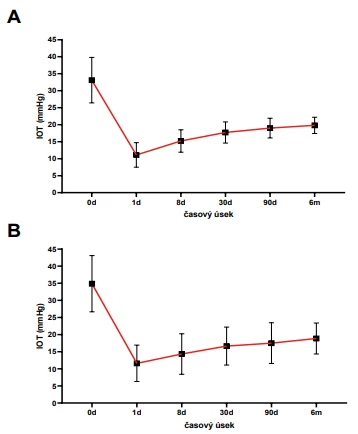
Obvyklý spôsob aplikácie mmC podobne ako pri trabekulektómii je pomocou špongie. V našom súbore pacientov bola priemerná hodnota predoperačného IOT 34,9 ±8,2 mmHg, prvý deň po operácii bola 11,6 ±5,3 mmHg a po 30 dňoch bola priemerná hodnota IOT 16,6 ±5,6 mmHg. Po 3 mesiacoch od operácie bola priemerná hodnota IOT 17,5 ±5,9 a po 6 mesiacoch po operácii bola priemerná hodnota IOT 18,9 ±4,5 mmHg. Pokles priemerných pooperačných hodnôt IOT bol štatisticky signifikantný voči predoperačnej priemernej hodnote IOT (Graf 1B).
Úspešná kontrola IOT bola definovaná ako dosiahnutie IOT ≤ 21 mmHg bez antiglaukómových medikamentov (úplný úspech) alebo so znížením počtu lokálnych antiglaukomatík (kvalifikovaný úspech). Miera úspešnosti bola stanovená pomocou Kaplanovej-Meierovej krivky prežitia a to u pacientov po trabekulektómii (Graf 2A) a po implantácii Preserflo microshunut (Graf 2B).
Graf 2. 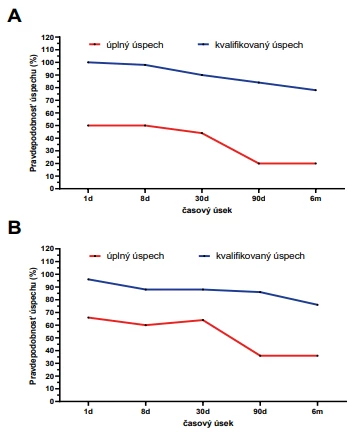
Kaplan-Meierova analýza prežitia úplnej alebo kvalifikovanej úspešnosti kontroly IOT u pacientov po trabekulektómii s aplikovaním mmC pomocou špongie u pacientov po (A) trabekulektómii alebo po (B) implantácii Preserflo microshuntu IOT – vnútroočný tlak, mmC – mitomycín C Okrem stanovenia hodnôt IOT boli u pacientov po trabekulektómii sledované aj vybrané parametre po 6-tich mesiacoch od operačného výkonu, ktoré sú uvedené v Tabuľke 2.
Tab. 1. Vybrané charakteristiky u pacientov predoperačne a po trabekulektómii s aplikáciou mitomycínu C pomocou špongie po 6 mesiacoch od operácie 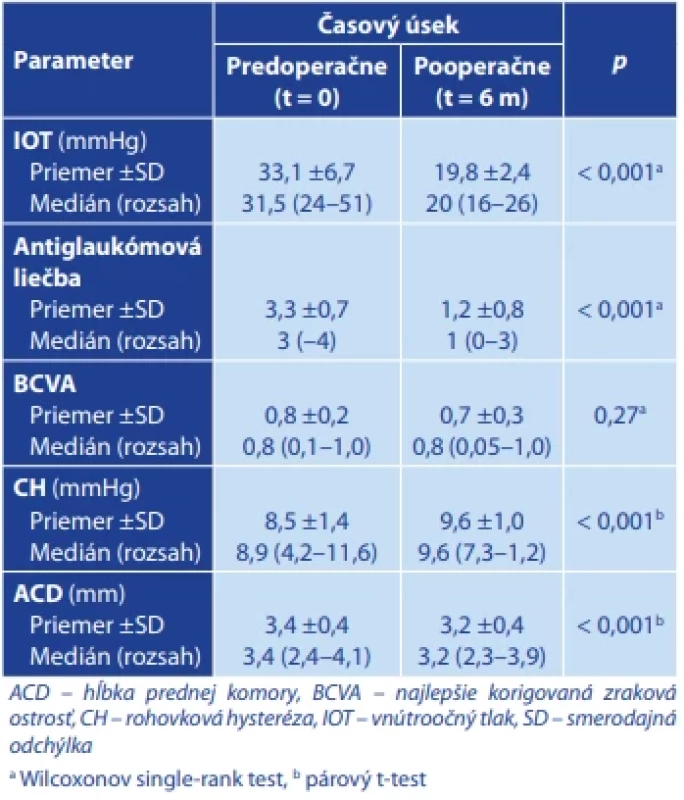
Počet antiglaukómových liekov sa u pacientov znížil z 3,3 ±0,7 na 1,2 ±0,8 po 6-tich mesiacoch po operácii. Priemerné hodnoty sledovaného parametra BCVA nepreukazovali štatisticky významné rozdiely, kde z predoperačnej priemernej hodnoty 0,8 sa BCVA zmenilo na hodnou 0,7. Hodnota CH v sledovanom súbore pacientov štatisticky významne narástla z priemernej hodnoty 8,5 ±1,4 mmHg na 9,6 ±1,0 mmHg po 6-tich mesiacoch po operácii, čo predstavuje nárast o 10,8 %. Priemerná hodnota ACD štatisticky signifikantne poklesla z hodnoty 3,4 ±0,4 mm na hodnotu 3,2 ±0,4 mm, čo predstavuje pokles o 0,10 mm.
U pacientov po implantácii Preserflo microshuntu, nárast hodnôt CH (približne o 25 %), ako aj zníženie antiglaukómovej liečby boli pooperačne štatisticky významné (Tabuľka 3). V prípade antiglaukómovej liečby boli predoperačne priemerné hodnoty 3,6 ±0,6 znížené na 0,9 ±0,9 po 3 aj 6 mesiacoch. Pooperačne nepotrebovalo žiadnu lokálnu antiglaukómovú liečbu až 66 % pacientov a u 38 % pacientov nebola potrebná liečba ani 6 mesiacov po operácii. Pooperačne nenastala v hodnotách BCVA žiadna signifikantná zmena v porovnaní so stavom pred operáciou, pričom predoperačné hodnoty boli priemerne 0,66, pooperačné 0,72. Nenastala ani žiadna signifikantná zmena v hĺbke prednej komory pooperačne (Tabuľka. 3).
Tab. 2. Vybrané charakteristiky u pacientov predoperačne a po implantácii Preserflo microshuntu s aplikáciou minomycínu C pomocou špongie po 6 mesiacoch od operácie 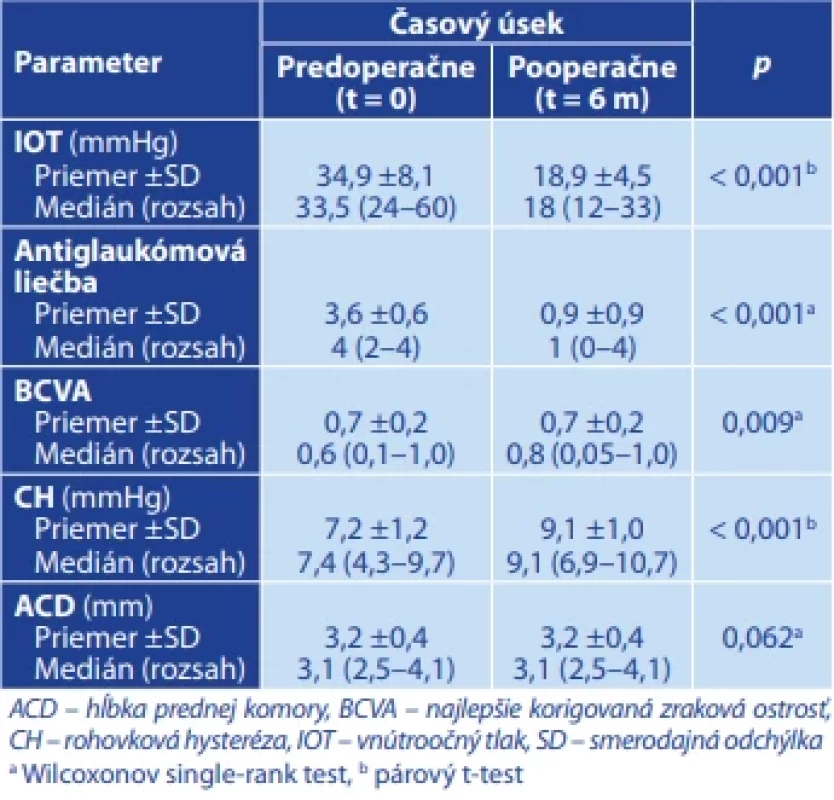
Čo sa týka typov glaukómu s otvoreným uhlom, najväčšia účinnosť bola dosiahnutá pri pigmentovom glaukóme (pokles o 58 %), nasledoval PGOU (pokles o 45 %) a potom PEX glaukóm (pokles o 33 %).
Ako každý chirurgický zákrok zahŕňajúci predný segment, má trabekulektómia potenciál spôsobiť poškodenie rohovky a je spojená so zrýchleným poklesom hustoty endotelových buniek rohovky (CECD). U všetkých pacientov v súbore sme zaznamenali signifikantný pokles hodnôt CECD, a to z pôvodnej hodnoty 2338,1 ±554 na 2185,4 ±546,8 (pokles o 6,54 %) po 6 mesiacoch od operačného zákroku. Najväčší pokles CECD hodnoty po 6 mesiacoch od operácii bol zaznamenaný u PEX glaukómu (o 8,4 %), nasledovaný PGOU glaukómom (o 6,3 %) a PIGM glaukómom (o 5,4 %). Štatisticky významný nárast koeficientu variability endotelových buniek (CV) z 25,7 ±3,3 na 26,6 ±3,5 po 6 mesiacoch po operácii (Tabuľka 4).
Tab. 3. Porovnanie predoperačných a pooperačných hodnôt CECD a CV u pacientov po trabekulektómii s aplikovaním mitomycínu C pomocou špongie s ohľadom na typ glaukómu 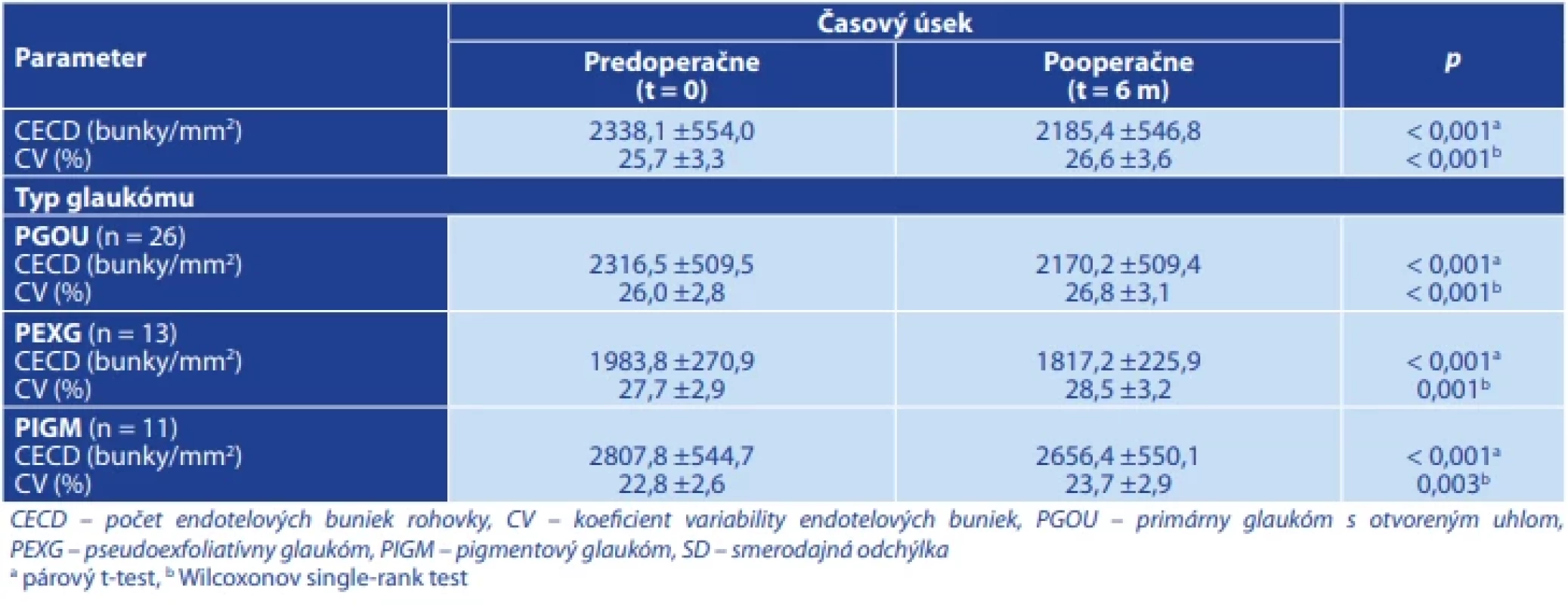
Pokles endotelových buniek pooperačne u pacientov po implantácii Preserflo microshuntu bol signifikantný u všetkých typov glaukómu, pol roka po operácii poklesol počet o približne 6,8 % pri primárnom glaukóme s otvoreným uhlom, o 9,6 % pri pseudoexfoliatívnom glaukóme a 8,7 pri pigmentovom. Najväčší pokles sme pozorovali pri pseudoexfoliatívnom glaukóme (Tabuľka 5).
Tab. 4. Porovnanie predoperačných a pooperačných hodnôt CECD a CV u pacientov po implantácii Preserflo microshuntu s aplikovaním mitomycínu C pomocou špongie s ohľadom na typ glaukómu 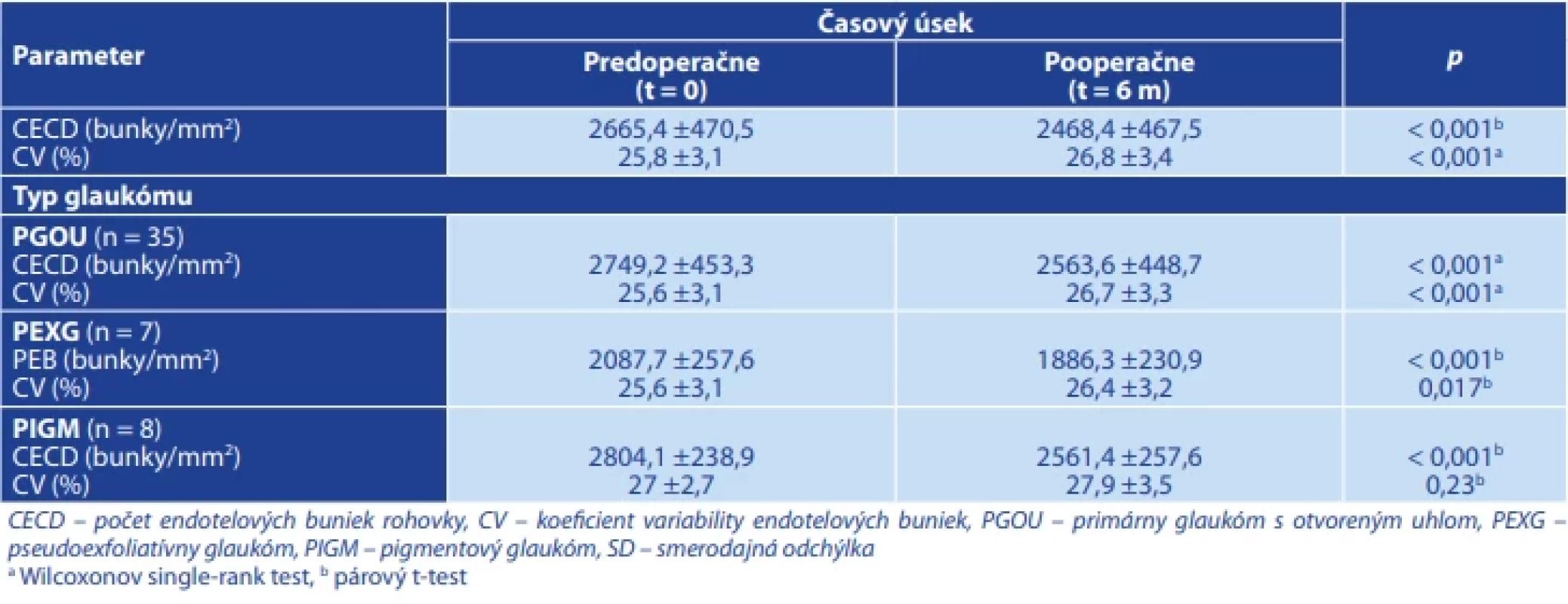
Z pooperačných komplikácií v súbore pacientov sme zaznamenali pooperačnú hypotenziu u 24 pacientov (48 %), splytčenie prednej komory aspoň o 1 mm u 15 pacientov (30 %), ablácie chorioidey u 17 pacientov (34 %) a hyfému u 13 pacientov (26 %). Z neskorých pooperačných komplikácií (po prvom mesiaci) sme zaznamenali roztvorenie operačnej rany u 4 pacientov (8 %) a zlyhanie filtrácie u 4 pacientov (8 %). Graf 3A.
Komplikácie po implantácii Preserflo microshuntu sú uvedené v Grafe 3B. Hypotenzia sa vyskytla u 12 % pacientov, hyféma v 10 % a u 8 % pacientov bola potrebná reoperácia (4 pacienti). U dvoch z týchto 4 pacientov bola prevedená revízia s MMC, po ktorej nastalo obnovenie filtrácie, u jedného pacienta bola potrebná cyklofotokoagulácia a u posledného implantácia druhého implantátu Preserflo microshunt. Výraznejšie krvácanie sa vyskytlo u pacienta s hematologickým ochorením, kde sa počas hospitalizácie sa podarilo krvácanie úspešne zvládnuť.
Graf 3. 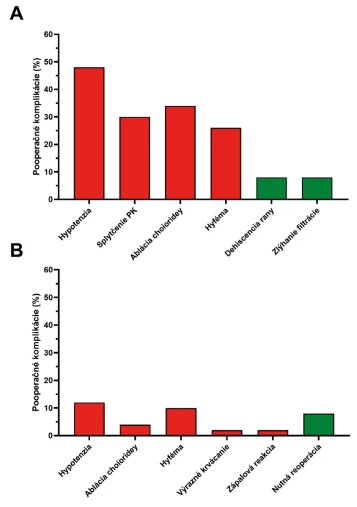
Výskyt pooperačných komplikácií u pacientov po (A) trabekulektómii alebo (B) implantácii Preserflo microshuntu s aplikovaním mmC pomocou špongie. Skoré komplikácie (do jedného mesiaca) sú označené červenou farbou, neskoré (viac ako jeden mesiac) zelenou farbou MMC – mitomycín C DISKUSIA
Hlavným cieľom antiglaukómovej liečby je zníženie a kontrola IOT za účelom zabránenia vzniku alebo zhoršovania poškodenia zrakového nervu a výpadom v zornom poli. Trabekulektómia ako hlavný predstaviteľ incíznej glaukómovej chirurgie je stále zlatým štandardom [3] a predstavuje optimálne riešenie u určitých skupín pacientov s glaukómom [4]. Spolu s operačnými technikami s drenážnymi implantátmi však prináša vyššiu pravdepodobnosť vzniku komplikácií. Toto viedlo k vývoju nových operačných metód, ktorých cieľom bola obdobná úspešnosť v zmysle redukcie IOT pri nižšom riziku vzniku peria pooperačných komplikácií. Tieto postupy sa nazývajú minimálne invazívne (MIGS) alebo menej invazívne (LIGS) a využívajú fyziologické odtokové cesty vnútroočnej tekutiny [5]. Väčšinou však vyžadujú náročnejšie a drahšie technické vybavenie a zdĺhavejšie vyučenie personálu na rozdiel od trabekulektómie, ktorá je finančne výhodná a relatívne nenáročná čo sa týka operačného vybavenia [6], avšak niekedy omnoho ťažšia na správnu realizáciu a vyžaduje si skúsenosť chirurga.
Napriek tomu musíme typ operácie voliť individuálne s ohľadom na pacienta a jeho cieľový IOT, povrch oka a stav spojovky. V roku 1968 Cairns predstavil trabekulektómiu, ktorá je odvtedy s úspechom využívaná [10]. Princípom je vytvorenie malej fistuly na rozhraní rohovky a skléry, ktorá sa prikryje sklerálnym lalokom čiastočnej hrúbky. Sklerálny lalok tvorí odpor odtoku vnútroočnej tekutiny. Vnútroočná tekutina je pomocou fistuly drénovaná do subtenonského priestoru, čím sa vytvorí filtračný vankúšik. Tekutina sa ďalej drenuje do obehu episklerálnymi a spojovkovými cievami. Sklerálny lalok kladie odpor, a tak vieme schopnosť odtoku vnútroočnej tekutiny regulovať pomocou upraviteľných stehov na ňom umiestnených [11]. To, ako sa vytvorí podspojovková jazva na mieste filtračného vankúšika a ako sa rana hojí, ovplyvní úspešnosť trabekulektómie [12].
Dôležitou a vážnou komplikáciou trabekulektómie je jej zlyhanie. Na zníženie rizika zlyhania a zvýšenie úspešnosti sú používané antifibrotické látky, ako je mmC a 5-fluorouracil (5-FU) [13–15]. mmC pre svoj antiproliferatívny účinok zabraňuje fibróze filtračného vankúšika a znižuje tak riziko zlyhania filtrácie [16]. Ak je použitý mmC, redukcia IOT je pozorovaná aj 5 rokov po operácii [17]. Riziká jeho použitia sú však početné, častejšie sa vyskytuje hyféma, avaskularita filtračného vankúšika, pooperačná hypotónia, ablácia chorioidey, splytčovanie prednej komory, zlyhanie filtrácie alebo hyperfiltrácia operačnej rany, prípadne môže vzniknúť až endoftalmitída [18]. V rámci týchto rizík stále nie je jednoznačný konsenzus akou metódou, v akých koncentráciách a s akou dĺžkou expozície je vhodné túto antifibrotickú látku perioperačne používať. Závery jednotlivých autorov sa líšia s ohľadom na úspešnosť a bezpečnosť aplikácie [19]. S ohľadom na koncentráciu mmC pri operačných výkonoch sa závery jednotlivých klinických štúdií líšia a nie je jasne zodpovedané, či existuje signifikantný rozdiel v úspešnosti a bezpečnosti operácie v prípade použitia koncentrácie mmC 0,2 mg/ml a 0,4 mg/ml [19]. Kitazawa a kol. vo svojej štúdii porovnávali koncentrácie mmC 0,2 mg/ml a 0,02 mg/ml s 5-minútovou expozíciou, kde autori naznačujú, že optimálna koncentrácia by mala byť niekde v rozmedzí oboch testovaných koncentrácií [20]. Niektorí autori deklarujú vyššiu úspešnosť a nižší IOT v prípade použitia vyšších koncentrácií mmC [19,21].
Najčastejší spôsob použitia mmC počas trabekulektómie je pomocou nasiaknutej špongie aplikovanej priamo na obnaženú skléru. Vo Veľkej Británii, ale aj v iných krajinách sveta, je preferencia tohto spôsobu až u 94 % chirurgov [22]. Záleží aj na veľkosti a tvare špongie, pričom pri veľkých a nepravidelných špongiách a ich nesprávnom umiestnení hrozí väčšie riziko vzniku komplikácie, ako je hypotónia, presakovanie a zápal filtračného vankúšika, prípadne zjazvenie spôsobené expozíciou mmC [23]. Väčšia oblasť pôsobenia špongie môže spôsobiť traumatizáciu spojovky so sťažením ďalšej operácie na tom istom mieste [24]. Zhang a kol. prezentovali metódu s použitím špongie 3,5 x 10 mm, ktorú umiestňujú vertikálne a dozadu s dlhou stranou do spojovkového lôžka pod sklerálny lalok bez toho, aby došlo ku kontaktu incízie rohovky [23]. Takáto aplikácia by mala byť pre spojovku minimálne traumatizujúca a redukuje komplikácie súvisiace s filtračným vankúšikom, pretože ten smeruje viac dozadu a je difúznejší. Koncentráciu mmC a čas expozície však ponechávajú autori na operatérovi.
V literatúre boli popísané prípady straty špongie s jej zabudnutím v operačnom poli, poškodenie spojovky a nemožnosť ošetrenia veľkej plochy skléry [25].
V našej práci sme porovnali súbory pacientov s glaukómom s otvoreným uhlom, v rámci ktorého boli pacienti operovaní s odlišnými operačnými technikami, a to tradičnou filtračnou operáciou – trabekulektómiou a menej invazívnou technikou formujúcou vankúšik – implantáciou Preserflo microshuntu. V oboch operačných prístupoch bola použitá anitproliferatívna látka mmC, ktorá sa aplikovala pomocou špongie. Pacienti mali diagnostikovaný glaukóm s otvoreným uhlom, a to buď PGOU, PEX alebo pigmentový glaukóm.
U všetkých pacientov bez ohľadu na typ operačného výkonu nastal pooperačne významný pokles hodnôt IOT.
Typ operačného výkonu – implantácia Preserflo microshuntu je vhodný na použitie pri primárnom glaukóme s otvoreným uhlom [26], podobné výsledky boli preukázané aj pri PEX glaukóme [27]. Navyše sa skúma aj jeho účinnosť pri iných sekundárnych glaukómoch ako je PEX a pigmentový glaukóm alebo pri refraktérnom uveitickom glaukóme, kde tiež preukázal priaznivú účinnosť [28], ktorá ale nedosahuje takú úspešnosť ako pri PGOU, PEX a pigmentovom glaukóme. Pri sekundárnych glaukómoch je po jeho implantácii vyššie riziko nutných operačných revízií [29]. Dôležitý je stav spojovky pred operáciou, ktorý následne ovplyvní priebeh hojenia a funkčnosť implantátu. Storp a kol. sledovali úspešnosť microshuntu na rôzne typy glaukómu, pričom najnižšia bola sledovaná pri sekundárnych glaukómoch, kde bol aj najvyšší počet nutných revíznych operácií [29]. Z týchto príčin sme do nášho sledovaného súboru zaradili zatiaľ len tri typy glaukómov s otvoreným uhlom – primárny glaukóm s otvoreným uhlom, zo sekundárnych glaukómov s otvoreným uhlom PEX a pigmentový glaukóm.
Preserflo microshunt je ab-externo subkonjunktiválne zariadenie, ktoré je možné použiť ako náhradu trabekulektómie pri glaukómoch s otvoreným uhlom. Je vyrobený z blokového kopolyméru styrénu a izobutylénu, je flexibilný a vysoko biokompatibilný. Tento materiál sa v minulosti využíval pri srdcových stentoch. Obmedzenie prietoku je založené na Haubsen-Poiseuillovej rovnici. Podľa nej by mal byť pre rýchlosti prúdenia 2,5 μl/min shunt schopný udržať tlak okolo 6,5 mmHg. Daný shunt vykazuje dobrú pooperačnú hypotenznú účinnosť a bezpečnosť. Ab-externo prístup umožňuje kontrolu hemostázy, presné umiestnenie a presné overenie prietoku [30].
Gubser a kol. (2023) sa vo svojej nedávnej štúdii zamerali na porovnanie strednodobej účinnosti implantácie Preserflo microshuntu s trabekulektómiou u pacientov s primárnym glaukómom s otvoreným uhlom so zameraním na zmeny funkčných a štrukturálnych parametrov [31]. Autori zistili, že primeranú hodnotu IOT a počet liekov na zníženie IOT možno znížiť implantáciou Preserflo microshuntu, a to s porovnateľnou účinnosťou ako trabekulektómia počas 2-ročného sledovania. Táto štúdia tiež ukázala, že štrukturálne glaukómové poškodenie môže pokračovať, zatiaľ čo funkčné glaukómové poškodenie zostáva po operácii glaukómu stabilné. Implantácia Preserflo microshuntu preukázala potenciál stabilizovať funkčné a štrukturálne glaukómové poškodenie.
Nedávno vykonaná multi-centrická kohortová štúdia preukázala, že vyššia intraoperačná koncentrácia mmC bola spojená so zníženým rizikom zlyhania (0,4 mg/ml oproti 0,2 mg/ml mmC) [32].
Aj keď je Preserflo microshunt zariadenie indikované pre pacientov so skorým až pokročilým primárnym glaukómom s otvoreným uhlom refrakterným na medikamentóznu terapiu, môže zohrávať úlohu aj pri liečbe iných typov glaukómu, a to aj v detskom veku [33].
Skúsenosti so zavedením Preserflo microshuntu na nové klinické pracoviská v Londýne dokázali, že Preserflo microshunt je bezpečné, klinicky účinné a náklady šetriace zariadenie. Skrátenie chirurgického času, pooperačné komplikácie a počet kontrolných návštev spôsobili, že použitie Preserflo microshuntu bolo priaznivé pre primárnu filtračnú chirurgiu primárneho glaukómu s otvoreným uhlom, ako aj pre prípady refraktérneho glaukómu, ktoré už predtým prekonali neúspešnú operáciu [34].
Pri porovnaní pacientov po trabekulektómii a po implantácii Preserflo microshuntu bol pri oboch metódach zaznamenaný porovnateľný pokles priemerných hodnôt IOT, ale existuje rozdiel medzi poklesom antiglaukómovej liečby po 6 mesiacoch v porovnaní s počtom liečby predoperačne, a to v prospech implantácie Preserflo microshuntu. Implantácia Preserflo microshuntu teda viedla k vyššej redukcii antiglaukómovej liečby pooperačne. Kvalifikovaný úspech bol pri oboch operáciách takmer identický v celom priebehu, úplný úspech bol na začiatku pozorovania vyšší v prospech Preserflo, no ich hodnoty sa priblížili alebo stretli od približne 90. dňa po 6. mesiac.
Podľa štúdie autorov Pillunat a kol. bolo zníženie IOT po 6 mesiacoch po oboch typoch operácií podobné, avšak pri trabekulektómii bolo signifikantne vyššie percento pooperačných intervencií [30]. Iné štúdie uvádzajú lepšie výsledky úspešnosti v zmysle hodnôt IOT a redukcie lokálnej liečby pri trabekulektómii po prvom roku od operácie, no potvrdzujú signifikantne menej komplikácií pri implantácii Preserflo microshuntu [35]. Čo sa týka výskytu komplikácií, signifikantne nižšie množstvo komplikácií po implantácii Preserflo microshuntu v porovnaní s trabekulektómiou bolo zaznamenané aj v našej práci. Po trabekulektómii sa vyskytla pooperačná hypotenzia u 48 % pacientov. Ďalej nasledovalo splytšenie prednej komory o aspoň 1 mm v 30 %, ablácie chorioidey v 34 % a hyféma v 26 %. Skupiny pacientov po implantácii Preserflo microshuntu mali signifikantne lepší bezpečnostný profil, v skupine pacientov s MMC aplikovanom pomocou špongie bola hypotenzia zaznamenaná u 12 % a hyféma u 10 % pacientov. Nižšie riziko komplikácií je vysvetlené s menej invazívnym operačným postupom, vďaka implantátu je prietok vnútroočnej tekutiny do subkonjunktiválneho priestoru regulovaný na rozdiel od trabekulektómie, kde je častokrát potrebná pooperačná úprava stehu pre upravenie filtrovania podľa individuálnych potrieb pacienta.
Vo oboch skupinách našich pacientov nastal pooperačne signifikantný pokles endotelových buniek. Početné práce dokumentujú pokles endotelových buniek po trabekulektómii s aj bez použitia mmC [36–39], pričom vyššie riziko poklesu bolo zaznamenané pri PEX a uveitickom glaukóme [36]. Signifikantný pokles endotelových buniek bol zaznamenaný aj jeden rok po implantácii Preserflo microshuntu [40]. Naopak, iní autori nezaznamenali signifikantný pokles endotelových buniek po 17 mesiacoch od implantácie Preserflo microshuntu [41]. Baker a kol. zistili porovnateľný pokles počtu endoteliálnych buniek po implantácii Preserflo microshuntu, ako aj po trabekulektómii [35].
Reakcia na hojenie a vznikajúca fibróza sú primárnymi determinantmi konečného vnútroočného tlaku. Fibrotizácia spojovky určuje hydraulickú vodivosť spojovky, ktorá riadi prietok tekutiny cez tkanivo. IOT medzi 10 a 14 mmHg je spojený s minimálnou fibrózou spojovky a pomalším zhoršením zorného poľa [42]. Ako každé hojenie rán, aj hojenie rán spojoviek zahŕňa komplexnú súhru medzi rastovými faktormi, cytokínmi, receptormi a enzýmami a krížovú komunikáciu medzi rôznymi typmi buniek. Včasná fáza hojenia rán spojovky po operácii glaukómu zahŕňa únik plazmatických proteínov (fibrinogén, plazminogén a fibronektín) a krvných buniek (trombocyty, polymorfonukleárne neutrofily a červené krvinky) z narušenej vaskulatúry. Premena fibrinogénu na fibrín má za následok tvorbu fibrínových zrazenín a zrážanie krvi. Kombinácia tvorby fibrínovej zrazeniny a uvoľnených proteínov vedie počas zápalovej fázy k migrácii a priťahovaniu neutrofilov, makrofágov a lymfocytov na miesto chirurgického zákroku [43].
Zníženie zápalu je štandardná paradigma na prevenciu zjazvenia po operácii alebo poranení, pretože chronický zápal je spojený s oveľa väčšou fibrózou. Lepšie pochopenie molekulárnych a bunkových mechanizmov procesov hojenia rán a spôsobu a mechanizmu účinku modulačných činidiel viedlo, k identifikácii a modulácii potenciálnych terapeutických cieľov a k efektívnejšiemu využívaniu existujúcich činidiel [44].
Úloha antifibrotických činidiel ako 5-FU a MMC v tradičnej filtračnej chirurgii je dobre známa a s ich používaním sa trabekulektómia stala úspešnejšou pri dosahovaní cieľového IOT. So zvyšujúcou sa účinnosťou sa však zvýšil aj výskyt komplikácií súvisiacich s tvorbou cýst. V dôsledku toho existuje veľký záujem o použitie cielenejšieho prístupu k modulácii hojenia rán. Kľúčovú úlohu v proliferačnej fáze hojenia operačných rán zohráva angiogenéza stimulovaná najmä vaskulárnym endotelovým rastovým faktorom (VEGF).
Viaceré štúdie hodnotili použitie ľudskej rekombinantnej monoklonálnej protilátky proti VEGF ako alternatívu alebo doplnok k MMC pri trabekulektómii [45–49]. Spôsoby podávania zahrňovali lokálne, subkonjunktiválne, intrakamerálne a intravitreálne [50]. Mnohé z týchto štúdií ukázali rozdiel v morfológii vankúšikov v očiach liečených látkami proti VEGF. Skoré pooperačné výsledky ukázali menej vaskulárnych a viac difúznych filtračných vankúšikov v porovnaní s MMC. Zdá sa však, že tento účinok mizne a dlhodobé výsledky vykazujú väčšiu vaskularitu a vyšší IOT, keď boli použité ako samostatné látky v porovnaní s MMC [45,48].
Nedávno publikovaná metaanalýza účinnosti anti-VEGF a MMC na hojenie rán po operácii glaukómu z celkovo publikovaných 369 klinických štúdií analyzovala 7 vhodných štúdií [51]. Metaanalýza neodhalila žiadne významné rozdiely v účinku anti-VEGF a MMC na hojenie rán po trabekulektómii. Na druhej strane, iná metaanalýza sa zamerala na porovnanie účinkov trabekulektómie samotnej alebo kombinovanej s intravitreálnymi injekciami anti-VEGF činidiel na liečbu neovaskulárneho glaukómu [52]. V porovnaní so samotnou trabekulektómiou zaznamenala trabekulektómia s anti-VEGF nižšie riziko pooperačných komplikácií. Zníženie IOT bolo významne väčšie v skupine s trabekulektómiou s anti-VEGF augmentáciou ako v skupine s trabekulektómiou od prvého týždňa po operácii. Podľa výsledkov tejto metaanalýzy môže pridanie intravitreálnej injekcie anti-VEGF látok k trabekulektómii zlepšiť krátkodobé výsledky pacientov s neovaskulárnym glaukómom.
Stupeň poškodenia tkaniva a reakcia hostiteľa pokiaľ ide o závažnosť a trvanie zápalu určuje rozsah zjazvenia spojovky. Moorfields Safer Surgery System je modifikovaná chirurgická technika, ktorej cieľom je minimalizovať inzult a modulovať účinky antimetabolitov [53]. Rozsah fibrózy spojoviek po glaukómovej filtračnej operácii sa bude medzi jednotlivcami líšiť, pretože je ovplyvnený rizikovými faktormi, ako je už existujúci zápal, trvanie a typ liečby očnými kvapkami a predchádzajúca anamnéza operácie [54]. Medzi ďalšie faktory fibrózy po GFS patrí materiál na šitie, rastové faktory odvodené od komorovej vody, mechanická transdukcia z prietoku vodnej tekutiny, signálne molekuly uvoľnené z miest uloženia extracelulárnej matrix, trans-diferenciácia myofibroblastov vedúca k ďalšiemu ukladaniu matrice [54]. Po trabekulektómii je systém hodnotenia Moorfieldsových vankúšikov [55] a užitočným nástrojom na predpovedanie dlhodobého výsledku IOT. Systém gradingu hodnotí zápal a efektívnu aplikáciu antimetabolitov.
Jednoduché zmeny v chirurgických technikách a aplikácia antimetabolitovej liečby výrazne zlepšili úspešnosť a znížili mieru komplikácií pri operácii glaukómu, ako je minimalizácia poškodenia tkaniva a aplikácia prispôsobenej dávky antifibrotického činidla. Modulácia hojenia rán spojoviek je naďalej predmetom záujmu, pretože je kľúčom k dosiahnutiu a udržaniu optimálneho vnútroočného tlaku (10–14 mmHg) po glaukómovej filtračnej operácii s cieľom prevencie progresie glaukómu spojenej s vyššími tlakmi. Nové spôsoby liečby vzniknú z lepšieho pochopenia tkanivovo špecifických molekulárnych, bunkových a biomechanických procesov. Inovatívne riešenia, ktoré môžu priamo a nepriamo modulovať zápalové a fibrotické procesy v optimálnom čase, dávkovaní a lokalite, prinesú priaznivejšie výsledky. Kombinácia liečby alebo sekvenčná liečba môže byť účinnejšia ako jedna látka, najmä u jedincov s vysokým rizikom zjazvenia. Glaukóm exponenciálne narastá s rýchlo starnúcou populáciou na celom svete a plán manažmentu, ktorý dokáže zvládnuť rozsah dopytu, by mal zahŕňať chirurgickú terapiu tak dostupnú a úspešnú ako je operácia katarakty.
ZÁVER
U pacientov po trabekulektómii a po implantácii PMS bol pozorovaný štatisticky významný pokles IOP a antiglaukómovej liečby s menším výskytom komplikácií po implantácii PMS. Je teda zrejmé, že pri aplikácii PMS je nižšia frekvencia pooperačných kontrol, nižšia spotreba medikamentov, skrátenie operačného času a aj menšie množstvo komplikácii a náročnosť ich riešenia. Má to veľký dopad na zrakovú rekonvalescenciu a aj na kvalitu života pacientov ako aj rýchlosť ich návratu do každodenného života.
Zdroje
1. Vision Loss Expert Group of the Global Burden of Disease Study. Global estimates on the number of people blind or visually impaired by glaucoma: A meta-analysis from 2000 to 2020. Eye. 2024;38 : 2036.
2. Chen W, Xu Y, Liu Z, Zhao J. Global, regional and national burden of Glaucoma: an update analysis from the Global Burden of Disease Study 2019. Int Ophthalmol. 2024;44 : 234.
3. Ramulu PY, Corcoran KJ, Corcoran SL, Robin AL. Utilization of various glaucoma surgeries and procedures in Medicare beneficiaries from 1995 to 2004. Ophthalmology. 2007;114 : 2265-2270.
4. Kalarn S, Le T, Rhee DJ. The role of trabeculectomy in the era of minimally invasive glaucoma surgery. Curr Opin Ophthalmol. 2022;33 : 112-118.
5. Tanna AP. 2023-2024 Basic and Clinical Science Course, Section 10: Glaucoma: American Academy of Ophthalmology; 2023.
6. Ichhpujani P, Singla E, Kalra G, Bhartiya S, Kumar S. Surgical trends in glaucoma management: the current Indian scenario. Int Ophthalmol. 2022;42 : 1661-1668.
7. Pinchuk L, Riss I, Batlle JF, et al. The development of a microshunt made from poly(styrene-block-isobutylene-block-styrene) to treat glaucoma. J Biomed Mater Res B Appl Biomater. 2017;105 : 211-221.
8. Governatori L, Oliverio L, Mermoud A, et al. PreserFlo MicroShunt versus trabeculectomy: an updated meta-analysis and systematic review. Graefes Arch Clin Exp Ophthalmol. 2024. DOI: 10.1007/ s00417-00024-06649-w
9. Khan A, Khan AU. Comparing the safety and efficacy of Preserflo Microshunt implantation and trabeculectomy for glaucoma: A systematic review and meta‐analysis. Acta Ophthalmol (Copenh). 2024;102:e443-e451.
10. Cairns JE. Trabeculectomy. Preliminary report of a new method. Am J Ophthalmol. 1968;66 : 673-679.
11. Ng WS, Jayaram H. Adjunctive modulation of wound healing during cataract surgery to promote survival of a previous trabeculectomy. Cochrane Database Syst Rev. 2021;8:CD013664.
12. Addicks EM, Quigley HA, Green WR, Robin AL. Histologic characteristics of filtering blebs in glaucomatous eyes. Arch Ophthalmol. 1983;101 : 795-798.
13. Fluorouracil Filtering Surgery Study one-year follow-up. The Fluorouracil Filtering Surgery Study Group. Am J Ophthalmol. 1989;108(6):625-635.
14. Lee GA, Liu L, Casson RJ, Danesh-Meyer HV, Shah P, ANZGS Trabeculectomy Consensus Group. Current practice of trabeculectomy in a cohort of experienced glaucoma surgeons in Australia and New Zealand. Eye. 2023;37 : 1139-1144.
15. Wilkins M, Indar A, Wormald R. Intra-operative mitomycin C for glaucoma surgery. Cochrane Database Syst Rev. 2005;2005:CD002897.
16. Wolters JEJ, van Mechelen RJS, Al Majidi R, et al. History, presence, and future of mitomycin C in glaucoma filtration surgery. Curr Opin Ophthalmol. 2021;32.
17. Bindlish R, Condon GP, Schlosser JD, D’Antonio J, Lauer KB, Lehrer R. Efficacy and safety of mitomycin-C in primary trabeculectomy: five-year follow-up. Ophthalmology. 2002;109 : 1336-1341.
18. Mosaed S, Dustin L, Minckler DS. Comparative outcomes between newer and older surgeries for glaucoma. Trans Am Ophthalmol Soc. 2009;107 : 127-133.
19. Seol BR, Lee SY, Kim YJ, Kim YK, Jeoung JW, Park KH. Comparison of the efficacy and safety of trabeculectomy with mitomycin C according to concentration: a prospective randomized clinical trial. J Clin Med. 2020;10 : 59.
20. Kitazawa Y, Suemori-Matsushita H, Yamamoto T, Kawase K. Low-dose and high-dose mitomycin trabeculectomy as an initial surgery in primary open-angle glaucoma. Ophthalmology. 1993;100 : 1624-1628.
21. Mietz H, Krieglstein GK. Three-year follow-up of trabeculectomies performed with different concentrations of mitomycin-C. Ophthalmic Surg Lasers. 1998;29 : 628-634.
22. Khan SA, Whittaker K, Razzaq MA, Arain UR. National survey of intraoperative mitomycin C use during trabeculectomy surgery in the UK. Int Ophthalmol. 2021;41 : 1309-1316.
23. Zhang X, Song Y, Liebmann J, Weinreb RN. A modified technique in applying sponge soaked with mitomycin C in trabeculectomy. Asian Pacific Journal of Ophthalmology. 2021;10 : 548-552.
24. Khaw PT, Chiang M, Shah P, Sii F, Lockwood A, Khalili A. Enhanced trabeculectomy: the moorfields safer surgery system. Dev Ophthalmol. 2012;50 : 1-28.
25. Guimarães ME, de Pádua Soares Bezerra B, de Miranda Cordeiro F, et al. Glaucoma surgery with soaked sponges with mitomycin C vs Sub-Tenon injection: short-term outcomes. Journal of Current Glaucoma Practice. 2019;13 : 50-54.
26. Gambini G, Carlà mm, Giannuzzi F, et al. PreserFlo® MicroShunt: an overview of this minimally invasive device for open-angle glaucoma. Vision (Basel). 2022;6 : 12.
27. Nobl M, Freissinger S, Kassumeh S, Priglinger S, Mackert MJ. One-year outcomes of microshunt implantation in pseudoexfoliation glaucoma. PLoS One. 2021;16:e0256670.
28. Triolo G, Wang J, Aguilar-Munoa S, Jayaram H, Barton K. Preserflo microshunt implant for the treatment of refractory uveitic glaucoma: 36-month outcomes. Eye. 2023;37 : 2535-2541.
29. Storp JJ, Vietmeier FE, Merté RL, et al. Long-term outcomes of the PRESERFLO MicroShunt implant in a heterogeneous glaucoma cohort. J Clin Med. 2023;12 : 4474.
30. Pillunat KR, Herber R, Haase MA, Jamke M, Jasper CS, Pillunat LE. PRESERFLO™ MicroShunt versus trabeculectomy: first results on efficacy and safety. Acta Ophthalmol (Copenh). 2022;100:e779-e790. 31. Gubser PA, Pfeiffer V, Hug S, et al. PRESERFLO MicroShunt implantation versus trabeculectomy for primary open-angle glaucoma: a two-year follow-up study. Eye Vis (Lond). 2023;10 : 50.
32. Rabiolo A, Toscani R, Sacchi M, et al. Risk factors for failure in glaucoma patients undergoing microshunt implantantion. Am J Ophthalmol. 2023;259 : 117-130. 33. Burgos-Blasco B, García-Feijóo J, Gines-Gallego C, et al. Efficacy and safety of the PreserFlo implant with mitomycin C in childhood glaucoma after previous failed glaucoma surgeries. Graefes Arch Clin Exp Ophthalmol. 2023;261 : 1349-1357. 34. Van Lancker L, Saravanan A, Abu-Bakra M, et al. Clinical outcomes and cost analysis of PreserFlo versus trabeculectomy for glaucoma management in the United Kingdom. Ophthalmol Glaucoma. 2023;6 : 342-357. 35. Baker ND, Barnebey HS, Moster MR, et al. Ab-Externo MicroShunt versus trabeculectomy in primary open-angle glaucoma: one-year results from a 2-year randomized, multicenter study. Ophthalmology. 2021;128 : 1710-1721. 36. Higashide T, Nishino T, Sakaguchi K, Yamada Y, Sugiyama K. Determinants of corneal endothelial cell loss after trabeculectomy with mitomycin C. J Glaucoma. 2019;28 : 61-67.
37. Hirooka K, Nitta E, Ukegawa K, Sato S, Kiuchi Y. Effect of trabeculectomy on corneal endothelial cell loss. Br J Ophthalmol. 2020;104 : 376-380.
38. Storr-Paulsen T, Norregaard JC, Ahmed S, Storr-Paulsen A. Corneal endothelial cell loss after mitomycin C-augmented trabeculectomy. J Glaucoma. 2008;17 : 654-657.
39. Arnavielle S, Lafontaine PO, Bidot S, Creuzot-Garcher C, D’Athis P, Bron AM. Corneal endothelial cell changes after trabeculectomy and deep sclerectomy. J Glaucoma. 2007;16 : 324-328.
40. Ibarz-Barberá M, Morales-Fernández L, Corroto-Cuadrado A, et al. Corneal endothelial cell loss after PRESERFLO™ MicroShunt implantation in the anterior chamber: anterior segment OCT tube location as a risk factor. Ophthalmol Ther. 2022;11 : 293-310.
41. Steindor FA, Trigaux C, Holtmann C, Spaniol K, Geerling G, Borrelli M. PRESERFLO MicroShunt®: efficacy and endothelial cell density. J Glaucoma. 2023: doi: 10.1097/IJG.0000000000002325.
42. No authors listed. The Advanced Glaucoma Intervention Study (AGIS): 7. The relationship between control of intraocular pressure and visual field deterioration.The AGIS Investigators. Am J Ophthalmol. 2000;130 : 429-440.
43. Van Bergen T, Van de Velde S, Vandewalle E, Moons L, Stalmans I. Improving patient outcomes following glaucoma surgery: state of the art and future perspectives. Clin Ophthalmol. 2014;2 : 857-867.
44. Khaw PT, Bouremel Y, Brocchini S, Henein C. The control of conjunctival fibrosis as a paradigm for the prevention of ocular fibrosis-related blindness. “Fibrosis has many friends”. Eye. 2020;34 : 2163 - 2174.
45. Grewal DS, Jain R, Kumar H, Grewal SP. Evaluation of subconjunctival bevacizumab as an adjunct to trabeculectomy a pilot study. Ophthalmology. 2008;115 : 2141-2145.
46. Fakhraie G, Ghadimi H, Eslami Y, et al. Short-term results of trabeculectomy using adjunctive intracameral bevacizumab: a randomized controlled trial J Glaucoma. 2016;25:e182-e188.
47. Akkan JU, Cilsim S. Role of subconjunctival bevacizumab as an adjuvant to primary trabeculectomy: a prospective randomized comparative 1-year follow-up study. J Glaucoma. 2015;24 : 1-8.
48. Pro MJ, Freidl KB, Neylan CJ, Sawchyn AK, Wizov SS, Moster MR. Ranibizumab versus mitomycin C in primary trabeculectomy – a pilot study. Curr Eye Res. 2015;40 : 510-505.
49. Kiddee W, Orapiriyakul L, Kittigoonpaisan K, Tantisarasart T, Wangsupadilok B. Efficacy of adjunctive subconjunctival bevacizumab on the outcomes of primary trabeculectomy with mitomycin C: a prospective randomized placebo-controlled trial. J Glaucoma. 2015;24 : 600-606.
50. Andrés-Guerrero V, Perucho-González L, García-Feijoo J, et al. Current perspectives on the use of anti-VEGF drugs as adjuvant therapy in glaucoma. Adv Ther. 2017;34 : 378-395.
51. Liu W, Liu B. Efficacy of anti-vascular endothelial growth factor and mitomycin C on wound healing after trabeculectomy in glaucoma patients: a meta-analysis. Int Wound J. 2023: doi: 10.1111/ iwj.14517.
52. Zhou X, Chen J, Luo W, Du Y. Short-term outcomes of trabeculectomy with or without anti-VEGF in patients with neovascular glaucoma: a systematic review and meta-analysis. Translational Vision Science and Technology. 2023;12 : 12.
53. Khaw PT, Chiang M, Shah P, Sii F, Lockwood A, Khalili A. Enhanced trabeculectomy: the moorfields safer surgery system. Dev Ophthalmol. 2017;59 : 15-35.
54. Schlunck G, Meyer-ter-Vehn T, Klink T, Grehn F. Conjunctival fibrosis following filtering glaucoma surgery. Exp Eye Res. 2016;142 : 76 - 82.
55. Wells AP, Crowston JG, Marks J, et al. A pilot study of a system for grading of drainage blebs after glaucoma surgery. J Glaucoma. 2004;13 : 454-460.
Štítky
Oftalmológia
Článok vyšiel v časopiseČeská a slovenská oftalmologie
Najčítanejšie tento týždeň
2026 Číslo 2- Pomocné látky v roztoku latanoprostu bez konzervačních látek vyvolávají zánětlivou odpověď a cytotoxicitu u imortalizovaných lidských HCE-2 epitelových buněk rohovky
- Konzervační látka polyquaternium-1 zvyšuje cytotoxicitu a zánět spojený s NF-kappaB u epitelových buněk lidské rohovky
- Dlouhodobé výsledky lokální léčby cyklosporinem A u těžkého syndromu suchého oka s 10letou dobou sledování
- Syndrom suchého oka
- Cyklosporin A v léčbě suchého oka − systematický přehled a metaanalýza
-
Všetky články tohto čísla
- Minimálně invazivní glaukomová chirurgie: iStent a Preserflo v léčbě primárního glaukomu s otevřeným úhlem. Přehled
- Choroidální neovaskulární membrána u dětí, dlouhodobé výsledky terapie anti-VEGF preparátem
- Preserflo MicroShunt verzus trabekulektómia: klinické výsledky 6-mesačnej retrospektívnej štúdie
- Metrické příčiny refrakčních vad oka
- Výsledky segmentálního sklerálního bucklingu s endoiluminátorem ve srovnání s konvenčním sklerálním bucklingem u primárního rhegmatogenního odchlípení sítnice: Srovnávací retrospektivní studie
- Subretinální triamcinolon acetonid a transpupilární termoterapie u ohraničeného choroidálního hemangiomu. Kazuistika
- Stoleté výročí vzniku Československé oftalmologické společnosti
- Česká a slovenská oftalmologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Minimálně invazivní glaukomová chirurgie: iStent a Preserflo v léčbě primárního glaukomu s otevřeným úhlem. Přehled
- Stoleté výročí vzniku Československé oftalmologické společnosti
- Preserflo MicroShunt verzus trabekulektómia: klinické výsledky 6-mesačnej retrospektívnej štúdie
- Subretinální triamcinolon acetonid a transpupilární termoterapie u ohraničeného choroidálního hemangiomu. Kazuistika
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



