-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Choroidální neovaskulární membrána u dětí, dlouhodobé výsledky terapie anti-VEGF preparátem
Choroidal Neovascular Membrane in Pediatric Patients: Long-Term Outcomes of Anti-VEGF Therapy
Aim: To evaluate the epidemiological data, etiology and clinical characteristics, and to assess the efficacy and safety of intravitreal anti-vascular endothelial growth factor (anti-VEGF) therapy in the treatment of choroidal neovascular membrane (CNV) in children and adolescents. The results are compared with data from previously published studies and case reports. Material and Methods: Retrospective analysis of medical records of patients treated for CNV at the Department of Pediatric Ophthalmology, University Hospital Brno, between January 2015 and April 2025. The cohort consisted of 12 patients, including 7 males and 5 females. All the cases involved unilateral disease; the right eye was affected in 7 patients and the left eye in 5. The mean age at onset was 11.8 years (range: 3–17 years). All underwent a comprehensive ophthalmological examination including optical coherence tomography (OCT); in 7 cases the diagnosis was confirmed by fluorescein angiography. The evaluated parameters included epidemiological data, clinical and morphological characteristics of CNV before and after anti-VEGF therapy. The etiology of CNV in our cohort was as follows: post-inflammatory/post-infectious in 6 cases, idiopathic in 3 cases, and one case each of myopic, post-traumatic, and neoplastic origin. The most common localization was subfoveal. All CNV lesions were classified as classic (type 2). Results: All patients achieved either anatomical or functional improvement. No ocular or systemic adverse effects related to intravitreal anti-VEGF therapy were observed during the study period. Conclusion: Early diagnosis and intervention with anti-VEGF therapy show favorable outcomes, including stabilization and remission of the disease. In our cohort, no adverse events or complications associated with intravitreal anti-VEGF administration were recorded. Continued research is essential in order to gain a further understanding of the pathogenesis of pediatric CNV and to optimize treatment strategies in children.
Keywords:
ranibizumab – anti-VEGF – choroidal neovascularization – pediatric CNV – choroidal neovascular membrane in children – secondary CNV
Autori: Kamila Pavlíková 1; Inka Krejčířová 1; Rudolf Autrata 1; Kateřina Šenková 1; Veronika Matušková 2
Pôsobisko autorov: Dětská oční klinika Fakultní nemocnice Brno, Lékařská fakulta Masarykovy univerzity Brno 1; Oční klinika Fakultní nemocnice Brno, Lékařská fakulta Masarykovy univerzity Brno 2
Vyšlo v časopise: Čes. a slov. Oftal., 82, 2026, No. 2, p. 73-80
Kategória: Původní práce
doi: https://doi.org/10.31348/2025/33Súhrn
Cíl: Posouzení epidemiologických dat, etiologie, klinických charakteristik a zhodnocení účinnosti a bezpečnosti terapie choroidální neovaskulární membrány (CNV) intravitreálním antiangiogenním preparátem (anti-VEGF) u dětí a adolescentů. Komparativní analýza našich výsledků s daty z dosud publikovaných studií a kazuistických sdělení. Materiál a metodika: Retrospektivní zhodnocení zdravotnické dokumentace souboru pacientů léčených pro CNV na Dětské oční klinice Fakultní nemocnice Brno v období od ledna roku 2015 do dubna 2025. Analyzovaný soubor zahrnoval 12 pacientů, z toho 7 pacientů mužského pohlaví a 5 pacientů ženského pohlaví. Ve všech případech se jednalo o unilaterální postižení, přičemž u 7 pacientů byla afekce lokalizována na pravém oku a u 5 pacientů na levém oku. Průměrný věk v době klinické manifestace činil 11,8 let (věkové rozmezí 3–17 let). Všichni pacienti podstoupili komplexní oftalmologické vyšetření včetně optické koherenční tomografie. V 7 případech byla diagnóza verifikována fluorescenční angiografií. Hodnocené parametry zahrnovaly epidemiologická data, klinické a morfologické charakteristiky CNV před zahájením a po ukončení terapie anti-VEGF preparátem. V našem souboru bylo etiologické spektrum CNV následující: v 6 případech se jednalo o zánětlivou etiologii, ve 3 případech byla příčina idiopatická. Dále jsme dokumentovali výskyt myopické, posttraumatické a neoplastické etiologie, přičemž každá z nich byla zastoupena jedním případem. Dominantně se jednalo o subfoveolární lokalizaci CNV. Ve všech případech byla CNV klasifikována jako klasická, odpovídající typu 2. Výsledky: U všech pacientů jsme dosáhli signifikantního zlepšení anatomických či funkčních parametrů a do doby publikace této práce nebyl zaznamenán výskyt očních či systémových nežádoucích účinků v souvislosti s intravitreální aplikací anti-VEGF preparátu. Závěr: Včasná diagnostika a intervence pomocí anti-VEGF léčby vykazují pozitivní výsledky, včetně stabilizace a remise onemocnění. V námi sledovaném souboru pacientů nebyly zaznamenány nežádoucí účinky ani komplikace asociované s aplikací anti-VEGF terapie. Pro další prohloubení znalostí o patogenezi pediatrické CNV a optimalizaci terapeutických strategií u dětské populace je nezbytný kontinuální výzkum v této oblasti.
Klíčová slova:
Choroidální neovaskularizace – CNV u dětí – ranibizumab – anti-VEGF – choroidální neovaskulární membrána u dětí – sekundární CNV
ÚVOD
Choroidální neovaskulární membrána (CNV) představuje v dětské populaci velmi vzácné onemocnění, které však může zapříčinit závažné poškození či dokonce ztrátu centrálního vidění, zejména pokud se léze nachází v centrální oblasti. Od CNV vyskytující se u dospělé starší populace se odlišuje především etiologií, ale také klinickým obrazem a odpovědí na terapeutické intervence [1]. Zatímco u starších pacientů je vznik CNV většinou asociován s věkem podmíněnou makulární degenerací (VPMD), u dětí se CNV rozvíjí sekundárně na podkladě jiného predisponujícího onemocnění [2].
CNV se formuje z novotvořených cév choroidey, které pronikají Bruchovou membránou do subretinálního prostoru nebo pod retinální pigmentový epitel (RPE). Iniciačním faktorem pro vznik CNV je narušení integrity Bruchovy membrány a patologické změny RPE [3].
V odborné literatuře je na základě etiologických faktorů definováno pět kategorií příčin vzniku sekundární CNV: zánětlivá/infekční, degenerativní/dystrofická, traumatická, myopická a neoplastická. V případech, kdy příčinu CNV nelze identifikovat, hovoříme o idiopatické CNV (Obrázek 1A, B, C) [4].
Obr. 1. 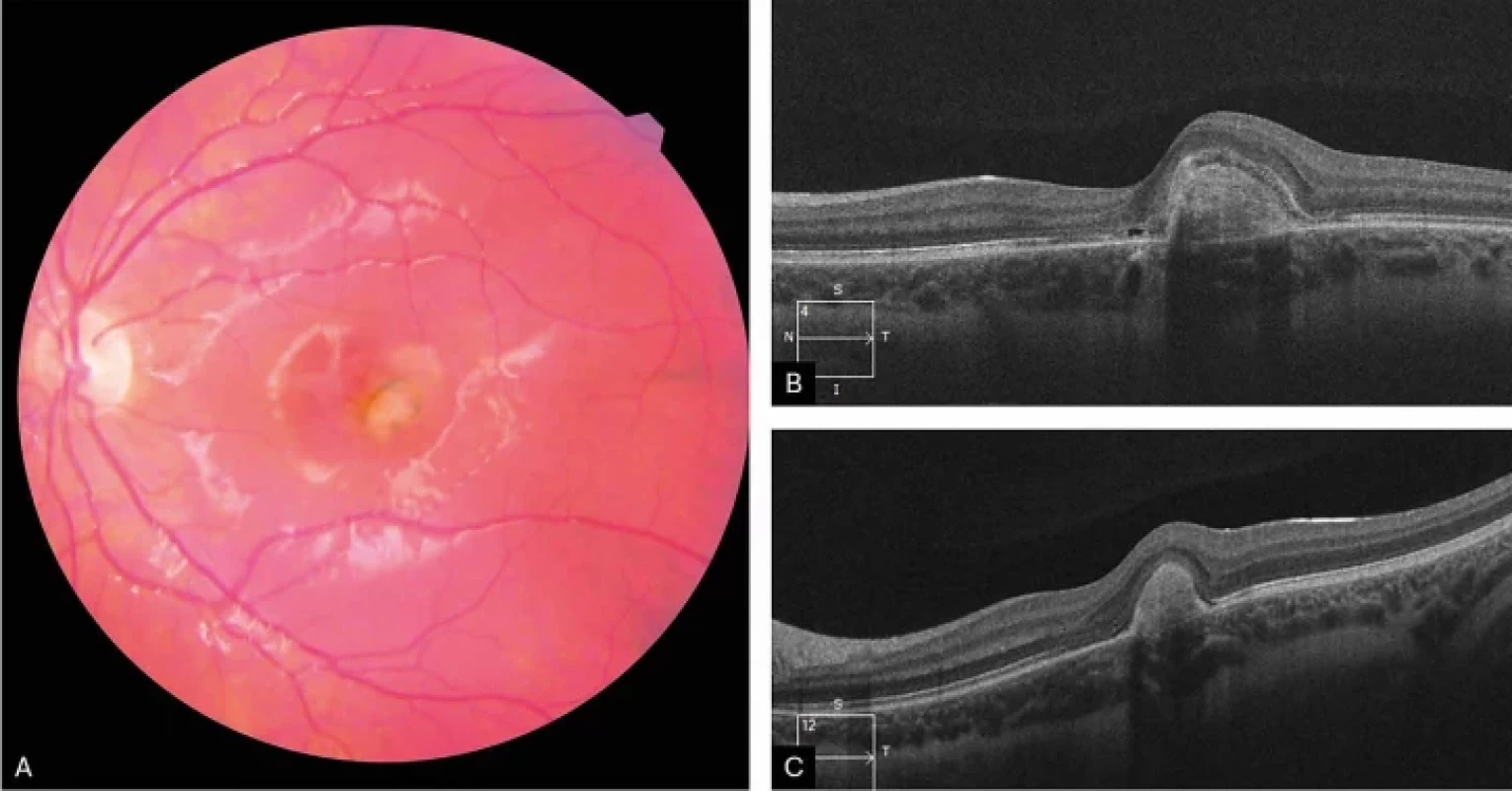
Fotografie očního pozadí pacientky s idiopatickou juxtafoveolární CNV před terapií (A), HD-OCT – lineární horizontální makulární sken pacientky před terapií (B), po aplikaci 3 injekcí ranibizumabu (C) CNV – choroidální neovaskulární membrána HD-OCT – optická koherentní tomografie s vysokým rozlišením JEDNOTLIVÉ KATEGORIE CNV
Zánětlivá/infekční (Obrázek 2A, B, C, D, E)
Obr. 2. 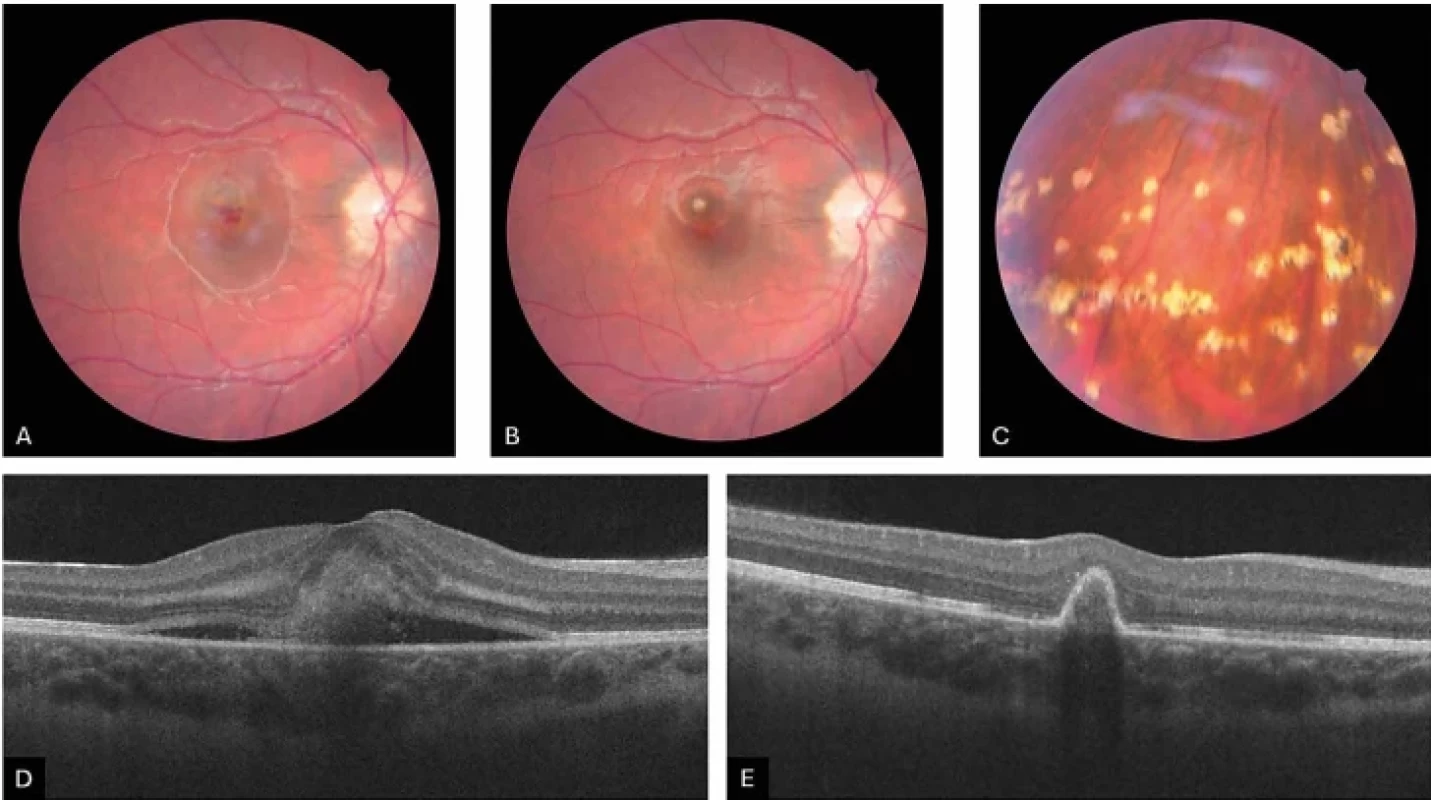
Fotografie očního pozadí pacientky s vnitřní tečkovitou choroidopatií před terapií (A), po aplikaci 3 injekcí ranibizumabu (B), nález ostře ohraničených bělavých ložisek v periferii sítnice (C). HD-OCT – lineární horizontální makulární sken sekundární zánětlivé CNV před terapií (D), po 3 intravitreálních aplikacích ranibizumabu (E) CNV – choroidální neovaskulární membrána HD-OCT – optická koherentní tomografie s vysokým rozlišením Dle nedávno publikovaných studií zahrnujících největší soubory pacientů představuje zánětlivá etiologie nejčastější příčinu choroidální neovaskulární membrány u dětí [5–7]. CNV se může manifestovat v různých stádiích intraokulárního zánětu, od aktivní choroiditidy či chorioretinitidy přes středně závažnou uveitidu až po panuveitidu [5]. Velmi častou příčinou zánětlivé CNV bývá oční toxoplazmová chorioretinitida. Stanovení frekvence výskytu CNV u tohoto onemocnění je problematické, jelikož postižení pacienti obvykle trpí skotomy v důsledku chorioretinitidy a často si ani neuvědomují další ztrátu zraku způsobenou CNV. Mezi další infekční příčiny zánětlivé CNV se řadí oční toxokaróza, rubeola, syfilis a v endemických oblastech představuje velmi častou příčinu oční histoplazmóza. Z neinfekčních příčin jsou významné vnitřní tečkovaná choroidopatie, multifokální chorioretinitida, Vogt-Koyanagi-Harada syndrom, serpiginózní chorioretinopatie a další [8].
Degenerativní/dystrofická (Obrázek 3A, B, C,)
Obr. 3. 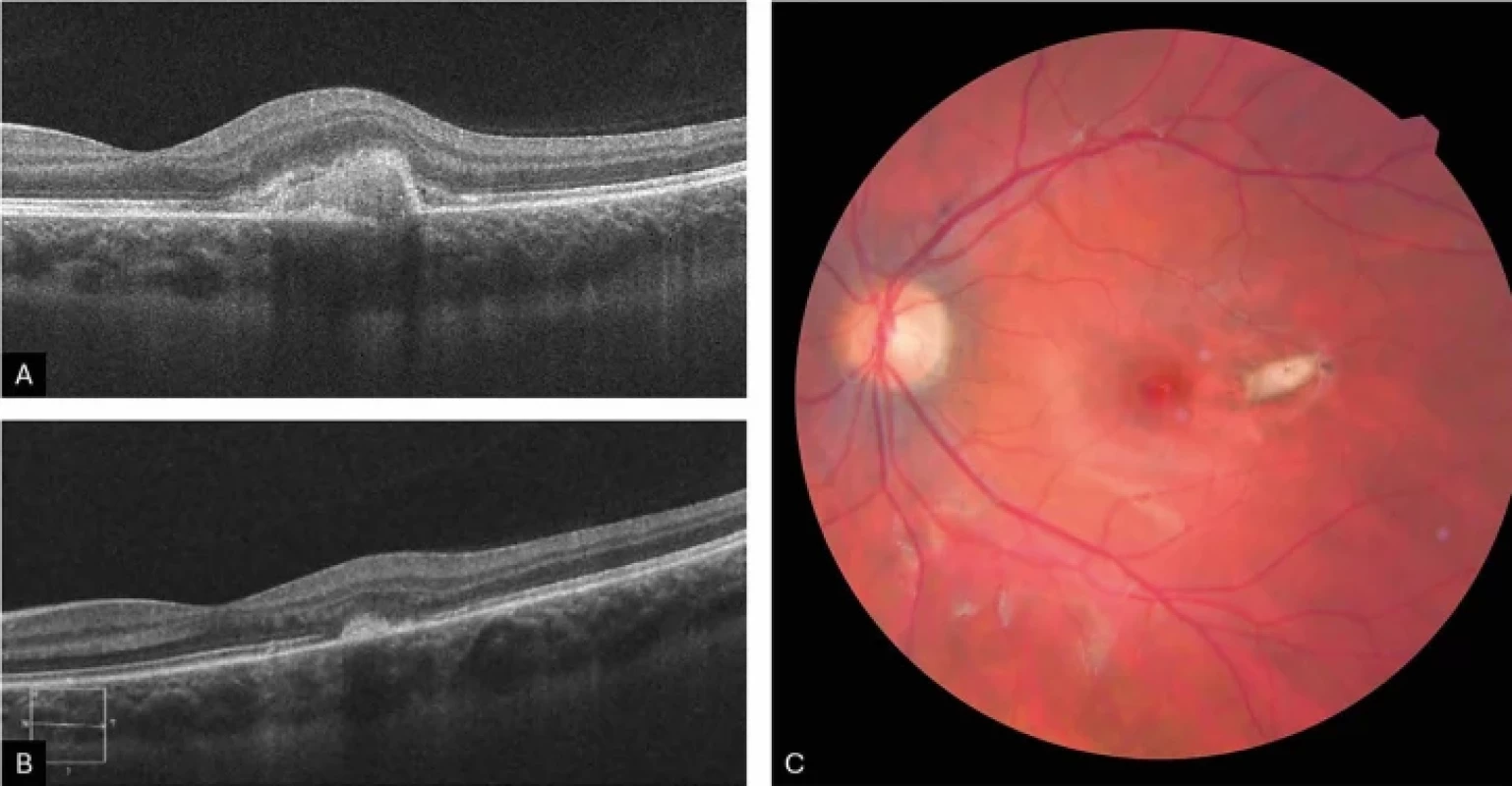
HD-OCT – lineární horizontální makulární sken sekundární myopické CNV na levém oku. Stav před terapií (A) a stav po aplikaci (B) jedné, a zároveň dostatečné, intravitreální injekce ranibizumabu. Fotografie očního pozadí při posledním kontrolním vyšetření (C), patrné fibrotizované extrafoveolární ložisko CNV CNV – choroidální neovaskulární membrána HD-OCT – optická koherentní tomografie s vysokým rozlišením CNV byla dokumentována u řady retinálních dystrofií, jako je Bestova vitelliformní dystrofie, Stargardtova choroba nebo retinitis pigmentosa. Do této kategorie dále spadá CNV při drúzách optického nervu či jiných anomáliích optického nervu jako kolobom, jamky terče nebo syndrom Morning glory. V případě anomálií optického nervu bývá CNV častěji lokalizována peripapilárně [1]. V kontextu patologické myopie představují predisponující faktory pro vznik CNV atrofie RPE a trhliny Bruchovy membrány, proto je výskyt myopické CNV pravděpodobnější u starších pacientů s degenerativní myopií. V dětské populaci se však vyskytuje vzácně.
Traumatická (Obrázek 4A, B, C, D, E)
Obr. 4. 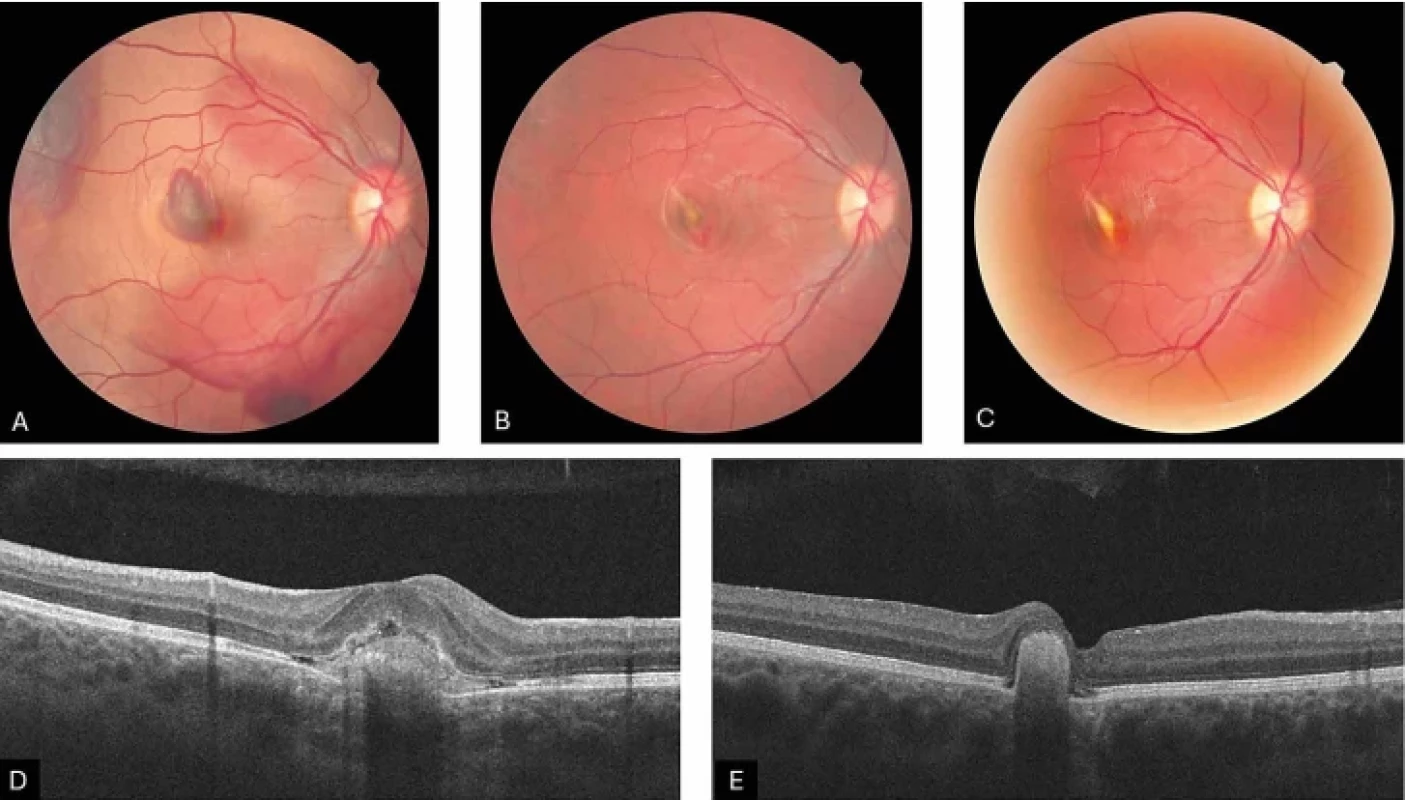
Fotografie očního pozadí pacienta s těžkou kontuzí bulbu, v makule se subretinálním krvácením a rupturou Bruchovy membrány v den úrazu (A), v době tvorby sekundární traumatické CNV (B) a při posledním kontrolním vyšetření (C). HD-OCT – lineární horizontální makulární sken sekundární traumatické CNV, stav před terapii (D) a stav po aplikaci 3 intravitreálních injekcí ranibizumabu (E) CNV – choroidální neovaskulární membrána HD-OCT – optická koherentní tomografie s vysokým rozlišením Většina posttraumatických CNV vzniká v průběhu hojení ruptury choroidální membrány, nejedná se však o pravidlo [9]. Rizikové faktory pro rozvoj CNV zahrnují blízkost ruptury k centru fovey a délku ruptury [10].
Neoplastická (Obrázek 5A, B, C, D, E)
Obr. 5. 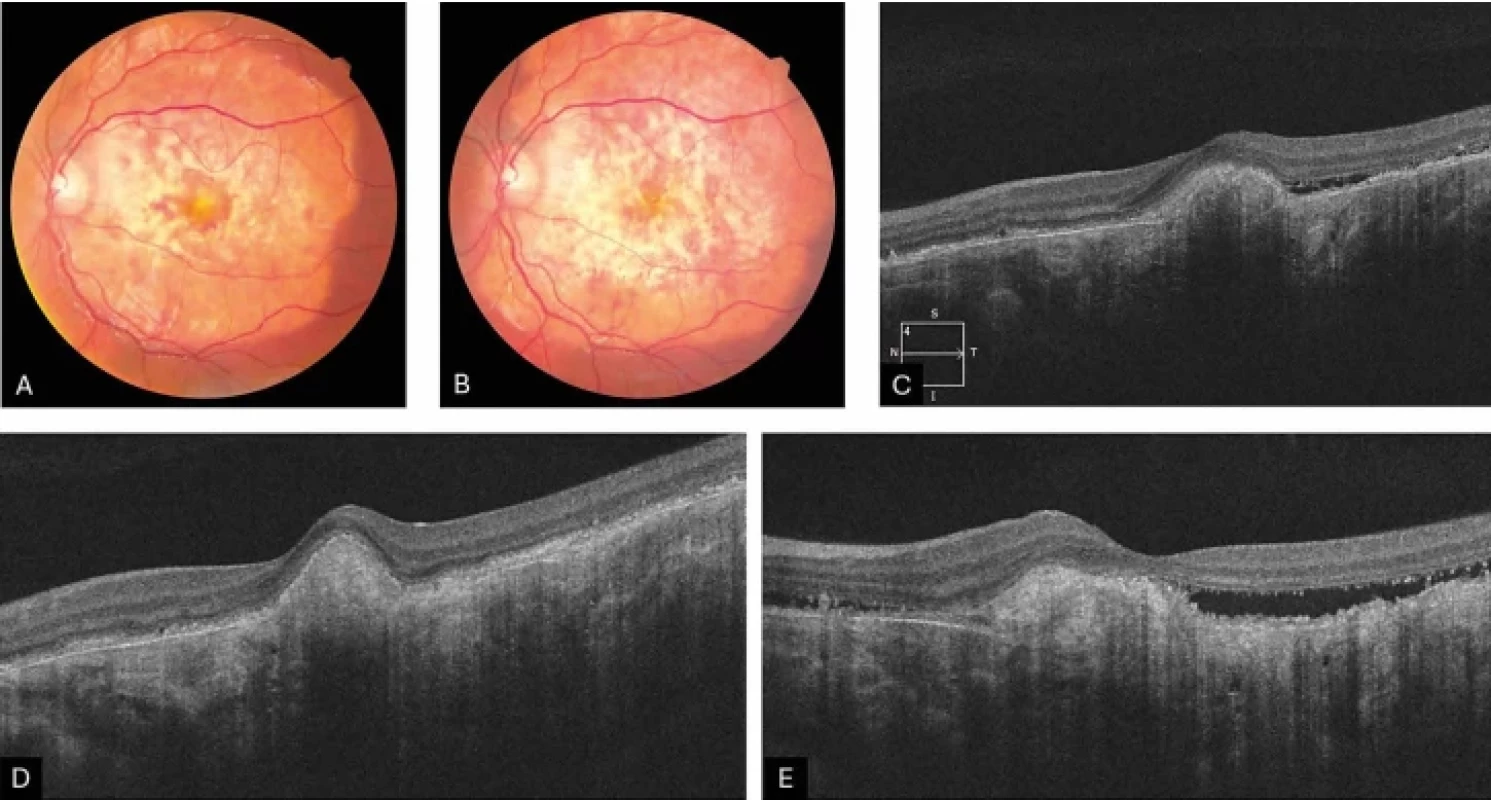
Fotografie očního pozadí pacienta s choroidálním osteomem v době vzniku sekundární neoplastické CNV (A) a při posledním kontrolním vyšetření (B). HD-OCT – lineární horizontální makulární sken sekundární neoplastické CNV před terapií (C), v době remise onemocnění (D) a při rekurenci aktivity CNV v posledním období sledování (E) CNV – choroidální neovaskulární membrána HD-OCT – optická koherentní tomografie s vysokým rozlišením V rámci této kategorie byly publikovány případy CNV u dětí na podkladě choroidálního osteomu nebo kombinovaného hamartomu sítnice a RPE. Choroidální osteom představuje vzácný benigní intraokulární tumor, který typicky postihuje mladé, jinak zdravé ženy v první nebo druhé dekádě života. Může být však diagnostikován i u mužů, starších osob či kojenců [11,12]. Většinou se jedná o unilaterální postižení, ačkoliv byly popsány i bilaterální případy [13,14]. Etiologie choroidálního osteomu není dosud plně objasněna. Mezi uvažované faktory patří zánět, trauma, hormonální změny a poruchy metabolismu vápníku. Klinicky se choroidální osteom manifestuje jako nažloutlá až oranžová, mírně elevovaná léze s dobře definovanými geografickými okraji. Nejčastější lokalizace je juxtapapilární či peripapilární oblast, může však zasahovat až do makuly. Prognóza tohoto onemocnění je obecně nepříznivá a závisí na přítomnosti komplikací, jako jsou dekalcifikace ložiska, atrofie RPE, přítomnost subretinální tekutiny či sekundární CNV. V současnosti neexistuje standardizovaný terapeutický protokol. Léčba se zaměřuje na management sekundárních komplikací a zahrnuje laserovou fotokoagulaci, transpupilární termoterapii, fotodynamickou terapii a intravitreální aplikaci anti-VEGF preparátů. Dle nejnovějších doporučení je při výskytu sekundární CNV u choroidálního osteomu považována za bezpečnou a účinnou intravitreální anti-VEGF terapie, a to bez ohledu na lokalizaci CNV [15,16].
V současné době představují intravitreální preparáty obsahující anti-VEGF látky standardní terapeutickou volbu v managementu CNV u dětských pacientů. Tyto látky inhibují angiogenezi a snižují vaskulární permeabilitu, což může vést ke stabilizaci nebo zlepšení zrakových funkcí [9]. S rostoucím množstvím dostupných klinických dat potvrzujících příznivý efekt anti-VEGF terapie u dětské CNV ustupují dříve preferované metody, jako jsou laserová fotokoagulace nebo fotodynamická terapie, do pozadí.
Vzhledem k nízké incidenci tohoto onemocnění jsou dosavadní poznatky založeny převážně na omezeném počtu retrospektivních studií a kazuistik, přičemž dosud nebyl vytvořen standardizovaný terapeutický protokol. S ohledem na charakter onemocnění a specifika dětské populace se realizace prospektivní randomizované kontrolované studie jeví jako málo pravděpodobná.
MATERIÁL A METODIKA
V našem souboru pacientů jsme retrospektivně analyzovali lékařské záznamy a obrazovou dokumentaci u 12 dětských pacientů, u nichž byla diagnostikována a anti - -VEGF preparátem léčena CNV na naší klinice v období od ledna 2015 do dubna 2025. Soubor tvoří 7 pacientů mužského pohlaví a 5 pacientek ženského pohlaví. U všech pacientů se jednalo o jednostranné postižení, přičemž častěji bylo postiženo pravé oko (n = 7) oproti levému oku (n = 5). Průměrný věk při manifestaci činil 11,8 let, s rozmezím od 3 do 17 let. Mezi analyzované epidemiologické a klinické parametry patřily: pohlaví, věk v době diagnostiky, klinické příznaky, počáteční nejlépe korigovaná zraková ostrost (NKZO), finální NKZO a počet aplikací. Dále byly hodnoceny morfologické parametry: lokalizace CNV, etiologie CNV, kategorie CNV, počáteční a finální centrální retinální tloušťka.
Všichni pacienti podstoupili podrobné vstupní oftalmologické vyšetření a laboratorní vyšetření krve. NKZO byla vyšetřena na Snellenových optotypech a následně přepočtena na hodnotu decimal. CNV byla detekována biomikroskopickým vyšetřením očního pozadí a optickou koherenční tomografií (OCT). K potvrzení diagnózy, určení typu CNV a stanovení její aktivity byla v 7 případech provedena fluorescenční angiografie. Subjektivní potíže při stanovení diagnózy zahrnovaly: rozmazané vidění, vnímání šedavého ložiska a skotom zorného pole. U dvou pacientů se žádné subjektivní potíže neprojevily a CNV byla diagnostikována během rutinní preventivní oční kontroly. Mezi oční patologie predisponující ke vzniku CNV v našem souboru patří: chorioretinitida (n = 5), vnitřní tečkovitá choroidopatie (n = 1), traumatická ruptura choroidey (n = 1), choroidální osteom (n = 1) a patologická myopie (n = 1). U 3 pacientů nebyla příčina objasněna a případy byly klasifikovány jako idiopatická CNV.
Pomocí OCT skenů jsme porovnávali vstupní a finální centrální retinální tloušťku. Na jednotlivých OCT horizontálních skenech s vysokým rozlišením jsme měřili retinální tloušťku v oblasti ložiska. Podle vzdálenosti ložiska CNV od foveolární avaskulární zóny byla CNV klasifikována jako subfoveolární, juxtafoveolární (do 199 µm od foveoly) a extrafoveolární (nad 200 µm od foveoly). Pomocí OCT byla rovněž sledována efektivita terapie identifikováním přítomnosti intraretinální nebo subretinální tekutiny. Všechny případy představovaly klasickou CNV neboli typ 2. Podle OCT vyšetření byla průměrná tloušťka sítnice v místě ložiska před zahájením terapie 624 µm (rozsah 451–1050 µm), po léčbě 488 µm (rozsah 356–733 µm). Průměrná počáteční centrální retinální tloušťka činila 325 µm (257–479 µm), finální pak 232 µm. Nejčastější lokalizací CNV byla subfoveolární oblast, která byla postižena u 7 pacientů, u 4 pacientů byla CNV juxtafoveolární a u jednoho pacienta byla lokalizována extrafoveolárně.
V průběhu terapie nebyl k dispozici standardizovaný protokol pro aplikaci anti-VEGF u dětí. U každého pacienta byl počet aplikací posuzován individuálně na základě aktivity onemocnění, lokalizace léze a typu základního očního onemocnění. V 9 případech bylo použito fixní dávkování s 3 injekcemi v měsíčních intervalech, přičemž po třetí injekci došlo k vymizení aktivity a další aplikace nebyla indikována. V případě myopické CNV byla na základě extrafoveolární lokalizace a jen mírně zhoršeného vidění aplikována jednotlivá dávka ranibizumabu, což vedlo k vymizení edému a regresi tloušťky ložiska. Pacientka byla dále sledována. V případě pacienta s choroidálním osteomem, v důsledku perzistence aktivity CNV a postupného zkracování intervalu mezi aplikacemi, je v příštím období plánován přechod na léčivo aflibercept, u kterého byla zaznamenána efektivita u pacientů nereagujících na bevacizumab nebo ranibizumab [17]. Ve všech případech byla použita standardní dávka léku určená i pro dospělé pacienty – ranibizumab (Lucentis, Novartis, 0,5 mg v 0,05 ml). Aplikace léčiva probíhala v celkové anestézii, pomocí jehly o průměru 30 gauge (0,3 mm) zavedené 3,5 až 4 mm posteriorně od limbu. Celkový průměrný počet aplikovaných injekcí u všech pacientů ve sledovacím období byl 3,4 (rozmezí 1 až 10). Ve 3 případech zánětlivé CNV, u nichž byla předpokládána infekční etiologie, byli pacienti před aplikací anti-VEGF léčby přeléčeni celkovou antibiotickou a kortikosteroidní terapií.
Mezi jednotlivými aplikacemi pacienti podstupovali pravidelná kontrolní ambulantní vyšetření, která zahrnovala zhodnocení NKZO, vyšetření štěrbinovou lampou, biomikroskopické vyšetření očního pozadí, případně fotografii očního pozadí a OCT vyšetření. Průměrná doba sledování činila 35 měsíců, s rozmezím od 5 do 97 měsíců.
VÝSLEDKY
Průměrná vstupní NKZO byla 0,277 decimal (logMAR 0,56), s rozmezím 0,014 až 1,0 decimal. Po ukončení terapie dosáhla průměrná finální NKZO hodnoty 0,65 decimal (logMAR 0,19), s rozmezím 0,133 až 1,0 decimal. Získaná zraková ostrost (ZO) byla průměrně 0,38 decimal. U žádného pacienta nebyl zaznamenán pokles ZO. Průměrné snížení centrální retinální tloušťky dosáhlo 94,9 µm. Ve všech případech byl pozorován pozitivní funkční nebo anatomický efekt. Po celou dobu sledování nebyl zaznamenán žádný nežádoucí oční ani systémový účinek spojený s aplikací ranibizumabu.
Bližší charakteristiku jednotlivých případů popisují tabulky. V Tabulce 1 jsou shrnuty následující epidemiologické a klinické údaje: pohlaví pacienta, věk v době diagnózy, iniciální a finální NKZO, počet intravitreálních injekcí. V Tabulce 2 jsou uvedeny morfologické údaje: lokalizace, etiologie a kategorie CNV, iniciální a finální centrální retinální tloušťka.
Obr. 6. Epidemiologické a klinické údaje pacientů 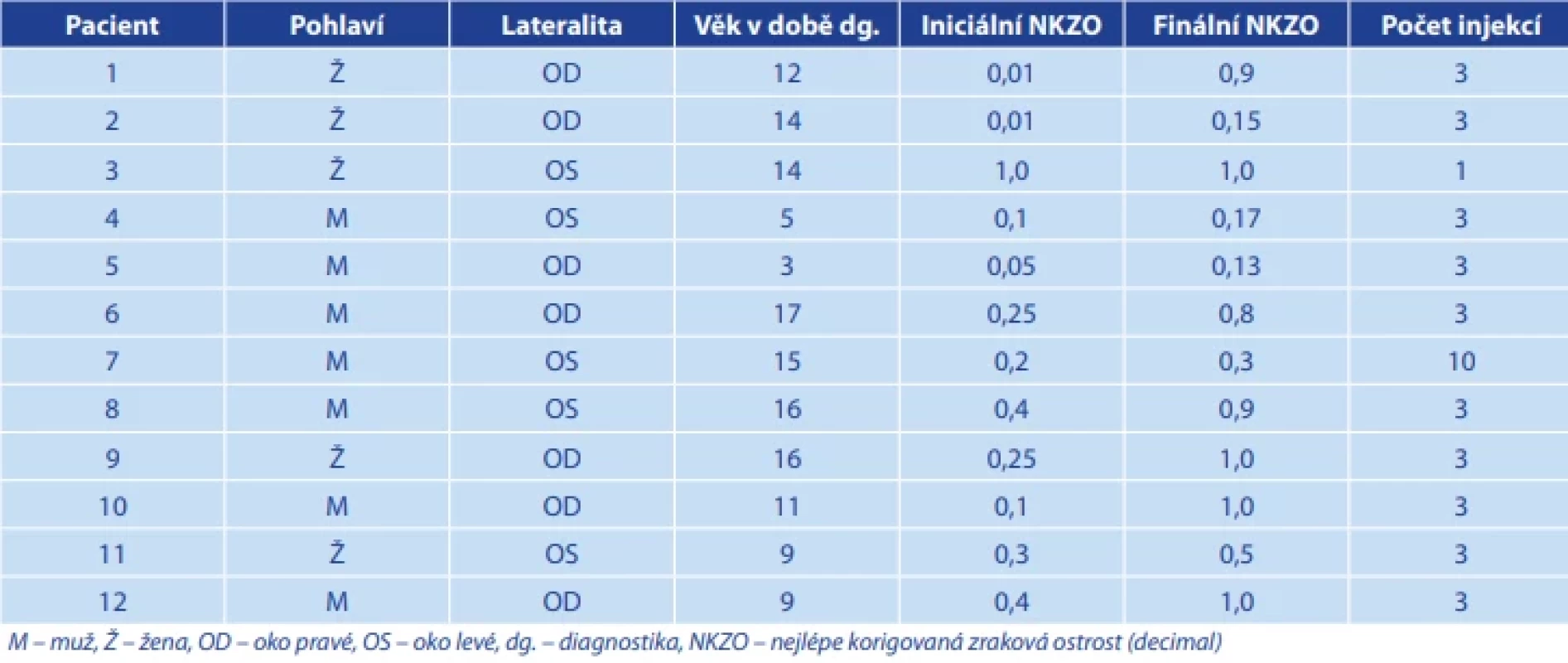
Obr. 7. Morfologické údaje CNV a změny CRT 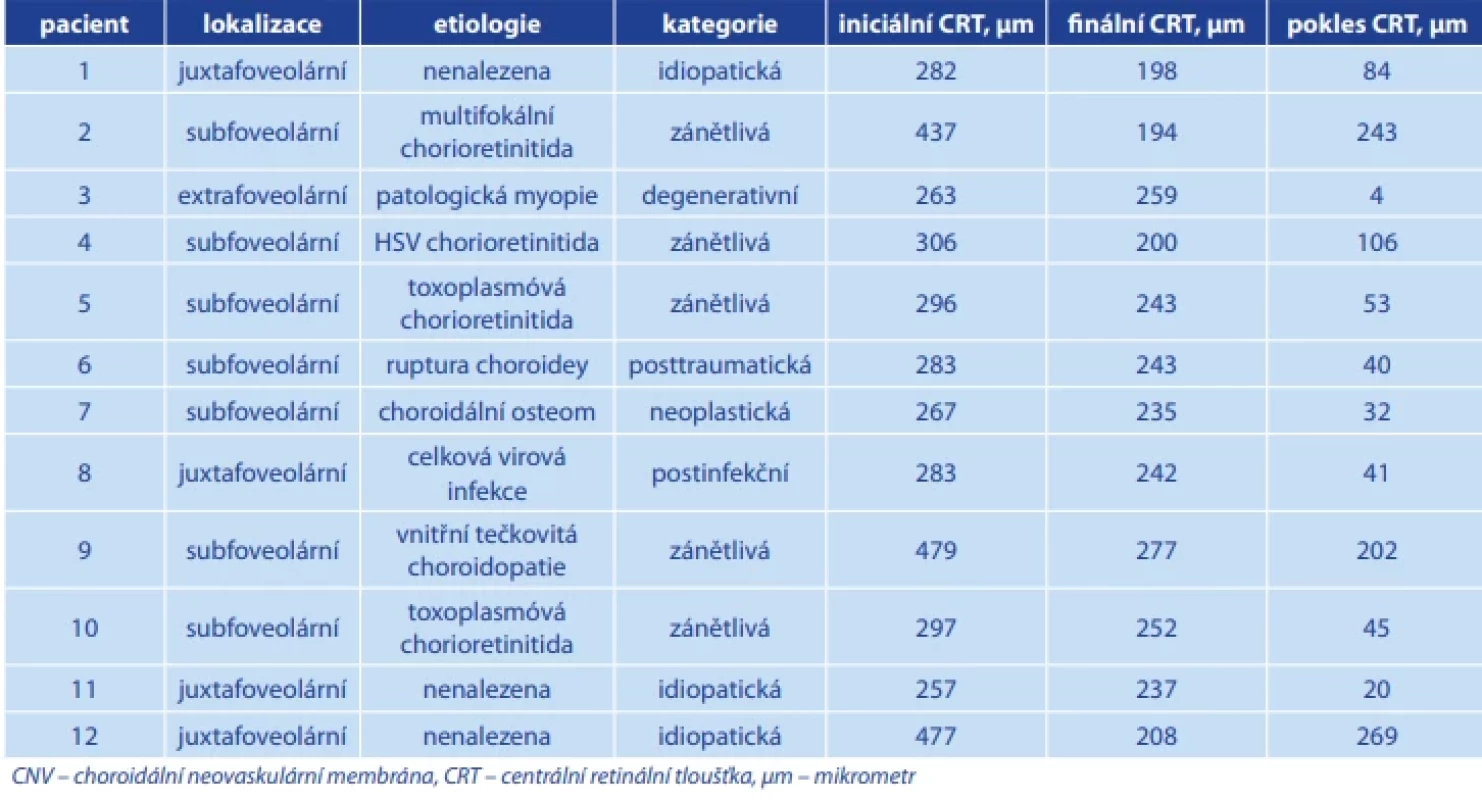
DISKUZE
Ačkoli je choroidální CNV v pediatrické populaci považována za vzácné onemocnění, její dopad z hlediska počtu prožitých let se zrakovým postižením je významný. Dosud bylo publikováno jen několik retrospektivních studií popisujících výskyt CNV u dětí. První a dosud jediná dostupná populační data o incidenci CNV byla zveřejněna v práci Moosajee et al. ze Spojeného království, která se týkala dětí ve věku 16 let nebo mladších, s roční incidencí 0,21 na 100 000 [7]. Znalosti o CNV u dospělých nelze přímo extrapolovat na pediatrickou populaci, neboť patogeneze a klinický průběh CNV u dětí se výrazně liší od těch u dospělých. Na rozdíl od vývoje CNV u starší populace, kdy je ve většině případů příčinou exsudativní VPMD, je u dětí často přítomno jiné základní oční onemocnění
Pokud jde o etiologii CNV u dětí, v odborné literatuře jsou uváděny různé nejčastější příčiny. Podle publikací autorů Moosajee, Rishi et al. je nejčastější příčinou zánětlivé onemocnění, zatímco ve studiích autorů Rego-Lorca, Padhi et al. je uváděna jako nejčastější příčina Bestova vitelliformní dystrofie [5–7,18,19]. V našem souboru pacientů byla nejčastější etiologie zánětlivá a infekční, která se vyskytovala v 50 % případů, následována idiopatickou etiologií. Idiopatická příčina byla zastoupena v našem souboru ve výši 25 %, což přibližně odpovídá podílu CNV s idiopatickým původem, jak je uváděno v jiných studiích [2,20,21].
Obecně lze konstatovat, že mezi nejčastější příčiny pediatrické CNV dle dostupných dat patří chorioretinitidy a Bestova vitelliformní dystrofie. V našem souboru jsme se však nesetkali s diagnózou hereditární retinální dystrofie, což může být důsledkem omezeného počtu pacientů. Průměrný věk při stanovení diagnózy pediatrické CNV se ve většině studií shoduje a pohybuje se mezi 11 a 12 lety.
V souladu s dosud publikovanými údaji byl v našem souboru pacientů zaznamenán výrazně vyšší výskyt subfoveolární formy CNV ve srovnání s formami juxtafoveolární a extrafoveolární [1,5,6,19,21]. Vyšší četnost klasické formy CNV oproti formám okultním či smíšeným odpovídá rovněž údajům uváděným v literatuře [19]. Tyto nálezy, stejně jako nižší počet aplikací ve srovnání s léčbou CNV u dospělé populace, pravděpodobně souvisejí s lepší funkční integritou RPE a absencí chronických degenerativních změn této vrstvy u dětských pacientů [21,22].
Terapeutický přístup u dětských pacientů s CNV je individuální a závisí na aktivitě, lokalizaci a přítomnosti dalších predisponujících onemocnění. Dále se může lišit podle zkušeností konkrétního pracoviště. Ve studii Zhang et al. je uvedeno, že efektivní terapií je 1 iniciální injekce anti-VEGF preparátu, následovaná režimem pro re nata [6]. V našem souboru pacientů bylo u 9 pacientů použito fixní aplikační schéma sestávající ze 3 injekcí v měsíčních intervalech. U myopické extrafoveolární CNV byla podána jednotlivá dávka s kompletním vymizením aktivity ložiska a v případě CNV spojené s choroidálním osteomem následovala, na základě perzistence aktivity CNV po fixní loadingové fázi, terapie v režimu pro re nata.
Průměrná NKZO při stanovení diagnózy v našem souboru činila logMAR 0,56, což je mírně vyšší hodnota, než uvádějí jiné studie. Například Rishi et al. uvádí logMAR 1,02 [5], Ranjan et al. průměrně logMAR 0,8 [23] a Rego - -Lorca et al. logMAR 0,57 [18]. Naopak Finn et al. uvádí průměrnou NKZO logMAR 0,53 při stanovení diagnózy [11]. Ve většině publikovaných studií došlo v průběhu sledování ke zlepšení ZO. Rishi et al. zaznamenali konečné zlepšení na logMAR 0,87, Ranjan et al. uvádí zlepšení z logMAR 0,8 na 0,4, zatímco Finn et al. dosáhli průměrné NKZO 0,37. V našem souboru došlo k významnému zlepšení NKZO z průměrného logMAR 0,56 na 0,19. Porovnáním výsledků z různých studií je patrná značná variabilita v klinických projevech a prognóze u pediatrických pacientů s CNV. Tato variabilita je pravděpodobně způsobena rozdíly v etiologii vzniku CNV a následných patofyziologických mechanismech, jež ovlivňují konečnou ZO a aktivitu onemocnění.
Zajímavým poznatkem je rozložení četnosti případů v našem souboru během sledovací periody. V letech 2015 a 2016 nebyla na naší klinice indikována žádná léčba injekcemi anti-VEGF pro CNV. Nejvyšší počet diagnostikovaných případů a indikací k terapii jsme zaznamenali v roce 2024 a v lednu a únoru tohoto roku. Nárůst incidence v posledních letech je pravděpodobně dán lepšími diagnostickými možnostmi a zvýšeným povědomím odborné veřejnosti o výskytu a možnostech terapie CNV u dětí. Některé studie naznačují, že může jít i o zvýšenou incidenci predisponujících onemocnění u této věkové skupiny [25].
Během sledování našich pacientů nebyly zaznamenány žádné nežádoucí oční příznaky. Je však třeba poznamenat, že dlouhodobé údaje o metabolismu anti-VEGF molekul u dětí dosud chybí. VEGF hraje klíčovou roli při normální angiogenezi, regulaci propustnosti cév a udržování funkcí hematoencefalické a hematoretinální bariéry. Není zatím jasné, jak sérové hladiny anti-VEGF ovlivňují vývoj dětského mozku [24]. Proto je nezbytné pečlivě sledovat dlouhodobé účinky inhibice těchto funkcí u dětské populace.
Vzhledem k vzácnosti pediatrické CNV nelze očekávat realizaci velkých randomizovaných kontrolovaných studií. Proto je pravděpodobné, že intravitreální anti-VEGF terapie bude nadále považována za indikaci mimo schválené použití (off-label) [20].
ZÁVĚR
CNV u dětí představuje velmi vzácné onemocnění, což souvisí s omezeným množstvím publikovaných dat, přičemž dosud neexistuje specifický terapeutický protokol pro léčbu tohoto onemocnění v dětské populaci. Bez adekvátní léčby však může CNV představovat významné ohrožení zraku. Terapie pediatrické CNV pomocí anti-VEGF preparátu se v našem souboru pacientů i v dosud publikovaných studiích jeví jako bezpečná a účinná metoda léčby této diagnózy u dětí.
Nicméně dosud neexistují dostupná data o dlouhodobých vedlejších účincích či metabolismu anti-VEGF molekul u dětí, které by se mohly odlišovat od dat získaných u dospělé populace. Proto je důležité se touto tématikou nadále systematicky zabývat a publikovat získaná klinická data.
Zdroje
1. Rego-Lorca D, Català-Mora J, López-de-Eguileta A, Díaz-Cascajosa J. Choroidal neovascularization in children: etiology, clinical characteristics and treatment outcomes. Arch Soc Esp Oftalmol (Engl Ed). 2024 Dec;99(12):534-539.
2. Cohen SY, Laroche A, Leguen Y, Soubrane G, Coscas GJ. Etiology of choroidal neovascularization in young patients. Ophthalmology. 1996 Aug;103(8):1241-1244.
3. Carneiro AM, Silva RM, Veludo MJ, et al. Ranibizumab treatment for choroidal neovascularization from causes other than age-related macular degeneration and pathological myopia. Ophthalmologica. 2011;225(2):81-88.
4. Goshorn EB, Hoover DL, Eller AW, Friberg TR, Jarrett WH, Sorr EM. Subretinal Neovascularization in Children and Adolescents. Journal of Pediatric Ophthalmology & Strabismus. 1995 May;32(3):178 - 782.
5. Rishi P, Bharat RPK, Rishi E, et al. Choroidal neovascularization in 111 eyes of children and adolescents. Int Ophthalmol. 2022 Jan;42(1):157-166.
6. Zhang T, Wang Y, Yan W, et al. Choroidal Neovascularization in Pediatric Patients: Analysis of Etiologic Factors, Clinical Characteristics and Treatment Outcomes. Front Med (Lausanne). 2021;8 : 735805.
7. Moosajee M, Abbouda A, Foot B, Bunce C, Moore AT, Acheson J. Active surveillance of choroidal neovascularisation in children: incidence, aetiology and management findings from a national study in the UK. Br J Ophthalmol. 2018 Apr;102(4):438-443.
8. Niederer R, Bar A, Al-Ani H, et al. Management of inflammatory choroidal neovascular membranes. Expert Review of Ophthalmology. 2021 Jan 2;16(1):47-60.
9. Rishi P, Gupta A, Rishi E, Shah BJ. Choroidal neovascularization in 36 eyes of children and adolescents. Eye (Lond). 2013 Oct;27(10):1158-1168.
10. Secrétan M, Sickenberg M, Zografos L, Piguet B. Morphometric characteristics of traumatic choroidal ruptures associated with neovascularization. Retina. 1998;18(1):62-666.
11. Choroidal osteoma in old age (an unexpectedly difficult diagnosis). Acta Ophthalmol. 2018 Dec;96(S261):67-68.
12. Aksoy Y, Çakir Y, Sevinçli S, Sönmez M, Ayata A. Choroidal osteoma in a preterm infant. Ind J Ophthalmol. 2018 Apr;66(4):583-585.
13. Fine HF, Ferrara DC, Ho IV, Takahashi B, Yannuzzi LA. Bilateral choroidal osteomas with polypoidal choroidal vasculopathy. Retin Cases Brief Rep. 2008;2(1):15-17.
14. Huang YM, Zhang L, Liang J, Yuan RD. Bilateral choroidal osteoma with unilateral polypoidal choroidal vasculopathy treated with conbercept. Int J Ophthalmol. 2020;13(6):1009-1012.
15. Gómez PD, Català-Mora J, López-de-Eguileta A, Díaz-Cascajosa J. Bilateral choroidal osteoma: long-term follow-up of secondary choroidal neovascularization in a child using antiangiogenic therapy. Japoos. 2024;Vol 28: Issue 2103869. doi:10.1016/j.jaapos.2024.103869
16. Zhang L, Ran QB, Lei CY, Zhang MX. Clinical features and therapeutic management of choroidal osteoma: A systematic review. Survey of Ophthalmology. 2023 Nov 1;68(6):1084-1092.
17. Saitta A, Nicolai M, Neri P, Reibaldi M, Giovannini A, Mariotti C. Rescue therapy with intravitreal aflibercept for choroidal neovascularization secondary to choroidal osteoma non-responder to intravitreal bevacizumab and ranibizumab. Int Ophthalmol. 2015 Jun;35(3):441-444.
18. Rego-Lorca D, Català-Mora J, López-de-Eguileta A, Díaz-Cascajosa J. Choroidal neovascularization in children: etiology, clinical characteristics and treatment outcomes. Archivos de la Sociedad Española de Oftalmología (English Edition). 2024 Dec;99(12):534-539.
19. Padhi TR, Anderson BJ, Abbey AM, et al. Choroidal neovascular membrane in paediatric patients: clinical characteristics and outcomes. Br J Ophthalmol. 2018 Sep;102(9):1232-1237.
20. Barth T, Zeman F, Helbig H, Oberacher-Velten I. Etiology and treatment of choroidal neovascularization in pediatric patients. Eur J Ophthalmol. 2016 Oct;26(5):388-393.
21. Kozak I, Mansour A, Diaz RI, et al. Outcomes of treatment of pediatric choroidal neovascularization with intravitreal antiangiogenic agents: the results of the KKESH International Collaborative Retina Study Group. Retina. 2014 Oct;34(10):2044-2052.
22. Kim R, Kim YC. Intravitreal ranibizumab injection for idiopathic choroidal neovascularization in children. Semin Ophthalmol. 2014 May;29(3):178-181.
23. Ranjan R, Salian R, Verghese S, et al. Pediatric choroidal neovascularization: Etiology and treatment outcomes with anti-vascular endothelial growth factors. Eur J Ophthalmol. 2022 Jul;32(4):2355-2367.
24. Sivaprasad S, Moore AT. Choroidal neovascularisation in children. Br J Ophthalmol. 2008 Apr;92(4):451-454.
25. Finn AP, Fujino D, Lum F, Rao P. Etiology, Treatment Patterns, and Outcomes for Choroidal Neovascularization in the Pediatric Population: An Intelligent Research in Sight (IRIS®) Registry Study. Ophthalmology Retina. 2022 Feb 1;6(2):130-138.
Štítky
Oftalmológia
Článok vyšiel v časopiseČeská a slovenská oftalmologie
Najčítanejšie tento týždeň
2026 Číslo 2- Pomocné látky v roztoku latanoprostu bez konzervačních látek vyvolávají zánětlivou odpověď a cytotoxicitu u imortalizovaných lidských HCE-2 epitelových buněk rohovky
- Konzervační látka polyquaternium-1 zvyšuje cytotoxicitu a zánět spojený s NF-kappaB u epitelových buněk lidské rohovky
- Dlouhodobé výsledky lokální léčby cyklosporinem A u těžkého syndromu suchého oka s 10letou dobou sledování
- Syndrom suchého oka
- Cyklosporin A v léčbě suchého oka − systematický přehled a metaanalýza
-
Všetky články tohto čísla
- Minimálně invazivní glaukomová chirurgie: iStent a Preserflo v léčbě primárního glaukomu s otevřeným úhlem. Přehled
- Choroidální neovaskulární membrána u dětí, dlouhodobé výsledky terapie anti-VEGF preparátem
- Preserflo MicroShunt verzus trabekulektómia: klinické výsledky 6-mesačnej retrospektívnej štúdie
- Metrické příčiny refrakčních vad oka
- Výsledky segmentálního sklerálního bucklingu s endoiluminátorem ve srovnání s konvenčním sklerálním bucklingem u primárního rhegmatogenního odchlípení sítnice: Srovnávací retrospektivní studie
- Subretinální triamcinolon acetonid a transpupilární termoterapie u ohraničeného choroidálního hemangiomu. Kazuistika
- Stoleté výročí vzniku Československé oftalmologické společnosti
- Česká a slovenská oftalmologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Minimálně invazivní glaukomová chirurgie: iStent a Preserflo v léčbě primárního glaukomu s otevřeným úhlem. Přehled
- Preserflo MicroShunt verzus trabekulektómia: klinické výsledky 6-mesačnej retrospektívnej štúdie
- Stoleté výročí vzniku Československé oftalmologické společnosti
- Subretinální triamcinolon acetonid a transpupilární termoterapie u ohraničeného choroidálního hemangiomu. Kazuistika
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



