-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Papilární léze prsu: Diagnostická úskalí a přehled jednotek
Papillary Breast Lesions: Diagnostic Challenges and Overview of Entities
Papillary breast lesions represent a morphologically and biologically diverse group of entities that include benign intraductal papillomas, papillomas with atypical ductal hyperplasia, with ductal or lobular carcinoma in situ, papillary ductal carcinoma in situ, encapsulated papillary carcinoma (with or without invasion), solid papillary carcinoma, and invasive papillary carcinoma. Accurate classification is often challenging particularly in core needle biopsies, and even in excision specimens can pose difficulties, especially for less experienced pathologists. This review summarizes the essential histological and immunohistochemical features of each lesion and highlights key diagnostic pitfalls and helpful clues in their differential diagnosis. While genetic testing is not routinely required for diagnostic purposes, recent studies have identified more or less distinct molecular alterations across the spectrum of papillary lesions. These findings may support future refinements in classification and understanding of these tumors.
Keywords:
papillary breast lesions – intraductal papilloma – encapsulated papillary carcinoma – solid papillary carcinoma
Autori: Zuzana Slobodová
Pôsobisko autorov: Ústav klinické a molekulární patologie, Lékařská fakulta Univerzity Palackého a Fakultní nemocnice Olomouc
Vyšlo v časopise: Čes.-slov. Patol., 61, 2025, No. 4, p. 178-189
Kategória: Přehledový článek
Súhrn
Papilární léze prsu představují morfologicky a biologicky různorodou skupinu jednotek, kam dle klasifikace WHO patří benigní intraduktální papilomy, papilomy s atypickou duktální hyperplazií, s duktálním či lobulárním karcinomem in situ, papilární duktální karcinom in situ, opouzdřený papilární karcinom s invazí nebo bez ní, solidní papilární karcinom a invazivní papilární karcinom. Správné zařazení jednotlivých lézí bývá obtížné zejména u core-cut biopsií, ale nejistotu může přinášet i vyhodnocení definitivních resekátů, především méně zkušeným patologům. Přehledový článek shrnuje základní histologické a imunohistochemické charakteristiky jednotlivých jednotek a upozorňuje na časté diagnostické pasti i užitečné orientační znaky. Ačkoliv genetické vyšetření nebývá pro diagnostiku nezbytné, recentní studie popisují méně či více specifické molekulární alterace napříč spektrem papilárních lézí. Tyto nálezy mohou v budoucnu přispět k zpřesnění klasifikace a hlubšímu porozumění biologie těchto nádorů.
Klíčová slova:
papilární léze prsu – intraduktální papilom – opouzdřený papilární karcinom – solidní papilární karcinom
* Adresa pro korespondenci:
MUDr. Zuzana Slobodová, Ph.D.
Ústav klinické a molekulární patologie LF UP a FN Olomouc Hněvotínská 3, 77900 Olomouc
tel.: 585 639 559
e-mail: zuzana.slobodova@fnol.czPapilární léze prsu, označované také jako papilární neoplazie, představují rozsáhlou skupinu nálezů, jejichž společným rysem je přítomnost papil s fibrovaskulárním stromatem pokrytým epitelem a myoepiteliální vrstvou nebo bez ní (1). Podle klasifikace WHO jde o morfologicky různorodé jednotky s odlišnou prognózou i terapeutickým přístupem. Zatímco benigní papilomy se vyskytují poměrně často a menší léze obvykle nenesou zvýšené riziko maligního přechodu (2), papilární karcinomy jsou méně časté a vyžadují závažnější terapeutické řešení, i přesto, že většina z nich má příznivou prognózu.
Největší diagnostickou výzvou je rozlišení těchto lézí, zejména při přítomnosti low-grade jaderných atypií. Interindividuální shoda v hodnocení a rozlišení benigních lézí, duktálního karcinomu in situ (DCIS) a invazivního karcinomu je často nedostatečná při použití samotného barvení hematoxylinem a eozinem (3). K přesné klasifikaci léze je klíčové zohlednit klinické údaje, zejména lokalizaci (centrální vs. periferní), velikost, počet lézí a případně i ohraničenost, přítomnost mikrokalcifikací či vaskularizaci.
Zásadním krokem v diagnostickém procesu je posouzení morfologického vzhledu, tedy identifikace papilárního uspořádání, ohraničení léze a známek invaze. Dále je třeba podrobně analyzovat buněčné složení, typy buněčných populací a jejich rozmístění, výskyt atypií, jaderných abnormalit a mitotickou aktivitu. Rozpoznání konkrétních buněčných populací bývá někdy obtížné a ve většině případů je nezbytné doplnit vyšetření o imunohistochemii. Klíčové je ověření přítomnosti či absence myoepiteliální vrstvy. K tomuto účelu se ve většině laboratoří používá kombinace alespoň dvou protilátek ze skupiny myoepiteliálních markerů např. p40, p63, calponin, CD10 a SMA a bazálních cytokeratinů např. CK5, CK5/6, CK14, 34βE12. Současně je důležité vyšetření hormonálních receptorů – estrogenového (ER) a progesteronového (PR) (4-7).
Interpretace imunohistochemie musí vždy vycházet z morfologického kontextu a zohlednit distribuci a imunoreaktivitu protilátek u jednotlivých populací, nutno však myslet na možnost variability, která je u některých protilátek vysoká. U některých jednotek je vhodné doplnit i vyšetření neuroendokrinních markerů jako jsou synaptofysin, chromogranin a INSM1 (8). Vzhledem k možným falešně negativním či pozitivním výsledkům imunohistochemického barvení pro myoepiteliální markery se doporučuje používat jejich kombinace (9).
Pro interpretaci jehlových biopsií a zajištění mezioborové komunikace je vhodné kromě klasického popisu zařadit nález také do systému klasifikace B1–B5 podle evropských doporučení (tab. 1). Tato klasifikace odráží biologické chování léze a je spojena se specifickými léčebnými doporučeními (10,11). Papilární léze detekované v punkčních biopsiích mohou být klasifikovány jako: B2 – benigní léze, B3 – léze s nejistým maligním potenciálem, B5a – in situ karcinom, B5b – invazivní karcinom. V dalším textu se podrobně zaměříme na jednotky s papilární morfologií, s důrazem na jejich rozpoznání a diferenciální diagnostiku v rámci doškolovacího charakteru tohoto článku (tab. 2).
Tabulka č. 1. Přehled interpretačních kategorií pro jehlové biopsie dle evropských doporučení.
Označení kategorie
Definice kategorie
Jednotky
B1
normální tkáň prsu / neinterpretovatelné
B2
benigní léze
fibrocystické změny, fibroadenom, sklerozující adenóza, duktektazie, nekróza tukové tkáně
B3
léze s nejistým maligním potenciálem
- sklerotické léze – radiální jizva, komplexní sklerozující léze, sklerotizovaný papilom
- papilární léze – bez malignity, ale nekompletně odstraněny
- lobulární intraepiteliální neoplazie
- atypická epiteliální proliferace duktálního typu
- „mucocele-like lesion“
- celulární fibroepiteliální léze
- vřetenobuněčné léze bez možnosti další klasifikace s ohledem na velikost vzorku
B4
podezření na malignitu
B5
B5a B5b B5c B5d
maligní
in situ karcinom invazivní karcinom prsu
nejednoznačné, zda jde o in situ či invazivní karcinom
jiné maligní procesy
Tabulka č. 2. Přehled papilárních lézí a jejich základních charakteristik.
Nenádorový epitel
Nádorový epitel
Fibrózní stroma papil
Myoepiteliální buňky papil
Myoepiteliální buňky periferie
ER/PR
IDP bez atypií
luminální a myoepiteliální
ne
širší, možná skleróza
pozitivní
pozitivní
pozitivní v luminální vrstvě
IDP s UDH
luminální a myoepiteliální, heterogenní v UDH
ne
širší, možná skleróza
pozitivní, v UDH disperzně
pozitivní
pozitivní luminální vrstvě, UDH disperzní pozitivita
IDP s myoepiteliální hyperplazií
luminální a myoepiteliální
ne
širší, možná skleróza
pozitivní, ložiskově pozitivní v hyperplazii
pozitivní
pozitivní v luminální vrstvě, negativní
v hyperplazii
IDP s ADH
luminální a myoepiteliální v papilách
monomorfní, do 3mm
širší i tenké
pozitivní v papilách, negativní v ADH
pozitivní
pozitivní difuzní
v neoplastické, disperzní v nenádorové populaci
IDP s DCIS
luminální a myoepiteliální v papilách
monomorfní, nad 3mm
širší i tenké
pozitivní v papilách, negativní v DCIS
pozitivní
pozitivní difuzní
v neoplastické, disperzní v nenádorové populaci
Papilární DCIS
Ne
monomorfní
tenké
ne
pozitivní
pozitivní silně difuzně
EPC
Ne
monomorfní kubický
tenké
ne
negativní v cca 80 %
pozitivní silně difuzně
SPC
Ne
monomorfní
tenké
ne / fokálně pozitivní
negativní v cca 80 %
pozitivní silně difuzně
IPC
Ne
monomorfní
tenké
ne
negativní
pozitivní silně difuzně
IDP – intraduktální papilom, UDH – běžná duktální hyperplazie, ADH – atypická duktální hyperplazie, DCIS – duktální karcinom in situ, EPC – enkapsulovaný papilární karcinom, SPC – solidní papilární karcinom, IPC – invazivní papilární karcinom, ER – estrogenový receptor, PR – progesteronový receptor
Intraduktální papilom (IDP) bez atypií
Intraduktální papilomy bez atypií, také označované jako NOS, jsou benigní léze prsu vznikající v lumen duktů. Jsou tvořeny keříčkovitě větvenými papilárními výběžky s osovým fibrovaskulárním stromatem, které je pokryto dvojvrstvým epitelem – vnitřní luminální a zevní myoepiteliální vrstvou (1). Většina těchto papilomů je lokalizována centrálně, kde často tvoří hmatné léze a mohou se klinicky projevit sekrecí z bradavky. Nejčastěji se objevují u starších žen v perimenopauze. Naopak periferní papilomy jsou vzácnější, bývají vícečetné, oboustranné, obvykle asymptomatické a jsou diagnostikovány převážně u mladších žen.
Histologicky je pro diagnózu zásadní zachování jak luminální, tak myoepiteliální vrstvy pokrývající arborizující fibrovaskulární stroma uvnitř dilatovaného duktu. Luminální epitel je tvořen buňkami kubického až cylindrického tvaru, bez mitotické aktivity nebo jen s ojedinělými mitózami. Morfologické změny mohou být pestré, epitel může vykazovat běžnou duktální hyperplazii, apokrinní, skvamózní, výjimečně mucinózní nebo chondroidní metaplazii, vzácně i kolagenní sferulózu. Myoepiteliální složka může být hyperplastická, a to ložiskově či difúzně (1,12,13).
U větších papilomů dochází snáze k infarktu v důsledku torze stopky a ke krvácení, spontánnímu i odběrovému. Častou změnou je sklerotizace a fibróza (obr. 1), která může vést ke ztrátě papilární architektury a vytvářet obraz pseudoinvaze, tedy přítomnosti abortivních duktů či štěrbin s epiteliální výstelkou ve fibrotickém stromatu. K odlišení od skutečné invaze napomáhá imunohistochemie myoepiteliálních markerů. Takové léze označujeme jako sklerotizující intraduktální papilomy. Sklerotizace se obvykle zintenzivňuje se stářím léze.
Pomocí imunohistochemie lze u papilomů detekovat zachovanou myoepiteliální vrstvu přiléhající ke stromatu, zatímco luminální vrstva bývá variabilní v závislosti na morfologických změnách. V přítomnosti apokrinní metaplazie může být myoepiteliální vrstva nerovnoměrná ale často kompletně chybí (14).
Papilární architektura může být méně zřejmá v případech běžné nebo floridní duktální hyperplazie (obr. 2). Typicky se v periferii objevují štěrbiny, buňky získávají vřetenitý charakter, vykazují proudění či syncyciální vzhled. Jsou heterogenní, překrývají se, mají nejasné hranice a jádra s nepravidelnostmi (např. zářezy, pseudoinkluze). Chybí však palisádování, monotónnost a low-grade jaderné atypie. Myoepiteliální buňky lze identifikovat pomocí markerů i ve formě menších až větších hnízd, zatímco ER bývá exprimován disperzně.
V rámci diferenciální diagnostiky je nezbytné odlišit solidní papilární karcinom, jehož vřetenité epitelie vykazují periferní palisádování, monotónní populaci s přítomností low-grade jaderných atypií. Nápadná může být, na rozdíl od papilomu, i mucinózní sekrece a redukce myoepitelií jak v papilách, tak v obvodu léze. Neuroendokrinní exprese je rovněž nápomocná v odlišení (13,15).
Kombinací floridní hyperplazie a sklerotizace zejména v okolí papilomu může docházet v okrajích papilomu k inkorporaci epiteliálních a glandulárních struktur do vaziva, což může také imitovat invazi. Tato situace může být komplikována i ložiskovou ztrátou myoepiteliální vrstvy, která však nebývá kompletně alterovaná. K přesnějšímu posouzení napomáhá imunohistochemické vyšetření s použitím ER a markerů myoepitelií, které typicky vykazují obraz hyperplazie, tj. promíchanou a disperzní distribuci obou populací. Navíc často chybí okolní DCIS a desmoplastická stromální reakce (15) (obr. 3). Podobný obraz může vzniknout i při zanesení epitelu do punkčního kanálu při biopsii, kdy reparativní proces přispívá k imitaci invaze.
Pokud je v papilomu přítomna výraznější myoepiteliální hyperplazie, může vzniknout podezření na adenomyoepiteliom. Ten se však vyznačuje relativně rovnoměrnou a výraznou přítomností myoepiteliální populace napříč celou lézí a jejich souvislým uspořádáním okolo tubulů, i když i zde je morfologická variabilita. Oproti tomu je hyperplazie u papilomů obvykle spíše ložisková (15, 16).
V případě výskytu chondroidní metaplazie může dojít k záměně za pleomorfní adenom nebo mukoepidermoidní karcinom, oboje vzácné léze prsu. Zatímco chondroidní metaplazie bývá v papilomech ložisková, u pleomorfního adenomu a mukoepidermoidního karcinomu postihuje rozsáhlejší oblast. K odlišení mukoepidermoidního karcinomu lze využít molekulárně genetické vyšetření, typicky bývá přítomna translokace t(11;19)(q21;p13) vedoucí ke genové fúzi CRTC1(MECT1)–MAML2 (1,16). Nutno však mít na paměti, že tyto genetické změny nemusí být v některých případech detekovatelné, např. u pleomorfních adenomů prsu se genetický profil známý ze slinných žláz prokazuje jen u části případů (16,17). Riziko upgradu benigních papilomů do karcinomu v definitivních excizích je velmi nízké – rozsáhlé metaanalýzy udávají míru pouze 5 % (18), v menších souborech jen 0,4 % (19). Oproti tomu přítomnost atypií v intraduktálním papilomu zvyšuje riziko upgradu na 20,4–36 % (18,19).
Obr. 1. Intraduktální papilom bez atypií s fokální sklerózou. A. Přehledový pohled na celý papilom (HαE, zvětšení 40x). B. Bližší pohled s evidentní papilární morfologií a částí změněnou sklerotizací (HαE, zvětšení 100x). C. Detail zaměřený na obě buněčné populace v papilomu se zachovalou obvodovou výstelkou duktu (HαE, zvětšení 200x). D. Calponin zobrazuje myoepiteliální vrstvu zachovalou také ve sklerotické části papilomu a v obvodové části (calponin, zvětšení 100x). E. CK5 je obdobný, zobrazuje myoepiteliální vrstvu papil, ve sklerotické části a obvodové části (CK5, zvětšení 100x). F. Estrogenový receptor (ER) značící luminální buňky papilárního povrchu, částečně zachovalé ve sklerotické části a také po obvodu duktu (ER, zvětšení 100x). 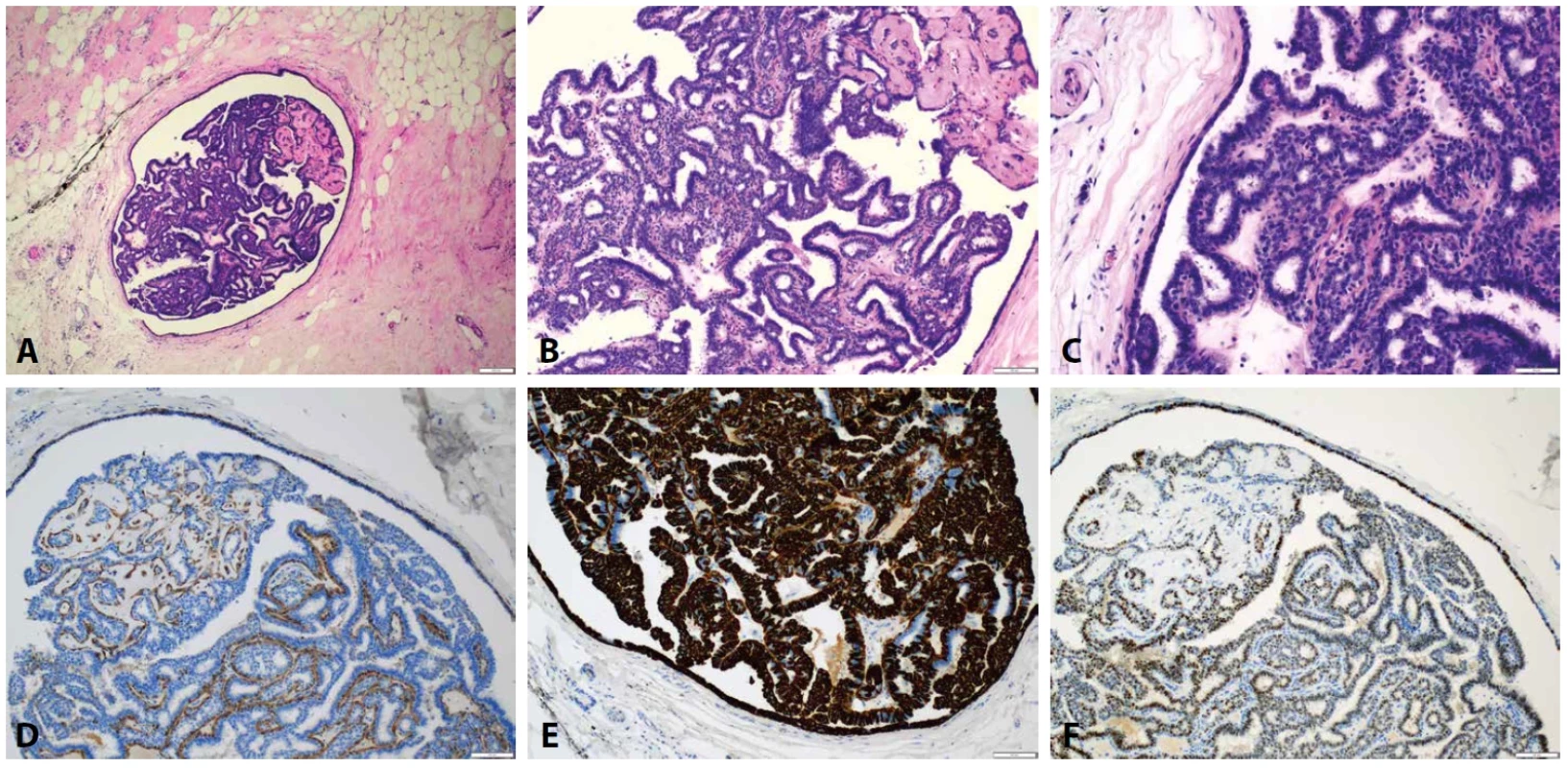
Intraduktální papilom s atypickou duktální hyperplazií (ADH), duktálním karcinomem in situ (DCIS) a dalšími prekurzorovými neoplastickými změnami
Intraduktální papilomy mohou být asociovány s atypickou duktální hyperplazií (ADH), která se vyznačuje uniformní buněčnou populací s cytologickými i architektonickými atypiemi typickými pro low-grade duktální neoplazii, přičemž rozsah postižení nepřesahuje 3 mm. Pokud je rozsah těchto atypií větší než 3 mm, léze je již klasifikována jako papilom s DCIS. U lézí se středními nebo těžkými jadernými atypiemi je diagnóza DCIS stanovena bez ohledu na rozsah (1). Starší literatura může ještě uvádět pojem „atypický papilom“, avšak ten není současnou aktuální WHO klasifikace z roku 2019 akceptován.
Z hlediska morfologie jsou neoplastické buňky stejné pro ADH i DCIS, oproti původní buněčné populaci papilomu jsou více uniformní, s hyperchromními jádry a typickými low-grade jadernými atypiemi (1,12). Pokud se benigní a neoplastická populace vyskytují současně, je v benigních částech zachována disperzní exprese ER a myoepiteliálních markerů, zatímco v oblastech ADH/DCIS myoepiteliální markery chybí a ER je exprimován difuzně (obr. 4). Obvodová bazální vrstva myoepitelií zůstává přítomna (1,12).
Relativně nedávno popsanou změnou v papilomu je atypická kolumnální změna/plochá atypie „columnar cell change with atypia“ /„flat epithelial atypia“, která bývá považována za prekurzorovou lézi pro ADH a DCIS. Imunohistochemický profil odpovídá ADH/DCIS s difuzní pozitivitou ER, absencí exprese CK5, nízkou expresí PR a vysokou expresí cyklinu D1 (20).
Další variantou neoplastické přeměny v rámci papilomů je ADH s neuroendokrinní diferenciací, která může progredovat do solidního papilárního karcinomu (SPC). Atypické buňky tvoří solidní proliferující oblasti s plasmocytoidní či vřetenitou morfologií, s přítomností jemných fibrovaskulárních papil. Typicky exprimují ER, vykazují ztrátu myoepiteliálních markerů a současně pozitivitu pro neuroendokrinní markery jako synaptofysin a chromogranin A (21,22).
Papilomy s atypickou lobulární hyperplazií jsou poměrně vzácné, avšak riziko jejich následné maligní transformace je srovnatelné s duktálními lézemi (1). Lobulární karcinom in situ nebo invazivní karcinom se může šířit nejen do lobulů a duktů, ale také do papilomů, někdy ve formě pagetoidního šíření. Nádorové buňky lobulárního typu typicky vykazují ztrátu E-cadherinu, absenci exprese myoepiteliálních markerů a pozitivitu pro ER. Diferenciální diagnostika zahrnuje papilomy s myoepiteliální proliferací (s pozitivními myoepiteliálními markery), papilomy s DCIS (se zachovalou expresí E-cadherinu) a in situ papilární karcinomy s dimorfní buněčnou populací (viz níže) (23).
U vzorků získaných jehlovou biopsií je třeba mít na paměti, že přítomnost ADH nebo DCIS v papilomu může ve finálním vzorku znamenat vyšší riziko upgradu do invazivního karcinomu. Toto riziko se v jednotlivých studiích značně liší, pohybuje se mezi 20,4 % (19), 36 % v metaanalýzách (18) a dokonce až 51 % v některých souborech (24). Tento fakt je jedním z důvodů, proč jsou papilární léze s atypiemi řazeny do kategorie B3 dle evropského klasifikačního systému.
Obr. 2. Intraduktální papilom s oblastí běžné duktální hyperplazie (UDH). A. Přehledový pohled na papilom s částečně zachovalou papilární architektonikou a solidnější oblastí UDH (HαE, zvětšení 100x). B. Detail na solidnější okrsek UDH s jadernou variabilitou (HαE, zvětšení 200x). C. CK5 značí zmnožené myoepitelie v hyperplazii a jejich bazální zachování v okrajově zachycených papilách a v obvodové části duktu (CK5, zvětšení 100x). D. Estrogenový receptor (ER) vykazuje disperzní distribucí v UDH a luminální expresi v obvodu duktu (ER, zvětšení 100x). 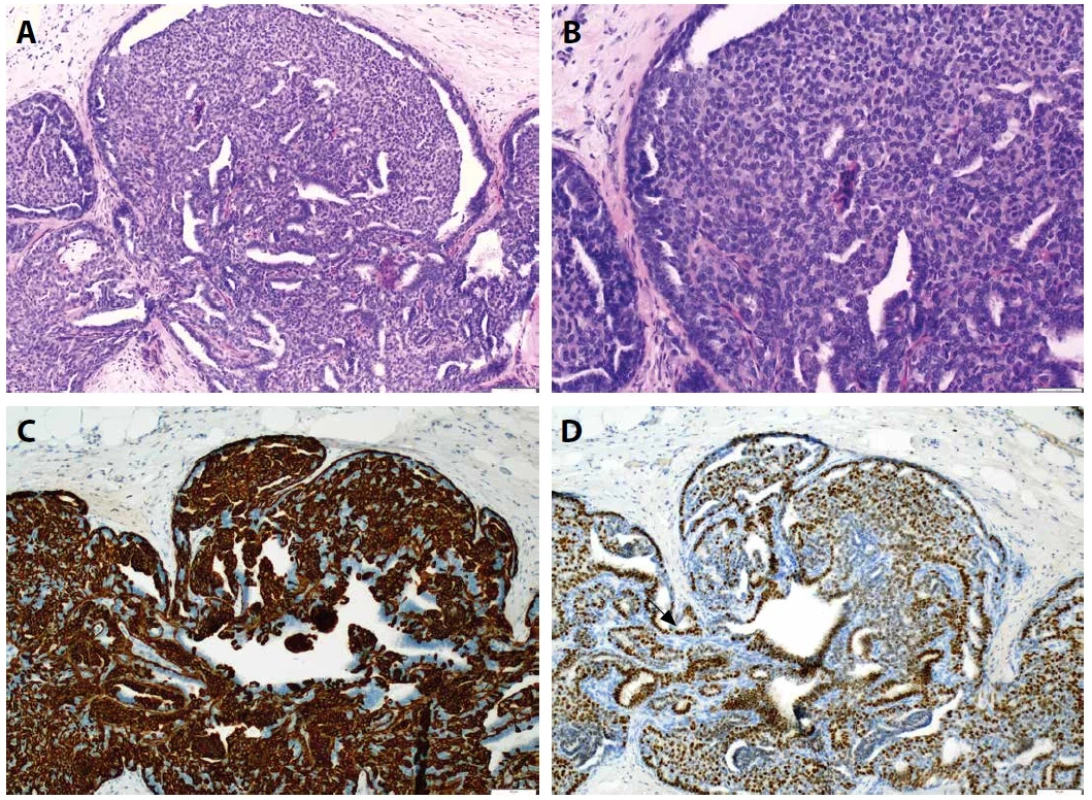
Obr. 3. Intraduktální papilom s oblastí pseudoinvaze. A. V přehledu papilom zachycující v oblasti fibrózní stěny duktu drobné tubuly budící dojem invazivního karcinomu (HαE, zvětšení 40x). B. Bližší pohled na zavzaté drobné tubulární struktury nepřesahující do přilehlé tukové tkáně, jsou limitované na nejbližší okolí (HαE, zvětšení 100x). C. Bazální vrstva papilomu, obvod duktu a stejně tak drobné tubuly ve stěně papilomu jsou lemované myoepiteliální vrstvou pozitivní v p63 (p63, zvětšení 100x). D Estrogenový receptor (ER) vykresluje luminální epitelie papilomu, v zavzatých tubulech jsou patrny pouze jednotlivé buňky ve variabilní intenzitě (ER, zvětšení 100x). 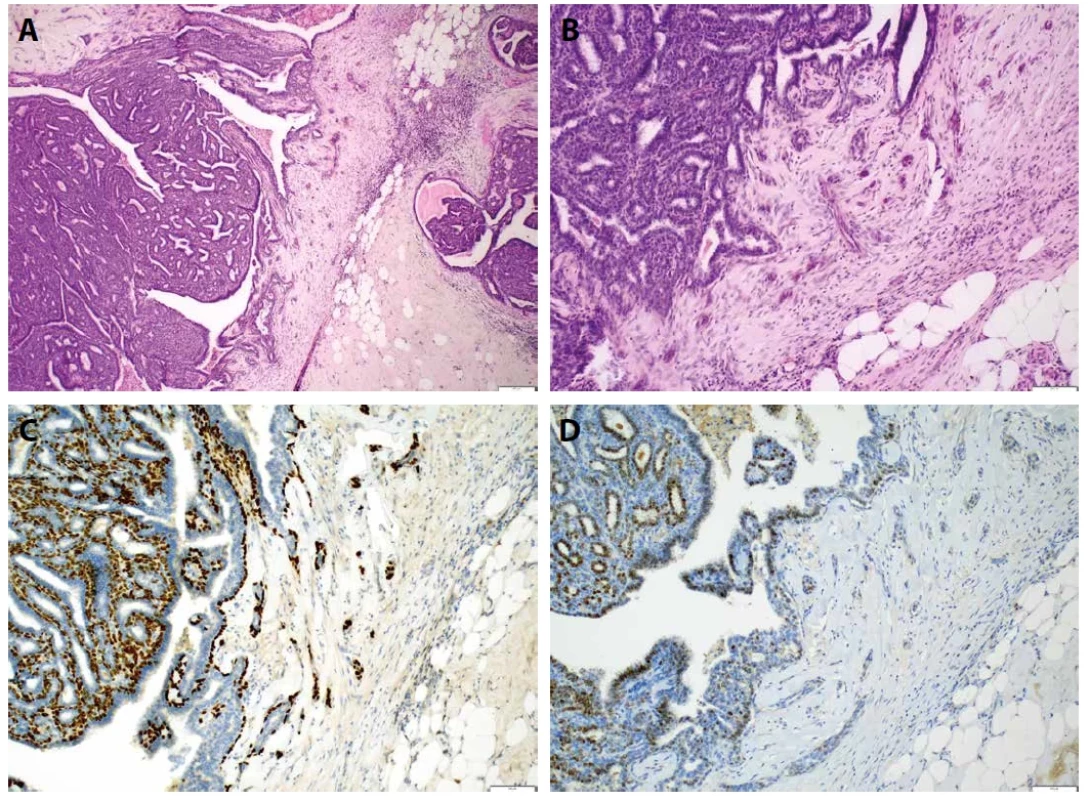
Papilární duktální karcinom in situ (DCIS)
Papilární DCIS představuje strukturální podtyp duktálního karcinomu in situ, v němž jsou dukty vyplněny fibrovaskulárními výběžky pokrytými dysplastickým epitelem bez přítomnosti myoepiteliální vrstvy na papilách, přičemž po obvodu duktu zůstává myoepiteliální vrstva zachována (1) (obr. 5). Obecně je DCIS segmentálně se šířící onemocnění, které může být lokalizováno jak centrálně, tak periferně, přičemž projevy onemocnění závisí právě na jeho umístění. Při retroareolární lokalizaci se může projevit výtokem z bradavky, ve většině případů je však papilární DCIS diagnostikován náhodně v rámci screeningového mamografického nebo ultrazvukového vyšetření (12). Často se vyskytuje současně s enkapsulovaným papilárním karcinomem (EPC) (1).
Dukty u tohoto typu léze vykazují různý stupeň dilatace a obsahují vícečetné papilární výběžky. Ty jsou zpravidla jemné, přičemž stromální fibróza není tak výrazná jako u intraduktálních papilomů (13). Morfologický obraz DCIS je variabilní, papilární růst bývá často kombinován s dalšími růstovými vzorci, čistě papilární struktura je relativně vzácná (12). Neoplastické epitelové buňky mohou navíc proliferací vyplnit prostory mezi jednotlivými papilami, což může vést k překrytí původní papilární architektury. Tyto nádorové epitelie bývají monomorfní, cylindrické, často s přítomnou stratifikací a nejčastěji odpovídají nízkému nebo střednímu stupni jaderné atypie (low až intermediální nukleární grade); vysoký stupeň atypie (high grade) se vyskytuje méně často (25).
Přestože většina papilárních DCIS vykazuje monomorfní charakter, existují i tzv. dimorfní varianty, u kterých se vyskytují větší bazální světlé buňky napodobující myoepitelie, označované jako globoidní buňky. Tyto buňky mají neoplastickou povahu, jejich jádra odpovídají neoplastickému epitelu, avšak jejich profil se odlišuje od myoepitelií. Jsou negativní na p63, calponin, CD10, S-100, GCDFP15 a bazální cytokeratiny CK5, ale vykazují pozitivitu luminálních cytokeratinů CK8/18 a ER. Naopak jsou negativní na PR, HER2 a p53 (26,27).
Myoepiteliální vrstva zůstává intaktní na periferii léze, zatímco v oblasti papil typicky chybí. Některé studie však popisují výskyt ojedinělých, disperzně uložených myoepitelií i na povrchu papil. Podle některých autorů může tento parciální zbytek myoepitelií přetrvávat v případech, kdy léze vznikla přeměnou z původního papilomu, jenž byl zcela prostoupen neoplastickými buňkami DCIS, tedy v případech tzv. papilomu s DCIS (viz předchozí kapitola). Naopak u primárně vzniklého (de novo) papilárního DCIS by se tyto disperzní myoepiteliální buňky na papilách vyskytovat neměly (28). Biologické chování papilárního DCIS odpovídá jiným typům DCIS a je primárně závislé na jaderném gradingu (25).
Obr. 4. Intraduktální papilom s oblastí ADH/DCIS. A. V přehledu zachycen papilom se splýváním papil s monomorfní oblastí ADH/DCIS, v okraji zachovalá částečně skerotizovaná papilární struktura (HαE, zvětšení 40x). B. Při bližším pohledu je monomorfní populace ADH/DCIS tvořena většími buňkami oproti okrajově zachycené papile s cylindrickým epitelem (HαE, zvětšení 100x). C. V detailu monomorfní neoplastická populace s pravidelnou distribucí buněk a mírnými jadernými atypiemi (HαE, zvětšení 200x). D. Absence calponinu v oblasti ADH/DCIS (calponin, zvětšení 100x). E. Obdobný obraz se ztrátou CK5 v neoplastické populaci (CK5, zvětšení 100x). F. Difuzní pozitivita ER v neoplastické populaci (ER, zvětšení 100x). 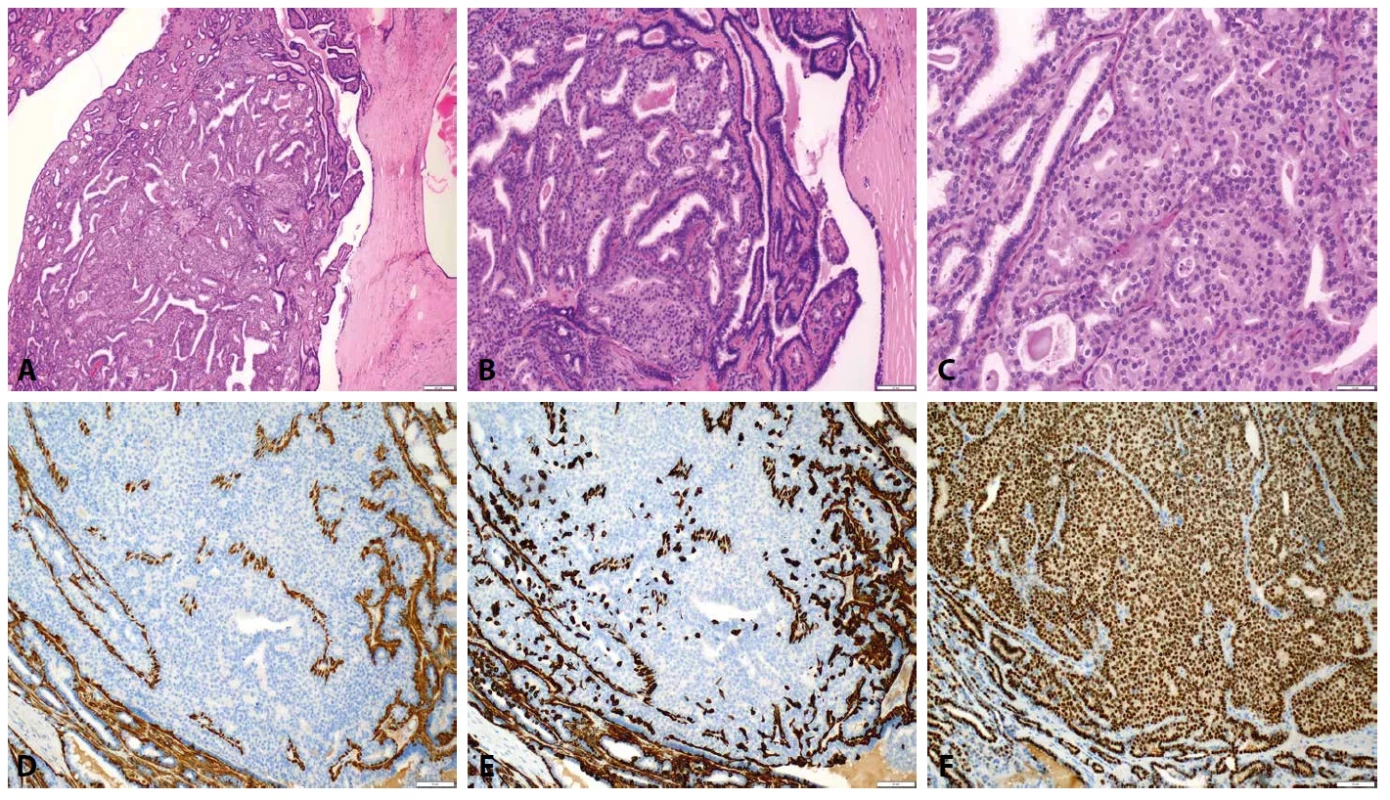
Obr. 5. Papilární DCIS a mikropapilární DCIS. A. V přehledu papilárně konfigurovaný DCIS (HαE, zvětšení 40x). B. Myoepitelie pozitivní v p63 jsou zachovalé prakticky pouze v obvodu duktu, v papilárních strukturách je patrna absence (p63, zvětšení 100x). C. ER je difuzně pozitivní v neoplastické populaci (ER, zvětšení 100x). D. Pro porovnání morfologie mikropapilární DCIS s absencí osových stromálních papil (HαE, zvětšení 100x). 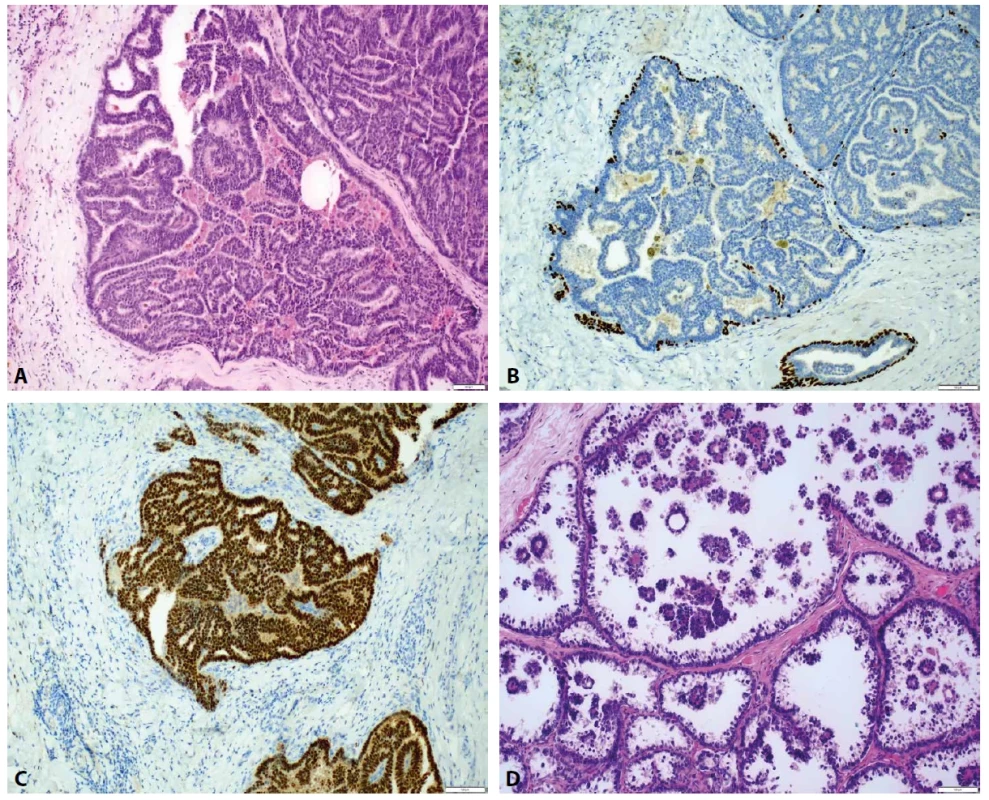
Obr. 6. Enkapsulovaný papilární karcinom (EPC). A. Část EPC s obvodovou výstelkou (HαE, zvětšení 100x). B. V přehledu EPC s invazí ve fibrózní kapsule ve formě invazivního karcinomu NST (HαE, zvětšení 40x). C. V bližším pohledu zachycen přechod EPC a invazivní komponenty (HαE, zvětšení 100x). D. Kompletní absence p63 myoepitelií v papilární i obvodové části EPC (p63, zvětšení 100x). E. Obdobný nález myoepiteliální absence v calponinu (calponin, zvětšení 100x). F. Difuzní exprese ER ve všech částech EPC (ER, zvětšení 100x). 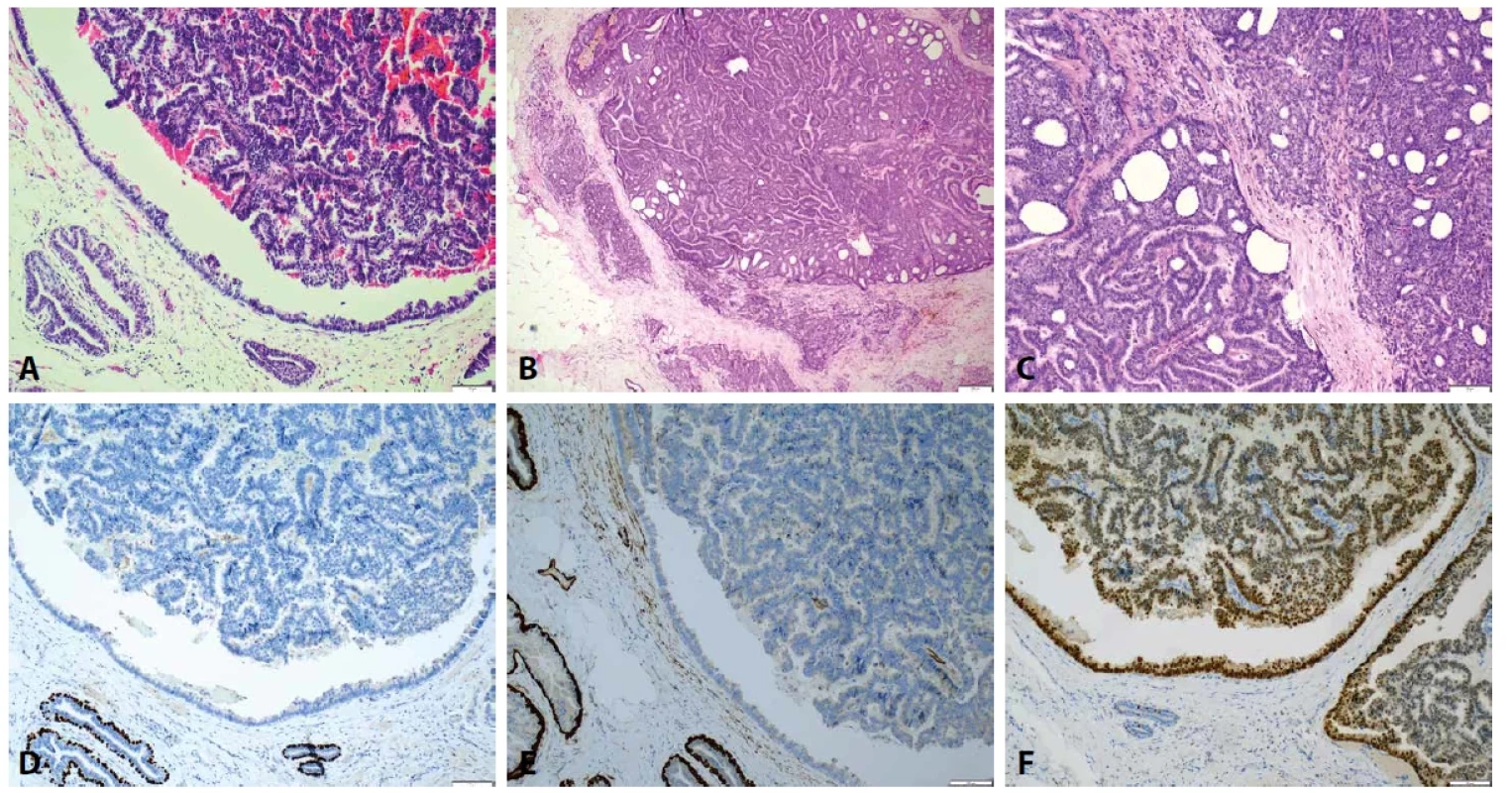
Opouzdřený (enkapsulovaný) papilární karcinom (EPC)
Enkapsulovaný papilární karcinom, dříve označovaný jako intracystický papilární karcinom, se vyznačuje cystickým prostorem s fibrovaskulárními papilami pokrytými neoplastickým epitelem nízkého až středního jaderného stupně. Typicky chybí myoepiteliální vrstva jak na povrchu papil, tak na periferii cysty, což se projevuje absencí exprese bazálních cytokeratinů. EPC je považován za neinvazivní lézi a je klasifikován jako Tis (1,29) (obr. 6).
Na rozdíl od intraduktálních papilomů (IDP) bývá EPC větší, často s výraznější cystickou i solidní komponentou. Méně často se objevuje jako multilokulární nebo tvořený několika uzlovitými strukturami. Pokud je uložen retroareolárně, bývá často hmatný. Vzhledem k jasně ohraničenému růstu a velikosti může klinicky imitovat fibroadenom (30). Nádor mívá expanzivní růst s hladkým periferním ohraničením tvořeným širokým fibrózním pouzdrem, z něhož vyrůstají větvené fibrovaskulární papily. Povrchový epitel bývá monomorfní, převážně cylindrický nebo kubický, i když se mohou vyskytovat oblasti s komplexní architekturou, např. stratifikace, solidní pruhy, kribriformní či mikropapilární formace a tzv. románské oblouky. Mezi méně časté morfologické varianty patří transicionální nebo vřetenobuněčný vzhled připomínající uroteliální karcinom, případně metaplastické skvamózní změny. Solidní či kribriformní komponenta může někdy zcela překrýt papilární strukturu. Čistě apokrinní typ EPC je velmi vzácný, v literatuře je považován za kontroverzní entitu (31,32).
Jádra nádorových buněk vykazují atypie nízkého až středního stupně. V nedávné době byla popsána i varianta s high-grade jadernými atypiemi, která se častěji vyskytuje u mladších žen a bývá spojena s vyšším rizikem invaze a metastáz do lymfatických uzlin (33). Podle různých studií představuje 2–14 % případů (34). Fibrózní pouzdro bývá silné, s výraznější depozicí kolagenu IV (13), i když se jeho tloušťka může lišit.
V okolních duktech EPC se u části pacientek vyskytují léze odpovídající low-grade DCIS. Pokud dojde k přestupu přes pouzdro, jedná se o invazivní karcinom, obvykle NST nebo mucinózního typu, přičemž papilární morfologie bývá vzácná (9). Určit přítomnost invaze však může být obtížné, zejména pokud jsou nádorové epiteliální buňky zavzaty do pouzdra. Tyto buňky se mohou do stromatu dostat arteficiálně během biopsie. Pokud je v okolí přítomna hemoragie, jizvení nebo granulomatózní reakce, je odlišení většinou snadné. Naopak přesun epitelu do stromatu bez těchto znaků a bez desmoplastické reakce je vzácný (13). Tyto případy mohou být nesprávně označeny jako mikroinvaze, avšak pravá invaze je definována přestupem nádorových struktur přes kapsulu s výskytem desmoplazie a jasnými buněčnými konturami, které nejsou typické po zavzaté/inkorporované buňky (15).
EPC typicky vykazuje silnou pozitivitu ER, ale exprese PR bývá variabilní. Proliferační aktivita měřená pomocí Ki67 je nízká, což odpovídá indolentnímu chování nádoru. HER2 bývá obvykle negativní, pozitivita se vyskytuje v maximálně 12,5 % případů (35). Vzácná apokrinní forma EPC a high-grade EPC často vykazují triple negativní fenotyp (ER–/PR–/HER2–), přičemž u některých případů byl zaznamenán basal-like subtyp s vysokou proliferační aktivitou (35).
V rámci diferenciální diagnostiky je třeba odlišit IDP, které postrádají cytologické atypie, mitózy jsou u nich vzácné a zachovává se myoepiteliální vrstva. Papilární DCIS se na rozdíl od EPC vyznačuje buněčnou hyperplazií s atypiemi a přítomností myoepiteliální vrstvy po obvodu duktu (34). Solidní papilární karcinom (SPC) lze odlišit na základě morfologie, kdy typicky převažuje nodularita, palisádování, intracelulární tvorba hlenu, neuroendokrinní diferenciace a chybí fibrózní kapsula. V úvahu přichází také solidní varianta lobulárního karcinomu, která může EPC napodobovat ostře ohraničeným růstem a částečně fibrózní pseudokapsulou s centrální fibrotizací. K přesnému odlišení napomáhá lobulární morfologie nádorových buněk a ztráta exprese E-cadherinu (15).
Obr. 7. Solidní papilární karcinom (SPC). A. V přehledu solidní formace SPC s jemnými papilami (HαE, zvětšení 40x). B. Detail na monomorfní neoplastickou populaci s rozetovitými formacemi oddělenými jemným stromatem fibrózních papil (HαE, zvětšení 200x). C. Invazivní SPC se zachycením invaze v tukové tkáni v podobě „skládačky puzzle“ (horní část obrázku) a mikropapilární morfologií (dolní část obrázku) (HαE, zvětšení 40x). D. Kompletní absence CK5 v neinvazivní oblasti SPC (CK5, zvětšení 100x). E. Difuzní exprese ER v neinvazivní oblasti SPC (ER, zvětšení 100x). F. Přítomna je difuzní exprese neuroendokrinních márkrů, zde zachycen chromogranin A (chromogranin A, zvětšení 100x). 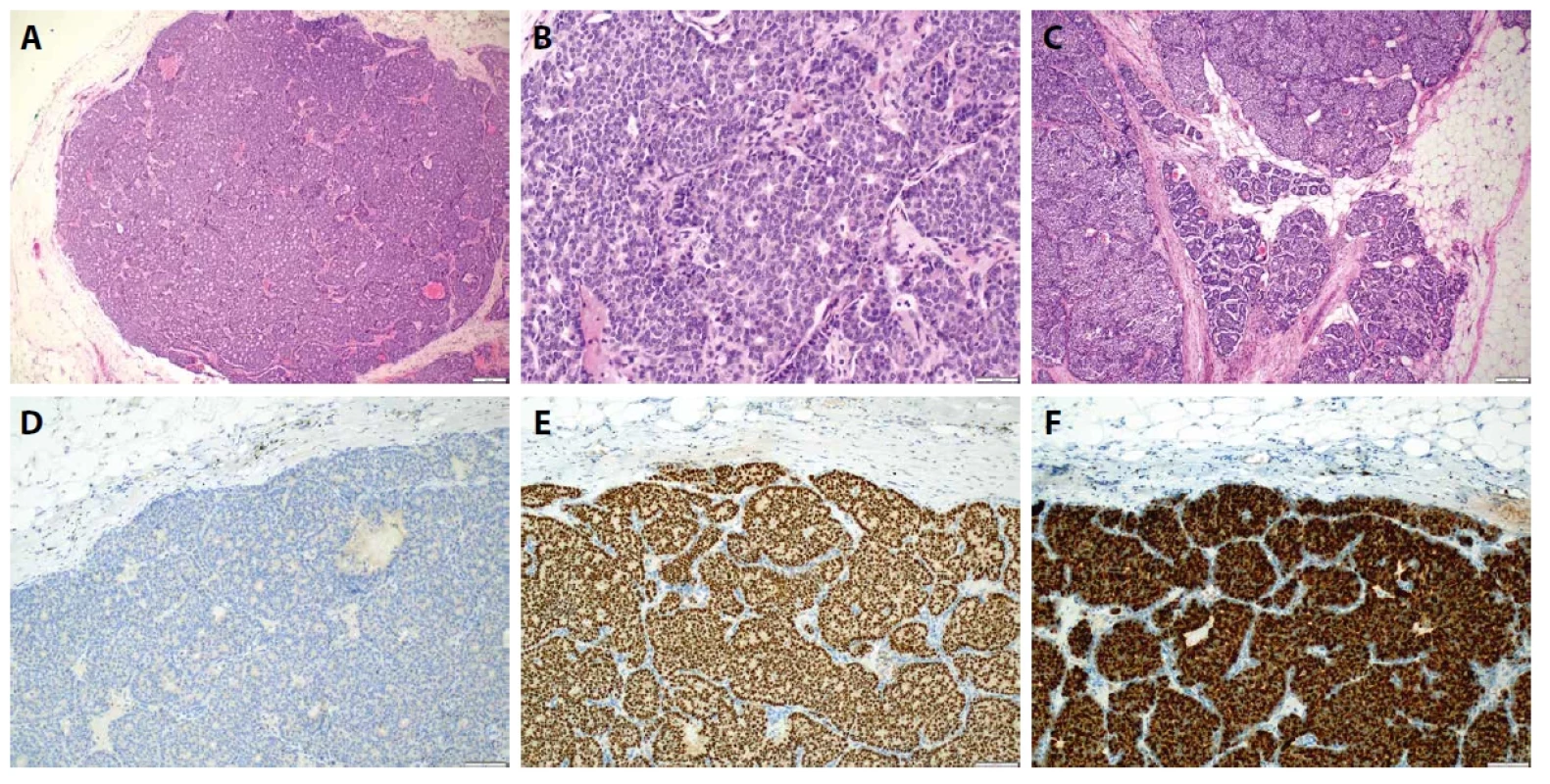
Obr. 8. Invazivní papilární karcinom. A. V přehledu zachyceny tenčí stromální papilární formace s jednoduchým větvením zde bez výraznější arborizace (HαE, zvětšení 40x). B. Detail na epiteliální povrch papil s kubickými až nízce cylindrickými epiteliemi v jedné vrstvě (HαE, zvětšení 200x). C. Kompletní absence myoepitelií v CK5 a negativita nádorové populace (CK5, zvětšení 100x). D. ER je exprimován difuzně v nádorových buňkách (ER, zvětšení 100x). 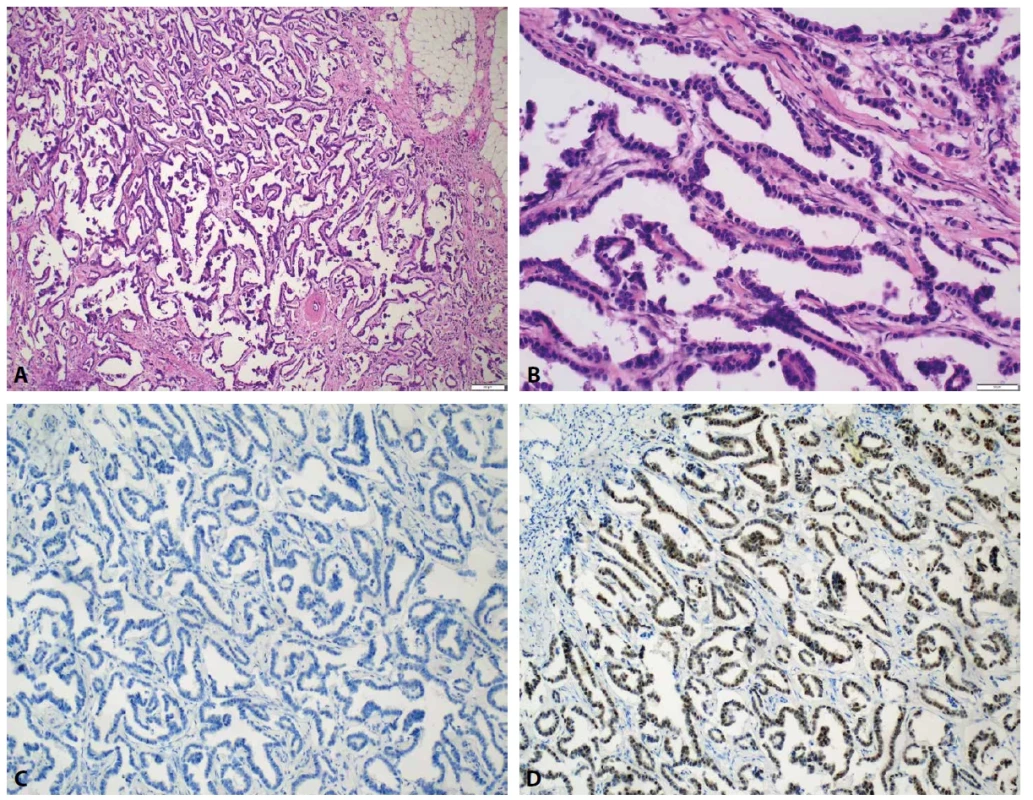
Solidní papilární karcinom (SPC)
Solidní papilární karcinom je papilární karcinom se solidním typem růstu, s přítomností jemných fibrovaskulárních výběžků. Často se u něj vyskytuje neuroendokrinní diferenciace a nádor se vyznačuje spíše indolentním chováním. Incidence je nízká, činí něco málo přes 1 % nádorů prsu, a postihuje převážně ženy v pozdní menopauze. Obvykle se projevuje jako hmatný tumor lokalizovaný retroareolárně s možnou krvavou sekrecí, i když se může objevit i v jiných částech prsu (1). Tumory jsou často dobře ohraničené s hladkými konturami a nodulární konfigurací, přičemž je třeba rozlišit mezi in situ a invazivní formou. Histologicky jsou noduly v rámci SPC in situ relativně velké a často těsně přiléhají k sobě s vmezeřeným fibrózním stromatem. Uvnitř nodulů se nachází jemné fibrovaskulární papily, které obvykle nemají výraznější fibrotizaci, což může pomoci s odlišením od benigních papilomů (15). Tyto papily oddělují solidní oblasti tvořené monomorfními nádorovými buňkami s nízkým až středním jaderným pleomorfismem. Jádra jsou kulatá až oválná, s drobnými jadérky, cytoplazma je světle eozinofilní a jemně granulární, místy s hlenovými vakuolami (36,12). Nádorové buňky mohou být kulaté, oválné či vřetenité a někdy tvoří pseudorozety, ale častější je periferní palisádování (12).
Většina SPC postrádá částečně nebo zcela myoepiteliální vrstvu po obvodu, což však nevylučuje, že se jedná o lézi in situ (37) (obr. 7). Pokud je obvodová vrstva myoepitelií zachovalá, lze považovat nález za DCIS, který se často vyskytuje v okolí SPC. Na rozdíl od EPC nebývá SPC opouzdřený, může se ale vyskytovat nekompletní či tenká pseudokapsula (15).
Floridní duktální hyperplazii lze odlišit zejména díky nepřítomnosti fibroepiteliálních papil, zachovalé myoepiteliální vrstvě, chybění rozet a neuroendokrinní diferenciace či produkce mucinu. Podobně i IDP s rozsáhlejší běžnou duktální hyperplazií (UDH), může představovat diferenciálně diagnostickou výzvu, avšak papily zde bývají evidentní (38).
Invazivní forma SPC je méně častá než forma in situ a při přítomnosti invaze bývá růst ve formě malých hnízd či čepů solidní papilární morfologie s roztřepenými, nepravidelnými okraji, často ve formě„skládačky puzzle“. Typická je indukce desmoplastické reakce nebo invaze do tukové tkáně. V takových případech je nádor označován jako invazivní SPC (1,12). Vzhledem k absenci myoepitelií v obou složkách není jejich přítomnost spolehlivým kritériem pro odlišení invaze. Snadněji je invaze rozpoznatelná při přítomnosti mucinózní diferenciace nebo invazivního karcinomu NST (1,12), méně často i jiných typů – lobulárního, tubulárního, kribriformního karcinomu nebo jejich kombinací (39). Chování a prognóza závisí na typu invazivní složky. Při přítomnosti invaze bývají nádorová jádra obvykle vyššího stupně (40). Imunohistochemicky vykazují in situ i invazivní SPC pozitivitu ER a PR, HER2 bývá negativní a proliferační index Ki-67 je nízký až střední. Většina nádorů odpovídá luminal A typu. Neuroendokrinní diferenciace je přítomna přibližně v 70 % případů, prokazatelná pomocí markerů jako synaptofysin, chromogranin a INSM1 (41,15). Neuroendokrinní znaky se mohou vyskytovat i v invazivní složce, zejména u mucinózního karcinomu hypercelulární varianty (Capella B typ) (1).
Do diferenciální diagnostiky spadají lobulární neoplazie, včetně rozsáhlého LCIS nebo invazivního lobulárního karcinomu se solidně papilárním růstem (42,43). Odlišení je možné na základě morfologie lobulárních buněk, ztráty buněčné kohezivity a negativity E-cadherinu.
Invazivní papilární karcinom (IPC)
Invazivní papilární karcinom představuje vzácný subtyp invazivního karcinomu prsu, charakterizovaný přítomností fibrovaskulárního stromatu obklopeného neoplastickým epitelem bez myoepiteliální vrstvy (obr. 8). Papilární morfologie musí dominovat alespoň v 90 % nádorové hmoty (1). Tento typ nádoru tvoří přibližně 0,5 % všech invazivních karcinomů, přičemž přesný podíl se liší podle jednotlivých studií. Je důležité podotknout, že invazivní karcinom vznikající z opouzdřeného papilárního karcinomu nebo solidního papilárního karcinomu bez přítomnosti papilární morfologie se jako invazivní papilární karcinom neklasifikuje (1). Infiltrativní růst je obdobný jako u jiných typů invazivních karcinomů a určujícím znakem je výrazná papilární architektura invazivních struktur.
Nádor se častěji vyskytuje u postmenopauzálních žen, má tendenci k větší velikosti, bývá nízkého gradu, diagnostikován v časnějším klinickém stadiu, méně často metastazuje do uzlin, vykazuje hormonální receptorovou pozitivitu a nízkou expresi HER2 (44, 45). Prognóza tohoto typu karcinomu je příznivější než u invazivního karcinomu NST, přesto však závisí na stejných faktorech jako jsou histologický grade, patologické stádium a molekulární subtyp (45).
Epitel vystýlající papily může mít variabilní morfologii, architektonicky mohou být kromě klasických papil přítomny i tubulární struktury. Jádra buněk jsou většinou nízkého gradu, mitotická aktivita se pohybuje v nízkém až středním rozmezí (1,12). K hodnocení stupně malignity se standardně využívá Nottinghamský gradingový systém. Odlišení od papilárního DCIS může být obtížné zejména při arteficiálním zhmoždění duktů. V diagnostice však napomáhá přítomnost jednoznačné invaze a absence myoepitelií. Diferenciace od EPC je možná na základě nepřítomnosti fibrózní kapsuly či pseudokapsuly, která je pro něj typická (15). Závažnou, byť relativně dobře rozlišitelnou diferenciální diagnózou je mikropapilární karcinom, který je tvořen morušovitými shluky buněk bez centrálního fibrovaskulárního stromatu (tzv. pseudopapily), lokalizovanými ve stromálních lakunách (46). V tomto případě je nápomocná imunohistochemie, konkrétně exprese epiteliálního membránového antigenu (EMA), která má pro mikropapilární karcinom charakteristický obrácený (inside-out) typ exprese.
Vzhledem k raritnímu výskytu čistě papilárního invazivního karcinomu je nezbytné zvažovat i možnost metastázy z jiných primárních ložisek. Nejčastěji to bývají nádory plic, ženského genitálního traktu, štítné žlázy nebo ledvin, zejména pokud nádor postrádá hormonální receptory a má netypický imunohistochemický profil (47). Diagnostickou výzvu může představovat také papilární karcinom s vysokými buňkami s obrácenou polaritou, který morfologicky připomíná papilární karcinom štítné žlázy a sdílí s ním i některé jaderné znaky (48,49). K diagnostice výše zmíněných metastatických lézí je obvykle dostačující imunohistochemický profil odpovídající danému primárnímu ložisku a zejména pečlivá anamnéza pacienta, která může výrazně snížit nutnost dalších laboratorních testů.
Tabulka č. 3. Přehled dalších nádorových lézí nabývající papilární architektoniku.
Morfologie
ME
ER/PR /HER2
Jiné
Adenom bradavky
kombinace adenózy, papil, sklerotizace, apokrinní a skvamózní metaplazie
ano
pozitivní ER/PR
Adenomyoepiteliom s papilárním růstem
vřetenitý, tubulární, lobulární, papilární růst, 2 vrstvy buněk – luminální a ME, maligní i benigní
ano
ER+/-
Karcinom z vysokých buněk s obrácenou polaritou
solidní nebo solidně papilární typ růstu, vysoké buňky s eozinofilní cytoplazmou, jádra na apikální straně, +/makrofágy
ne
slabá ER/PR pozitivita, HER2 nebo triple negativní
mutace IDH2, PIK3CA
Mikropapilární karcinom
morušovité shluky bez centrálního stromatu ve stromálních lakunách, +/produkce mucinu, jaderný grade střední až vysoký
ne
pozitivní ER/PR, HER2 + u 10 – 30 %
reverzní, luminální exprese EMA
Mucinózní cystadenokarcinom
multicytický, cylindrický epitel s intraa extracelulárním mucinem, papilární výběžky, mikropapily, častý DCIS v okolí
ne
triple negativní, vzácně ER/PR+
CK7+, CK20-, CDX2-
Sekreční karcinom s papilárním růstem
papilární, mikrocystické, solidní, tubulární formace, eozinofilní až pěnité buňky s PAS pozitivním sekretem
ne
triple negativní
fúzní gen ETV6-NTRK3, S-100+, mamaglobin+, SOX10+
ME – myoepitelie, ER – estrogenový receptor, PR – progesteronový receptor
Genetika papilárních lézí
Genetická vyšetření nejsou v případě papilárních lézí zpravidla nezbytná pro stanovení diagnózy, přesto byly u některých jednotek popsány specifické genetické alterace, které doplňují morfologické a imunofenotypové charakteristiky.
U čistých IDP je nejčastější genetickou změnou ztráta chromozomu X, dále bývá zaznamenána ztráta 16q a 7q a aktivační mutace v genu PIK3CA (50).
Přechod intraduktálního papilomu v atypickou duktální hyperplazii (ADH) nebo duktální karcinom in situ (DCIS) je pravděpodobně spojen se ztrátou 16q, 11q a ziskem 1q, zatímco mutace v PIK3CA zde naopak většinou chybí. Delece 16q byla popsána i u papilomů s „columnar cell change atypia/flat epithelial atypia“, a tato prekurzorová léze tak sdílí genetické znaky s ADH a DCIS (20).
Ztráta heterozygozity (LOH) v oblasti 16q23 se objevuje výlučně u maligních papilárních lézí, zatímco LOH v 16q21 a 16q13 je přítomna jak u benigních, tak maligních lézí. Ztráta heterozygozity v oblasti TP53 je asociována s maligním chováním (51). EPC s invazivní složkou častěji vykazuje rekurentní hotspot missense mutace genu PIK3CA v porovnání s neinvazivním EPC. U obou skupin jsou rovněž popisovány mutace nebo inzerce v genech KMT2A a CREBBP. Zatímco mRNA profil obou skupin je překrývající, rozdíly byly popsány v expresi 39 genů, které se podílejí na regulaci extracelulární matrix, buněčné adheze a organizaci kolagenních fibril (52). U SPC jsou zvýšeně exprimovány geny spojené s neuroendokrinní diferenciací, zejména RET, ASCL1 a DOK7 (12).
Další léze prsu s papilární architektonikou
Jednotek, jež mohou částečně nebo kompletně nabývat papilární architektoniku se v prsu vyskytuje řada. Níže naleznete krátký výčet jejich histologických změn, a pro stručnost a přehlednost jsou další zajímavosti uvedeny v tabulce (tab. 3).
Adenom bradavky je benigní epiteliální proliferace, která může napodobovat nebo kombinovat různé růstové vzory. Nejčastěji jde o variace adenózy, papilární či pseudopapilární morfologie, kribriformního, mikropapilárního růstu a různých typů metaplastických změn, které mohou nabývat pseudoinfiltrativní růst. Epitel je dvouvrstvý, tvořený luminální a myoepiteliální vrstvou (1,53).
Adenomyoepiteliom s papilárním růstem je bifázický tumor napodobující obdobnou jednotku ve slinné žláze. Základní konfigurace je tvořena žlázovými tubuly s luminální a myoepiteliální vrstvou. Maligní transformaci mohou podléhat obě buněčné populace (16).
Karcinom z vysokých buněk s obrácenou polaritou („tall cell carcinoma with reversed polarity“) je prognosticky příznivý tumor připomínající stejnojmennou variantu papilárního karcinomu štítné žlázy. Má solidní či solidně papilární růst. Nádorové buňky s objemnou eozinofilní cytoplazmou mají jádra uložená v apikální části buněk. Jádra jsou oválná, světlá, často se zářezy nebo pseudoinkluzemi. Někdy se vyskytují makrofágy (48,49).
Mikropapilární karcinom je agresivní varianta s častým lymfovaskulárním šířením. Je tvořen morušovitými shluky buněk bez centrálního fibrovaskulárního stromatu, ale ve stromálních lakunách. Typická je exprese epiteliálního membránového antigenu (EMA) na vnitřní straně membrány morušových shluků. Může se vyskytovat jako čistá jednotka, ale častěji představuje složku invazivního karcinomu NST, či invazivního mucinózního karcinomu (46).
Mucinózní cystadenokarcinom je vzácný, prognosticky příznivý typ karcinomu, morfologicky připomínající stejnojmenné karcinomy v pankreatu či vaječníku. Typický je multicystický růst s jemnými výběžky a papilami a produkce extracelulárního i intracelulárního mucinu v cylindrickém epitelu (54).
Sekreční karcinom s papilárním růstem je vzácný low grade karcinom, definovaný přítomností translokace zahrnující gen ETV6. Papilární morfologie je méně častá, buňky mají eozinofilní granulární až pěnitou cytoplazmu díky produkci PAS pozitivního sekretu (55).
ZÁVĚR
Papilární morfologie jsou problematickým typem růstu, který v diferenciální diagnostice zahrnuje množství jednotek jak primárních lézí prsu, ať už benigních, prekurzorových nebo maligní povahy, tak vzácně sekundárních nádorů metastazujících do prsu. Diagnostika těchto jednotek bývá obtížná a vyžaduje detailní zhodnocení růstového vzoru, ohraničení, buněčné morfologie a přítomnosti či absence myoepiteliální vrstvy. Nezastupitelnou roli hraje imunohistochemické vyšetření, nejen k průkazu myoepitelií, ale i k detekci hormonálních receptorů a případně dalších markerů, zejména pokud se zvažuje možnost sekundárního (metastatického) postižení prsu. V případě jehlových (core-cut) biopsií není někdy možné učinit jednoznačný závěr ani při použití všech pomocných vyšetření. U některých případů tak definitivní diagnostika zůstává až na vyšetření definitivního vzorku z operačního resekátu. Správné zařazení papilárních lézí vyžaduje kombinaci morfologického obrazu, imunohistochemického panelu a znalosti možných diagnostických nástrah. Cílem této práce je poskytnout přehled základních jednotek s papilární morfologií, poukázat na klíčové rozdíly mezi nimi a nabídnout praktické pomůcky pro jejich každodenní rozpoznávání v rutinní diagnostické praxi
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Zdroje
- WHO Classification of Tumours Editorial Board. Breast Tumours. 5th ed. Lyon (France): International Agency for Research on Cancer; 2019.
- Hodorowicz-Zaniewska D, Szpor J, Basta P. Intraductal papilloma of the breast management. Ginekol Pol 2019; 90(2): 100-103.
- Rakha EA, Ahmed MA, Ellis IO. Papillary carcinoma of the breast: diagnostic agreement and management implications. Histopathology 2016; 69(5): 862-870.
- Tse GM, Tan PH, Lui PC. The role of immunohistochemistry for smooth-muscle actin, p63, CD10 and cytokeratin 14 in the differential diagnosis of papillary lesions of the breast. J Clin Pathol 2007; 60(3): 315-320.
- Ichihara S, Fujimoto T, Hashimoto K, Moritani S, Hasegawa M, Yokoi T. Double immunostaining with p63 and high-molecular-weight cytokeratins distinguishes borderline papillary lesions of the breast. Pathol Int 2007; 57(3): 126-132.
- Tse GM, Tan PH, Moriya T. The role of immunohistochemistry in the differential diagnosis of papillary lesions of the breast. J Clin Pathol 2009; 62(5): 407-413.
- Grin A, O‘Malley FP, Mulligan AM. Cytokeratin 5 and estrogen receptor immunohistochemistry as a useful adjunct in identifying atypical papillary lesions on breast needle core biopsy. Am J Surg Pathol 2009; 33(11): 1615-1623.
- Yanai H, Ishida M, Yoshikawa K, Tsuta K, Sekimoto M, Sugie T. Immunohistochemical analyses of the expression profiles of INSM1, ATRX, DAXX and DLL3 in solid papillary carcinomas of the breast. Oncol Lett 2022; 23(4): 137.
- Agoumi M, Giambattista J, Hayes MM. Practical Considerations in Breast Papillary Lesions: A Review of the Literature. Arch Pathol Lab Med 2016; 140(8): 770-790.
- Cserni G, Francz M, Járay B, et al. Pathological Diagnosis, Work-Up and Reporting of Breast Cancer 1st Central-Eastern European Professional Consensus Statement on Breast Cancer. Pathol Oncol Res 2022; 28 : 1610373.
- Amendoeira I, Apostolikas N, Bellocq JP, et al. European Guidelines for Quality Assurance in Breast Cancer Screening and Diagnosis. (4th edn). Luxembourg: European Comission; 2006 : 219–311.
- Kulka J, Madaras L, Floris G, Lax SF. Papillary lesions of the breast. Virchows Arch 2022; 480(1): 65-84.
- Wei S. Papillary Lesions of the Breast: An Update. Arch Pathol Lab Med 2016; 140(7): 628-643.
- Tramm T, Kim JY, Tavassoli FA. Diminished number or complete loss of myoepithelial cells associated with metaplastic and neoplastic apocrine lesions of the breast. Am. J. Surg. Pathol 2011; 35(2); 202–211.
- Rakha EA, Ellis IO. Diagnostic challenges in papillary lesions of the breast. Pathology 2018; 50(1): 100-110.
- Schwartz CJ, Krings G. Salivary gland-like tumors of the breast: Histopathologic and genetic features with clinical implications. Semin Diagn Pathol 2024; 41(6): 272-284.
- Boac BM, Centeno BA. Pleomorphic adenoma of the breast with cytologic atypia on cytopathology: A potential diagnostic pitfall and literature review. Diagn Cytopathol 2022; 50(5): 265-269.
- Zhang X, Liu W, Hai T, Li F. Upgrade Rate and Predictive Factors for Breast Benign Intraductal Papilloma Diagnosed at Biopsy: A Meta-Analysis. Ann Surg Oncol 2021; 28(13): 8643-8650.
- Corbin H, Bomeisl P, Amin AL, Marshall HN, Gilmore H, Harbhajanka A. Upgrade rates of intraductal papilloma with and without atypia diagnosed on core needle biopsy and clinicopathologic predictors. Hum Pathol 2022; 128 : 90-100.
- de Boer M, Verschuur-Maes AHJ, Moelans C, van Diest PJ. Papillomatous breast lesions with atypical columnar cell features. J Clin Pathol 2023; 76(4): 228-233.
- Mihara Y, Takahashi R, Mizuochi S, Yamaguchi R, Akiba J. Additional report: recurrence of intraductal papilloma with atypical ductal hyperplasia as solid papillary carcinoma. Med Mol Morphol 2025; 58(1): 87-90.
- Mihara Y, Yamaguchi R, Takahashi R, Yano Y, Yano H. Intraductal papilloma with atypical ductal hyperplasia and neuroendocrine differentiation as a possible precursor lesion of solid papillary carcinoma. Med Mol Morphol 2023; 56(3): 227-232.
- Min KW, Min SK, Kwon MJ, Seo J, Park HR, Kim LS. Extensive Lobular Carcinoma In Situ with Pagetoid Spread into Multiple Papillomas of the Breast. Breast J 2016; 22(6): 693-695.
- Li JK, Xu YJ, Niu RL, et al. Atypical ductal hyperplasia diagnosed by US-guided core needle biopsy: clinical, pathological and US features associated with upgrading to malignancy. BMC Med Imaging 2025; 25(1): 168.
- Ni Y, Tse GM. Papillary lesions of the breast review and practical issues. Semin Diagn Pathol 2022; 39(5): 344-354.
- Bezić J, Smolić J, Bečić K. Dimorphic Invasive Breast Carcinoma with Tubulopapillary Features. International Journal of Surgical Pathology 2022; 31(7): 1314-1316.
- Lefkowitz M, Lefkowitz W, Wargotz ES. Intraductal (intracystic) papillary carcinoma of the breast and its variants: a clinicopathological study of 77 cases. Hum Pathol 1994; 25(8): 802-809.
- Collins LC, Schnitt SJ. Papillary lesions of the breast: selected diagnostic and management issues. Histopathology 2008; 52(1): 20-29.
- Rakha EA, Quinn C. Controversies regarding encapsulated papillary carcinoma of the breast: an approach to evaluation and categorisation. Histopathology 2025; 86(4): 497-513.
- Liu ZL, Zhang Q, Lu Q, Zhang C, Chen J, Dong YY, Liu LP. Clinical and imaging characteristics of encapsulated papillary carcinoma: a comparative analysis with intraductal papilloma. World J Surg Oncol 2025; 23(1): 244.
- Taniguchi K, Yamasaki R, Kajiwara Y, Ichimura K, Yoshino T. A Case Report on Apocrine Encapsulated Papillary Carcinoma of the Breast with Frank Invasion: A Diagnostic Quandary. Int J Surg Pathol 2022; 30(8): 939-944.
- Nomoto Y, Yoshinaka H, Ohi Y, et al. Apocrine papillary lesion: comparison of pathological findings from 22 years previously and the present. Breast Cancer 2019; 26(4): 524-528.
- Liu X, Wu H, Teng L, Zhang H, Lu J, Liang Z. High-grade encapsulated papillary carcinoma of the breast is clinicopathologically distinct from low/intermediate-grade neoplasms in Chinese patients. Histol Histopathol 2019; 34(2): 137-147.
- Changrong W, Zhibo Z, Jufeng G, Hongju Y, Feng Y, Jingjing X. Encapsulated Papillary Carcinoma of the Breast: A Review of Clinicopathologic Characteristics, Molecular Mechanisms, and Patient Management. Cancer Control 2024; 31 : 10732748241299071.
- Hashmi AA, Iftikhar SN, Munawar S, Shah A, Irfan M, Ali J. Encapsulated Papillary Carcinoma of Breast: Clinicopathological Features and Prognostic Parameters. Cureus 2020; 12(10): e11282.
- Jadhav T, Prasad SS, Guleria B, Tevatia MS, Guleria P. Solid papillary carcinoma of the breast. Autops Case Rep 2022; 12: e2021352.
- Guo S, Wang Y, Rohr J, Fan C, Li Q, Li X, Wang Z. Solid papillary carcinoma of the breast: A special entity needs to be distinguished from conventional invasive carcinoma avoiding over-treatment. Breast 2016; 26 : 67 - 72.
- Maeda I, Tajima S, Kanemaki Y, Tsugawa K, Takagi M. Use of immunohistochemical analysis of CK5/6, CK14, and CK34betaE12 in the differential diagnosis of solid papillary carcinoma in situ from intraductal papilloma with usual ductal hyperplasia of the breast. SAGE Open Med 2018; 6 : 2050312118811542.
- Sharma R, Thirunavukkarasu B, Elhence P, Vishnoi JR. Invasive solid papillary carcinoma with invasive lobular and invasive breast carcinoma, no special type: a rare association. BMJ Case Rep 2021; 14(5): e243628.
- Tariq MU, Idress R, Qureshi MB, Kayani N. Solid papillary carcinoma of breast; a detailed clinicopathological study of 65 cases of an uncommon breast neoplasm with literature review. Breast J 2020; 26(2): 211-215.
- Kudo N, Takano J, Kudoh S, Arima N, Ito T. INSM1 immunostaining in solid papillary carcinoma of the breast. Pathol Int 2021; 71(1): 51-59.
- Christgen M, Bartels S, van Luttikhuizen JL, et al. Subclonal analysis in a lobular breast cancer with classical and solid growth pattern mimicking a solid-papillary carcinoma. J Pathol Clin Res 2017; 3(3): 191-202.
- Koufopoulos N, Pateras IS, Gouloumis AR, et al. Diagnostically Challenging Subtypes of Invasive Lobular Carcinomas: How to Avoid Potential Diagnostic Pitfalls. Diagnostics (Basel) 2022; 12(11): 2658.
- Huang K, Appiah L, Mishra A, Bagaria SP, Gabriel ME, Misra S. Clinicopathologic Characteristics and Prognosis of Invasive Papillary Carcinoma of the Breast. J Surg Res 2021; 261 : 105-112.
- Chen S, Wang J, Yang L, Ji M, Chen S. Comparative analysis of clinicopathologic characteristics and molecular subtypes of invasive papillary carcinoma of the breast and invasive ductal carcinoma: results from SEER database. J BUON 2021; 26(5): 1991-2002.
- Yang YL, Liu BB, Zhang X, Fu L. Invasive Micropapillary Carcinoma of the Breast: An Update. Arch Pathol Lab Med 2016; 140(8): 799-805.
- Abe N, Matsumoto H, Motonari T, Nakada N, Zaha H, Tan PH, Yoshimi N. Invasive papillary carcinoma of the breast with an unusual immunophenotype. Pathol Int 2019; 69(3): 183-185.
- Toss MS, Billingham K, Egbuniwe IU, Moreno F, Abass A, Rakha EA. Breast Tumours Resembling the Tall Cell Variant of Thyroid Papillary Carcinoma: Are They Part of the Papillary Carcinoma Spectrum or a Distinct Entity? Pathobiology 2019; 86(2-3): 83-91.
- Kajo K, Ducár M, Dzuracký J, et al. Karcinóm prsníka z vysokých buniek s obrátenou polaritou opis troch prípadov s prehľadom literatúry. Cesk Patol 2023; 59(3): 132-138.
- Kader T, Elder K, Zethoven M, et al. The genetic architecture of breast papillary lesions as a predictor of progression to carcinoma. NPJ Breast Cancer 2020; 6 : 9.
- Yoshida M, Tsuda H, Yamamoto S, Kinoshita T, Akashi-Tanaka S, Hojo T, Fukutomi T. Loss of heterozygosity on chromosome 16q suggests malignancy in core needle biopsy specimens of intraductal papillary breast lesions. Virchows Arch 2012; 460(5): 497-504.
- Schwartz CJ, Boroujeni AM, Khodadadi-Jamayran A, et al. Molecular analysis of encapsulated papillary carcinoma of the breast with and without invasion. Hum Pathol 2021; 111 : 67-74.
- Weigelt MA, Sciallis AP, McIntire PJ, Ko JS, Billings SD, Ronen S. Nipple Adenoma: Clinicopathologic Characterization of 50 Cases. Am J Surg Pathol 2023; 47(8): 926-932.
- Moatasim A, Mamoon N. Primary Breast Mucinous Cystadenocarcinoma and Review of Literature. Cureus. 2022; 14(3): e23098.
- Shui R, Cheng Y, Bai Q, Yang W. Secretory breast carcinoma with a papillary-predominant pattern: an unusual morphological variant. Histopathology 2017; 71(3): 488-493.
Štítky
Patológia Súdne lekárstvo Toxikológia
Článok vyšiel v časopiseČesko-slovenská patologie

2025 Číslo 4-
Všetky články tohto čísla
- Patologie prsu – každodenní realita rutinní diagnostiky
- Svět molekulární biologie je paralelním vesmírem
- MONITOR aneb nemělo by vám uniknout, že...
- Papilární léze prsu: Diagnostická úskalí a přehled jednotek
- Imunohistochemické stanovení HER2 proteinu u karcinomů prsu – aktuální stav
- Vyšetřování prediktivních faktorů v léčbě karcinomu prsu
- Neobvyklý histopatologický nález v axilární uzlině pacientky s invazivním karcinomem NST: kazuistické sdělení a přehled literatury
- An unusual case of late recurrent adult granulosa cell tumor and mature teratoma arising within the same ovary, confirmed by NGS analysis
- Současné metody multiplexní imunohistochemie pro analýzu fixovaných tkáňových vzorků
- Česko-slovenská patologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Papilární léze prsu: Diagnostická úskalí a přehled jednotek
- Současné metody multiplexní imunohistochemie pro analýzu fixovaných tkáňových vzorků
- Patologie prsu – každodenní realita rutinní diagnostiky
- Imunohistochemické stanovení HER2 proteinu u karcinomů prsu – aktuální stav
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



