-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Imunohistochemické stanovení HER2 proteinu u karcinomů prsu – aktuální stav
Immunohistochemical assessment of HER2 protein in breast carcinomas – current status
The existing HER2 immunohistochemistry testing is currently experiencing changes in its scoring caused by the recent clinical trials results, especially DESTINY Breast 04 and 06. These trials demonstrated that any detectable immunohistochemical positivity of HER2 protein on tumor cells is a predictor of response to the new antibody-drug conjugate trastuzumab deruxtecan. These studies introduced new terms “HER2 low” and later “HER2 ultralow” to distinguish subgroups within the original category “HER2 negative”, which quickly became accepted in clinical practice. This article aims to explain these new terms and present Czech and international expert recommendations for testing and reporting of HER2 immunohistochemistry in relation to these new categories.
Keywords:
trastuzumab deruxtecan – HER2 immunohistochemistry – HER2 low
Autori: Pavel Fabian
Pôsobisko autorov: Oddělení onkologické patologie, Masarykův onkologický ústav, Brno
Vyšlo v časopise: Čes.-slov. Patol., 61, 2025, No. 4, p. 190-194
Kategória: Přehledový článek
Súhrn
Dosavadní hodnocení HER2 imunohistochemie doznává v současné době změny, vyvolané výsledky nedávných klinických studií, zejména DESTINY Breast 04 a 06, a totiž že jakákoliv detekovatelná imunohistochemická pozitivita HER2 proteinu na nádorových buňkách je prediktorem léčebné odpovědi na nový konjugát protilátky s chemoterapeutikem trastuzumab deruxtecan. Tyto studie použily pro rozlišení podskupin uvnitř původní kategorie „HER2 negativní“ nové pojmy „HER2 low“ a posléze „HER2 ultralow“, které se v klinické praxi velmi rychle vžily. Tento článek si klade za cíl vysvětlit tyto nové pojmy a představit česká a světová odborná doporučení k vyšetřování a reportování HER2 imunohistochemie ve vztahu k těmto novým kategoriím.
Klíčová slova:
trastuzumab deruxtecan – HER2 imunohistochemie – HER low
* Adresa pro korespondenci:
Pavel Fabian
Oddělení onkologické patologie Masarykův onkologický ústav, Brno tel.: 543133400
e-mail: pavel.fabian@mou.czPrognóza a predikce k HER2 cílené léčbě karcinomu prsu
HER2 protein byl na začátku devadesátých let minulého století hojně studovanou molekulou, bylo známo, že jeho vysoká exprese je u karcinomů prsu nositelem horší prognózy, souvisí s rezistencí k hormonální terapii a k některým chemoterapeutikům a naopak přináší zvýšenou citlivost k chemoterapii založené na antracyklinech (1-5). Brzy se ukázalo, že je také velmi významným terapeutickým cílem pro monoklonální protilátky (a později i tyrozinkinázové inhibitory) a současně prediktorem účinnosti této léčby (6,7). Dosavadní dichotomické hodnocení HER2 (negativní versus pozitivní) se vztahovalo k léčbě těmito přípravky, tedy trastuzumabem, pertuzumabem, lapatinibem a dalšími, kde prediktorem odpovědi na léčbu byla overexprese HER2 proteinu a/nebo amplifikace HER2 genu (7). Imunohistochemickou (IHC) pozitivitu (Obr.1A-D) HER2 IHC 3+ používáme jako náhradní marker pro amplifikaci (8-10). Kategorii HER2 IHC 2+ podrobujeme in situ hybridizaci (ISH), kategorie HER2 IHC 1+ a 0 pak jsme dosud označovali za negativní a nebyla pociťována potřeba rozlišovat mezi kategoriemi 0 a 1+ (11,12). V posledních letech došlo v onkologii k rozšíření konjugátů protilátek s chemoterapeutikem (antibody – drug conjugates, ADC), kde protilátka slouží jako specifický „doručovatel“, směřující toxické chemoterapeutikum přednostně do nádorových buněk. V léčbě karcinomů prsu se uplatňují sacituzumab govitekan, trastuzumab emtansine a trastuzumab deruxtecan (T-DXd) (13,14). Poslední dva jmenované využívají jako cíl protein HER2 a jako transportní protilátku trastuzumab; účinnost léčby byla nejprve potvrzena u nádorů s amplifikací genu HER2 (15,16), nicméně recentně se ukázalo, že prediktorem odpovědi na T-DXd je jakákoliv detekovatelná imunohistochemická pozitivita HER2 proteinu na nádorových buňkách. Šlo o průlomové studie DESTINY Breast 04 a DESTINY Breast 06 (DB 04/06) (17,18).
Je přitom prokázáno, že nositelem protinádorové aktivity u neamplifikovaných nádorů s nízkou expresí HER2 proteinu není, tak jako u nádorů amplifikovaných, blokáda HER2 proteinu a jeho dráhy, ale právě onen cíleně transportovaný T-DXd, neboť dvojkombinace trastuzumab + pertuzumab u nich neprokázala účinnost (19,20). Studie DB 04/06 použily při hodnocení HER2 imunohistochemie téměř nezměněná dosavadní standardní kritéria (použitá definice HER2 IHC skóre 0/1+ je mírně odlišná od ASCO/CAP guidelines – u popisu slabé nesouvislé membránové pozitivity se vypouští „barely perceptible staining“ a ponechává pouze „faint“) (17,21) i standardní test (VENTANA anti-HER2/ neu (4B5) Rabbit Monoclonal Primary Antibody (Roche) assay (Ventana 4B5)), ovšem pro rozlišení skupin uvnitř kategorie „negativní“ aplikovaly nová pojmenování, a to pojmy „HER2 low“ pro nádory HER2 IHC 1+ a HER2 IHC 2+/ISH negativní a posléze „HER2 ultralow“ pro nádory HER2 IHC 0 s jakoukoliv membránovou pozitivitou. Pro srovnání původních a nových kategorií viz (tab.1). Tyto pojmy se v klinické praxi velmi rychle vžily, a tak či onak pronikají i do patologie, respektive je pociťována klinická potřeba, abychom v patologii tuto terminologii používali.
Obr. 1. Imunohistochemický průkaz HER-2 proteinu. A. Kompletní negativita. B. Slabá pozitivita. C. Středně silná kompletní pozitivita. D. Silná kompletní pozitivita. E, F. Výsledek IHC při nedodržení podmínek preanalytické fáze (dlouhý čas studené ischemie; je zřetelná heterogenita i snížená intenzita barvení srovnej s D). E. Oblasti hůře fixované. F. Oblasti s lepší fixací. Barveno IHC anti-HER-2, originální zvětšení 400x. 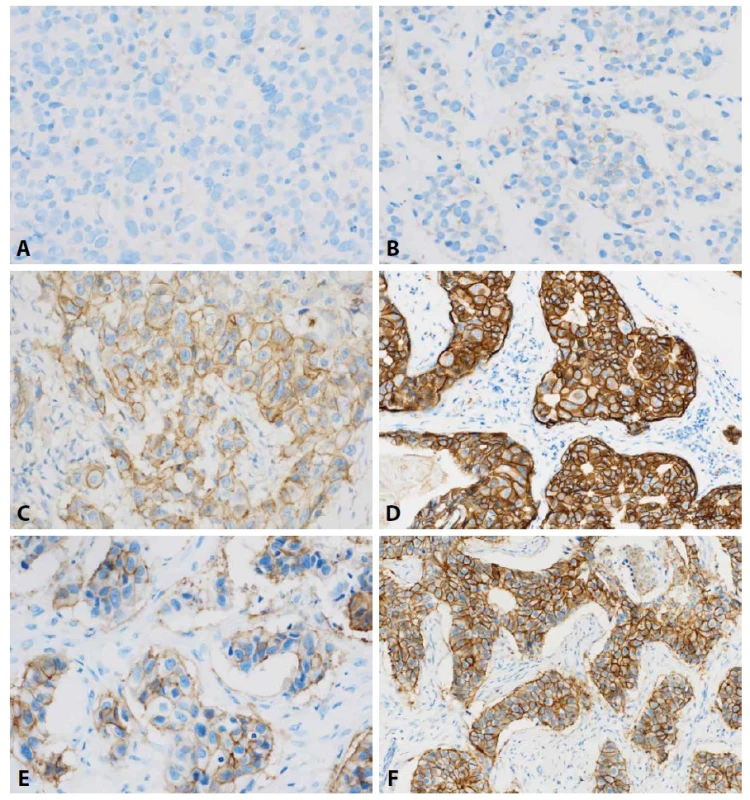
Tab. 1. Interpretace výsledků HER2 imunohistochemie a in situ hybridizace dle různých doporučení. Upraveno podle (18, 20, 26, 44).
Popis IHC / ISH v invazivním tumoru
Označení dle ASCO/CAP 2018
Závěr dle ASCO/ CAP 2018
Závěr dle ESMO 2023
Závěr dle CAP protokolu *
Doporučení SČP ČLS JEP
Žádné barvení
HER2 0
HER2 negativní
HER2 null
Negativní skóre 0 (0 / chybějící membránové barvení)
HER2 negativní (skóre 0)
Slabé barvení ≤ 10 % buněk
HER2 0
HER2 negativní
HER2 ultralow (nebo > žádné barvení < 1+)
Negativní skóre 0 (0+ / s membránovým barvením)
HER2 negativní (skóre 0; ultralow)
Nekompletní slabé barvení > 10 % buněk
HER2 1+
HER2 negativní
HER2 low
Negativní skóre 1+
HER2 negativní (skóre 1+; low)
Kompletní slabé až středně silné barvení > 10 % buněk, ISH negativní
HER2 2+ bez amplifikace
HER2 negativní
HER2 low
IHC nejednoznačné / HER2 negativní založeno na výsledcích IHC a ISH
HER2 nejednoznačné (skóre 2+) / HER2 negativní (HER2 +/FISH-; low)
Kompletní slabé až středně silné barvení > 10 % buněk, ISH pozitivní
HER2 2+ s amplifikací
HER2 pozitivní
HER2 pozitivní
IHC nejednoznačné / HER2 pozitivní založeno na výsledcích IHC a ISH
HER2 nejednoznačné (skóre 2+) / HER2 pozitivní (HER2 +/FISH+)
Silné kompletní barvení > 10 % buněk
HER2 3+
HER2 pozitivní
HER2 pozitivní
Pozitivní skóre 3+
HER2 pozitivní (skóre 3+)
IHC: imunohistochemie, ISH: in situ hybridizace, ASCO: American Association For Clinical Oncology, CAP: College Of American Pathologists, ESMO: European Society For Medical Oncology, SČP ČLS JEP: Společnost českých patologů České lékařské společnosti Jana Evangelisty Purkyně.
*CAP protokol: Reporting Template for Reporting Results of Biomarker Testing of Specimens from Patients with Carcinoma of the Breast
Aktualizované doporučené postupy pro HER2 testování
V roce 2007 vyšlo první společné doporučení ASCO / CAP (American Society for Clinical Oncology / College of American Pathologists) k HER2 testování, které tak sjednotilo a kodifikovalo dosavadní postupy (22). Mimo jiné kladlo zvláštní důraz na dodržení podmínek preanalytické fáze, zejména čas studené ischemie a délku trvání fixace formalínem. Tento text byl několikrát upřesněn a doplněn (12,23,24). Na tato ASCO / CAP guidelines se odvolávají prakticky všechny odborné publikace vznikající na poli HER2 testování a anti-HER2 léčby a jsou (neformálně) většinově odbornou veřejností v ČR přijímána jako doporučení k testování.
Poslední doplnění tohoto doporučení z roku 2023 (12), konstatují v reakci na shora uvedené poznatky o účinnosti T-DXd u „HER2 low“ tumorů, že způsob provádění testování ani způsob hodnocení dle starších ASCO / CAP guidelines se nemění, nicméně doporučuje se namísto pozitivní / negativní reportovat i semikvantitativní IHC skóre (0/1+/2+/3+) a zvážit doplnění odstavce o možné účinnosti ADC u nádorů HER2 1+ a 2+ neamplifikovaných. K implementaci pojmu„HER2 low“ do patologických reportů nicméně autorský kolektiv nenabádá.
European Society for Medical Oncology (ESMO) doporučení z roku 2023 uvádí analogicky, že při reportování výsledků by se patologové měli přidržet ASCO / CAP guidelines, přičemž by měli uvést hodnocení 0/1+/2+/3+, což umožní onkologovi rozhodnout se, zda je pacient vhodný pro léčbu trastuzumab deruxtecanem. Použití označení „HER2 low“ není v reportech upřednostňováno, jelikož jde o klinickou interpretaci HER2 statusu onemocnění (20).
Britská doporučení z prosince 2022 (11) mj. velmi detailně upřesňují interpretaci pro všechny možné kombinace kompletnosti, intenzity a procentuálního zastoupení HER2 IHC pozitivních nádorových buněk. Dále upozorňují na užitečnou pomůcku pro hodnocení intenzity barvení tzv. pravidlo zvětšení („magnification rule“), totiž že rozpoznatelnost pozitivních membrán při daném zvětšení objektivu definuje intenzitu, tj. membrány viditelné při přehledném zvětšení = silná pozitivita, membrány viditelné při objektivu 10× = střední pozitivita atd. (25). Reportování skóre 0/1+/2+/3+ je zde (stejně jako v ASCO / CAP a ESMO) doporučováno, na rozdíl od nich ovšem radí používat i termín „HER2 low“.
V tzv. templátech pro reportování biomarkerů u karcinomů prsu vydaných College of American Pathologists (CAP), konkrétně ve verzi z března 2025 (26) je kategorie „HER2 exprese menší než 1+“ deskriptivně reflektována, a to jako doporučené označení „IHC 0/absent membrane staining“ a „0+/ with membrane staining“.
Všechny uvedené texty se shodují, že v případě kategorií „HER2 low“ a „HER2 ultralow“ nejde o nový biologický subtyp v rámci karcinomů prsu, který by vykazoval zřetelnou prediktivní či prognostickou hodnotou. Tyto kategorie se nevydělují v genových expresních profilech a ani se neodlišují – po korekci na hormonální status tumoru – v parametrech přežití (27-30). Četnost nádorů„HER2 low“ je asi 50 % ze všech karcinomů prsu, přičemž zastoupení je výrazně vyšší mezi nádory luminálními než mezi nádory triple negativními (27,31). Hladina exprese stanovená stávajícími IHC testy jako 1+ nebo 2+ nekoreluje s odpovědí na léčbu ADC – nádory HER2 1+ reagují na T-DXd stejně úspěšně jako nádory HER2 2+ (17,20). Účinnost T-DXd u nádorů zcela bez IHC detekovatelné HER2 exprese nebyla zatím významněji zkoumána, ovšem ve studii DAISY (studie fáze II) se prokázalo, že nádory HER2 pozitivní měly podíl objektivní odpovědi (objective response rate (ORR)) na T-DXd 70,6 %, nádory „HER2 low“ měly ORR 37,5 %, nádory s expresí odpovídající definici „HER2 ultralow“ měly ORR 40 % a nádory bez membránového barvení měly ORR 25 % (32). Pokud se takové odpovědi u HER2 zcela negativních tumorů potvrdí i ve studiích fáze III, můžeme se dočkat dalších změn, např. úplného upuštění od„low/ultralow“ nomenklaturního konceptu.
Dosavadní testy nebyly konstruovány k detekcím nízkých hladin exprese, ale k diagnostice nádorů s HER2 overexpresí a/nebo amplifikací. Je tedy možné, že jiný typ protilátky či IHC kitu, případně test postavený na jiné než IHC metodice (např. založený na kvantifikaci mRNA) by mohl lépe selektovat nádory vhodné k terapii ADC (33). Na druhou stranu lze argumentovat, že závěry zmiňovaných klinických studií se vztahují právě k výsledkům HER2 testu tohoto konvenčního typu (11).
Přestože ve studiích DB04/06 byl použit kit Ventana 4B5 a ten byl též schválen FDA jako „companion diagnostic“, všechna doporučení shodně uvádějí, že není nutno v laboratořích měnit zavedené a validované testy, neboť zatím neexistují důkazy o odlišné odpovědi takto selektovaných pacientů na T-DXd či jiné ADC. Lze tedy použít kterýkoliv validovaný test za předpokladu, že poskytuje dokladovatelnou výkonnost (někde se přímo uvádí, že by měl být validován ve vztahu k Ventana 4B5 kitu) a účastní se externí kontroly kvality (33). Je nicméně opakovaně publikováno, že různé kity / protilátky mají různou senzitivitu, zejména v oblasti nízkých intenzit, a že detekují kategorii „HER2 low“ s různou výslednou četností. Jedna z prací ukazuje významně vyšší senzitivitu Ventana 4B5 oproti kitu Herceptest pharmDx pAb s polyklonální protilátkou pro platformu Autostainer (34). Při srovnání Ventana 4B5 a DAKO Herceptest pharmDx mAb (platforma Omnis s monoklonální protilátkou) je naopak zřetelná vyšší senzitivita Herceptestu (35). Velmi zajímavá práce srovnala také tyto dva nejčastěji používané testy za pomoci uměle vytvořených mikročástic s definovaným různě velkým množstvím molekul HER2 na jejich povrchu a za použití obrazové analýzy pak hodnotila různé parametry testu. Rozdíly mezi oběma testy jsou značné (potvrzuje se vyšší senzitivita HercepTestu mAb), přičemž pozoruhodné je, že dolní mez detekce (tj. nejnižší koncentrace molekuly na membráně, kdy lze detekovat nejslabší IHC reakci) se nachází na úrovni 1×105 molekul HER2 na mikročástici (v modelu nahrazuje buňku). Nevýhodou tohoto modelu je, že nemůže reflektovat problémy reálné praxe, zejména preanalytickou variabilitu (36). Je zajímavé zmínit, že ve výzkumném nastavení Ventana 4B5 testu ve studii DB 04 bylo použito UltraView detekčního kitu, nikoliv OptiView (17).
Ve studii DB 04 a 06 byly použity punkční biopsie, excizní vzorky či resekáty, a to z primárních tumorů i z metastatických ložisek (17,18). Prediktivní testování tedy lze provádět z jakéhokoliv typu nádorové tkáně. Některé druhy vzorků je nutno hodnotit obezřetně s přihlédnutím k preanalytické fázi, zejména kostní biopsie a cytobloky. HER2 exprese se může v průběhu evoluce nádorového onemocnění měnit a může být rozdílná mezi primárním a metastatickým ložiskem (37,38), je tedy racionální testovat každé nově bioptované ložisko karcinomu prsu, což ostatně bylo součástí už starších doporučení. Indikace terapie T-DXd se aktuálně týká metastatického onemocnění.
Technická doporučení
Pro maximální správnost IHC detekce HER2 je nutné dodržovat obecná doporučení pro zpracování tkání, tj. fixaci neutrálním pufrovaným formalínem v trvání 6-72 h, dbát na minimalizaci času studené ischémie (do 1 hod) atd. (Obr.1 E,F) (11,39). Ve vnitřních kontrolách by se měly používat materiály s rozsahem všech definovaných intenzit. Pro hodnocení velmi slabých pozitivit, v případě rozpaků, kdy obraz je nejednoznačný mezi 0 a 1+, je doporučeno použít objektiv velkého zvětšení a vyhledat konzultaci jiného patologa (11,12,20).
Konkordance výsledků skórování HER2 IHC mezi laboratořemi i mezi jednotlivými patology není příliš dobrá, nejméně uspokojivé jsou výsledky právě v zájmové oblasti rozlišení mezi 0 / „ultralow“ / 1+ (40-42). Zlepšení reprodukovatelnosti výsledků by mohlo přinést použití obrazové analýzy posílené o nástroje tzv. umělé inteligence (43).
Poznámky k praxi v České republice
V České republice je shoda na tom, že vzorky stanovené historicky jako HER2 0 je smysluplné v případě klinické potřeby přetestovat mohly by se z 0 posunout do kategorie 1+. Toto přetestování musí probíhat výhradně v referenčních laboratořích (RL), neboť jde o indikaci tzv. „centrové“ léčby. Dosavadní praxe znamenala dvojí testování přinejmenším poloviny všech karcinomů prsu vzorky v ne-referenčních laboratořích stanovené jako 2+ a 3+ a vzorky 0/1+ s vysokou pravděpodobností diskordantního fenotypu se posílaly ke konfirmaci certifikovanou IHC metodou a případnou ISH do RL. Nově by se přidaly vzorky 0/1+ u pacientek zvažovaných k léčbě T-DXd, takže dvojí testování HER2 IHC by se v součtu aplikovalo na většinu invazivních karcinomů prsu. To vedlo ke změně testovací strategie v ČR z dvoustupňové na jednostupňovou a k ukončení do značné míry nesystémového, výjimečného, historickým vývojem vzniklého postavení HER2 testování, které jako jediné prediktivní vyšetření částečně probíhalo mimo síť RL. Zde je nutné upozornit, že část ne-referenčních laboratoří nadále testování HER2 provádí a ve svých výsledkových protokolech reportuje, obvykle s dodatkem, že je vzorek přeposlán do RL. Informace o tomto výsledku HER2 však putuje s pacientem a jeho dokumentací. Není v silách ani v náplni práce onkologa v ambulanci zjišťovat a rozlišovat, ve které laboratoři se HER2 vyšetřilo a zda jde o laboratoř referenční či nikoliv. Přitom není podstatné, jestli výsledek HER2 je a jistě často je správný, ale nepochází-li z RL, není z hlediska úhrady terapie považován za validní a kromě rizika nesprávné indikace léčby je zde i riziko zamítnutí úhrady extrémně nákladné cílené léčby. Analogicky lze pohlížet na testování HER2 prováděné u DCIS, které nemá žádné opodstatnění v klinických guidelines, navíc skóre 0/1+/2+/3+ se výslovně vztahují k invazivním karcinomům a nelze je tedy aplikovat na nádory in situ, naopak může vést k mylnému chápání léze jako karcinomu invazivního.
ZÁVĚR
Testování HER2 proteinu u invazivního karcinomu prsu v ČR probíhá pouze v tzv. referenčních laboratořích, výsledky z ostatních laboratoří nejsou pro indikaci terapie validní. Testuje se jakýmkoliv certifikovaným kitem, necertifikované metody („laboratory developed test“) nejsou přípustné. Současně je povinné sledování vlastní výkonnosti laboratoře a povinná je i účast v externím hodnocení kvality. Pro vyhodnocení se aplikují kritéria ASCO / CAP se současným paralelním reportováním za použití klasifikátorů „low“ a „ultralow“ (44). Popsaná problematika prochází aktuálně vývojem a nelze vyloučit, že testování a reportování HER2 u karcinomů prsu dozná v budoucnu další změny.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Zdroje
- Soerjomataram I, Louwman MW, Ribot JG, Roukema JA, Coebergh JW. An overview of prognostic factors for long-term survivors of breast cancer. Breast Cancer Res Treat 2008; 107(3): 309-330.
- Lohrisch C, Piccart M. An overview of HER2. Semin Oncol 2001; 28(6 Suppl 18): 3-11.
- Ménard S, Fortis S, Castiglioni F, Agresti R, Balsari A. HER2 as a prognostic factor in breast cancer. Oncology 2001; 61 Suppl 2 : 67-72.
- Slamon DJ, Godolphin W, Jones LA, Holt JA, Wong SG, Keith DE et al. Studies of the HER-2/neu proto-oncogene in human breast and ovarian cancer. Science 1989; 244(4905): 707-712.
- Slamon DJ, Clark GM, Wong SG, Levin WJ, Ullrich A, McGuire WL. Human breast cancer: correlation of relapse and survival with amplification of the HER-2/neu oncogene. Science 1987; 235(4785): 177-182.
- Loibl S, Gianni L. HER2-positive breast cancer. Lancet 2017; 389(10087): 2415-2429.
- Ross JS, Fletcher JA, Bloom KJ, Linette GP, Stec J, Symmans WF et al. Targeted therapy in breast cancer: the HER-2/neu gene and protein. Mol Cell Proteomics 2004; 3(4): 379-398.
- Couturier J, Vincent-Salomon A, Nicolas A, Beuzeboc P, Mouret E, Zafrani B et al. Strong correlation between results of fluorescent in situ hybridization and immunohistochemistry for the assessment of the ERBB2 (HER-2/neu) gene status in breast carcinoma. Mod Pathol 2000; 13(11): 1238-1243.
- Yaziji H, Goldstein LC, Barry TS, Werling R, Hwang H, Ellis I et al. HER-2 testing in breast cancer using parallel tissue-based methods. JAMA 2004; 291(16): 1972-1977.
- Lebeau A, Deimling D, Kaltz C, Sendelhofert A, Iff A, Luthardt B et al. Her-2/neu analysis in archival tissue samples of human breast cancer: comparison of immunohistochemistry and fluorescence in situ hybridization. J Clin Oncol 2001; 19(2): 354-363.
- Rakha EA, Tan PH, Quinn C, Provenzano E, Shaaban AM, Deb R et al. UK recommendations for HER2 assessment in breast cancer: an update. J Clin Pathol 2023; 76(4): 217-227.
- Wolff AC, Somerfield MR, Dowsett M, Hammond MEH, Hayes DF, McShane LM et al. Human epidermal growth factor receptor 2 testing in breast cancer: ASCO–College of American Pathologists guideline update. J Clin Oncol 2023; 41(22): 3867-3872.
- Shaaban AM, Kaur T, Provenzano E. HER-2-Low Breast Cancer-Current Knowledge and Future Directions. Medicina (Kaunas) 2025; 61(4): 644.
- Gogia P, Ashraf H, Bhasin S, Xu Y. Antibody-Drug Conjugates: A Review of Approved Drugs and Their Clinical Level of Evidence. Cancers (Basel) 2023; 15(15): 3886.
- Cortés J, Hurvitz SA, Im SA, Iwata H, Curigliano G, Kim SB et al. Trastuzumab deruxtecan versus trastuzumab emtansine in HER2-positive metastatic breast cancer: long-term survival analysis of the DESTINY-Breast03 trial. Nat Med 2024; 30(8): 2208-2215.
- Cortés J, Kim SB, Chung WP, Im SA, Park YH, Hegg R et al. Trastuzumab Deruxtecan versus Trastuzumab Emtansine for Breast Cancer. N Engl J Med 2022; 386(12): 1143-1154.
- Modi S, Jacot W, Yamashita T, Sohn J, Vidal M, Tokunaga E et al. Trastuzumab deruxtecan in previously treated HER2-low advanced breast cancer. N Engl J Med 2022; 387(1): 9-20.
- Bardia A, Hu X, Dent R, Yonemori K, Barrios CH, O‘Shaughnessy JA et al. Trastuzumab Deruxtecan after Endocrine Therapy in Metastatic Breast Cancer. N Engl J Med 2024; 391(22): 2110-2122.
- Fehrenbacher L, Cecchini RS, Geyer CE Jr, Rastogi P, Costantino JP, Atkins JN et al. NSABP B-47/NRG Oncology Phase III Randomized Trial Comparing Adjuvant Chemotherapy With or Without Trastuzumab in High-Risk Invasive Breast Cancer Negative for HER2 by FISH and With IHC 1+ or 2. J Clin Oncol 2020; 38(5): 444-453.
- Tarantino P, Viale G, Press MF, Hu X, Penault-Llorca F, Bardia A et al. ESMO expert consensus statements (ECS) on the definition, diagnosis, and management of HER2-low breast cancer. Ann Oncol 2023; 34(8): 645-659.
- Shami R, Salgado R, Bardia A, Curigliano G, Hu X, Dent R et al. Analytical and clinical validation of PATHWAY HER2 (4B5) assay for assessment of HER2-low/HER2-ultralow status and eligibility for trastuzumab deruxtecan in DESTINY-Breast06. ESMO Open 2025; 10(6):105310.
- Wolff AC, Hammond ME, Schwartz JN, Hagerty KL, Allred DC, Cote RJ et al. American Society of Clinical Oncology/College of American Pathologists guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer. Arch Pathol Lab Med 2007; 131(1): 18-43.
- Wolff AC, Hammond ME, Hicks DG, Dowsett M, McShane LM, Allison KH et al. Recommendations for human epidermal growth factor receptor 2 testing in breast cancer: American Society of Clinical Oncology/College of American Pathologists clinical practice guideline update. Arch Pathol Lab Med 2014; 138(2): 241-256.
- Wolff AC, Hammond MEH, Allison KH, Harvey BE, Mangu PB, Bartlett JMS et al. Human Epidermal Growth Factor Receptor 2 Testing in Breast Cancer: American Society of Clinical Oncology/College of American Pathologists Clinical Practice Guideline Focused Update. Arch Pathol Lab Med 2018; 142(11): 1364-1382.
- Scheel AH, Penault-Llorca F, Hanna W, Baretton G, Middel P, Burchhardt Jet al. Physical basis of the ‚magnification rule‘ for standardized Immunohistochemical scoring of HER2 in breast and gastric cancer. Diagn Pathol 2018; 13(1): 19.
- https://documents.cap.org/documents/New-Cancer-Protocols-March-2025/Breast.Bmk_1.6.0.0.REL.CAPCP.pdf?_gl=1*cwmglp*_ ga*MjEzODQ1MjUyMC4xNzM4NjE5OTY0*_
- Agostinetto E, Rediti M, Fimereli D, Debien V, Piccart M, Aftimos P et al. HER2-Low Breast Cancer: Molecular Characteristics and Prognosis. Cancers (Basel) 2021; 13(11): 2824.
- Zhang H, Katerji H, Turner BM, Audeh W, Hicks DG. HER2-low breast cancers: incidence, HER2 staining patterns, clinicopathologic features, MammaPrint and BluePrint genomic profiles. Mod Pathol 2022; 35(8): 1075-1082.
- Tarantino P, Jin Q, Tayob N, Jeselsohn RM, Schnitt SJ, Vincuilla J et al. Prognostic and Biologic Significance of ERBB2-Low Expression in Early-Stage Breast Cancer. JAMA Oncol 2022; 8(8): 1177-1183.
- Peiffer DS, Zhao F, Chen N, Hahn OM, Nanda R, Olopade OI et al. Clinicopathologic Characteristics and Prognosis of ERBB2-Low Breast Cancer Among Patients in the National Cancer Database. JAMA Oncol 2023; 9(4): 500-510.
- Tarantino P, Hamilton E, Tolaney SM, Cortes J, Morganti S, Ferraro E et al. HER2-Low Breast Cancer: Pathological and Clinical Landscape. J Clin Oncol 2020; 38(17): 1951-1962.
- Mosele F, Deluche E, Lusque A, Le Bescond L, Filleron T, Pradat Y et al. Trastuzumab deruxtecan in metastatic breast cancer with variable HER2 expression: the phase 2 DAISY trial. Nat Med 2023; 29(8): 2110-2120.
- Shaaban AM, Kaur T, Provenzano E. HER2-Low Breast Cancer-Current Knowledge and Future Directions. Medicina (Kaunas) 2025; 61(4): 644.
- Scott M, Erminio M, Vandenberghe ME, Scorer P, Boothman AM, Barker C. Prevalence of HER2 low in breast cancer subtypes using the VENTANA anti-HER2/neu (4B5) assay. J Clin Oncol 2021; 39(15): 1021-1021.
- Rüschoff J, Friedrich M, Nagelmeier I, Kirchner M, Andresen LM, Salomon K et al. Comparison of HercepTest™ mAb pharmDx (Dako Omnis, GE001) with Ventana PATHWAY anti-HER-2/neu (4B5) in breast cancer: correlation with HER2 amplification and HER2 low status. Virchows Arch 2022; 481(5): 685-694.
- Aidt F, Sierra M, Salomon K, Noumsi G. Comparing the Sensitivity of HER2 Epitope Detection of HercepTest mAb pharmDx (Dako Omnis, GE001) and Ventana PATHWAY Anti-HER-2/neu (4B5) Using IHC Calibrators. Appl Immunohistochem Mol Morphol 2024; 32(10): 469-475.
- Aurilio G, Disalvatore D, Pruneri G, Bagnardi V, Viale G, Curigliano G et al. A meta-analysis of oestrogen receptor, progesterone receptor and human epidermal growth factor receptor 2 discordance between primary breast cancer and metastases. Eur J Cancer 2014; 50(2): 277-289.
- Miglietta F, Griguolo G, Bottosso M, Giarratano T, Lo Mele M, Fassan M et al. Evolution of HER2-low expression from primary to recurrent breast cancer. NPJ Breast Cancer 2021; 7(1): 137.
- Tozbikian G, Bui MM, Hicks DG, Jaffer S, Khoury T, Wen HY et al. Best practices for achieving consensus in HER2-low expression in breast cancer: current perspectives from practising pathologists. Histopathology 2024; 85(3): 489-502.
- Baez-Navarro X, van Bockstal MR, Nawawi D, Broeckx G, Colpaert C, Doebar SC et al. Interobserver Variation in the Assessment of Immunohistochemistry Expression Levels in HER2-Negative Breast Cancer: Can We Improve the Identification of Low Levels of HER2 Expression by Adjusting the Criteria? An International Interobserver Study. Mod Pathol 2023; 36(1): 100009.
- Schildhaus HU, Badve S, D’Arrigo C, Farshid G, Lebeau A, Peg Vet al. A Global Ring Study: Concordance Between Ventana PATHWAY anti-HER2/neu (4B5) Companion Diagnostic Assay and Comparators in Detecting HER2-low Breast Cancer. Mod Pathol 2025. In press.
- Wu S, Shang J, Li Z, Liu H, Xu X, Zhang Z et al. Interobserver consistency and diagnostic challenges in HER2-ultralow breast cancer: a multicenter study. ESMO Open 2025; 10(2): 104127.
- Brevet M, Li Z, Parwani A. Computational pathology in the identification of HER2-low breast cancer: Opportunities and challenges. J Pathol Inform 2023; 15 : 100343.
- www.patologie.info/standardy/66
Štítky
Patológia Súdne lekárstvo Toxikológia
Článok vyšiel v časopiseČesko-slovenská patologie

2025 Číslo 4-
Všetky články tohto čísla
- Patologie prsu – každodenní realita rutinní diagnostiky
- Svět molekulární biologie je paralelním vesmírem
- MONITOR aneb nemělo by vám uniknout, že...
- Papilární léze prsu: Diagnostická úskalí a přehled jednotek
- Imunohistochemické stanovení HER2 proteinu u karcinomů prsu – aktuální stav
- Vyšetřování prediktivních faktorů v léčbě karcinomu prsu
- Neobvyklý histopatologický nález v axilární uzlině pacientky s invazivním karcinomem NST: kazuistické sdělení a přehled literatury
- An unusual case of late recurrent adult granulosa cell tumor and mature teratoma arising within the same ovary, confirmed by NGS analysis
- Současné metody multiplexní imunohistochemie pro analýzu fixovaných tkáňových vzorků
- Česko-slovenská patologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Papilární léze prsu: Diagnostická úskalí a přehled jednotek
- Současné metody multiplexní imunohistochemie pro analýzu fixovaných tkáňových vzorků
- Patologie prsu – každodenní realita rutinní diagnostiky
- Imunohistochemické stanovení HER2 proteinu u karcinomů prsu – aktuální stav
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



