-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Kouření jako faktor ovlivňující účinnost psychofarmakoterapie
Smoking as a determinant of psychopharmacotherapy effectiveness
Tobacco smoking represents one of the most significant preventable risk factors worldwide, affecting not only somatic but also psychiatric disorders. Its prevalence is markedly higher among individuals with mental illness compared to the general population. Smoking influences both overall health status and effectiveness of pharmacotherapy, primarily through alterations in the pharmacokinetics of many drugs. The key mechanism is the induction of cytochrome P450 1A2 (CYP1A2) activity by polycyclic aromatic hydrocarbons contained in cigarette smoke. The dynamics of these changes are relatively rapid – following smoking cessation, a decline in CYP1A2 activity can be observed within several days, which may result in a sharp increase in plasma concentrations of drugs metabolized by this enzyme. Clinically relevant interactions with cigarette smoke are particularly evident in antipsychotics metabolized via CYP1A2, such as clozapine and olanzapine. Smoking may reduce their plasma concentrations by tens of percent, leading to decreased therapeutic efficacy, whereas abrupt smoking cessation may increase the risk of toxicity. Finally, a case report is presented to illustrate the clinical impact of smoking on clozapine pharmacokinetics in a patient with a psychotic disorder, emphasizing the importance of actively monitoring this factor in psychiatric practice.
Keywords:
mental disorders – pharmacokinetics – smoking cessation – clozapine – olanzapine – antipsychotic agents – cytochrome p450 – tobacco smoking
Autori: Veronika Krejčí 1,2; Tomáš Petr 3; Lucie Kališová 3
Pôsobisko autorov: Oddělení klinické farmacie, ÚVN – VFN, Praha 1; Farmakologický ústav 1. LF UK a VFN v Praze 2; Klinika psychiatrie a neuropsychiatrie 2. LF UK a ÚVN – VFN, Praha 3
Vyšlo v časopise: Čes. a slov. Psychiat., 122, 2026, No. 2, pp. 51-57.
Kategória:
doi: https://doi.org/10.48095/cccsp202601Súhrn
Kouření tabáku představuje celosvětově jeden z nejvýznamnějších preventabilních rizikových faktorů nejen somatických, ale i psychiatrických onemocnění. U osob s duševní poruchou je jeho prevalence výrazně vyšší než v běžné populaci. Kouření ovlivňuje celkový zdravotní stav i účinnost farmakoterapie, především prostřednictvím změn farmakokinetiky řady léčiv. Klíčovým mechanizmem je indukce aktivity cytochromu P450 1A2 (CYP1A2) polycyklickými aromatickými uhlovodíky obsaženými v cigaretovém kouři. Dynamika změn je přitom poměrně rychlá – po zanechání kouření dochází k poklesu aktivity CYP1A2 již během několika dnů, což může vést k prudkému zvýšení plazmatických koncentrací léčiv metabolizovaných tímto enzymem. Významný klinický dopad má interakce cigaretového kouře zejména u antipsychotik metabolizovaných přes CYP1A2, jako jsou klozapin a olanzapin. Kouření může snižovat jejich plazmatické koncentrace až o desítky procent, což v důsledku vede ke snížení účinnosti terapie. Naopak náhlé zanechání kouření může zvyšovat riziko toxicity. Závěrem je prezentována kazuistika, která ilustruje klinický dopad náhlého zanechání kouření na farmakokinetiku klozapinu u pacienta s psychotickým onemocněním a zdůrazňuje význam aktivního sledování tohoto faktoru v psychiatrické praxi.
Klíčová slova:
antipsychotika – duševní poruchy – farmakokinetika – cytochrom P450 – odvykání kouření – klozapin – olanzapin – kouření tabáku
Úvod
Prevalence kouření je u osob s duševními poruchami výrazně vyšší než v běžné populaci. Zatímco v obecné populaci kouří přibližně 20–30 % dospělých, u pacientů s psychickými poruchami se prevalence pohybuje mezi 40–80 % v závislosti na diagnóze, přičemž nejvyšší podíl kuřáků je dlouhodobě popisován u schizofrenie [1,2]. Kuřáci s vážnou duševní nemocí vykazují silnější závislost, menší povědomí o důsledcích kouření a méně pokusů s kouřením přestat [3]. Na rozdíl od obecné populace, kde prevalence kouření ve vyspělých zemích klesá, u duševně nemocných tento trend pozorován není [4,5]. Vyšší výskyt kouření u psychiatrických pacientů je dán kombinací biologických, psychologických a sociálních faktorů. Předpokládá se sdílená genetická a neurobiologická predispozice, zejména porucha systému odměny v CNS [6]. Tento mechanizmus může zároveň snižovat schopnost jednotlivce přestat kouřit. Motivace k zanechání kouření nemusí být u duševně nemocných kuřáků ve srovnání se zdravou populací zásadně narušena a s adekvátním podporou mohou dosáhnout abstinence [7]. Lidé s duševním onemocněním mají vysokou prevalenci nemocí způsobených kouřením a vysokou mortalitu z těchto příčin. Důsledkem je výrazně vyšší výskyt onkologických a kardiovaskulárních onemocnění a nižší střední délka života u této skupiny pacientů ve srovnání s běžnou populací [8,9]. Kouření může zároveň sloužit jako forma „samoléčby“ k ovlivnění úzkosti, negativní afektivity, kognitivního deficitu či nežádoucích účinků psychofarmak, především prostřednictvím účinku nikotinu na nikotinové acetylcholinové receptory a dopaminergní systém [10]. Sociální faktory, nižší důraz na léčbu tabákové závislosti v psychiatrii a omezená podpora odvykání rovněž významně přispívají k přetrvávající vysoké prevalenci kouření v této populaci [11–15]. Z pohledu farmakoterapie má kouření zásadní důsledky – chronické kuřáctví může ovlivňovat metabolizmus celé řady léčiv, vč. psychofarmak, zejména prostřednictvím indukce jaterních enzymů. Tento faktor je přitom často podceňován při nastavování, vedení a optimalizaci léčby.
Vliv kouření na metabolizmus léčiv
Kouření tabáku má různé biologické účinky, které představují významné zdravotní riziko, jak bylo uvedeno výše. Specifické nebezpečí představují rovněž farmakokinetické interakce složek cigaretového kouře s léčivy. Tyto interakce se nevyskytují v případě užívání tabáku v alternativních formách, jako jsou zahřívaný tabák (např. IQOS) nebo bezdýmné produkty (žvýkací tabák, náhradní nikotinová terapie apod.) [16–18]. Ovšem i takto užívaný nikotin může mít jiné toxikologické, fyziologické a návykové aspekty [19]. Je nutné uvést, že bezpečnost užívání těchto forem nebyla prokázána a není znám dopad na zdraví při krátkodobém a dlouhodobém užívání.
Multifaktoriální ovlivnění aktivity cytochromu CYP1A2
Aktivita CYP1A2 je výrazně ovlivněna řadou endogenních i exogenních faktorů, z nichž významné místo zaujímá expozice polycyklickým aromatickým uhlovodíkům (PAU), což jsou produkty neúplného spalování, které se nacházejí v cigaretovém kouři. Kouření indukuje expresi CYP1A2 prostřednictvím aktivace aryl-hydrokarbonového receptoru (AhR). Tím dochází ke zvýšené transkripci genu CYP1A2 a následnému zvýšení enzymové aktivity a posléze i rychlosti biotransformace některých léčiv [20,21]. Kromě kouření mohou CYP1A2 ovlivňovat i další faktory – genetický polymorfismus, zánětlivé procesy (např. zvýšené CRP snižuje aktivitu), hormonální vliv (např. estrogeny snižují aktivitu) [22]. Výsledná aktivita CYP1A2 je tedy multifaktoriálně modulovaná (obr. 1), přičemž kouření zůstává jedním z nejsilnějších známých exogenních induktorů [23].
Obr. 1. Multifaktoriální ovlivnění aktivity cytochromu CYP450 1A2. 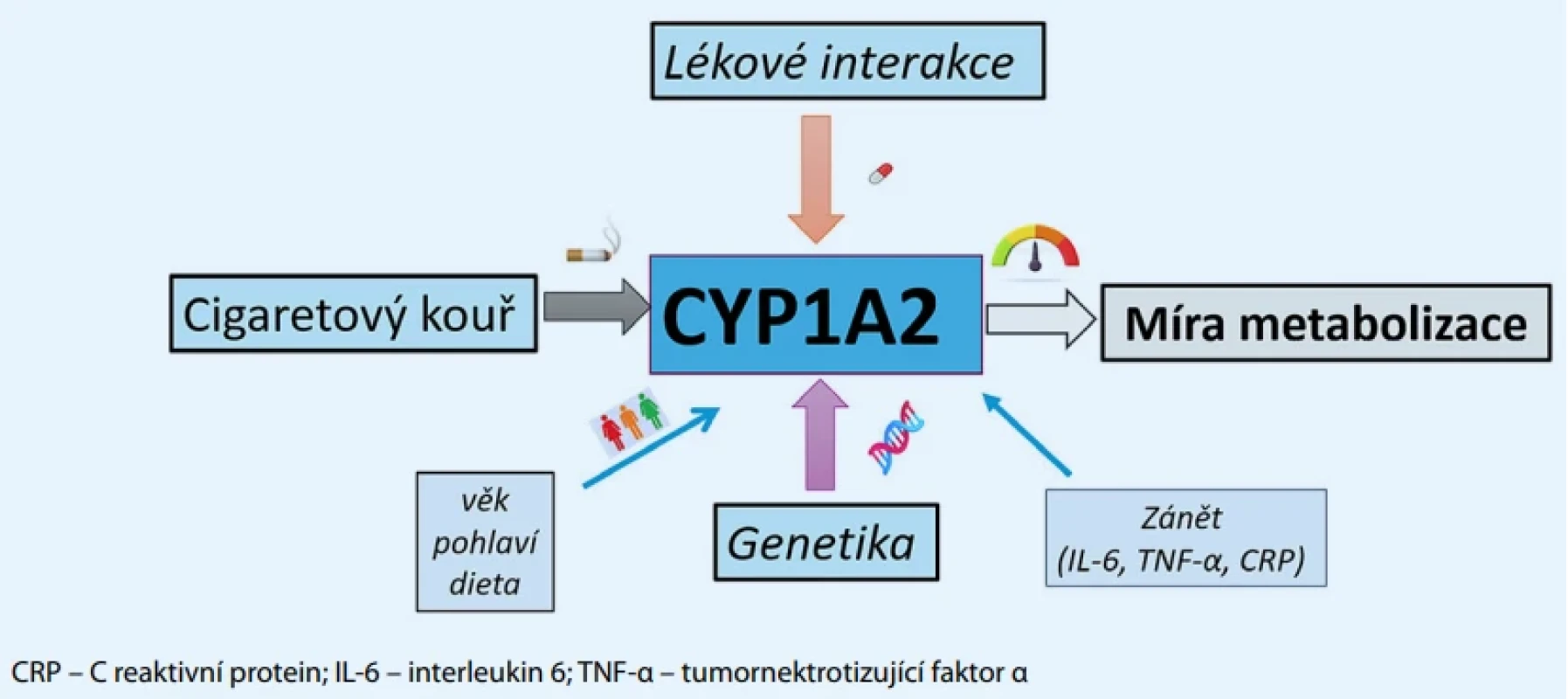
Obr. 2. Multifaktoriální ovlivnění aktivity cytochromu CYP450 1A2. 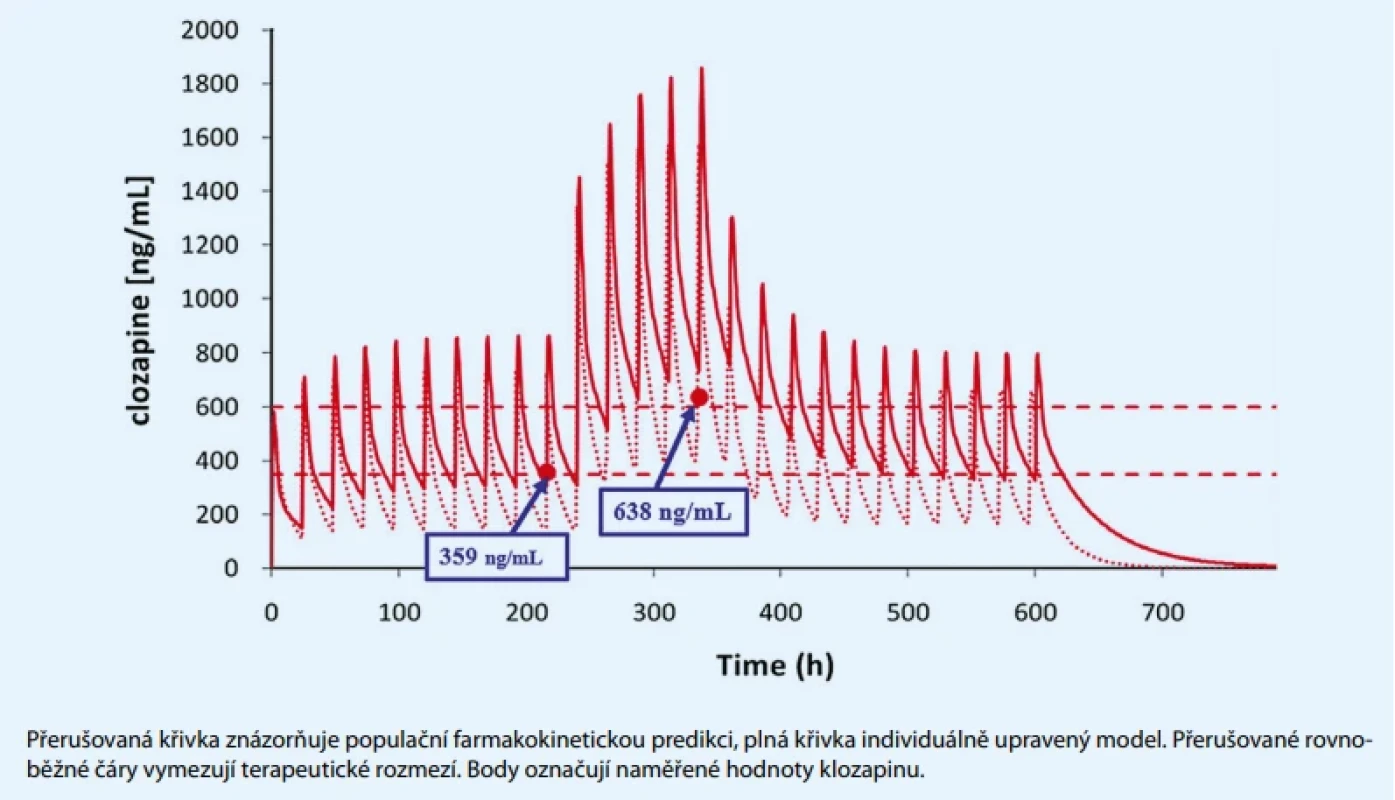
Dynamika změn aktivity CYP1A2 v závislosti na kuřáckém statu
Při náhlé změně kuřáckého chování, tedy při zanechání kouření nebo jeho opětovném zahájení, dochází k relativně rychlým změnám v aktivitě CYP1A2. Po ukončení/přerušení kouření (např. v důsledku hospitalizace) se funkce tohoto enzymu snižuje již během 1–2 dnů, přičemž maximální pokles nastává mezi 3. a 7. dnem. Podle Fabera et al. došlo u těžkých kuřáků k poklesu přibližně o 36 % během 7 dnů [24]. Tato změna vede ke zvýšení plazmatických koncentrací substrátů CYP1A2, což zvyšuje riziko nežádoucích účinků či toxicity. Naopak při zahájení kouření se indukce enzymu rozvíjí v průběhu několika dnů, přičemž maxima je dosaženo obvykle do jednoho týdne [25]. To vede ke snížení plazmatických koncentrací léčiv, což může způsobit ztrátu účinnosti léčby a klinickou dekompenzaci onemocnění. Z farmakoterapeutického hlediska je proto zásadní již během prvního týdne po změně kuřáckého statu zvážit úpravu dávkování léčiv metabolizovaných majoritně přes CYP1A2 [26].
Farmakoterapie ovlivnitelná cigaretovým kouřem
Mezi léčiva, jejichž účinnost a bezpečnost může být významně ovlivněna působením složek cigaretového kouře, patří zejména látky metabolizované majoritně izoenzymem CYP1A2. Klinicky významné je to především u léčiv s úzkým terapeutickým indexem, ve skupině psychofarmak se jedná především o klozapin a olanzapin, z dalších skupin léčiv lze uvést jako příklad teofylin (tab. 1). Kouření může snížit jejich plazmatické koncentrace o 30–60 % a tím ovlivnit jejich účinnost. Náhle zanechání kouření naopak zvyšuje potenciální riziko toxicity [27].
Tab. 1. Vybraná léčiva ovlivnitelná cigaretovým kouřem (nezohledňuje další možné vlivy na aktivitu CYP 1A2 jako např. lékové interakce). 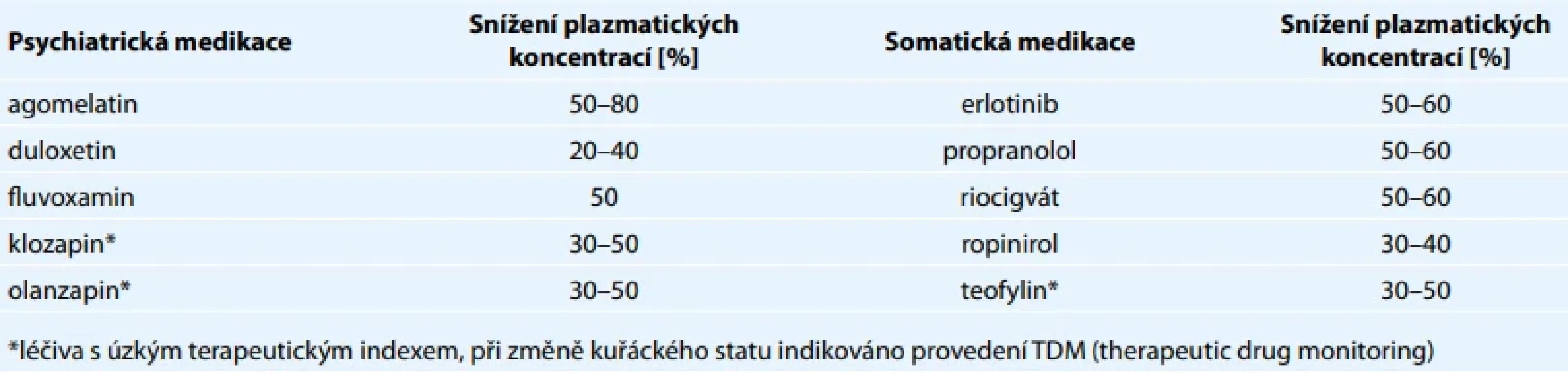
*léčiva s úzkým terapeutickým indexem, při změně kuřáckého statu indikováno provedení TDM (therapeutic drug monitoring) U léčiv uvedených v tab. 1 může změna v kuřáckém chování pacienta vést k rychlým a klinicky významným změnám farmakokinetiky. Tyto změny jsou důsledkem ovlivnění enzymové aktivity, zejména izoenzymu CYP1A2, a mohou se projevit již během několika dnů.
Při zanechání kouření dochází k poklesu indukce CYP1A2, což vede ke snížení clearance jeho substrátů a zvýšení jejich plazmatických koncentrací. V klinické praxi je proto vhodné zvážit preventivní redukci dávky přibližně o 25–30 % a/nebo zahájit častější laboratorní a fyzikální monitoraci (např. krevní obraz s diferenciálem, jaterní enzymy, krevní tlak, tepovou frekvenci, případně provedení TDM – Therapeutic Drug Monitoring). Tato opatření jsou zásadní zejména u léčiv s úzkým terapeutickým indexem metabolizovaných CYP1A2, jako jsou klozapin, olanzapin či teofylin [24,28].
Naopak při zahájení kouření lze očekávat postupnou indukci CYP1A2, což zvyšuje clearance těchto léčiv. To může vést k poklesu účinnosti léčby a vyššímu riziku relapsu psychiatrických symptomů nebo ztráty účinnosti u somatických stavů. I v těchto případech je vhodné zvážit úpravu dávkování a pečlivé klinické sledování pacienta [29]. Intenzita metabolické indukce je obecně výraznější u kuřáků, kteří kouří více než 20 cigaret denně. Při plné indukci je metabolická aktivita CYP1A2 zvýšená 1,5–1,8násobně [30].
U řady léčiv je v těchto situacích vhodné využít terapeutické monitorování léčiv (TDM), které umožňuje přesnější nastavení dávkování na základě objektivních farmakokinetických dat. U psychofarmak představuje TDM důležitý nástroj pro optimalizaci dávek antipsychotik a antidepresiv při zanechání kouření nejen v průběhu hospitalizace, což přispívá ke zvýšení bezpečnosti a účinnosti léčby. Měření plazmatických koncentrací teofylinu je rovněž dobře zavedenou a běžně dostupnou metodou, která usnadňuje individualizaci farmakoterapie. Kombinace kvantifikace koncentrace léčiva v plazmě s informacemi o farmakologických vlastnostech přípravku a individuálních charakteristikách pacienta v kontextu klinického stavu umožňuje cíleně přizpůsobit léčbu jeho potřebám [31].
Kouření jako faktor ovlivňující farmakoterapii depresivních stavů
Při volbě antidepresiv je nezbytné zohlednit vliv kouření na farmakokinetiku léčiv metabolizovaných cytochromem CYP1A2. Mezi antidepresiva významně metabolizovaná CYP1A2 patří zejména fluvoxamin, duloxetin a agomelatin (tab. 2). U kuřáků byly prokázány nižší plazmatické koncentrace těchto léčiv ve srovnání s nekuřáky, což může vést k nedostatečné léčebné odpovědi nebo mylnému hodnocení terapie jako neúčinné [24,32,33].
Tab. 2. Vliv kouření na plazmatické koncentrace antidepresiv. 
Fluvoxamin
Fluvoxamin je primárně metabolizován CYP1A2 a CYP2D6 a zároveň je silným inhibitorem CYP1A2, což činí jeho farmakokinetiku zvláště citlivou na kuřácký status. Studie ukazují, že kuřáci mohou mít až o 50 % nižší plazmatické koncentrace fluvoxaminu než nekuřáci při stejné dávce [31,32]. Klinicky se to může projevit pomalejším nástupem účinku nebo nedostatečným antidepresivním efektem.
V praxi je u kuřáků často nutná vyšší cílová dávka fluvoxaminu, obvykle v horní části dávkovacího rozmezí (200–300 mg/den), za předpokladu dobré tolerance. Zároveň je vhodné sledovat klinickou odpověď s ohledem na kuřácký status a při dostupnosti využít terapeutické monitorování léčiv (TDM), které může pomoci odlišit farmakokinetickou příčinu neúčinnosti od skutečné farmakodynamické rezistence [31].
Zásadní klinické riziko představuje náhlé zanechání kouření u pacientů léčených fluvoxaminem, kdy dochází k útlumu aktivity CYP1A2 a rychlému vzestupu plazmatických koncentrací, což může vést k nežádoucím účinkům (sedace, nauzea, tremor) [34]. V těchto případech je doporučeno včasné snížení dávky a klinické monitorování.
Duloxetin
Duloxetin je metabolizován CYP1A2 a CYP2D6. U kuřáků byly popsány signifikantně nižší sérové koncentrace, v průměru o 20–40 %, což může vést ke snížení účinnosti [24,33]. Rutinní navyšování dávky není jednoznačně doporučeno, nicméně při nedostatečné odpovědi je vhodné zohlednit kuřácký status a zvážit buď opatrnou titraci, nebo volbu jiného antidepresiva.
Agomelatin
Agomelatin je téměř výhradně metabolizován CYP1A2 a kouření může vést k významnému poklesu jeho expozice [35]. To může být jedním z důvodů selhání léčby u kuřáků, ačkoli dostupná data jsou omezenější než u fluvoxaminu. Vzhledem k užšímu dávkovému rozmezí agomelatinu je v těchto případech často racionálnější změna antidepresiva než eskalace dávky.
Při změně kuřáckého chování, ať již jde o redukci počtu cigaret, či úplnou abstinenci, dochází ke snížení indukce CYP1A2 a tím ke zvýšení plazmatických koncentrací uvedených léčiv. Tento proces probíhá dynamicky během několika dnů až dvou týdnů. Proto je nezbytné v tomto období sledovat výskyt nežádoucích účinků (zejména nauzea, poruchy spánku, gastrointestinální obtíže či zvýšená sedace u fluvoxaminu) a podle klinické situace upravit dávkování. Kontrola by měla proběhnout přibližně do 1–2 týdnů od změny kuřáckého návyku, následně pak individuálně dle klinického průběhu. Na místě je edukace pacienta o potenciálním riziku změny účinku medikace a v případě potřeby kontaktovat ambulantního psychiatra při zanechání kouření.
Farmakologické aspekty léčby klozapinem a olanzapinem u kuřáků
Velmi významná a v klinické praxi častá je interakce cigaretového kouře s klozapinem a olanzapinem, které jsou primárně metabolizovány izoenzymem CYP1A2. Kuřáci potřebují k dosažení optimálních plazmatických koncentrací vyšší dávky než nekuřáci, přičemž náhlé zanechání kouření vede k výraznému zvýšení plazmatických koncentrací (obvykle o 30–50 %, v některých případech až o 70 % a více). Tsuda et al. prokázali, že k udržení stejné plazmatické koncentrace klozapinu je u kuřáků nezbytná přibližně dvojnásobná denní dávka oproti nekuřákům [36]. Podle de Leona je korekční faktor dávky klozapinu 1,5násobek v průběhu 2–4 týdnů po změně kuřáckého návyku, zatímco Lowe a Ackman doporučují po zanechání kouření snížit dávku klozapinu o 30–40 %, aby byly zachovány původní plazmatické koncentrace [37,38].
U olanzapinu je vliv kouření sice méně výrazný než u klozapinu, ale klinicky relevantní. Kuřáci mají nižší plazmatické koncentrace oproti nekuřákům při srovnatelných dávkách a při zanechání kouření lze očekávat jejich nárůst přibližně o 30–40 %. Doporučuje se proto po ukončení kouření zvážit redukci dávky olanzapinu o 25–30 % a sledovat klinický stav pacienta, případně doplnit TDM, je-li dostupné (tab. 3) [31,34,39–42]. Optimálně se doporučuje provést stanovení plazmatické koncentrace před změnou a následně jeden týden po změně kuřáckého návyku.
Tab. 3. Doporučení pro praxi – kouření a léčba klozapinem/olanzapinem [31,34,40–42]. ![Doporučení pro praxi – kouření a léčba klozapinem/olanzapinem [31,34,40–42].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/eb3f4bb95c50ad47778678bcd19daca8.png)
TDM psychofarmak se doporučuje provádět při ustálené plazmatické koncentraci, tedy nejméně po 5 eliminačních poločasech léčiva podávaného ve stabilní dávce, u klozapinu je to asi týden a u olanzapinu až 10 dní. Je potřeba zohlednit i lékovou formu, která může měnit farmakokinetiku samotného léčiva (např. depotní přípravky antipsychotik) [31]. V praxi se odběr vzorků na stanovení plazmatické koncentrace nejčastěji realizuje v době bezprostředně před aplikací další dávky, kdy dosahují nejnižší koncentrace (trough). Pro tyto plazmatické koncentrace jsou stanovena doporučená terapeutická rozmezí. U depotních přípravků s obsahem olanzapinu se TDM provádí po dosažení ustálené plazmatické koncentrace. Vzhledem k odlišné farmakokinetice v tomto případě může trvat týdny až měsíce a odběr se následně provádí před aplikací další dávky.
Při interpretaci plazmatických koncentrací je klíčová multidisciplinární spolupráce mezi lékařem, sestrou a klinickým farmaceutem. Před úpravou dávky je nutné zohlednit terapeutický efekt, nežádoucí účinky a jejich závislost na dávce. Plazmatická koncentrace odráží stav v krevním řečišti, nikoli v centrálním nervovém systému, a obvykle jde o jednorázový odběr, nikoli průběh v čase. Interpretaci ovlivňují i individuální faktory, jako jsou distribuční objem, pohlaví, stav eliminačních orgánů, lékové interakce, změny generických přípravků či adherence. Referenční terapeutické rozmezí je orientační, je stanoveno pro dospělé pacienty (18–65 let) s psychotickými poruchami a nelze jej univerzálně aplikovat, a to zejména u dětí, seniorů či pacientů s afektivními poruchami. Klinický stav pacienta je proto vždy zásadní při rozhodování o dávce antipsychotika [31].
Kazuistika – vliv změny v kuřáckém chování na plazmatické koncentrace klozapinu
Pacient, muž ve věku 35 let, s diagnózou paranoidní schizofrenie (F20.0), BMI 26, bez přítomnosti významných somatických komorbidit. Dlouhodobě byl stabilizován na léčbě klozapinem v dávce 300 mg denně podávané ve večerní dávce. Jinou chronickou medikaci neužíval.
Pacient byl pravidelným kuřákem s dlouhodobě stabilním kuřáckým návykem, udával kouření přibližně 20–30 cigaret denně bez výraznějších změn v intenzitě kouření. Při aktivním kouření byla stanovena plazmatická koncentrace klozapinu 359 ng/ml, což odpovídalo dolní hranici terapeutického rozmezí (350–600 ng/ml) (graf 1).
Pacient byl následně hospitalizován na akutním nekuřáckém psychiatrickém oddělení, kde došlo k náhlému přerušení kouření, přičemž byla zajištěna náhradní nikotinová terapie. V průběhu hospitalizace na akutní psychiatrii byla dle potřeby ordinována fakultativní medikace klonazepam 0,5 mg 1 tableta při tenzi a úzkosti, zolpidem 10 mg při insomnii a laktulóza 20 ml 2–3× denně při zácpě.
Šestý den hospitalizace došlo k postupnému rozvoji pravděpodobně nežádoucích účinků léčby klozapinem – sedace, tachykardie a hypotenze. Jiné možné příčiny zhoršení klinického stavu byly vyloučeny. Bylo indikováno provedení TDM klozapinu a zjištěna plazmatická koncentrace 638 ng/ml, což představovalo nárůst přibližně o 78 % a mírné překročení horní hranice terapeutického rozmezí (graf 1.). Pozorovaný vzestup plazmatické koncentrace klozapinu odpovídal známému mechanizmu indukce izoenzymu CYP1A2 cigaretovým kouřem. Po přerušení kouření pravděpodobně došlo k poklesu metabolické clearance klozapinu a následnému zvýšení jeho plazmatické koncentrace.
Na základě klinického stavu pacienta a výsledku TDM byla dávka klozapinu snížena na 250 mg denně s cílem minimalizovat riziko toxicity. Pacient byl dále pečlivě sledován se zaměřením na vitální funkce a klinické projevy nežádoucích účinků. Součástí intervence byla edukace pacienta a jeho blízkých o vlivu kouření na farmakoterapii a doporučení pravidelného monitorování plazmatických koncentrací klozapinu při dalších změnách kuřáckého chování.
Závěr
Kouření tabáku představuje významný faktor ovlivňující farmakokinetiku řady léčiv, zejména těch, která jsou metabolizována prostřednictvím izoenzymu CYP1A2. Změny kuřáckého chování mohou vést k významným výkyvům plazmatických koncentrací některých léčiv, a tím ke zvýšenému riziku toxicity, nebo naopak ke snížení jejich terapeutické účinnosti. Z toho důvodu je nezbytné systematicky dokumentovat kuřácký status pacienta nejen při vstupním vyšetření, ale i v průběhu hospitalizace a ambulantní péče. Stejně důležité je předávání těchto informací při přechodu mezi jednotlivými úrovněmi zdravotní péče, zejména v propouštěcí zprávě.
Po propuštění z hospitalizace může u pacientů docházet ke změnám kuřáckých návyků, ať už k obnovení kouření, jeho omezení, nebo k přechodu na alternativní nikotinové formy. Ambulantní lékař by měl na tyto změny adekvátně reagovat, vč. případné úpravy farmakoterapie. Nedílnou součástí péče je rovněž edukace pacientů a jejich blízkých o možných důsledcích náhlého přerušení či obnovení kouření na účinnost a bezpečnost užívané medikace. Přínosné je také šíření povědomí o vlivu kouření na plazmatické koncentrace léčiv mezi zdravotníky tak, aby na změny v kuřáckých návycích pacientů správně reagovali (např. sestra v centru duševního zdraví neboli CDZ, která zjistí, že pacient přešel na elektronické cigarety, může o této změnit informovat ambulantního psychiatra, pro něhož může jít o cennou informaci v nastavování vhodné léčby).
Při jakékoli změně kuřáckého chování (zahájení, přerušení, významná změna intenzity kouření nebo přechod na alternativní nikotinové formy) je nutné pečlivě sledovat klinický stav pacienta, zvážit monitorování plazmatických koncentrací léčiv a podle potřeby flexibilně upravovat jejich dávkování. Význam TDM je zvláště patrný u látek s úzkým terapeutickým indexem, jako jsou klozapin, olanzapin či teofylin, u nichž může i relativně malá změna aktivity CYP1A2 vést k závažným klinickým důsledkům. TDM se v tomto kontextu ukazuje jako cenný nástroj umožňující individualizaci terapie. Včasné rozpoznání změn koncentrací léčiv v kontextu klinického stavu pacienta může zabránit rozvoji nežádoucích účinků a podpořit udržení terapeutické účinnosti. Tento přístup zlepšuje kvalitu péče a představuje klíčový krok k bezpečné a efektivní farmakoterapii.
Zdroje
1. World Health Organization. WHO report on the global tobacco epidemic 2023: Addressing new and emerging products. WHO 2023 [online]. Available from: https: //www.who.int.
2. Cook BL, Wayne GF, Kafali EN et al. Trends in smoking among adults with mental illness and association with federal parity law. JAMA 2014; 311 (2): 172–182. doi: 10.1001/jama.2013.284985.
3. Šagud M, Vuksan-Ćusa B, Jakšić N et al. Smoking in schizophrenia: an updated review. Psychiatr Danub 2018; 30 (Suppl 4): 216–223.
4. Fornaro M, Carvalho AF, De Prisco M et al. The prevalence, odds, predictors, and management of tobacco use disorder or nicotine dependence among people with severe mental illness: systematic review and meta--analysis. Neurosci Biobehav Rev 2022; 132 : 289–303.
5. de Leon J, Diaz FJ. A meta-analysis of worldwide studies demonstrates an association between schizophrenia and tobacco smoking behaviors. Schizophr Res 2005; 76 (2–3): 135–157. doi: 10.1016/j.schres.2005.02.010.
6. Apollonio D, Philipps R, Bero L. Interventions for tobacco use cessation in people in treatment for or recovery from substance use disorders. Cochrane Database Syst Rev 2016; 11: CD010274. doi: 10.1002/14651858.CD010274.pub2.
7. Siru R, Hulse GK, Khan RJK et al. Motivation to quit smoking among hospitalised individuals with and without mental health disorders. Aust N Z J Psychiatry 2010; 44 (7): 640–647. doi: 10.3109/00048671003627413.
8. Dineley KT, Pandya AA, Yakel JL. Nicotinic ACh receptors as therapeutic targets in CNS disorders. Trends Pharmacol Sci 2015; 36 (2): 96–108. doi: 10.1016/j.tips.2014.12.002.
9. Baca CT, Yahne CE. Smoking cessation during substance abuse treatment: what you need to know. J Subst Abuse Treat 2009; 36 (2): 205–219. doi: 10.1016/j.jsat.2008.06.003.
10. Evins AE, Korhonen T, Kinnunen TH et al. Neurobiological and behavioral mechanisms of smoking in persons with psychiatric disorders. J Dual Diagn 2013; 9 (2): 87–98. doi: 10.1080/15504263.2013.778806.
11. Poshor K, Kališová L. Proč nemocní schizofrenií kouří. Psychiatrie 2023; 27 (1): 19–24.
12. Tidey JW, Miller ME. Smoking cessation and reduction in people with chronic mental illness. BMJ 2015; 351: h4065. doi: 10.1136/bmj.h4065.
13. Petr T, Kasal M. Zkušenosti se zaváděním nekuřácké politiky na oddělení akutní psychiatrické péče v ÚVN. Čes a slov Psychiatr 2020; 116 (4): 177–182.
14. Prochaska JJ. Smoking and mental illness – breaking the link. N Engl J Med 2011; 365 : 196–198. doi: 10.1056/NEJMp1105248.
15. Center for Behavioral Health Statistics and Quality. Results from the 2016 National Survey of Drug Use and Health: Detailed tables. SAMHSA 2017.
16. Auer R, Concha-Lozano N, Jacot-Sadowski I et al. Heat-not-burn tobacco cigarettes: smoke by any other name. JAMA Intern Med 2017; 177 (7): 1050–1052. doi: 10.1001/jamainternmed.2017.1419.
17. Glasgow SM, Zacharasiewicz A, Dockrell M. Heated tobacco products: an overview. Tob Prev Cessat 2021; 7 : 36. doi: 10.18332/tpc/135095.
18. World Health Organization. Heated tobacco products (HTPs): information sheet. WHO 2020 [online]. Available from: https: //www.who.int.
19. Besaratinia A, Tommasi S. An epigenetic lens onto the post-genomic era of tobacco research. Environ Mol Mutagen 2021; 62 (1): 9–23. doi: 10.1002/em.22392.
20. Nebert DW, Dalton TP, Okey AB et al. Role of aryl hydrocarbon receptor-mediated induction of the CYP1 enzymes in environmental toxicity and cancer. J Biol Chem 2004; 279 (23): 23847–23850. doi: 10.1074/jbc.R400004200.
21. Garduño A, Wu T. Tobacco smoke and CYP1A2 activity in a U.S. population with normal liver enzyme levels. Int J Environ Res Public Health 2021; 18 (5): 2225. doi: 10.3390/ijerph18052225.
22. Zanger UM, Schwab M. Cytochrome P450 enzymes in drug metabolism: regulation of gene expression, enzyme activities, and impact of genetic variation. Pharmacol Ther 2013; 138 (1): 103–141.
23. Dobrinas M, Cornuz J, Oneda B et al. Impact of smoking, smoking cessation, and genetic polymorphisms on CYP1A2 activity and inducibility. Clin Pharmacol Ther 2011; 90 (1): 117–125. doi: 10.1038/clpt.2011.64.
24. Faber MS, Fuhr U. Time response of cytochrome P450 1A2 activity on cessation of heavy smoking. Clin Pharmacol Ther 2004; 76 (2): 178–184. doi: 10.1016/j.clpt.2004.04.003.
25. Scottish Pharmaceutical Society. Considering drug interactions with smoking. Specialist Pharmacy Service 2023 [online]. Available from: https: //www.sps.nhs.uk.
26. Oxford Health NHS Foundation Trust. Smoking cessation: effects on psychotropic and other medications. Oxford Health Formulary 2023 [online].
27. Anderson GD, Lynn AM. Optimizing CNS drug therapy in pediatrics: pharmacokinetic, pharmacodynamic, and pharmacogenetic considerations. Clin Pharmacol Ther 2009; 86 (5): 475–480.
28. Tees, Esk and Wear Valleys NHS Foundation Trust. Medicines and smoking guidance. TEWV NHS FT 2024 [online].
29. Maideen NMP. Tobacco smoking and its drug interactions with comedications involving CYP and UGT enzymes and nicotine. World J Pharmacol 2019; 8 (2): 14–25. doi: 10.5497/wjp.v8.i2.14.
30. Gee SH, Taylor DM, Shergill SS et al. Effects of a smoking ban on clozapine plasma concentrations in a nonsecure psychiatric unit. Ther Adv Psychopharmacol 2017; 7 (2): 79–83. doi: 10.1177/2045125316677027.
31. Hiemke C, Bergemann N, Clement HW et al. Consensus guidelines for therapeutic drug monitoring in neuropsychopharmacology: update 2017. Pharmacopsychiatry 2018; 51 (1–2): 9–62. doi: 10.1055/s-0043-116492.
32. Spigset O. Effect of cigarette smoking on serum levels of antidepressants. Acta Psychiatr Scand 1999; 100 (3): 203–210. doi: 10.1111/j.1600-0447.1999.tb10853.x.
33. Llerena A, Dorado P, Ramírez R et al. Pharmacokinetic variability of duloxetine: role of CYP1A2 and CYP2D6. Pharmacogenomics 2012; 13 (10): 1147–1158. doi: 10.2217/pgs.12.94.
34. Desai HD, Seabolt J, Jann MW. Smoking in patients receiving psychotropic medications: a pharmacokinetic perspective. CNS Drugs 2001; 15 (6): 469–494. doi: 10.2165/00023210-200115060-00004.
35. European Medicines Agency. Valdoxan (agomelatine): EPAR – product information. EMA 2018.
36. Tsuda Y, Saruwatari J, Yasui-Furukori N. Effects of smoking on the disposition of olanzapine and clozapine: a meta-analysis. BMJ Open 2014; 4 (3): e004216. doi: 10.1136/bmjopen-2013-004216.
37. de Leon J. Atypical antipsychotic dosing: the effect of smoking and caffeine. Psychiatr Serv 2004; 55 (5): 491–493. doi: 10.1176/appi.ps.55.5.491.
38. Lowe EJ, Ackman ML. Impact of tobacco smoking cessation on stable clozapine or olanzapine treatment. Ann Pharmacother 2010; 44 (4): 727–732. doi: 10.1345/aph.1M398.
39. Horvat M, Kadija M, Ščavničar A et al. Association of smoking cigarettes, age, and sex with serum concentrations of olanzapine in patients with schizophrenia. Biochem Med (Zagreb) 2023; 33 (3): 030702.
40. Zevin S, Benowitz NL. Drug interactions with tobacco smoking. Clin Pharmacokinet 1999; 36 (6): 425–438. doi: 10.2165/00003 088-199936060-00004.
41. Haslemo T, Eikeseth PH, Tanum L et al. Influence of smoking on the pharmacokinetics of clozapine. Eur J Clin Pharmacol 2006; 62 (12): 1049–1053. doi: 10.1007/s00228-006-0200-9.
42. Carrillo JA, Herraiz AG, Ramos SI et al. Role of CYP1A2 activity in the variability of olanzapine plasma concentrations. J Clin Psychopharmacol 2003; 23 (2): 119–127. doi: 10.1097/00004714-200304000-00003.
Štítky
Adiktológia Detská psychiatria Psychiatria
Článok vyšiel v časopiseČeská a slovenská psychiatrie
Najčítanejšie tento týždeň
2026 Číslo 2- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Hluboká stimulace globus pallidus zlepšila klinické příznaky u pacientky s refrakterním parkinsonismem a genetickou mutací
-
Všetky články tohto čísla
- Příliš otevřené dveře? Proč jsou naše ambulance přeplněny klienty, kterým neumíme správně pomoci
- Kouření jako faktor ovlivňující účinnost psychofarmakoterapie
- Pramipexol v léčbě farmakorezistentní deprese
- Diagnóza a jinakost – myšlení Emmanuela Lévinase jako inspirace pro současnou psychiatrickou praxi
- Psychiatrická klinika 1. LF UK a VFN v Praze otevřela nové Centrum denních stacionářů pro adolescenty a dospělé
- EPA 2026
- Když standardní léčba nestačí – ambulantní terapie depresivní poruchy přípravkem SPRAVATO®
- Česká a slovenská psychiatrie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Příliš otevřené dveře? Proč jsou naše ambulance přeplněny klienty, kterým neumíme správně pomoci
- Kouření jako faktor ovlivňující účinnost psychofarmakoterapie
- Když standardní léčba nestačí – ambulantní terapie depresivní poruchy přípravkem SPRAVATO®
- Diagnóza a jinakost – myšlení Emmanuela Lévinase jako inspirace pro současnou psychiatrickou praxi
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



