-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
CENTRÁLNÍ SERÓZNÍ CHORIORETINOPATIE. PŘEHLED
Autori: K. Myslík Manethová 1,2
Pôsobisko autorov: Oční oddělení, Fakultní Thomayerova nemocnice, Praha 1; Fakultní nemocnice Královské Vinohrady a 3. lékařská fakulta Univerzity Karlovy, Praha 2
Vyšlo v časopise: Čes. a slov. Oftal., 3, 2023, No. Ahead of Print, p. 1001-1013
Kategória: Recenze
doi: https://doi.org/10.31348/2023/27Súhrn
Centrální serózní chorioretinopatie (CSC) je onemocnění charakterizované serózním odchlípením neuroretiny zejména v zadním pólu oka. Často je doprovázené serózním odloučením retinálního pigmentového epitelu (RPE) a sdružené s prosakováním tekutiny do subretinálního prostoru skrze defektní RPE. CSC nejčastěji postihuje muže v produktivním věku. Přesná patofyziologie onemocnění není zcela známa. Na základě angiografického vyšetření s indocyaninovou zelení (ICG), která odhalila zvýšenou permeabilitu choroidálních cév, a optické koherenční tomografie (OCT) ukazující zvýšenou tloušťku choroidey se předpokládá choroidální vaskulopatie jako primární příčina vzniku CSC. Ve většině případů má CSC dobrou prognózu se spontánní resorpcí subretinální tekutiny (SRT) a úpravou zrakových funkcí. U malého procenta pacientů však onemocnění přechází do chronického či rekurentního průběhu a může vést k nevratným funkčním i anatomickým změnám sítnice s konečným klinickým obrazem difuzní retinální pigmentové epitelopatie (DRPE). Optimální léčebný přístup k pacientům s CSC zůstává kontroverzní. V posledních dekádách se v léčbě chronických forem CSC (cCSC) používalo nespočet léčebných přístupů; tyto zahrnovaly například laserovou fotokoagulaci, medikamentózní léčbu, standardní fotodynamickou terapii (PDT) či anti-VEGF. V posledních letech se v léčbě cCSC preferuje méně destruktivní metoda, kterou je PDT v redukovaných dávkovacích schématech, ať už s redukovanou dávkou verteporfinu nebo použité energie laserového paprsku. Je prokázána srovnatelná účinnost a bezpečnost při použití redukovaných schémat PDT u pacientů s cCSC, u kterých došlo ke zlepšení nejlépe korigované zrakové ostrosti i redukci SRT.
Klíčová slova:
Choroidální neovaskularizace – centrální serózní chorioretinopatie – retinální degenerace – multimodální zobrazení – fotodynamická terapie
ÚVOD
Centrální serózní chorioretinopatie (CSC) je onemocnění charakterizované serózním odchlípením neuroretiny zejména v oblasti zadního pólu oka [1]. Často je doprovázené serózním odloučením retinálního pigmentového epitelu (RPE) a sdružené s prosakováním tekutiny do subretinálního prostoru skrze defektní RPE. CSC nejčastěji postihuje muže v produktivním věku [2]. Přesná patofyziologie onemocnění není zcela známa. Na základě angiografického vyšetření s indocyaninovou zelení (ICG), která odhalila zvýšenou permeabilitu choroidálních cév [3], a optické koherenční tomografie (OCT) ukazující zvýšenou tloušťku choroidey [4] se předpokládá choroidální vaskulopatie jako primární příčina vzniku CSC.
Ve většině případů má CSC dobrou prognózu se spontánní resorpcí subretinální tekutiny (SRT) a úpravou zrakových funkcí. U malého procenta pacientů však onemocnění přechází do chronického či rekurentního průběhu a může vést k nevratným funkčním i anatomickým změnám sítnice s konečným klinickým obrazem difuzní retinální pigmentové epitelopatie (DRPE) [3].
Optimální léčebný přístup k pacientům s CSC zůstává kontroverzní. V posledních dekádách se v léčbě chronických forem CSC (cCSC) používalo nespočet léčebných přístupů; tyto zahrnovaly například laserovou fotokoagulaci [5], medikamentózní léčbu [6,7], standardní fotodynamickou terapii (PDT) [8] či působky proti růstovému endoteliálnímu faktoru (anti-VEGF) [9]. V posledních letech se v léčbě cCSC preferuje méně destruktivní metoda, kterou je PDT v redukovaných dávkovacích schématech (rPDT), ať už s redukovanou dávkou verteporfinu nebo použité energie laserového paprsku [10–12]. Alkin, Chan a Uetani prokázali srovnatelnou účinnost a bezpečnost při použití redukovaných schémat PDT (reduced-dose nebo reduced-fluence PDT) u pacientů s cCSC, u kterých došlo ke zlepšení nejlépe korigované zrakové ostrosti (NKZO) i redukci SRT, přičemž nebyly zaznamenány žádné komplikace ve sledovaném souboru [13–15].
V České repulice dosud neexistují standardy pro léčbu této klinické jednotky. A protože onemocnění postihuje typicky mladší pacienty v produktivním věku s vysokými nároky na kvalitu zraku, zůstává nadále správné načasování a stanovení léčby akutní, zejména pak chronické formy CSC výzvou. Zatímco dříve se léčba opírala výhradně o laserové ošetření sítnice [16], v posledních letech se v léčbě zvláště chronických forem CSC uchyluje k šetrnějším metodám, jakými jsou PDT nebo intravitreální aplikace antiangiogenních látek [17,18].
HISTORIE
Historicky prvně bylo onemocnění makuly s rekurentním serózním odchlípením sítnice popsáno v roce 1866 von Graefem jako rekurentní centrální retinitis [19]. Téměř o sto let později roku 1955 použil Bennet pojem centrální serózní retinopatie, neboť se domníval, že tekutina pochází z prosakujících retinálních cév nikoliv na podkladě zánětu, nýbrž angiospasmu [20]. V 60. letech, díky uvedení fluorescenční angioskopie do klinické praxe, Maumenee zjistil, že tekutina pod sítnici proniká skrze poškozený RPE [21]. Díky dalšímu studiu charakteristik fluorescenční angiografie (FAG) u CSC poskytl Gass v roce 1967 detailnější pohled na patogenezi onemocnění, klinický obraz a poukázal, že CSC postihuje obojí – sítnici i choroideu. Zavedl nově termín idiopatická centrální serózní choroidopatie [22]. Vzhledem k tomu, že zvýšená permeabilita choroidálního řečiště vedoucí k průsaku tekutiny skrz poškozený RPE a následně k odchlípení neurosenzorické části retiny se obecně uznává jako příčina vzniku onemocnění, přiklání se současné názvosloví k pojmu centrální serózní chorioretinopatie [23].
Při vyšetření chorioretinálních onemocnění zaznamenalo v posledních letech velký rozmach tzv. multimodální zobrazení. Díky novodobým vyšetřovacím technikám (“enhanced depth imaging” OCT, “swept-source” OCT, OCT-angiografie) je CSC vedle polypoideální choroidální vaskulopatie, pachychoroidní neovaskulopatie a pachychoroidní pigmentové epiteliopatie nově řazena k tzv. pachychoroidním onemocněním, u nichž je klíčovým znamením zvýšená tloušťka choroidey (řecká předpona pachy – znamená tlustý) [24]. Pro CSC je dále typická dilatace Hallerovy vrstvy choroidálních cév a komprese nad nimi ležící choriokapilaris [25].
SYMPTOMY, DEMOGRAFIE, RIZIKOVÉ FAKTORY
Onemocnění je charakterizováno nejprve mírným rozostřením vidění, které je následováno různým stupněm poklesu centrální zrakové ostrosti (ZO) (6/6–6/60), mikropsiemi, deformací obrazu, hypermetropizací, snížením kontrastní citlivosti, změnou vnímání barev, různým stupněm centrálního skotomu. Symptomy bývají většinou dočasné a častěji jednostranné, i když oboustranné postižení je poměrně frekventní [23]. Ne zřídka může CSC probíhat asymptomaticky nebo může být serózní odchlípení sítnice zachyceno zcela náhodně při léčbě kontralaterálního postiženého oka [25]. Incidence CSC je odlišná v různých etnických skupinách. Vyšší incidence je udávána mezi Asiaty a bělochy v porovnání s černošskou populací. U Asiatů je také častěji popisován bilaterální a multifokální charakter onemocnění [26]; vysoké ablace RPE a neuroretiny, jež jsou častější právě u asijské populace, mohou být mylně považovány za Haradovu nemoc [27]. Predominantně bývají postiženi muži mezi 30.–50. rokem (průměrná incidence výskytu onemocnění u mužů a u žen je v poměru 8–9 : 1) [28,29]. Spaide ve své práci uvedl průměrný věk pacientů s CSC 51 let, zároveň ale připustil, že u starších pacientů, u nichž se onemocnění může s větší pravděpodobností projevovat difuzním rozpadem RPE nebo přítomností sekundární choroidální neovaskularizace (CNV), se mohly prvotní známky onemocnění vyskytnout léta před stanovením diagnózy [3]. Věkem podmíněná makulární degenerace (VPMD) s CNV může v některých případech připomínat CSC, proto u pacientů nad 50 let je nutné VPMD vyloučit [30]. Navzdory skutečnosti, že onemocnění má idiopatický charakter, je známo, že CSC bývá častěji asociována se stavy endogenního hyperkortizolismu (např. u Cushingova syndromu, těhotenství) a u dlouhodobé systémové léčby glukokortikoidy (léčba roztroušené sklerózy, astmatu, Crohnovy choroby), kdy dochází ke zvýšené adrenergní stimulaci určitých tkání ovlivňující změny krevního tlaku a tkáňovou homeostázu [31–33]. Dále je zvýšená incidence CSC popisována u žen v průběhu těhotenství (stav se zvýšenou hladinou volného cirkulujícího endogenního kortizolu), u pacientů po orgánové transplantaci s chronickým užíváním imunosupresiv a kortikoidní terapie či jako důsledek protrahované stresové zátěže [32,34,35]. Poměrně značný význam je přisuzován i psychosociálním aspektům. Horniker v roce 1927 jako první naznačil souvislost mezi psychickým rozrušením a zvýšeným rizikem rozvoje CSC; onemocnění sám označoval jako retinitis centralis angioneurotica [36]. Ovšem až v roce 1986 Yannuzzi definitivně prokázal asociaci mezi CSC a tzv. osobností typu „A“ (tj. osobnost koronární se sklonem k časnému rozvoji kardiovaskulárního onemocnění). Tato asociace je dána pravděpodobně zvýšenou hladinou katecholaminů v cirkulaci [37]. V českém oftalmologickém slangu se CSC označuje jako “nemoc manažerů”. Podle dalších literárních zdrojů byla zvýšená incidence onemocnění popsána i u pacientů užívajících inhibitory fosfodiesterázy typu 5 pro erektilní dysfunkci [38], sympatomimetické látky jako pseudoefedrin, oxymetazolin, 3,4-methylendioxy-N-methylamfetamin [39] či při vyšší konzumaci alkoholu [35]. Mateo-Montoya a jiní prokázali zvýšenou incidenci u pacientů s pozitivitou testu na Helicobacter pylori, jehož přítomnost může vyvolat i extraintestinální onemocnění včetně CSC (ureáza, kterou Helicobacter pylori produkuje, aktivuje krevní destičky, což v oblasti choroidey může vést k vaskulární kongesci a následně choroidální ischemii) [40,41]. Hypertenze, spánková obstrukční apnoe, kouření, alkohol, antihistaminika, alergická respirační onemocnění jsou v literatuře další uváděné rizikové faktory [42].
Ačkoliv se jedná o získané onemocnění, genetická vnímavost hraje v patofyziologii CSC důležitou roli stejně jako genetický polymorfismus [43]. Pravděpodobná spojitost mezi genem pro komplementový faktor H a CSC byla prokázána několika na sobě nezávislými studiemi [44–46]. Přesný mechanismus vlivu faktoru H v patogenezi CSC však není znám.
PROGNÓZA
CSC se může vyskytovat ve 2 základních formách – akutní a chronické. Určení chronicity onemocnění není autoritami přesně definováno. Někteří autoři definují chronicitu jako perzistující SRT po dobu 6 měsíců [47], zatímco recentní klinické studie se přiklání k délce trvání onemocnění minimálně 3 měsíce [12]. Ve většině případů akutních forem CSC dochází do 3 měsíců od propuknutí nemoci ke spontánní resorpci SRT s úpravou zrakových funkcí s konečnou centrální ZO nezřídka 0,8 a lépe (v 80–90 % případů) [48]. Avšak i přes zlepšení centrální ZO si pacienti po odeznění onemocnění mohou stěžovat na dyschromatopsii (poruchu barevného vnímání), snížení kontrastní citlivosti, metamorfopsie (vnímání deformovaného obrazu), centrální skotom, vzácně šeroslepost. Podle výsledků práce Oota a kolektivu, kteří zkoumali denzitu čípků makulární krajiny u pacientů s výslednou ZO 20/20 a lepší, došlo i po resorpci SRT a při zachování elipsoidní zóny (EZ) ke snížení hustoty čípků v původně postižené oblasti [49]. Tato data mohou vysvětlit reziduální zrakové obtíže i u pacientů s vynikající výslednou ZO a kompletní anatomickou úpravou. Samotné stanovení NKZO tak nemusí plnohodnotně reflektovat skutečnou kvalitu zrakových funkcí u pacientů s CSC. CSC může vést k trvalému poškození zraku, pokud se SRT nevstřebá nebo se ataky opakují, stav tak přechází do chronického stadia. Až 52 % postižených zaznamená rekurenci onemocnění do 1 roku od první ataky [50]. Dlouhotrvající odchlípení neuroretiny vede k buněčné smrti fotoreceptorů, progresi atrofie RPE, subretinální fibróze, rozvoji sekundární CNV či cystoidní makulární degeneraci a tím k permanentnímu snížení zrakových funkcí s centrální ZO 0,1 a horší. Konečný klinický obraz je prezentován DRPE, nad níž může, ale také nemusí být přítomná SRT [23].
PATOFYZIOLOGIE ONEMOCNĚNÍ
Přesná patofyziologie onemocnění není do detailu známa a předpokládá se, že zahrnuje poněkud různorodou etiologii a mechanismy vedoucí ve svém důsledku k rozsáhlým abnormalitám choroidální cirkulace a následnému porušení RPE [51]. Díky novým zobrazovacím a vyšetřovacím technikám vzniklo několik teorií vysvětlujících možný vznik onemocnění; každá se svým způsobem může na vzniku a progresi onemocnění alespoň z části podílet. Vhled do problematiky patofyziologie CSC a její dynamiky poskytují nejlépe fluorescenční a indocyaninová angiografie. Anatomické poměry oka při CSC pak nejlépe zachycuje OCT (zejména pak její hloubkové zobrazení tzv. enhanced depth imaging EDI-OCT) a OCT-angiografie – OCT-A).
Teorie dysfunkce choroidey
Současné chápání patogeneze CSC klade největší důraz na roli choroidey. Již Gass se domníval, že fokální zvýšení permeability choriokapilaris je primární příčinou poškození nad ní ležící vrstvy RPE vedoucí k odloučení RPE, seróznímu odchlípení neuroretiny a u přibližně 10–15 % pacientů k formaci sérofibrinózních subretinálních exsudátů [1]. Zvýšení permeability choroideálního řečiště je pravděpodobně způsobeno stázou v cévním řečišti choroidey, ischemií nebo zánětem, čemuž nasvědčuje zvýšená fluorescence vnitřní choroidey zejména ve střední části ICG angiogramu [3,52]. Guyer a kolektiv navrhl potenciální model patogeneze CSC založené na ICG-videoangiografii (ICG-V). ICG angiogram odhalil dilataci velkých choroidálních cév a multifokální ložiska hyperfluorescence prakticky ve všech choroidálních vrstvách. Autoři zaznamenali difuzní ložiska hyperpermeability v okolí aktivních prosakujících míst, které byly patrné na ICG-V nikoliv však při vyšetření FAG. Proto dospěli k závěru, že hyperpermeabilita byla spíše na úrovni choroidey, která je lépe vyšetřitelná pomocí ICG, než-li na úrovni RPE, jehož stabilita je lépe patrná na FAG. Choroidální hyperpermeabilita zvyšuje hydrostatický tlak v choroidálním prostoru, který dále zvyšuje nároky na vrstvu RPE; vede k jeho odchlípení, zeslabení, defektu až dekompenzaci. Následně dochází k průsaku, tedy difúzi vody, elektrolytů a proteinů do subretinálního prostoru, čímž dochází k odchlípení neurosenzorické části sítnice [53]. Narušené buňky RPE zároveň ztrácí svoji schopnost pumpovat tekutinu v retrográdním směru – tedy ze subretinálního prostoru do oblasti choroidey. Buňky RPE mohou dokonce fokálně ztrácet svoji polaritu a aktivně pumpovat tekutinu do subretinálního prostoru [54]. Stav limituje absorpci SRT a rozhoduje tak o velikosti, tvaru nebo chronicitě serózního odchlípení neuroretiny a/nebo RPE. Spontánní resorpce tekutiny může nastat, jestliže se zhojí defekt v RPE a zároveň je-li funkce RPE alespoň částečně zachována. Příčina zvýšené permeability není zcela známa, avšak předpokládá se, že stáza ve venózní části choroidálního řečiště, choroidální ischemie či zánět mohou hrát důležitou roli [52,55,56]. Ve studii Prunteho a Flammera dilatované kapiláry a drénující venuly v jednom nebo více choroidálních lobulech následované ložiskovým zpožděním v arteriálním plnění mohou vysvětlit příčinu poškození vrstvy RPE nad těmito ložisky zvýšené choroidální propustnosti. Tyto závěry podporují myšlenku lokálního lobulárního choroidálního zánětu či ischemické choroiditidy [52]. Abnormální regulace krevního průtoku choroideou může být hlavním mechanismem vedoucím ke změnám typických pro „pachychoroideu“ [57]. Primární role choroidey je nově podpořena nálezy na EDI-OCT prokazujícími zvýšenou tloušťku této vrstvy u pacientů s CSC [4].
Z výše uvedeného vyplývá, že intenzivní exsudace choroidálního řečiště u aktivní CSC je způsobena primárně narušením cévní stěny, abnormalitou nebo poruchou autoregulace choroidálního krevního toku [58], nikoliv přítomností CNV. Důkazy hovořící pro choroidální vaskulopatii v etiopatogenezi CSC jsou silné, ovšem stále chybí přesně vymezit základní mechanismus vzniku choroidální léze.
Teorie dysfunkce RPE
Dysfunkce RPE zaujímá významnou roli v patogenezi CSC, i proto zastánci této teorie upřednostňují poruchu na úrovni RPE jako primární příčinu vzniku onemocnění [59–61]. FAG u pacientů s aktivní CSC odhaluje jeden či více zdrojů průsaku způsobujících serózní odchlípení retinálního pigmentového listu a/nebo neuroretiny. Typický nález na FAG demonstruje tekutinu proudící do subretinálního prostoru skrze defekt pevných spojení mezi buňkami retinálního pigmentového listu. Tato fokální ložiska průsaku skrze RPE, jež jsou typická pro akutní formu CSC, byla prvním vodítkem ke stanovení patogeneze onemocnění a byla považována za primární příčinu akumulace SRT [48]. Ačkoliv je dnes široce uznávána spíše teorie dysfunkce choroidey, úloha RPE hraje v průběhu onemocnění zásadní roli. Na rozdíl od akutní formy CSC, kdy dochází k poškození jedné nebo několika málo buněk RPE a se zánikem těchto zdrojů průsaku serózní odchlípení ve většině případů regreduje spontánně, u chronické formy reprezentované difuzním rozpadem RPE (dobře patrný na autofluorescenci i FAG) dochází k plošnému porušení RPE jako zevní hematookulární bariéry a schopnosti pumpovat tekutinu v retino-choroidálním směru, což vede k chronické kumulaci tekutiny v subretinálním prostoru a dalšímu poškození buněk RPE [23].
Teorie kombinované dysfunkce choroidey a RPE
Pravděpodobně se na vzniku a průběhu onemocnění podílí obě teorie, tedy zvýšená propustnost choroidálních cév, elevace hydrostatického tlaku v choroidey a narušená funkce RPE [23].
Role kortikoidů v rozvoji CSC
CSC indukovaná kortikosteroidy byla poprvé popsána v roce 1984 [62]. Od té doby byla publikována řada klinických i experimentálních prací dokazujících, že endogenní i exogenní kortikosteroidy přispívají k rozvoji CSC [31,63–66]. Jampol a spol. ve své publikaci uvedli, že kortikosteroidy mohou zvyšovat citlivost choroidálních cév nebo buněk RPE na efekt endogenních katecholaminů [67]. CSC byla častěji zachycena i u pacientů s vyšší hladinou endogenních kortikoidů (Cushingův syndrom, těhotenství, stres), podobně jako u pacientů s hyperkortizolismem v důsledku léčby očních (uveitida, skleritida, neuritida optiku) či systémových nemocí (asthma bronchiale, hepatitida, alergická rinosinusitida) [31–33,68–71]. Existují důkazy o vlivu glukokortikoidů na transkripci a expresi adrenergních receptorů, pro což svědčí dlouhodobý efekt kortikoidů na genomové úrovni zprostředkovaný intracelulárními receptory. Na buněčné úrovni dochází vlivem glukokortikoidů k zvýšené expresi beta-adrenergních receptorů [72]. Na molekulární úrovni prokázali stejní autoři glukokortikoidní efekt na expresi beta-adrenergních receptorů přítomností vyšší hladiny intracelulární receptorové mRNA. Podobně i Sakaue zjistil, že exprese a zvýšení množství alfa-1ß-adrenergních receptorů na povrchu buněk je indukováno glukokortikoidy [73]. Ovlivnění exprese na genomové úrovni není okamžité a je dáno dlouhodobou expozicí vyšších hladin kortikosteroidů. Účinek kortikoidů na non-genomové úrovni je promptní a je dán jejich přímou interakcí s glukokortikoidními receptory již přítomnými na buněčných membránách; tyto zahrnují iontové kanály nebo receptory pro neurotransmitery [67,74]. Jejich aktivací dochází k poškození endotelových buněk choriokapilaris, a tedy k její vyšší permeabilitě a degeneraci nad ní ležící vrstvy RPE [37,75].
Patofyziologie ztráty ZO u CSC
Zeslabení foveolární krajiny, cystoidní makulární degenerace, poškození fotoreceptorů centrální krajiny jsou považovány za důvody snížení centrální ZO u CSC [76,77]. Cystoidní makulární degenerace byla prvně popsána Iidou jako cystoidní intraretinální dutiny bez průkazu průsaku na FAG [76]. Délka onemocnění nejméně 5 let a subretinální fibróza jsou považovány za hlavní rizikové faktory [77]. Klíčovým faktorem výsledných zrakových funkcí je zachování zevních retinálních vrstev. Ztráta fotoreceptorů a buněk RPE vede při dlouho trvajícím odchlípení neuroretiny k významnému snížení zrakových funkcí [78].
KLASIFIKACE CSC
Cílem jakékoliv klasifikace onemocnění je rozdělit širokou škálu projevů jednoho onemocnění do podkategorií, které nám pomohou určit jeho pravděpodobný vývoj, prognózu a co nejvhodnější plán léčby. Doposud bylo publikováno několik klasifikací CSC, ale žádná plnohodnotně neobsáhla všechny projevy nemoci. Velmi zjednodušeně se onemocnění až doposud dělilo na akutní a chronickou formu [23]. Daruich a kol. recentně navrhl novou klasifikaci, která jednotlivé (i vzácné) projevy CSC zahrnuje [79] a tato klasifikace je nyní obecně uznávaná [80]:
1) Akutní CSC: Nejčastější typ postihující spíše mladší pacienty a způsobující akutní lokalizované odchlípení RPE a/nebo neuroretiny s mírným až středním zhoršením zrakových funkcí. Na FAG nalézáme jeden nebo více zdrojů prosakování barviva. V 95 % dochází ke spontánní resorpci SRT a úpravě zrakových funkcí, může však u některých pacientů zanechat poruchu vnímání barev [81].
2) Perzistující CSC: SRT v určitém procentu případů přetrvává déle než 3 měsíce. U těchto pacientů zpravidla indikujeme novou FAG/ICG, abychom mohli identifikovat místa průsaku. Výsledkem angiografie může být průsak v původním místě, nový zdroj průsaku či žádná prokázaná aktivita. Pokud se prokáže nový zdroj průsaku, pak je onemocnění považováno za perzistující.
3) Rekurentní CSC: Je definována jako opětovná přítomnost SRT po jejím zdokumentovaném kompletním vstřebání a vzniká až u 50 % pacientů v prvním roce nemoci [82]. Na FAG můžeme nelézt stejný zdroj průsaku či de novo vzniklý hot-spot.
4) Chronická CSC: Serózní elevace RPE a/nebo neuroretiny trvající déle než 3 měsíce na podkladě chronických změn a alterace funkce RPE. Dlouhotrvající odchlípení neurosenzorické sítnice vede k dalšímu prohlubování alterace RPE, vzniku typických plošných atrofických stop RPE a atrofii fotoreceptorů [83]. Tato varianta bývá ve svém pokročilém stádiu nazývána také jako DRPE a je typická různým rozsahem ložisek atrofie RPE s nebo bez odchlípení neuroretiny [84].
5) Inaktivní CSC: Případy s anamnézou CSC epizody, avšak toho času bez známek SRT.
Vedle výše uvedených základních typů existuje i menší skupina pacientů, u kterých má CSC atypický klinický obraz:
Atypická CSC: U pokročilých chronických forem (trvajících několik let) se vedle přetrvávající serózní ablace neuroretiny a mnohačetných atrofických ložisek RPE mohou vyskytovat cystoidní makulární degenerace [76], multifokální CSC [85] či nepravidelné ploché ablace RPE (tzv. wavy RPE), pod kterými se může skrývat již počínající sekundární CNV typu I [86,87]. CNV na podkladě CSC nebývá zcela zřetelně prokázána na FAG, mnohdy ani na ICG, nově však může být s velkou senzitivitou i specificitou detekována pomocí OCT-A [88,89].
Bulózní CSC: Vzácnou klinickou variantou chronické CSC je bulózní serózní odchlípení sítnice (Obrázek 1). Maximum SRT bývá vlivem gravitace v dolních kvadrantech, někdy můžeme dokonce nalézt masivní ložiska subretinálního fibrinu [90].
Obr. 1. Barevné foto fundu, sken optické koherenční tomografie a fluorescenční angiografie (Visucam Zeiss, Heidelberg Spectralis, Myslík Manethová) 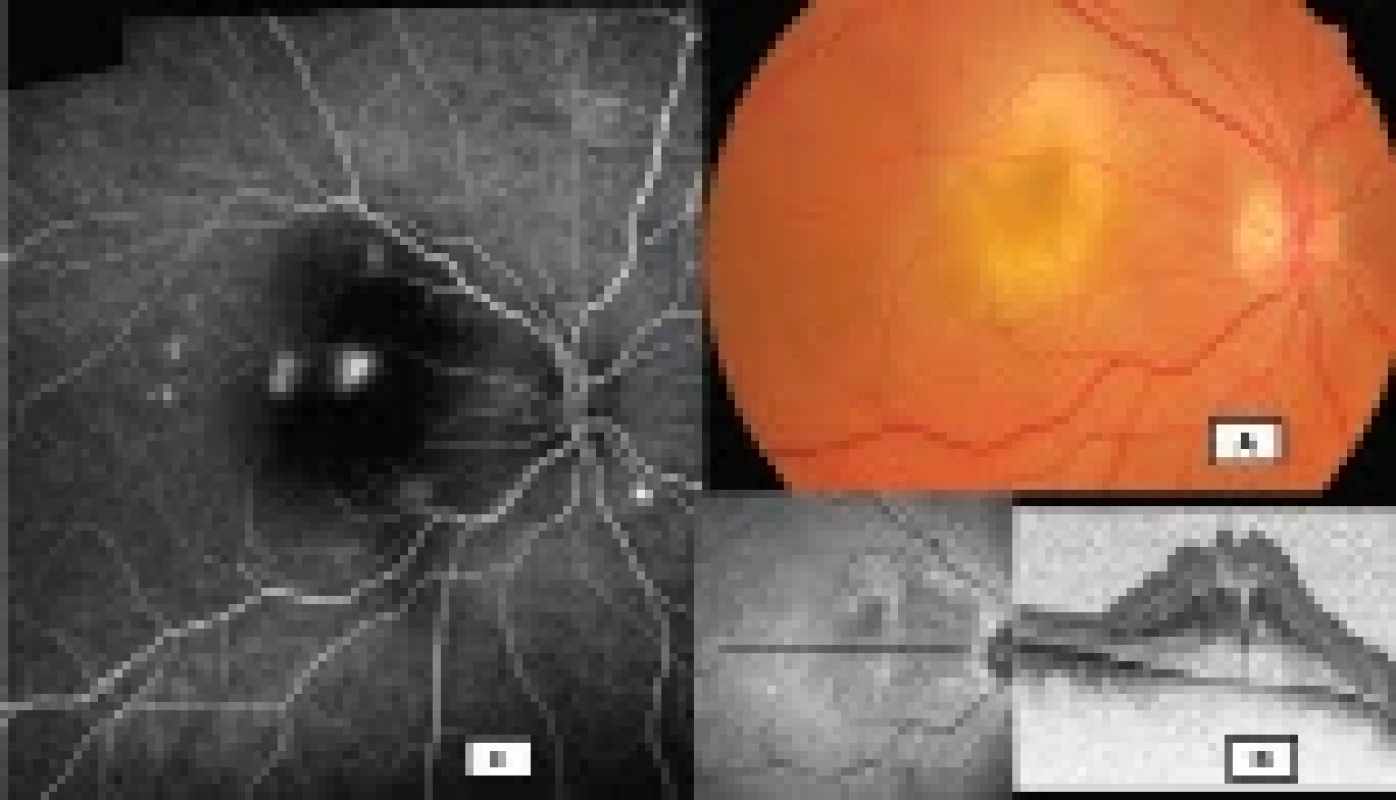
u 38letého pacienta s atypickou – bulózní – formou centrální serózní chorioretinopatie:
(A) barevný snímek excesivní žlutavé subretinální fibrinové exsudace v centru makuly s radiálním řasením
sítnice, (B) transfoveolární lineární sken se subretinální hyperreflexivní masou a výraznou destratifikací vnitřních retinálních
vrstev, (C) širokoúhlá fluorescenční angiografie s mnohačetnými aktivními hot-spoty různé intenzityVYŠETŘOVACÍ METODY CSC
Vyšetření zrakové ostrosti do dálky
Vyšetření ZO patří mezi základní a nejdůležitější funkční oční vyšetření. V běžné praxi jsou nejčastěji používané Snellenovy optotypy, které však neumožňují standardizované vyšetření, změna velikosti písmen mezi řádky není pravidelně progresivní, písmena mají různou obtížnost čitelnosti. Přesnější určení ZO je dosaženo užitím ETDRS optotypů. Jejich výhodou je stejný počet písmen v řádku, stejná obtížnost čitelnosti jednotlivých znaků, přičemž dodržují geometrickou progresi velikosti optotypů v jednotlivých řádcích. Opakované testování vykazuje oproti Snellenově metodice velmi podobné výsledky, které je možné použít v klinickém výzkumu a poskytují detailnější (jemnější) změny hodnot zrakové ostrosti ve sledovaném období.
Biomikroskopické vyšetření očního pozadí
Při biomikroskopickém vyšetření pacienta s CSC odhalujeme typické odchlípení neuroretiny, které je patrné jako ostře ohraničený, transparentní „puchýř“ na zadním pólu oka. Foveální reflex nebývá zpravidla patrný, spíše bývá nahrazen tzv. haló efektem daným odrazem světla od odloučené neuroretiny. Retina v místě odchlípení je normální tloušťky beze změny transparence. Fovea může mít v biomikroskopickém obrazu až lehce nažloutlou barvu danou zviditelněním xantofylu centrální části sítnice. Mohou být přítomny četná žluto-bělavá fibrinová depozita pokrývající zadní plochu elevované neuroretiny [23]. Typické jsou nepravidelnosti RPE, které se zdůrazňují s chronicitou stavu. Při důkladné biomikroskopii (následně ověřené pomocí OCT) můžeme nalézt jedno či více ložisek serózního odchlípení RPE. Subretinální tekutina může v případě dlouhého trvání nemoci stimulovat fibrotické změny, které mohou vést k trvalým funkčním změnám. Ve většině případů však dochází k postupné resorpci fibrinových depozit. Podmínky predisponující k exsudaci fibrinu jsou rozsáhlé či mnohačetné PED (ablace RPE), chronická nebo rekurentní forma onemocnění, systémová léčba kortikosteroidy, těhotenství, orgánová transplantace [23].
V případech excesivní exsudace může dokonce docházet až k bulóznímu seróznímu odchlípení sítnice s maximem v dolních kvadrantech [90]. U chronických forem je typická spíše plochá serózní separace neuroepitelu nad ložisky dystroficky změněného RPE, které může místy přecházet až do plošné atrofie. Tyto atrofie se nejčastěji nachází v makulární a peripapilární krajině a vlivem gravitace při chronické exsudaci „zatékají” směrem dolů (Obrázek 2) [91].
Obr. 2. Fluorescenční angiografie 54letého pacienta s chronickou formou centrální serózní chorioretinopatie (Heidelberg Spectralis, Myslík Manethová): 
širokoúhlé zobrazení pozdní venózní fáze s širokým ložiskem difuzního
rozpadu retinálního pigmentového listu a typickou gravitační stopou nad terénem dystroficky změněného retinálního
pigmentového epitelu při dlouhodobé subretinální exsudaciZOBRAZOVACÍ METODY CSC
Barevné foto očního pozadí
Na podobném zobrazovacím principu jako je nepřímá oftalmoskopie jsou založeny přístroje umožňující záznam obrazu sítnice na klasické či digitální fotografie. Foto očního pozadí je vhodné k hodnocení stavu, monitorování progrese a efektu léčby onemocnění. V současnosti je metoda postupně nahrazována technikami, které aktuální klinický nález i jeho vývoj v čase zachytí ve větších detailech (OCT, FAG/ICG, OCT-A). Přesto má barevná fotka očního pozadí stále své místo zejména ve fotodokumentaci atypických či vzácnějších forem CSC.
Fluorescenční angiografie
Fluorescenční angiografii považujeme za nejstarší a zároveň základní vyšetřovací techniku pro stanovení diagnózy, zhodnocení nálezu i vyloučení ostatních diferenciálních diagnóz u CSC. FAG je invazivní zobrazovací metoda, která slouží k vyšetření průtoku krve zejména retinálním a v menší míře choroidálním cévním řečištěm za použití kontrastní látky aplikované intravenózně (sodná sůl fluoresceinu). Vyšetření poskytuje dynamické informace o stavu vnitřní i zevní hemato-okulární bariéry a částečně o kondici vrstvy RPE.
Charakteristickým nálezem v časné fázi angiogramu je přítomnost jednoho či několika zdrojů prosakování barviva na úrovni defektního RPE s postupně se zvyšující fluorescencí a rozsahem do pozdní venózní fáze, tzv. “inkblot”. Přibližně v 10 % případů je patrná typická formace tzv. „smokestack“, kdy barvivo pozvolna difunduje do prostoru serózního odchlípení neuroretiny a vytváří tak obraz podobný stoupajícímu „kouři z komína“ [23].
U chronických forem onemocnění nemusí být zastiženy žádné jednoznačné bodové zdroje hyperfluorescence, ale spíše oblasti s difuzním window defektem v časných fázích a zvýšené plošné fluorescence v pozdních fázích angiogramu, které jsou patrné u difuzních atrofických změn RPE u chronických stádií onemocnění. Dle charakteru nálezu a dynamiky změn v průběhu angiogramu lze posuzovat míru aktivity onemocnění a tím zvolit adekvátní léčebný přístup [48,92–94]. Cystoidní makulární degenerace či CNV na podkladě CSC nemusí být FAG zcela prokazatelná a vždy je benefitem použít multimodální zobrazení pro větší pravděpodobnost záchytu všech abnormalit a pro vyslovení správné diagnózy [76,89].
FAG se považuje za základní vyšetřovací metodu u tohoto onemocnění a slouží jako předloha pro eventuální ošetření sítnice laserovou koagulační stopou v místě bodové hyperfluorescence zaznamenané v časné fázi angiogramu nebo laserovou termostimulační stopou při fotodynamické terapii v místě plošné hyperfluorescence v pozdních fázích angiogramu. FAG je též prospěšná v diferenciální diagnostice a umožňuje vyloučit onemocnění, která mají s CSC podobný klinický obraz (Vogt-Koyanagi-Harada syndrom, CNV při VPMD, infekční onemocnění zadního segmentu oka apod.).
Indocyaninová angiografie (ICG)
ICG angiografie rozšířila znalosti o patogenezi tohoto onemocnění. Díky svým vlastnostem detekuje zejména hlubší vrstvy – choroideu – tedy místo vzniku patologie. Princip vyšetření se shoduje s postupem při fluoresceinové angiografii, pouze je jako barvivo použita indocyaninová zeleň, která je velmi rychle vázána na bílkoviny krevní plazmy (98 %). Po expozici excitačním světlem ICG emituje fluorescentní světlo o vlnové délce v intervalu 805–835 nm, což vysvětluje poměrně vysokou transmisi skrze oční tkáně (xantofyl a melanin RPE, opalescentní čočka, choroidea). Z tohoto důvodu je ICG angiografie vhodná pro vizualizaci choroidální vaskulární sítě a nabízí proto přesné zhodnocení rozsahu choroidální léze u pacientů s CSC [48,55,56]. V úvodní fázi angiogramu se zpravidla objevuje zpoždění v plnění choroidey; časná hypofluorescence svědčí pro nonperfúzi choriokapilaris. Tato vede k dilataci venózního řečiště, které se ve střední fázi angiogramu znázorňuje jako geografická ložiska zvýšené fluorescence daná hyperpermeabilitou zejména velkých cév choroidálního řečiště, tzv. Hallerovy vrstvy. Oblasti hyperfluorescence se do pozdní venózní fáze centrifugálně rozšiřují a nemusí být striktně lokalizovány pouze v místech korespondujících s místy průsaku viditelnými při FAG vyšetření (naopak velmi často mohou být pozorovány i v místech, které se jeví klinicky normální, nebo na kontralaterálním nepostiženém oku). V pozdní venózní fázi dochází buď k vymývání barviva z tkání nebo hyperfluorescence přetrvává, což mimo jiné závisí na míře aktivity onemocnění [48,55,92–95]. Jednoznačně výhodné je provedení simultánního FAG a ICG a jejich vzájemné porovnání. Choroidální vaskulární hyperpermeabilita je společným znakem všech forem CSC [94,95]. Ložiska hyperfluorescence (aktivity) na FAG však velmi často zcela neodpovídají oblastem zvýšené aktivity prokázané pomocí ICG (Obrázek 3). Z tohoto důvodu můžeme právě jejich vzájemným srovnáním určit vývoj aktivity lépe než z metod provedených samostatně.
ICG zobrazení je nepostradatelnou vyšetřovací metodou před plánovanou PDT a určuje zcela exaktně rozsah, četnost a lokalizaci choroidální léze, která nemusí být na FAG snímku patrná. Stejně tak má ICG své nezastupitelné místo v případech, kdy nedojde k uspokojivé odpovědi na léčbu či má CSC rekurentní průběh a mohou se v čase aktivovat další (jiná) choroidální ložiska [96].
Obr. 3. Simultánní fluoresceinový a indocyaninový angiografický snímek u 58letého pacienta s multifokální chronickou formou centrální serózní chorioretinopatie (Heidelberg Spectralis, Myslík Manethová): 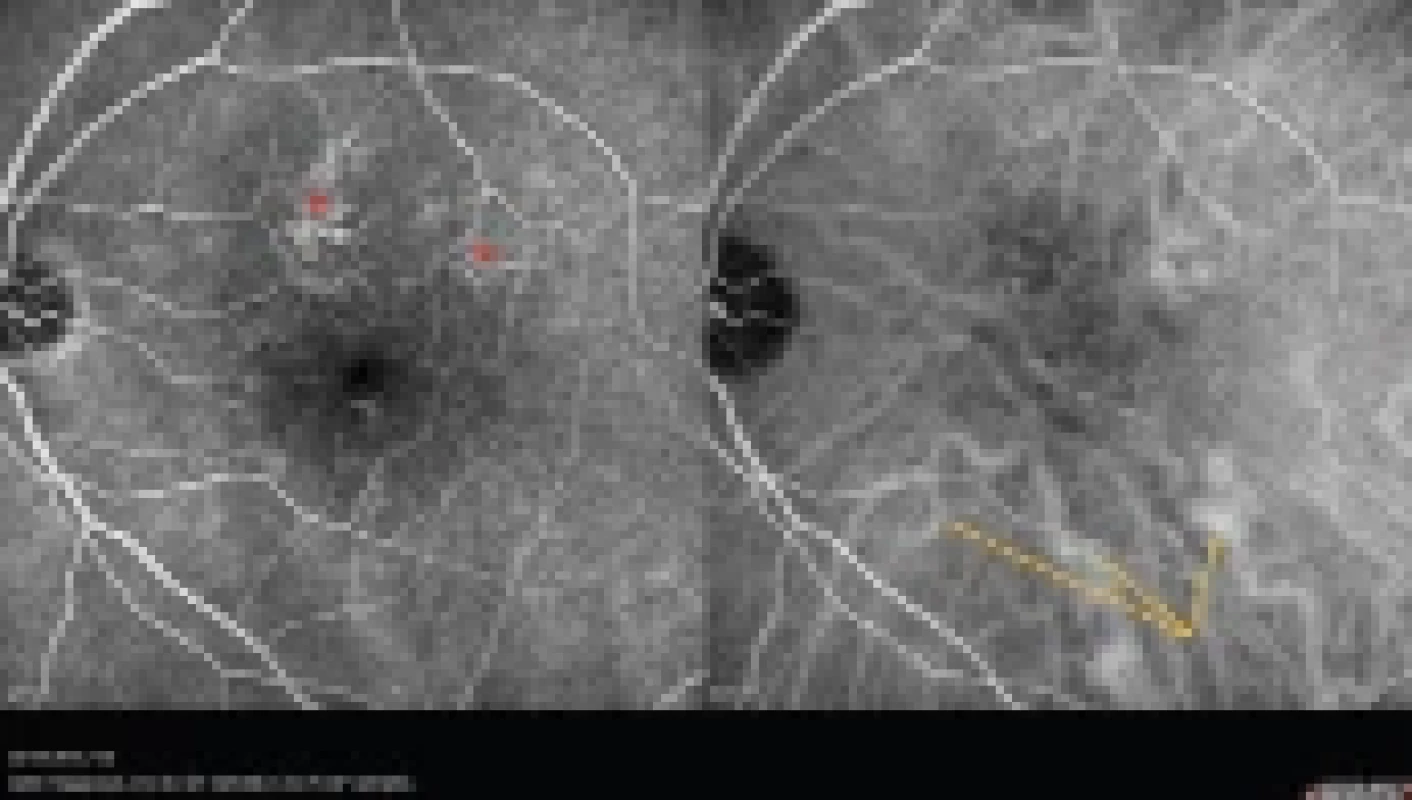
střední fáze angiogramu
se zvýšenou fluorescencí patologicky změněného retinálního pigmentového listu při horní temporální arkádě (červená
hvězdička); na indocyaninové angiografii jsou při dolní temporální arkádě patrné 3 významně dilatované a prosakující
velké choroidální cévy Hallerovy vrstvy, které však na fluoresceinové angiografii nejsou zřetelné (žluté šipky)Optická koherenční tomografie
Díky spektrálně doménové OCT (SD-OCT) a v poslední době i díky tzv. enhanced depth imaging OCT (EDI-OCT) a en face swept-source OCT (SS-OCT), které umožňují zobrazení retinochoroidální tkáně v celé své tloušťce, můžeme anatomii a částečně i patofyziologii CSC lépe porozumět. OCT je bezkontaktní, neinvazivní, nonmydriatická, bezpečná, rychlá, efektivní vyšetřovací metoda, která je ke kvantitativnímu hodnocení CSC, monitoraci vývoje a efektu léčby používána jako metoda první volby. Jedná se o vysoce specializované vyšetření makuly na principu nízkokoherenční interferometrie s vysokým rozlišením, která formou řezu umožňuje zobrazení sítnicových, ale i choroidálních struktur s vysokou rozlišovací schopností až 3 µm [97]. Díky své vysoké rozlišovací schopnosti poskytuje detailní informace o strukturách na úrovni vitreoretinálního rozhraní, jednotlivých vrstev sítnice, RPE, Bruchovy membrány a díky současným možnostem i jednotlivých vrstev choroidey. Typickým nálezem na OCT u CSC bývá přítomnost hyporeflektivní (areflektivní) tekutiny pod vrstvou RPE a neuroepitelu. V místě serózního odloučení neuroretiny dochází k elongaci a ztluštění zevních segmentů fotoreceptorů, místy až k jejich erozi vznikající jako mechanická abraze při výrazné exsudativní aktivitě nad defektem RPE [79]. V 50–100 % případů CSC je přítomna ablace RPE [98,99]. Různě vysoké ablace RPE serózního charakteru jsou typické pro časnější formy onemocnění a nejčastěji se vyskytují nad ložisky zvýšené choroidální permeability [79]. U chronických lézí spíše pozorujeme nepravidelné ploché zvlnění vrstvy RPE a přítomnost denzního (hypo - i hyperreflektivního) materiálu mezi Bruchovou membránou a RPE, který na OCT zobrazení vytváří tzv. “double layer sign” [99,100]. Dalším znakem spíše chronických lézí jsou hyperreflektivní tečky patrné v sítnicových vrstvách, v subretinálním prostoru i v oblasti vnitřní choroidey, které korespondují s hyperautofluorescentními ložisky patrnými na sítnici [101–103]. Zdá se, že větší množství hyperreflexivních teček koreluje s delším trváním nemoci i horší prognózou výsledné ZO [104]. V případě rekurentního či několikaletého trvání nemoci můžeme často na OCT skenech nalézt cystoidní makulární degeneraci (CMD), ztenčení zevní nukleární vrstvy (ONL) sítnice, disrupci zóny elipsoidů (junkce mezi zevními a vnitřními segmenty fotoreceptorů) či membrány limitans externy (ELM), absenci fotoreceptorů nebo povšechnou atrofii retinálních vrstev [102].
Ve srovnání se zdravou populací prokázala EDI-OCT u pacientů s CSC povšechně větší tloušťku choroidey a velkých choroidálních cév tzv. Hallerovy vrstvy, a naopak ztenčení vrstvy Sattlerovy společně s choriokapilaris v postiženém i kontralaterálním oku; toto je pravděpodobně způsobeno jak tlakem dilatovaných cév, tak i primární atrofií choriokapilaris při hypoperfúzi tkáně [99,105]. Změna tloušťky choroidey může být fokální či difuzní a nemusí zcela korelovat s ložisky hyperfluorescence na ICG v místech vaskulární hyperpermeability Hallerovy vrstvy [106]. Tyto nálezy dále podporují myšlenku, že CSC může být způsobena lokálně zvýšeným hydrostatickým tlakem choroidey [4,28,105,107]. Vzhledem k tloušťce choroidey je CSC soudobou nomenklaturou řazena mezi tzv. pachychoroidní onemocnění (společně s pachychoroidní pigmentovou epitelopatií, pachychoroidní neovaskulopatií, polypoidální choroidální vaskulopatií, choroidální fokální exkavací) [24] (Obrázek 4).
Obr. 4. Kombinovaný snímek fluorescenční angiografie a transfoveolární lineární sken optické koherenční tomografie (Heidelberg Spectralis, Myslík Manethová) 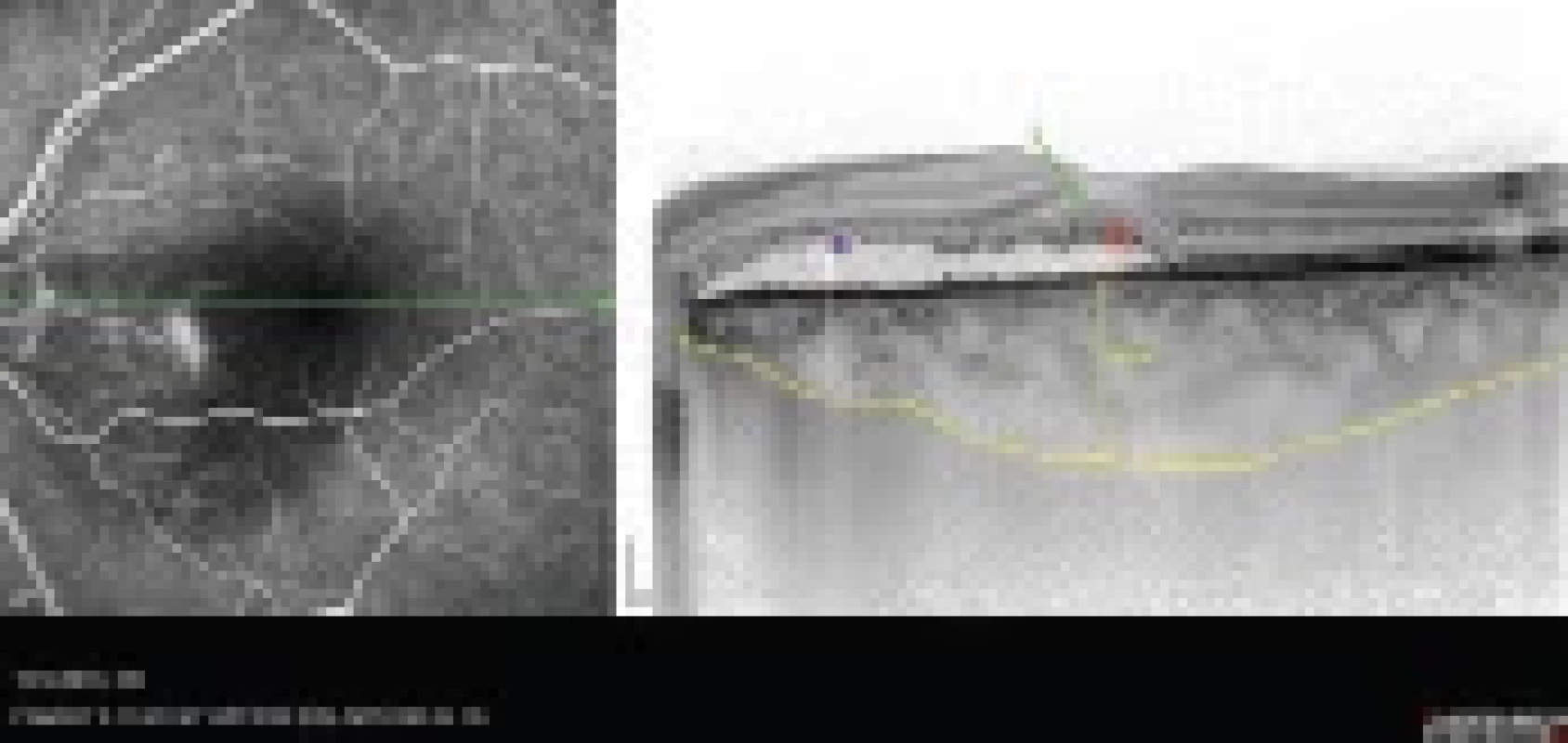
48letého pacienta s chronickou dlouhotrvající centrální serózní chorioretinopatií
s typickou elongací a ztluštěním fotoreceptorů, přítomnými hyperreflektivními tečkami (červená hvězdička),
zachovanou zevní limitující membránou (zelená šipka), vyznačenou výrazně dilatovanou lobulární choroideou
(žlutě) a ložiskovou abrazí fotoreceptorů v makulopapilárním svazku (fialová hvězdička)Optická koherenční tomografická angiografie
OCT-A je novou, slibnou, neinvazivní metodou, pomocí níž lze bez použití intravenózní kontrastní látky vyšetřit retinální i choroidální cévní řečiště s vysokou rozlišovací schopností ve všech vrstvách sítnice i choroidey. Principem OCT-A je detekce pohybu částic; za předpokladu, že jedinými pohybujícími se partikulemi v jinak nehybném oku jsou krevní elementy (erytrocyty). Jedná se tedy o snímání krevního toku v cévách sítnice i cévnatky – tzv. flow, neboli průtok. OCT-A snímky mohou být hodnoceny sumárně nebo izolovaně v jednotlivých vaskulárních vrstvách, což umožňuje velmi detailní analýzu vaskulatury v různých úrovních bez zastření struktur, jako tomu bývá při průsaku či nahromadění barviva u klasické FAG [89]. Na OCT-A snímcích obvykle detekujeme abnormální průtok velkými dilatovanými cévami choroidey i dilatovanými cévami choriokapilaris. Abnormální průtok choriokapilaris, který se na snímku projeví jako tmavá zóna, svědčí pro redukci průtoku korelující s nálezem na ICG u akutních, ale zejména chronických forem [108].
Costanzo a kol. popsali na OCT-A 3 specifické nálezy v oblasti choriokapilaris: tmavé oblasti, tmavé body a abnormální choroidální cévy. Tmavé oblasti jsou popisovány jako difuzní či fokální setřelé nepřesně ohraničené oblasti s nízkým nebo nedetekovatelným průtokem, zatímco tmavé body jsou černá, jednotlivá nebo mnohačetná ostře ohraničená ložiska s žádným detekovatelným krevním průtokem na úrovni choriokapilaris. Tmavé oblasti většinou korespondují se zónami SRT, kdežto tmavé body s ablacemi RPE. Abnormální choroidální cévy jsou popisovány jako zřetelné, ostře vymezené, spletité dilatované cévy o vysokém průtoku. Interpretace těchto abnormálních choroidálních cév by měla být provedena obezřetně, protože v mnoha případech je není snadné odlišit od choroidální neovaskulární sítě [89,109]. Navíc nám dnes OCT-A mnohem lépe umožňuje detekovat přítomnost sekundární CNV, obvykle se vyskytující pod nepravidelně undulujícím RPE, která není velmi často na FAG či ICG vyšetření detekovatelná [87,89,110,111]. OCT-A
se tímto stává zcela revoluční zobrazovací metodou, která nám poskytuje nejen poměrně exaktní informace o struktuře, ale nepřímo i o funkci retinochoroidální tkáně, a neměla by při vyšetření zejména chronických forem CSC chybět.Autofluorescence očního pozadí (FAF)
Autofluorescence, neinvazivní zobrazovací metoda, získala v poslední dekádě velkou popularitu. Jako jediná vyšetřovací technika umožňuje detekci metabolické aktivity fyziologicky nebo patologicky přítomných fluoroforů sítnice in vivo (např. lipofuscinových granul, kolagenu, elastinu, fibrinu), tedy struktur vyznačujících se různou mírou autofluorescence. Během vyšetření se mohou aplikovat 2 typy FAF vyšetření: short-wave FAF (SW-FAF) nebo near-infrared FAF (NIR-FAF). SW-FAF je vyzařována lipofuscinovými granuly RPE a poskytuje tak informaci o kondici RPE. NIR-FAF pochází z melaninového pigmentu choroidey a RPE. Ačkoliv NIR-FAF je používána méně často, klinické studie ukázaly, že může být u CSC mnohem citlivější v detekci změn zevních retinálních vrstev [112,113].
Typické pro fyziologický FAF je tmavé zobrazení terče zrakového nervu a cév pro nepřítomnost autofluorescentních fluoroforů a homogenní autofluorescence RPE [93,114,115]. U očí s akutní CSC je charakteristický skvrnitý obraz zvýšené autofluorescence v zóně abladovaného smyslového epitelu daný přítomností subretinálních či intraretinálních precipitátů a depozit se zvýšeným obsahem lipofuscinu (akumulace zevních segmentů fotoreceptorů, které nejsou fagocytovány porušeným RPE, nebo nahromadění makrofágů s fagocytovanými zevními segmenty) [114]. V časné fázi jsou patrná ložiska hypoautofluorescence korespondující s místy průsaku u 70–100 % případů, tedy v místě defektního RPE [116,117].
U chronických forem, stejně jako u akutních, většina očí vykazuje hypoautofluorescenci v místě průsaku zřetelném na FAG, které je dáno přítomností subretinální tekutiny i různým stupněm poškození RPE. Patognomický nález u dlouhotrvajících stavů je smíšená autofluorescence různé intenzity. Hypoautofluorescentní jsou zejména ložiska nad dystroficky změněným RPE, žádná autofluorescence se nenachází v místech atrofie RPE. Zpočátku bývají hyperautofluorescentní, pokud je přítomna subretinální tekutina, ale postupně se stávají hypoautofluorescentní při pozvolné degradaci buněk RPE, až jejich úplné atrofii. Studie prokázaly poměrně dobrou korelaci mezi nálezy na FAF a retinální senzitivitou kvantifikovanou mikroperimetrií i ZO, a proto může být FAF užita pro odhad míry funkčních změn očí s CSC, ale i pro prognózu změny NKZO v souvislosti s léčebným zásahem [117].
Makulární mikroperimetrie
Makulární mikroperimetrie detekuje sníženou makulární senzitivitu u pacientů s CSC a může být užitečnou subjektivní vyšetřovací metodou k hodnocení odpovědi na fotodynamickou léčbu. Výsledky klinických studií naznačují, že pouze vyšetření ZO samo o sobě může výrazně podhodnotit změny makulárních funkcí, které doprovází úspěšnou léčbu CSC. Makulární mikroperimetrie se ukázala vhodnou metodou k přesnému zhodnocení senzitivity sítnice u pacientů léčených pomocí PDT či mikropulzního laseru, u kterých bylo prokázáno zlepšení citlivosti v centrální oblasti sítnice po léčbě [117,118].
Multifokální elektroretinografie
Multifokální elektroretinografie (mfERG) slouží k objektivnímu zhodnocení funkčních změn sítnice u pacientů s CSC. Zlepšení NKZO a centrální retinální tloušťky po léčbě pomocí PDT bylo v korelaci s odpovědí na mfERG; ačkoliv po vstřebání subretinální tekutiny došlo k významnému zlepšení záznamu na mfERG, nebývá dosaženo původních hodnot [119,120].
Laboratorní vyšetření
Výsledky laboratorních vyšetření nejsou pro stanovení diagnózy ve většině případů přínosné. Přesto se v poslední době uvádí souvislost se zvýšenými hladinami sérového inhibitoru aktivátoru plasminogenu 1 u pacientů s CSC [35]. Mohou být zachyceny i vyšší hodnoty endogenního kortisolu, který se považuje za jeden z hlavních rizikových faktorů vzniku CSC, nebo abnormální hodnoty krevních koagulačních parametrů (např. nižší hladina růstového faktoru z krevních destiček) [79,121]. Neexistuje však laboratorní test, který by byl pro diagnostiku tohoto onemocnění specifický.
TERAPIE CSC
I přes všechny pokroky v diagnostice, vyšetřovacích i léčebných možnostech zůstává optimální nastavení a zvolení adekvátní léčby CSC nadále sporné. Tato kontroverze je dána faktem, že onemocnění má sice vysokou tendenci ke spontánní úpravě s vynikající prognózou výsledné ZO, na druhou stranu však dlouhotrvající odchlípení sítnice může vést ke značným irreverzibilním anatomickým a následně funkčním změnám (Obrázek 5). Principem léčby je navodit znovu přiložení neuroretiny, zlepšit nebo zachovat ZO a minimalizovat riziko rekurencí. Při výběru vhodné léčebné metody je vždy nutné brát v úvahu možný dočasný průběh onemocnění, lokalizaci patologického ložiska a stav RPE.
Obr. 5. Transfoveolární lineární sken optické koherenční tomografie (Heidelberg Spectralis, Myslík Manethová) 61letého pacienta s chronickou centrální serózní chorioretinopatií zobrazující: 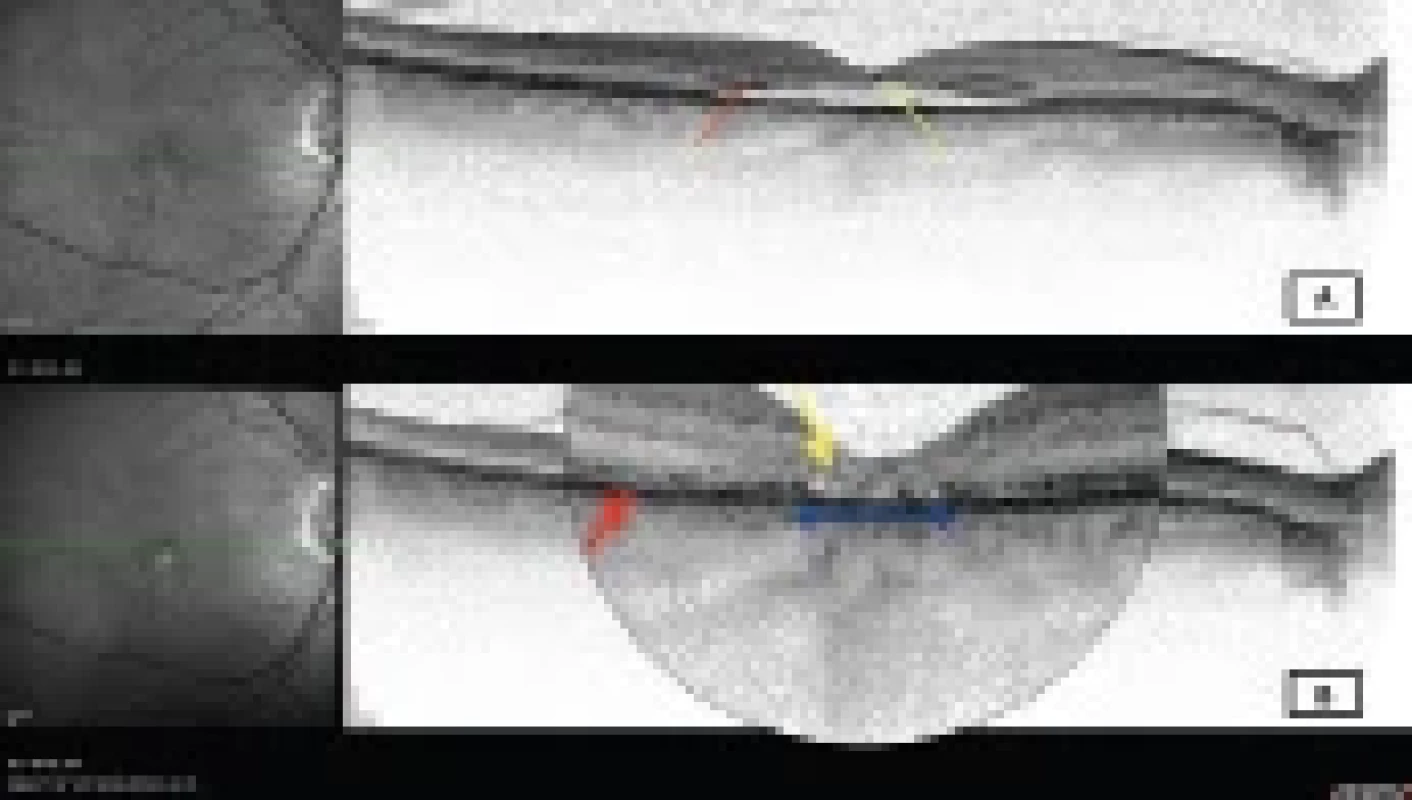
(A) plochou serózní elevaci v oblasti
centrální makuly; při okraji odchlípení je linie fotoreceptorů ještě zachována (červená šipka), zatímco subfoveolárně již
linie fotoreceptorů při dlouholeté přítomnosti subretinální tekutiny chybí (žlutá šipka). (B) zachycuje stav po fotodynamické
terapii s poloviční dávkou verteporfinu s uspokojivým anatomickým efektem, ovšem transfoveolární lineární
sken odhaluje celkovou atrofii retiny v centrální části makuly s atrofií vrstvy retinálního pigmentového epitelu subfoveolárně
(modrá šipka) nad ní patrnou absencí linie fotoreceptorů (žlutá šipka) a naopak poměrně dobře zachovanou
interdigitační zónou při okraji původního odchlípení neuroretiny (červená šipka)Konzervativní přístup – observace a modifikace rizikových faktorů
V případě akutní fáze onemocnění, zvláště je-li serózní odchlípení neuroretiny způsobeno konkrétním zdrojem průsaku, se spontánní resorpce SRT vyskytne ve většině případů (80–90 %) do 3 měsíců od propuknutí choroby [47,122]. Proto se v akutní fázi (v prvních 3 měsících nemoci) doporučuje spíše observace stavu a snaha o redukci rizikových faktorů. Vhodné je snížení či úplné vysazení kortikoidní terapie, pokud pacient tuto léčbu chronicky užívá, úprava životního stylu s minimalizací stresových podnětů, případně nasazení konzervativní léčby. Existují však situace, kdy by měla být léčba nastavena i dříve. Jsou to například vysoké nároky pacienta na zlepšení zraku (řidiči z povolání, grafici apod), rekurentní forma nemoci nebo v případě, kdy neléčená CSC na kontralaterálním oku vedla k významnému snížení zraku.
Medikamentózní terapie
Přestože již proběhla řada studií zkoumajících efekt perorálně podávaných léků, neexistuje v současné době žádný kauzální lék. Pozitivní vliv beta-blokátorů, anxiolytik, antidepresiv, nesteroidních antiflogistik, resorbencií, vasoprotektiv, vitaminoterapie nebyl prokázán [123]. Kortikosteroidy dříve standardně používané ke konzervativní léčbě CSC se dnes již vůbec nedoporučují, poněvadž v odborné literatuře existuje celá řada sdělení, podle kterých může celkové i parabulbární podání kortikoidů vznik CSC vyprovokovat [35,66]. Dlouhodobá kortikoidní terapie souvisí s prolongovanou přítomností SRT i difuzními změnami RPE a u pacientů, kteří z jakéhokoliv důvodu nemohou dávky kortikoidů omezit, se často potýkáme s vleklým, na léčbu obtížně reagujícím chronickým onemocněním. Péče o tyto pacienty vyžaduje mezioborovou spolupráci a doporučení oftalmologa u pacientů s CSC, u kterých to jejich zdravotní stav dovoluje, dlouhodobou kortikoidní terapii vysadit nebo nahradit alternativní léčbou (např. biologickou terapií). Alkin a kolektiv uvádí pozitivní efekt nepafenacu 0,1 % v léčbě akutních forem CSC [124]. V literatuře se objevují nové poznatky o pozitivním účinku antagonistů mineralokortikoidních receptorů, zejména eplerenonu. Podle recentních výsledků klinických studií ovlivňuje eplerenon více patofyziologických cest, čímž podporuje rychlejší vstřebávání tekutiny a je účinnější u chronických stavů [125,126]. V případě rozsáhlých atrofií RPE je však jeho účinnost limitovaná [127]. Další prospektivní klinické studie jsou nezbytné k potvrzení jeho bezpečnosti, účinnosti a ke stanovení, které klinické formy CSC by z léčby eplerenonem profitovaly.
Laserová terapie
Konvenční argonový laser se již léta používá ke zvládnutí akutní i chronické fáze CSC [16]. Vzhledem k vysokému procentu spontánní resorpce SRT se doporučuje s intervencí vyčkat 3 měsíce od propuknutí onemocnění [128]. Pokud nedojde ke spontánnímu přiložení neuroretiny a bod průsaku je od centra fovey dostatečně vzdálen (více jak 500 µm), je indikována přímá laserová fotokoagulace ložiska průsaku (hyperfluorescence dle FAG). Pokud je ložisko průsaku vzdáleno od středu fovey méně než 500 µm nebo pokud je již vyjádřeno difuzní postižení RPE, doporučuje se zvolit jinou léčebnou alternativu [128]. Po laserové koagulaci místa průsaku dochází v nekomplikovaných případech k anatomickému přiložení neuroretiny obvykle do 2 týdnů od provedení zákroku. Úprava centrální ZO vyžaduje zpravidla dvojnásobek času. Fotokoagulace obvykle zkracuje dobu trvání onemocnění, akceleruje resorpci SRT, avšak nemá vliv na konečnou ZO [129].
Cílem laserové fotokoagulace je zajizvení defektního RPE, kterým proniká tekutina do subretinálního prostoru. Bodová laserová koagulace ložiska se provádí cíleně na základě předešlé fluorescenční (či indocyaninové) angiografie. Principem duálního hojícího efektu fotokoagulačního laseru je přímý termický vliv, ale také sekundární expanze buněk RPE z okolní zdravé tkáně a přehojení RPE defektu [130]. V místě působení laserového paprsku dochází k tepelné destrukci tkáně i přilehlé neurosenzorické sítnice a v místě ošetření se může objevit absolutní skotom. Možné nežádoucí účinky laserové fotokoagulace by měly být brány v úvahu, zvláště je-li nutné použít laser v blízkosti fovey nebo v makulopapilárním svazku. K dalším možným komplikacím patří náhodné zasažení fovey, krvácení, fibróza, sekundárně vzniklá CNV, pomalé progresivní zvětšení místa atrofie RPE původní laserové stopy (zvětšení stopy může časem postihnout foveu a způsobit ireverzibilní ztrátu ZO) [16].
Modalitou ke konvenčnímu laseru je tzv. subthreshold či mikropulzní laser. Principem mikropulzního laseru je rozdělení kontinuálního laserového paprsku vlnové délky 810 nm (nebo 577 nm) na jednotlivé krátké pulzy oddělené pauzou, což minimalizuje vznik tepelné energie, která má vůči tkáni laserované i okolní mutilující účinek. Spíše než destruktivní účinek má mikropulzní laser efekt stimulující. Podporuje biologickou odpověď tkáně, která vede k obnově integrity a fyziologické funkce buněk RPE s reabsorpcí SRT. Podprahová diodová mikropuzlní laserová terapie by mohla být v budoucnu efektivní a bezpečnou léčebnou modalitou pro cCSC [118].
Fotodynamická terapie – PDT (photodynamic therapy)
Vedle laserové terapie se v posledních letech s úspěchem používá léčba pomocí fotodynamické terapie, jejíž zavedení do praxe bylo založeno na myšlence, že CSC primárně postihuje choroideu. PDT se původně používala k léčbě solidních tumorů, později k léčbě vlhké formy VPMD [131]. Pozitivní výsledky léčby chronické formy CSC fotodynamickou terapií s použitím fotosenzibilizující látky verteporfinu byly poprvé publikovány Yannuzzim a Piccolinem v roce 2003 [77,132]. Od té doby byla v léčbě CSC potvrzena účinnost i bezpečnost ICG-navigované PDT řadou klinických studií [11,13,135–136].
Princip PDT spočívá v intravenózním podání fotosenzibilizující látky verteporfinu (Visudyne, Novartis AG, Bülach, Switzerland) a její aktivaci působením laserového světla v červených vlnových délkách. Protože k indukci fotochemické reakce dochází intravazálně, nedochází během PDT k termálnímu poškození tkání. PDT indukuje v místě ozáření zúžení choroidálních cév, vede k jejich modifikaci, redukuje choroidální perfúzi a v důsledku těchto změn snižuje choroidální exsudaci [137,138]. Dle závěrů klinických studií umožňuje PDT rychlejší resorpci SRT v porovnání se skupinou pacientů, kteří jsou léčeni laserovou fotokoagulací [132,139]. K určení přesné lokalizace a rozsahu léze se využívá výsledků ICG (střední venózní fáze), podle kterých je během ošetření laserový paprsek cílen přesně na ložisko/ložiska hyperfluorescence [94,140]. PDT může být aplikována ve standardní dávce i délce ozáření ložiska, která se používá v léčbě vlhké formy VPMD (parametry dle TAP studie: laserový paprsek vlnové délky 689 nm aplikován po dobu 83 sekund expozicí 600 mW/cm², do 5 minut po skončení intravenózní infuze verteporfinu – v dávce 6 mg/m², energie 50 J/cm²)
[137]. Vzhledem k potenciálnímu nebezpečí, které s sebou léčba standardní PDT nese (zhoršení ZO, širší destrukce normálního i již porušeného RPE s atrofickými změnami, potenciální choroidální ischemie, riziko rozvoje sekundární CNV), jsou v posledních letech upřednostňovány alternativní režimy dávkování verteporfinu i působícího laserového paprsku při tzv. “safety-enhaced” PDT. Buď je použita redukovaná dávka záření při tzv. „reduced (half)-fluence“ (HF-PDT, poloviční expozice – 42 sec., nebo poloviční energie – 25 J/cm2) nebo redukovaná dávka verteporfinu při tzv. „reduced (half)-dose“ (HD-PDT, poloviční dávka Visudynu, tedy 3 mg/m²) [12,28,128,133,141].Výsledky studií porovnávající „safety-enhanced“ PDT a konvenční PDT jsou srovnatelné. Při dosažení podobného anatomického i funkčního efektu „safety-enhanced“ PDT minimalizuje škodlivý účinek na perfúzi choriokapilaris a její atrofizující vliv na RPE a tloušťku retiny [12,133]. Autoři Nicoló a Kim ve svých publikacích porovnávali funkční a anatomické výsledky u pacientů s cCSC léčených HF-PDT a HD-PDT. Shodně uvádí, že mezi těmito léčebnými modalitami nejsou statisticky signifikantní rozdíly v anatomických ani funkčních výsledcích, Nicoló pouze uvádí rychlejší absorpci SRT v případě HD-PDT [10,141].
Redukovaná PDT je díky velmi pozitivním výsledkům a uspokojivému bezpečnostnímu profilu demonstrovaného dosud provedenými klinickými studiemi považována za léčbu první volby, ačkoliv se v indikaci pro CSC jedná o léčbu tzv. off-label [142,143].
Anti-VEGF terapie
Vzhledem k patofyziologii onemocnění je užití anti-VEGF preparátů k léčbě CSC sporné. Řada klinických studií poskytla nejednoznačné výsledky efektu anti-VEGF preparátů v léčbě CSC [18,144,145]. Onemocnění samo o sobě není spojováno s vyšší hladinou VEGF ve sklivci a účinek anti-VEGF léčby u CSC bez přítomné CNV nebyl vesměs prokázán [146]. Jiná situace však nastává u komplikovaných případů sekundární CNV na podkladě CSC. Zejména v posledních 5 letech, kdy se díky pokroku v multimodálním zobrazení (OCT-A) daří prokazovat CNV asociovanou s CSC patologií s mnohem větší senzitivitou i specificitou, nabývá užití anti-VEGF preparátů v těchto případech na stále větším významu, u nejtěžších stavů pak v kombinaci s PDT [147]. Předchozí klinické studie prokázaly anatomický i funkční efekt bevacizumabu, ranibizumabu a afliberceptu v léčbě CNV asociované s CSC [146,148,149]. Existují však jen velmi omezená data dokazující účinnost a bezpečnost kombinované léčby PDT a anti-VEGF. Asahi demonstroval pozitivní výsledky kombinované terapie HD-PDT + aflibercept u pacientů nereagujících na konvenční léčbu (laserfotokoagulace, monoterapie PDT, monoterapie anti-VEGF), větší úspěch zaznamenal především u očí komplikovaných CNV [150].
Ranibizumab je v ČR jediný registrovaný lék, který může být použit k léčbě vzácných forem CNV, tedy i těch na podkladě CSC.
Další léčebné alternativy
Přestože v léčbě CSC neexistuje žádná kauzální medikamentózní léčba, řada menších klinických studií prokázala pozitivní výsledky v léčbě CSC při použití finasteridu (inhibitor syntézy dihydrotestosteronu) v dávce 5mg denně nebo kyseliny acetylsalicylové působící proti choroidální vaskulární kongesci, ischemii a zánětlivým změnám doprovázejícím CSC [28]. Dobré výsledky mohou být také dosaženy eradikací infekce Helicobacter pylori v indikovaných případech a léčbou obstrukční spánkové apnoe jako možných rizikových faktorů vyvolávajících toto onemocnění [28,35].
ZÁVĚR
Dnešní technické pokroky v diagnostice a léčbě CSC v kombinaci s našimi klinickými zkušenostmi představují výrazné zlepšení prognózy našich pacientů s CSC, u kterých je nutná nejen správná diagnostika onemocnění založená na multimodálním zobrazení, ale především správné nastavení a načasování adekvátní léčby. Z našich dosavadních výsledků také vyplývá, že by léčba chronických forem CSC měla být zahájena v časných stádiích, abychom docílili co možná nejlepších anatomických a funkčních výsledků, dokud ještě nejsou vyjádřeny irreverzibilní změny jako DRPE nebo komplikující CNV.
Zdroje
1. Atlas of Macular Diseases: Gass JDM. Stereoscopic Diagnosis and Treatment. 4th edition: Mosby, 1997.1061,52-70. ISBN: 978-0815134169.
14. Chan WM, Lai TY, Lai RY, et al. Safety enhanced photodynamic therapy for chronic central serous chorioretinopathy: one-year results of a prospective study. Retina. 2008;28(1):85-93.
18. Lim SJ, Roh MI, Kwon OW, Woong OH. Intravitreal bevacizumab injection for central serous chorioretinopathy. Retina. 2010;30(1):100-106.
20. Bennet G. Central serous retinopathy. Br J Ophthalmol. 1955;39 : 605-618.
21. Maumenee AE. Macular Diseases: Clinical Manifestations. Trans Am Acad Ophthalmol Otolaryngol. 1965;69 : 605-613.
22. Gass JDM. Pathogenesis of disciform detachment of the neuroepithelium: II. Idiopathic central serous choroidopathy. Am J Ophthalmol. 1967;63 : 587-615.
23. Ryan SJ. Retina. Volume II, 4th edition, Baltimore (USA): Elsevier Mosby, 2006. 1889, 1135-1161. ISBN: 9780323025980.
24. Gallego-Pinazo R, Dolz-Marco R, Gomez-Ulla F, Mrejen S, Freund KB. Pachychoroid diseases of the macula. Med Hypothesis Discov Innov Ophthalmol. 2014;3(4):111-115.
25. Lehmann M, Bousquet E, Beydoun T, et al. Pachychoroid: an inherited condition? Retina. 2015;35(1):10-16.
35. Haimovici R, Koh S, Gagnon DR, et al. Risk factors for central serous chorioretinopathy: a case-control study. Ophthalmology. 2004;111(2):244-249.
36. Horniker E. Su di unaforma di retinite central di originevasoneurotica. Ann Ottalmol. 1927;55 : 830-840.
37. Yannuzzi LA. Type A behavior and central serous chorioretinopathy. Trans Am Ophthalmol Soc. 1986;84 : 799-845.
45. de Jong EK, Breukink MB, Schellevis RL, et al. Chronic central serous chorioretinopathy is associated with genetic variants implicated in age-related macular degeneration. Ophthalmology. 2015;122(3):562-570.
46. Schellevis RL, Van Dijk EHC, Breukink MB, et al. Role of the complement system in chronic central serous chorioretinopathy: a genome-wide association study. JAMA Ophthalmol. 2018;136(10):1128-1136.
47. Yannuzzi LA. Central serous chorioretinopathy: a personal perspective. Am J Ophthalmol. 2010;149(3):361-363.
48. Schachat APW, C.P.; Hinton, D.R. Ryan’s Retina. Volume II, 6th edition edition: Elsevier, 2018. 2976. ISBN: 978-0-323-40197-5.
56. Hayashi K, Hasegawa Y, Tokoro T. Indocyanine green angiography of central serous chorioretinopathy. Int Ophthalmol. 1986;9(1):37-41.
57. Tomasso L, Benatti L, Rabiolo A, et al. Retinal vessels functionality in eyes with central serous chorioretinopathy. Br J Ophthalmol. 2018;102(2):210-214.
59. Cheung CMG, Lee WK, Koizumi H, Dansingani K, Lai TYY, Freund KB. Pachychoroid disease. Eye Lond Engl. 2019;33(1):14-33. doi: 10.1038/s41433-018-0158-4
60. Negi A, Marmor MF. Mechanisms of subretinal fluid resorption in the cat eye. Invest Ophthalmol Vis Sci. 1986;27(11):1560-1563.
61. Wang C, Cao G-F, Jiang Q, Yao J. TNF- promotes human retinal pigment epithelial (RPE) cell migration by inducing matrix metallopeptidase 9 (MMP-9) expression through activation of Akt/mTORC1 signaling. Biochem Biophys Res Commun. 2012;425(1):33-38.
66. Carvalho-Recchia CA, Yannuzzi LA, Negrao S, et al. Corticosteroids and central serous chorioretinopathy. Ophthalmology. 2002;109(10):1834-1837.
71. Gass JD, Slamovits TL, Fuller DG, Gieser RG, Lean JS. Posterior chorioretinopathy and retinal detachment after organ transplantation. Arch Ophthalmol. 1992;110(12):1717-1722.
72. Hadcock JR, Malbon CC. Regulation of beta-adrenergic receptors by "permissive" hormones: glucocorticoids increase steady-state levels of receptor mRNA. Proc Natl Acad Sci USA. 1988;85(22):8415-8419.
76. Iida T, Yannuzzi LA, Spaide RF, Borodoker N, Carvalho CA, Negrão S. Cystoid macular degeneration in chronic central serous chorioretinopathy. Retina. 2003;23(1):1-7
77. Piccolino FC, Eandi CM, Ventre L, Rigault De La Longrais, RC. Grignolo, FM. Photodynamic therapy for chronic central serous chorioretinopathy. Retina. 2003;23(6):752-763.
78. Piccolino FC, de la Longrais RR, Ravera G, et al. The foveal photoreceptor layer and visual acuity loss in central serous chorioretinopathy. Am J Ophthalmol. 2005;139(1):87-99.
79. Daruich A, Matet A, Dirani A, et al. Central serous chorioretinopathy: recent findings and new physiopathology hypothesis. Prog Retin Eye Res. 2015;48 : 82-118.
80. Chhablani J. Central serous chorioretinopathy. Elsevier Science, 2019.27-34. ISBN: 9780128168004.
82. Aggio FB, Roisman L, Melo GB, Lavinsky D, Cardillo JA, Farah ME. Clinical factors related to visual outcome in central serous chorioretinopathy. Retina. 2010;30(7):1128-1134.
84. Yannuzzi LA, Slakter JS, Kaufman SR, Gupta K. Laser treatment of diffuse retinal pigment epitheliopathy. Eur J Ophthalmol. 1992;2(3):103-114.
86. Quaranta-El Maftouhi M, El Maftouhi A, Eandi CM. Chronic central serous chorioretinopathy imaged by optical coherence tomographic angiography. Am J Ophthalmol. 2015;160(3):581-587 e1.
87. Bousquet E, Bonnin S, Mrejen S, Krivosic V, Tadayoni R, Gaudric A. Optical Coherence Tomography Angiography of Flat Irregular Pigment Epithelium Detachment in Chronic Central Serous Chorioretinopathy. Retina. 2018;38(3):629-638.
88. Bonini Filho MA, de Carlo TE, Ferrara D, et al. Association of Choroidal Neovascularization and Central Serous Chorioretinopathy With Optical Coherence Tomography Angiography. JAMA Ophthalmol. 2015;133(8):899-906.
89. Costanzo E, Cohen SY, Miere A, et al. Optical Coherence Tomography Angiography in Central Serous Chorioretinopathy. J Ophthalmol. 2015;2015 : 134783.
90. Balaratnasingam C, Freund KB, Tan AM, Sarraf D, Jampol LM, Yannuzzi LA. Bullous variant of central serous chorioretinopathy: expansion od phenotypic features using multimethod imaging. Ophthalmology. 2016;123(7):1541-1552.
91. Yannuzzi LA, Shakin JL, Fisher YL, Altomonte MA. Peripheral retinal detachments and retinal pigment epithelial atrophic tracts secondary to central serous pigment epitheliopathy. Ophthalmology. 1984;91(12):1554-1572.
95. Stanga PE, Lim JH, Hamilton P. Indocyanine green angiography in chorioretinal diseases: an evidenced-based update.Ophthalmology. 2003;110(1):15-21.
96. Yannuzzi LA. Indocyanine green angiography: a perspective on use in the clinical setting. Am J Ophthalmol. 2011;151(1):745751. e1.
97. Iida T, Hagimura N, Sato T, Kishi S. Evaluation of central serous chorioretinopathy with optical coherence tomography. Am J Ophthalmol. 2000;129(1):16-20.
100. Shin YU, Lee BR. Retro-mode imaging for retinal pigment epithelium alterations in central serous chorioretinopathy. Am J Ophthalmol. 2012;154(1):155-163.
101. Kon Y, Iida T, Maruko I, Saito M. The optical coherence tomography-ophthalmoscope for examination of central serous chorioretinopathy with precipitates. Retina. 2008;28(6):864-869.
102. Yalcinbayir O, Gelisken O, Akova-Budak B, et al. Correlation of spectral domain optical coherence tomography findings and visual acuity in central serous chorioretinopathy. Retina. 2014;34(4):705-712.
107. Jirarattanasopa P, Ooto S, Tsujikawa A, Hirata M, Matsumoto A, Yoshimura N. Assessment of macular choroidal thickness by optical coherence tomography and angiographic changes in central serous chorioretinopathy. Ophthalmology. 2012;119(8):1666-1678.
108. Teussink MM, Breukink MB, van Grinsven MJ, Hoyng CB, Klevering BJ. OCT angiography compared to fluorescein and indocyanine green angiography in chronic central serous chorioretinopathy. Invest Ophthalmol Vis Sci. 2015;56 : 5229-5237.
109. Chan SY, Wang Q, Wei WB, Jonas, JB. Optical Coherence Tomographic Angiography in Central Serous Chorioretinopathy. Retina. 2016;36(11):2051-2058.
110. Rabiolo A, Zucchiatti I, Marchese A, et al. Multimodal retinal imaging in central serous chorioretinopathy treated with oral eplerenone or photodynamic therapy. Eye (Lond). 2018;32(1):55-66.
111. Pichi F, Morara M, Veronese C, Ciardella AP. The overlapping spectrum of flat irregular pigment epithelial detachment investigated by optical coherence tomography angiography. Int Ophthalmol. 2018;38(3):975-983.
115. Holz FG, Bindewald-Wittich A, Fleckenstein M, Scholl HPN, Steffen Schmitz-ValckenbergFam-Study Group. Progression of geographic atrophy and impact of fundus autofluorescence patterns in age-related macular degeneration. Am J Ophthalmol. 2007;143(3):463-472.
116. Maruko I, Iida T, Ojima A, Sekiryu T. Subretinal dot-like precipitates and yellow materiál in central serous serous chorioretinopathy. Retina. 2011;31(4):759-765.
117. Ehrlich R, Mawer NP, Mody CH, Brand CS, Squirrell D. Visual function following photodynamic therapy for central serous chorioretinopathy: a comparison of automated macular microperimetry versus best-corrected visual acuity. Clin Exp Ophthalmol. 2012;40(1):e32-39.
120. Lai TY, Lai RY, Ngai JW, Chan WM, Li H, Lam DSC. First and second-order kernel multifocal electroretinography abnormalities in acute central serous chorioretinopathy. Doc Ophthalmol. 2008;116(1):29-40.
121. Caccavale A, Romanazzi F, Imparato M, et al. Central serous chorioretinopathy: a pathogenetic model. Clin Ophthalmol. 2011;5 : 239-243.
123. Chrapek O, Rehak J. Léčba centrální serózní chorioretiniopatie-naše zkušenosti. [Treatment of central serous chorioretinopathy-personal experience]. Cesk Slov Oftalmol. 2002;58(1):51-56. Czech.
124. Alkin Z, Osmanbasoglu OA, Ozkaya A, Karatas G, Yazici AT, Demirok A. Topical nepafenac in treatment of acute central serous chorioretinopathy. Med Hypothesis Discov Innov Ophthalmol. 2013;2(4):96-101.
125. Schwartz R, Habot-Wilner Z, Martinez MR, et al. Eplerenone for chronic central serous chorioretinopathy-a randomized controlled prospective study. Acta Ophthalmol. 2017;95(7):e610-e618.
126. Rahimy E, Pitcher JD, 3rd, Hsu J, et al. A Randomized Double-Blind Placebo-Control Pilot Study of Eplerenone for the Treatment of Central Serous Chorioretinopathy (Ecselsior). Retina. 2018;38(5):962-969.
127. Cakir B, Fischer F, Ehlken C, et al. Clinical experience with eplerenone to treat chronic central serous chorioretinopathy. Graefes Arch Clin Exp Ophthalmol. 2016;254(11):2151-2157.
128. Boscia F. When to treat and when not to treat patient with central serous retinopathy. Retina Today. [online], April 2010. Available from: https://retinatoday.com/articles/2010-apr/when-to-treat-and-not-to-treat-patients-with-central-serous-retinopathy
129. Gilbert CM, Owens SL, Smith PD, Fine SL. Long-term follow-up of central serous chorioretinopathy. Br J Ophhalmol. 1984;68(11):815-820.
130. Gass JD. Pathogenesis of disciform detachment of the neuroepithelium. Am J Ophthalmol. 1967;63(3 Suppl):1-139.
131. Dougherty TJ, Gomer CJ, Henderson BW, et al. Photodynamic therapy. J Natl Cancer Inst. 1998;90(12):889-905.
132. Yannuzzi LA, Slakter JS, Gross NE, et al. Indocyanine green angiography-guided photodynamic therapy for treatment of chronic central serous chorioretinopathy: a pilot study. Retina. 2003;23(3):288-298.
133. Koss M. Treating Chronic Central Serous Chorioretinopathy: The goal is a treatment with inceased Access and decreased effects. Retina Today. 2013;8 : 68-70.
134. Lai TY, Chan WM, Li H, Lai RYK, Liu DTL, Lam DSC. Safety enhanced photodynamic therapy with half dose verteporfin for chronic central serous chorioretinopathy: a short term pilot study. Br J Ophthalmol. 2006;90(7):869-874.
135. Fujita K, Imamura Y, Shinoda K, Hashizume K, Mizota A, Yuzawa M. One-year outcomes with half-dose verteporfin photodynamic therapy for chronic central serous chorioretinopathy. Ophthalmology. 2015;122(3):555-561.
136. Tseng CC, Chen SN. Long-term efficacy of half-dose photodynamic therapy on chronic central serous chorioretinopathy. Br J Ophthalmol. 2015;99(8):1070-1077.
137. Schmidt-Erfurth U, Hasan T. Mechanisms of action of photodynamic therapy with verteporfin for the treatment of age-related macular degeneration. Surv Ophthalmol. 2000;45(3):195-214.
138. Schmidt-Erfurth U, Laqua H, Schlotzer-Schrehard U, Viestenz A, Naumann GOH. Histopathological changes following photodynamic therapy in human eyes. Arch Ophthalmol. 2002;120(6):835-844.
139. Maier M, Valet V, Feucht N, Lohmann CP. Therapieoption bei chronischer Chorioretinopathia centralis serosa [Therapy options for chronic central serous chorioretinopathy]. Ophthalmologe. 2011;108(11):1027-1031. German.
140. Stanga PE, Lim JI, Hamilton P. Indocyanine green angiography in chorioretinal diseases: indications and interpretation: an evidence-based update. Ophthalmology. 2003;110(1):15-21; quiz 22-3.
141. Nicolo M, Eandi CM, Alovisi C, et al. Half-fluence versus half-dose photodynamic therapy in chronic central serous chorioretinopathy. Am J Ophthalmol. 2014;157(5):1033-1037.
142. van Dijk EHC, Fauser S, Breukink MB, Downes SM, Hoyng CB, Boon CJF. Half-dose photodynamic therapy versus high-density subthreshold micropulse laser treatment in patients with chronic central serous chorioretinopathy: the PLACE trial. Ophthalmology. 2018;125(10):1547-1555.
143. Manethová K, Ernest J, Hrevuš M, Jirásková N. Assessment of the Efficacy of Photodynamic Therapy in Patients with Chronic Central Serous Chorioretinopathy. Cesk Slov Oftalmol. 2019;75(6):298-308. doi:10.31348/2019/6/2
144. Bae SH, Heo J, Kim C, Park TK, Moon SW, Chung H. Low-fluence photodynamic therapy versus ranibizumab for chronic central serous chorioretinopathy: one-year results of a randomized trial. Ophthalmology. 2014;121(2):558-565.
145. Chan WM, Lai TY, Liu DT, Lam DSC. Intravitreal bevacizumab (avastin) for choroidal neovascularization secondary to central serous chorioretinopathy, secondary to punctate inner choroidopathy, or of idiopathic origin. Am J Ophthalmol. 2007;143(6):977-983.
146. Lim JW, Kim MU, Shin MC. Aqueous humor and plasma levels of vascular endothelial growth factor and interleukin-8 in patients with central serous chorioretinopathy. Retina. 2010;30(9):1465-1471.
147. Myslík Manethová K, Ernest J. Retrospective analysis of the presence of choroidal neovascularisation using optical coherence tomography angiography in the treatment of chronic central serous chorioretinopathy with the aid of photodynamic therapy. Cesk Slov Oftalmol. 2021;77(3):122-131. doi: 10.31348/2021/14
148. Konstantinidis L, Mantel I, Zografos L, Ambresin A. Intravitreal ranibizumab in the treatment of choroidal neovascularization associated with idiopathic central serous chorioretinopathy. Eur J Ophthalmol. 2010;20(5):955-958.
149. Broadhead GK, Chang A. Intravitreal aflibercept for choroidal neovascularisation complicating chronic central serous chorioretinopathy. Graefes Arch Clin Exp Ophthalmol. 2015;253(6):979-981.
150. Asahi MG, Chon AT, Gallemore E, Gallemore RP. Photodynamic therapy combined with antivascular endothelial growth factor treatment for recalcitrant chronic central serous chorioretinopathy. Clin Ophthalmol. 2017;11 : 2051-2056.
Štítky
Oftalmológia
Článok vyšiel v časopiseČeská a slovenská oftalmologie
Najčítanejšie tento týždeň
2023 Číslo Ahead of Print- Dlouhodobé výsledky lokální léčby cyklosporinem A u těžkého syndromu suchého oka s 10letou dobou sledování
- Pomocné látky v roztoku latanoprostu bez konzervačních látek vyvolávají zánětlivou odpověď a cytotoxicitu u imortalizovaných lidských HCE-2 epitelových buněk rohovky
- Konzervační látka polyquaternium-1 zvyšuje cytotoxicitu a zánět spojený s NF-kappaB u epitelových buněk lidské rohovky
- Syndrom suchého oka
- Cyklosporin A v léčbě suchého oka − systematický přehled a metaanalýza
-
Všetky články tohto čísla
- SOUČASNÝ POHLED NA SPEKTRUM PACHYCHOROIDNÍCH ONEMOCNĚNÍ. PŘEHLED
- ULTRAZVUKOVÉ VYŠETŘENÍ ORBITY PŘI ENDOKRINNÍ ORBITOPATII – PRŮVODCE VYŠETŘENÍM A DOPORUČENÍ PRO PRAXI. PŘEHLED
- VÝPOČETNÍ TOMOGRAFIE A MAGNETICKÁ REZONANCE ORBITY V DIAGNOSTICE A LÉČBĚ ENDOKRINNÍ ORBITOPATIE – ZKUŠENOSTI Z PRAXE. PŘEHLED
- DETERMINATION OF CORNEAL POWER AFTER REFRACTIVE SURGERY WITH EXCIMER LASER: A CONCISE REVIEW
- EYELID SCHWANNOMA. A CASE REPORT
- SOUČASNÝ STAV UMĚLÉ INTELIGENCE V NEUROOFTALMOLOGII. PŘEHLED
- CENTRÁLNÍ SERÓZNÍ CHORIORETINOPATIE. PŘEHLED
- LÉČBA VITREÁLNÍHO SEEDINGU RETINOBLASTOMU. PŘEHLED
- Česká a slovenská oftalmologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- CENTRÁLNÍ SERÓZNÍ CHORIORETINOPATIE. PŘEHLED
- ULTRAZVUKOVÉ VYŠETŘENÍ ORBITY PŘI ENDOKRINNÍ ORBITOPATII – PRŮVODCE VYŠETŘENÍM A DOPORUČENÍ PRO PRAXI. PŘEHLED
- SOUČASNÝ POHLED NA SPEKTRUM PACHYCHOROIDNÍCH ONEMOCNĚNÍ. PŘEHLED
- VÝPOČETNÍ TOMOGRAFIE A MAGNETICKÁ REZONANCE ORBITY V DIAGNOSTICE A LÉČBĚ ENDOKRINNÍ ORBITOPATIE – ZKUŠENOSTI Z PRAXE. PŘEHLED
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



