-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Flavonoidy – hlavné obsahové látky listov Philadelphus tenuifolius Rupr. et Maxim.
Flavonoids – main constituents of the leaves of Philadelphus tenuifolius Rupr. et Maxim.
The paper deals with the isolation and identification of the constituents of the leaves of Philadelphus tenuifolius Rupr. et Maxim. A methanolic extract was used to isolate quercetin-3-O-glucoside (isoquercitrin), and a butanolic extract to isolate kaempferol-3-O-glucoside-7-O-rhamnoside. Isolates were identified by physical-chemical data, comparison with authentic samples and literature data. The above-mentioned compounds were isolated from Philadelphus tenuifolius Rupr. et Maxim. for the first time.
Keywords:
Philadelphus tenuifolius • Hydrangeaceae • flavonoid glycosides
Autoři: Daniel Grančai; Silvia Fialová; Viktor Huszár; Janka Karlovská; Emil Švajdlenka
Vyšlo v časopise: Čes. slov. Farm., 2014; 63, 120-122
Kategorie: Původní práce
Souhrn
Predložená práca sa zaoberá izoláciou a identifikáciou flavonoidov prítomných v listoch pajazmínu tenkolistového (Philadelphus tenuifolius Rupr. et Maxim.). Z metanolového extraktu listov tejto rastliny bol izolovaný kvercetín-3-O-glukozid (izokvercitrín), z butanolového extraktu kempferol-3-O-glukozid-7-O-ramnozid. Izolované látky boli identifikované pomocou fyzikálno-chemických metód, porovnaním výsledkov so štandardami a literatúrou. Z rastlinného druhu Philadelphus tenuifolius Rupr. et Maxim. boli izolované prvýkrát.
Kľúčové slová:
Philadelphus tenuifolius • Hydrangeaceae • flavonoidové glykozidyÚvod
Philadelphus tenuifolius Rupr. et Maxim. – pajazmín tenkolistový z čeľade Hydrangeaceae je ker dosahujúci výšku 2–2,5 m. Rastie v zmiešaných lesoch, pochádza z východnej Sibíri, severnej Číny a Kórei. Obsahovým látkam tohto druhu a ich biologickým účinkom bolo doteraz venovaných málo prác. Zistenie cytotoxickej a antimikrobiálnej aktivity etanolového extraktu1–3) nás viedlo k štúdiu sekundárnych metabolitov, ktoré sa môžu na nich podieľať. V rode Philadelphus L. boli doteraz opísané najmä látky polyfenolového charakteru ako flavonoidy a aromatické kyseliny4), ktorých obsah v nadzemných častiach rastliny bol stanovený kolorimetricky5). Z konárov príbuzného druhu Philadelphus coronarius L. boli izolované triterpény a kyseliny6). Z listov to boli kumaríny, steroly, triterpény7) a flavonoidové glykozidy8–10). Z listov Philadelphus tenuifolius Rupr. et Maxim. boli doteraz izolované látky nepolárneho charakteru – triterpény taraxerol, stigmasteryl-3-O-β-D-glukozid a kumaríny umbeliferón a eskulín11).
Predložená práca opisuje izoláciu a identifikáciu obsahových látok metanolového a butanolového extraktu z listov Philadelphus tenuifolius Rupr. et Maxim. a prináša nové poznatky o ich výskyte v tejto časti rastliny.
Pokusná časť
Materiál a metódy
Pri izolácii a identifikácii obsahových látok Philadelphus tenuifolius Rupr. et Maxim. sa použil metanolový a butanolový extrakt z listov. Listy sa nazbierali v Arboréte Mlyňany, v Ústave dendrobiológie Slovenskej akadémie vied v septembri 2009 a usušili pri laboratórnej teplote.
Na separáciu obsahových látok sa použil silikagél zn. Silpearl, pripravený podľa Pitru a Štěrbu12) a Sephadex LH-20, na tenkovrstvovú chromatografiu Silufol UV 254 a 366 nm a Lucefol Quick (Kavalier, Votice, ČR) a silikagélové platne Kiesselgel 60 F254 (Merck). Detekcia chromatogramov sa robila UF žiarením pri 254 a 366 nm, kyselinou sírovou v éteri (1 : 4) s následným zahriatim na 120 °C, Neuovým skúmadlom a anilínftalátom13). Rozpúšťadlá použité pri chromatografii boli vopred predestilované.
Pri navažovaní sa používali analytické váhy Chyo JL-200 (Chyo, Japonsko). Teploty topenia sa merali na Kofflerovom bloku (VEB Analytik, Dresden) a nie sú korigované. Ultrafialové spektrá sa merali na prístroji Specord UV-VIS (Jena) v metanole a po pridaní špecifických diagnostických skúmadiel14). Hmotnostné spektrum na HPLC prístroji Agilent 1100 HP liquid chromatograph s MS ion trap detektorom. 1H NMR a 13C NMR spektrá boli merané na Varian MERCURY plus NMR spektrometri (Varian, Palo Alto, CA, USA) pracujúcom pri frekvencii 300 MHz (1H) a 75 MHz (13C). Kyslá hydrolýza sa robila 2% kyselinou sírovou; vodná fáza sa potom neutralizovala na DOWEX-e (FLUKA AG CHEMISCHE FABRIK BUCHS SG) podľa literatúry15, 16).
Extrakcia a izolácia látok
Usušené a pomleté listy Philadelphus tenuifolius Rupr. et Maxim. (460 g) sme extrahovali v Soxhletovej aparatúre a po odparení rozpúšťadla vo vákuu sme získali petroléterový (27,3 g), chloroformový (14,1 g), metanolový (42,5 g) a butanolový (2,2 g) extrakt.
Metanolový extrakt sme delili kolónovou chromatografiou na silikagéli č. 3 s obsahom 13 % vody. Kolónu sme eluovali zmesou rozpúšťadiel chloroform : metanol : cyklohexán v rôznom pomernom zastúpení. Eluáty sme zachytávali v množstvách približne po 50 ml. Tieto sme postupne odparovali a na základe výsledkov tenkovrstvovej chromatografie spojili do 23 frakcií hrubého delenia.
Frakciu č. 8 sme rechromatografovali na stĺpci Sephadexu LH-20 v sústave izopropanol : metanol s nárastom polárnej zložky. Frakcie sme zachytávali po cca 10 ml a na základe výsledkov tenkovrstvovej chromatografie pospájali do 12 frakcií. Z frakcie č. 6 sme kryštalizáciou z metanolu získali látku I.
Rovnakým spôsobom sme delili látky prítomné v butanolovom extrakte. Kolónu sme eluovali zmesou rozpúšťadiel chloroform : metanol : cyklohexán v rôznom pomernom zastúpení. Eluáty sme zachytávali v množstvách približne po 50 ml. Na základe výsledkov tenkovrstvovej chromatografie sme získali 9 frakcií hrubého delenia.
Frakciu č. 6 sme rechromatografovali na silikagéli č. 4 v sústave chloroform : metanol (90 : 10, 85 : 15 a 80 : 20). Frakcie sme zachytávali po 5 ml a na základe výsledkov tenkovrstvovej chromatografie pospájali do 7 frakcií. Z frakcie č. 4 sme kryštalizáciou z metanolu získali látku II.
Výsledky a diskusia
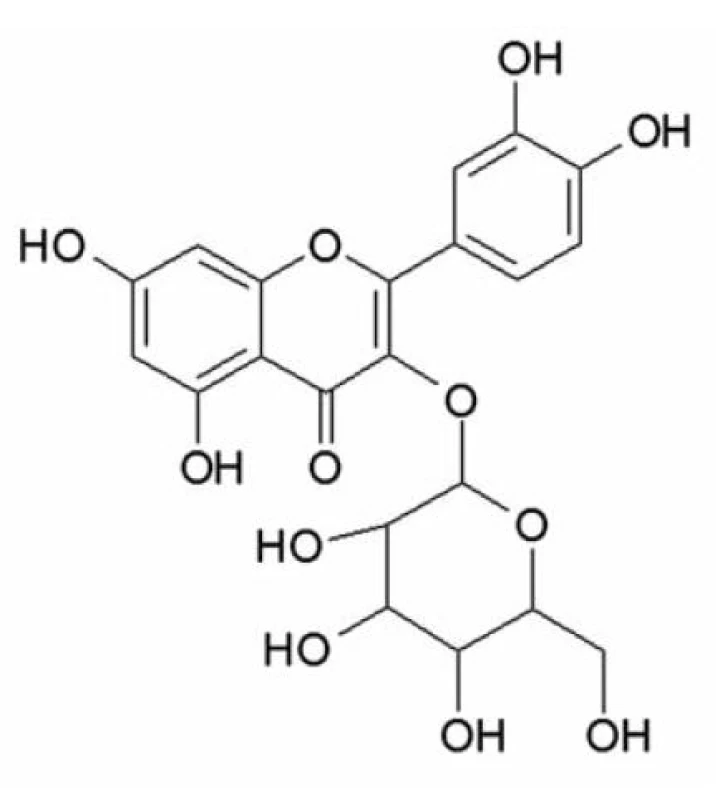
Látka I (8,5 mg) (obr. 1) bola izolovaná vo forme svetložltých mikrokryštálov s teplotou topenia 182–184 °C. Hmotnostné spektrum vykazuje molekulový ión [M-H] o m/z 463 (glykozid kvercetínu, cukor 162) a fragment o m/z 301 (aglykón). Utrafialové spektrum v metanole vykazuje pásy typické pre flavón: λMeOHmax nm: 254, 265sh, 293 a 358.
Po pridaní špecifických diagnostických skúmadiel sme namerali nasledujúce posuny maxím:
λNaOMemax nm: 270, 320 sh, 409
λAlCl3max nm: 270, 295sh, 430
λAlCl3/HClmax nm: 265, 295sh, 400
λNaOAcmax nm: 267, 398
λNaOAc/H3BO3max nm: 256, 368
1H NMR (300MHz, CD3OD) d: 7.7 (1/2(2H), d, J = 2.06 Hz); 7.59 (1/2(2H), dd, J = 8.5 Hz; J = 2.06 Hz); 6.87 (1H, d, J = 5.50 Hz); 6.40 (1H, d, J = 2.05 Hz); 6.21 (1H, d, J = 2.05 Hz); 5.25 (1H, d, J = 7.62 Hz); 3.73–3.19 (6H, m)
13C NMR (75.5 MHz, CD3OD) d: 197.55; 166.11; 163.13; 159.03; 158.53; 149.90; 145,97; 135.63; 123.22 (2C); 117.56; 116.03; 105.72; 104.25; 99.92; 94.72; 78.45; 78.15; 75.76; 71.24; 62.57
Na základe výsledkov spektrálnej analýzy a tenkovrstvovej chromatografie na Silufole možno predpokladať, že látka (I) je glykozid kvercetínu. Aglykón získaný kyslou hydrolýzou bol zhodný so štandardom kvercetínu. Cukorná zložka sa zhodovala so štandardom glukózy. Látku (I) sme identifikovali ako kvercetín-3-O-glukozid (izokvercitrín).
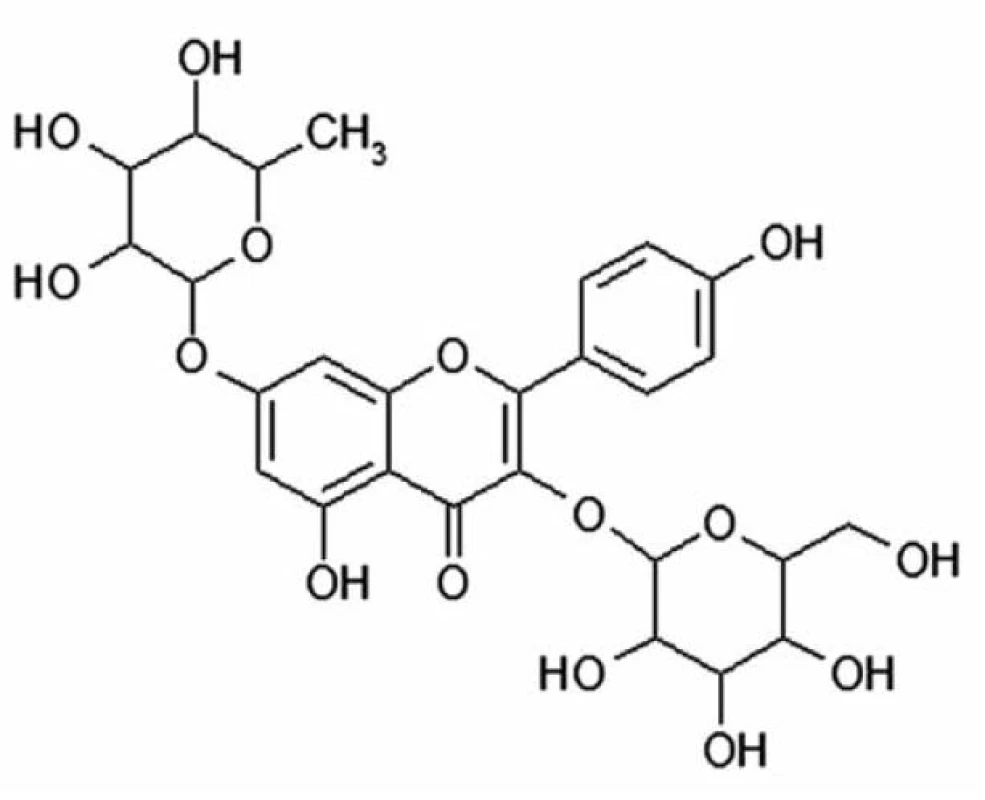
Látka II (11,5 mg) (obr. 2) bola izolovaná vo forme žltých mikrokryštálov s teplotou topenia 183–186 °C. Hmotnostné spektrum vykazuje molekulový ión [M-H] o m/z 593 (diglykozid kempferolu, cukry 162 a 146 v rôznych polohách) a fragment o m/z 448, 432 a 286. Utrafialové spektrum v metanole vykazuje pásy typické pre flavón: λMeOHmax nm: 268, 295sh a 355.
Po pridaní špecifických diagnostických skúmadiel sme namerali nasledujúce posuny maxím:
λNaOMemax nm: 276, 323 sh, 407
λAlCl3max nm: 274, 304sh, 407
λAlCl3/HClmax nm: 274, 304sh, 399
λNaOAcmax nm: 277, 395
λNaOAc/H3BO3max nm: 266, 362
1H NMR (300MHz, DMSO) d: 7.57 (2H, m); 6.87 (1H, d, J = 8.79 Hz); 6.46 (1H, d, J = 2.34 Hz); 6.23 (1H, d, J = 2.34 Hz); 5.44 (1H, m); 3.57 (2H, m); 3.36–3.11 (4H, m)
13C NMR (75.5 MHz, DMSO) d: 177.25; 163.77; 160.75; 156.24 (2C); 148.08; 144,47; 133.16; 121.57; 121.04; 115.93; 115.06; 103.84; 100.63; 98.49; 93.52; 77.18; 76.80; 73.80; 69.50; 60.58
Na základe výsledkov spektrálnej analýzy a tenkovrstvovej chromatografie na Silufole možno predpokladať, že látka (II) je glykozid kempferolu. Aglykón získaný kyslou hydrolýzou bol zhodný so štandardom kempferolu. Cukorné zložky sa zhodovali so štandardami glukózou a ramnózou. Látku (II) sme identifikovali ako kempferol-3-O-glukozid-7-O-ramnozid.
Práca bola realizovaná s podporou grantovej úlohy č. 1/0059/11 VEGA Ministerstva školstva SR. „Skríning biologických aktivít vybraných druhov liečivých rastlín a identifikácia ich aktívnych konštituentov“.
Stret záujmov: žiadny.
Došlo 10. marca 2014 / Prijato 21. marca 2014
prof. RNDr. Daniel Grančai, CSc. (∗) • S. Fialová • V. Huszár
Univerzita Komenského v Bratislave, Farmaceutická fakulta
Katedra farmakognózie a botaniky
Odbojárov 10, 832 32 Bratislava, SR
e-mail: grancai@fpharm.uniba.sk
J. Karlovská
Univerzita Komenského v Bratislave, Farmaceutická fakulta
Katedra fyzikálne chémie liečiv, NMR laboratórium
E. Švajdlenka
Veterinární a farmaceutická univerzita Brno, Farmaceutická fakulta
Ústav přírodních léčiv
Zdroje
1. Jantová S., Nagy M., Ružeková L., Grančai D. Cytotoxic Effects of Plant Extracts from the Families Fabaceae, Oleaceae, Philadelphaceae, Rosaceae and Staphyleaceae. Phytother. Res. 2001; 15, 22–25.
2. Jantová S., Nagy M., Ružeková L., Grančai D. Antibacterial Activity of Plant Extracts from the Families Fabaceae, Oleaceae, Philadelphaceae, Rosaceae and Staphyleaceae. Phytother. Res. 2000; 14, 601–603.
3. Vaľko V., Pravdová E., Nagy M., Grančai D., Ficková M. Cytotoxicity of plant extracts from genus Philadelphus L. Chem. Listy 2007; 101, 292–293.
4. Billek K., G., Kindl H. Über die phenolischen Inhaltstoffe der Familie Saxifragaceae. Monatsch. Chem. 1962; 93, 85–98.
5. Grančai D., Mučaji P., Nagy M. Stanovenie vybraných sekundárnych metabolitov a extraktívnych látok vo Philadelphus coronarius L. Čes. slov. Farm. 1999; 48, 265–267.
6. Mučaji P., Grančai D., Nagy M., Czigleová S., Ubik K. Obsahové látky konárov Philadelphus coronarius L. Farm. Obzor 2001; 70, 311–314.
7. Mučaji P., Grančai D., Nagy M., Czigleová S., Buděšínský M., Ubik K. Nepolárne obsahové látky listov Philadelphus coronarius L. Čes. slov. Farm. 2001; 50, 274–276.
8. Vaľko V., Grančai D. Flavonoidové glykozidy vo Philadelphus coronarius L. Farm. Obzor 2005; 74, 150–152.
9. Grančai D., Vaľko V., Švajdlenka E. Obsahové látky Philadelphus coronarius L. Čes. slov. Farm. 2010; 59, 219–221.
10. Grančai D., Fialová S., Karlovská J., Švajdlenka E. Sekundárne metabolity listov Philadelphus coronarius L. Farm. Obzor 2011; 80, 162–164.
11. Grančai D., Vaľko V., Švajdlenka E. Nepolárne obsahové látky v listoch Philadelphus tenuifolius Rupr. et Maxim. Farm. Obzor 2012; 81, 67–69.
12. Pitra J., Štěrba J. Třídění silikagélu pro chromatografii. Chem. Listy 1963; 57, 389–391.
13. Šaršúnová M., et al. Chromatografia na tenkých vrstvách vo farmácii a v klinickej biochémii. Bratislava: Osveta 1977.
14. Mabry T. J., Markham K. R., Thomas M. R. The systematic identification of flavonoids, New York: Springer Verlag 1970.
15. Friedrich H. Arch. Farm. 1962; 295, 59.
16. Friedrich H. Arch. Farm. 1962; 295, 465.
17. Devon T. K., Scott A. I. Handbook of Naturally Occuring Compounds: Vol. I Acetogenins, Shikimates and Carbohydrates. New York: Academic Press 975.
Štítky
Farmácia Farmakológia
Článok vyšiel v časopiseČeská a slovenská farmacie

2014 Číslo 3-
Všetky články tohto čísla
- Pokroky ve využití instrumentálního měření barevnosti ve vývoji, výrobě a v kontrole jakosti léčiv, léčivých přípravků a farmaceutických pomocných látek II*
- Příprava a hodnocení orálního gelu obsahujícího silici z jedle sibiřské (Abies sibirica Ledeb.)
- Hradec Králové hostil mladé farmaceutické chemiky z celé Evropy
- Flavonoidy – hlavné obsahové látky listov Philadelphus tenuifolius Rupr. et Maxim.
- Formulácia benzetóniumchloridu do gélov
- 9th World Meeting on Pharmaceutics, Biopharmaceutics and Pharmaceutical Technology – PBP Meeting
- Vliv formulačních a procesních proměnných na vlastnosti chitosanových mikrosfér připravených vnější iontovou gelací
- Lekárne a lekárnici v okrese Žilina pred rokom 1990
- Jandoušova česká lékopisná terminologie z roku 1864
- Racionalizace v československém lékárenství ve 20. století – farmaceutická sekce Komise pro racionalisaci a normalisaci v lékařství, zvěrolékařství a lékárnictví – 1. část
- Česká a slovenská farmacie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Jandoušova česká lékopisná terminologie z roku 1864
- Příprava a hodnocení orálního gelu obsahujícího silici z jedle sibiřské (Abies sibirica Ledeb.)
- Vliv formulačních a procesních proměnných na vlastnosti chitosanových mikrosfér připravených vnější iontovou gelací
- Racionalizace v československém lékárenství ve 20. století – farmaceutická sekce Komise pro racionalisaci a normalisaci v lékařství, zvěrolékařství a lékárnictví – 1. část
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy