-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
PŘEHLED RIZIKOVÝCH FAKTORŮ VZNIKU DEMENCE
OVERVIEW OF RISK FACTORS FOR DEMENTIA
Dementia is a complex syndrome with a rapidly growing global incidence. It has a dramatic impact, not only on the life of the patient who has been diagnosed, but also on the lives of his or her loved ones. At the same time, the costs associated with dementia are significantly higher than the costs of other major diseases. Research confirms that the elimination of known modifiable risk factors can lead to a potential significant reduction in the incidence of dementia. In the absence of effective treatment, knowledge of the risk factors and primary prevention are essential measures for global public health. Risk factors are divided into modifiable and non-modifiable, according to the extent to which they are influenced by the individual's lifestyle. The following article gives an overview of these risk factors for dementia, according to the conclusions of current research, as well as recommendations for prevention.
Keywords:
dementia – prevention – Alzheimer‘s disease – Vascular dementia – risk factors
Autori: Mgr. Hlaváčová Simona
Pôsobisko autorov: Soukromá klinika LOGO s. r. o.
Vyšlo v časopise: Listy klinické logopedie 2022; 6(2): 27-33
Kategória: Hlavní téma
doi: https://doi.org/10.36833/lkl.2022.024Súhrn
Demence je komplexní syndrom s rapidně rostoucí celosvětovou incidencí. Má dramatický dopad nejen na život pacienta, jemuž byla diagnostikována, ale i na život jeho blízkých. Současně jsou náklady spojené s demencí výrazně vyšší než náklady na jiná významná onemocnění. Výzkumy potvrzují, že eliminace známých modifikovatelných rizikových faktorů může vést k potenciální signifikantní redukci incidence demence, vzhledem k absenci efektivní léčby je tak znalost rizikových faktorů a primární prevence zásadním opatřením světového veřejného zdravotnictví. Rizikové faktory se dělí na modifikovatelné a nemodifikovatelné podle toho, nakolik jsou ovlivnitelné životním stylem jedince. Následující článek podává přehled těchto rizikových faktorů vzniku demence podle závěrů aktuálního výzkumu a také doporučení pro prevenci.
Klíčová slova:
demence – Alzheimerova nemoc – prevence – rizikové faktory – vaskulární demence
Úvod
Demence je syndrom charakterizovaný progresivní a ireversibilní ztrátou vyšších nervových kortikálních funkcí, zejména paměti. Kognitivní úpadek je spojen s dalšími významnými změnami nálady a chování, což vede ke kompletní dezintegraci osobnosti se zhoršením chápání a emoční kontroly, motivace a sociálního chování (Jirák, Koukolík, 2004).
Nejčastější příčinou demence je Alzheimerova nemoc, mezi další příčiny patří například vaskulární onemocnění, Parkinsonova nemoc, frontotemporální demence nebo demence s Lewyho tělísky.
V roce 2015 demence celosvětově postihovala zhruba 47 milionů lidí (zhruba 5 % světové starší populace). Studie predikují, že v roce 2030 by to mohlo být 75 milionů a v roce 2050 dokonce 132 milionů. Současná data ukazují, že ročně onemocní demencí téměř 9,9 milionů lidí, což znamená, že nový případ demence se objeví každé tři minuty. Zhruba 60 % lidí s demencí v současnosti žije v zemích s nízkých a středním příjmem a očekává se, že v těchto zemích se objeví i většina (75 %) nových případů (WHO, 2017, Prince et al., 2015).
Absence efektivní léčby demence znamená, že redukce rizikových faktorů je jedním z klíčových výzev veřejného zdravotnictví dnešní doby. Příčiny demence jsou komplexní a přesahující. Intenzivní sběr dat v průběhu posledních let identifikoval modifikovatelné rizikové faktory pro vznik demence a ukázal, že zaměření na tyto rizikové faktory má potenciál zabránit zásadnímu množství případů (Walsh et al., 2022).
Aktuální vědecké studie potvrzují kumulativní efekt zvyšujícího se počtu rizikových faktorů pro vznik demence (Peters et al., 2019). Rizikové faktory pro vznik demence se klasifikují jako modifikovatelné a nemodifikovatelné. Mezi nemodifikovatelné faktory patří věk, pohlaví a genetické faktory. Rostoucí počet důkazů pak podporuje zejména devět potenciálně modifikovatelných rizikových faktorů: nízké vzdělání, hypertenzi, poruchu sluchu, kouření, obezitu, depresi, nízkou fyzickou aktivitu, diabetes mellitus a sociální izolovanost. Tyto faktory byly stanoveny v roce 2017 Lancet Commission pro prevenci, intervenci a péči u demence (Livingston et al., 2017). Novější přesvědčivé vědecké důkazy přidávají k těmto faktorům mimo jiné ještě i nadměrnou konzumaci alkoholu, traumatické poranění mozku a znečištění ovzduší. Těchto celkem devět modifikovatelných faktorů je zodpovědných za zhruba 40 % světového výskytu demence (tabulka 1, Livingston et al., 2020).
Tab. 1. Přehled rizikových faktorů vzniku demence s modelem redukce prevalence při eliminaci modifikovatelných faktorů (Livingston et al., 2020) 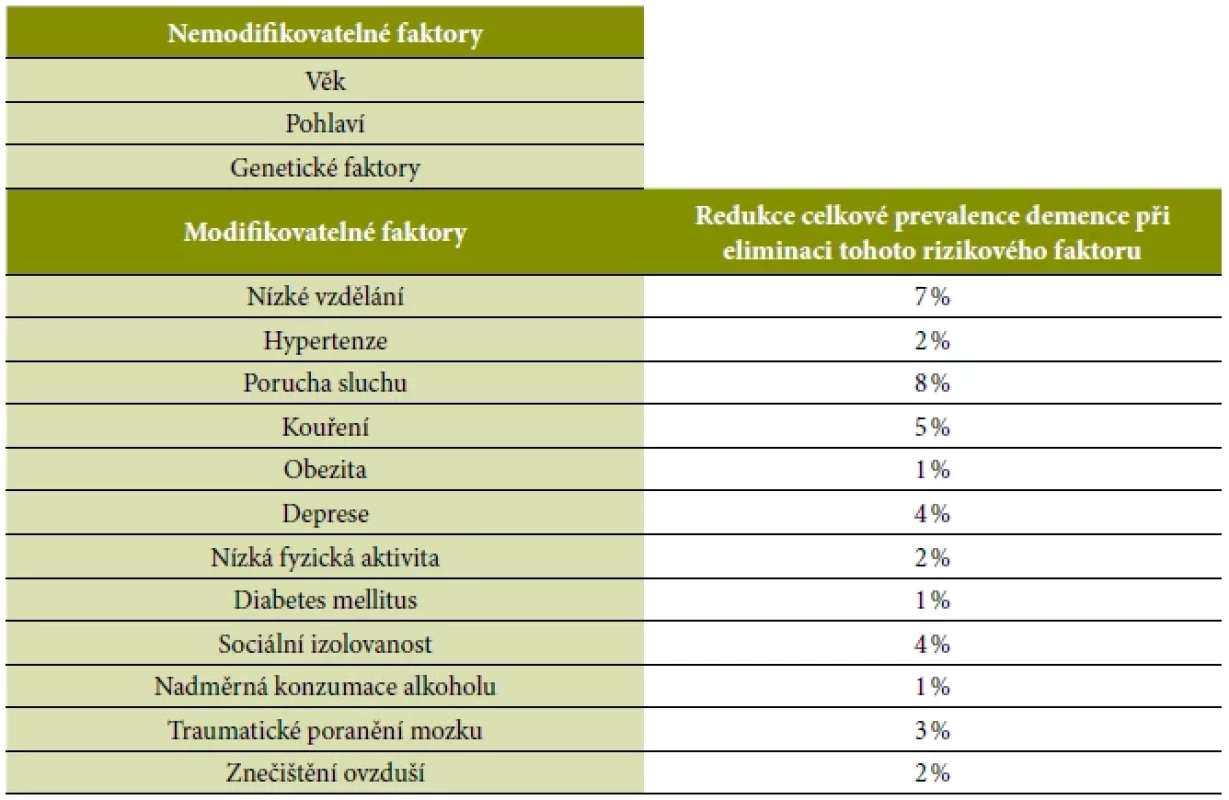
Nemodifikovatelné rizikové faktory
Věk
Množství kohortových studií v Evropě a Spojených státech amerických ukázalo, že se riziko demence zvyšuje v souvislosti s věkem (Kukull et al., 2002, Ganguli et al., 2000, Lopez-Pousa et al., 2004). Tato souvislost byla pozorována napříč všemi subtypy demencí. Efekt stárnutí je relativně konzistentním rizikovým faktorem napříč různými etnickými skupinami. Některé studie dokonce našly souvislost mezi věkem rodičů při porodu a rizikem vzniku demence u dítěte (pravděpodobně vzhledem k chromosomálním abnormalitám), ale tato souvislost nebyla potvrzena (Chen et al., 2009). U lidí mezi 65 až 69 lety je výskyt demence zhruba u dvou lidí ze sta. Riziko demence se zdvojnásobuje každých pět let. To znamená, že ve věku 90 let jde o statistický výskyt třicet tři lidí ze sta (Gardner et al., 2013). Za významnou rolí stárnutí jako rizikového faktoru výskytu demence stojí pravděpodobně dva hlavní důvody. Jedním z nich je to, že u staršího člověka je vyšší pravděpodobnost výskytu zdravotních potíží, které mohou zvyšovat riziko demence. Patří mezi ně vyšší krevní tlak, vyšší výskyt kardiovaskulárních onemocnění, snížená fyzická aktivita, slabší imunitní systém, nižší schopnost zotavení po zraněních a případné delirium (Pereira et al., 2021). Dalším důvodem je také to, že vývoj demence trvá delší časové období, než jsou pozorovány první znatelné symptomy.
Pohlaví
Pohlaví patří mezi další faktory související se vznikem demence. Metaanalýza z roku 2016 (Niu et al.) ukazuje, že Alzheimerova nemoc se vyskytuje častěji u žen než u mužů. U vaskulární demence je situace opačná. Oproti tomu u populace bez kognitivního deficitu podávají ženy staršího věku lepší výsledky v měření epizodické paměti než muži, navzdory tomu, že je u nich větší pravděpodobnost onemocnění Alzheimerovou nemocí, pro kterou je ztráta paměti typická (Olaya et al., 2017). Avšak relativní rozdíly v paměti v závislosti na pohlaví jsou podstatně menší než rozdíly ve výskytu demence. Některé studie uvádí velké množství rozdílů v závislosti na pohlaví v prevalenci rizikových a protektivních faktorů (Gilsanz et al., 2017, Cherbuin et al., 2015, McMcDermott et al., 2017). Například muži středního věku se dvakrát častěji než ženy účastní fyzických aktivit a mívají o 50 % větší pravděpodobnost vzniku diabetes. Ženy obvykle mívají méně modifikovatelných rizikových faktorů v průběhu života (zejména ve středním věku), avšak větší citlivost na efekt hypertenze. Je proto možné, že větší množství malých efektů rozdílů souvisejících s pohlavím v rámci modifikovatelných faktorů vede k pozorovaným celkovým rozdílům v oblasti faktoru pohlaví (Anstey et al., 2021).
Genetické faktory
Mnoho studií se věnuje spojitosti genetických faktorů se vznikem demence. V tzv. hypotéze amyloidní kaskády, což je aktuálně nejužívanější teorie objasňující patogenezi Alzheimerovy nemoci (Benek et al., 2012, Ono a Watanabe-Nakayama, 2021), je za hlavní spouštěč považován beta - -amyloid. Ten vzniká z transmembránového APP (amyloidového prekurzorového proteinu). Mutace genů APPPSEN1 (presenilin 1) a PSEN2 (presenilin 2) může způsobit časný začátek Alzheimerovy nemoci, ačkoliv se to týká jen mála procent případů. Většina případů demence se týká starších dospělých, kteří mají více genetických rizikových faktorů. Velkou roli hraje gen APOE4 (apolipoprotein E) v pozdním začátku Alzheimerovy nemoci. S rostoucím počtem alel tohoto genu stoupá riziko Alzheimerovy nemoci s pozdním začátkem z 20 % na 90 % a věk nástupu onemocnění klesá z 84 na 68 let (Corder et al., 1993). Polygenetické rizikové skóre kombinující více rizikových alel pro Alzheimerovu nemoc představuje predikci incidence demence a poskytuje kvantitativní měřítko genetického rizika demence. Je možné, že genetická rizika mohou být kompenzována modifikovatelnými faktory, ale studie zatím neprokazují v této oblasti jasné závěry (Lourida et al. 2019). Silný vliv genetických faktorů se předpokládá například i u tauopatií (např. frontotemporální demence), kdy je zjištěna specifická mutace genu pro tau protein MAPT (s mikrotobuly asociovaný protein tau) (Rusina et al., 2015).
Modifikovatelné rizikové faktory
Livingston et al. (2020) stanovují na základě výzkumů vysoké kvality celkem 12 zásadních modifikovatelných rizikových faktorů vzniku demence. Patří sem nižší vzdělání, hypertenze, porucha sluchu, kouření, obezita, deprese, nízká fyzická aktivita, diabetes, sociální izolovanost, nadměrná konzumace alkoholu, traumatické poranění mozku a znečištění ovzduší.
Nízké vzdělání
Matematický regresní model předpokládá, že kroky vedoucí ke zvýšení vzdělání v populaci by mohly být tím nejefektivnějším krokem k prevenci Alzheimerovy nemoci (de la Fuente Fernandez, 2006). Asociace mezi mírou vzdělání a rizikem vzniku demence je často zkoumaným tématem v prospektivních studiích vzhledem k tomu, že se jedná o nejužívanější prostředek kognitivní rezervy. Závěry metaanalýzy těchto studií (Xu et al. 2015) nasvědčují tomu, že jsou tyto dvě proměnné ve vztahu „dávky a odezvy“. Stále je však nejasné, jak úroveň edukace ovlivňuje riziko vzniku demence kvantitativně. Existuje několik potenciálních mechanismů, jejichž prostřednictvím vzdělání ovlivňuje pravděpodobnost vzniku demence. Jedním z nich je skutečnost, že úroveň vzdělání je spojena s životním stylem, faktory ovlivňujícími riziko kardiovaskulárních onemocnění, socioekonomickým statusem a mentálně stimulující aktivitou, tedy s faktory také spojovanými s výskytem demence. Závěry některých studií nasvědčují tomu, že vyšší úroveň vzdělání může poskytovat protekci před amyloidními plaky (depozity patologického beta-amyloidu (Bennett et al. 2005) a tauopatiemi (Rolstad et al., 2010). Zobrazovací studie zároveň ukazují, že vyšší úroveň vzdělání je pozitivně spojována s mozkovou rezervou včetně množství cerebrální tkáně (včetně šedé a bílé hmoty mozkové) (Foubert-Samier et al., 2012).
Hypertenze
Vztah mezi hypertenzí ve středním věku a kognitivním úpadkem v pozdějším věku je plně akceptovaný fakt (Machaczka et al., 2020). Etiopatogenetický mechanismus, prostřednictvím kterého může hypertenze způsobovat deterioraci kognitivních funkcí, zatím není jasně stanoven, ale největší význam zde má onemocnění malých mozkových cév. Avšak vliv krevního tlaku na kognitivní funkce se mění v závislosti na věku. Některá data u starší populace naznačují, že také epizody hypotenze nebo excesivní redukce krevního tlaku můžou způsobovat nebo zhoršovat úpadek kognitivních funkcí (Sierra, 2020).
Sluchová ztráta
Spojitost mezi vznikem demence a sluchovou ztrátou byla opakovaně prokázána (např. Lin et al., 2011, Gurgel et al., 2015), avšak kauzální vysvětlení toho, jak ztráta sluchu zvyšuje riziko demence, není zatím zřejmé. Nabízí se několik možných spojitostí. Jedna z nich je založena na vlivu sluchové ztráty na kortikální zpracování, druhá na tom, že ztráta sluchu vede k sociální izolaci, u které je souvislost s demencí také prokázána. Třetím prominentním vysvětlením je společná příčina obou onemocnění a možnost toho, že ztráta sluchu je ranou manifestací skryté patologie (Thomson et al., 2017).
Kouření
Kouření zvyšuje riziko Alzheimerovy nemoci a může zvyšovat riziko dalších typů demence (vaskulární, nespecifikované). Jedná se o obzvláště rizikový faktor u lidí nad 65 let. Přerušení kouření snižuje riziko na úroveň lidí, kteří nikdy nekouřili. Riziko vzniku demence při kouření je vyšší u lidí, kteří nejsou nositelé APOE4. Výzkumy také ukazují, že mortalita spojená s demencí je vyšší u kuřáků (Zhong et al., 2015). Studie využívající magnetickou rezonanci ukázaly, že kuřáci mají menší objem šedé kůry mozkové a přítomnost lakunárních infarktů u chronických kuřáků bývá také často s výskytem demence asociována (Cho et al., 2016). Redukovaná délka dožití u chronických kuřáků pak také může reálný dopad kouření na riziko vzniku demence zastírat (Janoutová et al., 2018).
Obezita
Obezita a demence můžou mít mnoho společných faktorů. Některé z nich zahrnují komorbidní stavy plynoucí z obezity, mezi které patří diabetes s inzulinovou rezistencí, hypertenze a kardiovaskulární onemocnění, přičemž všechna tato onemocnění mohou mít negativní dopad na mozek. Vysoké BMI zvyšuje riziko demence vzhledem ke sloučeninám, které jsou vylučovány tukovou tkání (Anjum et al., 2018). Při užití indexu tělesné hmotnosti (body mass index, BMI) jako statistického nástroje měli pacienti s obezitou o 74 % vyšší riziko demence a pacienti s nadváhou o 35 % vyšší riziko demence než osoby s normální váhou (Fenclová et al., 2020).
Deprese
Metaanalýza z roku 2020 (Santabárbara et al.) nalezla statisticky významnou spojitost mezi výrazně vyšším rizikem demence a depresí. Spojitost mezi depresí a demencí může záviset na věku, ve kterém došlo k první depresivní epizodě. Deprese v mladším věku je spojována s větší chronicitou, horším psychosociálním fungováním, kvalitou života a s více genetickými faktory. Lidé, kteří zažili více depresivních epizod, mohou opakovaně aktivovat úroveň steroidů vedoucí k poruše oblasti hipokampu. V současnosti vzrůstá počet studií potvrzujících spojitost mezi depresí a zánětlivými markery a mezi záněty v nervovém systému a beta-amyloidovým zatížením (Wion, 2018). Deprese současně představuje rizikový faktor pro infarkt myokardu nebo cévní mozkovou příhodu, faktory, které také mohou vést k rozvoji demence (Santabárbara et al., 2020). Nejvíce je symptomatologie deprese popisována u Alzheimerovy nemoci, ale již v časných fázích onemocnění se objevuje například i u Huntingtonovy choroby nebo vaskulární demence (Dostál, 2011).
Nízká fyzická aktivita
Udává se, že 3 % případů demence by bylo možné předejít pouhým zvýšením fyzické aktivity jedinců. Stále vzrůstající počet důkazů potvrzuje význam fyzické aktivity a cvičení pro prevenci a eventuální zpomalení patologických procesů a problémů spojených s demencí. V metaanalýze zahrnující 15 prospektivních kohortových studií (Sofi et al., 2011) byla vyšší úroveň fyzické aktivity spojena s výraznou redukcí v nástupu demence. Potvrzena byla také důležitá role fyzické aktivity u pacientů s již diagnostikovanou demencí. Fyzické cvičení pomáhalo zlepšit významné oblasti, jako například kognici. Cvičení také pomáhá při managementu behaviorálních a psychologických symptomů demence (Demurtas et al., 2020).
Diabetes mellitus
Jedinci s diagnostikovaným diabetes mellitus mají výrazně vyšší riziko vzniku demence. Diabetes mellitus je spojován s 1,5–2,5krát větším rizikem vzniku demence u starších lidí. Za možné biologické mechanismy zodpovědné za tuto spojitost lze považovat kardiovaskulární rizikové faktory, glukózový toxický a oxidační stres, hyperinzulinemii, zánět a hypoglykemické epizody (Ninomiya, 2019). Kognitivní dysfunkce se liší podle typu diabetu. Do demence častěji progreduje kognitivní dysfunkce u diabetu 2. typu, přičemž konkrétně ve vyšším věku bývá tento typ spojován s vyšším rizikem vaskulární demence a i demence u Alzheimerovy nemoci (Tůma, 2007).
Sociální izolovanost
Sociální izolovanost je spojována s incidencí demence do té míry, že je její dopad srovnatelný s dopadem jiných rizikových faktorů, jako je nízká vzdělanost, fyzická inaktivita nebo deprese. Metaanalýza z roku 2015 (Kuiper et al.) potvrzuje, že lidé s absencí sociálních kontaktů a četnějšími pocity osamělosti jsou ve zvýšeném riziku vzniku demence. Jedním z možných vysvětlení je, že zapojení do intelektuálních, sociálních a fyzických aktivit stimuluje mozek, dochází k ovlivnění jeho struktur a vede k lepšímu využívání mozkových sítí. Druhým vysvětlením může být redukce stresu, který je spojován až s dvojnásobným zvýšením rizika vzniku Alzheimerovy nemoci vzhledem ke strukturálním změnám v hipokampu (Kim et al., 2015).
Nadměrná konzumace alkoholu
Lehká až střední konzumace alkoholu ve středním věku byla po určitou dobu v různých observačních studiích asociována se sníženým rizikem kognitivních poruch a demence. Ale závěry byly rozporuplné a vzhledem k vysokému počtu metodologických nedostatků v těchto výzkumech nemůže být tato kauzalita zatím pevně stanovena (Rehm et al. 2019). Oproti tomu bylo v zobrazovacích a observačních studiích prokázáno, že dlouhodobá nadměrná konzumace alkoholu je spojována se změnami ve struktuře mozku stejně tak jako s kognitivním, exekutivním narušením a se zvýšeným rizikem vzniku všech typů demence (Kruman et al., 2012). Toto může souviset také s negativním ovlivňováním kardiovaskulárního a gastrointestinálního systému, s podílem na rozvoji nádorových onemocnění a neurotoxickým působením nadměrné konzumace alkoholu (Fenclová et al., 2020). Práh konzumace alkoholu, při kterém dochází k narušení kognice (návratně či nenávratně), však zatím nebyl přesně stanoven (Rehm et al., 2019).
Traumatické poranění mozku
Riziko Alzheimerovy nemoci (nejčastějšího typu demence) roste už s jedním středně těžkým až těžkým traumatickým poraněním mozku (TPM) (Perry et al., 2016). Opakované lehké TPM zvyšují riziko chronické traumatické encefalopatie, degenerativního onemocnění spojovaného se syndromem demence (Růžička, 2018). TPM může být také rizikovým faktorem pro vznik jiných neurodegenerativních onemocnění, která mohou být spojována s demencí. Specifickými rizikovými faktory posilujícími riziko vzniku demence u pacientů po TPM jsou například snížené kognitivní nebo neuronální rezervy a související proměnné u osob vyššího věku a přítomnost alel rizikového APOE4. Za neuropatologické znaky spojující TPM s neurokognitivními syndromy jsou považovány stavy, kdy akutní TPM vede k amyloidové patologii a jiným neurodegenerativním proteinopatiím, nebo kdy chronická traumatická encefalopatie sdílí znaky s neurodegenerativními demencemi. Patří sem také stav, kdy TPM vede k narušení neurálních sítí a bílé hmoty mozkové (Mendez, 2017).
Znečištění ovzduší
Znečištění ovzduší je současný a stále narůstající globální problém. Je potvrzen jako kauzativní faktor u několika onemocnění, jako jsou například onemocnění srdce, cévní mozková příhoda a rakovina (Landrigan et al., 2018) a současně je spojováno i s rizikem vzniku demence. Se zvýšeným rizikem vzniku demence je spojována vysoká expozice prachovým částicím (PM2.5), oxidu dusičitému (NO2), oxidům dusíku (Nox) a oxidu uhelnatému (CO) (Peters et al., 2019). Na rozdíl od jiných modifikovatelných faktorů je možnost jedince převzít kontrolu nad expozicí znečištěnému ovzduší značně limitována.
Závěr
Demence dramaticky ovlivňuje nejen život pacientů a jejich blízkých, ale má také výrazný vliv na ekonomiku, neboť celosvětové náklady spojené s demencí jsou odhadovány na 1 trilion dolarů ročně (Patterson, 2018). Walsh et al. (2022) ve své studii navrhuje v rámci prevence demence přístup orientovaný na celou populaci (na rozdíl od přístupu orientovaného na zodpovědnost jedince). V rámci tohoto přístupu navrhuje zejména celosvětovou prioritizaci edukace dětí, implementaci veřejných zdravotních opatření, která povedou k redukci rizika hypertenze v celé populaci, a vývoj opatření pro podporu sociální, kognitivní a fyzické aktivity napříč celým životem (bez vědeckých důkazů pro doporučení nějaké konkrétní specifické aktivity). Mimo to pak také doporučuje podporu výzkumu rizik ztráty sluchu v průběhu života, redukci rizika vážných poranění mozku v relevantních zařízeních (např. dopravě), národní a mezinárodní opatření pro redukci znečištění vzduchu a pokračování ve snahách o redukci kouření u dětí i dospělých. V rámci zodpovědnosti jedince navrhuje důkladnou léčbu hypertenze, využívání sluchových pomůcek u lidí se ztrátou sluchu a redukci konzumace alkoholu na méně než 21 jednotek za týden. Dále zdůrazňuje potřebu prevence poranění hlavy u rizikových osob, odvyknutí kouření a redukci obezity včetně souvisejícího udržení fyzické aktivity po maximální možnou dobu.
Mgr. Simona Hlaváčová
Soukromá klinika LOGO s.r.o.
Vsetínská 20
63900 Brno
Česká republika
E-mail: hlavac.simona@gmail.com.
Přijato k recenzi: 24. 9. 2022
Přijato k publikaci: 30. 10. 2022
licensed under CC BY-NC
Zdroje
- ANJUM, I., FAYYAZ, M., WAJID, A., SOHAIL, W., ALI, A., 2018. Does Obesity Increase the Risk of Dementia: A Literature Review. Cureus. 10(5), s. e2660 [cit. 2022-09-23]. DOI:10.7759/cureus.2660.
- ANSTEY, K. J., PETERS, R., MORTBY, M. E. et al., 2021. Association of sex differences in dementia risk factors with sex differences in memory decline in a population-based cohort spanning 20–76 years. Sci Rep. 11, s. 7710 [cit. 23. 9. 2022]. DOI: 10.1038/ s41598-021-86397-7.
- BENEK, O., MUSÍLEK, K., KUČA, K., 2012. Mitochondriální enzym ABAD a jeho role v rozvoji a léčbě Alzheimerovy nemoci. Čes. slov. Farm. 61, s. 144-149 [cit. 23. 9. 2022]. Dostupné z: https://www.prolekare.cz/casopisy/ceska-slovenska-farmacie/2012-4-7/ mitochondrialni-enzym-abad-a-jeho-role-v-rozvoji-a-lecbe-alzheimerovy-nemoci-39241/download?hl=cs
- CORDER, E. H., SAUNDERS, A. M., STRITTMATTER, W. J. et al., 1993. Genedose of apolipoprotein E type 4 allele and the risk ofAlzheimer‘s disease in late onset families. Science. 261, s. 921-3 [cit. 23. 9. 2022]. Dostupné z: https://www.science.org/doi/10.1126/ science.8346443?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
- DE LA FUENTE-FERNANDEZ, R., 2006. Impact of neuroprotection onincidence of Alzheimer’s disease. PLoS One. 1, s. e52 [cit. 23. 9. 2022]. DOI: 10.1371/journal.pone.0000052.
- DEMURTAS, J., SCHOENE, D., TORBAHN, G. et al., 2020. Physical Activity and Exercise in Mild Cognitive Impairment and Dementia: An Umbrella Review of Intervention and Observational Studies. J Am Med Dir Assoc. 21(10), s. 1415-1422. e6 [cit. 23. 9. 2022]. DOI: 10.1016/j.jamda.2020.08.031.
- DOSTÁL, V., 2011. Vztah demence a deprese. Psychiatr. praxi. 12(4), s. 145-148 [cit. 23. 9. 2022]. Dostupné z: https://www. psychiatriepropraxi.cz/artkey/psy-201104-0003_Vztah_demence_a_deprese.php
- FENCLOVÁ, E., ALBRECHT, J., HARSA, P., JIRÁK, R., 2020. Rizikové faktory Alzheimerovy nemoci. Čes a slov Psychiat. 116(2), s. 59-65 [cit. 23. 9. 2022]. Dostupné z: http://www.cspsychiatr.cz/dwnld/CSP_2020_2_59_65.pdf
- FOUBERT-SAMIER, A., CATHELINE, G., AMIEVA, H., DILHARREGUY, B., HELMER, C., ALLARD, M., DARTIGUES, J. F., 2012. Education, occupation, leisureactivities, and brain reserve: a population-based study. Neurobiology of aging. 33(2), s. 423.e15-423. e25 [cit. 23. 9. 2022]. DOI: 10.1016/j.neurobiolaging.2010.09.023.
- GANGULI, M., DODGE, H. H., CHEN, P., BELLE, S., DEKOSKY, S. T., 2000. Ten-year incidence of dementia in a rural elderly US community population: the MoVIES Project. Neurology. 54(5), s. 1109-1116 [cit. 23. 9. 2022]. DOI:10.1212/wnl.54.5.1109.
- GARDNER, R. C., VALCOUR, V., YAFFE, K., 2013. Dementia in the oldest old: a multi-factorial and growing public health issue. Alz Res Therapy. 5, č. článku 27 [cit. 23. 9. 2022]. DOI: 10.1186/alzrt181.
- GILSANZ, P., MAYEDA, E. R., GLYMOUR, M. M. et al., 2017. Female sex, early-onset hypertension, and risk of dementia. Neurology. 89(18), s. 1886-1893 [cit. 23. 9. 2022]. DOI:10.1212/WNL.0000000000004602.
- GURGEL, R. K., WARD, P. D., SCHWARTZ, S., NORTON, M. C., FOSTER, N. L., TSCHANZ, J. T., 2014. Relationship of hearing loss and dementia: a prospective, population-based study. Otol Neurotol. 35(5), s. 775-781 [cit. 23. 9. 2022]. DOI:10.1097/ MAO.0000000000000313.
- CHEN, J. H., LIN, K. P., CHEN, Y. C., 2009. Risk factors for dementia. J Formos Med Assoc.108(10), s. 754-764 [cit. 2022-09-23]. DOI:10.1016/S0929-6646(09)60402-2.
- CHERBUIN, N., MORTBY, M. E., JANKE, A. L., SACHDEV, P. S., ABHAYARATNA, W. P., ANSTEY, K. J., 2015. Blood pressure, brain structure, and cognition: opposite associations in men and women. Am J Hypertens. 28(2), s. 225-231 [cit. 23. 9. 2022]. DOI:10.1093/ ajh/hpu120.
- CHO, H., KIM, C., KIM, H. J. et al., 2016. Impact of smoking on neurodegeneration and cerebrovascular disease markers incognitively normal men. Eur J Neurol. 23(1), s. 110-119 [cit. 23. 9. 2022]. DOI: 10.1111/ene.12816.
- JANOUTOVÁ, J., AMBROZ, P., KOVALOVÁ, M., MACHACZKA, O. et al., 2018. Epidemiologie mírné kognitivní poruchy. Cesk Slov Neurol N. 81(3), s. 284-289 [cit. 23. 9. 2022]. DOI: 10.14735/amcsnn2018284.
- JIRÁK, R., KOUKOLÍK. F. 2004. Demence: neurobiologie, klinický obraz, terapie. Praha: Galén. ISBN 80-7262-268-4.
- KIM, E. J., PELLMAN, B., KIM, J. J., 2015. Stress effect on the hippocampus: a critical review. Learn. Mem. 22, s. 411-416 [cit. 23. 9. 2022]. DOI: 10.1101/lm.037291.114.
- KUIPER, J. S., ZUIDERSMA, M., OUDE VOSHAAR, R. C. et al., 2015. Social relationships and risk of dementia: A systematic review and meta-analysis of longitudinal cohort studies. Ageing Res Rev. 22, s. 39-57 [cit. 23. 9. 2022]. DOI: 10.1016/j.arr.2015.04.006.
- KUKULL, W. A, HIGDON, R., BOWEN, J. D. et al., 2002. Dementia and Alzheimer disease incidence: a prospective cohort study. Arch Neurol. 59(11), s. 1737-1746 [cit. 2022-09-23]. DOI:10.1001/archneur.59.11.1737.
- LANDRIGAN, P. J., FULLER, R., ACOSTA, N. J. R., ADEYI, O., ARNOLD, R. et al., 2018. The Lancet Commission on pollution and health. Lancet. 391, s. 462-512 [cit. 23. 9. 2022]. DOI:10.1016/S0140-6736(17)32345-0.
- LIN, F. R., METTER, E. J., O'BRIEN, R. J., RESNICK, S. M., ZONDERMAN, A. B., FERRUCCI, L., 2011. Hearing loss and incident dementia. Arch Neurol. 68(2), s. 214-220 [cit. 23. 9. 2022]. DOI:10.1001/archneurol.2010.362.
- LIVINGSTON, G., HUNTLEY, J., SOMMERLAD, A. et al., 2020. Dementia prevention, intervention, and care: 2020 report of the Lancet Commission. Lancet. 396(10248), s. 413-446 [cit. 23. 9. 2022]. DOI:10.1016/S0140-6736(20)30367-6.
- LIVINGSTON, G., SOMMERLAD, A., ORGETA, V. et al., 2017. Dementia prevention, intervention, and care. Lancet. 390(10113), s. 2673-2734 [cit. 23. 9. 2022]. DOI:10.1016/S0140-6736(17)31363-6.
- LOPEZ-POUSA S., VILALTA-FRANCH J., LLINAS-REGLA J. et al., 2004. Incidence of dementia in a rural community in Spain: theGirona cohort study. Neuroepidemiology. 23, s. 170-177 [cit. 23. 9. 2022]. DOI:10.1159/000078502.
- LOURIDA, I., HANNON, E., LITTLEJOHNS, T. J. et al., 2019. Association of Lifestyle and Genetic Risk With Incidence of Dementia. JAMA. 322(5), s. 430-437 [cit. 23. 9. 2022]. DOI:10.1001/jama.2019.9879.
- MACHACZKA, O., JANOUTOVÁ, J., AMBROZ, P., ZATLOUKALOVÁ, A., JANOUT, V., 2020. Vztah hypertenze a demence – stručný přehled. Profese online. 13(1), s. 22-28 [cit. 23. 9. 2022]. DOI: 10.5507/pol.2020.005.
- MCDERMOTT, K. L., MCFALL, G. P., ANDREWS, S. J, ANSTEY, K. J., DIXON, R. A., 2017. Memory Resilience to Alzheimer‘s Genetic Risk: Sex Effects in Predictor Profiles. J Gerontol B Psychol Sci Soc Sci. 72(6), s. 937-946 [cit. 23. 9. 2022]. DOI:10.1093/geronb/gbw161.
- MENDEZ, M. F., 2017. What is the Relationship of Traumatic Brain Injury to Dementia? J Alzheimers Dis. 57(3), s. 667-681 [cit. 23. 9. 2022]. DOI:10.3233/JAD-161002. NINOMIYA, T., 2019. Epidemiological Evidence of the Relationship Between Diabetes and Dementia. Adv Exp Med Biol. 1128, s. 13-25 [cit. 23. 9. 2022]. DOI:10.1007/978-981-13-3540-2_2.
- NIU, H., ALVAREZ-ALVAREZ, I., GUILLEN-GRIMA, F., AGUINAGA-ONTOSO, I., 2016. Prevalence and incidence of Alzheimer’s disease in Europe: A meta-analysis. Neurologia. 32, s. 523-532 [cit. 23. 9. 2022]. DOI: 10.1016/j.nrl.2016.02.016.
- OLAYA, B., BOBAK, M., HARO, J. M., DEMAKAKOS, P., 2017. Trajectories of verbal episodic memory in middle-aged and older adults: Evidence from the English longitudinal study of ageing. J. Am. Geriatr. Soc. 65, s. 1274-1281 [cit. 23. 9. 2022]. DOI: 10.1111/ jgs.14789.
- ONO, K. a T. WATANABE-NAKAYAMA, 2021. Aggregation and structure of amyloid β-protein. Neurochemistry International [online]. [cit. 23. 9. 2022]. 151, s. 1-7. ISSN 01970186 DOI: 10.1016/j.neuint.2021.105208.
- PATTERSON C., 2018. World Alzheimer report 2018. The State of the Art of Dementia Research: New Frontiers. An Analysis of Prevalence, Incidence, Cost and Trends. Alzheimer‘s Disease International [cit. 23. 9. 2022]. Dostupné z: http://www.alz.co.uk/research/ world-report-2018
- PEREIRA, J. V., AUNG THEIN, M. Z., NITCHINGHAM, A., CAPLAN, G. A., 2021. Delirium in older adults is associated with development of new dementia: a systematic review and meta-analysis. Int J Geriatr Psychiatry. 36(7), s. 993-1003 [cit. 23. 9. 2022]. DOI:10.1002/gps.5508.
- PERRY, D. C., STURM, V. E., PETERSON, M. J. et al., 2016. Association of traumatic brain injury with subsequent neurological and psychiatric disease: a meta-analysis. J Neurosurg. 124(2), s. 511-526 [cit. 23. 9. 2022]. DOI:10.3171/2015.2.JNS14503.
- PETERS, R., EE, N., PETERS, J., BOOTH, A., MUDWAY, I., ANSTEY, K. J., 2019. Air Pollution and Dementia: A Systematic Review. J Alzheimers Dis. 70(s1), s. S145-S163 [cit. 23. 9. 2022]. DOI:10.3233/JAD-180631.
- PETERS, R. et al., 2019. Combining modifiable risk factors and risk of dementia: A systematic review and meta-analysis. BMJ Open. 9, e022846 [cit. 23. 9. 2022]. DOI10.1136/bmjopen-2018-022846.
- PRINCE, M., WIMO, A., GUERCHET, M., ALI, G. C., WU, YUTZU, PRINA, M., 2015. World Alzheimer Report 2015. The global impact of dementia: ananalysis of prevalence, incidence, cost and trends. London: Alzheimer‘s Disease International [cit. 23. 9. 2022]. Dostupné z: http://www.alz.co.uk/research/world-report-2015
- REHM, J., HASAN, O. S. M., BLACK, S. E. et al., 2019. Alcohol use and dementia: a systematic scoping review. Alz Res Therapy. 11(1). [cit. 23. 9. 2022]. DOI:10.1186/s13195-018-0453-0.
- RUSINA, R., MATĚJ, R., RŮŽIČKA, E., ROTH, J., 2015. Diferenciální diagnostika tauopatií – klinický pohled. Cesk Slov Neurol N. 78/111(5), s. 526-534 [cit. 23. 9. 2022]. DOI: 10.14735/amcsnn2015526.
- RŮŽIČKA, F. 2018. Traumata jako příčina extrapyramidových syndromů. Cesk Slov Neurol N. 81(1), s. 8 [cit. 23. 9. 2022]. Dostupné z: https://www.csnn.eu/casopisy/ceska-slovenska-neurologie/2018-1-8/traumata-jako-pricina-extrapyramidovych-syndromu-62890
- SANTABÁRBARA, J., VILLAGRASA, B., GRACIA-GARCÍA, P., 2020. Does depression increase the risk of dementia? Updated meta-analysis of prospective studies. Actas Esp Psiquiatr. 48(4), s. 169-180 [cit. 23. 9. 2022]. Dostupné z: https://www.actaspsiquiatria. es/repositorio//22/126/ENG/22-126-ENG-169-80-840128.pdf
- SIERRA, C., 2020. Hypertension and the Risk of Dementia. Front Cardiovasc Med.7, s. 5 [cit. 23. 9. 2022]. DOI:10.3389/fcvm.2020.00005.
- SOFI, F., VALECCHI, D., BACCI, D. et al., 2011. Physical activity and risk of cognitive decline: a meta-analysis of prospective studies. J Intern Med. 269(1), s. 107-117 [cit. 23. 9. 2022]. DOI:10.1111/j.1365-2796.2010.02281.x.
- THOMSON, R., AUDUONG, P., MILLER, A., GURGEL, R., 2017. Hearing loss as a risk factor for dementia: A systematic review: Hearing Loss and Dementia Systematic Review. Laryngoscope Investigative Otolaryngology. 2(2), s. 69-79. [cit. 23. 9. 2022]. DOI: 10.1002/ lio2.65.
- TŮMA, I., 2007. Diabetes mellitus a kognitivní poruchy. Vnitř Lék. 53(5), s. 486-488 [cit. 23. 9. 2022]. Dostupné z: https:// casopisvnitrnilekarstvi.cz/pdfs/vnl/2007/05/04.pdf
- WALSH, S., GOVIA, I., WALLACE, L. et. al., 2022. A whole-population approach is required for dementia risk reduction. Lancet Healthy Longev. 3(1), s. e6-e8 [cit. 23. 9. 2022]. DOI:10.1016/S2666-7568(21)00301-9. WION, D., 2018. The temporal relationshipbetween Alzheimer’s Diseaseand depressive symptoms: variable matters. Am J Psychiatry. 175(8), s. 793 [cit. 23. 9. 2022]. DOI: 10.1176/appi.ajp.2018.18020164
- WHO, 2017. Global action plan on the public health response to dementia 2017–2025. Geneva: World.Health Organization; ISBN 978-92-4-151348-7. WHO, 2015. The epidemiology and impact of dementia: current state and future trends. Geneva: World Health Organization; document WHO/MSD/MER/15.3 [cit. 23. 9. 2022]. Dostupné z: http://www.who.int/mental_health/neurology/dementia/dementia_ thematicbrief_epidemiology.pdf
- XU, W., TAN, L., WANG, H. F. et. al., 2016. Education and Risk of Dementia: Dose-Response Meta-Analysis of Prospective Cohort Studies. Mol Neurobiol. 53(5), s. 3113-3123 [cit. 23. 9. 2022]. DOI:10.1007/s12035-015-9211-5.
- ZHONG, G., WANG, Y., ZHANG, Y., GUO, J. J., ZHAO, Y., 2015. Smoking is associated with an increased risk of dementia: a meta-analysis of prospective cohort studies with investigation of potential effect modifiers [published correction appears in PLoS One. 2015; 10(4):e0126169]. PLoS One. 10(3), s. e0118333. [cit. 23. 9. 2022]. DOI: 10.1371/journal.pone.0118333.
Štítky
Logopédia Praktické lekárstvo pre deti a dorast
Článok vyšiel v časopiseListy klinické logopedie
Najčítanejšie tento týždeň
2022 Číslo 2- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Hluboká stimulace globus pallidus zlepšila klinické příznaky u pacientky s refrakterním parkinsonismem a genetickou mutací
- Léčba bolesti a horečky u dětí
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Gastroezofageální reflux a gastroezofageální refluxní onemocnění u kojenců a batolat
-
Všetky články tohto čísla
- EDITORIAL
- POROZUMĚNÍ ŘEČI V KONTEXTU JAZYKOVÝCH DEFICITŮ U OSOB S NEUROKOGNITIVNÍMI PORUCHAMI
- TERAPIE PRIMÁRNÍ PROGRESIVNÍ AFÁZIE V AKTUÁLNÍM VÝZKUMU
- POROZUMĚNÍ VĚTÁM U PACIENTKY S MÍRNOU KOGNITIVNÍ PORUCHOU AMNESTICKÉHO TYPU: KAZUISTIKA
- PŘEHLED RIZIKOVÝCH FAKTORŮ VZNIKU DEMENCE
- PROSTOROVÝ NEGLEKT U PACIENTŮ PO CÉVNÍ MOZKOVÉ PŘÍHODĚ
- PACIENT SE ZÍSKANOU PORUCHOU ŘEČOVÝCH SCHOPNOSTÍ V PRAXI KLINICKÉHO NEUROPSYCHOLOGA, KAZUISTIKA
- ODKAZY NA ZAJÍMAVÉ ZÁVĚREČNÉ PRÁCE S TEMATIKOU KOGNITIVNĚ-KOMUNIKAČNÍCH PORUCH
- STRUČNÝ DOTAZNÍK DĚTSKÉHO SLOVNÍKU SSDS 16-42: PŘEDSTAVENÍ SCREENINGOVÉHO DIAGNOSTICKÉHO NÁSTROJE PRO VČASNÉ ODHALENÍ DĚTÍ S OPOŽDĚNÍM VE VÝVOJI JAZYKOVÝCH SCHOPNOSTÍ
- SOCIÁLNĚ PRAGMATICKÁ KOMUNIKAČNÍ PORUCHA
- AUTOSTIGMATIZACE V KOKTAVOSTI – ÚVODNÍ VÝZKUM ZA VYUŽITÍ POLSKÉ ADAPTACE ŠKÁLY VNÍMÁNÍ KOKTAVOSTI
- RECENZE DIAGNOSTICKÉHO MATERIÁLU TEPO – TEST POROZUMĚNÍ VĚTÁM
- RECENZE KNIHY DEMENCE: HODNOTICÍ TECHNIKY A NÁSTROJE
- STIMULUJÚCE A PODPORUJÚCE PROSTREDIE JE AZDA NAJDÔLEŽITEJŠIE PRE ZAČÍNAJÚCEHO ODBORNÍKA ROZHOVOR S PROF. ZSOLTEM CSÉFALVAYEM
- Listy klinické logopedie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- SOCIÁLNĚ PRAGMATICKÁ KOMUNIKAČNÍ PORUCHA
- PŘEHLED RIZIKOVÝCH FAKTORŮ VZNIKU DEMENCE
- RECENZE DIAGNOSTICKÉHO MATERIÁLU TEPO – TEST POROZUMĚNÍ VĚTÁM
- STRUČNÝ DOTAZNÍK DĚTSKÉHO SLOVNÍKU SSDS 16-42: PŘEDSTAVENÍ SCREENINGOVÉHO DIAGNOSTICKÉHO NÁSTROJE PRO VČASNÉ ODHALENÍ DĚTÍ S OPOŽDĚNÍM VE VÝVOJI JAZYKOVÝCH SCHOPNOSTÍ
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




