-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Léčba Castlemanovy choroby z pohledu roku 2026
Treatment of Castleman disease from the perspective of the year 2026
Background: New drugs are continuously entering clinical practice, and therefore opinions on the treatment of Castleman disease are constantly being updated. The text provides information on the treatment of this disease from the perspective of the year 2026. Objective: The treatment of choice for unicentric Castleman disease is surgical removal of the lesion. If its size does not allow for surgery, preoperative pharmacological treatment may be used. There is less experience with radiotherapy in this indication. For multicentric Castleman disease (MCD), it is necessary to rule out possible but rarely detectable etiological causes, infection with human herpesvirus-8 (HHV-8), and association with POEMS syndrome. In HHV-8 positive cases, combinations of rituximab with cytostatics (liposomal doxorubicin, etoposide, or polychemotherapy) are used. In cases of MCD associated with POEMS syndrome, the aim of treatment is to suppress monoclonal gammopathy, which is considered the cause of both MCD and POEMS syndrome. Siltuximab is the treatment of choice for idiopathic multicentric Castleman disease (iMCD). It achieves a therapeutic response in less than 50% of unselected patients. If siltuximab treatment is administered only to patients with markedly elevated inflammatory markers, the number of therapeutic responses is higher. For patients who do not respond adequately to siltuximab, it is necessary to seek second - or third-line treatments. The efficacy of certain drugs in iMCD has been demonstrated not only through case reports but also in clinical studies (rituximab in combination with cytostatics, cyclophosphamide in combination with thalidomide or bortezomib, and sirolimus monotherapy). The efficacy of several other drugs has been shown through case reports or small patient series (anakinra, ruxolitinib, lenalidomide). Given the low incidence of the disease (3–5 per 1 million inhabitants), individual documented cases also provide valid guidance for treatment decisions. This text provides an overview of all experience with the treatment of this disease. Conclusion: The first-line treatment for iMCD is siltuximab. However, the disease has multiple etiopathogeneses, which is why siltuximab achieved disease symptom resolution in only half of the cases in an unselected population. For second - or third-line treatment, it is necessary to use one of the drugs with proven efficacy in iMCD.
Keywords:
sirolimus – rapamycin – bortezomib – Castleman disease – siltuximab – anakinra – rituximab – ruxolitinib – daratumab
Autori: Z. Adam 1; Z. Řehák 2; I. Boichuk 1; T. Horváth 3; Z. Adamová 4,5; M. Štork 1; L. Pour 1
Pôsobisko autorov: Interní hematologická a onkologická klinika LF MU a FN Brno 1; Oddělení nukleární medicíny, MOU Brno 2; Chirurgická klinika LF MU a FN Brno 3; Chirurgické oddělení, Nemocnice Frýdek-Místek 4; Chirurgické oddělení, Vsetínská nemocnice 5
Vyšlo v časopise: Klin Onkol 2026; 39(2): 86-98
Kategória: Přehled
doi: https://doi.org/10.48095/ccko202686Súhrn
Východiska: Do klinické praxe se neustále dostávají nové a nové léky, a proto se kontinuálně vyvíjejí názory na léčbu Castlemanovy choroby. Text přináší informace o léčbě uvedené choroby z úhlu pohledu roku 2026. Cíl: Léčbou volby pro unicentrickou Castlemanovu chorobu je operační odstranění ložiska. Pokud to jeho velikost nedovoluje, je možné použít předoperační medikamentózní léčbu. Méně zkušeností je s radioterapií v této indikaci. U multicentrické Castlemanovy choroby (multicentric Castleman disease – MCD) je třeba vyloučit možné, ale vzácně detekovatelné etiologické příčiny, infekci humánním herpetickým virem-8 (HHV-8) a asociaci s POEMS syndromem. U HHV-8 pozitivních forem se používají kombinace rituximabu s cytostatiky (lipozomální doxorubicin, etoposid) či s polychemoterapií. V případě asociace MCD s POEMS syndromem je cílem léčby potlačení monoklonální gamapatie, která je považována za příčinu jak MCD, tak i POEMS syndromu. Pro idiopatickou multicentrickou Castlemanovu chorobu (iMCD) je léčbou volby siltuximab. Ten dosahuje u neselektovaných nemocných léčebné odpovědi v < 50 % případů. Pokud je léčba siltuximabem podána pouze pacientům s výrazně zvýšenými markery zánětu, je počet léčebných odpovědí vyšší. Pro pacienty nereagující dostatečně na siltuximab je nutno hledat léčbu 2. či 3. linie. Účinnost některých léků byla u iMCD prokázána nejen formou popisů případů, ale i klinickými studiemi (rituximab v kombinaci s cytostatiky, cyklofosfamid v kombinaci s thalidomidem anebo s bortezomibem a monoterapie sirolimem). U několika dalších léků byla účinnost prokázána formou popisů případů či malých sérií pacientů (anakinra, ruxolitinib, lenalidomid). Vzhledem k nízké incidenci nemoci (3–5 / 1 mil. obyvatel) jsou pro rozhodování o léčbě validní i jednotlivé popsané případy. V textu uvádíme přehled všech zkušeností s léčbou této nemoci. Závěr: Léčbou první linie pro iMCD je siltuximab. Choroba má však více etiopatogenezí, proto siltuximab u neselektované populace dosáhl vymizení symptomů nemoci jen v polovině případů. Pro léčbu 2. či 3. linie je nutno použít některý z léků s prokázanou účinností u iMCD.
Klíčová slova:
sirolimus – rapamycin – rituximab – bortezomib – Castlemanova choroba – siltuximab – anakinra – ruxolitinib – daratumab
Úvod
V připravovaném článku, který vyjde v čísle 3 časopisu Klinická onkologie s názvem „Chronicky zvýšená teplota či horečka s nevelkou lymfadenopatií může být Castlemanova choroba, pokud se neprokáže maligní, autoimunitní anebo infekční příčina lymfadenopatie“, budou popsány klinické příznaky, laboratorní nálezy, diagnostická kritéria a průběhy jednotlivých forem Castlemanovy choroby, jak unicentrické (unicentric Castleman disease – UCD), tak multicentrické formy (multicentric Castleman disease – MCD). Léčbě této choroby věnujeme samostatný text.
Úvodem připomeňme terminologii. U většiny případů MCD zůstává etiopatogeneze choroby neobjasněna a pro tyto případy je používán termín idiopatická multicentrická Castlemanova choroba – iMCD. Zatím se podařilo odhalit pouze dvě možné příčiny choroby, které jsou ale detekovatelné pouze u velmi malé části pacientů s MCD. Je to infekce humánním herpetickým virem (HHV-8), který se replikuje v lymfatické tkáni, indukuje zvýšenou tvorbu interleukinu-8 a symptomy nemoci. Tyto formy jsou označovány jako HHV-8+MCD. Druhou, stejně vzácnou příčinou je monoklonální gamapatie s POEMS syndromem se znaky MCD. V těchto případech je etiopatogeneze nalézána v produktech klonálních plazmocytů, které indukují rozvoj POEMS syndromu se znaky MCD. Tyto výjimečné případy jsou označovány jako POEMS-MCD.
V předchozím textu jsme poukázali na značné odlišnosti v klinickém průběhu jednotlivých forem iMCD. Nejagresivnější formy tvoří skupinu iMCD-TAFRO. TAFRO je akronym vytvořený z charakteristických symptomů: trombocytopenie, anasarka, (fever) horečka / retikulinová fibróza, renální dysfunkce, organomegalie.
Nejméně agresivní je nedávno definovaná forma iMCD – idiopatická plazmocytická lymfadenopatie (idiopathic multicentric Castleman disease-idiopa-thic plasmocytic lymphadenopathy – iMCD-IPL).
A mezi těmito dvěma zcela odlišnými formami iMCD se prostírá idiopatická Castlemanova choroba – blíže nespecifikovaná (iMCD-not otherwise specified – iMCD-NOS), do níž spadá většina nemocných.
Obrovský rozdíl mezi nejagresivnějšími a nejméně agresivními průběhy MCD, na něž jsme upozornili v předchozím textu, mají jen jedno vysvětlení – nejednotnou etiopatogenezi vzniku iMCD. A proto není univerzálního léku, který by pomohl všem pacientům s MCD, a pro každého pacienta je nutno najít optimální léčebný postup individuálně. Máme ale informace o lécích, které u pacientů s MCD pomohly po neúspěchu předchozí léčebné linie.
Účinnost některých léků je doložena klinickými studiemi, jiných pouze četnějšími popisy případů či malých sérií pacientů. Incidence iMCD je velmi malá, 3–5 případů / 1 mil obyvatel, což znesnadňuje organizaci klinických studií. A proto jsou popisy případů potvrzujících účinnost jednotlivých léčiv relevantním argumentem pro jejich použití v rámci 2. či následující linie léčby. Snaha o předložení podrobných informací nezbytných pro rozhodování o léčbě konkrétního pacienta je důvodem vysokého počtu odkazů na literaturu v tomto textu.
Mezinárodní léčebné doporučení pro iMCD uvádí siltuximab jako lék 1. linie, a to z těchto důvodů:
- je to jediný lék s registrací a úhradou pro léčbu Castlemanovy choroby;
- je to velmi dobře tolerovaný lék, a to jak podle publikovaných zpráv, tak dle našich zkušeností.
Pokud má pacient to štěstí, že siltuximab jeho chorobu potlačí, je to pro něj velké plus oproti ostatním, u nichž je třeba hledat alternativu léčby. Použití dalších nových léků účinných u iMCD je možné jen se schválením plátce zdravotní péče. V následujícím textu předkládáme přehled zkušeností jak se siltuximabem, tak i s dalšími léky. V textu uvedená fakta by mohla pomoci v domluvě s plátcem zdravotní péče v případech pacientů, jejichž choroba není potlačena siltuximabem.
Léčba unicentrické Castlemanovy choroby
Léčba unicentrické Castlemanovy choroby (UCD) je doménou operačních oborů. Postupně se zvětšující ložisko UCD tlačí na své okolí a to způsobuje bolesti či jiné příznaky, pro něž jsou indikována zobrazovací vyšetření. Nález patologické expanze, obvykle v hrudníku, v břišní dutině anebo v pánvi, pak staví lékaře před otázku, zda je možné tuto expanzi kompletně operačně odstranit. Pokud je ložisko odstranitelné, tak chirurg přistoupí k radikální operaci.
Pokud expanzivní patologické ložisko není odstranitelné, tak je nutné zvolit jednu z cest ke stanovení histologické povahy ložiska. Obvykle se volí mezi operační biopsií a CT navigovanou punkční biopsií. Ložiska UCD jsou tvořena nejčastěji hyalinně vaskulárním histomorfologickým typem, výjimečně typem plazmocelulárním či smíšeným. U neoperabilních případů UCD s lokální expanzí a s útlakem okolních struktur je možné podat medikamentózní léčbu, vedoucí ke zmenšení ložiska na operabilní velikost. Tento postup ilustruje obr. 1. Některé publikace přínos této předoperační léčby popírají, ale námi popsaný případ s PET/CT s aplikací fluorodeoxyglukózy (FDG-PET/CT) dokumentovaným zmenšením ložiska na operabilní rozměry zase potvrzuje možnost zmenšení ložiska vhodnou léčbou. Pacientka měla již před zjištěním UCD stanovenu diagnózu roztroušené sklerózy a potíže způsobené touto neurologickou chorobou regredovaly při léčbě rituximabem a bendamustinem.
Obr. 1. Případ unicentrické Castlemanovy nemoci [2]. Zmenšení velikosti ložiska po léčbě rituximabem, bendamustinem a dexametazonem umožnilo kurativní operaci. ![Případ unicentrické Castlemanovy nemoci [2]. Zmenšení velikosti ložiska po léčbě rituximabem, bendamustinem a dexametazonem umožnilo kurativní operaci.](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/f8428de5351b2b76185c87ad047c231a.png)
Alternativou medikamentózní předoperační léčby je radioterapie nebo embolizační léčba.
Ve vzácných případech, kdy neoperabilní ložisko neobtěžuje nositele útlakem okolní tkáně, ale zato způsobuje systémovou zánětlivou reakci, je lékem volby siltuximab, jehož podávání by tuto zánětlivou reakci mělo odstranit [1–3]. U 3–5 % pacientů s UCD se objeví komplikace typu paraneoplastického pemfigu a někdy i bronchiolitis obliterans. U případů s paraneoplastickým pemfigem je doporučována před operačním řešením intenzivní léčba, která se může skládat z rituximabu v kombinaci se steroidy a dalšími léky. Tato cílená léčba může být doplněna podáváním nitrožilních imunoglobulinů v imunomodulačních dávkách.
U asymptomatického ložiska UCD je na zvážení jen sledování. Je zde však riziko pozdější transformace do sarkomu z folikulárních dendritických buněk, pro něž je lépe operaci neodkládat.
Léčba multicentrické Castlemanovy choroby s průkazem infekce virem HHV-8
Multicentrická Castlemanova choroba s prokázanou infekcí HHV-8, zvaným též virus Kaposiho sarkomu, je v našich podmínkách výjimečná a s její léčbou nemáme vlastní zkušenosti. Označujeme ji zkratkou HHV-8+MCD. V databázi domácí literatury Medvik.cz není popsána.
Zahraniční literatura popisuje u HHV-8+MCD, zvláště pak pro podskupinu s pozitivitou HHV-8 a pozitivitou HIV, vysoké riziko transformace do agresivního lymfomu. Přítomnost infekce HHV-8 při absenci infekce HIV je nejčastěji u osob na kombinované imunosupresivní léčbě po orgánové transplantaci. Vyšší výskyt HHV-8 infekcí se popisuje v subsaharských oblastech. Přepokládá se přenos sexuálním kontaktem a vyšší výskyt se popisuje u homosexuálních mužů.
Histologické vyšetření lymfadenopatie u HHV-8+MCD má často plazmablastický charakter, což může imponovat jako lymfom. Průběh nemoci u tohoto spektra pacientů může být velmi agresivní a může imitovat hemofagocytující lymfohistiocytózu.
Mezinárodní doporučení pro tento typ nemoci nebylo publikováno, a tak nutno vycházet z popisů menších sérií pacientů. Léčba má vždy za úkol destrukci lymfocytů, v nichž se replikuje virus HHV-8. K tomu se používá rituximab v kombinaci s chemoterapií obvyklou u lymfomů. Pouze u oligosymptomatických případů HHV-8+MCD byl použit rituximab v monoterapii. U pacientů se závažnějšími příznaky byl použit rituximab v kombinaci s cytostatiky. Jednotlivé klinické studie popisují použití kombinace rituximabu s etoposidem, který se také používá pro léčbu hemofagocytující lymfohistiocytózy. Dále je používána kombinace rituximabu s cyklofosfamidem, doxorubicinem, vinkristinem a prednisonem (R-CHOP), s následnou udržovací léčbou rituximabem. Pokud je přítomna navíc i infekce HIV, tak se musí léčit i tato infekce antivirotiky proti infekci HIV [4–7]. Proti infekci HHV-8 zatím nemáme účinné antivirotikum.
V menší studii 17 pacientů s MCD se současným průkazem viru HHV-8 i viru HIV použili pro léčbu kombinaci rituximabu a lipozomálního doxorubicinu 20 mg/m2 společně s antivirovou terapií. Léčebnou odpověď popisují u 88 % nemocných [8].
Prognóza těchto pacientů je podstatně méně příznivá než u HHV-8 negativních nemocných.
Ze 73 pacientů HIV+HHV-8+ a 26 pacientů HIV−HV-8+ progredovalo 12 pacientů HIV − a 24 HIV+ pacientů při mediánu sledování 51 měsíců. Pětileté přežití bez progrese (progression free survival – PFS) z tohoto souboru dosáhlo pouze 54 % léčených [9].
Léčba POEMS-MCD
Informaci o léčbě této formy jsou dostupné jen z popisu případů a vyplývá z nich, že léčebné úspěchy jsou často jen marginální. Léčba se v těchto případech orientuje na potlačení monoklonální gamapatie všemi dostupnými prostředky, včetně vysokodávkované chemoterapie s podporou autologních kmenových buněk. V databázi PubMed jsou i popisy POEMS-MCD s negativní imunofixací s normálním cytologickým nálezem v kostní dřeni. Flowcytometrická analýza kostní dřeně v těchto popisech případů chybí. Případ POEMS-MCD, kdy nebyl přítomný monoklonální imunoglobulin, léčili podobně jako pacienty s prokázaným monoklonálním imunoglobulinem [10–13].
V případech POEMS-MCD se doporučuje analýza B-buněčné klonality a imunofenotypizace v odebraném vzorku, imunofixační elektroforéza k detekci monoklonálního imunoglobulinu a flow-cytometrické vyšetření klonality plazmocytů v kostní dřeni. Tato pečlivá analýza prokázala klonální populaci v 83 % případů POEMS-MCD [14].
Léčba HHV-8 a HIV negativních forem idiopatické multicentrické Castlemanovy choroby
Nadprodukce interleukinu-6 je sice častou, ale ne univerzální příčinou iMCD [15]. Odlišnou etiopatogenezí jednotlivých případů iMCD se vysvětlují rozdíly v účinnosti léků u jednotlivých nemocných. Cílená blokáda interleukinu-6 dosahuje požadované léčebné odpovědi sotva v 50 % případů [16]. Pro léčbu iMCD je sice mezinárodními doporučeními definován lék první volby, kterým je siltuximab, ale citované mezinárodní doporučení popisuje také další účinné léčebné postupy pro nemocné refrakterní na siltuximab [17]. Analogicky s jinými léky, které byly dříve podávány v monoterapii a nyní je podáváme v kombinaci, se domníváme, že podobný vývoj bude mít i léčba siltuximabem. V následujících letech by mohl výzkum Castlemanovy choroby urychlit mezinárodní registr ACCELERATE [18]. Jednu z nejnovějších analýz léčby z tohoto registru uvedeme i v tomto textu.
Siltuximab, inhibitor interleukinu-6
Pro léčbu první volby je v roce 2026 doporučována blokáda interleukinu-6. V této indikaci je registrován siltuximab. Alternativou je tocilizumab [17]. Podmínkou pro jeho podání je diagnóza idiopatické formy Castlemanovy choroby, tedy nepřítomnost infekce HHV-8 a infekce HIV. Siltuximab je chimérická IgG1 protilátka, která tvoří stabilní komplexy s bioaktivními formami interleukinu-6 a brání jeho vazbě na rozpustné i membránové vazebné receptory. Siltuximab se podává v doporučené dávce 11 mg/kg formou intravenózní infuze 1× za 3 týdny až do případného selhání léčby (anebo nepřijatelné toxicity). Po dosažení léčebného efektu je možné intervaly prodlužovat na 6 týdnů, jak bylo prokázáno klinickou studií. Lék dlouze setrvává v oběhu, terminální poločas byl 20,6 dne. U pacientů se sníženou funkcí ledvin (clearance kreatininu ≥ 15 ml/min) není třeba upravovat dávku. Lék nebyl testován u osob se závažnou renální insuficiencí a nebyl testován u závažné dysfunkce jater. Americký úřad FDA tento lék začlenil do skupiny C, což jsou léky, které (pokud možno) by se neměly podávat těhotným anebo kojícím.
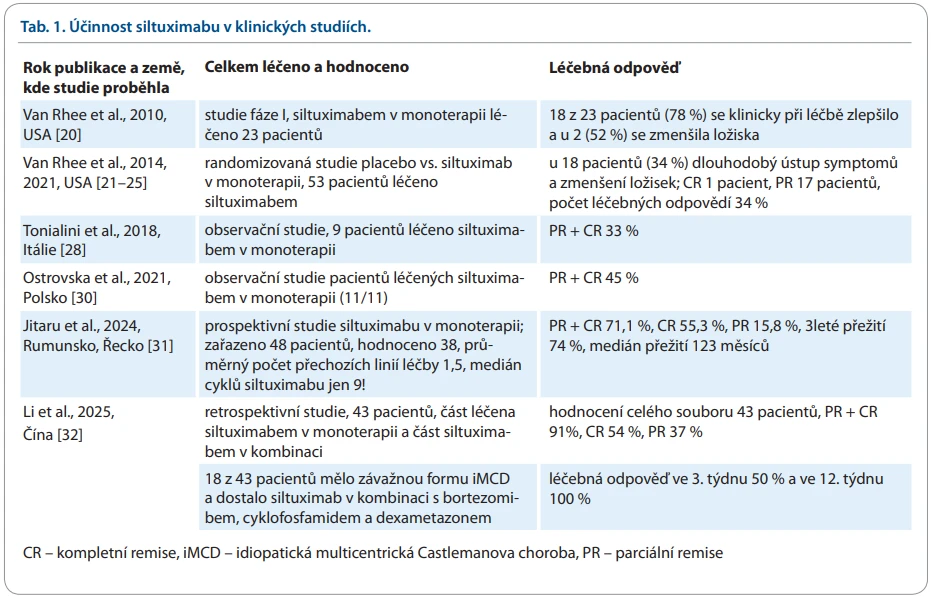
Ošetřující lékař si musí být vědom, že přípravek siltuximab může maskovat známky akutního zánětu, včetně potlačení horečky a reaktantů akutní fáze. Může způsobit zvýšení hodnoty triglyceridů a cholesterolu v séru. Proto se požaduje, aby pacienti vždy před podáním siltuximabu měli počet neutrofilů vyšší než 1,0×109/l a počet trombocytů vyšší než 50×109/1. Při závažné infekci by se léčba siltuximabem měla vždy dočasně přerušit [19]. Výsledky klinických studií, v nichž byl použit siltuximab, jsou uvedeny v tab. 1.
Výsledky klinické studie fáze I byly zveřejněny v roce 2010 [20] a na ni navázala registrační studie, u níž proběhlo několik hodnocení. Registrační studie popsala 34 % léčebných odpovědí. Poslední analýza této studie z roku 2022 potvrdila, že pacienti, kteří se dostali do remise, v ní pak při pravidelném podávání siltuximabu dlouhodobě setrvávají. Dlouhodobá léčba je smysluplná u pacientů, kteří na něj reagují [21–25].
Efektivitu a toleranci dlouhodobé léčby dokumentuje popis pacientky, která siltuximab dostávala po dobu 15 let, stále jej dobře tolerovala a setrvávala v remisi [26].
Zda bude možné léčbu bezpečně po letech přerušit, zatím nevíme. V jednom případě přerušení léčby po 10 letech byl popsán rychlý relaps choroby [27].
V Evropě proběhlo zprvu jen několik drobných studií. Autoři z Itálie zveřejnili studii o devíti pacientech s podobným počtem odpovědí, jako měla registrační studie [28]. Další práce z Itálie již popisuje léčbu deseti pacientů [29]. V Polsku vznikla taktéž malá klinické studie [30]. Největší klinická studie v Evropě proběhla na území Řecka a Rumunska. Do této rumunsko-řecké studie byli zařazeni již léčení pacienti, průměrný počet přechozích léčebných linií byl 1,5. Překvapivý je téměř dvojnásobný počet léčebných odpovědí oproti registrační studii. Medián podaných cyklů siltuximabu přitom činil jen devět aplikací [31].
V roce 2025 byla také zveřejněna první analýza léčby čínských pacientů siltuximabem. Autoři nelpěli dogmaticky na monoterapii siltuximabem a u pacientů s agresivnějším průběhem podali siltuximab v kombinaci s bortezomibem a cyklofosfamidem. Je možné, že podobně jako při léčbě jiných chorob kombinace léků dosáhne více léčebných odpovědí než monoterapie. Klinická studie, která proběhla v Číně, měla jako první léčebný protokol obsahující kombinaci siltuximabu a dalšího léku [32]. Je možné, že touto cestou se podaří rychleji potlačit chorobu a pak jen postačí pokračovat siltuximabem jako udržovací léčbou.
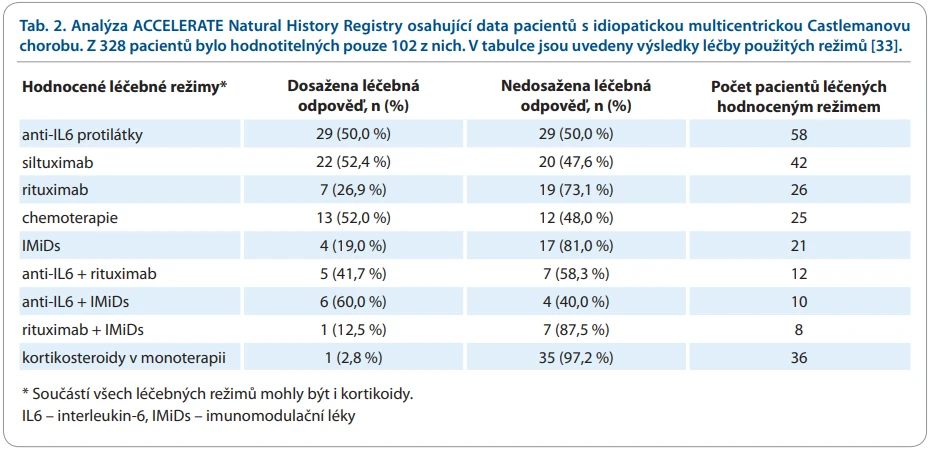
V roce 2025 byla také zveřejněna první analýza z registru ACCELERATE. Pro analýzu vybrali 328 pacientů s iMCD, z nich bylo pouze 102 hodnotitelných. Neobvyklé je, že u více než poloviny (59,8 %) pacientů byla naplněna kritéria iMCD-TAFRO. Autoři citované analýzy potvrdili léčebnou odpověď na léky blokující interleukin-6 u 50 % léčených. Dále srovnali výsledky léčby siltuximabem s léčbou rituximabem. Došli k závěru, že léčba siltuximabem dosahuje lepších výsledků. Ale jak je vidět z tab. 2, nebyla vyhodnocena kombinace rituximabu s lékem ze skupiny cytostatik [33].
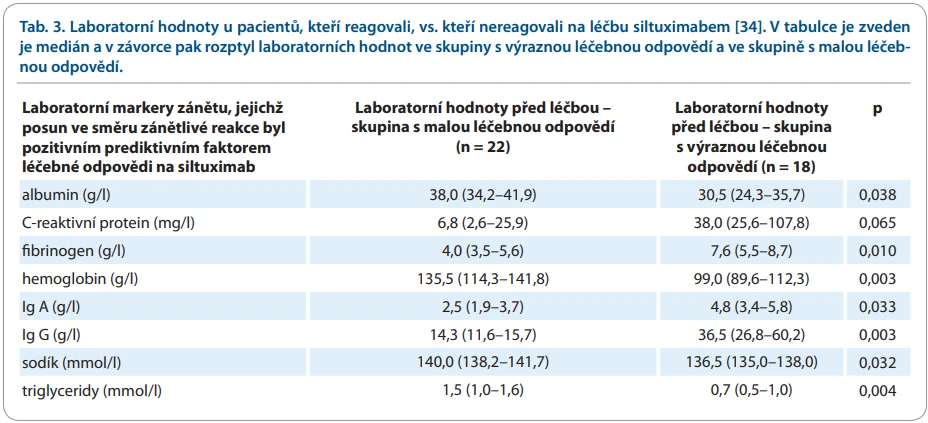
Pozornost byla věnována možnosti predikce léčebné odpovědi na siltuximab. V tab. 3 jsou uvedeny laboratorní hodnoty pacientů, jejichž choroba reagovala nebo nereagovala na léčbu siltuximabem. Pacienti s vysokými hodnotami zánětlivých ukazatelů (zvýšené CRP, zvýšený fibrinogen, zvýšený imunoglobulin IgG a snížená koncentrace hemoglobinu) jsou nejlepšími kandidáty na léčbu siltuximabem [34].
Predikci léčebné odpovědi se věnovali autoři další studie. Analyzovali hodnoty proteinu s názvem C-X-C Motif Chemokine Ligand-13 (CXCL13) a zjistili, že produkce tohoto proteinu je ve většině případů iMCD zvýšená. Časný a signifikantní pokles hladiny CXCL13 jasně odlišil pacienty s léčebnou odpovědí na siltuximab od pacientů bez léčebné odpovědi na něj. Pokles hodnot 8. den po podání siltuximabu o více než 17 % přesvědčivě předpověděl léčebnou odezvu [35].
Siltuximab je velmi dobře tolerovaný lék, takže je báječné, pokud se tímto netoxickým lékem podaří chorobu potlačit. Nežádoucí účinky této léčby jsou výjimečné. Siltuximabem jsme léčili dva pacienty, v jednom případě jsme léčbu přerušili, neboť pacientka si přála mít dítě, což se jí podařilo. U druhého pacienta léčba pokračuje a je podstatně účinnější než předchozí léčba rituximabem anebo anakinrou [36,37].
Siltuximab však není lékem jen pro Castlemanovu chorobu, uplatnil se u refrakterní Stillovy nemoci a také u VEXAS syndromu [38,39].
Rituximab, anti-CD20 monoklonální protilátka
Anti-CD20 protilátka (rituximab) se stala standardním lékem B lymfomů a autoimunitních chorob. Rituximab je základním lékem pro HHV-8 pozitivní MCD, jak zmíněno v předchozím odstavci, ale stejně účinný je u HHV-8 negativní iMCD. Pokud se u iMCD použije rituximab v monoterapii, tak je sice obvykle léčebné odpovědi dosaženo, ale její trvání je kratší než při použití rituximabu v kombinaci s cytostatiky, která jsou účinná u lymfoproliferací [40,41].
O použití další anti-CD20 protilátky pro léčbu iMCD, obinutuzumabu, jsme zatím nenašli žádnou zprávu. Použití obinutuzumabu by připadalo v úvahu při intoleranci rituximabu.
Léčebná kombinace rituximabu s cyklofosfamidem je dobře tolerovaná, stejně jako kombinace s bendamustinem. V dalších případech byl použit rituximab v kombinaci s bortezomibem nebo s etoposidem, případně s lipozomálním doxorubicinem. Zkušenosti s léčbou rituximabem v kombinaci s dalšími léky jsou zachyceny jak formou popisů případů [40–43], tak i několika klinickými studiemi [44,45].
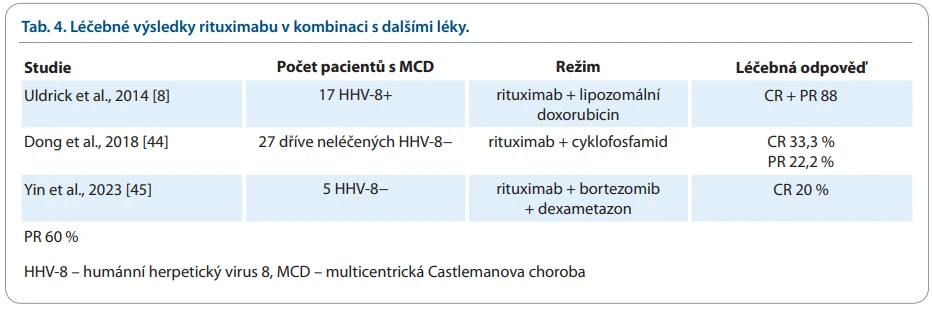
Kombinace rituximabu s cyklofosfamidem byla hodnocena u 27 případů iMCD, léčebné odpovědi bylo dosaženo u 55, 5 % z nich. Kompletní remise (complete remission – CR) bylo dosaženo u 33,3 % (9/27) a parciální remise (partial remission – PR) u 22,2 % (6/27) léčených. Pětileté OS bylo 81 % [44].
Další malá studie testovala kombinaci rituximabu s bortezomibem a dexametazonem u pěti pacientů, z nichž jeden měl iMCD-TAFRO. Po čtyřech cyklech této léčby dosáhlo kompletní remise 20 % pacientů a parciální remise 60 % pacientů [45]. Pro agresivnější případy (iMCD-TAFRO) je doporučována kombinace rituximabu s etoposidem anebo s bortezomibem [46].
Léčba rituximabem je spojována se snížením rizika transformace do lymfomu. To prokázali autoři z Paříže, kteří dlouhodobě sledovali 113 HIV pozitivních pacientů s MCD. Rituximabem léčili 48 nemocných a pouze u jednoho pacienta se vyvinul lymfom. Druhá skupina (65 pacientů) nebyla léčena rituximabem a za stejné období se lymfom vyvinul u 17 z těchto pacientů. Tento rozdíl byl statisticky významný [47].
O účinnosti rituximabu v monoterapii či v kombinaci s dalšími léky není pochyb. V jednom případě byla monoterapie rituximabem dokonce účinná i u pacienta s iMCD-TAFRO [48].
Klinické studie u MCD s rituximabem v kombinaci s dalšími léky shrnuje tab. 4.
Na našem pracovišti jsme léčbu rituximabem v kombinaci s cyklofosfamidem podali celkem čtyřem pacientům s iMCD. U tří jsme dosáhli kompletní remise a u jednoho pacienta s agresivnější formou nemoci jenom parciální remise. Ten je nyní léčen siltuximabem a na této léčbě je konečně asymptomatický [49,50]. Kombinaci rituximabu s bendamustinem jsme podali ke zmenšení UCD a k dosažení operability [2].
Anakinra, inhibitor receptoru interleukinu-1
Z dalších inhibitorů cytokinů má u nemocných s iMCD prokázanou účinnost anakinra, inhibitor receptoru pro interleukin-1. Tento lék si pacienti aplikují denně v podkožní injekci. Je lékem volby pro četné autoinflamatorní choroby, a tedy i pro nemocné se syndromem Schnitzlerové, který patří jak mezi autoinflamatorní choroby, tak mezi monoklonální gamapatie. Anakinra je lék s velmi dobrou tolerancí, jak jsme se přesvědčili také při léčbě Stillovy nemoci dospělých a SAPHO syndromu [51–53].
U více případů refrakterních forem iMCD s neúspěchem jedné či dvou linií léčby nakonec došlo ke zlepšení po zahájení léčby anakinrou [54–60]. Klinická studie s anakinrou nebyla u iMCD zatím provedena, a proto jsme výsledky publikovaných popisů případů shrnuli do tab. 5. Tento přehled opravňuje k použití anakinry u případů iMCD při neúspěchu iniciální léčby siltuximabem. Na našem pracovišti jsme anakinru po několik měsíců podávali jednomu pacientovi s iMCD, ale dosáhli jsme jen PR.
Inhibitory TNF-α
Inhibitorů TNF-α je dnes k dispozici více a všechny jsou hodně podávány revmatology u četných chorob pojiva. U Castlemanovy choroby je však pouze jedna zmínka o možnosti léčby anti-TNF-α preparáty [61]. Účinnost této skupiny léčiv u MCD tedy není klinicky ověřena.
Ruxolitinib, inhibitor Janusových kináz
Ruxolitinib inhibuje Janusovy kinázy (JAK), které jsou zapojeny do signálních drah mnoha cytokinů a růstových faktorů. Janusovy kinázy hrají významnou úlohu v regulaci krvetvorby a imunitních funkcí. U polycytemie a myelofibrózy je popsána nadměrná signalizace zprostředkovaná právě Janusovými kinázami (JAK1 a JAK2). Proto je ruxolitinib lékem používaným pro léčbu pravé polycytemie a myelofibrózy [62].
V literatuře je popsáno více případů iMCD, u nichž byla po selhání léčby 1. linie dosažena léčebná odpověď ruxolitinibem [53–66]. Pro přehlednost jsme informace z těchto popisů případů shrnuli do tab. 6.
Sirolimus
Sirolimus, známý také jako rapamycin a prodávaný pod obchodním jménem Rapamune, má silné imunosupresivní a antiproliferativní vlastnosti díky své schopnosti inhibovat signální dráhu mTOR. Proto se používá jako imunosupresivum po transplantaci orgánů. Mimo transplantační medicínu byla jeho účinnost prokázána u lymfangioleiomyomatózy, kde má standardní indikaci [67]. Léčebný efekt má sirolimus také u vaskulárních anomálií, a to i u dětí [68–72]. U pacientů léčených sirolimem byla nižší incidence neoplazií a spekuluje se o zpomalení stárnutí vlivem tohoto léku [73]. Sirolimus byl použit i pro léčbu retroperitoneální fibrózy [74]. Tyto pozitivní vlastnosti sirolimu využili brněnští hematologové pro léčbu autoimunitní hemolytické anemie v dětském věku [75]. Sirolimus je tedy velmi účinným lékem, z něhož profitují pacienti po transplantaci, ale také pacienti s cévními malformacemi a některými imunitně podmíněnými chorobami, i když tyto indikace jsou mimo oficiální registraci.
Molekulárně-biologické studie u pacientů s iMCD prokázaly, že signální dráha mTOR je silně aktivována [76–79]. Citované poznání iniciovalo testování sirolimu u pacientů, kteří nereagovali na inhibici interleukinu-6. Sirolimus skutečně potlačil agresivní formy iMCD nereagující na léčbu siltuximabem [80–82]. Tyto zprávy pak vedly k vytvoření klinické studie, do níž bylo zařazeno 26 pacientů s iMCD refrakterní k předchozí léčbě. Medián věku souboru byl 40,5 (23–60) roku a medián počtu předchozích léčebných linií byl 2 (1–5) roky. U 18 (69,2 %) pacientů z 26 léčených vymizely symptomy a upravily se patologické laboratorní hodnoty. Medián intervalu nastoupení léčebné odpovědi byl 1,9 (0,5–14,6) měsíce. Medián sledování od zahájení léčby sirolimem byl 11,7 měsíce. Většina pacientů s dosaženou remisí byla pak sirolimem dlouhodobě léčena. Autoři této klinické studie uvádějí, že sirolimus byl velmi dobře tolerován, nežádoucí účinky byly minimální. Považují jej za velmi vhodný lék pro 2. či další linii léčby iMCD [83]. Japonští lékaři v roce 2020 otevřeli nekomerční prospektivní klinickou studii testující účinnost sirolimu u pacientů rezistentních k blokádě interleukinu-6 [84]. Zkušenosti se sirolimem u iMCD shrnuje tab. 7.
Imunomodulační léky (thalidomid, lenalidomid)
Účinnost thalidomidu u iMCD je doložena nejen četnými popisy úspěšně léčených pacientů s iMCD [85–90], ale také klinickou studií [91]. A z účinnosti thalidomidu lze usuzovat na účinnost i dalších léků z této skupiny, lenalidomidu a pomalidomidu. Tyto tři léky mají skupinové pojmenování immunomodulatory (IMiD) drugs a podstatou jejich terapeutického efektu je vazba na cereblon. Uvedené léky se zásadně odlišují nežádoucími účinky. Dříve jsme thalidomid u této diagnózy také používali v kombinaci s cyklofosfamidem a potvrdili jsme léčebnou odpověď [92].
Thalidomid má však velmi četné nežádoucí účinky, takže život při léčbě thalidomidem je dosti obtížný. Mimo jiné ovlivňuje negativně i psychiku nemocných, která je již narušena nemocí, jak je dokumentováno v knize Maligní onemocnění, psychika a stres [93]. Po zkušenostech s thalidomidem jak v této indikaci, tak u pacientů s mnohočetným myelomem jednoznačně upřednostňujeme lenalidomid před thalidomidem. Lenalidomid v mnoha případech iMCD rezistentních na léčbu 1. linie dosáhl léčebné odpovědi a je podstatně lépe tolerován než thalidomid.
S lenalidomidem však nebyla u iMCD provedena žádná klinická studie, jeho doporučení pro konkrétní pacienty lze vyvodit pouze ze zkušeností se starším preparátem z této skupiny thalidomidem a z citovaných popisů případů, u nichž bylo léčebné odpovědi dosaženo lenalidomidem [94–98].
Zhou et al. použili s úspěchem monoterapii lenalidomidem u tří pacientů refrakterních na léčbu 1. linie, v níž nebyl siltuximab [94]. Cai et al. popisují léčbu 1. linie, v níž tocilizumab potencoval léčbu lenalidomidem [95].
Zhang et al. popsali léčbu sedmi případů iMCD-TAFRO, z nichž jeden dostal v rámci léčby refrakterní choroby lenalidomid a dosáhl léčebné odpovědi [96].
Na našem pracovišti jsme popsali pacienta s iMCD a vaskulitidou s komplikacemi po léčbě thalidomidem, který se zlepšil po léčbě lenalidomidem. Po jejím přerušení došlo k recidivě, takže v současnosti u něj se schválením plátce zdravotní péče probíhá udržovací léčba lenalidomidem [97,98].
Lenalidomid je dalším lékem pro pacienty, jejichž choroba neodpovídá na iniciální léčbu siltuximabem. Jeho použití je mimo jiné dokumentováno analýzou registru ACCELERATE v tab. 2.
Daratumumab
Daratumumab je protilátka proti antigenu CD38, který je přítomný na plazmocytech.
Účinnost daratumumabu byla popsána u dvou pacientů s refrakterní formou iMCD k přechozím léčbám [99,100]. Protože iMCD-idiopatická plazmocytóza uzlin (iMCD-LPL) má blízko k nemoci asociované s imunoglobulinem IgG4, není bez zajímavosti první práce, která popsala léčebný účinek daratumumabu u této nemoci [101].
Bortezomib
Bortezomib se stal standardním lékem pro mnohočetný myelom. Má však širší použití a jeho účinnost je popsána formou popisů případů u četných nemocných s Castlemanovou chorobou [102–105].
K dispozici je nyní jedna studie, která hodnotila účinnost kombinace bortezomibu s cyklofosfamidem a dexametazonem u nemocných s iMCD, kteří byli refrakterní na iniciální léčbu. Léčebné odpovědi bylo dosaženo u 15 pacientů (62,5 %) a pouze 5 pacientů (20,8 %) na této léčbě progredovalo. U ostatních (16,7 %) byla nemoc hodnocena jako stabilní. Roční přežití činilo 92 % [106].
Kombinace bortezomibu s cyklofosfamidem a dexametazonem je další alternativou, ale ne pro pacienty s iMCD, u nichž byla již dříve zjištěna neuropatie. Neuropatie je jednou z komplikací vyskytujících se u nemocných s iMCD.
Inhibice Brutonovy kinázy
Inhibitory Brutonovy kinázy jsou nejnovější terapií pro Waldenströmovu makroglobulinemii a jiné nízce agresivní lymfoproliferace. První zprávy o účinnosti tohoto léku u iMCD byly zveřejněny v letech 2024 a 2025.
V malé studii s 10 pacienty dosáhl orelabrutinib 70 % celkových léčebných odpovědí, CR bylo dosaženo jen u 20 % léčených. Časový interval do nastoupení léčebné odpovědi byl překvapivě docela dlouhý, medián byl 9,8 (5,9–20,5) měsíce, což je neobvykle dlouho a trochu to zpochybňuje pozitivní závěrečné hodnocení [107].
Druhá prospektivní studie byla uzavřena po léčbě pěti pacientů, protože nebylo dosaženo léčebného efektu, a autoři tohoto pozorování se domnívají, že inhibitory Brutonovy kinázy nebudou vhodným lékem pro iMCD [108]. Není tedy jasné, zda se v této indikaci inhibitory Brutonovy kinázy uplatní.
Polychemoterapie
Dříve, před dostupností výše uvedené léčby, se pro léčbu iMCD používaly léčebné režimy používané pro léčbu lymfomů. V současnosti jsou cytostatika kombinována s novými léky [17,46].
Anti-CD19 protilátka inebilizumab – nový lék pro léčbu choroby asociované s imunoglobulinem IG4 (IgG4-RD)
V roce 2025 se objevil zcela nový lék pro léčbu IgG4-RD. Je to humanizovaná IgG1 kappa monoklonální protilátka, cílící na antigen CD19. Její podání vede k hlubokému a dlouhodobému poklesu počtu B buněk. Antigen CD19 se objevuje na B buňkách dříve než antigen CD20 a setrvává na nich déle, je přítomný na plazmablastech, a dokonce i na některých plazmatických buňkách. Proto léčba cílená na potlačení CD19 pozitivních buněk se jeví u nemoci IgG4-RD výhodnější než léčba cílená na CD20 pozitivní buňky, zasáhne širší spektrum B buněk. Účinek byl prokázán v randomizované klinické studii srovnávající inebilizumab s placebem. Inebilizumab byl podán v dávce 300 mg v dny 1 a 15 a pak až ve 26. týdnu 52týdenní periody. Daná léčba výrazně snížila počet relapsů. Tento lék má schválené i další indikace, mezi něž patří neuromyelitis optica [109–112]. Vzhledem k blízkosti iMCD-IPL se možná v budoucnu použije tento lék.
Sledování po léčbě
I pokud se podaří dosáhnout CR, měli by být pacienti trvale dispenzarizováni.
Cílem dispenzarizace je sledování léčebné odpovědi a detekce případného relapsu. Je vhodné sledovat jak laboratorní parametry, tak vývoj nemoci pomocí FDF–PET/CT nebo FDG–PET/MR. Aktivní choroba iMCD vykazuje střední míru akumulace, hodnoty SUVmax se pohybují kolem průměru 5–6, maximální standardizovaná hodnota utilizace (standardized utilisation value – SUVmax) může dosáhnout 10. FDG-avidita se neliší dle histologického typu a míra akumulace odpovídá laboratorním odchylkám. FDG-PET/CT, příp. FDG-PET/MR je tedy nejen užitečnou zobrazovací metodou pro nasměrování biopsie na ložiska nejvíce akumulující FDG, ale také pro sledování v průběhu léčby a po jejím ukončení, protože podávání přesné informace o aktivitě nemoci, ale také o možné transformaci do lymfomu, případně o duplicitním onemocnění [113–117]. To jsou argumenty pro začlenění pozitronové emisní tomografie do plánu kontrol v průběhu léčby a po jejím ukončení.
Kontrolní vyšetření jsou přínosná vzhledem k popisovaným rizikům:
- pacienti s UCD mají vyšší riziko pozdějšího vzniku sarkomu z folikulárních dendritických buněk a lymfomů jakéhokoliv typu;
- pacienti s HIV+HHV-8+ MCD mají 15× vyšší riziko vzniku lymfomů než HIV pozitivní populace bez MCD;
- HIV−HHV-8+ MCD mají 15% riziko vzniku lymfomů a Kaposiho sarkomu;
- u HIV−HHV-8 − pacientů s iMCD (což je většina pacientů) je 3× vyšší riziko vzniku maligní nemoci ve srovnání se stejně starou populací [17].
Závěr
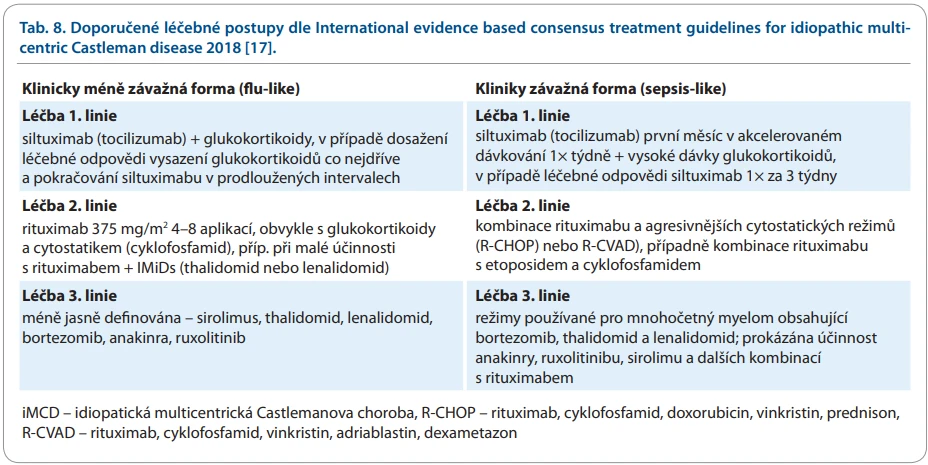
Castlemanova choroba je velmi vzácná nemoc, data z Evropy o jejím výskytu nemáme, v USA se uvádí incidence 3–5 / 1 mil. obyvatel. Její diagnostika je spíše výjimečná a obvykle je dlouhý interval mezi prvními příznaky a stanovením diagnózy. A pokud již je iMCD diagnostikována, pak jistě těmto pacientům bude v rámci 1. linie nabídnuta léčba siltuximabem, jediným lékem s oficiální registrací i úhradou. Siltuximab je léčbou volby dle mezinárodního doporučení (tab. 8). Srovnání siltuximabu a tocilizumabu dopadlo ve prospěch siltuximabu z hlediska intenzity a počtu nežádoucích účinků [118]. Ale ne všichni pacienti na léčbu siltuximabem odpoví a pak stojí ošetřující lékař před otázkou, jaký lék otestovat v další léčbě. Tento text si klade za cíl být přehledem, dle něhož lze vést léčbu dalších linií. V poslední době se v odborné literatuře objevují popisy kombinované léčby siltuximabu s dalšími biologickými léky. Zda se dostanou do běžného užívání nebo zda budou objeveny prediktivní faktory pro jednotlivé léčebné alternativy, se dozvíme v následujících letech.
Dedikace
Publikace byla vytvořena na podporu těchto aktivit: MZ ČR – RVO (FNBr, 65269705) a Institucionální aktivity MOÚ: MZ ČR – RVO (MOÚ, 00209805).
Zdroje
1. van Rhee F, Oksenhendler E, Srkalovic G et al. International evidence-based consensus diagnostic and treatment guidelines for unicentric Castleman disease. Blood Adv 2020; 4 (23): 6039–6050. doi: 10.1182/bloodadvances.2020003334.
2. Horváth T, Frola L, Adam Z et al. Léčba unicentrické Castlemanovy choroby rituximabem, bendamustinem a dexametazonem zmenšila objem expanzivního ložiska v horním mediastinu a umožnila jeho radikální odstranění. Klin Onkol 2025; 38 (2): 132–143. doi: 10.48095/ccko2025132.
3. Penka I, Kala Z, Zetelová A et al. Castleman disease – surgical treatment. Case report. Rozhl Chir 2016; 95 (12): 457–461.
4. Melikyan AL, Egorova EK, Julhakyan HL et al. Human herpesvirus type 8-positive multicentric Castleman disease. Clin Lymphoma Myeloma Leuk 2016; 16 (Suppl): S159–S165. doi: 10.1016/j.clml.2016.03.009.
5. Kantarci FE, Eren R, Gündoğan C et al. A HHV-8 positive, HIV negative multicentric Castleman disease treated with R-CEOP chemotherapy and valganciclovir combination. J Infect Chemother 2016; 22 (7): 483–485. doi: 10.1016/j.jiac.2016.01.002.
6. Murphy C, Hawkes E, Chionh F et al. Durable remission of both multicentric Castleman‘s disease and Kaposi‘s sarcoma with valganciclovir, rituximab and liposomal doxorubicin in an HHV-8-positive, HIV-negative patient. J Clin Pharm Ther 2017; 42 (1): 111–114. doi: 10.1111/ jcpt.12472.
7. Osa M, Maeda T, Misawa K et al. Clinical response to liposomal doxorubicin and rituximab in HHV-8-associated multicentric Castleman‘s disease in an HIV-positive patient. J Infect Chemother 2016; 22 (12): 804–807. doi: 10.1016/j.jiac.2016.06.004.
8. Uldrick TS, Polizzotto MN, Aleman K et al. Rituximab plus liposomal doxorubicin in HIV-infected patients with KSHV-associated multicentric Castleman disease. Blood 2014; 124 (24): 3544–3552. doi: 10.1182/blood-2014-07-586800.
9. Rasmussen C, Gérard L, Fadlallah J et al. Higher rate of progression in HIV - than in HIV+ patients after rituximab for HHV8+ multicentric Castleman disease. Blood Adv 2023; 7 (18): 5663–5669. doi: 10.1182/bloodadvances.2023010316.
10. Min C, Liu A, Xu Y et al. A case report of Castleman disease variant of POEMS syndrome presenting with prominent polyserositis and renal impairment. Front Med (Lausanne) 2025; 12 : 1537944. doi: 10.3389/fmed.2025.1537944.
11. Sevindik OG, Mutlu YG, Aydin BB et al. First-line usage of daratumumab, lenalidomide, dexamethasone (DRd) combination in a case of Castleman disease variant of polyneuropathy, organomegaly, endocrinopathy, monoclonal gammopathy, and skin changes syndrome (CD-POEMS). Hemasphere 2022; 6 (7): e728. doi: 10.1097/HS9.0000000000000728.
12. Lee YM, Choi YS, Kim JM. POEMS syndrome: presented as idiopathic multicentric Castleman disease of plasma cell variant for eight years and dramatic treatment with siltuximab followed by autologous peripheral blood stem cell transplantation. Diagnostics (Basel) 2022; 12 (4): 998. doi: 10.3390/diagnostics12040998.
13. Haider SA, Iram S, Rashid AA et al. POEMS (polyneuropathy, organomegaly, endocrinopathy, monoclonal plasma cell disorder, and skin changes) syndrome as a sequela of Castleman disease: a case report. Cureus 2023; 15 (11): e49330. doi: 10.7759/cureus.49330.
14. Rodriguez-Merino L, Montes-Moreno S. Castleman disease-type histopathological patterns of lymph nodes in patients with plasma cell neoplasia and POEMS syndrome. Ann Diagn Pathol 2025; 74 : 152414. doi: 10.1016/j.anndiagpath.2024.152414.
15. Milota T, Střížová Z, Sobotková M et al. The role of interleukin 6 in the pathogenesis and therapy of Castleman disease – an immunologist’s perspective. Cas Lek Cesk 2023; 162 (2–3): 106–111.
16. Ferrero S, Ragaini S. Dichotomic response to interleukin-6 blockade in idiopathic multicentric Castleman disease: two case reports. J Med Case Rep 2021; 15 (1): 105. doi: 10.1186/s13256-021-02726-4.
17. van Rhee F, Voorhees P, Dispenzieri A et al. International, evidence-based consensus treatment guidelines for idiopathic multicentric Castleman disease. Blood 2018; 132 (20): 2115–2124. doi: 10.1182/blood-2018-07-862334.
18. Lukáč M, Khor J, Coren F et al. Register ACCELERATE: využitie inovatívnej metódy pri výskume Castlemanovej choroby. Klin Farmakol Farm 2021; 35 (3): 87–95.
19. Nikanjam M, Yang J, Capparelli EV. Population pharmacokinetics of siltuximab: impact of disease state. Cancer Chemother Pharmacol 2019; 84 (5): 993–1001. doi: 10.1007/s00280-019-03939-7.
20. van Rhee F, Fayad L, Voorhees P et al. Siltuximab, a novel anti-interleukin-6 monoclonal antibody, for Castleman‘s disease. J Clin Oncol 2010; 28 (23): 3701–3708. doi: 10.1200/JCO.2009.27.2377.
21. Van Rhee F, Wong RS, Munshi N et al. Siltuximab for multicentric Castleman‘s disease. A randomized double blind placebo controlled trial. Lancet Oncol 2014; 15 (9): 966–974. doi: 10.1016/S1470-2045 (14) 70319-5.
22. van Rhee F, Casper C, Voorhees PM et al. A phase 2, open-label, multicenter study of the long-term safety of siltuximab (an anti-interleukin-6 monoclonal antibody) in patients with multicentric Castleman disease. Oncotarget 2015; 6 (30): 30408–30419. doi: 10.18632/oncotarget.4655.
23. van Rhee F, Rossi JF, Simpson D et al. Newly diagnosed and previously treated multicentric Castleman disease respond equally to siltuximab. Br J Haematol 2021; 192 (1): e28–e31. doi: 10.1111/bjh.17177.
24. van Rhee F, Casper C, Voorhees PM et al. Long-term safety of siltuximab in patients with idiopathic multicentric Castleman disease: a prespecified, open-label, extension analysis of two trials. Lancet Haematol 2020; 7 (3): e209–e217. doi: 10.1016/S2352-3026 (19) 30257-1.
25. van Rhee F, Rosenthal A, Kanhai K et al. Siltuximab is associated with improved progression-free survival in idiopathic multicentric Castleman disease. Blood Adv 2022; 6 (16): 4773–4781. doi: 10.1182/bloodadvances.2022007112.
26. Lang E, Sande B, Brodkin S et al. Idiopathic multicentric Castleman disease treated with siltuximab for 15 years: a case report. Ther Adv Hematol 2022; 13 : 20406207221082552. doi: 10.1177/20406207221082552.
26. Gao YH, Li J, Zhang L et al. Rapid relapse of idiopathic multicentric Castleman disease after siltuximab discontinuation in a case with complete remission for more than 10 years. Turk J Haematol 2024; 41 (4): 283–285. doi: 10.4274/tjh.galenos.2024.2024.0339.
28. Tonialini L, Bonfichi M, Ferrero S et al. Siltuximab in relapsed/refractory multicentric Castleman disease: experience of the Italian NPP program. Hematol Oncol 2018; 36 (4): 689–692. doi: 10.1002/hon.2532.
29. Rossini B, Cecchi N, Clemente F et al. Real-practice management and treatment of idiopathic multicentric Castleman disease with siltuximab: a collection of clinical experiences. Drugs Context 2024; 13 : 2023-9-4. doi: 10.7573/dic.2023-9-4.
30. Ostrowska B, Szymczyk A, Olszewska-Szopa M et al. Efficacy of siltuximab in the treatment of idiopathic multicentric Castleman disease, the first Polish, real-world experience with long-term observation. Leuk Lymphoma 2021; 62 (12): 3031–3034. doi: 10.1080/10428194.2021.1941926.
31. Jitaru C, Symeonidis A, Badelita S et al. Siltuximab in idiopathic multicentric Castleman disease: real-world experience. J Hematol 2024; 13 (5): 207–215. doi: 10.14740/jh1343.
32. Li SY, Gao YH, Dang Y et al. Real-world data of siltuximab for Chinese patients with iMCD: combination with BCD regimen as a potential approach for severe cases. Ann Hematol 2025; 104 (3): 1713–1720. doi: 10.1007/s00277-025-06329-7.
33. Pierson SK, Lim MS, Srkalovic G et al. Treatment consistent with idiopathic multicentric Castleman disease guidelines is associated with improved outcomes. Blood Adv 2023; 7 (21): 6652–6664. doi: 10.1182/bloodadvances.2023010745.
34. Morra DE, Pierson SK, Shilling D et al. Predictors of response to anti-IL6 monoclonal antibody therapy (siltuximab) in idiopathic multicentric Castleman disease: secondary analyses of phase II clinical trial data. Br J Haematol 2019; 184 (2): 232–241. doi: 10.1111/bjh.15588.
35. Pierson SK, Katz L, Williams R et al. CXCL13 is a predictive biomarker in idiopathic multicentric Castleman disease. Nat Commun 2022; 13 (1): 7236. doi: 10.1038/s41467-022-34873-7.
36. Adam Z, Zeman D, Chodacki A et al. Therapy of Castleman’s disease with siltuximab – case report and review of literature. Klin Onkol 2023; 36 (4): 320–329.
37. Adam Z, Pour L, Zeman D et al. Castlemanova choroba, plazmocelulární varianta (příčina dlouhodobě zvýšených zánětlivých markerů u mladé ženy a léčebné možnosti při snaze o zachování fertility). Med Umění 2022; 5 (73): 33–39.
38. Moreau J, Leurs A, Ledoult E et al. Siltuximab as a salvage therapy in multi-refractory adult-onset Still‘s disease: a case series. Rev Med Interne 2025; 46 (7): 415–420. doi: 10.1016/j.revmed.2025.05.002.
39. Cáceres-Nazario B, Rivenbark J, Saha MK et al. Novel use of siltuximab in a patient with VEXAS Syndrome. Ann Hematol 2025; 104 (2): 1259–1267. doi: 10.1007/s00277-024-06037-8.
40. Ocio EM, Sanchez-Guijo FM, Diez-Campelo M et al. Efficacy of rituximab in an aggressive form of multicentric Castleman disease associated with immune phenomena. Am J Hematol 2005; 78 (4): 302–305. doi: 10.1002/ajh.20283.
41. Jain P, Verstovsek S, Loghavi S et al. Durable remission with rituximab in a patient with an unusual variant of Castleman‘s disease with myelofibrosis-TAFRO syndrome. Am J Hematol 2015; 90 (11): 1091–1092. doi: 10.1002/ajh.24015.
42. Ramasamy K, Gandhi S, Tenant-Flowers M et al. Rituximab and thalidomide combination therapy for Castleman disease. Br J Haematol 2012; 158 (3): 421–423. doi: 10.1111/j.1365-2141.2012.09157.x.
43. Zhu L, Liu Y, Yu F et al. Successful treatment of idiopathic multicentric Castleman disease with rash as the initial symptom using a rituximab-based regimen. J Hematol 2024; 13 (5): 245–249. doi: 10.14740/jh1313.
44. Dong Y, Zhang L, Nong L et al. Effectiveness of rituximab-containing treatment regimens in idiopathic multicentric Castleman disease. Ann Hematol 2018; 97 (9): 1641–1647. doi: 10.1007/s00277-018-3347-0.
45. Yin X, Liu Y, Zhong C et al. Rituximab-bortezomib-dexamethasone induce high response rates in iMCD in clinical practice. Br J Haematol 2023; 203 (5): 803–806. doi: 10.1111/bjh.19000.
46. Rehman MEU, Chattaraj A, Neupane K et al. Efficacy and safety of regimens used for the treatment of multicentric Castleman disease: a systematic review. Eur J Haematol 2022; 109 (4): 309–320. doi: 10.1111/ejh.13823.
47. Gérard L, Michot JM, Burcheri S et al. Rituximab decreases the risk of lymphoma in patients with HIV-associated multicentric Castleman disease. Blood 2012; 119 (10): 2228–2233. doi: 10.1182/blood-2011-08-376012.
48. Servati S, Mohammadi I, Rajai Firouzabadi S. First-line treatment of TAFRO syndrome with rituximab: a case report and literature review. Ann Hematol 2025; 104 (5): 3035–3046. doi: 10.1007/s00277-025-06327-9.
49. Adam Z, Szturz P, Krejčí M et al. Treatment of 14 cases of Castleman’s disease: the experience of one centre and an overview of literature. Vnitr Lek 2016; 62 (4): 287–298.
50. Adam Z, Szturz P, Koukalová R et al. PET-CT documented remission of multicentric Castleman disease after treatment with rituximab: case report and review. Vnitr Lek 2015; 61 (3): 251–259.
51. Szturz P, Sedivá A, Zurek M et al. Anakinra treatment in Schnitzler syndrome – results of the first retrospective multicenter study in six patients from the Czech Republic. Klin Onkol 2014; 27 (2): 111–126. doi: 10.14735/amko2014111.
52. Adam Z, Král Z, Řehák Z et al. Léčba Stillovy nemoci vzniklé v dospělosti anakinrou. Farmakoter Rev 2024; 9 (3): 227–232.
53. Adam Z, Šedivá A, Zeman D et al. Successful treatment of SAPHO syndrome (chronic nonbacterial osteomyelitis and acne) with anakinra and denosumab. Case report and review of therapy. Vnitr Lek 2023; 69 (5): E4–E14. doi: 10.36290/vnl.2023.065.
54. Galeotti C, Tran TA, Franchi-Abella S et al. IL-1RA agonist (anakinra) in the treatment of multifocal Castleman disease: case report. J Pediatr Hematol Oncol 2008; 30 (12): 920–924. doi: 10.1097/MPH.0b013e31818ab31f.
55. El-Osta H, Janku F, Kurzrock R. Successful treatment of Castleman‘s disease with interleukin-1 receptor antagonist (Anakinra). Mol Cancer Ther 2010; 9 (6): 1485–1488. doi: 10.1158/1535-7163.MCT-10-0156.
56. Jouvray M, Terriou L, Meignin V et al. Pseudo-adult Still‘s disease, anasarca, thrombotic thrombocytopenic purpura and dysautonomia: an atypical presentation of multicentric Castleman‘s disease. Discussion of TAFRO syndrome. Rev Med Interne 2016; 37 (1): 53–57. doi: 10.1016/j.revmed.2015.04.006.
57. Soudet S, Fajgenbaum D, Delattre C et al. Schnitzler syndrome co-occurring with idiopathic multicentric Castleman disease that responds to anti-IL-1 therapy: a case report and clue to pathophysiology. Curr Res Transl Med 2018; 66 (3): 83–86. doi: 10.1016/j.retram.2018.06.001.
58. Borocco C, Ballot-Schmit C, Ackermann O et al. The French paediatric cohort of Castleman disease: a retrospective report of 23 patients. Orphanet J Rare Dis 2020; 15 (1): 95. doi: 10.1186/s13023-020-1345-5.
59. Lanzillotta M, Sant’Angelo M, Kaneko N et al. Treating life-threatening TAFRO syndrome with interleukin-1 inhibition. Eur J Intern Med 2021; 87 : 121–123. doi: 10.1016/j.ejim.2021.02.006.
60. Palmeri S, Ferro J, Natoli V et al. Efficacy of high-dose intravenous anakinra in pediatric TAFRO syndrome: report of two cases and literature review. Pediatr Blood Cancer 2025; 72 (8): e31759. doi: 10.1002/pbc.31759.
61. Mumau MD, Gonzalez MV, Ma C et al. Identifying and targeting TNF signaling in idiopathic multicentric Castleman‘s disease. N Engl J Med 2025; 392 (6): 616–618. doi: 10.1056/NEJMc2412494.
62. Bogoczová E, Čičátková P, Palová M et al. Zkušenosti s léčbou ruxolitinibem u pacientů s myelofibrózou a pravou polycytemií na českých hematologických pracovištích. Trans Hematol Dnes 2017; 23 (1): 30–40.
63. Lust H, Gong S, Remiker A et al. Idiopathic multicentric Castleman disease with TAFRO clinical subtype responsive to IL-6/JAK inhibition: a pediatric case series. Pediatr Blood Cancer 2021; 68 (10): e29261. doi: 10.1002/pbc.29261.
64. Killian M, Viel S, Chalayer E et al. JAK1/2 inhibition in severe TAFRO syndrome: a case report. Ann Intern Med 2021; 174 (5): 719–721. doi: 10.7326/L20-1051.
65. Kakutani T, Nunokawa T, Chinen N et al. Treatment-resistant idiopathic multicentric Castleman disease with thrombocytopenia, anasarca, fever, retikulin fibrosis, renal dysfunction, and organomegaly managed with Janus kinase inhibitors: a case report. Medicine (Baltimore) 2022; 101 (48): e32200. doi: 10.1097/MD.0000000000032200.
66. Gao YH, Duan MH, Li J et al. Ruxolitinib for the treatment of refractory idiopathic multicentric Castleman disease: a case report. Turk J Haematol 2024; 41 (1): 61–63. doi: 10.4274/tjh.galenos.2024.2023.0477.
67. Doubková M, Štefánková M, Čan V et al. Lymphangioleiomyomatosis. Klin Onkol 2019; 32 (5): 367–374. doi: 10.14735/amko2019367.
68. Ozeki M, Endo S, Yasue S et al. Sirolimus treatment for intractable vascular anomalies (SIVA): an open-label, single-arm, multicenter, prospective trial. Pediatr Int 2025; 67 (1): e70002. doi: 10.1111/ped.70002.
69. Wiegand S, Dietz A, Wichmann G. Efficacy of sirolimus in children with lymphatic malformations of the head and neck. Eur Arch Otorhinolaryngol 2022; 279 (8): 3801–3810. doi: 10.1007/s00405-022-07378-8.
70. Seront E, Van Damme A, Legrand C et al. Preliminary results of the European multicentric phase III trial regarding sirolimus in slow-flow vascular malformations. JCI Insight 2023; 8 (21): e173095. doi: 10.1172/jci.insight.173095.
71. Seront E, Hermans C, Boon LM et al. Targeted treatments for vascular malformations: current state of the art. J Thromb Haemost 2024; 22 (11): 2961–2975. doi: 10.1016/j.jtha.2024.07.013.
72. Durán-Romero AJ, Hernández-Rodríguez JC, Ortiz-Álvarez J et al. Efficacy and safety of oral sirolimus for high-flow vascular malformations in real clinical practice. Clin Exp Dermatol 2022; 47 (1): 57–62. doi: 10.1111/ced.14841.
73. Blagosklonny MV. Cancer prevention with rapamycin. Oncotarget 2023; 14 : 342–350. doi: 10.18632/oncotarget.28410.
74. Gao H, Liu S, Mai Y et al. Combined therapy of prednisone and mTOR inhibitor sirolimus for treating retroperitoneal fibrosis. Ann Rheum Dis 2023; 82 (5): 688–697. doi: 10.1136/ard-2022-223736.
75. Fiamoli V, Blatný J, Pejchalová A et al. Sirolimus – alternativa pro léčbu autoimunitní hemolytické anémie způsobené tepelnými protilátkami (WAIHA). Trans Hematol Dnes 2019; 25 (3): 264–268.
76. Arenas DJ, Floess K, Kobrin D et al. Increased mTOR activation in idiopathic multicentric Castleman disease. Blood 2020; 135 (19): 1673–1684. doi: 10.1182/blood.2019002792.
77. Pierson SK, Shenoy S, Oromendia AB et al. Discovery and validation of a novel subgroup and therapeutic target in idiopathic multicentric Castleman disease. Blood Adv 2021; 5 (17): 3445–3456. doi: 10.1182/bloodadvances.2020004016.
78. Stern RM, Berliner N. Targeting the mTOR pathway in idiopathic multicentric Castleman disease. J Clin Invest 2019; 129 (10): 4086–4088. doi: 10.1172/JCI131332.
79. Fajgenbaum DC, Langan RA, Japp AS et al. Identifying and targeting pathogenic PI3K/AKT/mTOR signaling in IL-6-blockade-refractory idiopathic multicentric Castleman disease. J Clin Invest 2019; 129 (10): 4451–4463. doi: 10.1172/JCI126091.
80. Bevacqua M, Baldo F, Pastore S et al. Sirolimus and everolimus in a pediatric center: a case series and review of the literature. Paediatr Drugs 2019; 21 (3): 185–193. doi: 10.1007/s40272-019-00337-7.
81. Sumiyoshi R, Koga T, Furukawa K et al. A case of tocilizumab-refractory idiopathic multicentric Castleman‘s disease successfully treated with sirolimus. Clin Immunol 2021; 233 : 108887. doi: 10.1016/j.clim.2021. 108887.
82. Bayram E, Pehlivan UA, Fajgenbaum DC et al. Refractory idiopathic multicentric Castleman disease responsive to sirolimus therapy. Am J Hematol 2023; 98 (2): 361–364. doi: 10.1002/ajh.26783.
83. Liu YT, Gao YH, Zhao H et al. Sirolimus is effective for refractory/relapsed idiopathic multicentric Castleman disease: a single-center, retrospective study. Ann Hematol 2024; 103 (10): 4223–4230. doi: 10.1007/s00277-024-05783-z.
84. Koga T, Takemori S, Hagimori N et al. An open-label continuation trial of sirolimus for tocilizumab-refractory idiopathic multicentric Castleman disease: study protocol for an investigator-initiated, multicenter, open-label trial (SPIRIT compliant). Medicine (Baltimore) 2020; 99 (50): e23291. doi: 10.1097/MD.0000000000023291.
85. Wang X, Ye S, Xiong C et al. Successful treatment with bortezomib and thalidomide for POEMS syndrome associated with multicentric mixed-type Castleman‘s disease. Jpn J Clin Oncol 2011; 41 (10): 1221–1224. doi: 10.1093/jjco/hyr120.
86. Lin Q, Fang B, Huang H et al. Efficacy of bortezomib and thalidomide in the recrudescent form of multicentric mixed-type Castleman‘s disease. Blood Cancer J 2015; 5 (3): e298. doi: 10.1038/bcj.2015.12.
87. Miltenyi Z, Toth J, Gonda A et al. Successful immunomodulatory therapy in Castleman disease with paraneoplastic pemphigus vulgaris. Pathol Oncol Res 2009; 15 (3): 375–381. doi: 10.1007/s12253-008-9133-x.
88. Jung CP, Emmerich B, Goebel FD et al. Successful treatment of a patient with HIV-associated multicentric Castleman disease (MCD) with thalidomide. Am J Hematol 2004; 75 (3): 176–177. doi: 10.1002/ajh.10467.
89. Starkey CR, Joste NE, Lee FC. Near-total resolution of multicentric Castleman disease by prolonged treatment with thalidomide. Am J Hematol 2006; 81 (4): 303–304. doi: 10.1002/ajh.20538.
90. Tatekawa S, Umemura K, Fukuyama R et al. Thalidomide for tocilizumab-resistant ascites with TAFRO syndrome. Clin Case Rep 2015; 3 (6): 472–478. doi: 10.1002/ccr3.284.
91. Zhang L, Zhao AL, Duan MH et al. Phase 2 study using oral thalidomide-cyclophosphamide-prednisone for idiopathic multicentric Castleman disease. Blood 2019; 133 (16): 1720–1728. doi: 10.1182/blood-2018-11-884577.
92. Adam Z, Szturz P, Křen L et al. PET-CT documented fast onset of treatment response to cyclophosphamide, thalidomide and dexamethasone in patients with multicentric Castlemans disease. Case description and treatment information overview. Vnitr Lek 2013; 59 (4): 301–312.
93. Adam Z, Klimeš J, Pour L et al. Maligní onemocnění psychika a stres. Praha: Grada Publishing 2021.
94. Zhou X, Wei J, Lou Y et al. Salvage therapy with lenalidomide containing regimen for relapsed/refractory Castleman disease: a report of three cases. Front Med 2017; 11 (2): 287–292. doi: 10.1007/s11684-017-0510-2.
95. Cai S, Zhong Z, Li X et al. Treatment of multicentric Castleman disease through combination of tocilizumab, lenalidomide and glucocorticoids: case report. Medicine (Baltimore) 2019; 98 (46): e17681. doi: 10.1097/MD.0000000000017681.
96. Zhang Y, Suo SS, Yang HJ et al. Clinical features and treatment of 7 Chinese TAFRO syndromes from 96 de novo Castleman diseases: a 10-year retrospective study. J Cancer Res Clin Oncol 2020; 146 (2): 357–365. doi: 10.1007/s00432-019-03120-w.
97. Szturz P, Adam Z, Chovancová J et al. Lenalidomide: a new treatment option for Castleman disease. Leuk Lymphoma 2012; 53 (10): 2089–2091. doi: 10.3109/10428194.2011.621564.
98. Szturz P, Adam Z, Moulis M et al. Our experience in treatment of multicentric plasma-cell Castleman disease associated with vasculitis manifestations – case report and literature review. Vnitr Lek 2012; 58 (9): 679–690.
99. Sevindik OG, Mutlu YG, Aydin BB et al. Usage of daratumumab, lenalidomide, dexamethasone (DRd) combination in a case of Castleman disease variant of polyneuropathy, organomegaly, endocrinopathy, monoclonal gammopathy, and skin changes syndrome (CD-POEMS). Hemasphere 2022; 6 (7): e728. doi: 10.1097/HS9.0000000000000728.
100. Shi Y, Li J, Zhang L. Daratumumab for the treatment of refractory idiopathic multicentric Castleman disease: a case report. Ann Hematol 2022; 101 (11): 2529–2531. doi: 10.1007/s00277-022-04926-4.
101. Coulomb D, Szablewski V, Robert N et al. A case of refractory IgG4-related disease successfully treated with daratumumab and lenalidomide. Rheumatology (Oxford) 2025; 64 (2): 895–897. doi: 10.1093/rheumatology/keae448.
102. Peng Q, Wu F, Shi Y et al. Idiopathic multicentric Castleman‘s disease mimicking immunoglobulin G4-related disease responding well to bortezomib: a case report. BMC Nephrol 2023; 24 (1): 290. doi: 10.1186/s12882-023-03335-7.
103. Khan AA, Siraj F, Bhargava M et al. Successful treatment of multicentric Castleman‘s disease accompanying myeloma with bortezomib. BMJ Case Rep 2012; 2012: bcr2012007646. doi: 10.1136/bcr-2012-007646.
104. Liu XH, Zhang L, Li J et al. Rare forms of idiopathic multicentric Castleman disease presenting with intrahepatic cholestatic jaundice successfully treated with the bortezomib-based regimen: two case reports. Ann Hematol 2023; 102 (4): 977–979. doi: 10.1007/s00277-022-05066-5.
105. Lin Q, Fang B, Huang H et al. Efficacy of bortezomib and thalidomide in the recrudescent form of multicentric mixed-type Castleman‘s disease. Blood Cancer J 2015; 5 (3): e298. doi: 10.1038/bcj.2015.12.
106. Zhang L, Zhang MY, Cao XX et al. A prospective, multicenter study of bortezomib, cyclophosphamide, and dexamethasone inrelapsed/refractory iMCD. Leuk Lymphoma 2022; 63 (3): 618–626. doi: 10.1080/10428194.2021.1999437.
107. Gao YH, Li SY, Dang Y et al. Efficacy and safety of orelabrutinib in relapsed/refractory idiopathic multicentric Castleman disease: a single-centre, retrospective study. Br J Haematol 2025; 206 (1): 152–158. doi: 10.1111/bjh.19827.
108. Zhang L, Gao YH, Li SY et al. A prospective study of zanubrutinib, a Bruton tyrosine kinase inhibitor, in relapsed/refractory idiopathic multicentric Castleman disease. Int J Hematol 2024; 119 (6): 631–637. doi: 10.1007/s12185-024-03747-7.
109. Frampton JE. Inebilizumab: first approval. Drugs 2020; 80 (12): 1259–1264. doi: 10.1007/s40265-020-01370-4.
110. Nie T, Blair HA. Inebilizumab: a review in neuromyelitis optica spectrum disorder. CNS Drugs 2022; 36 (10): 1133–1141. doi: 10.1007/s40263-022-00949-7.
111. Stone JH, Khosroshahi A, Zhang W et al. Inebilizumab for treatment of IgG4-related disease. N Engl J Med 2025; 392 (12): 1168–1177. doi: 10.1056/NEJMoa240 9712.
112. Li S, Gao Y, He Y et al. A case report of AQP4-IgG-seropositive refractory neuromyelitis optica spectrum disorder patient with Sjögren‘s syndrome and pancytopenia treated with inebilizumab. Front Neurol 2024; 15 : 1371515. doi: 10.3389/fneur.2024.1371515.
113. Koa B, Borja AJ, Aly M et al. Emerging role of 18F-FDG PET/CT in Castleman disease: a review. Insights Imaging 2021; 12 (1): 35. doi: 10.1186/s13244-021-00963-1.
114. Koukalová R, Selingerová I, Řehák Z et al. FDG - -PET/ CT for initial staging and response assessment in Castleman disease – retrospective single-center study of 29 cases. Klin Onkol 2021; 34 (2): 120–127. doi: 10.48095/ccko2021120.
115. Bitektine E, Hagh-Daoust H, Michel RP et al. The value of a pet scan in selecting the best lymph node to biopsy, and confirming the diagnosis of idiopathic multicentric Castleman disease with HLH and EBV viremia in a previously healthy adult. Eur J Case Rep Intern Med 2024; 11 (12): 004908. doi: 10.12890/2024_ 004908.
116. Han EJ, O JH, Jung SE et al. FDG PET/CT findings of Castleman disease assessed by histologic subtypes and compared with laboratory findings. Diagnostics (Basel) 2020; 10 (12): 998. doi: 10.3390/diagnostics10 120998.
117. Wang G, Xu Q, Liu Y et al. 18F-FDG PET/CT metabolic parameters are correlated with clinical features and valuable in clinical stratification management in patients of Castleman disease. Cancer Imaging 2025; 25 (1): 12. doi: 10.1186/s40644-025-00833-9.
118. Nishimura Y, Habermann T, Dispenzieri A. Comparative safety of tocilizumab and siltuximab in Castleman disease: pharmacovigilance study. Am J Hematol 2025; 101 (1): 165–168. doi: 10.1002/ajh.70122.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článek Není ct jako CT
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2026 Číslo 2- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Fixní kombinace tramadol/paracetamol je doporučenou volbou v léčbě chronické bolesti v ordinaci praktického lékaře
-
Všetky články tohto čísla
- Není ct jako CT
- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- Intravaskulárna propagácia adenomyózy v krvných cievach myometria a uterinného leiomyómu u pacientky s mutáciou génu fumaráthydratázy – zriedkavý nález imitujúci malígnu neopláziu
- Second recurrence of breast cancer 36 years after initial surgery and 18 years after the first recurrence – an extremely rare case
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
- Cancer patients admitted to intensive care unit
- Nádory GIT – chemoterapie a precizní léčba se synergicky doplňují
- Snižování škod rizikového chování v onkologické prevenci
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy