-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Intravaskulárna propagácia adenomyózy v krvných cievach myometria a uterinného leiomyómu u pacientky s mutáciou génu fumaráthydratázy – zriedkavý nález imitujúci malígnu neopláziu
Intravascular propagation of adenomyosis within the blood vessels of the myometrium and uterine leiomyoma in a patient harboring germline mutation in the fumarate hydratase gene – a rare finding simulating malignancy
Background: Hereditary leiomyomatosis and renal cell carcinoma is a rare genetic disorder characterized by a predisposition to the development of multiple cutaneous and uterinne leiomyomas with a potential for malignant transformation and a risk of renal carcinoma. Case: A 39-year-old woman suffered from this disease underwent hysterectomy due to uterus myomatosus. Histologically, some tumors showed typical appearance of fumarate hydratase-deficient leiomyomas. There were foci of adenomyosis in the myometrium. As an incidental finding, multiple thin-walled blood vessels filled with conglomerates of endometrial stroma and glandular epithelium were found in the myometrium and leiomyoma. At the first look, this feature suggested an intravascular cancer propagation. However, this endometrial tissue showed bland appearance with no atypia or mitoses and revealed low proliferative activity. Even after extensive sampling of the uterus, no malignant neoplasia was revealed. The finding was reported as intravascular form of adenomyosis. Conclusion: A propagation of adenomyosis within the uterine blood vessels is a rare histological finding causing diagnostic difficulties as it resembles intravascular spreading of malignant neoplasm. Although this is not a tumor entity, it represents an important differential diagnosis in the oncopathological practice. The pathologist’s knowledge about this phenomenon is crucial to avoid confusion with vascular dissemination of malignancy.
Keywords:
adenomyosis – fumarate hydratase – leiomyomatosis – intravascular propagation
Autori: V. Bartoš 1; B. Hudec 2; E. Baloghová 3
Pôsobisko autorov: Martinské bioptické centrum, s. r. o., Martin, Slovensko 1; II. Gynekologicko-pôrodnícka klinika SZU, Fakultná nemocnica s poliklinikou F. D. Roosevelta, Banská Bystrica, Slovensko 2; Dermatovenerologické oddelenie, Fakultná nemocnica s poliklinikou, Nové Zámky, Slovensko 3
Vyšlo v časopise: Klin Onkol 2026; 39(2): 112-116
Kategória: Kazuistika
doi: https://doi.org/10.48095/ccko2026112Súhrn
Východisko: Syndróm hereditárnej leiomyomatózy a renálneho karcinómu je vzácne genetické ochorenie charakteristické predispozíciou k vzniku mnohočetných kožných a uterinných leiomyómov s potenciálom ich malígnej transformácie a rizikom vzniku karcinómu obličky. Prípad: 39-ročná žena s týmto ochorením podstúpila hysterektómiu pre uterus myomatosus. Histologicky niektoré uzly vykazovali znaky charakteristické pre fumaráthydratáza-deficientné leiomyómy. V myometriu sa vyskytovali ložiská adenomyózy. Incidentálny nález v myometriu aj v leiomyóme predstavovali početné tenkostenné krvné cievy obsahujúce v lúmene agregáty endometriálnej strómy a žľazového epitelu. Tento nález na prvý pohľad vzbudzoval dojem intravaskulárnej nádorovej propagácie. Endometriálne tkanivo v týchto agregátoch však malo blandný vzhľad, bolo bez atypií, bez mitóz a vykazovalo nízku proliferačnú aktivitu. Ani po extenzívnom spracovaní vzoriek maternice nebola odhalená malígna neoplázia. Nález bol reportovaný ako intravaskulárna forma adenomyózy. Záver: Propagácia adenomyózy v krvných cievach maternice je zriedkavý histologický nález spôsobujúci diagnostické rozpaky, pretože pripomína intravaskulárne šírenie malígnej neoplázie. Hoci nejde o nádorové ochorenie, v onkopatologickej praxi predstavuje významnú diferenciálnu diagnózu. Znalosť bioptika o tomto fenoméne je kľúčová, aby sa predišlo zámene za vaskulárnu disemináciu malignity.
Klíčová slova:
adenomyóza – leiomyomatóza – fumaráthydratáza – intravaskulárna propagácia
Úvod
Syndróm hereditárnej leiomyomatózy a renálneho karcinómu (hereditary leiomyomatosis and renal cell cancer – HLRCC) je vzácne genetické ochorenie charakteristické predispozíciou k vzniku mnohočetných kožných a uterinných leiomyómov a rizikom vzniku karcinómu obličky. Príčinou syndrómu je autozomálne dominantne dedičná heterozygotná mutácia tumor supresorového génu FH (fumarat hydratase gene) na chromozóme 1q42.3-43, ktorý kóduje enzým fumaráthydratázu [1–3]. Mutácie génu FH môžu byť príčinou dvoch rôznych ochorení: 1) autozomálne recesívne dedičného deficitu fumaráthydratázy, k vzniku ktorej je nutná mutácia obidvoch génových alel [1]. Ide o raritné metabolické ochorenie prejavujúce sa hypotóniou, encefalopatiou a psychomotorickou retardáciou a obvykle vedie k úmrtiu v rannom veku; 2) autozomálne dominantne dedičného syndrómu HLRCC, k vzniku ktorého postačuje mutácia jednej alely génu [1]. Kožné leiomyómy sú zvyčajne prvou klinickou manifestáciou ochorenia, postihujú väčšinu pacientov s HLRCC a s vekom ich počet stúpa [1,2]. Leiomyómy maternice u žien s HLRCC vznikajú v mladšom veku, bývajú mnohopočetné, väčšie a majú vyššie riziko malígnej transformácie na leiomyosarkóm [1,2]. U časti pacientov (15–20 %) dochádza k vzniku karcinómu obličky, najmä papilárneho karcinómu s agresívnym správaním [1,2]. Treba však podotknúť, že HLRCC má značnú fenotypovú variabilitu. Môžu sa vyskytovať mnohopočetné kožné leiomyómy, alebo len jeden, prípadne sa kožné lézie vôbec nemusia prejaviť. Renálny karcinóm je diagnostikovaný len u niektorých pacientov a uterinné leiomyómy taktiež nemusia byť vždy prítomné. Variabilita expresie fenotypových znakov sa popisuje aj u jedincov v rámci jednej rodiny [1]. V predkladanom príspevku je opísaný prípad mladej ženy s mutáciou génu FH, u ktorej bola v myomatóznej maternici histologicky potvrdená propagácia adenomyózy v krvných cievach imitujúca malignitu. Čitateľov sa snažíme oboznámiť o tomto zaujímavom fenoméne, ktorý podľa našich vedomostí zatiaľ nebol v českej a slovenskej literatúre publikovaný a s ktorým sa možno občas stretnúť v bioptickej praxi.
Opis prípadu
Prezentujeme 39-ročnú ženu s geneticky potvrdeným nosičstvom aberantného génu FH (c.912_918del), ktorá podstúpila hysterektómiu pre uterus myomatosus. Klinicky ju trápila pretrvávajúca hypermenorea so sekundárnou anémiou. Bola po dvoch cisárskych rezoch. Na mutáciu bola testovaná z dôvodu pozitívneho nálezu u jej matky a tiež brata jej matky, ktorý zomrel vo veku 45 rokov na zhubný nádor obličky. Aj matka mala v minulosti odstránenú maternicu pre myomatózny uterus. Pacientka bola dispenzarizovaná u dermatológa s kontrolami 2× ročne. Anamnesticky mala cca 8 rokov na pravej hornej končatine s maximom v oblasti nad lakťom podkožné uzlíky farby kože, bez bolestivosti, bez secernácie. Prejavy imponovali ako možné leiomyómy. Odporučené mala histologické vyšetrenie na potvrdenie diagnózy, ktoré zatiaľ (podľa dostupných informácií) realizované nebolo. Klinické prejavy v období medzi kontrolami boli nemenné, nové lézie nepribudli. Z dermatologického hľadiska bola bez liečby.
Pre vyššie zmieňované gynekologické ťažkosti mala vykonanú hysterektómiu s obojstranou salpingektómiou. Maternica (rozmerov 13 × 10 × 6 cm) obsahovala početné dobre aj menej ohraničené intramurálne a submukózne hnedobelavé uzly, najväčší priemeru 2,5 cm. Endometrium bolo nízke, nesuspektného vzhľadu. Histologicky vyšetrované uzly tela maternice pozostávali z konvenčných leiomyómov bez bunkových atypií s nízkou proliferačnou aktivitou (Ki-67 index < 5 %), ako aj z leiomyómov vykazujúcich špecifické celulárne a jadrové atypie charakteristické pre fumaráthydratáza (FH) -deficientné leiomyómy (imunohistochemicky dezmín+, estrogénové receptory minoritne slabo+, progesterónové receptory+, proteín p53–, proteín p16 zonálne+), bez zvýšenej mitotickej aktivity s minimálnou proliferačnou aktivitou (Ki-67 index cca 2–3 %).
Korporálne endometrium malo atrofizovaný a nepravidelne proliferačný vzhľad bez bunkových atypií. Najmä v submukóznych úsekoch myometria sa vyskytovali ložiská adenomyózy (obr. 1). Veľmi zaujímavý, z histopatologického hľadiska však znepokojujúci nález v myometriu v tesnej blízkosti fumaráthydratáza-deficientného leiomyómu, ale aj priamo v ňom boli početné tenkostenné krvné cievy obsahujúce v lúmene agregáty endometriálnej strómy a žľazového epitelu (obr. 2–3). Tento nález na prvý pohľad vzbudzoval dojem intravaskulárnej nádorovej propagácie. Endotel ciev bol imunohistochemicky pozitívny na CD31 (obr. 4) a negatívny na marker D2-40, čo potvrdzovalo krvný a nie lymfatický pôvod. Intraluminózne agregáty tkaniva vykazovali charakteristický endometriálny imunofenotyp, epitel pozitívny na PAX-8 a cytokeratín 7 (obr. 5) a stróma pozitívna na CD10 (obr. 6). V mnohých cievach endometriálne tkanivo adherovalo k endotelovej výstelke, čo vylučovalo jeho sekundárne zanesenie do ciev počas laboratórneho spracovania. Žľazový epitel aj stróma v týchto konglomerátoch mali diferencovaný vzhľad, boli bez atypií, bez mitóz a vykazovali len nízku proliferačnú aktivitu pod 10 % (obr. 7).
Obr. 1. Atrofizované endometrium (vpravo) s ložiskami adenomyózy v priľahlom myometriu (vľavo). (Farbenie hematoxylín & eozín, zväčšenie 40×). 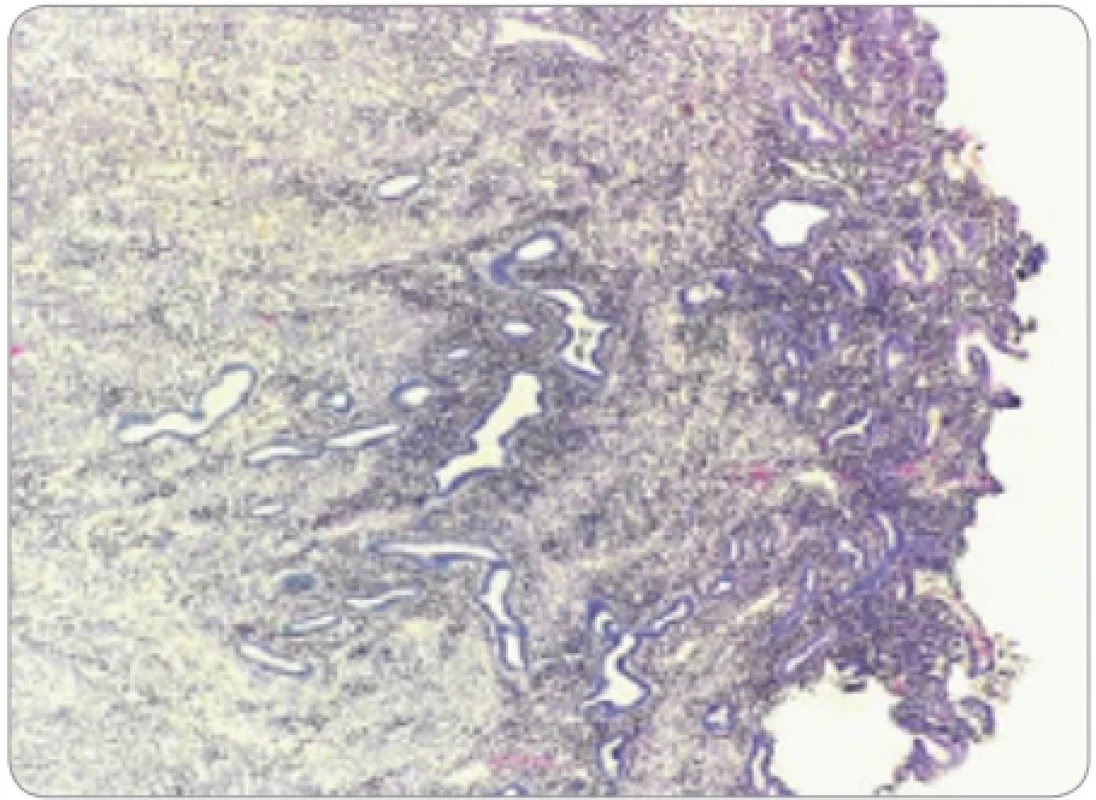
Obr. 2. Agregáty endometriálneho tkaniva v krvných cievach myometria. (Farbenie hematoxylín & eozín, zväčšenie 200×). 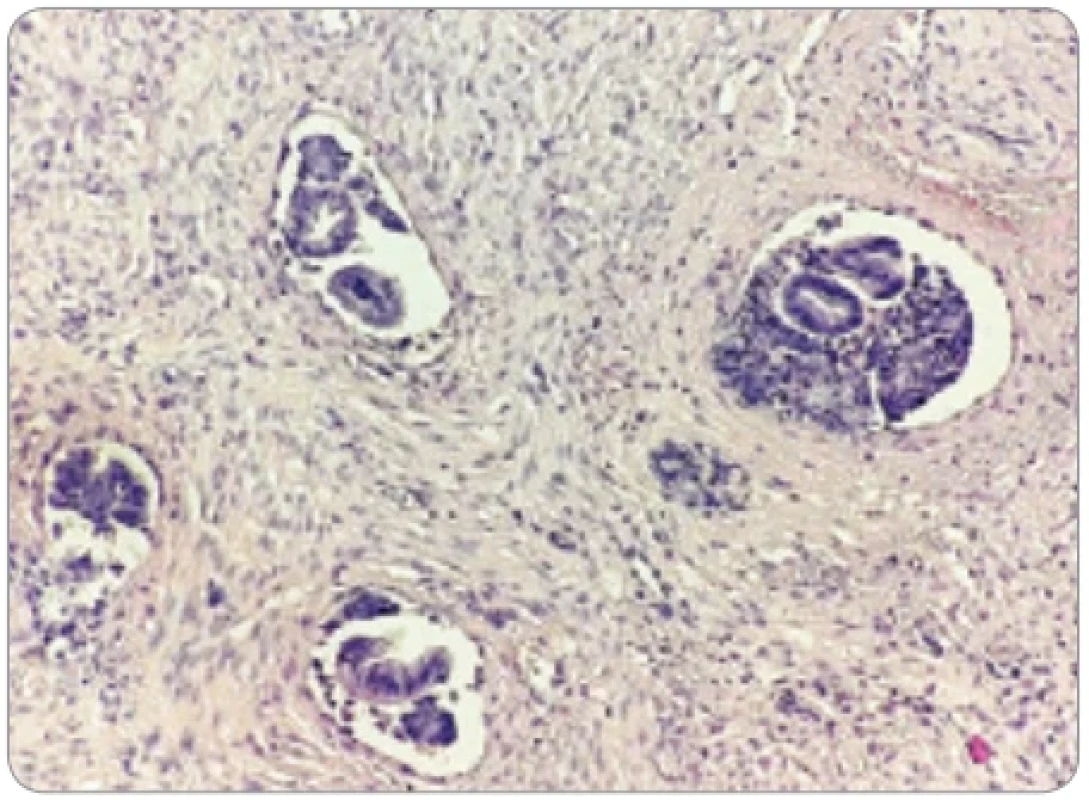
Obr. 3. Agregáty endometriálneho tkaniva v krvných cievach myometria. (Farbenie hematoxylín & eozín, zväčšenie 200×). 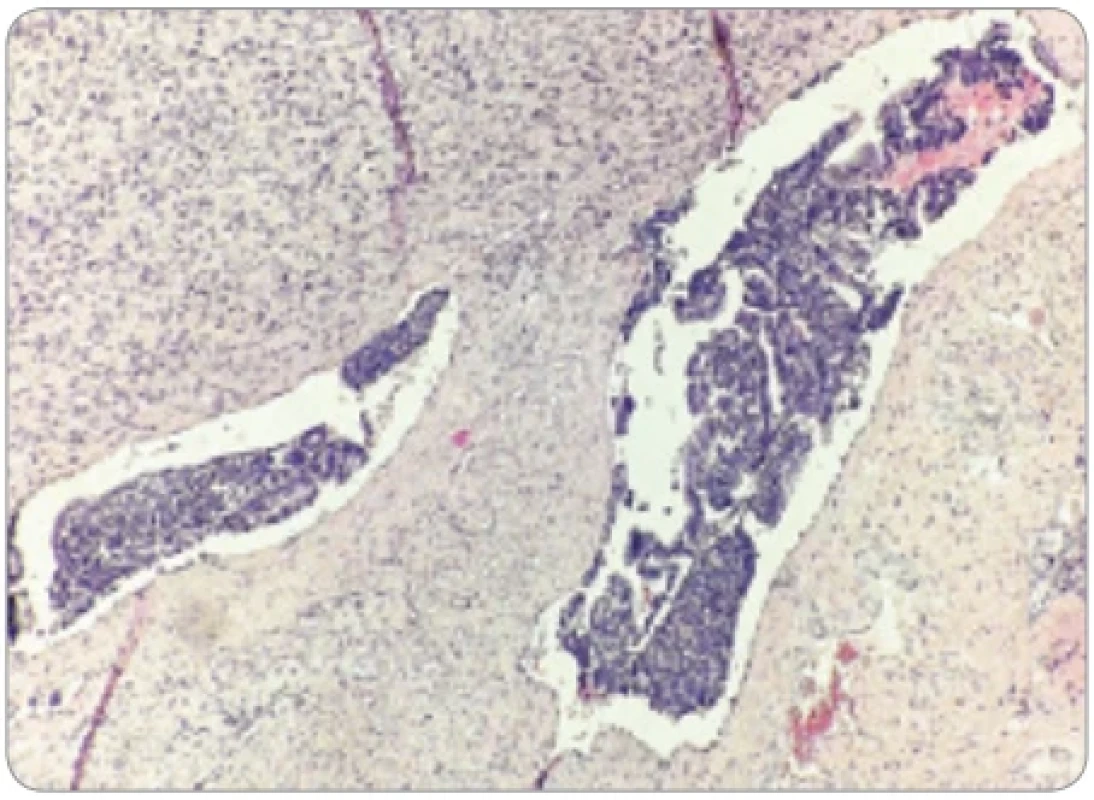
Obr. 4. Imunohistochemická pozitivita endotelu ciev obsahujúcich agregáty endometriálneho tkaniva na CD31. (Zväčšenie 200×). 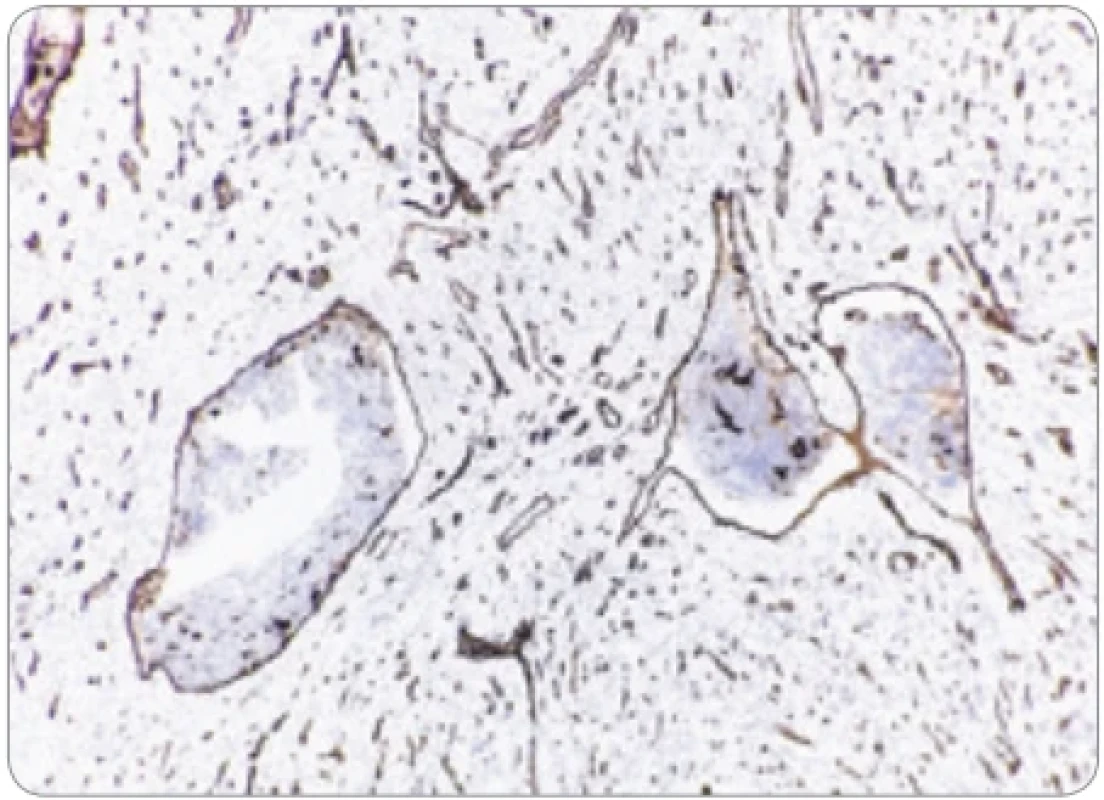
Obr. 5. Imunohistochemická pozitivita endometriálneho žľazového epitelu v cievach na CK 7. (Zväčšenie 200×). 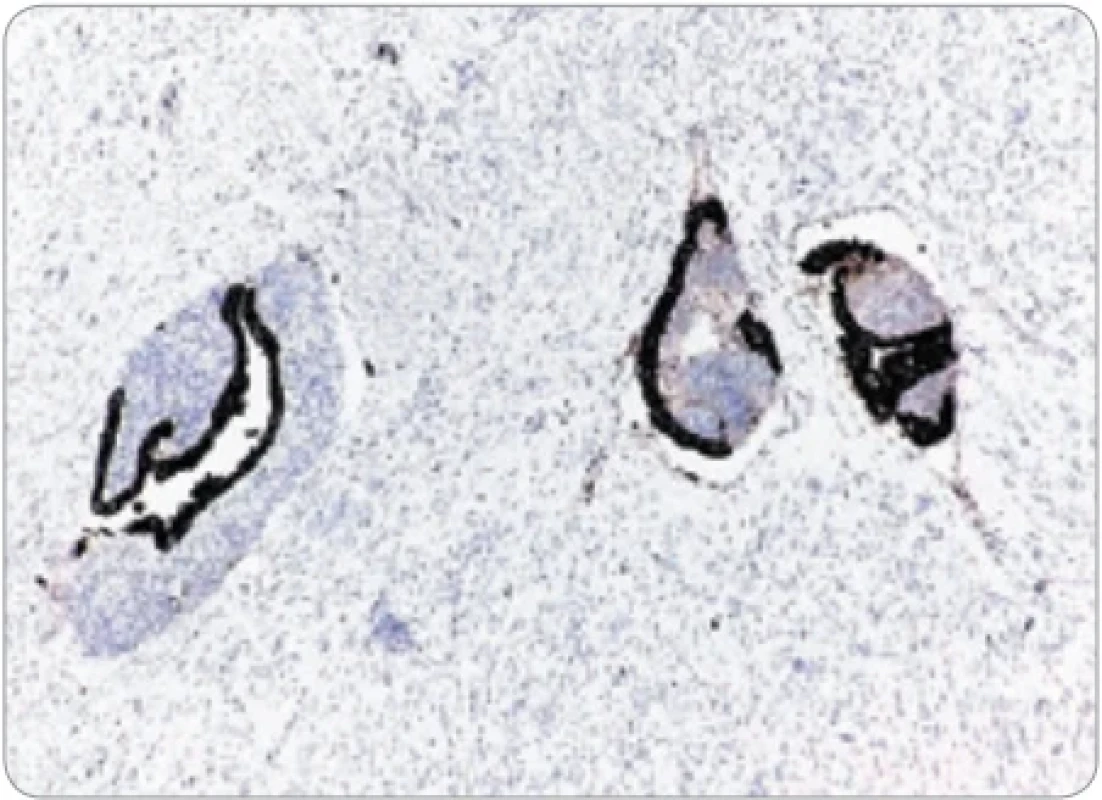
Obr. 6. Imunohistochemická pozitivita endometriálnej strómy v cievach na CD10. (Zväčšenie 200×). 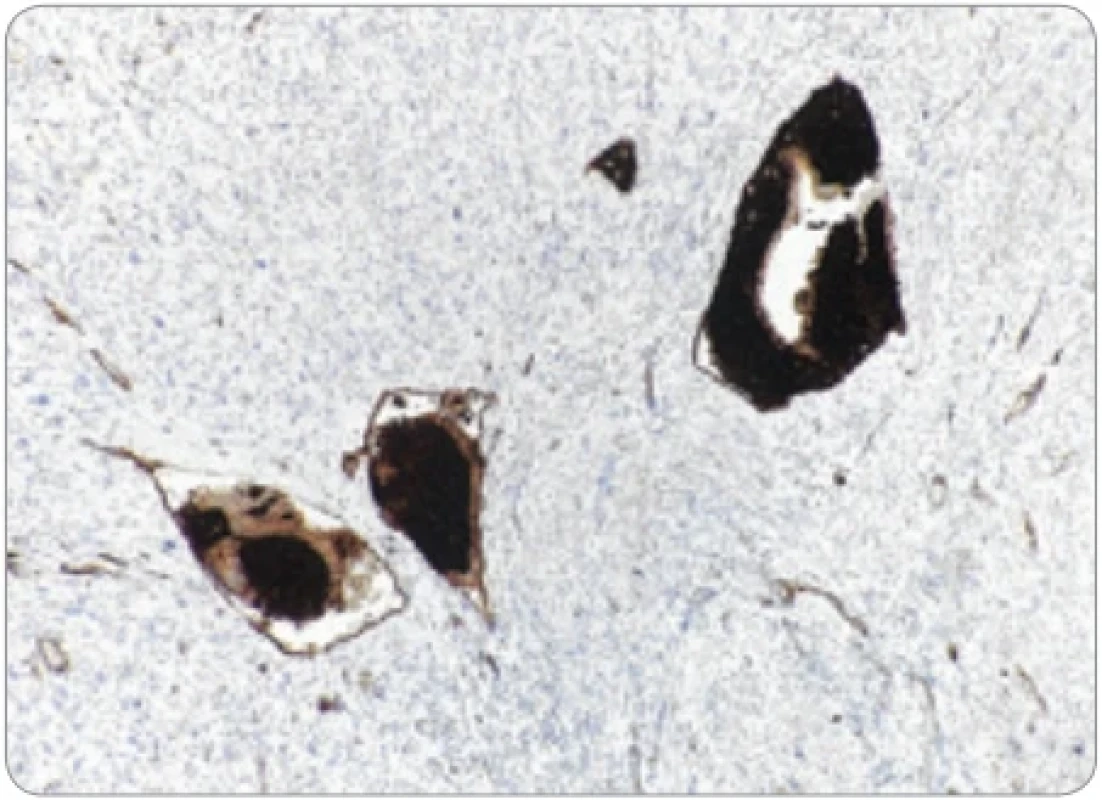
Obr. 7. Minimálna proliferačná aktivita (Ki-67 index & 5 %) endometriálneho tkaniva v cievach. (Zväčšenie 200×). 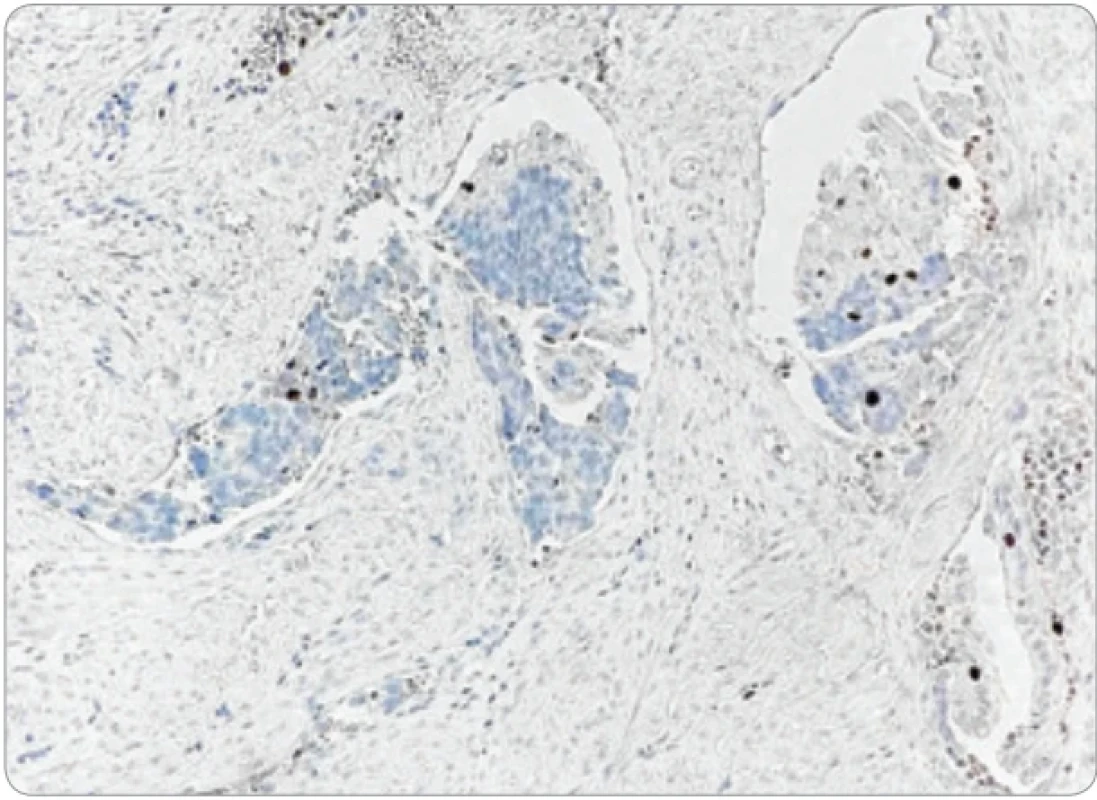
Resekát maternice sme makroskopicky opakovane revidovali a tkanivo z endometria, myometria aj leiomyómov mnohonásobne doexcidovávali (celkom spracovaných 24 parafínových blokov). Aj v niektorých nových excíziách sme opätovne zachytili tieto štruktúry, zaujímavé však bolo, že sa vyskytovali iba v bezprostrednom okolí jedného z leiomyómov a priamo v ňom, v iných lokalitách sme ich neidentifikovali. Endometrium a taktiež ložiská adenomyózy boli bez bunkových atypií, známky malígnej neoplázie sme nepotvrdili. Patológ sa v bioptickom reporte zmienil o tomto náleze, ktorý označil za intravaskulárnu formu adenomyózy. Pacientka je vzhľadom na multisystémovú manifestáciu daného genetického ochorenia klinicky stále sledovaná.
Diskusia
V našej kazuistike prezentujeme zriedkavý prípad mladej pacientky s nosičstvom mutácie FH s diagnózou uterus myomatosus. Pri mikroskopickom vyšetrení niektoré uterinné leiomyómy vykazovali viaceré znaky tzv. fumaráthydratáza-deficientných leiomyómov, ku ktorým patria zvýšená celularita, bizarné jadrá vrátane jadier aranžovaných do tvaru retiazky, eozinofilné cytoplazmatické a prominujúce jadrové inklúzie a perinukleárne „halo“ [4]. Tieto atypické črty nútia patológa uvažovať o závažnejšej diagnóze, najmä o hladkosvalovom nádore s neistým malígnym potenciálom (smooth muscle tumor of uncertain malignant potential – STUMP) a leiomyosarkóme. V našom prípade vzhľadom na absencia nekróz, minimálnu proliferačnú aktivitu a nezvýšenú mitotickú aktivitu nádor nespĺňal znaky malígnej neoplázie.
Najzaujímavejší nález predstavovala intravaskulárna propagácia endometriálneho tkaniva v krvných cievach myometria a leiomyómu, ktorá je zdrojom záujmu kazuistiky. Tento fenomén bol doteraz opísaný vo viacerých literárnych zdrojoch, ale jeho pôvod ostáva nejasný. Pravdepodobne prvýkrát ho publikoval v roku 1984 Reitzenstein [5] u 55-ročnej ženy, ktorej potvrdil v myometriu v blízkosti ložísk adenomyózy v lúmene vén agregáty endometriálnej strómy a žliaz. Identický obraz dokumentovali vo svojej práci mexickí autori [6] u 35-ročnej a 51-ročnej ženy, taktiež v asociácii s adenomyózou. Doposiaľ boli publikované dve pôvodné štúdie zaoberajúce sa touto problematikou. V staršej práci z roku 1989 Sahin et al. [7] zaznamenali v súbore 277 hysterektómií intravaskulárne fragmenty endometriálneho tkaniva (intravascular endometrial tissue fragments) v 14 prípadoch a všetky v asociácii s adenomyózou, čo v rámci tejto skupiny predstavovalo 17,9 %. V novšej štúdii z roku 2010 Meenakshi a McCluggage [8] potvrdili zo súboru 434 prípadov adenomyózy intravaskulárne agregáty v 54 prípadoch (12,4 %). V texte ich označujú termínom intravaskulárna adenomyóza. Vždy išlo o tenkostenné stredne veľké cievy vzhľadu vén. Agregáty endometriálneho tkaniva v cievach zväčša adherovali k cievnej stene a protrudovali do lúmenu, zriedkavejšie voľne plávali v lúmene. Obidve publikácie konštatujú [7,8], že pri adenomyóze, najmä jej extenzívnej forme postihujúcej aj hlbšie myometrium, ide o relatívne častý nález. Na druhej strane Pérez Buendína et al. [9] zo súboru 68 hysterektómií obsahujúcich adenomyózu zaznamenali tento nález iba v jednom prípade (1,4 %). Bez ohľadu na názory jednotlivých autorov je evidentné, že tento fenomén sa vyskytuje iba v koincidencii s adenomyózou a teda s ňou priamo súvisí. Ani jedna doteraz publikovaná práca však nepodáva relevantné vysvetlenie mechanizmu jeho vzniku, autori v diskusii prezentujú iba dohady. Adenomyóza je ochorenie charakteristické výskytom ektopických endometriálnych žliaz a strómy vo vnútri myometria [10]. Postihuje takmer 20 % žien v reprodukčnom veku [10]. Patogenetické mechanizmy jej vzniku sú stále neobjasnené. Podľa najpopulárnejšej teórie bazálne endometrium invaginuje do priľahlej svaloviny, možno v dôsledku slabosti svalových vlákien alebo zvýšeného uterinného tlaku [8]. Iná hypotéza predpokladá, že adenomyóza vzniká primárne v myometriu (a nie z endometria) z multipotentných kmeňových buniek, pravdepodobne pericytov, ktoré obkolesujú cievy. Tieto bunky sa transformujú do endometriálnych stromálnych buniek a tie následne indukujú tvorbu epitelovej zložky. Vytvorené agregáty by mohli následne prerastať do lúmenu priľahlých krvných ciev [8]. Analógom je výskyt endometriálneho tkaniva v cievach mimo maternice, ktorý je opísaný napr. v paraadnexách [12] alebo vo vaječníku [13] a predstavuje formu intravaskulárnej endometriózy. V našom prípade je zaujímavé, že tento nález bol iba ložiskový v okolí jedného leiomyómu a sčasti aj priamo v ňom. Nepozorovali sme koncentráciu ložísk adenomyózy okolo ciev, ani ich priamy kontakt s nimi a teda nemôžeme potvrdiť, že by išlo o prerastanie adenomyózy do ciev s ich následnou intravaskulárnou propagáciou.
Z praktického hľadiska je dôležité, že intravaskulárny komponent adenomyózy pravdepodobne nemá žiadny klinický význam. Jeho hlavné úskalie však spočíva v tom, že môže byť chybne interpretovaný ako intravaskulárne šírenie malígnej neoplázie. Preto je dôležité, aby bioptik o tomto fenoméne vedel. V praxi môže byť zamenený najmä za low-grade endometriálny stromálny sarkóm [8,9]. K tomu dochádza zvlášť vtedy, keď je postihnutie ciev mnohopočetné a keď má adenomyóza, vrátane intravaskulárneho komponentu, len minimálne množstvo žľazovej zložky – tzv. stromálna adenomyóza. Low-grade endometriálny stromálny sarkóm má síce blandný cytomorfologický vzhľad, ale vykazuje infiltratívny rastový charakter, má zvýšenú proliferačnú aktivitu a obsahuje aspoň sporadické mitózy [8,9].
Záver
Propagácia adenomyózy v krvných cievach maternice je zriedkavý histologický nález, ktorý spôsobuje diagnostické rozpaky, pretože pripomína intravaskulárne šírenie malígnej neoplázie. Hoci nejde o nádorové ochorenie, v onkopatologickej praxi predstavuje významnú diferenciálnu diagnózu. Vedomosť bioptika o tomto fenoméne je kľúčová, aby sa predišlo zámene za vaskulárnu disemináciu malignity. Vždy je nutné extenzívne spracovanie tkaniva resekátu na odhalenie prípadnej malignity, či už v endometriu, alebo v samotných ložiskách adenomyózy.
Zdroje
1. Plevová P, Hladíková A, Tesařová M. Hereditární leiomyomatóza a renální karcinom – HLRCC/mnohopočetná kožní a děložní leiomyomatóza – MCUL. Klin Onkol 2012; 25 (Suppl): S55–S58.
2. Dudková S, Štork J, Kodet O. Klinický případ: bolestivé noduly na zádech. Čes-slov Derm 2017; (92) 4 : 184–188.
3. Křepelová A. Dědičné formy nádoru ledvin – spektrum predispozičních genu a jejich testování. Klin Onkol 2006; 19 (Suppl): 82–84.
4. Batra N, Rekhi B, Menon S et al. An octad of fumarate hydratase-deficient uterine leiomyomas: case series with review of literature from a single institution. Indian J Pathol Microbiol 2025; 68 (1): 69–78.
5. Reitzenstein M. Endometriose „unterwegs“. Fallbeschreibung einer intravasalen endometriose. Gebunsh. u. Frauenheilk 1984; 44 : 516–517
6. Hernández MA, Estrada HR, Estrada MI et al. Tejido endometrial en vasos del miometrio. Comunicación de dos casos y revisión de la bibliografía. Ginecol Obstet Mex 2008; 76 (4): 228–232.
7. Sahin AA, Silvia EG, Landon G et al. Endometrial tissue in myometrial vessels not associated with menstruation. Int J Gynecol Pathol 1989; 8 (2): 139–146. doi: 10.1097/00004347-198906000-00007.
8. Meenakshki M, McCluggage WG. Vascular involvement in adenomyosis: report of a large series of a common phenomenon with observations on the pathogenesis of adenomyosis. Int J Gynecol Pathol 2010; 29 (2): 117–121. doi: 10.1097/PGP.0b013e3181b7018d.
9. Pérez Buendía J, Marín Sánchez MP, Guijarro Campillo AR et al. Intravascular involvement in adenomyosis: an endometriosis dissemination pathway? [online]. Available from: https: //www.sciencerepository.org/intravascular-involvement-in_IJSCR-2023-1-103.
10. Lacheta J. Děložní adenomyóza: patogeneze, diagnostika, symptomatologie a léčba. Čes Gynekol 2019; 84 (3): 240–246.
11. Souza Filho MLP, Costa TP, Freitas Junior NP et al. The many faces of endometriosis. Autops Case Rep 2022; 12: e2021409. doi: 10.4322/acr.2021.409.
12. Ooi K, Valentine R. Intravascular endometrial tissue in an ovary of a patient with abnormal endometrial histology. Pathology 1994; 26 (2): 212–214. doi: 10.1080/00313029400169501.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článek Není ct jako CT
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2026 Číslo 2- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Fixní kombinace tramadol/paracetamol je doporučenou volbou v léčbě chronické bolesti v ordinaci praktického lékaře
-
Všetky články tohto čísla
- Není ct jako CT
- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- Intravaskulárna propagácia adenomyózy v krvných cievach myometria a uterinného leiomyómu u pacientky s mutáciou génu fumaráthydratázy – zriedkavý nález imitujúci malígnu neopláziu
- Second recurrence of breast cancer 36 years after initial surgery and 18 years after the first recurrence – an extremely rare case
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
- Cancer patients admitted to intensive care unit
- Nádory GIT – chemoterapie a precizní léčba se synergicky doplňují
- Snižování škod rizikového chování v onkologické prevenci
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



