-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Výsledky léčby Hodgkinova lymfomu v České republice
Treatment outcomes of Hodgkin lymphoma in the Czech Republic
Background: The aim of this analysis was to assess the efficacy of treatment and its impact on prognosis of patients with Hodgkin’s lymphoma (HL) enrolled in the Czech HL Registry. Patients and methods: Overall 2,241 patients with classical HL (cHL) and 130 patients with nodular lymphocyte-predominant Hodgkin lymphoma (NLPHL) treated between 2000 and 2024 were analyzed. Median age at diagnosis was 37 years in cHL and 42 years in NLPHL. Results: The most common chemotherapy regimen in early and intermediate stages was ABVD (doxorubicin, bleomycin, vinblastine, dacarbazine) in combination with radiotherapy (RT). Moreover, two cycles of escalated BEACOPP (bleomycin, etoposide doxorubicin, cyclophosphamide, vincristine, procarbazine, prednisone) combined with two cycles of ABVD and RT were used in patients aged < 60 years in intermediate stages. The most common therapy in advanced stages was escalated BEACOPP (4–8 cycles) in patients aged < 60 years and ABVD (6–8 cycles) in patients aged ≥ 60 years. Patients with NLPHL were treated with RT alone or with combination of rituximab and chemotherapy or with a combination of RT based on clinical stages. The 10-year progression–free survival (PFS) and overall survival (OS) in patients with cHL aged < 60 years were: in early stages 91.5% and 94.2%, in intermediate stages 91.0% and 96.6% and in advanced stages 83.9% and 92.6%, respectively. The 10-year PFS and OS in cHL ≥ 60 years were: in early stages 67.0% and 74.2%, in intermediate stages 36.4% and 45.7%, in advanced stages 41.6% and 52.0%, respectively. The 10-year PFS and OS in NLPHL patients were 77.5% and 95.8%. Conclusion: Based on the data from the Czech HL Registry, the prognosis of HL patients aged < 60 years is excellent: the 10-year OS is achieved in more than 90% of cases. Median OS of patients aged ≥ 60 years is 10 years. Implementation of checkpoint inhibitors or brentuximab vedotin into the first-line treatment will further improve its efficacy and reduce the toxicity.
Keywords:
Hodgkin lymphoma – ABVD – BEACOPP
Autori: H. Móciková; J. Michalka; A. Sýkorová; M. Lukášová; K. Hradská; N. Černá; J. Baranová; J. Marková; Ľ. Gahérová; M. Maco; E. Maule; A. Janíková; P. Štěpánková; A. Kredátusová; J. Ďuraš; V. Procházka; Z. Král; T. Kozák
Pôsobisko autorov: Hematologická klinika 3. LF UK a FN Královské Vinohrady, Praha 1; Interní hematologická a onkologická klinika LF MU a FN Brno 2; IV. interní hematologická klinika LF v Hradci Králové UK a FN Hradec Králové 3; Hematoonkologická klinika LF UP a FN Olomouc 4; Klinika hematoonkologie LF OU a FN Ostrava 5; Institut biostatistiky a analýz, s. r. o, Brno 6
Vyšlo v časopise: Klin Onkol 2026; 39(1): 45-55
Kategória: Původní práce
doi: https://doi.org/10.48095/ccko202645Súhrn
Východiska: Cílem analýzy bylo vyhodnocení účinnosti léčby a jejího vlivu na prognózu pacientů s Hodgkinovým lymfomem (HL) zařazených do českého registru HL. Soubor pacientů a metody: Do analýzy bylo zařazeno 2 241 hodnotitelných pacientů s klasickým HL (cHL) a 130 pacientů s HL s nodulární lymfocytární predominancí (nodular lymphocyte-predominant Hodgkin lymphoma – NLPHL), kteří byli léčeni v letech 2000–2024. Medián věku při diagnóze cHL byl 37 let a u NLPHL 42 let. Výsledky: Nejčastějším režimem u pacientů v časných a intermediárních stadiích byl režim ABVD (doxorubicin, bleomycin, vinblastin, dakarbazin) s radioterapií (RT), navíc u pacientů ve věku < 60 let v intermediárních stadiích byly použity dva cykly eskalovaného režimu BEACOPP (bleomycin, etoposid, doxorubicin, cyklofosfamid, vinkristin, prokarbazin, prednison) v kombinaci s dvěma cykly ABVD a RT. V pokročilém stadiu byl u pacientů ve věku < 60 let nejčastěji použit eskalovaný režim BEACOPP (4–8 cyklů) a u pacientů ve věku ≥ 60 let režim ABVD (6–8 cyklů). U pacientů s NLPHL byla použita dle klinického stadia samostatná RT nebo kombinace rituximabu s chemoterapií +/−RT. U pacientů s cHL ve věku < 60 let bylo 10leté přežití bez progrese (progression free survival – PFS) a celkové přežití (overall survival – OS) v iniciálních stadiích 91,5 % a 94,2 %, v intermediárních stadiích 91,0 % a 96,6 % a v pokročilých stadiích 83,9 % a 92,6 %. U cHL ve věku ≥ 60 let bylo 10leté PFS a OS v iniciálních stadiích 67,0 % a 74,2 %, v intermediárních stadiích 36,4 % a 45,7 %, v pokročilých stadiích 41,6 % a 52,0 %. U NLPHL bylo 10leté PFS a OS 77,5 % a 95,8 %. Závěr: Podle dat z registru je prognóza HL výborná u pacientů ve věku < 60 let – 10letého OS dosahuje více než 90 % pacientů. Ve věku ≥ 60 let je medián přežití kolem 10 let. Zavedení checkpoint inhibitorů a brentuximab vedotinu do 1. linie léčby dále zlepší účinnost a sníží toxicitu léčby.
Klíčová slova:
Hodgkinův lymfom – ABVD – BEACOPP
Úvod
Registr Hodgkinova lymfomu prospektivně sbírá a vyhodnocuje prognostické faktory a léčbu pacientů s Hodgkinovým lymfomem (HL) v České republice (ČR). Do registru jsou zahrnuta data z pěti center v ČR (Hematologická klinika FN Královské Vinohrady Praha, Interní hematologická a onkologická klinika FN Brno, Interní hematologická klinika FN Hradec Králové, Hematoonkologická klinika FN Olomouc a Klinika hematoonkologie FN Ostrava), která jsou vedena v databázi Institutu biostatistiky a analýz, s. r. o. Cílem této analýzy bylo vyhodnocení účinnosti léčby a její vliv na dlouhodobé přežití pacientů s HL. V současnosti se zkoumá význam cirkulující nádorové DNA pro biologii cHL a NLPHL při diagnóze a v relapsu, dále pro sledování minimální reziduální nemoci v průběhu léčby a po léčbě. K úspěšné léčbě HL v ČR významně přispěla spolupráce s Německou studijní skupinou Hodgkinova lymfomu (German Hodgkin Study Group – GHSG), která umožnila aktivní zapojení hematologických klinik z Prahy a z Brna do mezinárodních randomizovaných studií GHSG fáze III. Proto i léčba všech klinických stadií byla vedena převážně podle výsledků klinických studií GHSG.
Pacienti a metody
Všichni pacienti podepsali informovaný souhlas s účastí v registru Hodgkinova lymfomu včetně sběru dat a statistických analýz, který byl schválen multicentrickou etickou komisí ve Fakultní nemocnici Královské Vinohrady v Praze. Tato analýza byla provedena v souladu s Helsinskou deklarací. Histologické nálezy byly potvrzeny čtením v referenčních ústavech patologie ČR. Z celkového počtu 2 800 pacientů bylo do analýzy zařazeno 2 241 pacientů s cHL (80,0 %) a 130 pacientů s NLPHL (4,6 %) s vyplněnými formuláři, kteří byli léčeni v letech 2000–2024. Medián věku při diagnóze byl 37 let (rozmezí 18–91) u cHL a 42 let (rozmezí 18–76) u NLPHL.
Standardní diagnostický postup zahrnoval fyzikální a laboratorní vyšetření, pozitronovou emisní tomografii v kombinaci s počítačovou tomografií (PET/CT) nebo samostatné CT krku, hrudníku, břicha a malé pánve. V rámci určení klinického stadia po zavedení PET/CT se od roku 2014 upustilo od rutinního vyšetření kostní dřeně [1]. Charakteristiky pacientů cHL a NLPHL jsou uvedeny v tab. 1 a 2.
Tab. 1. Charakteristika pacientů s klasickým Hodgkinovým lymfomem. 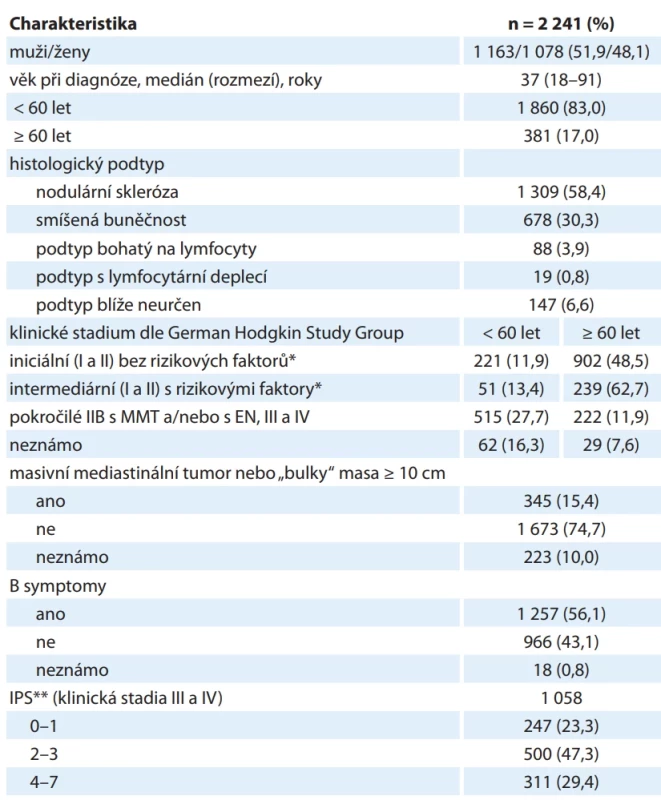
*rizikové faktory: masivní mediastinální tumor (MMT) > 1/3 průměru hrudníku nebo mediastinální masa > 10 cm, extranodální postižení (EN), FW > 50 mm/h (bez B symptomů) nebo FW > 30 mm/h (s B symptomy); **Mezinárodní prognostické skóre
(IPS): albumin v séru < 40 g/l, Hb < 105 g/l, mužské pohlaví, klinické stadium IV, věk > 45 let, leukocyty > 15×109 /l, lymfocyty < 0,6×109 /l nebo < 8 % z leukocytůTab. 2. Charakteristika pacientů s Hodgkinovým lymfomem s nodulární lymfocytární predominancí. 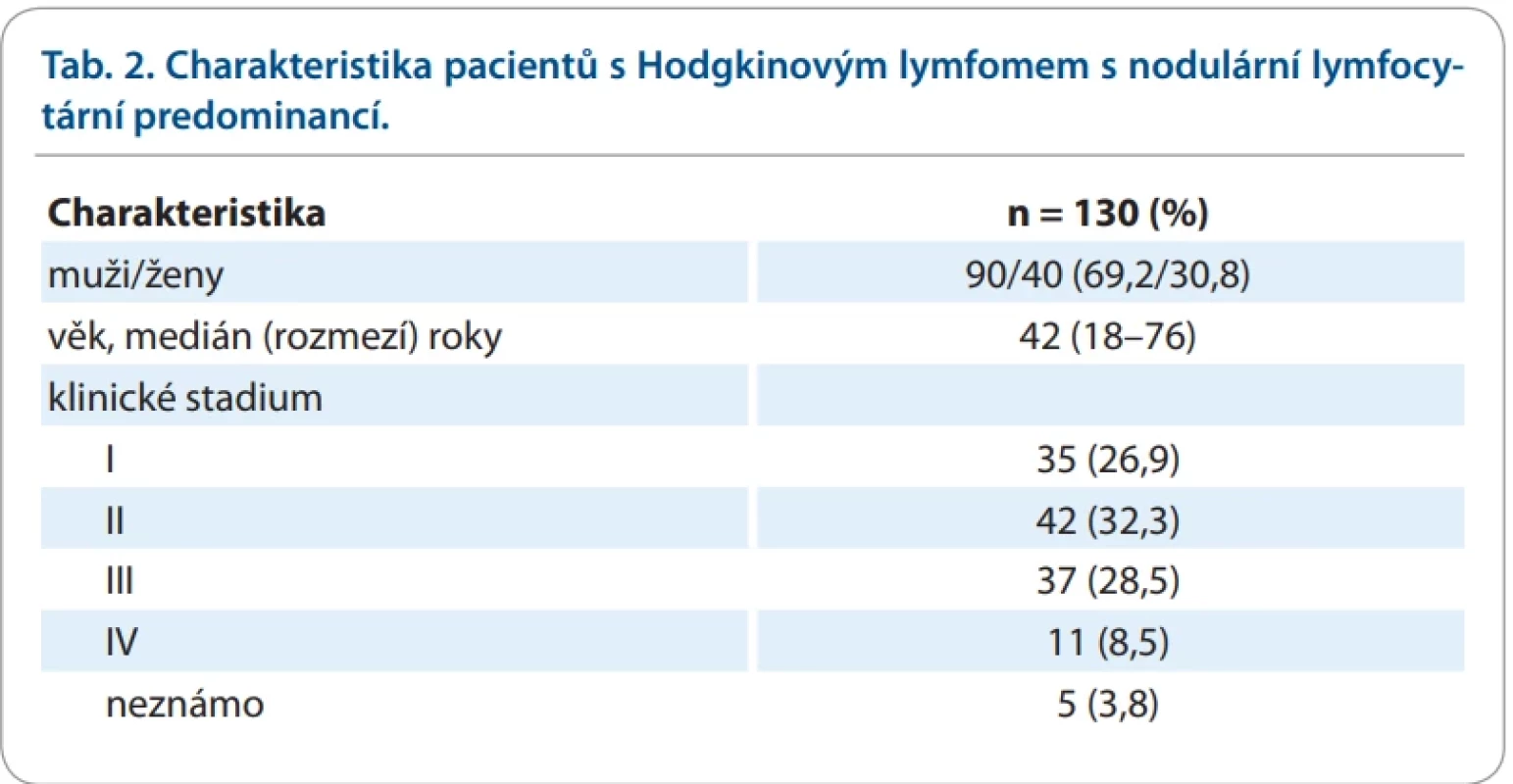
Do iniciálních stadií byli zařazeni pacienti v klinickém stadiu I nebo II bez rizikových faktorů. Do intermediárních stadií byli zařazeni pacienti v klinickém stadiu I nebo II s rizikovými faktory: masivní mediastinální tumor (> třetina průměru hrudníku) nebo extranodální postižení, postižení ≥ tří oblastí lymfatických uzlin, vysoká sedimentace (> 30 mm/h s B symptomy, > 50 mm/h bez B symptomů). Výjimku tvořili pacienti v klinickém stadiu IIB s masivním mediastinálním tumorem a/nebo s extranodálním postižením, dále pacienti s nádorovou masou o velikosti ≥ 10 cm, kteří byli zařazeni do pokročilých stadií. Pacienti v klinickém stadiu III nebo IV byli zařazeni do pokročilých stadií. Mezinárodní prognostické skóre (IPS) pro pacienty v pokročilém stadiu III a IV je uvedeno v tab. 1.
Odpověď na léčbu (kompletní remise, parciální remise, stabilní nemoc, progrese) byla hodnocena po ukončení léčby podle Chesonových kritérií z let 1999, 2007 a od roku 2014 podle Luganské klasifikace [1–3].
Přežití bez progrese (progression-free survival – PFS) bylo definováno jako časový interval od data zahájení 1. linie léčby do data relapsu/progrese nebo data úmrtí z jakékoliv příčiny. Celkové přežití (overall survival – OS) bylo hodnoceno od data diagnózy do data posledního sledování nebo do úmrtí z jakékoliv příčiny. Křivky přežití byly odhadnuty Kaplan-Meierovou metodou a porovnání mezi podskupinami bylo provedeno pomocí log-rank testu.
Výsledky
První linie léčby
Medián sledování pacientů s cHL byl 146 měsíců. Podle registru HL v ČR v letech 2000–2024 bylo celkem 272 pacientů léčeno pro iniciální stadia cHL, z toho 221 pacientů ve věku < 60 let a 51 pacientů ve věku ≥ 60 let. Podaná chemoterapie, RT a odpovědi na léčbu jsou uvedeny v grafech 1a,b. Desetileté PFS u pacientů v věku < 60 let bylo 91,5 % (95% interval spolehlivosti (IS) 87,1–96,0) a ve věku ≥ 60 let 67,0 % (95% IS 52,5–85,6) (graf 2a). Desetileté OS u pacientů ve věku < 60 let bylo 94,2 % (95% IS 90,2–98,4) a ve věku ≥ 60 let 74,2 % (95% IS 60,4–91,3) (graf 3a).
Graf 1a. Iniciální stadia – léčba pacientů ve věku < 60 let (n = 221). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1b. Iniciální stadia – léčba pacientů ve věku ≥ 60 let (n = 51). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1c. Intermediární stadia – léčba pacientů ve věku < 60 let (n = 515). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1d. Intermediární stadia – léčba pacientů ve věku ≥ 60 let (n = 62). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1e. Pokročilá stadia – BEACOPPesk.+ modifi kace a kombinace a jiné (n = 809 pacientů ve věku < 60 let). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese, PR
– parciální remise, SD – stabilní nemocGraf 1f. Pokročilá stadia – ABVD + modifi kace a kombinace (n = 93 pacientů ve věku ≥ 60 let). 
CHT – chemoterapie, RT – radioterapie Graf 1g. Pokročilá stadia – léčba pacientů ve věku ≥ 60 let. 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese, PR – parciální remise,
RT – radioterapie, SD – stabilní nemocGraf 2a. Klasický Hodgkinův lymfom – PFS dle věku a klinického stadia. 
Analýza z let 2000–2024 (n = 2 241).
GHSG – German Hodgkin Study Group, KS – klinické stadiumGraf 2b. Pokročilé stadium klasického Hodgkinova lymfomu u pacientů ve věku < 60 let – přežití bez progrese dle chemoterapie v 1. linii. 
Analýza z let 2000–2024.
CHT – chemoterapiePro intermediární stadia cHL s výjimkou stadia IIB s masivním mediastinálním tumorem a/nebo s extranodálním postižením bylo ve výše uvedeném období léčeno 515 pacientů ve věku < 60 let a 62 pacientů ve věku ≥ 60 let. Podaná chemoterapie, RT a odpovědi na léčbu jsou uvedeny v grafech 1c,d. Desetileté PFS u pacientů ve věku < 60 let bylo 91,0 % (95% IS 88,2–93,9) a ve věku ≥ 60 let 36,4 % (95% IS 22,1–60,0) (graf 2a). Desetileté OS u pacientů ve věku < 60 let bylo 96,6 % (95% IS 94,7–98,6) a ve věku ≥ 60 let 45,7 % (95% IS 29,5–70,6) (graf 3a).
Pro pokročilá stadia cHL (stadia IIB s masivním mediastinálním tumorem a/nebo s extranodálním postižením, stadia III a IV) bylo ve výše uvedeném období léčeno 902 pacientů ve věku < 60 let a 239 pacientů ve věku ≥ 60 let. Podaná chemoterapie, RT a odpovědi na léčbu jsou uvedeny v grafech 1e – g. Desetileté PFS u pacientů ve věku < 60 let bylo 83,9 % (95% IS 81,1–86,8) a ve věku ≥ 60 let 41,6 % (95% IS 33,0–52,4) (graf 2a). Desetileté OS u pacientů ve věku < 60 let bylo 92,6 % (95% IS 90,5–94,8) a ve věku ≥ 60 let 52,0 % (95% IS 43,0–63,0) (graf 3a). PFS u pacientů ve věku < 60 let bylo signifikantně delší po léčbě eskalovaným BEACOPP oproti režimu ABVD či kombinaci (p = 0,011) (graf 2b). Rovněž bylo signifikantně delší OS u pacientů ve věku < 60 let po léčbě eskalovaným BEACOPP oproti režimu ABVD (p < 0,001) (graf 3b).
Medián sledování u pacientů s NLPHL byl 7,9 roku. Ze 130 pacientů s NLPHL bylo léčeno 118 pacientů RT nebo kombinací chemoterapie s rituximabem +/ − RT, u dalších 12 pacientů nebyla léčba zadána do registru HL. Způsob léčby a odpověď na léčbu u NLPHL jsou uvedeny v grafu 4. Z hlediska prognózy bylo vyhodnoceno celkem 110 pacientů. Pětileté a 10leté PFS bylo 84,2 % (95% IS 76,9–92,2) a 77,5 % (95% IS 68,4–87,7). Pětileté a 10leté OS bylo 98,2 % (95% IS 95,7–100,0) a 95,8 % (95% IS 91,8–100,0).
Graf 3a. Klasický Hodgkinův lymfom – celkové přežití dle věku a klinického stadia. 
Analýza z let 2000–2024 (n = 2 241).
GHSG – German Hodgkin Study Group, KS – klinické stadiumGraf 3b. Pokročilé stadium klasického Hodgkinova lymfomu u pacientů ve věku < 60 let – celkové přežití dle chemoterapie v 1. linii. 
Analýza z let 2000–2024.
CHT – chemoterapieGraf 4. Léčba pacientů s Hodgkinovým lymfomem s nodulární lymfocytární predominancí (n = 118). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese, PR – parciální remise, SD – stabilní nemoc Léčba relapsu
Medián sledování u relabovaných pacientů od data relapsu byl 7,6 roku. Podle dat v registru HL bylo v období od 2000 do 2023 vyhodnoceno 268 pacientů s relapsem HL, z nich 233 bylo ve věku≤ 65 let a 35 pacientů ve věku > 65 let. Medián OS u pacientů ve věku ≤ 65 let nebyl dosažen, 5leté OS bylo 75,2 % (95 % IS 69,4–81,6), naproti tomu signifikantně kratší bylo přežití u pacientů ve věku > 65 let: medián OS byl 1,3 roku (95 % IS 0,9–nedosaženo; p < 0,001) a 5leté OS bylo 24,6 % (95 % IS 11,5–52,5). Z 233 pacientů ve věku ≤ 65 let bylo léčeno vysokodávkovanou chemoterapií s následnou autologní transplantací kmenových buněk (autologous stem cell transplant – ASCT) 131 (56 %) pacientů. Pětileté OS od data relapsu je významně lepší u pacientů ve věku ≤ 65 let, kteří dostali ASCT, oproti těm, kteří ASCT nepodstoupili: 82,7 % (95% IS 75,7–90,4) vs. 65,8 % (95% IS 56,6–76,5), p = 0,008; hazard ratio (HR) 1,96 (95% IS 1,18–3,28).
Nivolumab byl podán v relapsu cHL u 44 pacientů, charakteristiky pacientů a odpovědi na léčbu uvádí tab. 3. Medián sledování od zahájení nivolumabu byl 38,6 měsíce. Medián, 2leté a 5leté PFS byly 13,5 měsíce, 30,5 % a 5,7 % (graf 5). Medián, 2leté a 5leté OS byly 58,8 měsíce, 77,4 % a 37,5 % (graf 5).
Tab. 3. Charakteristika pacientů léčených nivolumabem a léčebná odpověď na nivolumab. 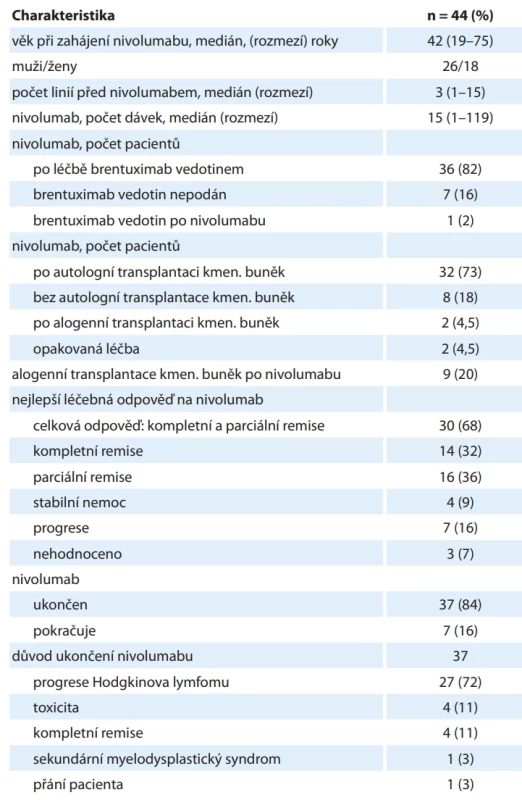
Graf 5. Přežití bez progrese a celkové přežití při léčbě nivolumabem u pacientů s relapsem klasického Hodgkinova lymfomu. 
OS – celkové přežití, PFS – přežití bez progrese Pembrolizumab byl podán v relapsu cHL u 48 pacientů, charakteristiky pacientů a odpovědi na léčbu uvádí tab. 4. Medián sledování od zahájení léčby pembrolizumabem byl 11,5 měsíce. Medián, 2leté a 5leté PFS byly 16,5 měsíce, 33,5 % a 26,8 % (graf 6). Dvouleté a 5leté OS byly 83,3 % a 77,3 %, mediánu nebylo dosaženo (graf 6).
Tab. 4. Charakteristika pacientů léčených pembrolizumabem a léčebná odpověď na pembrolizumab. 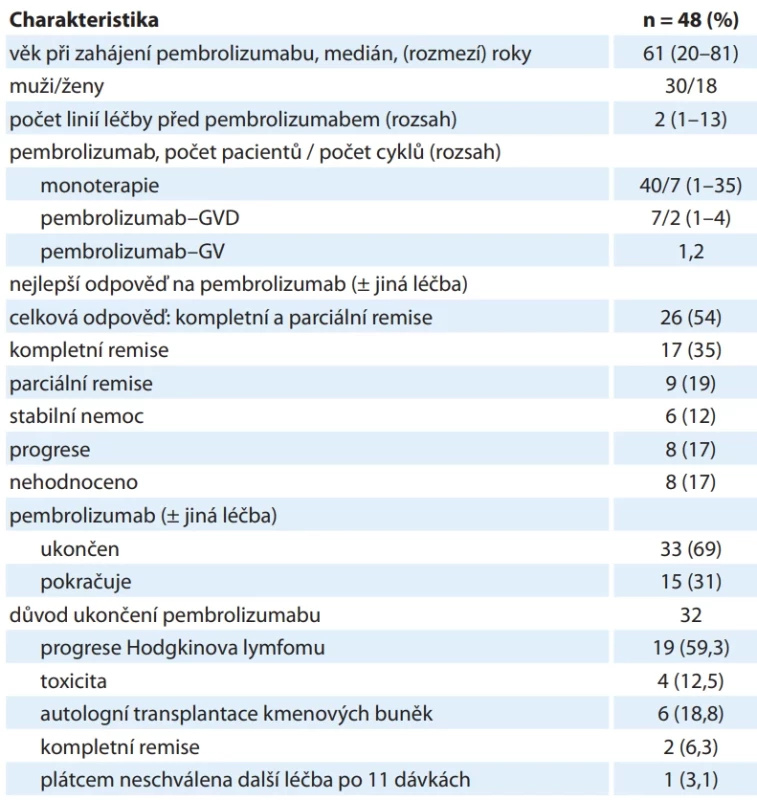
GVD – gemcitabin, vinorelbin, lipozomální doxorubicin Graf 6. Celkové přežití a přežití bez progrese při léčbě pembrolizumabem u pacientů s relapsem klasického Hodgkinova lymfomu. 
OS – celkové přežití, PFS – přežití bez progrese Diskuze
Desetileté výsledky PFS a OS v našem souboru pacientů v iniciálním stadiu ve věku < 60 let jsou srovnatelné s výsledky studie pro iniciální stadia GHSG HD10 : 87,2 % a 94,1 % [4,5]. Desetileté PFS a OS u našich pacientů z registru HL ve věku ≥ 60 let byly horší, což odpovídá obecně horší prognóze starších pacientů s nutností redukce chemoterapie vzhledem ke komorbiditám. Z analýzy studií GHSG HD10 a HD13 pro iniciální stadia vyplynulo, že u starších pacientů je nutné vysadit bleomycin po dvou cyklech ABVD, aby se zabránilo vzniku plicní toxicity a zvýšenému riziku úmrtí na ni [6,7]. Snahy o vynechání RT po dvou cyklech ABVD u PET-2 negativních pacientů ve studii GHSG HD16 pro iniciální stadia [8,9] vedly k významné ztrátě účinnosti, proto aktuálním standardem léčby v ČR pro tuto skupinu pacientů v iniciálním stadiu zůstávají dva cykly ABVD a „involved site“ RT (ISRT) 20 Gy [10].
V GHSG studii HD11 pro intermediární stadia byly nejlepší výsledky dosaženy čtyřmi cykly ABVD + 30 Gy „involved field“ RT (IFRT). Tato kombinace měla 10leté PFS a OS 83,3 % a 90,9 % [5,11]. Ve studii GHSG HD14 pro intermediární stadia byly nejlepší výsledky dosaženy u pacientů ve věku < 60 let kombinací dvou cyklů eskalovaného BEACOPP + dvou cyklů ABVD + 30 Gy IFRT [12]: 10leté PFS bylo 91,2 % a OS 94,1 % [13]. Výše uvedené režimy byly nejčastěji podány i v kohortě našich pacientů v intermediárním stadiu, proto 10leté výsledky PFS a OS u pacientů ve věku < 60 let byly srovnatelné s uvedenými podskupinami pacientů ve studiích HD11 a HD14. Obdobně jako u časných stadií i u intermediárních stadií ve věkové skupině ≥ 60 let, která byla léčena převážně režimem ABVD a jeho modifikacemi, bylo 10leté PFS a OS horší oproti populaci ve věku < 60 let. Současným standardem léčby v ČR u pacientů v intermediárním stadiu ve věku < 60 let je podání dvou cyklů eskalovaného BEACOPP a dvou cyklů ABVD, po kterých je možné vynechat RT u těch pacientů, kteří podle studie GHSG HD17 dosáhli PET-4 negativní kompletní remise [14]. U pacientů ve věkové skupině ≥ 60 let je v ČR indikováno podání dvou cyklů ABVD + dvou cyklů AVD a 30 Gy ISRT [10].
Studie GHSG HD9 s úspěchem zavedla do léčby cHL v pokročilém stadiu ve věku < 60 let eskalovaný BEACOPP [15]. Další studie GHSG HD12, HD15, HD18 postupně snížily počet cyklů z osmi na čtyři u pacientů s negativním PET po dvou cyklech chemoterapie a umožnily vynechání RT u pacientů, kteří dosáhli PET negativní kompletní remise po ukončení chemoterapie [16–19]. Intenzifikace léčby u PET-2 pozitivních pacientů přidáním rituximabu k eskalovanému BEACOPP nezlepšila 3leté PFS [18,19]. Pětileté výsledky PFS a OS všech pacientů v registru HL v pokročilých stadiích ve věku < 60 let a zejména těch, kteří byli léčeni eskalovaným BEACOPP (90,7 % a 96,9 %), jsou srovnatelné se studiemi GHSG HD15 a HD18. Podle českého registru HL PFS u pacientů v pokročilém stadiu ve věku < 60 let bylo signifikantně delší po léčbě eskalovaným BEACOPP (4–8 cyklů) oproti 6–8 cyklům ABVD (p = 0,011). Rovněž bylo signifikantně delší OS u našich pacientů ve věku < 60 let po léčbě eskalovaným BEACOPP oproti režimu ABVD (p < 0,001). Čtyřleté výsledky studie GHSG HD21 prokázaly, že režim BRECADD (brentuximab vedotin, etoposid, cyklofosfamid, doxorubicin, dakarbazin, dexametazon) je ještě účinnější a má méně nežádoucích účinků oproti režimu eskalovaný BEACOPP (4leté PFS 94,3 % vs. 90,9 %, hazard ratio 0,66 a 4leté OS 98,6 % vs. 98,2 %), proto je 4/6 cyklů BRECADD jedním ze současných standardů léčby v 1. linii u pokročilých stadií v ČR a jeho použití v běžné praxi bylo již zahájeno [10,20]. Podle dat z registru HL jsou 10leté výsledky PFS a OS u pacientů v pokročilém stadiu ve věku ≥ 60 let na léčbě ABVD a jeho modifikacích neuspokojivé. Studie SWOG S1826 prokázala u pacientů ve věku ≥ 12 let včetně populace ≥ 60 let v pokročilých stadiích III a IV, že šest cyklů léčby nivolumabu v kombinaci s AVD (N-AVD) je účinnější než šest cyklů brentuximab vedotinu v kombinaci s AVD (BV-AVD) [21]: 2leté PFS bylo 92 % po N-AVD ve srovnání s 83 % po BV-AVD (HR 0,45). Režim N-AVD je rovněž jedním ze současných standardů léčby v ČR u pacientů v klinickém stadiu III nebo IV, který se aktuálně již používá u pacientů zejména ve věku ≥ 60 let [10].
Na základě RNA sekvenování a cirkulující nádorové DNA byly definovány tři lymfocytárně predominantní ekotypy NLPHL (LPE): LPE1 a LPE2 byly charakterizovány imunosupresivním mikroprostředím s vysokou expresí B2M na nádorových buňkách, vyčerpáním CD8 T lymfocytů a lepším PFS ve srovnání s LPE3 [22]. K základní kohortě (n = 109, 65 % LPE1/2) byla ve validační kohortě (n = 62, 61 % LPE1/2) použita data a vzorky od 62 pacientů s NLPHL z českého registru HL. Ve srovnání s literaturou, kde je medián věku u pacientů s NLPHL uveden v rozmezí 35–40 let [23], je medián věku pacientů v registru HL vyšší – 42 let. V naší hodnocené kohortě 130 pacientů převažují muži, ale podíl klinických stadií I a II je nižší (59,2 %) oproti literatuře (75 %) [23]. Pouze 7 pacientů absolvovalo chirurgickou exstirpaci bez další léčby a 23 pacientů v časném stadiu IA mělo samostatnou RT 30 Gy [24]. Nejčastější použitou chemoterapií v pokročilých stadiích byl R-C (H) OP (rituximab, cyklofosfamid, doxorubicin, vinkristin, prednison) s RT, nebo bez ní (41 pacientů) [25,26]. Podle sledování v registru HL mají pacienti s NLPHL v souladu s literaturou velmi dobrou prognózu, což dokládají 5leté a 10leté výsledky PFS a OS.
Standardem léčby relapsu klasického HL ve věku ≤ 65 let zůstává záchranná chemoterapie s následnou vysokodávkovanou chemoterapií a ASCT. Data z registru HL potvrzují lepší OS u pacientů ve věku ≤ 65 let, pokud měli provedenou ASCT, ve srovnání s pacienty bez ASCT. Podle registru European Bone Marrow Transplantation (EBMT) byla v ČR v letech 2020–2024 provedena ASCT u 122 pacientů s HL (v průměru 24 ASCT ročně). U pacientů s vysokým rizikem dalšího relapsu se podává konsolidace brentuximab vedotinem à 3 týdny do maximálního počtu 16 cyklů [27]. Retrospektivní analýzy léčby brentuximab vedotinem u relabovaných nebo refrakterních pacientů s cHL včetně konsolidace po ASCT s využitím dat z českého registru HL byly již publikovány [28–30], proto nejsou předmětem tohoto sdělení. Ve druhém relapsu po ASCT se i podle českých standardních doporučení podává checkpoint inhibitor nivolumab do relapsu [10,31]. V relapsu bylo v naší kohortě odléčeno nivolumabem 44 pacientů, z nich 32 % dosáhlo kompletní remise a celkové odpovědi 68 %. Podíl remisí byl u našich pacientů vyšší oproti studii CheckMate-205 (21 % a 71 %), ale 5leté PFS (5,7 %) a OS (37,5 %) byly v naší neselektované kohortě pacientů horší oproti studii CheckMate-205 (17,9 % a 66,6 %). U pacientů nevhodných k ASCT je podle aktuálních standardních doporučení ve druhém relapsu indikován checkpoint inhibitor pembrolizumab [10,32,33], který se podává do celkového počtu 35 cyklů. Pembrolizumab byl použit v relapsu u 48 pacientů, z nich 35 % dosáhlo kompletní remise a celkové odpovědi 54 % (ve studii Keynote 087 kompletní remise 27,6 % a celková odpověď 71 %). Pětileté PFS (26,8 %) a OS (77,3 %) u naší kohorty pacientů jsou srovnatelné se studií Keynote 087 (14,2 % a 70,7 %).
Závěr
Data z registru HL potvrzují dlouhodobě velmi dobrou prognózu: 10leté přežití dosahuje až 90 % pacientů ve věku < 60 let a pacienti věkové skupiny ≥ 60 let mají medián přežití kolem 10 let. Se zavedením nových léčebných možnosti jako je BRECADD a N-AVD se očekává snížení toxicity a zvýšení účinnosti léčby zejména u pacientů ve věku ≥ 60 let. V relapsu zůstává standardem léčby u mladších pacientů ASCT. V relapsu jsou účinné léky jako nivolumab, pembrolizumab nebo brentuximab vedotin.
Poděkování
Tato práce byla realizována za podpory Agentury pro zdravotnický výzkum MZ ČR NU22-03-00182, za podpory programu Cooperatio – výzkumná oblast onkologie a hematologie a za podpory MH CZ – DRO (FNOL, 00098892).
Zdroje
1. Cheson BD, Fisher RI, Barrington SF et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol 2014; 32 (27): 3059–3068. doi: 10.1200/JCO.2013.54.8800.
2. Cheson BD, Horning SJ, Coiffier B et al. Report of an international workshop to standardize response criteria for non-Hodgkin’s lymphomas. NCI Sponsored International Working Group. J Clin Oncol 1999; 17 (4): 1244. doi: 10.1200/JCO.1999.17.4.1244.
3. Cheson BD, Pfistner B, Juweid ME et al. Revised response criteria for malignant lymphoma. J Clin Oncol 2007; 25 (5): 579–586. doi: 10.1200/JCO.2006.09.2403.
4. Engert A, Plütschow A, Eich HT et al. Reduced treatment intensity in patients with early-stage Hodgkin‘s lymphoma. N Engl J Med 2010; 363 (7): 640–652. doi: 10.1056/NEJMoa1000067.
5. Sasse S, Bröckelmann PJ, Goergen H et al. Long-term follow-up of contemporary treatment in early-stage Hodgkin lymphoma: updated analyses of the German Hodgkin study group HD7, HD8, HD10, and HD11 trials. J Clin Oncol 2017; 35 (18): 1999–2007. doi: 10.1200/JCO.2016.70.9410.
6. Behringer K, Goergen H, Hitz F et al. Omission of dacarbazine or bleomycin, or both, from the ABVD regimen in treatment of early-stage favourable Hodgkin‘s lymphoma (GHSG HD13): an open-label, randomised, non--inferiority trial. Lancet 2015; 385 (9976): 1418–1427. doi: 10.1016/S0140-6736 (14) 61469-0.
7. Böll B, Goergen H, Behringer K et al. Bleomycin in older early-stage favorable Hodgkin lymphoma patients: analysis of the German Hodgkin Study Group (GHSG) HD10 and HD13 trials. Blood 2016; 127 (18): 2189–2192. doi: 10.1182/blood-2015-11-681064.
8. Fuchs M, Goergen H, Kobe C et al. Positron emission tomography-guided treatment in early-stage favorable Hodgkin lymphoma: final results of the International, randomized phase III HD16 trial by the German Hodgkin Study Group. J Clin Oncol 2019; 37 (31): 2835–2845. doi: 10.1200/JCO.19.00964.
9. Fuchs M, Jacob AS, Kaul H et al. Follow-up of the GHSG HD16 trial of PET-guided treatment in early-stage favorable Hodgkin lymphoma. Leukemia 2024; 38 (1): 160–167. doi: 10.1038/s41375-023-02064-y.
10. Belada D, Trněný M. Diagnostické a léčebné postupy u nemocných s maligními lymfomy. XV. Vydání. 2025 [online]. Dostupné z: https: //www.lymphoma.cz/_uploads/attachments/KLS_guidelines_2025_31579.pdf.
11. Eich HT, Diehl V, Görgen H et al. Intensified chemotherapy and dose-reduced involved-field radiotherapy in patients with early unfavorable Hodgkin‘s lymphoma: final analysis of the German Hodgkin Study Group HD11 trial. J Clin Oncol 2010; 28 (27): 4199–4206. doi: 10.1200/JCO.2010.29.8018.
12. von Tresckow B, Plütschow A, Fuchs M et al. Dose--intensification in early unfavorable Hodgkin‘s lymphoma: final analysis of the German Hodgkin Study Group HD14 trial. J Clin Oncol 2012; 30 (9): 907–913. doi: 10.1200/JCO.2011.38.5807.
13. Gillessen S, Plütschow A, Fuchs M et al. Intensified treatment of patients with early stage, unfavourable Hodgkin lymphoma: long-term follow-up of a randomised, international phase 3 trial of the German Hodgkin Study Group (GHSG HD14). Lancet Haematol 2021; 8 (4): e278–e288. doi: 10.1016/S2352-3026 (21) 00029-6.
14. Borchmann P, Plütschow A, Kobe C et al. PET-guided omission of radiotherapy in early-stage unfavourable Hodgkin lymphoma (GHSG HD17): a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2021; 22 (2): 223–234. doi: 10.1016/S1470-2045 (20) 30601-X.
15. Diehl V, Franklin J, Pfreundschuh M et al. Standard and increased-dose BEACOPP chemotherapy compared with COPP-ABVD for advanced Hodgkin‘s disease. N Engl J Med 2003; 348 (24): 2386–2395. doi: 10.1056/ NEJMoa022473.
16. Borchmann P, Haverkamp H, Diehl V et al. Eight cycles of escalated-dose BEACOPP compared with four cycles of escalated-dose BEACOPP followed by four cycles of baseline-dose BEACOPP with or without radiotherapy in patients with advanced-stage Hodgkin‘s lymphoma: final analysis of the HD12 trial of the German Hodgkin Study Group. J Clin Oncol 2011; 29 (32): 4234–4242. doi: 10.1200/JCO.2010.33.9549.
17. Engert A, Haverkamp H, Kobe C et al. Reduced-intensity chemotherapy and PET-guided radiotherapy in patients with advanced stage Hodgkin‘s lymphoma (HD15 trial): a randomised, open-label, phase 3 non-inferiority trial. Lancet 2012; 379 (9828): 1791–1799. doi: 10.1016/S0140-6736 (11) 61940-5.
18. Borchmann P, Goergen H, Kobe C et al. PET-guided treatment in patients with advanced-stage Hodgkin‘s lymphoma (HD18): final results of an open-label, international, randomised phase 3 trial by the German Hodgkin Study Group. Lancet 2017; 390 (10114): 2790–2802. doi: 10.1016/S0140-6736 (17) 32134-7.
19. Kreissl S, Goergen H, Buehnen I et al. PET-guided eBEACOPP treatment of advanced-stage Hodgkin lymphoma (HD18): follow-up analysis of an international, open-label, randomised, phase 3 trial. Lancet Haematol 2021; 8 (6): e398–e409. doi: 10.1016/S2352-3026 (21) 00101-0.
20. Borchmann P, Ferdinandus J, Schneider G et al. Assessing the efficacy and tolerability of PET-guided BrECADD versus eBEACOPP in advanced-stage, classical Hodgkin lymphoma (HD21): a randomised, multicentre, parallel, open-label, phase 3 trial. Lancet 2024; 404 (10450): 341–352. doi: 10.1016/S0140-6736 (24) 01315-1.
21. Herrera AF, Leblanc ML, Castellino SM et al. Nivolumab-AVD in advanced stage classic Hodgkin lymphoma. N Engl J Med 2024; 391 (15): 1379–1389. doi: 10.1056/ NEJMoa2405888.
22. Subramanian A, Shengqin S, Flerlage J et al. Distinct cell state ecosystems for nodular lymphocyte-predominant Hodgkin lymphoma. Nat Commun 2025; 16 (1): 8473. doi: 10.1038/s41467-025-63339-9.
23. Salvaris RT, Allanson BM, Collins G et al. Nodular lymphocyte-predominant Hodgkin lymphoma: advances in disease biology, risk stratification, and treatment. Haematologica 2024; 109 (11): 3476–3487. doi: 10.3324/haematol.2024.285903.
24. Nogova L, Reineke T, Eich HT et al. Extended field radiotherapy, combined modality treatment or involved field radiotherapy for patients with stage IA lymphocyte-predominant Hodgkin’s lymphoma: a retrospective analysis from the German Hodgkin Study Group (GHSG). Ann Oncol 2005; 16 (10): 1683–1687. doi: 10.1093/annonc/mdi323.
25. Fanale MA, Cheah CY, Rich A et al. Encouraging activity for R-CHOP in advanced stage nodular lymphocyte-predominant Hodgkin lymphoma. Blood 2017; 130 (4): 472–477. doi: 10.1182/blood-2017-02-766121.
26. Wilson MR, Bagguley T, Smith A et al. Frontline management of nodular lymphocyte predominant Hodgkin lymphoma-a retrospective UK multicentre study. Br J Haematol 2019; 186 (6): e214–e217. doi: 10.1111/bjh.16109.
27. Moskowitz CH, Nademanee A, Masszi T et al. Brentuximab vedotin as consolidation therapy after autologous stem-cell transplantation in patients with Hodgkin‘s lymphoma at risk of relapse or progression (AETHERA): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2015; 385 (9980): 1853–1862. doi: 10.1016/S0140-6736 (15) 60165-9.
28. Desai SH, Spinner MA, Evens AM et al. Overall survival of patients with cHL who progress after autologous stem cell transplant: results in the novel agent era. Blood Adv 2023; 7 (23): 7295–7303. doi: 10.1182/bloodadvances.2023011205.
29. Michalka J, Král Z, Marková J et al. Konsolidační léčba brentuximab vedotinem u pacientů s relabujícím/refrakterním klasickým Hodgkinovým lymfomem po provedení autologní transplantace hematopoetických kmenových buněk v České republice. Onkologie 2023; 17 (4): 267–272. doi: 10.36290/xon.2023.051.
30. Král Z, Michalka J, Móciková H et al. Treatment of relapsed/refractory Hodgkin lymphoma: real-world data from the Czech Republic and Slovakia. J Cancer 2019; 10 (21): 5041–5048. doi: 10.7150/jca.29308.
31. Ansell SM, Bröckelmann PJ, von Keudell G et al. Nivolumab for relapsed/refractory classical Hodgkin lymphoma: 5-year survival from the pivotal phase 2 Check - -Mate 205 study. Blood Adv 2023; 7 (20): 6266–6274. doi: 10.1182/bloodadvances.2023010334.
32. Kuruvilla J, Ramchandren R, Santoro A et al. Pembrolizumab versus brentuximab vedotin in relapsed or refractory classical Hodgkin lymphoma (KEYNOTE-204): an interim analysis of a multicentre, randomised, open-label, phase 3. Lancet Oncol 2021; 22 (4): 512–524. doi: 10.1016/S1470-2045 (21) 00005-X.
33. Armand P, Zinzani PL, Lee HJ et al. Five-year follow-up of KEYNOTE-087: pembrolizumab monotherapy for relapsed/refractory classical Hodgkin lymphoma. Blood 2023; 142 (10): 878–886. doi: 10.1182/blood.2022019386.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článek Dimenze onkochirurgie IIČlánek O tvrdosti dat
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2026 Číslo 1- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
- Fixní kombinace tramadol/paracetamol je doporučenou volbou v léčbě chronické bolesti v ordinaci praktického lékaře
-
Všetky články tohto čísla
- Dimenze onkochirurgie II
- O tvrdosti dat
- Kožní nemoci způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci (monoklonální gamapatie kožního významu)
- Změny hemostázy a další poruchy způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci
- Fenomén nádeje, ako neoddeliteľná súčasť starostlivosti o onkologického pacienta v terminálnom štádiu
- Výsledky léčby Hodgkinova lymfomu v České republice
- Rozsah reportování při vyšetření predispozice k nejčastějším solidním nádorům dospělého věku pomocí sekvenování nové generace
- Logopedická intervence u pacientky s mnohočetným myelomem a dysfagií – případová studie z klinické praxe
- Strategie snižování rizik „harm reduction“ jako součást primární prevence
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Rozsah reportování při vyšetření predispozice k nejčastějším solidním nádorům dospělého věku pomocí sekvenování nové generace
- Výsledky léčby Hodgkinova lymfomu v České republice
- Kožní nemoci způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci (monoklonální gamapatie kožního významu)
- Logopedická intervence u pacientky s mnohočetným myelomem a dysfagií – případová studie z klinické praxe
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



