-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Epidémia vírusových hepatitíd B a C u hospitalizovaných onkologických pacientov
Outbreak of viral hepatitis B and C in hospitalized cancer patients
The Regional Public Health Office recorded 47 cases of he-patitis B and C in 39 patients hospitalized in the regional hospital between September 2009 and July 2010. The outbreak cases included in the study met the previously set standard definition. Based on the epidemiological investigations a hypothesis was formulated on the route of infection transmission through the administration of parenteral solutions using a peripheral venous cannula during hospitalization. A retrospective cohort study revealed a statistically significant association between parenteral therapy administered using a peripheral venous cannula and disease (for viral hepatitis B: X2 = 49.53, p < 0.001 and viral hepatitis C: X2 = 22.42, p < 0.001). The results were in accordance with the failures to comply with the sanitary-epidemiological standards revealed by audits at the respective departments.
Key words:
hepatitis – parenteral therapy – peripheral venous cannula
Autoři: A. Kološová 1; J. Gašparovič 2
Působiště autorů: Regionálny úrad verejného zdravotníctva so sídlom v Komárne 1; Slovenská zdravotnícka univerzita v Bratislave, Národné referenčné centrum pre vírusové hepatitídy 2
Vyšlo v časopise: Epidemiol. Mikrobiol. Imunol. 63, 2014, č. 4, s. 260-264
Kategorie: Souhrnná sdělení, původní práce, kazuistiky
Souhrn
Regionálny úrad verejného zdravotníctva zaevidoval 47 prípadov ochorení na vírusovú hepatitídu B a C, ktoré boli dokázané u 39 pacientov hospitalizovaných v regionálnej nemocnici v čase od septembra 2009 do júla 2010. Do epidémie boli zaradené prípady podľa vopred stanovenej štandardnej definície. Na základe epidemiologického vyšetrovania bola formulovaná hypotéza o predpokladanom spôsobe prenosu inokuláciou pri podávaní parenterálnych roztokov cez periférnu venóznu kanylu počas hospitalizácie. Metódou retrospektívnej kohortovej štúdie bola preukázaná štatisticky významná súvislosť medzi podávaním parenterálnej liečby cez periférnu venóznu kanylu a vznikom ochorení (pre vírusovú hepatitídu B: X2 = 49,53, p < 0,001 a vírusovú hepatitídu C: X2 = 22,42, p < 0,001). Výsledky boli v súlade so zistenými nedostatkami pri kontrole hygienicko-epidemiologického režimu na oddelení.
Kľúčové slová:
hepatitída – parenterálna liečba – periférna venózna kanylaÚVOD
Odhaduje sa, že približne 40 % svetovej populácie malo kontakt alebo sú nosičmi vírusu hepatitídy B (HBV). Hepatitída B (VHB) je jedným z najvýznamnejších infekčných ochorení na svete. Jej prevalencia varíruje v rozmedzí 0,1 % až do 20 %. Oblasti s nízkou prevalenciou sú napríklad krajiny západnej Európy, USA, Kanada, Austrália a Nový Zéland. Vysoká prevalencia tohto ochorenia bola zistená v oblasti južnej Ázie, Číny a Subsaharskej Afriky [1]. Vo väčšine vyspelých krajín neprekračuje prevalencia HBsAg v bežnej populácii 1–2 %.
Infekcia vírusom hepatitídy C (HCV) predstavuje významný celosvetový zdravotnícky problém najmä preto, že môže viesť ku vzniku cirhózy a hepatocelulárneho karcinómu. Akútna forma vírusovej hepatitídy C (VHC) vo väčšine prípadov prebieha bez významných klinických príznakov, čím veľmi často uniká pozornosti. U väčšiny pacientov však ochorenie prechádza do chronicity, tiež s asymptomatickým priebehom. Vo svete je v súčasnosti viac ako 170 miliónov ľudí infikovaných HCV [2]. Počet hlásených prípadov akútnych, ale predovšetkým novozistených chronických VHC, má na Slovensku podľa údajov RÚVZ v Banskej Bystrici dlhodobo stúpajúci trend [3].
Popisovaná epidémia bola evidovaná na onkologickom oddelení nemocnice všeobecného typu. Prvé ochorenie bolo hlásené dňa 3. 6. 2010, jednalo sa o prípad akútnej VHB. Prvé príznaky však boli zistené už vo februári 2010. Tento, ako aj nasledujúce 2 prípady (akútna VHC + prekonaná VHB, koinfekcia VHB+VHC) boli najskôr vyšetrované ako sporadické. Epidemiologické vyšetrenie s podozrením na epidémiu bolo prvýkrát vykonané dňa 23. 6. 2010.
Cieľom vyšetrovania epidémie bolo prerušiť šírenie nákazy, aktívne vyhľadať chorých v ohnisku nákazy, objasniť príčiny vzniku epidémie s cieľom zabrániť jej opakovaniu.
Na základe epidemiologického vyšetrenia a výkonu štátneho zdravotného dozoru na oddelení bola formulovaná hypotéza, podľa ktorej k prenosu nákazy došlo počas hospitalizácie pacientov na onkologickom oddelení inokuláciou v súvislosti s podávaním parenterálnych roztokov cez PVK.
SÚBOR A EPIDEMIOLOGICKÁ METODIKA
Sledovaný súbor tvorilo 312 potenciálne exponovaných pacientov (161 mužov a 151 žien), ktorí boli hospitalizovaní v čase od septembra 2009 do júla 2010 na onkologickom oddelení nemocnice. Súbor bol stanovený na základe najdlhšieho inkubačného času od vzniku príznakov prvého ochorenia. Išlo o pacientov s onkologickým ochorením prevažne gastrointestinálneho traktu. Priemerný vek pacientov bol 66 rokov (v rozsahu od 20 do 90). Viacerí z nich boli na oddelení hospitalizovaní opakovane. Priemerný počet hospitalizácií na pacienta bol 2,1 (rozsah od 1 po 12). Oddelenie disponovalo 33 lôžkami. Približne pol roka pred vznikom epidémie došlo na oddelení k personálnym zmenám. Odber krvi na laboratórny dôkaz hepatitídy bol realizovaný u 165 osôb (52,9 %). Zvyšní pacienti zo súboru odber realizovaný nemali, najmä z dôvodu úmrtia do doby rozpoznania epidémie, ojedinele z dôvodu odmietnutia vyšetrenia.
HBsAg reaktívne vzorky boli testované na prítomnosť vírusu komerčne dostupnou hybridizačnou metódou Versant HBV DNA3.0 Assay (bDNA). Genotypizácia HBV DNA pozitívnych vzoriek bola urobená použitím nested PCR a fragmentovej analýzy [10].
Prítomnosť HCV v reaktívnych vzorkách bola testovaná komerčne dodávanými štandardizovanými súpravami Cobas Amplicor HCV v 2.0. Genotypizácia HCV RNA pozitívnych vzoriek sa vykonala komerčnými štandardizovanými súpravami Linear Array Hepatitis C Genotyping Test, založenými na reverznej hybridizácii PCR amplikónov.
Za potvrdený prípad akútnej VHB bol v súlade so štandardnou definíciou pre oznamovanie prenosných chorôb do siete Spoločenstva považovaný každý prípad so zodpovedajúcimi klinickými príznakmi a pozitívnymi anti-HBc IgM protilátkami, ktorý bol súčasne v epidemiologickej súvislosti (hospitalizácia na onkologickom oddelení v čase od 1. 9. 2009 do 4. 7. 2010). [4]. Nakoľko epidémia bola protrahovaná a rozpoznaná v neskoršom štádiu, kedy prítomnosť anti-HBc IgM už u niektorých osôb nebolo možné potvrdiť, boli definované aj pravdepodobné prípady akútnej VHB. Za pravdepodobný prípad bolo považované ochorenie s pozitívnymi výsledkami svedčiacimi pre prebiehajúce ochorenie (HbsAg, HbeAg, HBV DNA), avšak bez dôkazu anti-Hbc IgM, prítomnými klinickými príznakmi ochorenia, epidemiologickou súvislosťou a predchádzajúcim negatívnym HBsAg (nie viac ako pred 12 mesiacmi).
Ako prípad akútnej (novozískanej) VHC bol definovaný pacient s HCV RNA pozitivitou, s predchádzajúcou negativitou anti-HCV protilátok, ktorý bol v čase od 1. 9. 2009 do 4. 7. 2010 hospitalizovaný na onkologickom oddelení.
V rámci opatrení na zabránenie šíreniu nákazy bol exponovaným osobám nachádzajúcim sa v inkubačnom čase (vo vzťahu k poslednej expozícii) nariadený lekársky dohľad, pasívna a aktívna imunizácia proti vírusovej hepatitíde B (VHB). Exponované osoby, avšak už mimo inkubačného času, boli vyšetrené za účelom vylúčenia chronicky prebiehajúceho ochorenia. Oddelenie bolo prechodne uzatvorené, vykonaná bola celoplošná dezinfekcia, aktualizované štandardné postupy, opakovane preškolený personál, zabezpečenie informovanosti ďalších pracovísk nemocnice.
Všetci pacienti s ochorením zodpovedajúcim niektorej z definícií prípadu boli podrobne epidemiologicky vyšetrení. Anamnéza bola získaná od pacientov, rodinných príslušníkov, ošetrujúcich lekárov a zo zdravotnej dokumentácie. Údaje relevantné z hľadiska možného prenosu nákazy (transfúzie krvi, operácie, endoskopické vyšetrenia, podávanie parenterálnych roztokov, hospitalizácie, sexuálni partneri a i.) boli preverené predvolaním darcov krvi, výkonom štátneho zdravotného dozoru v dotknutých zdravotníckych zariadeniach a vyšetrením kontaktov.
Na zistenie vzťahu medzi expozíciou parenterálnym roztokom a vznikom ochorenia na VHB a VHC bola využitá retrospektívna kohortová štúdia. Zo 165 laboratórne vyšetrených pacientov bolo do štúdie zaradených pri VHB 151 pacientov (91,5 %) a pri VHC 159 (96,4 %). Zvyšní boli vyradení z dôvodu predpokladanej imunity voči danému ochoreniu v čase expozície (prekonanie ochorenia v minulosti, resp. chronicky prebiehajúce ochorenie). Pacienti boli rozdelení do 2 skupín – exponovaní a neexponovaní intravenóznej liečbe. Na štatistické spracovanie bol použitý program EpiInfo.
Graf 1. Rozvoj prvých príznakov ochorenia (stanovenie diagnózy) u pacientov hospitalizovaných na onkologickom oddelení v čase od 9/2009 do 7/2010; n = 39 Fig. 5. Onset of symptoms (diagnosis) in patients hospitalized at the oncology department between September 2009 and July 2010; n = 39 
VÝSLEDKY
V období od februára 2010 do januára 2011 sme evidovali 47 prípadov ochorení na vírusovú hepatitídu u pacientov hospitalizovaných na onkologickom oddelení tej istej nemocnice. Ochorenie sa vyskytlo u 39 osôb, z toho 22 osôb malo potvrdenú VHB, 9 osôb VHC a u 8 osôb bola zaznamenaná koinfekcia VHB+VHC. Prvé ochorenie, s rozvojom príznakov už od februára 2010, bolo diagnosticky doriešené a orgánu verejného zdravotníctva hlásené až v júni 2010. U 4 osôb bolo ochorenie rozpoznané na základe vyhľadania lekárskej pomoci pacientom pre rozvoj klinických príznakov. Ďalších 35 chorých bolo aktívne vyhľadaných v ohnisku nákazy a v rámci lekárskeho dohľadu. Najväčší počet prípadov bol evidovaný v mesiaci júl 2011 (obr. 1). Hospitalizáciu si vyžiadalo 7 pacientov. Dve osoby ochoreli na VHB napriek začatiu profylaktického očkovania (pasívna a 2 dávky aktívnej imunizácie po 40 µg). Priemerný vek chorých bol 67 rokov s minimom 48 a maximom 84 rokov.
Epidemiologickým vyšetrením boli v anamnéze pacientov zistené rizikové faktory uvedené v tabuľke 1. Pacienti mali parenterálnu liečbu podávanú s použitím výhradne jednorazového materiálu, vždy cez periférnu venóznu kanylu (PVK). Na preplach PVK bol používaný bolus fyziologického roztoku s heparínom, pričom obe zložky boli aspirované z viacdávkových balení používaných pre viacerých pacientov.
Tab. 1. Rizikové faktory* Table 1. Risk factors* 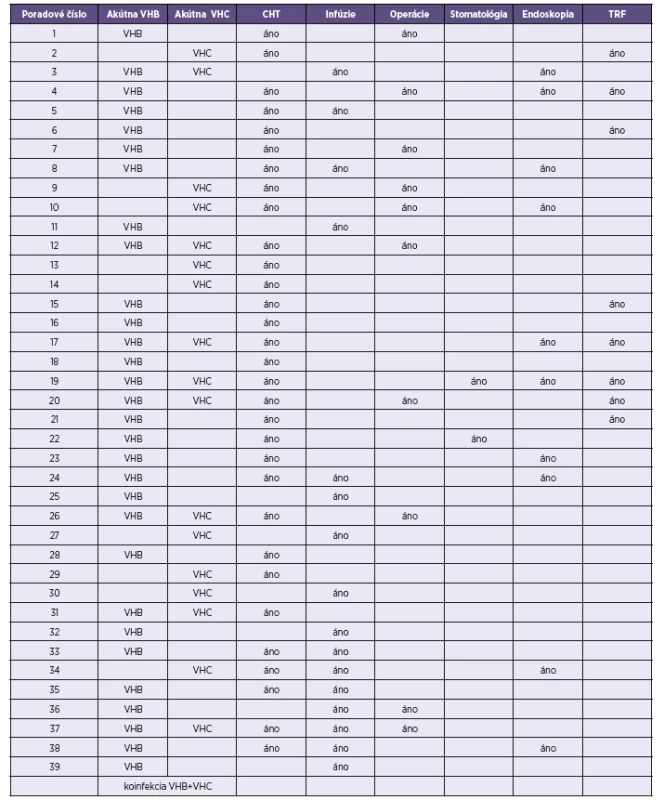
CHT – chemoterapia, TRF – transfúzia krvi *V anamnéze pacientov hospitalizovaných na rádioonkologickom oddelení v čase od 9/2009 do 7/2010, u ktorých došlo k vzniku ochorenia na VHB, VHC. CHT – chemotherapy, TRF – blood transfusion *In history of patients hospitalized at the radiology-oncology department between September 2009 and July 2010 and diagnosed with viral hepatitis B and C while in hospital. Počas výkonu štátneho zdravotného dozoru na oddelení boli zistené nedostatky v hygienicko-epidemiologickom režime (kríženie pracovných plôch určených na manipuláciu s parenterálnymi roztokmi a plôch na manipuláciu s biologicky kontaminovaným materiálom, opakované používanie koncoviek PVK, nedostatky v hygiene rúk, nesprávna manipulácia s nebezpečným biologicky kontaminovaným odpadom a ďalšie).
Podozrenie svedčiace pre pravdepodobnosť prenosu nákazy iným faktorom prenosu (krvné deriváty, endoskopické vyšetrenie, operácie, stomatologický výkon) sa epidemiologickým vyšetrovaním nepotvrdilo.
Testovaním hypotézy bola preukázaná štatisticky významná súvislosť vzniku ochorení s podávaním parenterálnej liečby v prípade oboch typov hepatitídy: pre VHB: X2 = 49,53, p < 0,001 a VHC: X2 = 22,42, p < 0,001. Súčasťou vyšetrovania epidémie bola laboratórna diagnostika vrátane molekulárno-biologických metód. Súbor vyšetrovaných vzoriek v NRC pre vírusové hepatitídy tvorilo 37 sér pacientov s pozitívnymi výsledkami testovania skríningovými a nadstavbovými metódami. V 34 prípadoch išlo o pacientov s akútnou hepatitídou, prípadne koinfekciou, získanou v rámci epidémie. V 3 prípadoch boli vyšetrené séra pacientov s chronickým ochorením prítomným už v čase hospitalizácie, ktorí mohli byť potenciálnymi prameňmi nákazy. Od zvyšných 5 pacientov s akútnym ochorením sa séra na ďalšie vyšetrenie už nepodarilo získať.
U 26 HBsAg reaktívnych vzoriek (25 od pacientov s akútnym ochorením a 1 od pacienta s chronickým ochorením) bol stanovený počet kópií HBV a následne u všetkých pozitívnych vzoriek bol určený genotyp. Rozsah vírusovej nálože sa pohyboval v intervale 3 900 ≥ 100 mil. kópií/ml. Všetci analyzovaní pacienti mali genotyp A.
U 18 pacientov bolo vykonané vyšetrenie na prítomnosť HCV. U troch sa jednalo o chronické ochorenie (potenciálne pramene nákazy). Z 15 akútnych prípadov sa u 3 už z opakovaného odberu nepodarilo prítomnosť HCV dokázať, preto stanovenie genotypu nebolo možné. Vo zvyšných vzorkách sér 12 pacientov bola dokázaná HCV RNA pozitivita, z toho v 11 prípadoch bol potvrdený genotyp 1b a v 1 prípade bol genotyp neurčiteľný. Rovnaký genotyp (1b) bol stanovený aj u prípadov chronického ochorenia.
Po prijatí nápravných opatrení na oddelení došlo k prerušeniu šírenia nákazy a k zvládnutiu epidémie.
DISKUSIA
Oneskorené rozpoznanie prvého prípadu a tým aj samotnej epidémie, zabránilo včasnému prijatiu účinných opatrení na zabránenie šíreniu nákazy. Opakovaná hospitalizácia pacientov, v čase pred prijatím nápravných opatrení, viedla k nárastu počtu možných prameňov nákazy.
Epidemiologickým vyšetrovaním a využitím jednoduchej analytickej metódy boli zistené skutočnosti naznačujúce nozokomiálny pôvod ochorení. Výsledky genotypizácie získané vyšetrením vzoriek sér pacientov podporujú toto tvrdenie. Je však nutné uviesť, že genotyp HBV u chorých v bežnej populácii daného regiónu nie je známy. Na Slovensku, tak ako v celej Európe, sú pacienti najčastejšie infikovaní HCV s genotypom 1 a v menšej miere s genotypom 3 a 2.
S podobnými prípadmi prenosu vírusovej hepatitídy v zdravotníckych zariadeniach sa stretávame aj v odbornej literatúre. Prenos VHB medzi pacientmi popisuje práca autorov Lanini S. et al. Sledovali výskyt VHB pomocou údajov z PubMed databázy a databázy pre nozokomiálne nákazy. Celkovo analyzovali 30 publikácií popisujúcich 33 epidémií spôsobených HBV, v ktorých bolo 471 pacientov a 16 úmrtí. Podľa autorov práce bol najvyšší výskyt týchto nákaz na dialyzačných jednotkách (30,3 %), nasledovaných nemocničnými oddeleniami (21,2 %), sanatóriami (21,2 %), chirurgickými oddeleniami (15,2 %) a ambulanciami (12,1 %). Ako cesty prenosu infekcie boli detegované viacdávkové balenia liekov (30,3 %), opakovane používané pomôcky na odber kapilárnej krvi (27,2 %), endomyokardiálne biopsie (9,1 %) a viacnásobné pochybenia v dodržiavaní štandardných postupov (9,1 %) [5].
Autori Burns K. et al. publikovali prácu o nozokomiálnych infekciách VHB v dvoch nemocniciach v Írsku od januára 2005 do marca 2006. Akútna infekcia bola zistená u pacienta, ktorého rizikovým faktorom bol nedávny chirurgický výkon. Podrobnou analýzou sa zistilo, že tento pacient bol jedným z piatich prípadov akútnej infekcie VHB. Ďalší štyria boli infikovaní v iných dvoch nemocniciach počas 15 mesiacov. Definitívny faktor prenosu sa nepodarilo identifikovať. Nedali sa však vylúčiť pochybenia pri štandardných postupoch, akými je aplikácia injekcie alebo flebotómia. Neskôr boli zistené ďalšie dva sekundárne prípady v komunite získanej infekcie u kontaktov dvoch nozokomiálne infikovaných pacientov [6].
V USA bola publikovaná práca, kde State Department of Health v Oklahome mal doručenú informáciu o 6 pacientoch s nevysvetliteľnou infekciou VHC, ktorí boli liečení na rovnakom oddelení pre liečbu bolesti. Po prešetrení celej udalosti sa z celkového počtu 908 pacientov dalo testovať 795 (87,6 %). VHC sa zistila u 71 pacientov a u 31 pacientov bola zistená VHB. Vyšetrením bolo preukázané používanie rovnakej ihly a striekačky pri podávaní sedatív viacerým pacientom. Spôsobom prenosu HCV a HBV bolo používanie rovnakých injekčných ihiel medzi pacientmi [7].
Nakoľko sa v popisovanej epidémii jedná prevažne o pacientov s onkologickým ochorením, je nutné zmieniť sa aj o ďalšej alternatíve. Viaceré štúdie uvádzajú možnú reaktiváciu VHB a VHC infekcie pri chemoterapii alebo imunosupresívnej liečbe. Frekvencia reaktivácie nie je dobre známa. Yeo W. et al. vykonali prospektívnu štúdiu, kde sledovali 626 onkologických pacientov s cytotoxickou liečbou počas 12 mesiacov. U 72 (12 %) bola zistená HBsAg pozitivita. Počas chemoterapie bol u 34 (44 %) zaznamenaný vzostup aminotransferáz. Z nich u 15 (44 %) bol tento efekt pripísaný reaktivácii VHB, chronickej aktívnej VHB – 1 pacient (3 %), VHC 1 pacient (3 %), malígnej infiltrácii – 2 pacienti (6 %) a hepatotoxickej chemoterapii 11 pacientov (32 %). U 4 zostala príčina neznáma [8]. Uvedený autor v ďalšej práci spolu s kolektívom autorov uvádza, že VHB reaktivácia je dobre známa u pacientov s hematologickou malignitou, ale existuje len málo údajov o pacientoch s inou formou rakoviny. Vo svojej práci sledovali počas 18 mesiacov 41 HBsAg pozitívnych pacientok s karcinómom prsníka počas chemoterapie formou pravidelnej analýzy HBV DNA. Spolu bola reaktivácia dokázaná u 17 z nich (41 %) [9].
Ako vidieť, viaceré štúdie poukazujú na reaktiváciu hepatitídy najmä u pacientov s pozitívnym HBsAg v anamnéze pred začatím podávania chemoterapie. V našom súbore však boli pacienti pred podávaním liečby anamnesticky negatívni.
V štúdii z osemdesiatych rokov, ktorá bola míľnikom v tejto problematike, bádatelia z Hong Kongu sledovali virologicky, serologicky a biochemicky reaktiváciu u 100 pacientov s lymfómom počas chemoterapie. Takmer u polovice z 27 HBsAg pozitívnych pacientov (48 %) bola dokázaná reaktivácia počas alebo krátko po chemoterapii v porovnaní s pacientmi, ktorí nemali žiadne známky prebiehajúcej alebo predchádzajúcej hepatitídy (0 z 22). Len u 2 z 51 (4 %) sérologicky potvrdenej prekonanej VHB (bez HBsAg ale s protilátkami proti core antigénu – antiHBc) v sére sa vyvinula reaktivácia so znovuobjavením sa HBsAg v sére. Tento stav bežne označovaný ako reverzná sérokonverzia predstavuje extrémnu formu sérokonverzie [10].
Reverznej sérokonverzii sa vo svojej práci venujú aj Blanpain et al., ktorí opisujú 3 pacientov po orgánovej transplantácii. Zároveň uvádzajú ďalších 16 prípadov ochorenia z literárnej revue. Všetci pacienti boli imunosuprimovaní z dôvodu chemoterapie pre neoplazmu, užívanie imunusupresívnej liečby pre transplantáciu, infekciu HIV alebo AIDS. U všetkých týchto pacientov sa znovu objavila HBsAg a HBV DNA pozitivita, došlo k strate anti-HBs a anti-HBc. Incidencia VHB reaktivácie medzi transplantovanými pacientmi s anti-HBs a anti-HBc bola autormi odhadnutá približne na 5%, rovnako ako v prípade pacientov dostávajúcich chemoterapiu pre malígny lymfóm [11]. Je však len málo pravdepodobné, že by sa v našom súbore jednalo v takom počte pacientov (12,5 %) o reverznú sérokonverziu. Východiskové hodnoty anti-HBs a anti-HBc u našich pacientov neboli známe, anamnesticky však prekonanie vírusovej hepatitídy B alebo C v minulosti neudávali.
ZÁVER
Výsledky našej práce podporujú tvrdenie, že sa mohlo jednať o nozokomiálny prenos nákazy, ku ktorému došlo pravdepodobne inokuláciou v súvislosti s podávanou parenterálnou liečbou. Epidémia poukazuje na skutočnosť, že ani používanie jednorazového špeciálneho zdravotníckeho materiálu nijako nezaručuje stopercentnú ochranu pacienta pred možnosťou prenosu nákazy. Nesprávna manipulácia so zdravotníckym materiálom, nedostatočná hygiena rúk a pochybenia v bariérovej ošetrovateľskej technike patria medzi závažné nedostatky, ktoré môžu viesť k šíreniu nákazy. Je preto nesmierne dôležité venovať náležitú pozornosť štandardným postupom pri liečbe a ošetrovaní pacientov. Vzhľadom na parenterálny spôsob prenosu je rovnako nevyhnutné dodržiavať požiadavky bezpečnosti práce z hľadiska expozície zamestnancov biologickým faktorom pri práci.
Do redakce došlo dne 16. 5. 2014.
Adresa pro korespondenci:
MUDr. Andrea Kološová
Regionálny úrad verejného zdravotníctva so sídlom v Komárne
Mederečská 39
945 01 Komárno
Slovenská republika
e-mail: andrea.kolosova@gmail.com
Zdroje
1. Wasley A, Grytda S, Gallagher K. Surveillance for acute viral hepatitis-Unated States, 2006. MMWR Surveill Summ, 2008;57 : 1.
2. Kupčová V. Účinky interferónu alfa na fibrogenézu pri chronickej hepatitíde C. Trendy v hepatológii, 2009;1 : 24–27.
3. Kristián P, Mikas J, Schréter I. Epidemiológia hepatitídy C. Trendy v hepatológii, 2010;1 : 12–17.
4. Rozhodnutie komisie z 28. apríla 2008, ktorým sa mení a dopĺňa rozhodnutie 2002/253/ES, ktorým sa stanovujú definície ochorení pre oznamovanie prenosných chorôb do siete Spoločenstva na základe rozhodnutia Európskeho parlamentu a Rady č. 2119/98/ES. Úradný vestník Európskej únie SK. L159/46
5. Lanini S, Lauria FN, Fusco FM, et al. Patient to patient transmission of hepatitis B virus: A symptomatic review of reports on outbreaks between 1992–2007. BCM Medicine, 2009;7: article number 5.
6. Burns K, Heslin J, Crowley B, et al. Nosocomial outbreak of hepatitis B virus infection involving two hospitals in the Republic of Ireland. Journal of Hospital Infection, 2011;78 : 279-283. Dostupný na www: http://www.ncbi.nlm.nih.gov/pubmed/21530000
7. Comstock RD, Mallonee S, Fox JL, et al. A large nosocomial outbreak of hepatitis C and hepatitis B among patients receiving pain remediation treatments. Infection Control and Hospital Epidemiology, 2004;25 : 576-583.
8. Yeo W, Chan PK, Zhong S, et al. Frequency of hepatitis B virus reactivation in cancer patients undergoing cytotoxic chemotherapy: a prospective study of 626 patients with identification of risk factors. Journal of Medical Virology, 2000; 62(3):299-307. Dostupný na www: http://www.ncbi.nlm.nih.gov/pubmed/11055239.
9. Yeo W, Chan PK, et al. Hepatitis B virus reactivation in breast cancer patients receiving cytotoxic chemotherapy: A prospective study. Journal of Medical Virology, 2003, Vo 70, Issue 4, pages 553–561. Dostupné na www: onlinelibrary.wiley.com/doi/10.1002/jmv.10430/ 10. Hoofnagle, J.H., Hepatology, Vol. 49, No. 5, Suppl., 2009.
11. Blanpalin C, Knoop C, Delforge M-L, et al. Reactivation of hepatitis B after transplantation in patients with pre-existing anti-hepatitis B surface antigen antibodies. Transplantation, 1998;66 : 883–886.
Štítky
Hygiena a epidemiológia Infekčné lekárstvo Mikrobiológia
Článek Rejstříky
Článok vyšiel v časopiseEpidemiologie, mikrobiologie, imunologie
Najčítanejšie tento týždeň
2014 Číslo 4- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Očkování proti virové hemoragické horečce Ebola experimentální vakcínou rVSVDG-ZEBOV-GP
- Koronavirus hýbe světem: Víte jak se chránit a jak postupovat v případě podezření?
-
Všetky články tohto čísla
- Prevalenční studie nozokomiálních nákaz ve fakultních nemocnicích v České republice
- Epidémia vírusových hepatitíd B a C u hospitalizovaných onkologických pacientov
- Vstup do léčby a adherence k léčbě VHC u injekčních uživatelů drog v ČR
- Trend pertuse u dětí do jednoho roku života v České republice v letech 1997–2013
- Současnost klinických studií očkovacích látek v České republice
- Epidemiologie a rizikové faktory u legionelózy
-
Infekce způsobené netyfovými sérovary salmonel na Klinice infekčních chorob
Fakultní nemocnice Brno v letech 2011–2013 – retrospektivní studie - Séroprevalence Anaplasma phagocytophilum u pacientů se suspektní lymeskou borreliózou
- Ojedinělý případ izolovaného výskytu Mycobacterium tuberculosis v perikardiálním výpotku
- Surveillance západonilské horečky u koní v České republice v letech 2011–2013
- 26. Pečenkovy epidemiologické dny Luhačovice 16.–18. září 2014
- Rejstříky
- Epidemiologie, mikrobiologie, imunologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Prevalenční studie nozokomiálních nákaz ve fakultních nemocnicích v České republice
- Séroprevalence Anaplasma phagocytophilum u pacientů se suspektní lymeskou borreliózou
- Současnost klinických studií očkovacích látek v České republice
-
Infekce způsobené netyfovými sérovary salmonel na Klinice infekčních chorob
Fakultní nemocnice Brno v letech 2011–2013 – retrospektivní studie
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



