-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Kombinace systémové a chirurgické léčby u pacienta s primárně inoperabilním renálním karcinomem podkovovité ledviny: význam multioborové spolupráce – aktualizované výsledky 3letého sledování
Combination of systemic and surgical treatment in a patient with primarily inoperable renal cell carcinoma in a horseshoe kidney: the importance of multidisciplinary collaboration – updated results of 3-year follow-up
Primarily inoperable, locally advanced renal cell carcinoma represents a significant challenge in uro-oncology. Although systemic therapy is not a standard component of treatment in this setting, in carefully selected patients it may lead to disease regression and enable subsequent surgical resection. We present updated results of a 3-year follow-up of a patient with an initially inoperable finding in whom systemic therapy created the conditions for a subsequent successful surgical intervention.
Keywords:
renal cell carcinoma – systemic therapy – regression – surgical management
Autori: Jiří Herman 1; Vladimír Študent jr. 1; Aleš Vidlář 1; Anežka Zemánková 2; Igor Hartmann 1
Pôsobisko autorov: Urologická klinika LF UP a FN Olomouc 1; Onkologická klinika LF UP a FN Olomouc 2
Vyšlo v časopise: Ces Urol 2026; 30(1): 30-34
Kategória: Kazuistika
doi: https://doi.org/10.48095/cccu2026004Súhrn
Primárně inoperabilní, lokálně pokročilý renální karcinom představuje významnou výzvu v uroonkologii. Ačkoliv systémová léčba není v této indikaci standardní součástí terapeutického postupu, u pečlivě vybraných pacientů může vést k regresi onemocnění a umožnit následnou chirurgickou resekci. Prezentujeme aktualizované výsledky 3letého sledování pacienta s iniciálně inoperabilním nálezem, u něhož systémová terapie vytvořila podmínky pro následnou úspěšnou chirurgickou intervenci.
Klíčová slova:
renální karcinom – systémová terapie – regrese – chirurgická léčba
Úvod
Renální karcinom je z hlediska incidence 14. nejčastějším nádorovým onemocněním celosvětově. V roce 2022 dosáhl počet nově diagnostikovaných případů karcinomu ledviny 434 419 (což představuje 2,2 % všech nádorů na světě), zatímco počet úmrtí činil 155 702 (což představuje 1,6 % všech nádorů na světě) [1]. Česká republika vykazuje celosvětově jednu z nejvyšších incidencí zhoubných nádorů ledvin [2]. U metastatického světlobuněčného renálního karcinomu (ccRCC – clear-cell renal cell carcinoma) je standardem léčby systémová terapie, u lokalizovaného onemocnění je to chirurgická resekce [3]. Klinickou výzvu představují nádory lokálně pokročilé, a tedy obtížně operabilní, u nichž není systémová léčba před operací zatím standardně indikována, avšak může být zvážena u vybraných specifických případů s cílem zmenšení rozsahu primárního tumoru a dosažení operability [4]. V roce 2023 jsme prezentovali krátkodobé výsledky resekce podkovovité ledviny s primárně inoperabilním ccRCC, který regredoval po systémové léčbě, čímž byl umožněn záchovný výkon na ledvině [5]. Cílem této kazuistiky je přinést dlouhodobé výsledky sledování tohoto pacienta.
Kazuistika
Pacient, 52 let, bez závažnějších komorbidit či renální insuficience, s výchozím stavem podle Eastern Cooperative Oncology Group (ECOG) 0, byl došetřován pro ataku makroskopické hematurie. CT vyšetření břicha odhalilo objemný tumor pravé části podkovité ledviny velikosti 150 × 120 × 100 mm, klinické stadium cT4 N0 M0 (obr. 1). Konfirmační biopsie byla provedena pod ultrazvukovou kontrolou. Pro velikost, lokální invazi a rizikovost chirurgického výkonu byla po zvážení multioborovou komisí nasazena systémová léčba nivolumab 240 mg i.v. à 2 týdny + cabozantinib 40 mg p.o. denně dle protokolu klinické studie Checkmate 9ER, která započala 1. 12. 2021. Z důvodu rozvoje hepatotoxicity byla po 6 týdnech kombinovaná léčba deeskalována na monoterapii cabozantinibem. Kontrolní CT vyšetření 3 měsíce od zahájení léčby (obr. 2) prokázalo parciální regresi onemocnění, a proto bylo rozhodnuto o pokračování monoterapie cabozantinibem po dobu dalších 3 měsíců. Následná další regrese (obr. 3) umožnila radikální nefrektomii s R0 resekcí (obr. 4). Pacient zůstává již 3. rok v kompletní remisi (obr. 5).
Obr. 1. CT břicha s kontrastní látkou před zahájením terapie v transverzální a koronární projekci dokumentuje objemný tumor podkovovité ledviny velikosti 150 × 120 × 100 mm. Fig. 1. Contrast-enhanced abdominal CT in transverse and coronal planes prior to treatment initiation demonstrating a bulky tumour of the horseshoe kidney measuring 150 × 120 × 100 mm. 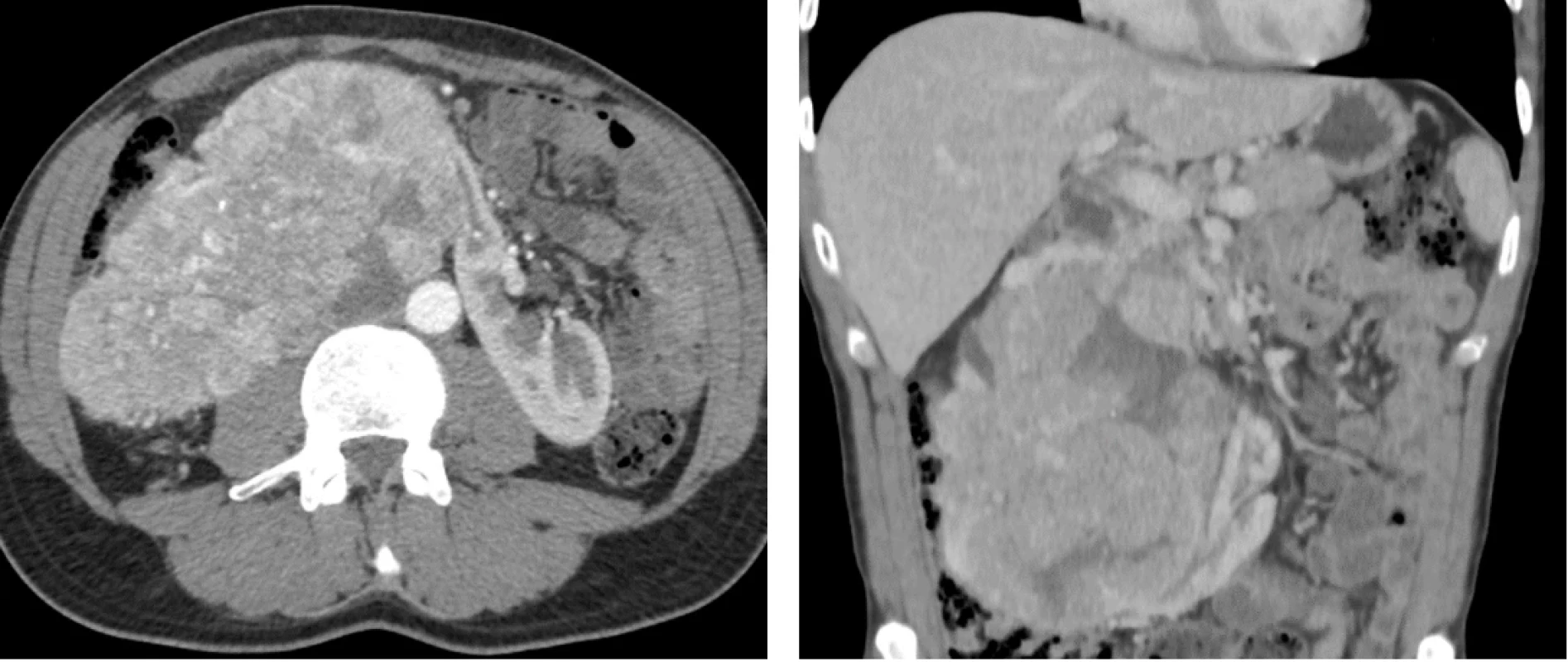
Obr. 2. CT břicha s kontrastní látkou za 3 měsíce od zahájení léčby v transverzální a koronární projekci dokumentuje parciální regresi onemocnění, velikost tumoru 90 × 60 × 100 mm. Fig. 2. A 3-month follow-up contrast-enhanced abdominal CT in transverse and coronal planes demonstrating partial disease regression, tumor size 90 × 60 × 100 mm. 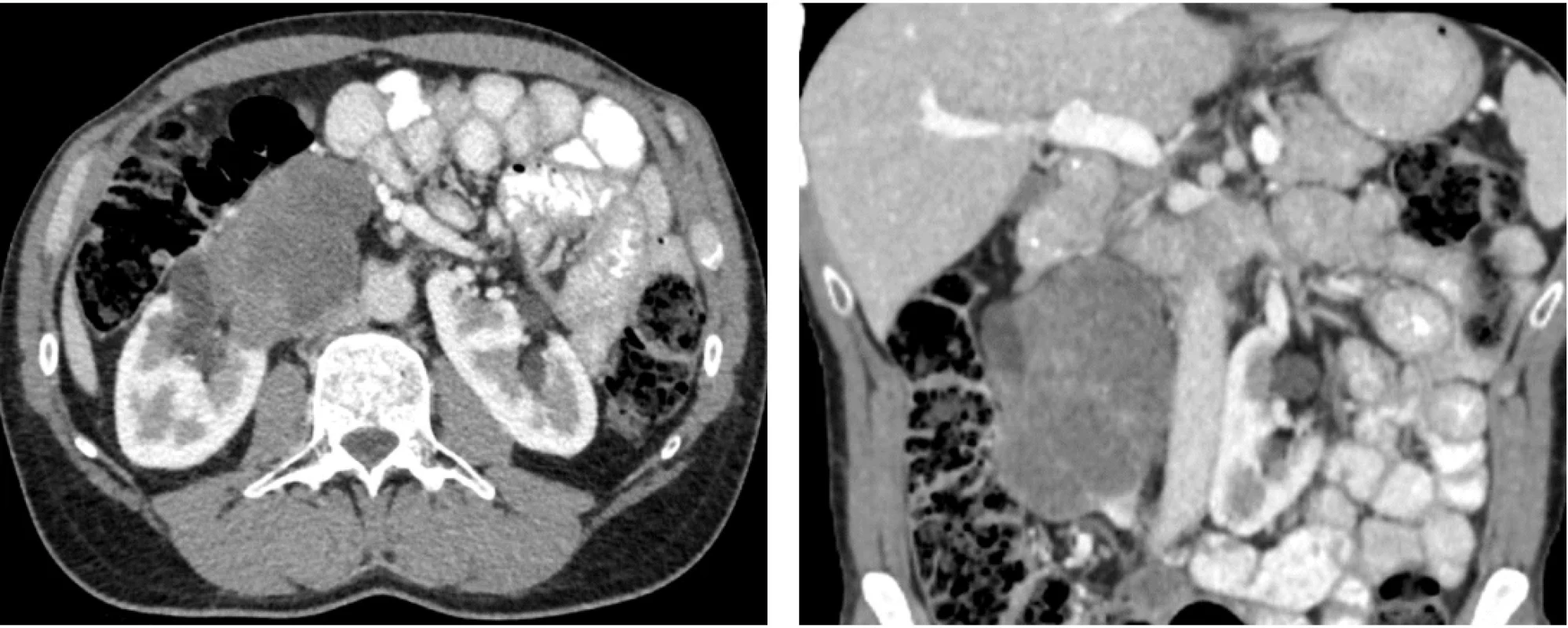
Obr. 3. CT břicha s kontrastní látkou za 6 měsíců od zahájení léčby v transverzální a koronární projekci, velikost tumoru 90 × 50 × 95 mm. Fig. 3. A 6-month follow-up contrast-enhanced abdominal CT in transverse and coronal planes, tumor size 90 × 50 × 95 mm. 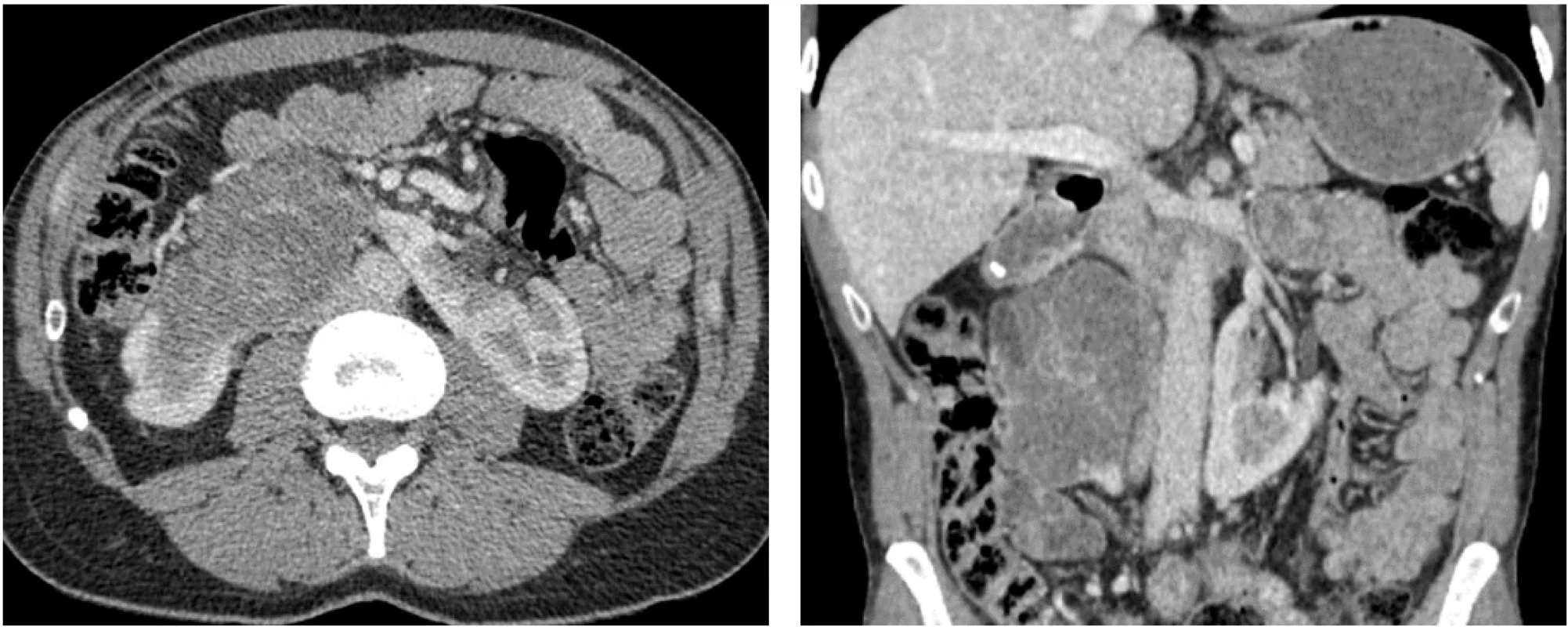
Obr. 4. CT břicha s kontrastní látkou v transverzální a koronární projekci po radikální nefrektomii. Fig. 4. Contrast-enhanced abdominal CT in transverse and coronal planes following radical nephrectomy. 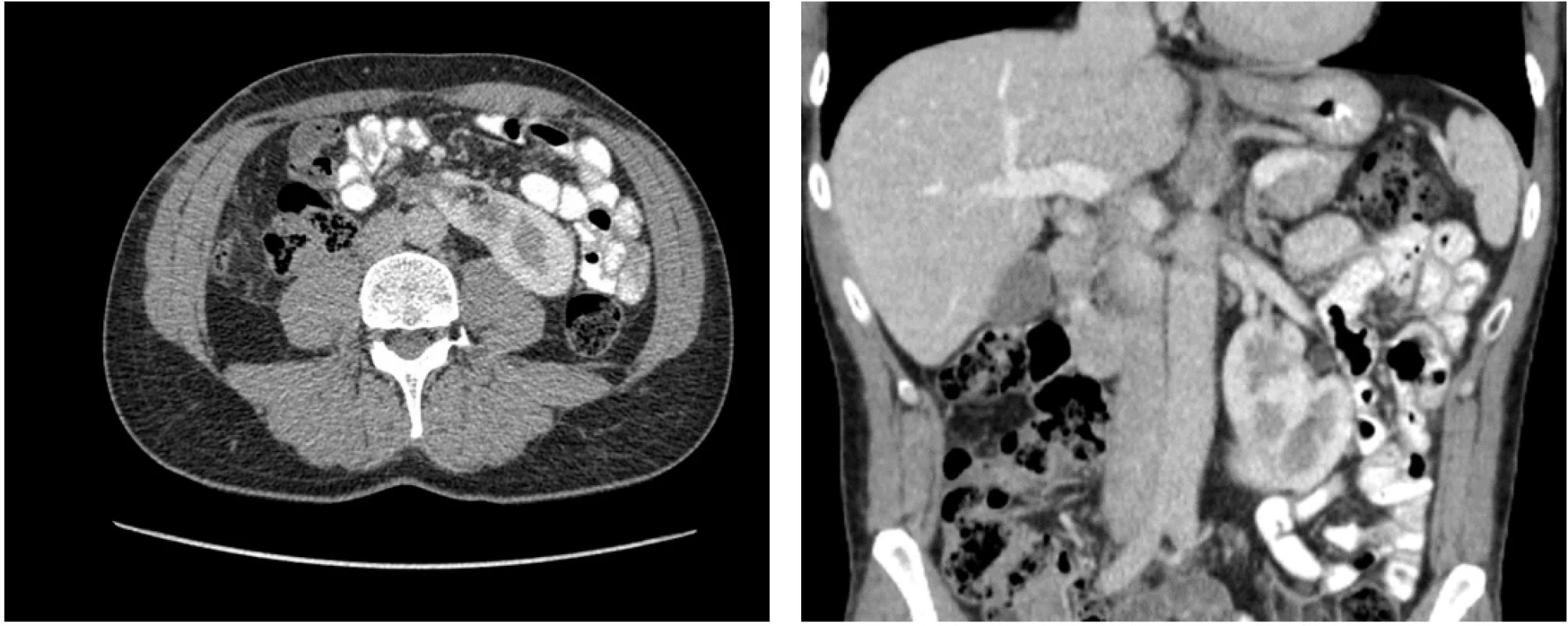
Obr. 5. CT břicha s kontrastní látkou v transverzální a koronární projekci 3 roky od započetí léčby. Fig. 5. Contrast-enhanced abdominal CT in transverse and coronal planes performed three years after initiation of treatment. 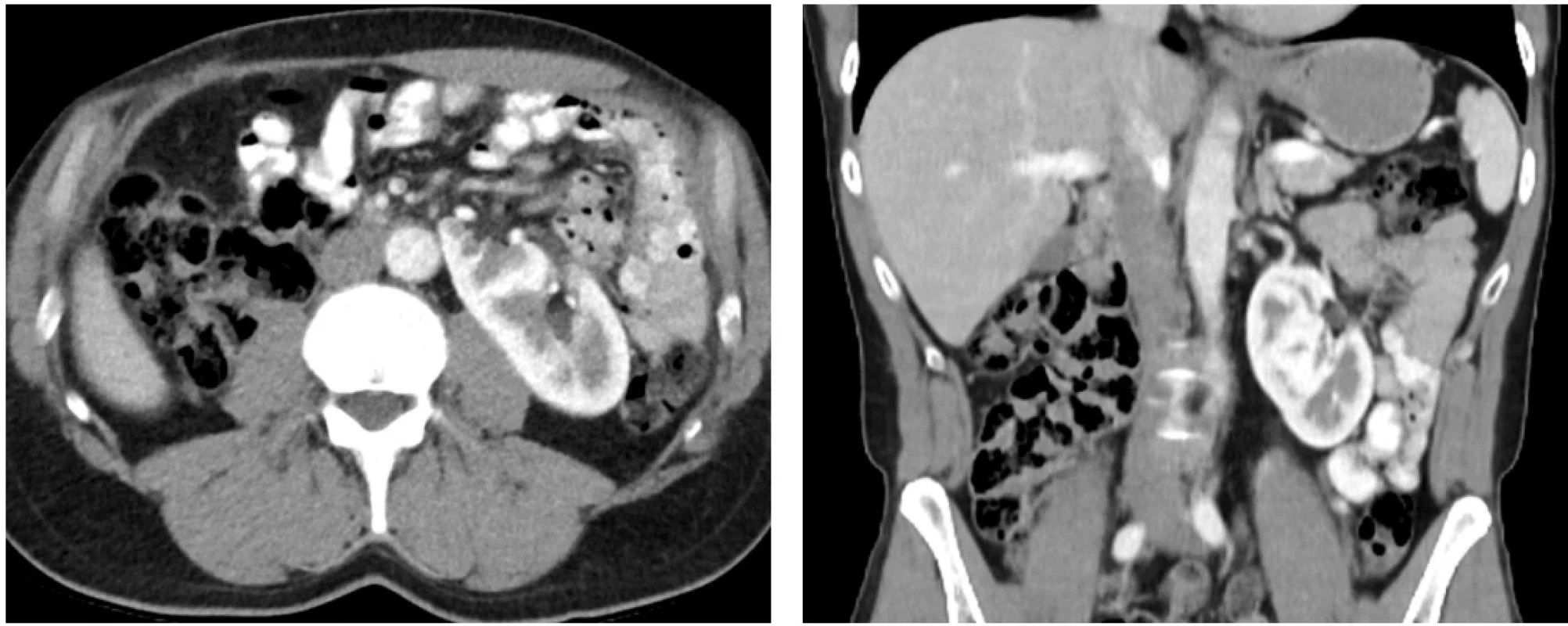
Diskuze
Neoadjuvantní systémová léčba u vstupně inoperabilního RCC představuje možnost, jak u vybraných pacientů dosáhnout regrese onemocnění a následně umožnit chirurgický výkon. Přestože chirurgická resekce zůstává základní modalitou léčby lokalizovaného RCC [3], u lokálně pokročilých nádorů může být primární operace technicky neproveditelná nebo spojena s nepřijatelným rizikem komplikací a ztráty renální funkce.
Dosavadní klinické zkušenosti ukazují, že neoadjuvantní léčba, zejména s využitím tyrosinkinázových inhibitorů, může vést ke zmenšení primárního tumoru a změně jeho operability, a to i u původně inoperabilních nálezů [6,7]. Efekt této léčby však bývá variabilní a významné patologické odpovědi jsou vzácné. Kombinace imunoterapie s cílenou léčbou rozšířily léčebné možnosti u metastatického onemocnění a v jednotlivých případech byly úspěšně použity i v neoadjuvantním kontextu [8].
Předkládaná kazuistika navazuje na naši dříve publikovanou práci [5]. Přinášíme výsledky dlouhodobého sledování, které potvrzuje přetrvávající kompletní remisi onemocnění i několik let po chirurgickém výkonu. Specifickým aspektem tohoto případu je postižení podkovovité ledviny, které je spojeno se zvýšenou chirurgickou náročností [9]. V této situaci může neoadjuvantní léčba přispět nejen ke zmenšení rozsahu tumoru, ale i k bezpečnějšímu plánování chirurgického výkonu s cílem dosažení radikální resekce při maximálním zachování funkčního renálního parenchymu.
V současné době není role neoadjuvantní léčby u RCC dosud jasně vymezena a chybí konsenzus ohledně výběru pacientů, délky léčby i hodnocení odpovědi [10]. Dosavadní klinické studie hodnotící neoadjuvantní léčbu RCC tvoří převážně menší studie fáze II [11]. Jediná randomizovaná studie fáze III v perioperačním uspořádání (studie PROSPER) neprokázala statisticky významný přínos a byla předčasně ukončena pro nedostatečnou účinnost [12]. K negativním výsledkům mohly přispět i metodologické aspekty studie, jako byla heterogenita zařazených nádorů, krátká doba předoperační léčby nivolumabem a vysoký podíl cenzorovaných dat.
V budoucnu se potřebujeme komplexněji zaměřit na tuto problematiku, definovat rizikové skupiny pacientů, identifikovat způsoby hodnocení efektu neoadjuvantí léčby, které léčebné režimy jsou vhodné a také jak dlouhá by měla neoadjuvantní systémová terapie být [11]. Je třeba také zdůraznit nutnost individuální indikace a mezioborové spolupráce při zvažování neoadjuvantního přístupu. Neoadjuvantní léčba zatím zůstává off-label postupem a může být spojena s významnou toxicitou, což vyžaduje pečlivý výběr pacientů a jejich důsledné sledování [13].
Závěr
V této práci prezentujeme dlouhodobé sledování pacienta se vstupně inoperabilním RCC, u něhož neoadjuvantní systémová léčba umožnila následnou radikální chirurgickou resekci a vedla k dlouhodobé kompletní remisi onemocnění.
Neoadjuvantní terapie může u vybraných pacientů s lokálně pokročilým RCC a nepříznivými anatomickými poměry představovat cestu k dosažení kurativního chirurgického výkonu. Její indikace by měla být zvážena zatím jen v individuálních případech a podání by mělo být založeno na rozhodnutí multidisciplinárního týmu.
Střet zájmů: Autoři prohlašují, že nemají žádný konflikt zájmů.
Prohlášení o podpoře: Zpracování tohoto článku nebylo podpořeno žádnou společností.
Zdroje
1. Bray F, Laversanne M, Sung H et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2024; 74(3): 229–263. doi: 10.3322/caac.21834.
2. International Agency for Research on Cancer. GLOBOCAN 2020: Cancer today – kidney cancer internet. Lyon: IARC 2020. [online]. Available from: https://gco.iarc.who.int/today/data/factsheets/cancers/29-Kidney-fact-sheet.pdf.
3. EAU Guidelines. Edn. presented at the EAU EAU Guidelines, Madrid 2025. [online]. Available from: https://uroweb.org/guidelines/renal-cell-carcinoma.
4. Bindayi A, Hamilton ZA, McDonald ML et al. Neoadjuvant therapy for localized and locally advanced renal cell carcinoma. Urol Oncol 2018; 36(1): 31–37. doi: 10.1016/j.urolonc.2017.07.015.
5. Zemankova A, Studentova H, Kopova A et al. Neoadjuvant nivolumab and cabozantinib in advanced renal cell carcinoma in a horseshoe kidney – how to achieve a safe and radical resection? A case report and review of the literature. Front Oncol 2023; 13 : 1115901. doi: 10.3389/fonc.2023.1115901.
6. Bilen MA, Jiang JF, Jansen CS et al. Neoadjuvant cabozantinib in an unresectable locally advanced renal cell carcinoma patient leads to downsizing of tumor enabling surgical resection: a case report. Front Oncol 2021; 10 : 622134. doi: 10.3389/fonc.2020.622134.
7. Roy AM, Briggler A, Tippit D et al. Neoadjuvant cabozantinib in renal-cell carcinoma: a brief review. Clin Genitourin Cancer 2020; 18(6): e688–e691. doi: 10.1016/j.clgc.2020.04.003.
8. Ingels A, Campi R, Capitanio U et al. Complementary roles of surgery and systemic treatment in clear cell renal cell carcinoma. Nat Rev Urol 2022; 19(7): 391–418. doi: 10.1038/s41585-022-00592-3.
9. Roussel E, Tasso G, Campi R et al. Surgical management and outcomes of renal tumors arising from horseshoe kidneys: results from an international multicenter collaboration. Eur Urol 2021; 79(1): 133–140. doi: 10.1016/j.eururo.2020.09.012.
10. European Association of Urology. EAU Guidelines on Renal Cell Carcinoma 2024. [online]. Available from: https://uroweb.org/guidelines/renal-cell-carcinoma.
11. Bex A, Jewett M, Lewis B et al. A call for a neoadjuvant kidney cancer consortium: lessons learned from other cancer types. Eur Urol 2025; 87(4): 385–389. doi: 10.1016/j.eururo.2025.01.007.
12. Allaf ME, Kim SE, Master V et al. Perioperative nivolumab versus observation in patients with renal cell carcinoma undergoing nephrectomy (PROSPER ECOG-ACRIN EA8143): an open-label, randomised, phase 3 study. Lancet Oncol 2024; 25(8): 1038–1052. doi: 10.1016/S1470-2045(24)00211-0.
13. Motzer RJ, Rini BI, McDermott DF et al. Nivolumab plus ipilimumab versus sunitinib in first-line treatment for advanced renal cell carcinoma: extended follow-up of efficacy and safety results from a randomised, controlled, phase 3 trial. Lancet Oncol 2019; 20(10): 1370–1385. doi: 10.1016/S1470-2045(19)30413-9.
Štítky
Detská urológia Nefrológia Urológia
Článok vyšiel v časopiseČeská urologie
Najčítanejšie tento týždeň
2026 Číslo 1- Aktuálne európske odporúčania pre liečbu renálnej koliky v dôsledku urolitiázy
- MUDr. Šimon Kozák: V algeziológii nič nefunguje zázračne cez noc! Je dôležité nechať si poradiť od špecialistov
- Vyšetření T2:EGR a PCA3 v moči při záchytu agresivního karcinomu prostaty
- Lék v boji proti benigní hyperplazii prostaty nyní pod novým názvem Adafin
-
Všetky články tohto čísla
- 30. ročník časopisu
- Když guidelines nestačí
- Verifikace ischemie ledviny při selektivním klampování větve renální tepny při robotické resekci tumoru ledviny pomocí ICG a NIR zobrazení – video
- Robotem asistovaná enukleace prostaty – alternativa transvezikální prostatektomie pro výrazně zvětšenou prostatu
- Roboticky asistovaná transvezikální prostatektomie – video
- Roboticky asistovaná nefroureterektomie (RA-NUE) – video
- Retrospektivní unicentrická studie mikrovlnné ablace v terapii cT1 renálních karcinomů
- Roboticky asistovaná Anderson-Hynesova pyeloplastika pro obstrukci pyeloureterální junkce u dětí
- Kombinace systémové a chirurgické léčby u pacienta s primárně inoperabilním renálním karcinomem podkovovité ledviny: význam multioborové spolupráce – aktualizované výsledky 3letého sledování
- Retrokavální ureter
- Zpráva z 2. vinohradského kazuistického dne
- Zpráva z uroonkologické sekce konference PragueONCO 2026
- Pokyny pro autory
- Česká urologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Retrospektivní unicentrická studie mikrovlnné ablace v terapii cT1 renálních karcinomů
- Verifikace ischemie ledviny při selektivním klampování větve renální tepny při robotické resekci tumoru ledviny pomocí ICG a NIR zobrazení – video
- Roboticky asistovaná nefroureterektomie (RA-NUE) – video
- 30. ročník časopisu
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



