-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Sledování bezpečnosti a účinnosti přípravku amisulpridu (Solian®) v podmínkách běžné klinické praxe
Monitoring Safety and Efficiency of the Preparation Amisulpride (Solian®) in Common Clinical Practice
The tolerability and safety of amisulpride (f.o. Solian®) has been followed for 3 months in 2 135 out-patients with schizophrenia. Totally 2 963 of side - effects in 1 243 treated (e.g. 58.22% of all treated) were observed. 2 437 side effects (82.24%) were evaluated as mildly severe, 499 (16.84 %) as moderately severe and 27 (0.91 %) as severe. According to expectation, the most frequently observed side-effects were fatigue and drowsiness (23.39), further insomnia (14.75 %) and anxiety (14.65% of all side-effects). On the other side few prolactin-dependent side-effects have been observed (6.40 % of all side-effects in 8.38 % of treated). The occurrence of menstrual abnormalities has been very rare, only in 3 cases (0.26% of all women into the study), which might be explained by the age of women included. There was a high dependence of side effects occurrence on concomitant medication. Whatever co-medication has increased significantly the occurrence of 4 out of 8 most frequently observed side effects, e.g. insomnia, fatigue and drowsiness, anxiety and extrapyramidal symptoms. Both positive and negative symptoms were improved during the 3-months therapy. With a mean daily dose of 476.6 ±176.49 mg a very good and good effect on negative symptoms was seen in 88.43% of treated, on positive symptoms in 88.24% of treated.
Key words:
amisulpride, adverse events, positive and negative symptoms in schizophrenia.
Autoři: E. Češková; J. Suchopár 1
Působiště autorů: Psychiatrická klinika LF MU a FN, Brno přednostka prof. MUDr. E. Češková, CSc. ; Infopharm a. s., Praha 1
Vyšlo v časopise: Čes. a slov. Psychiat., 105, 2009, No. 2, pp. 53-60.
Kategorie: Původní práce
Souhrn
Po dobu 3 měsíců byla sledována bezpečnost a účinnost podávání amisulpridu (f.o. Solian®) u 2135 nemocných se schizofrenií. Bylo zaznamenáno celkem 2963 nežádoucí účinky u 1243 pacientů, tj. 58,22 % všech léčených. 2437 nežádoucích účinků (82,24 %) bylo hodnoceno jako málo intenzivních, 499 (16,84 %) jako středně intenzivních a 27 (0,91 %) jako velmi intenzivních. Dle očekávání nejčastějším nežádoucím účinkem byla únava nebo ospalost (celkem 23,39 % všech nežádoucích účinků), dále nespavost (4,75 % všech nežádoucích účinků) a úzkost (14,65 % všech nežádoucích účinků). Na druhou stranu bylo zaznamenáno relativně málo nežádoucích účinků souvisejících s hyperprolaktinémií (6,40 % všech nežádoucích účinků u 8,38 % léčených). Výskyt poruch menstruačního cyklu byl vzácný, byly pozorovány pouze 3 případy (0,26 % všech pacientek zařazených do sledování), což je vysvětlitelné relativně vyšším věkem léčených žen. Byla nalezena statisticky významná závislost výskytu některých nežádoucích účinků a souběžně podávaného léčiva. Jakákoli souběžná medikace statisticky významně zvyšovala výskyt čtyř z osmi nejčastěji uváděných nežádoucích účinků, tj. nespavosti, únavy a ospalosti, úzkosti a extrapyramidových příznaků. Během tříměsíční terapie bylo pozorováno zlepšení pozitivních i negativních symptomů schizofrenie. V případě negativních symptomů byl efekt terapie hodnocen jako velmi dobrý a dobrý u 88,43 % pacientů, v případě pozitivních symptomů u 88,24 % pacientů při průměrné dávce amisulpridu 476,60±176,49 mg denně.
Klíčová slova:
amisulprid, nežádoucí účinky, pozitivní a negativní symptomy schizofrenie.ÚVOD
Přípravek Solian® obsahuje léčivou látku amisulprid. Amisulprid je blokátor dopaminových receptorů D2 a D3. Je indikován k léčbě akutní i chronické schizofrenie. Souhrnně bylo o něm referováno i v naší literatuře [2, 25, 19]. Výsledky novějších metaanalýz naznačují, že amisulprid patří k relativně účinnějším antipsychotikům (AP) 2. generace [8, 12]. Amisulprid je v rámci AP 2. generace jedinečný vzhledem k svému účinku – v nižších dávkách významně ovlivňuje depresivní a negativní příznaky, ve vyšších dávkách pozitivní symptomatologie [5].
Randomizované kontrolované studie jsou tradičně zlatým standardem. Jsou prováděny s cílem prokázat rozdíl mezi léčebnými postupy a jsou rozhodující pro registraci v dané indikaci. Nejde však o reprezentativní vzorek nemocných a zkoušejících a závěry často nejsou aplikovatelné na heterogenní populaci v běžné klinické praxi. Populace schizofreniků do nich zahrnutých bývají mladší, s časnějším začátkem nemoci, menším počtem proběhlých epizod. Vyřazovací kritérium bývá nonkompliance a komorbidita [9]. Naproti tomu observační studie reflektují běžnou klinickou praxi. K jejich nevýhodám patří heterogenní populace a nejednotná metodika, prospektivní studie nemívají referenční skupiny. Dnes jsou randomizované kontrolované studie a observační studie považovány za komplementární. Je nepochybné, že teprve podávání v realitě všedního dne prověří kvality nového psychofarmaka. V ČR firma vyrábějící amisulprid iniciovala observační studii zabývající se sledováním bezpečnosti a účinnosti přípravku Solian® v podmínkách běžné klinické praxe (projekt byl označen 006-2006-SOL).
VLASTNÍ STUDIE
CÍLE
Hlavním cílem projektu bylo zjištění výskytu nežádoucích účinků a tolerance přípravku Solian® v ambulantní praxi. Osloveni byli psychiatři pracující v ambulantních zařízeních.
METODIKA
Výběr pacientů
Jediným kritériem pro zařazení do studie bylo podávání amisulpridu. Nebyla stanovena žádná vylučovací kritéria. Do sledování mohl být zařazen každý pacient již léčený přípravkem Solian® dle rozhodnutí jeho lékaře. Délka sledování byla 3 měsíce u každého pacienta.
Hodnocení
Bylo prováděno pomocí dotazníku. Lékař vyplnil pro každého zařazeného pacienta dotazník. Základní okruhy informací obsažených v dotazníku:
Identifikace lékaře a pacienta, charakteristika onemocnění, tělesná hmotnost a obvod pasu (pokud byly měřeny) na začátku a na konci sledování, výskyt nežádoucích účinků, doba objevení se nežádoucích účinků (a informace zda byl nežádoucí účinek lékařem ohlášen Státnímu ústavu pro kontrolu léčiv v Praze), základní charakteristika účinnosti (účinek na pozitivní a negativní symptomy onemocnění).
Statistické zpracování
Kvantitivní údaje jsou prezentovány průměrem ± směrodatná odchylka, ostatní údaje jsou popsány četností a procentuální četností. Pro porovnání rozdílu kvantitativních údajů byl použit dvouvýběrový t-test, případně neparametrické Mann-Whitney nebo Kolmogorov-Smirnov test, dále neparametrický Wilcoxonův párový test. Pro hodnocení souvislosti kvalitativních veličin byl použit χ2 test nezávislosti v kontingenční tabulce. Hladina významnosti byla zvolena α=0,05.
VÝSLEDKY
Studie probíhala od 1. 4. 2006 do 30. 11. 2006, na sběru dat se podílelo 274 ambulantních psychiatrů.
Charakteristika souboru
Bylo zařazeno celkem 2135 pacientů, z toho bylo 1133 žen (53,07 %) a 1002 (46,93 %) mužů. Průměrný věk činil 41,27±13,76 roku (rozpětí 15-90 let), z toho u žen 43,72±14,13 roku a u mužů 38,50±12,79 roku, což je statisticky významně odlišné (p<0,001). Ve věkové struktuře podle jednotlivých decennií převažovali pacienti ve věku 21-30 let (n=535, tj. 25,06 %), následovali pacienti ve věku 31-40 let (n=517, tj. 24,22 %), ve věku 41-50 let (n=451, 21,12 %) a ve věku 51-60 let (n=401, 18,78 %).
Onemocnění schizofrenií (nebyly hodnoceny jednotlivé formy schizofrenie) trvalo průměrně u všech nemocných 9,74±8,5 roku a bylo průměrně delší u žen (10,33±8,94) než u mužů (9,08±7,94), což se statisticky významně liší (p=0,0295). Nejvyšší zastoupení měli pacienti s onemocněním trvajícím do 1 roku (n=351, tj. 16,44 %), následovaní skupinou s trváním onemocnění 2-3 roky (n=324, tj. 15,18 %).
Z přidružených onemocnění se nejčastěji vyskytovala dyslipidémie, která postihovala 220 pacientů (tj. 10,30 %), dále se často vyskytoval diabetes (n=109, tj. 5,11 %) a porušená glukózová tolerance (n=111, tj. 5,20 %). Celkem 857 pacientů (tj. 40,14 %) byli kuřáci. U 184 pacientů bylo uvedeno, že mají sklon k alkoholismu a u dalších 110 pacientů (tj. 5,15 %) bylo uvedeno, že mají sklon k užívání jiných návykových látek.
Léčba
Dávkování
Průměrná dávka amisulpridu činila 476,60± 176,49 mg denně (50 - 1200 mg denně). Nejčastější dávkování bylo 400 mg denně (n=988, tj. 46,28 %), následováno dávkováním 600 mg denně (n=555, 26,00 %), 800 mg denně (n=163, 7,63 %), 200 mg denně (n=153, 7,16 %) a dávkováním 300 mg (n=105, 4,91 %). Výše dávky se statisticky významně lišila vzhledem k pohlaví a komorbiditě. Muži měli signifikantně vyšší dávky než ženy (490,8 ±180,0 vs. 464,0±172,4; p<0,001). Nemocní s porušenou glukózovou tolerancí, kuřáci a pravidelní konzumenti alkoholu měli také významně vyšší dávky než nemocní bez těchto komorbidit (tab. 1).
Tab. 1. Faktory ovlivňující výši dávky léčivého přípravku Solian®. 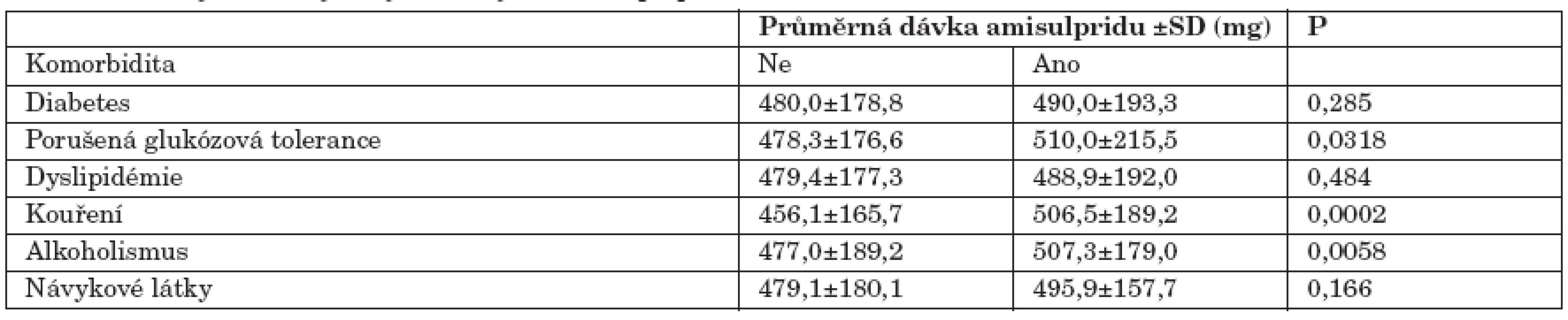
Předchozí léčba
Terapie antipsychotiky byla v minulosti zaznamenána u celkem 1610 pacientů (tj. 75,41 %), z toho u 1481/1610 (91,9 %) byla podávána atypická antipsychotika.
Současná přídatná léčba
Z tzv. psychiatrických léčiv bylo podáváno celkem 2398 léčivých přípravků. Nejčastěji byla současně s amisulpridem podávána antidepresiva (n=721, tj. 33,7 % zařazených nemocných), zejména ze skupiny specifických inhibitorů zpětného vychovávání serotoninu, SSRI (n=428, tj. 59,5 % všech léčených současně antidepresivy) a z nich pak nejčastěji sertralin (n=160) a citalopram (n=141); dále benzodiazepinová anxiolytika (n=576, tj. 27 % zařazených), z nich nejvíce byl podáván klonazepam (n=366) a alprazolam (n=101). Z antipsychotik (n=571, tj. 26,7 % zařazených) převažovala AP 1. generace (n=426) s nejčastějším podáváním levomepromazinu (n=139). Ze stabilizátorů nálady (n=328, tj. 15,5 % zařazených), byl preferován valproát (n=143), dále lamotrigin (n= 88), karbamazepin (n=58) a lithium (n=39) (tab. 2).
Tab. 2. Souběžná medikace tzv. psychiatrickými léčivy. 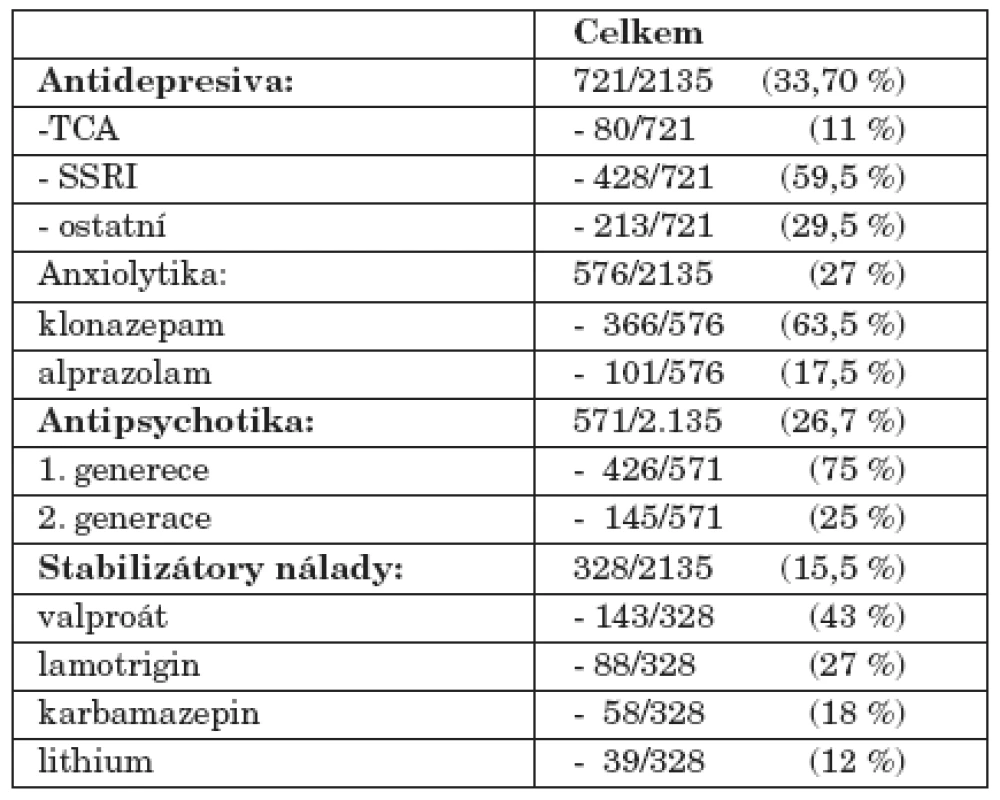
Z tzv. nepsychiatrických léčiv dominovala kardiovaskulární léčiva používaná při terapii hypertenze (metoprolol) a dyslipidémie (simvastatin).
NEŽÁDOUCÍ ÚČINKY
Celkem byly pozorovány 2963 nežádoucí účinky u 1243 (58,22 %) léčených. U 417 (19,53 %) byl pozorován jeden nežádoucí účinek, u 349 (16,34 %) byly pozorovány dva, u 231 (10,82 %) byly pozorovány tři, u 145 (6,79 %) byly pozorovány čtyři, u 50 (2,34 %) bylo pozorováno pět , u 37 (1,73 %) šest, u 9 (0,42 %) sedm a u 5 ( 0,23 %) bylo pozorováno osm nežádoucích účinků.
Lékaři označili 2437 (tj. 82,25 %) nežádoucích účinků jako málo intenzivních, 499 jako středně intenzivních (tj. 16,84 %) a 27 nežádoucích účinků jako velmi intenzivních (tj. 0,91 %). Byl pozorován pouze jeden závažný nežádoucí účinek, který spontánně odezněl po ukončení terapie, bez nutnosti jakýchkoli dalších intervencí. Velmi často (≥ 10 %), často (≥ 1 %) a méně často (≥ 0,1 %) se vyskytovalo 8 následujících nežádoucích účinků (uvedeno v sestupném pořadí):
- 1. Nejčastějším nežádoucím účinkem byla únava nebo ospalost, která se vyskytla v 693 případech (32,46 % všech pacientů zařazených do sledování) a tvořila celkem 23,39 % všech nežádoucích účinků; středně a velmi intenzivní únava a ospalost se vyskytla u 138 (6,46 %) zařazených a tvořila 4,66 % všech nežádoucích účinků.
- 2. Druhým nejčastějším nežádoucím účinkem byla nespavost, která se vyskytla u 437 (20,47 %) léčených a tvořila celkem 14,75 % všech nežádoucích účinků. Středně a velmi intenzivní nespavost se vyskytla v 98 případech (4,59 % všech pacientů) a tvořila 3,31 % všech nežádoucích účinků.
- 3. Třetím nejčastějším nežádoucím účinkem byla úzkost, která se vyskytla v 434 případech (20,33 % všech pacientů zařazených do sledování) a tvořila celkem 14,65 % všech nežádoucích účinků; středně a velmi intenzivní úzkost se vyskytla v 64 případech (3,00 % léčených) a tvořila 2,16 % všech nežádoucích účinků.
- 4. Čtvrtým nejčastějším nežádoucím účinkem bylo zvyšování tělesné hmotnosti, které se vyskytlo v 359 případech (16,81 % všech zařazených) a tvořilo 12,12 % nežádoucích účinků. Středně a velmi intenzivní zvyšování tělesné hmotnosti se vyskytlo v 73 případech (3,42 % zařazených) a tvořilo 2,46 % všech nežádoucích účinků. Hmotnost byla dále měřena před vstupem a na konci sledování u 1318 l (61 %) léčených. U mužů činila průměrná hmotnost před vstupem do sledování (n=587) 83,57±13,05 kg a po minimálně tříměsíčním podávání amisulpridu činila 84,40±12,98 kg, což byl statisticky významný nárůst (p<0,001). U žen byla hmotnost před sledováním (n=731) 71,66±12,77 kg, za tři měsíce 72,81±12,88 kg, což byl statisticky významný nárůst (p<0,001).
Obvod pasu byl sledován před vstupem a na konci sledování u 303 léčených (14,19 %). Průměrný obvod pasu před vstupem do sledování u mužů činil (n=151) 94,43±20,62 a po minimálně tříměsíční léčbě činil 92,62±14,47, což nebylo statisticky významné. Průměrný obvod pasu u žen před sledováním byl (n=152) 82,18±15,82, po tříměsíčním sledování byl 81,89±13,84, což bylo statisticky významné snížení (p<0,05). Hmotnost u této skupiny nemocných u mužů byla na začátku sledování 86,36 ±14,33 a po třech měsících 86,88 ±14,00 (p<0,05), u žen 72,13 ±14,56, respektive 73,24 ± 14,93 (p<0,001).
- 5. Bolest hlavy se vyskytovala u 354 (16, 58 % léčených) a tvořila 11,04 % všech vedlejších příznaků, střední a velmi intenzivní u 27 (1,2 % léčených), tj. 0,91 % všech nežádoucích účinků.
- 6. Extrapyramidová symptomatologie (EPS) se vyskytla u 304 (14,24 % léčených) a tvořila 10,26 % všech nežádoucích účinků, střední a závažné intenzity u 57 (2,67 %) léčených, tj. 1,92 % všech nežádoucích účinků.
- 7. Nežádoucí účinky amisulpridu vyvolané zvýšením hladin prolaktinu: bolesti prsů, gynekomastie a/nebo galaktorea se vyskytly u 179 (8,38 %) zařazených do sledování a tvořily celkem 6,04 % všech nežádoucích účinků. Středně a velmi intenzivní bolesti prsů, gynekomastie a/nebo galaktorea se vyskytly ve 33 (1,55 % všech pacientů zařazených do sledování) případech a tvořily 1,11 % všech nežádoucích účinků. Zvláště byl hodnocen výskyt poruch menstruačního cyklu, který byl pozorován u 3 (0,26 %) žen zařazených do sledování), tj. 0,10 % všech nežádoucích účinků.
- 8. Hyperkineze byla pozorována u 151 (7,06 %) léčených, tj. 5,09 % všech nežádoucích účinků, střední a závažná intenzita v 17 případech a tvořily 0,59 % všech nežádoucích účinků. Souhrnně je uveden jejich výskyt a intenzita v tabulce 3.
Tab. 3. Výskyt a intenzita pozorovaných nežádoucích účinků při léčbě amisulpridem (v sestupném pořadí dle výskytu u zařazených nemocných (n=2135). 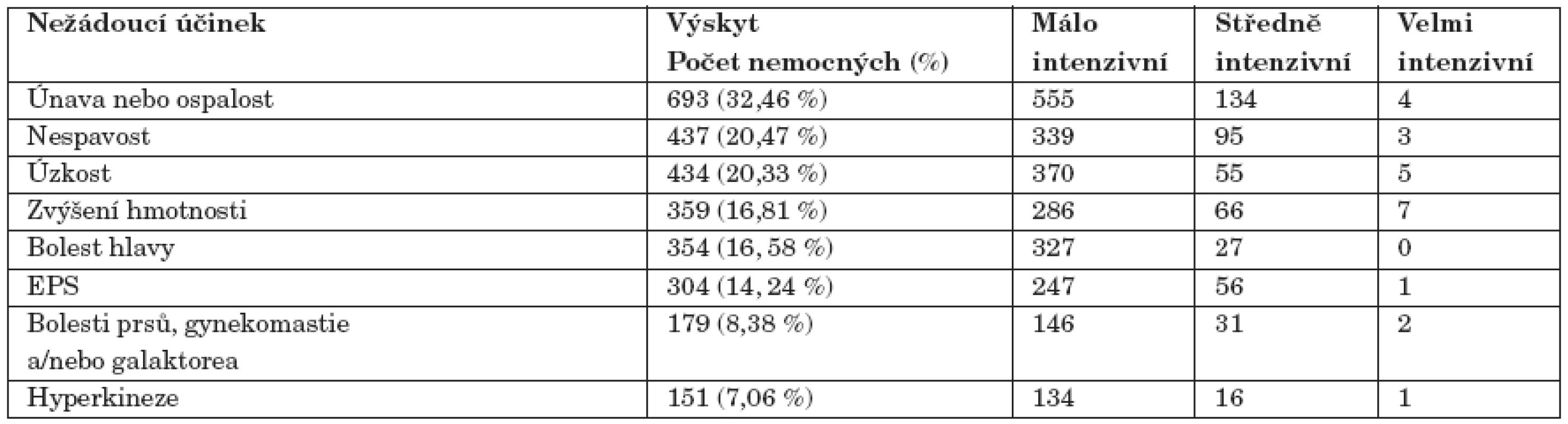
CELKOVÝ VÝSKYT NEŽÁDOUCÍCH ÚČINKŮ
Celkový výskyt nežádoucích účinků statisticky významně nesouvisel s věkem ani pohlavím, ale s výší dávky sledované populace. Nemocní s nežádoucími vedlejšími účinky měli signifikantně vyšší dávky amisulpridu (p<0,001).
Jednotlivé nežádoucí účinky
Z jednotlivých vedlejších účinků měli vyšší dávky amisulpridu nemocní s výskytem nespavosti (p<0,05), únavy a ospalosti (p<0,05) a zvyšováním tělesné hmotnosti (p<0,001). Výskyt bolesti prsů, gynekomastie anebo galaktorea byl statisticky významně častější u žen (p<0,001).
U pacientů současně užívajících jiné léčivé přípravky byl zaznamenán statisticky významně vyšší výskyt únavy a ospalosti (p<0,001) i nespavosti (p<0,001), úzkosti (p<0,001), EPS (p<0,05) a zvyšování hmotnosti (p<0,05) ve srovnání s pacienty, kteří žádné další léčivé přípravky neužívali (tab. 4).
Tab. 4. Současná komedikace jakýmkoliv léčivým přípravkem a výskyt nežádoucích účinků. 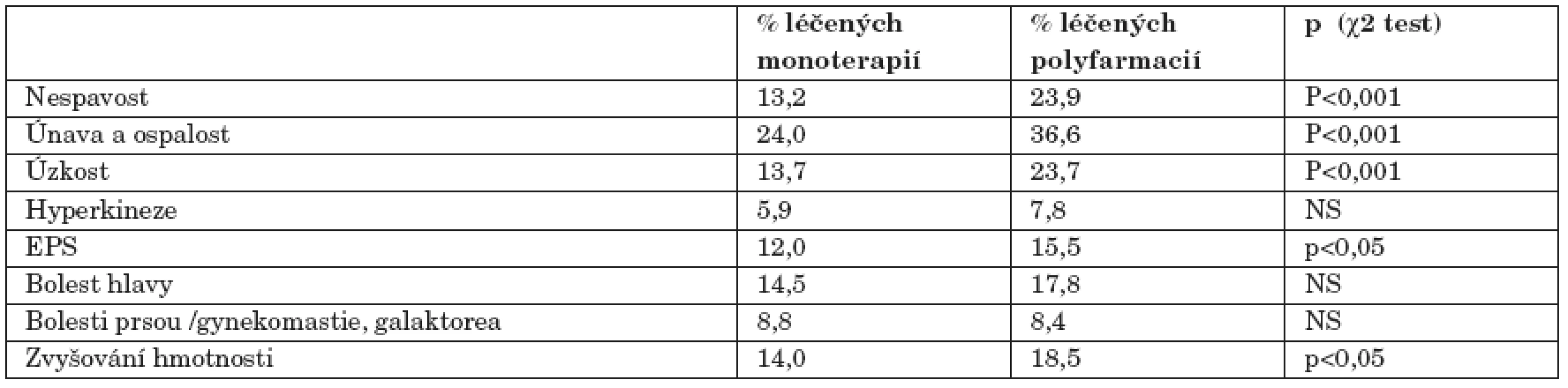
U 411 pacientů (tj. 19,25 %) se nežádoucí účinky vyskytly během prvního týdne podávání amisulpridu, u 601 pacientů (tj. 28,15 %) v období od 2. týdne do konce prvního měsíce a u 128 pacientů (tj. 6,00 %) se nežádoucí účinky objevily v období od 2. měsíce po zahájení podávávání amisulpridu.
ÚČINNOST
Z hlediska ovlivnění negativních a pozitivních symptomů základního onemocnění byl v případě negativních symptomů efekt terapie amisulpridem hodnocen jako velmi dobrý u 902 pacientů (tj. 42,25 %) a dobrý u 986 pacientů (tj. 46,18 %), tedy klinicky významný vliv u 88,43 % pacientů. Naopak dostatečný a nedostatečný efekt terapie u negativních symptomů byl pozorován u 92 pacientů (tj. 4,31 %). V případě pozitivních symptomů byl efekt terapie hodnocen jako velmi dobrý u 1059 pacientů (tj. 49,60 %) a dobrý u 825 pacientů (tj. 38,64 %), celkem tedy u 88,24 % pacientů. Naopak dostatečný a nedostatečný efekt terapie u negativních symptomů byl pozorován u 59 pacientů (tj. 2,76 %) (tab. 5).
Tab. 5. Vliv terapie amisulpridem na negativní a pozitivní symptomy schizofrenie dle hodnocení psychiatrů. 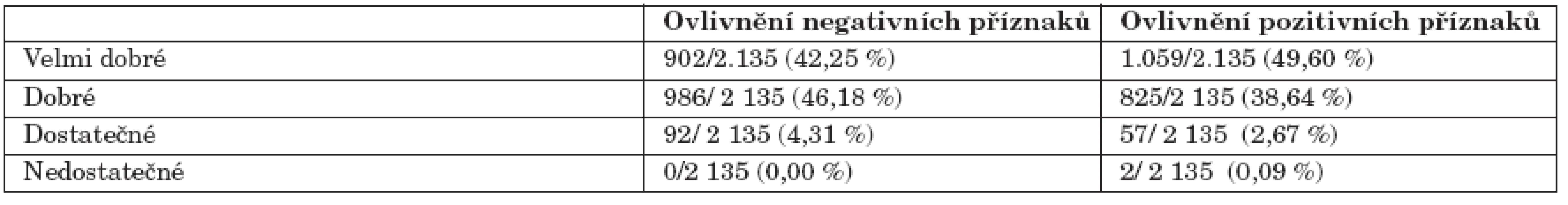
DISKUSE
Do naturalistické studie byli nejčastěji zařazováni pacienti středního věku, s trváním nemoci 9 roků, většinou již léčeni antipsychotiky. 25 % nemocných bylo ve věkové kategorii 21-30 roků a stejné procento nebylo dosud antipsychotiky léčeno, což ukazuje, že u těchto nemocných byl amisulprid lékem první volby. V našem souboru byly ženy významně starší než muži a tomu částečně odpovídalo i delší trvání nemoci. Tento údaj není překvapující vzhledem k tomu, že u žen začíná onemocnění později a bývá méně devastující.
Naše výsledky ukazují, že psychicky nemocní jsou zatíženi relativně vysokou tělesnou morbiditou. Dyslipidémie byla zjištěna u 10,30 %, diabetes u 5,11 % a porušená glukózová tolerance u 5,20 % léčených. Tyto údaje potvrzuje somatická komedikace. Zjištěné údaje jsou do určité míry podobné publikovaným studiím. Např. ve studii CATIE (Clinical Antipsychotic Trials of Intervention Effectiveness) se u nemocných s chronickou schizofrenií a průměrným věkem 40 roků hyperlipidémie vyskytovala u 12-17 %, diabetes typu 1 nebo 2 u 9 až 12 %, hypertenze u 17-20 % [14]. V našem souboru jsme nalezli vysoké procento kuřáků (40,14 %) a nemocných se sklonem k alkoholismu či nadužívání jiných návykových látek (15 %). Ve studii CATIE mělo problém s alkoholem 20-27 %. Ve studii ZODIAC, observační studii zabývající se kardiální prognózou u nemocných se schizofrenií, mělo bazálně 18 % zařazených nemocných hypertenzi, 15 % hyperlipidémii, 7,7 % diabetes a 46,5 % bylo kuřáků [24].
Průměrná dávka amisulpridu byla 476,60± 176,49 mg denně, což vcelku dobře koresponduje s denní definovanou dávkou stanovenou Světovou zdravotnickou organizací (400 mg). U žen byla zaznamenána významně nižší průměrná denní dávka, což není překvapující vzhledem k antropologickým rozdílům a lepšímu průběhu onemocnění. Kuřáci, nemocní inklinující k abúzu a jedinci s narušenou glukózovou tolerancí, měli signifikantně vyšší průměrné denní dávky. O kouření i alkoholu je známo, že jsou metabolickými induktory, avšak amisulprid je primárně vylučován močí a je relativně minimálně metabolizován [23]. Vysvětlení může spočívat v tom, že u nemocných s abúzem obecně se jedná o závažnější onemocnění vyžadující vyšší dávkování. Pokud se týká narušené glukózové tolerance, je nutné také brát v úvahu závažnost onemocnění.
Polyfarmacie je v podmínkách reality všední praxe vysoká. V našem souboru byla u jedné třetiny nemocných podávána současně antidepresiva a u jedné čtvrtiny anxiolytika. Z antidepresiv byla nejvíce zastoupena SSRI, která patří k nejvíce předepisovaným antidepresivům vůbec. Kombinace AP byla zaznamenána u 26,7 %. Téměř identické procento jsme zjistili při retrospektivní analýze chorobopisného materiálu nemocných se schizofrenní psychózou hospitalizovaných na Psychiatrické klinice FN v Brně v r. 2000. 27 % nemocných již přicházelo k hospitalizaci s kombinací AP [3].
Nežádoucí účinky byly pozorovány u více než poloviny léčených (58,22 %). Nejčastěji byl pozorován jeden (19,53 %) nebo dva nežádoucí účinky (tj. 16,34 % léčených). Vedlejší účinky byly převážně mírné intenzity (82,25 % všech pozorovaných vedlejších účinků). Frekvence výskytu jednotlivých nežádoucích účinků byla v souhlase s SPC a literaturou.
Nejčastějšími byly hypersomnie a únava, které se vyskytovaly u třetiny léčených a insomnie a úzkost u jedné pětiny léčených. Tyto významně souvisely s komedikací ve smyslu zvýšení jejich incidence. Poruchy spánku a únava také významně souvisely s dávkou amisulpridu. Výskyt v našem souboru je vyšší než udávaný v komparativních studiích a přehledech [7], nutno však vzít v úvahu vliv komedikace a dále skutečnost, že střední a silná intenzita potíží byla pozorována u > 7 % léčených.
Do středu pozornosti se dostávají zejména metabolické nežádoucí účinky a z těchto konkrétně zvyšování hmotnosti. Je to dáno skutečností, že nemocní se schizofrenií jsou rizikovou skupinou. Očekávaná délka života je o 20 % kratší (57 roků muži, 65 roků ženy), nacházíme u nich zvýšenou morbidita a mortalitu na kardiovaskulární onemocnění, prevalence diabetu a obezity je u nich 1,5 - 2,0x vyšší. Není jasné, zda je schizofrenie sama o sobě zodpovědná za zvýšenou prevalenci metabolických abnormit. AP mohou dále přispívat ke zvýšenému riziku tím, že způsobují metabolické vedlejší účinky [1].
V naší studii byla z metabolických parametrů sledována u části souboru (61 %) hmotnost a parametr ukazující na množství břišního tuku, tj. obvod pasu (15 % léčených). U mužů došlo v průměru ke zvýšení hmotnosti o 0,83 kg a u žen o 1,15 kg, což je statisticky signifikantní. Klinická relevance takového nárůstu hmotnosti je malá, i když určitý trend naznačuje. U těch nemocných, u kterých byl měřen obvod pasu, došlo jak u mužů tak i u žen ke zmenšení, které u žen dosahovalo hranice významnosti, avšak jejich hmotnost se zvýšila. Tento rozpor je vysvětlitelný pochopitelnými nepřesnostmi v měření obvodu pasu a údaje nelze smysluplně interpretovat. Podávání AP, zvláště některých atypických, je spojeno s výrazným přírůstkem hmotnosti a do určité míry tomu korespondujícím zvýšeným rizikem rozvoje dyslipidémie a diabetu. Nejvyšší je toto riziko u klozapinu a olanzapinu. Amisulprid ve dvojitě slepém srovnání s olanzapinem signifikantně méně zvyšoval hmotnost po 2 měsících podávání (2,7 ± 3,9 kg vs 0,9 ± 3,2 kg) i po 6 měsících (3,9 ±5,3 vs. 1,6± 4,9 kg) [16, 18]. Amisulprid také na rozdíl od olanzapinu vedl k signif. snížení glykémie [18]. V prospektivní, otevřené studii srovnávajících amisulprid, ziprasidon, klozapin a olanzapin po dobu 4 týdnů bylo zjištěno, že u léčených amisulpridem a ziprasidonem došlo ke snížení BMI, celkového cholesterolu a ke zvýšení HDL cholesterolu [21]. Přírůstek hmotnosti spojený s léčbou přispívá ke snížení kompliance a kvality života a zvýrazňuje stigmatizaci. Nejlepší léčbou metabolických vedlejších účinků je prevence a ta spočívá na prvním místě ve správné volbě AP a pravidelném monitorování. Dopaminoví antagonisté by mohli být skupinou s minimálním rizikem. Tento fakt je již v povědomí psychiatrů. Více než tři čtvrtiny dotazovaných lékařů uvádělo jako důvod změny z olanzapinu na amisulprid přírůstek hmotnosti na olanzapinu nebo očekávání, že amisulprid je spojen s menším přírůstkem hmotnosti [15]. Pokud se týká kvalitativního hodnocení přírůstku hmotnosti, výskyt v našem souboru (12%) odpovídá literárním údajům, zvláště když vezmeme v úvahu, že středně a velmi intenzivní zvyšování tělesné hmotnosti se vyskytlo pouze u 3,42 % zařazených [7]
Z AP 2. generace je amisulprid, podobně jako risperidon, spojován s výskytem EPS v souvislosti s výší dávky a s prolaktin-dependentními nežádoucími účinky. EPS se vyskytly v naší studii u 14,24 %, avšak střední a závažné intenzity dosahovaly pouze u 2,67 % léčených. V našem použitém rozmezí dávek amisulpridu udává literatura výskyt v rozmezí 10-40 % léčených [20]. Amisulprid má podobný výskyt EPS jako risperidon [22] a ve srovnání s typickými AP méně EPS, což se také odráží v nižším užití anticholinergik a nižším výskytu drop-outů [11].
Prolaktin-dependentní nežádoucí účinky, tj. bolesti prsů, gynekomastie a/nebo galaktorea, se vyskytly u 8,38 %, střední a velká intenzita se vyskytla u 1,55 % všech zařazených léčených. Výskyt prolaktin – dependentních účinků se udává při podávání amisulpridu mezi 6-10 % [6, 26], což je v souhlasu s našimi údaji. Výskyt poruch menstruačního cyklu byl vzácný, celkem byly pozorovány pouze u 3 (0,26 % všech pacientek zařazených do sledování) léčených, tj. 0,10 % všech nežádoucích účinků. V literatuře bývá udáván vyšší výskyt, kolem 6 % [17]. Naše údaje mohou být vysvětlitelné věkovým složením pacientek – průměrný věk 43 roků.
Hyperkineze nebyla podrobněji specifikována a zahrnovala široké spektrum občasných nepřiměřených svalových pohybů, včetně tardivní dyskineze. Lze předpokládat, že jasně vyjádřená tardivní dyskineze byla v 17 uvedených případech (0,59 % všech nežádoucích účinků).
Nalezené vztahy mezi výskytem nežádoucích účinků a výší dávky jsou očekávatelné. Zajímavé je zjištění většího výskytu nespavosti, únavy a ospalosti, ale také úzkosti, EPS a zvyšování hmotnosti u nemocných se současnou komedikací. Nepochybně vzájemné vztahy budou oboustranné a komplexní, nicméně polyfarmacie je stále častější a je nutné si uvědomit, že někdy kombinace léků mohou být kontraproduktivní [4, 10].
V naší studii byl velmi dobře hodnocen vliv amisulpridu na negativní symptomatologii. Dle lékařů byl u 88,4 % léčených (tj. stejně jako u pozitivních příznaků) pozorován velmi dobrý a dobrý efekt u negativních příznaků. Toto koresponduje s literárními údaji. Amisulprid jako ostatní atypická AP byl minimálně stejně účinný jako typická AP v ovlivnění pozitivních příznaků, v ovlivnění negativních příznaků byl lepší nejen než placebo, ale také než typická AP [13].
ZÁVĚR
Amisulprid lze považovat za dobře tolerované atypické antipsychotikum. Z hlediska snášenlivosti je charakterizován nízkým přírůstkem hmotnosti a zřejmě i minimálním rizikem pro rozvoj metabolických vedlejších účinků, které však byly doposud u tohoto přípravku málo cíleně sledovány. Z hlediska účinnost lze vyzvednout jeho dobrý účinek nejen na pozitivní ale i na negativní symptomatologii.
Poděkování
Dovoluji si tímto poděkovat všem ambulantním psychiatrům, kteří se na studii podíleli a RNDr. Čermákové za statistické zpracování.
Finanční podpora Výzkumným záměrem
MSM0021622404.
Prof. MUDr. Eva Češková, CSc.
Psychiatrická klinika LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: eceska@med.muni.cz
Zdroje
1. Capasso, R. M., Lineberry, T. W., Bostwick, J. M. et al.: Mortality in schizophrenia and schizoaffective disorder: an Olmsted County, Minnesota cohort: 1950-2005. Schizophr. Res., 98, 2008, pp. 287-295.
2. Česková, E.: Amisulprid – nové benzamidové antipsychotikum II. generace (Souhrnné sdělení). Čes. a slov. Psychiat., 96, 2000, s. 418-415.
3. Češková, E., Kašpárek, T., Ondrušová, M.: Kombinace antipsychotik. Čes. a slov. Psychiat., 97, 2001, 6, s. 286-290.
4. Češková, E.: Kombinace antidepresiv. Remedia, 15, 2005, 6, s. 520-524.
5. Češková, E.: Deniban v léčbě dystymie. Čes. a slov. Psychiat., 103, 2007, s. 73-79.
6. Collona, L., Saleem, P., Donde-Nouvel, L., Rein, W.: Long-term safety and efficacy of amisulpride in subchronic or chronic schizophrenia. Int. Clin. Psychopharmacol., 14, 1999, pp. 1-10.
7. Coulouvrat, C., Dondey-Nouvel, L.: Safety of amisulpride (Solian): a review of 11 clinical studies. Int. Clin. Psychopharmacol., 14, 1999, pp. 209-218.
8. Davis, J. M., Chen, N., Glick, I. D.: A meta-analysis of the efficacy of second generation antipsychotics. Arch. Gen. Psychiatry, 60, 2003, pp. 553-563.
9. Hoffer, A., Hummer, M., Huber, R. et al.: Selection bias in clinical trials with antipsychotics. J. Clin. Psychopharmacol., 20, 2000, pp. 699-702.
10. Lam, R. W., Wan, D. D., Cohen, N. L., Kennedy, S. H.: Combining antidepressants for treatment-resistant depression: a review. J. Clin. Psychiatry, 63, 2002, pp. 685-693.
11. Leucht, S., Pitschel-Walz, G., Engel, R. R., Kissling, W.: Amisulpride, an unusual atypical antipsychotic: a meta-analysis of randomized controlled trials. Am. J. Psychiatry, 159, 2002, pp. 180-189.
12. Leucht, S., Barnes, T. R. E., Kissling, W. et al.: Relapse prevention in schizophrenia with new-generation antipsychotics: a systematic review and exploratory meta-analysis of randomized, controlled trials. Am. J. Psychiatry, 160, 2003, pp. 1209-1222.
13. Leucht, S.: Amisulpride, a selective dopamine antagonist and atypical antipsychotic: results of a meta-analysis of randomized controlled trials. Int. J. Neuropsychopharmacol., 7, 2004, suppl 1, S15-S20.
14. Lieberman, J. A., Stroup, T. S., McEvoy, J. P. et al.: Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N. Engl. J. Med., 353, 2005, pp. 1209-1223.
15. Linden, M., Eich, F. X., Pyrkosch, L.: Do differences in atypical antipsychotics matter in routine practice. Medication switch from olanzapine and risperidone to amisulpride. Int. Clin. Psychopharmacol., 22, 2007, pp. 175-178.
16. Martin, S., Ljo, H., Peuskens, J. et al.: SOLIANOL Study Group: A double-blind, randomised comparative trial of amisulpride versus olanzapine in the treatment of schizophrenia: short-term results at two months. Curr. Med. Res. Opin., 18, 2002, pp. 355-362.
17. Mortimer, A., Martin, S., Loo, H., Peuskens, J: SOLIANOL Study Group: A double-blind, randomized comparative trial of amisulpride versus olanzapine for 6 months in the treatment of schizophrenia. Int. Clin. Psychopharmacol., 19, 2004, pp. 63-69.
18. Peusken, J., De Hert, M., Mortimer, A.: For the SOLIANOL Study Group. Metabolic control in patients with schizophrenia treated with amisulpride or olanzapine. Int. Clin. Psychopharmacol., 22, 2007, pp.145-152.
19. Piderman, V., Látalová, K.: Amisulprid – mýty a fakta. Psychiatrie pro praxi, 5, 2004, s. 24-27.
20. Rein, W., Coulouvrat, C., Dondeys-Nouvel, L.: Safety profile of amisulpride in short-and long-term use. Acta Psychiatr. Scand., 101, 2000, pp. 23-27.
21. Rettenbacher, M. A., Ebenbichler, C., Hofer, A. et al.: Early changes of plasma lipids during treatment with atypical antipsychotics. Int. Clin. Psychopharmacol., 21, 2006, pp. 369-372.
22. Sechter, D., Peuskens, J., Fleuron, O. et al.: Amisulpride s tudy group: Amisulpride versus risperidone in chronic schizophrenia: results of a 6-month double-blind study. Neuropsychopharmacology, 27, 2002, pp. 1071-1081.
23. Spine, E., Delon, J.: Metabolic drug interactions with newer antipsychotics: a comparative review. Basic Clin. Pharmacol. Toxico, 100, 2007, pp. 4-22.
24. Strom, B. L., Faich, G. A., Reynolds, R. F. et al.: The Ziprasidone observational study of cardiac outocomes (ZODIAC): design and baseline subjekt characteristics. J. Clin. Psychiatry, 69, 2008, pp. 114-121.
25. Švestka, J.: Nová psychofarmaka. Amisulprid – atypický preparát ve skupině antipsychotik 2. generace. Psychiatrie, 3, 2000, s. 191-200.
26. Wetzel, H., Grunder, G., Hillert, A. et al.: Amisulpride versus flupenthixol in schizophrenia with predominantly positive symptomatology – a double-blind controlled study comparing a selective D2 like antagonist to a mixed D1/D2-like antagonist. Psychopharmacology, 137, 1998, pp. 223-232.
Štítky
Adiktológia Detská psychiatria Psychiatria
Článek REFERÁTY Z PÍSEMNICTVÍČlánek Voltaire a jeho „arganismus“Článek REFERÁTY Z PÍSEMNICTVÍČlánek Kuffnerova cena 2009Článek Čím stonali mocníČlánek Recenze knihyČlánek Recenze knihyČlánek Recenze knihyČlánek Recenze knihy
Článok vyšiel v časopiseČeská a slovenská psychiatrie
Najčítanejšie tento týždeň
2009 Číslo 2- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Hluboká stimulace globus pallidus zlepšila klinické příznaky u pacientky s refrakterním parkinsonismem a genetickou mutací
-
Všetky články tohto čísla
- Ekonomická krize a psychofarmaka
- Sledování bezpečnosti a účinnosti přípravku amisulpridu (Solian®) v podmínkách běžné klinické praxe
- Genderové rozdíly u pacientů se schizofrenií
- REFERÁTY Z PÍSEMNICTVÍ
- Psychické následky úrazů a hodnocení ztížení společenského uplatnění
- Možnosti a meze psychoterapie u bipolární poruchy
- Voltaire a jeho „arganismus“
- REFERÁTY Z PÍSEMNICTVÍ
- 47. výroční setkání ACNP (American College of Neuropsychopharmacology)
- Z jednání výboru Psychiatrické společnosti 4. března 2009
- Národní psychiatrická cena profesora Vladimíra Vondráčka
- Cena výboru Psychiatrické společnosti ČLS JEP a České psychiatrické společnosti o.s.
- Kuffnerova cena 2009
- Čím stonali mocní
- Recenze knihy
- Recenze knihy
- Recenze knihy
- Recenze knihy
- Česká a slovenská psychiatrie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Psychické následky úrazů a hodnocení ztížení společenského uplatnění
- Možnosti a meze psychoterapie u bipolární poruchy
- Sledování bezpečnosti a účinnosti přípravku amisulpridu (Solian®) v podmínkách běžné klinické praxe
- Voltaire a jeho „arganismus“
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



