-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Waldenströmova makroglobulinemie – klinické projevy a přehled léčby včera, dnes a zítra
Waldenström’s macroglobulinemia – clinical symptoms and review of therapy yesterday, today and tomorrow
Background: Waldenström macroglobulinemia (WM) is a lymphoplasmocytic lymphoma with immunoglobulin M monoclonal protein. The incidence of this disease is very low (0.4/100,000), so that this disease can be regarded as an orphan’s disease. It means that new drugs are often tested and registered for more frequent diseases. Purpose: In this review we will focus on the efficacy of the new drugs for WM. Results: The current treatment options for symptomatic WM patients include alkylating agent cyclophosphamide and anti-CD20 monoclonal antibodies. Therapy with rituximab and bendamustin resulted in longer therapeutic response then therapy with rituximab, cyclophosphamide and dexamethasone. Many drugs, used in multiple myeloma (MM), shoved promising results in WM patients. Bortezomib is effective in WM, but its neurotoxicity is higher in WM than in MM patients. Therefore, new proteasome inhibitors, carfilzomib and ixazomib, are better tolerated as documented in several studies. New types of antiCD20 antibody (obinutuzumab) can be used in patients with rituximab intolerance. in five of our patients with WM, obinutuzumab and bendamustin reached deeper responses than therapies administered in previous lines of therapy. Oral Bruton tyrosine kinase (BTK) inhibitor ibrutinib alone and in combination with rituximab have extended the treatment options for WM patients. New BTK inhibitors (e. g. acalabrutinib, zanubrutinib, and vecabrutinib) were tested and their lower toxicity (atrial fibrillation) was documented. Moreover, the BCL2 inhibitor venetoclax is newly tested. Conclusion: New antiCD20 antibody (obinutuzumab) is of advantage in patients with WM with rituximab intolerance as well as bendamustin and new proteasome inhibitors (ixazomib and carfilzomib) or new BTK inhibitors with lower cardiotoxicity. Many of the abovementioned drugs do not have official registration for WM and can be administrated with the consent of the health care provider only. Thus, this work brings evidence of their efficacy.
Keywords:
ibrutinib – obinutuzumab – Waldenström macroglobulinemia – ixazomib – bendamustin – carfilzomib
Autori: Z. Adam 1; L. Pour 1; D. Zeman 2; M. Krejčí 1; I. Boichuk 1; M. Krejčí 1; M. Štork 1; V. Sandecká 1; Z. Král 1
Pôsobisko autorov: Interní hematologická a onkologická klinika LF MU a FN Brno 1; Oddělení klinické bio chemie, Ústav laboratorní medicíny LF MU a FN Brno 2
Vyšlo v časopise: Klin Onkol 2023; 36(3): 177-191
Kategória: Přehled
doi: https://doi.org/10.48095/ccko2023177Súhrn
Východiska: Waldenströmova makroglobulinemie (WM) je lymfoplazmocytární lymfom produkující monoklonální imunoglobulin typu IgM. Incidence této nemoci je nízká (0,4/100 000), takže tuto chorobu lze považovat za tzv. nemoc-sirotka. To znamená, že nové léky jsou testovány a registrovány většinou pro častější diagnózy, než je WM. Cíl: V tomto textu shrnujeme informace o účinnosti nových léků pro WM. Výsledky: Z klasických chemoterapeutik se nyní za nejúčinnější lék v kombinaci s rituximabem považuje bendamustin, který dosahuje dlouhodobější léčebné odpovědi než cyklofosfamid s rituximabem a dexametazonem. Mnoho léků používaných pro léčbu mnohočetného myelomu (MM), má dobrou účinnost také u WM. Bortezomib je vysoce účinný, ale neurotoxicita tohoto léku u WM je vyšší než u MM. Novější léky ze skupiny inhibitorů proteazomu, ixazomib a karfilzomib, s nižší neurotoxicitou jsou lépe tolerovány u WM, jak bylo prokázáno v několika studiích. Nové typy antiCD20 monoklonálních protilátek jsou přínosem obzvláště v případech intolerance rituximabu. Pět našich pacientů netolerujících rituximab ukončilo léčbu kombinací bendamustinu a obinutuzumabu. Všichni pacienti léčení touto kombinací dosáhli hlubší léčebné odpovědi po obinutuzumabu a bendamustinu, než bylo dosaženo v přechozích léčebných liniích. Registrace prvního perorálního inhibitoru Brutonovy tyrozinkinázy (BTK) ibrutinibu pro monoterapii či kombinaci s rituximabem rozšířilo léčebné možnosti u pacientů refrakterních k iniciální léčbě. Nové léky ze skupiny inhibitorů BTK (akalabrutinib, zanubrutinib, vekabrutinib) byly již u této nemoci testovány a ukázalo se, že mají nižší toxicitu při srovnatelném léčebném účinku. Kardiální komplikace typu fibrilace síní byly méně časté. A nově je testován také BCL2 inhibitor venetoklax. Závěr: Nová antiCD20 protilátka (obinutuzumab) je přínosem pro pacienty s WM s intolerancí rituximabu stejně jako bendamustin a nové inhibitory proteazomu (ixazomib a karfilzomib) nebo nové inhibitory BTK s nižší toxicitou. Mnoho z výše zmíněných léků nemá oficiální registraci pro WM a lze je podat pouze se souhlasem plátce zdravotní péče, proto tento text přináší důkazy o jejich účinnosti.
Klíčová slova:
ibrutinib – obinutuzumab – ixazomib – Waldenströmova makrogobulinemie – bendamustin – karfilzomib
Úvod
Waldenströmova makroglobulinemie (WM) je choroba, která je řazena do skupiny nemocí s názvem monoklonální gamapatie, jejichž hlavním definujícím znakem je monoklonální imunoglobulin [1]. WM je definována morfologickou přítomností lymfoplazmocytárního lymfomu v kostní dřeni (příp. i extramedulárně) a biochemickým nálezem monoklonálního imunoglobulinu typu IgM (M-IgM). WM vzniká z monoklonální gamapatie nejistého významu (monoclonal gammapathy of undetermined signifikance – MGUS) typu IgM (MGUS-IgM) postupnou transformací, podobně jako mnohočetný myelom (MM) vzniká transformací z MGUS-IgG či MGUS-IgA nebo z MGUS lehkých řetězců [1].
U pacientů s MGUS-IgM byly prokázány dva rizikové faktory pro transformaci do WM: abnormální poměr volných lehkých řetězců (free light chain – FLC) a koncentrace M-IgM > 15 g/l. Tyto faktory byly asociovány s 55% progresí po 20 letech. V případě jednoho rizikového faktoru to bylo 41 %, zatímco u pacientů bez těchto rizikových faktorů jen 19 % [2].
Názory na počty transformací MGUS do symptomatické formy WM se liší; jedna z posledních prací uvádí, že po 10 letech bylo 38 % transformací z MGUS-IgM do symptomatické formy WM [3]. Tyto studie jsou argumentem, proč by osoby s MGUS-IgM měly být sledovány s cílem včas odhalit transformaci do symptomatické krevní nemoci vyžadující léčbu třeba i s pomocí FDG-PET/CT, jak popsali Sandecká et al. [4].
Diskriminace pacientů s WM
Dle morfologické klasifikace patří WM do skupiny chorob nazvaných „low grade“ lymfoproliferace neboli též nízce agresivní lymfoproliferace, podobně jako chronická B-lymfocytární leukemie či folikulární lymfom, ale WM je podstatně vzácnější než tyto dvě jmenované nemoci. Proto často registrační studie nových léčiv WM opomíjejí, a tak lze na WM pohlížet jako na tzv. nemoc-sirotka (orphan disease), o kterou v registračních studiích nových léků není zájem. A pacienti s WM právem mohou mít pocit, že jsou diskriminováni, když potenciálně účinné léky jsou testovány a registrovány pro pacienty s chorobami sice ze stejné skupiny, ale s vyšší incidencí. A proto přinášíme tento přehled účinnosti nových léků u pacientů s WM. Jejich úhradu lze pro léčbu pacientů s WM získat pouze se souhlasem plátce zdravotní péče, zatímco pro jiné nemoci ze skupiny lymfoproliferací jsou již Státním ústavem pro kontrolu léčiv schválené; proto jsme v tomto textu ponechali více citací dokladujících pravdivost prezentovaných faktů.
Epidemiologická data
Incidence WM byla v USA stanovena na 4,1 na 1 mil. obyvatel u bělošské populace, u Afroameričanů je méně častá – 1,8 na 1 mil. obyvatel [5]. Pokud údaje o incidenci u bělošské populace v USA přeneseme na ČR, tak by to bylo 40 nově diagnostikovaných pacientů ročně. Uvedený počet odpovídá naší zkušenosti, tj. poměr pacientů s MM k počtu pacientů s WM) je přibližně 10 : 1.
Medián přežití pacientů s WM souvisí s věkem, pacienti mladší 70 let mají medián přežití > 10 let, pacienti ve věku 70–79 let mají medián přežití kolem 7 let [6]. Tab. 1 ilustruje vliv věku, v němž byla stanovena diagnóza na prognózu, a také počet úmrtí z jiných příčin v různých věkových kategoriích. Grafické znázornění lze nalézt v citované publikaci [6].
Tab. 1. Přežití pacientů v závislosti na věku, v němž byla stanovena diagnóza a zahájena léčba [6]. ![Přežití pacientů v závislosti na věku, v němž byla stanovena diagnóza a zahájena léčba [6].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/ba9d44960066cf52972bcc59839600aa.png)
Celá analyzovaná kohorta měla medián sledování 7 let, medián celkového přežití (OS) celé kohorty byl 7 let a pětileté a desetileté přežití bylo 62 a 39 %. V podskupině s datem stanovení diagnózy v letech 1991–2000 byl medián sledování 13 let, medián OS v této podskupině byl 6 let. Pro podskupinu s datem stanovení diagnózy v letech 2001–2010 byl medián sledování 5 let a medián OS 8,2 roku. Délka života od stanovení diagnózy byla v obou podskupinách zásadně ovlivněna věkem, v němž byla stanovena diagnóza a zahájena léčba, jak ilustrují data. Tato analýza mimo jiné potvrdila prodloužení OS vlivem nových v posledních letech dostupných léků. Zásadní vliv věku stanovení diagnózy na prognózu WM zde uvádíme proto, aby mladší pacienti nebyli stresování údajem OS platným pro celou skupinu pacientů, neboť tato podskupina má podstatně příznivější prognózu.
WM – Waldenströmova makroglobulinemiePříznaky nemoci
Svou morfologickou podstatou, lymfoplazmocytárním lymfomem, patří tato nemoc do skupiny nízce agresivních CD20+ B-lymfoproliferací a sdílí s nimi i příznaky uvedené v levém sloupci tab. 2. Choroba pravidelně infiltruje kostní dřeň, ale může také postihnout uzliny, příp. způsobit hepato/splenomegalii a jen výjimečně infiltruje mozek či jiné parenchymatózní orgány [7,8]. Expanze lymfoplazmocytárního lymfomu v kostní dřeni vede k cytopenii a produkce cytokinů patologickými buňkami k B-symptomům neboli k systémové zánětlivé reakci organizmu. Takže nemoc je často diagnostikována v rámci hledání příčiny febrilií či subfebrilií nejasného původu dle publikovaných guidelines pro jejich diagnostiku.
Tab. 2. Příznaky Waldenströmovy makroglobulinemie. 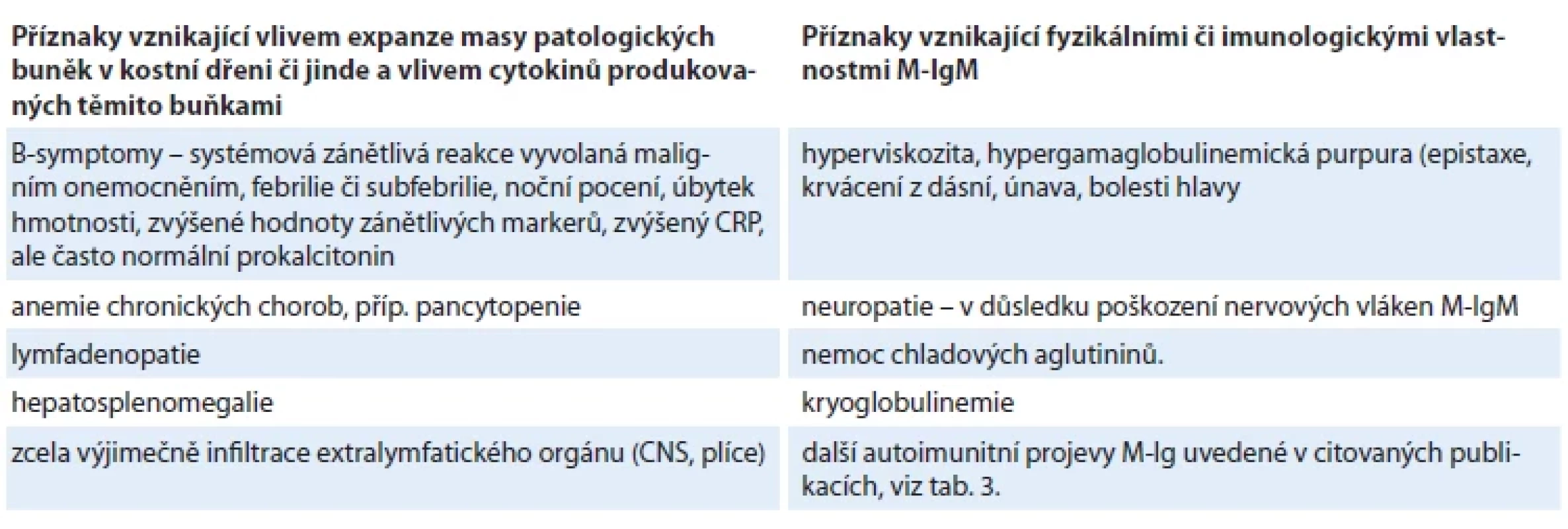
CRP – C-reaktivní protein, M-IgM – monoklonální imunoglobulin typu IgM Tvorba M-IgM však této lymfoproliferaci přidává další rozměry. Vlivem tvorby M-IgM jsou projevy této nemoc podstatně pestřejší, než je tomu u ostatních chorob ze skupiny low grade lymfomů. Některé příznaky vyvolané monoklonálním imunoglobulinem lze odvodit od jeho fyzikálních vlastností (kryoglobulinemie, hyperviskozita). V důsledku hyperviskozity dochází ke krvácení z nosu a z dásní. Retinální krvácení pak může být příčinou poruchy zraku, ale hyperviskozitou mohou být postiženy i mozkové funkce.
Další příznaky nemoci mohou být způsobeny imunologickou vazbou M-IgM na tělu vlastní antigeny. V těchto případech WM způsobuje autoimunitní poškození organizmu, jak je popsáno v české, slovenské a zahraniční literatuře [9,10]. Prací analyzujících četnost protilátkové aktivity monoklonálního imunoglobulinu je velmi málo, vybrali jsme z nich práci dánských autorů (tab. 3). M-IgM má mnohem častěji vlastnosti autoprotilátky než M-IgG nebo M-IgA.
Tab. 3. Frekvence autoimunitní poškození orgánů a tkání monoklonálním imunoglobulinem typu IgM v souboru 57 pacientů s Waldenströmovou makroglobulinemií [9]. ![Frekvence autoimunitní poškození orgánů a tkání monoklonálním imunoglobulinem typu IgM v souboru 57 pacientů
s Waldenströmovou makroglobulinemií [9].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/21157499b654d2b07ce5662056e72508.png)
MAG – myelin-asociovaný glykoprotein Pro chirurgy je důležité vědět o této nemoci, že často bývá provázena krvácivými projevy. Na jejich etiopatogenezi se podílí jak hyperviskozita, tak interakce M-IgM s trombocyty a proteiny koagulační kaskády, čímž dochází k projevům získané von Willebrandovy choroby, k trombocytopatii či k jiným poruchám hemostázy. Takže komplexní vyšetření hemostázy by mělo obsahovat u těchto pacientů i analýzu funkce trombocytů.
Koagulopatie těchto pacientů nám občas bránila provést trepanobiopsii pro riziko krvácení. Léčebná plazmaferéza s náhradou odebrané plazmy pacienta konzervami mražené plazmy a albuminu tuto koagulopatii často odstranila, a pak jsme bez problémů provedli trepanobiopsii.
Stanovení diagnózy
Mezinárodní klasifikace nemocí definuje diagnózu WM (MKN-10 kód C88.0) následovně: přítomnost M-IgM, infiltrace kostní dřeně lymfoplazmocytárním lymfomem, tj. klonálními lymfocyty, lymfoplazmocytoidními buňkami a plazmocyty. Typický imunofenotyp je CD19, CD20 a negativní CD5, CD10 a CD23. Tento typ lymfomu není tvořen jen jedním morfologickým typem buněk, proto stanovit diagnózu z aspirátu kostní dřeně se obvykle nedaří. Stanovení diagnózy lymfoplazmocytární infiltrace kostní dřeně dle Owena také neobsahuje žádné procentové kritérium patologických buněk v kostní dřeni na rozdíl od MM [11]. To zdůrazňujeme, protože v publikacích z Mayo Clinic byla a je stále používána definice vyžadující 10% podíl patologických buněk v kostní dřeni [12]. Toto procentové kritérium však nebylo skupinou zvanou International Workshop on Waldenström Macroglobulinaemia a skupinou European Myeloma Network akceptováno [13].
Definice dle Owena také neobsahuje hraniční koncentraci M-IgM na rozdíl od MM, protože koncentrace M-IgM nekoreluje s mírou infiltrace kostní dřeně. Koncentrace M-IgM mj. závisí na poměru klonálních lymfocytů, lymfoplazmocytů a plazmocytů. Pokud je více patologických plazmocytů a méně patologických lymfocytů, tvoří se více M-IgM, pokud je více patologických lymfocytů a méně patologických plazmocytů, tvoří se méně M-IgM.
A proto se setkáváme s pacienty, kteří mají masivní infiltraci kostní dřeně a jen nevelkou koncentraci M-IgM a naopak. Na rozdíl od mnohočetného MM u WM není přímá závislost koncentrace M-IgM na míře infiltrace v kostní dřeni [11]!
Uvádí se i možnost transformace MGUS-IgM do MM typu IgM, ale tyto případy jsou podstatně vzácnější a odlišit tyto dvě jednotky není zcela jednoduché, jak popisují Elba et al. [14]. Diagnózy připadající v úvahu při průkazu IgM uvádí tab. 4.
Tab. 4. Klinické jednotky spojené s monoklonálním imunoglobulinem typu IgM dle doporučení pro diagnostiku a léčbu z roku 2021 [12]. ![Klinické jednotky spojené s monoklonálním imunoglobulinem typu IgM dle doporučení pro diagnostiku a léčbu
z roku 2021 [12].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/72a5c8e880bdf4d5cea00af10aaf0a05.png)
MGUS – monoklonální gamapatie nejistého významu Termín asymptomatická (doutnající) WM se používá pro případy, kdy v kostní dřeni je jednoznačná infiltrace odpovídající lymfoplazmocytárnímu lymfomu a nejsou přítomny příznaky nemoci, které by zhoršovaly kvalitu života člověka, a není nutná léčba. Termín symptomatická WM znamená, že tato nemoc již snižuje kvalitu života člověka a je třeba ji léčit.
Jak již bylo výše uvedeno, pacienti s aktivní nemocí mají občas závažné koagulační problémy, protože M-IgM může interferovat s koagulační kaskádou, a pak je provedení trepanobiopsie spojeno s určitým rizikem. A v této situaci je přínosné flowcytometrické vyšetření kostní dřeně [15].
Se stanovením diagnózy souvisí dnes i podrobnější molekulárně biologické vyšetření, které bylo ale v časopise Klinická onkologie i v další české literatuře opakovaně podrobně diskutováno, a proto jen na tyto publikace odkazujeme [16,17].
V databázi PubMed je do roku 2022 pouze jedna práce zaměřená na analýzu zobrazení WM metodou PET/CT s využitím fludeoxyglukózu (FDG). Před zahájením léčby podstoupilo toto vyšetření celkem 35 pacientů. Kombinované PET/CT zobrazení detekovalo pozitivní nálezy u 83 % pacientů se symptomatickou chorobou, zatímco konvenční CT nacházelo patologické nálezy pouze u 20 % vyšetřených. Abnormální signál z kostní dřeně byl ale detekován jen u 43 % pacientů. Autoři této práce uzavírají, že FDG-PET/CT může pomoci upřesnit množství patologické tkáně [18]. Fakt, že jen necelá polovina pacientů měla zvýšenou akumulaci FDG v kostní dřeni, i když u nich byla histologicky prokázána její infiltrace, se vysvětluje nízkou proliferační rychlostí patologických buněk, která je spojená s nízkou FDG aviditou.
Aktivita nemocí se hodnotí dle vývoje celkového a monoklonálního imunoglobulinu. Obě metody informují o vývoji koncentrace monoklonálního imunoglobulinu, ale dle našich pozorování se progrese výrazněji odráží v dynamice zvyšování celkového IgM (stanovený nefelometrií) než v dynamice zvyšování monoklonálního IgM (stanovený elektroforézou a následnou denzitometrií). Proto u těchto pacientů sledujeme jak vývoj koncentrace monoklonálního IgM, tak i vývoj koncentrace polyklonálních imunoglobulinů IgG, IgM a IgA stanovených nefelometrií.
S progresí či ústupem nemoci souvisí také vývoj koncentrace hemoglobinu. U pacientů, u nichž byla vstupně zvýšená hodnota CRP (jako projev zánětlivé reakce vyvolané lymfoplazmocytárním lymfomem), lze i na CRP pohlížet jako na ukazatel aktivity choroby [19].
Vývoj poměru FLC je u této choroby trochu přehlížený ukazatel, ale dle citovaných publikací [20] i vlastních zkušeností taktéž odráží vývoj aktivity nemoci. Poměr FLC je obsažen i v prognostickém indexu pro transformaci MGUS-IgM do symptomatické formy WM [2].
Léčba
IgM gamapatie se pomalu kontinuálně vyvíjí z MGUS-IgM přes asymptomatickou formu do symptomatické formy WM, která již vyžaduje léčbu. A tak bylo nutno řešit otázku, kdy je optimální zahájit léčbu? Odpovědi na tuto otázku byly opakovaně publikovány [12,13,19,21]. Současná platná doporučení pro zahájení léčby jsou uvedena v tab. 5.
Tab. 5. Indikace pro zahájení léčby Waldenströmovy makroglobulinemie dle „European Myeloma Network recommendations on diagnosis and management of patients with rare plasma cell dyscrasias“ [13,21] a dle doporučení České myelomové skupiny [19]. ![Indikace pro zahájení léčby Waldenströmovy makroglobulinemie dle „European Myeloma Network recommendations
on diagnosis and management of patients with rare plasma cell dyscrasias“ [13,21] a dle doporučení České myelomové skupiny
[19].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/aba87eeddb27541882050eba73057a29.png)
Někteří pacienti s výrazně zvýšenou hodnotnou M-IgM a infiltrací kostní dřeně přesahující 30 % nemusí mít žádné symptomy a roky nevyžadují léčbu, a to i při koncentraci celkové bílkoviny kolem 100 g/l. Naopak pacienti s nízkou koncentrací monoklonálního imunoglobulinu a minimální infiltrací kostní dřeně mohou již vyžadovat léčbu, protože monoklonální imunoglobulin poškozuje tělo nemocného (neuropatie, amyloidová depozita, anemie s chladovými aglutininy, kryoglobulinemie). Symptomatická hyperviskozita je vzácná při koncentraci celkového IgM < 40 g/l, obvykle se začíná manifestovat až při koncentraci IgM > 40 g/l. Příznaky nemoci zůstávají v průběhu času stejné a jsou zachyceny již ve starších citovaných publikacích českých a slovenských autorů evidovaných v databázi medvik.cz, zatímco názory na optimální léčbu se rychle mění a cílem tohoto textu je hlavně nastavit zrcadlo vývoji názorů na léčbu z pohledu roku 2022.
Léčba v minulých letech
Prvním lékem, dnes již nepoužívaným, byl chlorambucil (Leukeran) a posléze i další alkylační cytostatika a později jejich kombinace. Na přelomu tisíciletí se krátkodobě dostaly do popředí kombinace fludarabinu s cyklofosfamidem, které nás lékaře zpočátku fascinovaly vysokým počtem léčebných odpovědí, ale po prvním nadšení začaly přicházet zprávy o vysoké frekvenci hematologických komplikací (dlouhodobý dřeňový útlum, vysoká frekvence vzniku myelodysplastického syndromu s přechodem do akutní myeloidní leukemie). Tyto pozdní hematologické komplikace vedly k opuštění kombinace fludarabinu s cyklofosfamidem, přesněji řečeno k nedoporučení používat tuto kombinaci v první nebo druhé linii léčby. Kombinace fludarabinu s cyklofosfamidem dnes může být zvažována pouze u velmi pokročilých forem nemoci, když již není v nabídce jiný lék s nižší toxicitou. Každopádně dnes nelze nabízet kombinaci fludarabinu s cyklofosfamidem pacientům v rámci první či druhé linie léčby. Intenzivní léčebné režimy používané pro léčbu agresivních lymfomů přestaly být v této indikaci také používány, protože byly zbytečně toxické [19,22,23].
Přínos antiCD20 protilátek pro léčbu WM
Z pohledu imunofenotypu patologických buněk patří lymfoplazmocytární lymfom, morfologický podklad WM, do skupiny, kterou nazýváme CD20 pozitivní lymfoproliferace. A proto je rituximab dnes již standardní součástí léčby této nemoci. Díky nepřítomnosti dlouhodobé toxicity a absenci myelosupresivního působení je součástí všech léčebných kombinací používaných pro léčbu WM.
Rituximab samotný však nedosahuje dostatečné léčebné odpovědi. Počet léčebných odpovědí (minimální odpověď (minimal response – MR) a parciální odpověď (partial response – PR)) dosahuje < 55 % a je podstatně horší, než jsou výsledky kombinovaných režimů. Autoři metaanalýzy publikovaných dat dospěli k závěru, že počet léčebných odpovědí je vyšší v dvojkombinacích než v monoterapii rituximabem (73 vs. 44 %) [24].
Rituximab má dokonce nižší počet léčebných odpovědí než alkylační cytostatika chlorambucil nebo kladribin. Proto samotný rituximab je doporučován autory z Mayo Clinic pouze pro pacienty s periferní neuropatií způsobenou monoklonálním imunoglobulinem IgM, kteří ale při komplexním vyšetření nemají symptomatickou formu WM [25].
Podání antiCD20 protilátek, jako je rituximab, je spojené s rizikem dočasného vzestupu koncentrace monoklonálního imunoglobulinu, aniž by to znamenalo progresi. Tomuto fenoménu se říká IgM-flare. Dočasný vzestup koncentrace M-IgM může zvýšit viskozitu séra. Při kombinaci rituximabu s chemoterapií je tento fenomén méně výrazný, ale také jej u našich pacientů pozorujeme [26].
Proto se někdy v případech vyšší koncentrace celkové bílkoviny a M-IgM přidávají antiCD20 monoklonální protilátky až od 2. cyklu léčby. Na zvážení je udržovací léčba rituximabem, i když ne zcela ve všech studiích byla přínosem [27].
Rituximab v kombinaci s cyklofosfamidem byl dlouho zlatým standardem, v druhém desetiletí tohoto století byl považován za optimální kombinaci dosahující maximálního efektu při minimálních nežádoucích účincích.
Rituximab a cyklofosfamid dosahují celkové četnosti odpovědí (overal response rate – ORR) 83 % při minimální toxicitě a 2leté bezpříznakové přežití (progression free survival – PFS) je 67 % a 2leté tumor specifické přežití je 90 % [28]. Recentní analýza 72 pacientů z Mayo Clinic léčených kombinací rituximab, cyklofosfamid a dexametazon popisuje ORR 83 %, medián PFS byl 35 měsíců a medián celkového přežití (overal survival – OS) byl 95 měsíců [29].
Rituximab je používán již více než 20 let. Byl schválen pro klinickou praxi úřadem Food and Drug Administration (FDA) v listopadu roku 1997 a úřadem European Agency for the Evaluation of Medicinal Products (EMA) v červnu roku 1998.
Pro pacienty s WM je rituximab standardně používán s cyklofosfamidem, nyní již bez nutnosti schvalování revizními lékaři [28,29].
V dalších letech byly testovány protilátky s jiným cílem, s navázaným toxinem nebo bez něj, a probíhaly snahy o optimalizaci antiCD20 monoklonální protilátky s cílem zvýšit její vazebnou kapacitu na CD20 antigen nebo zvýšit aktivitu této protilátky.
Ofatumumab byl syntetizován tak, aby se vázal na nový membránový epitop a aby ve srovnání s rituximabem vedl k výraznější, na komplementu závislé cytotoxicitě [30]. Ale i přes vyšší vazebnou kapacitu nebyla v rámci srovnávací studie u pacientů s folikulárním lymfomem prokázána superiorita ofatumumabu nad rituximabem.
Nicméně podání ofatumumabu se objevilo v doporučení pro léčbu WM z roku 2016 [31] a v odborné literatuře je několik publikací, které pozitivně hodnotí použití této látky u pacientů s WM a pro léčbu pacientů s touto nemocí ji doporučují [32,33].
Další testovanou látkou byl obinutuzumab. Obinutuzumab byl schválen úřadem FDA v listopadu 2013 a evropským úřadem EMA v květnu 2014 v kombinaci s chlorambucilem pro léčbu dříve neléčených pacientů s chronickou B-lymfocytární leukemií. V únoru roku 2016 byl na základě studie GADOLIN úřadem FDA schválen také obinutuzumab v kombinaci s bendamustinem, a to pro léčbu refrakterních folikulárních lymfomů [34]. Opět byl tedy schválen lék pro dvě relativně časté nemoci ze skupiny tzv. low grade lymfoproliferací, zatímco WM zase zůstala stranou zájmu těchto studií jako nemoc-sirotek, i když se předpokládá efekt pro celou skupinu těchto low grade lymfoproliferací.
Obinutuzumab je typ II anti-CD20 protilátky s nižší cytotoxicitou závislou na komplementu, ale s větší intenzitou buněčné cytotoxicity závislé na protilátce. In vitro je obinutuzumab účinnější než rituximab [35]. Srovnávací studie rituximabu, ofatumumabu a obinutuzumabu provedené in vitro a na xenograftovém modelu uvádějí, že z těchto tří antiCD20 monoklonálních protilátek je nejúčinnější právě obinutuzumab [36].
V případě chronické lymocytární leukemie (CLL) a folikulárního lymfomu je na rozdíl od WM již hodně klinických studií publikovaných in extenso, které popisují úspěšné použití obinutuzumabu. Pro rozhodování o léčbě jsou vždy nejdůležitější velké srovnávací studie, a proto stručně uvedeme jejich výsledky.
V rámci randomizované studie fáze II GAUSS byla srovnána monoterapie obinutuzumabem a rituximabem. V tomto prvním randomizovaném srovnání byla testována monoterapie obinutuzumabem anebo rituximabem u 175 nemocných s relabujícími indolentními lymfomy po předchozí léčbě kombinovanými režimy s rituximabem. Pacienti dostali v týdenních intervalech čtyři infuze buď rituximabu v dávce 375 mg/m2, nebo obinutuzumabu (celková dávka 1 000 mg). Po ukončení těchto čtyř aplikací dostávali pacienti s léčebnou odpovědí stejnou účinnou látku v rámci udržovací léčby ve 2měsíčních intervalech po dobu 2 let. V podskupině pacientů s folikulárním lymfomem (n = 149) byla ORR o 11 % vyšší po obinutuzumabu než po rituximabu (44,6 vs. 33,3 %; p = 0,08). Tento výsledek byl zřetelný v celé skupině pacientů, v níž nezávislý panel hodnotitelů prokázal vyšší ORR po obinutuzumabu (44,6 %) než po rituximabu (26,7 %) (p = 0,01). Vyšší ORR se však nepromítla do prodloužení PFS [37].
V klinické studii GALLIUM bylo randomizováno 1 202 pacientů s folikulárními lymfomy do skupiny léčené standardní chemoterapií buď s klasickou dávkou rituximabu, nebo s klasickou dávkou obinutuzumabu. Obinutuzumab byl v této studii podáván v 1. cyklu 1., 8. a 15. den v dávce 1 000 mg a pak vždy 1. den dalšího cyklu. Rituximab byl podáván v standardní dávce 375 mg/m2 1. den každého cyklu. První hodnocení, které bylo provedeno při mediánu sledování 34,5 měsíce, prokázalo, že chemoterapie v kombinaci s obinutuzumabem měla lepší výsledky, nižší riziko progrese a nižší riziko úmrtí než chemoterapie v kombinaci s rituximabem. Tříleté PFS při použití obinutuzumabu a rituximabu bylo 80,0 vs. 73,3 % [38].
Stejně tak další analýza stejné studie publikovaná s mediánem sledování 41,1 měsíce prokázala, že PFS bylo delší ve skupině s obinutuzumabem a chemoterapií ve srovnání se skupinou léčenou rituximabem a chemoterapií. Studie GALLIUM tedy již prokázala signifikantní prodloužení PFS při podání obinutuzumabu, ale prodloužení PFS se v této studii nepromítlo do signifikantních rozdílů v OS [39,40].
Další publikace pozitivní hodnocení obinutuzumabu u low grade lymfomů (folikulární lymfom) jen potvrdily [41–44].
Do skupiny low grade lymfomů patří také CLL, u ní byl také srovnáván obinutuzumab s rituximabem v rámci německé studie CLL-11. V této studii byla použita pro pacienty s CLL vyšší dávka rituximabu 500 mg/m2, nikoliv standardní dávka 375 mg/m2. Obinutuzumab byl použit v klasické dávce 1 000 mg pro jedno podání. Lepší výsledky měla skupina léčená obinutuzumabem a chlorambucilem ve srovnání se skupinou léčenou rituximabem a chlorambucilem [45].
Obinutuzumab byl pochopitelně také testován u difuzního velkobuněčného lymfomu (diffuse large B-cell lymphoma – DLBCL) v rámci studie GOYA. Ve skupinách léčených obinutuzumabem + chemoterapií anebo rituximabem + chemoterapií nebyly u pacientů s DLBCL zaznamenány signifikantní rozdíly [46, 47]. Ke stejným závěrům dospěly studie publikované zatím jen ve formě abstraktů [48].
Z výše uvedených výsledků klinických studií vyplývá, že obinutuzumab je účinnější než rituximab ve skupině low grade lymfomů, ale tato přednost, zřetelná velmi dobře u folikulárního lymfomu a CLL, se nepotvrdila ani ve skupině pacientů s DLBCL, ani ve skupině pacientů s lymfomem marginální zóny [49]. Výsledky uvedených srovnávacích studií uvádí tab. 6.
Tab. 6. Klinické studie, které měly za cíl srovnat účinnost obinutuzumabu a rituximabu v monoterapii nebo v kombinaci s chemoterapií. 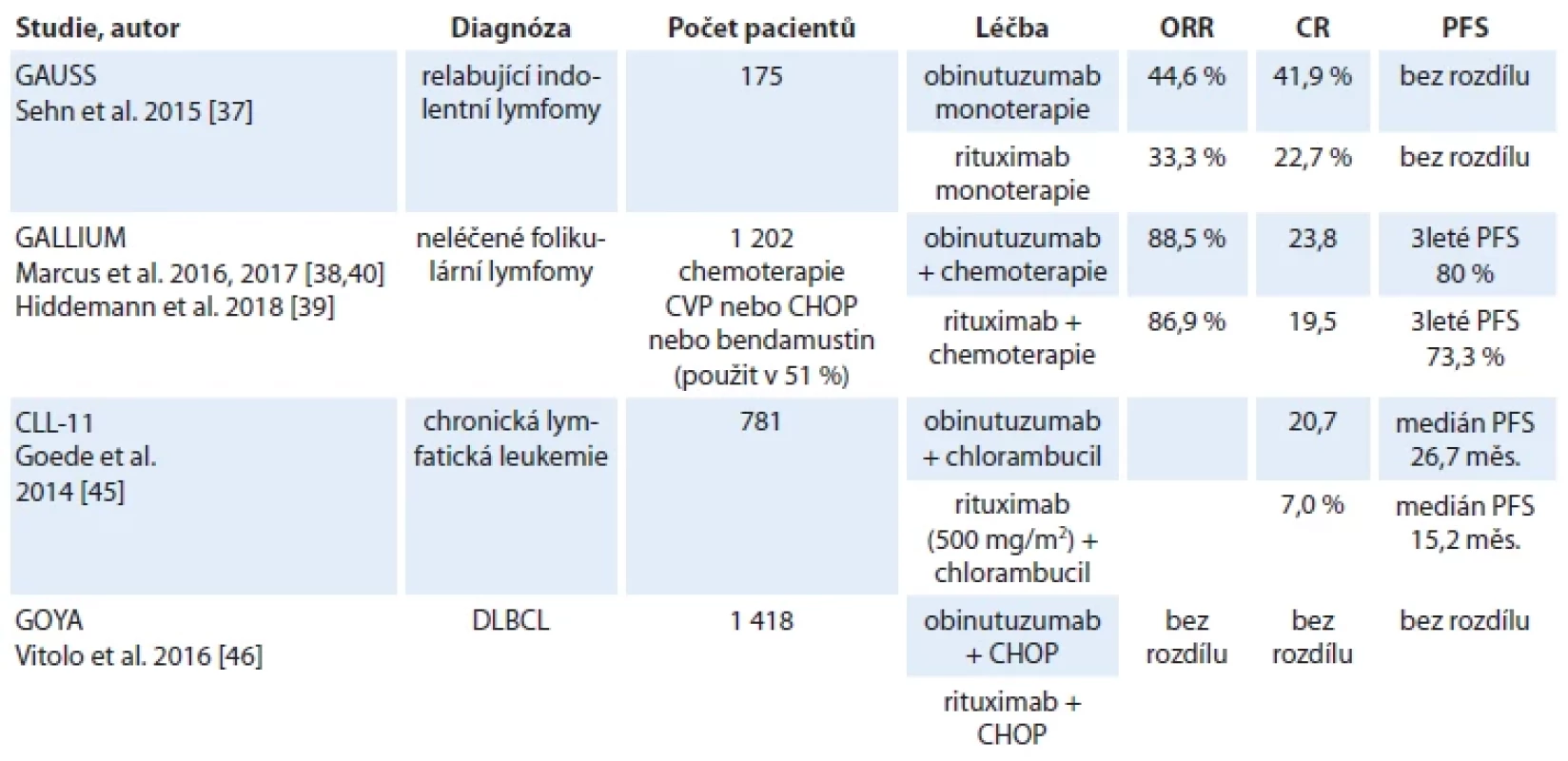
CR – kompletní odpověď, CVP – cyklofosfamid, vinkristin, prednison, CHOP – cyklofosfamid, adriamycin, vinkristin, prednison, DLBCL – difuzní velkobuněčný lymfom, ORR – celkový počet léčebných odpovědí, PFS – přežití bez progrese K dubnu 2022 byla zveřejněna pouze jedna metaanalýza vyhodnocující role antiCD20 protilátek u pacientů s nehodgkinskými lymfomy s následujícími závěry:
kombinace obinutuzumab + chemoterapie signifikantně zlepšuje PFS ve srovnání s kombinací rituximab + + chemoterapie;
kombinace ofatumumabu a chemoterapie dosahuje nižší ORR než rituximab a chemoterapie;
90Y-ibritumomab tiuxetan ve srovnání s rituximabem + chemoterapií zvyšuje ORR [50].
V roce 2019 byla zveřejněna i ekonomická analýza použití obinutuzumabu u pacientů s folikulárním lymfomem v USA. Autoři této analýzy dospěli k závěru, že použití obinutuzumabu s chemoterapií je efektní i z pohledu vynaložených nákladů a dosažených výsledků [51]. Tato analýza má však platnost pouze pro zemi, v níž byla provedena.
Protože WM se svým biologickým chováním patří do stejné kategorie CD20 pozitivních low grade lymfoproliferací jako folikulárním lymfom či CLL, je velmi pravděpodobné, že kombinace s obinutuzumabem budou dosahovat vyššího počtu léčebných odpovědí s delším trváním, jak to prokázaly klinické studie v případě CLL anebo folikulárního lymfomu (tab. 3). Naše první zkušenost [52] by tomu nasvědčovala. V březnu 2022 ukončilo tuto léčbu již pět našich pacientů s WM, kteří netolerovali rituximab. Konstatovali jsme, že ve všech případech bylo dosaženo hlubší léčebné odpovědi než v předchozích liniích léčby, a doufáme, že se to projeví i delším intervalem PFS. To činí kombinaci obinutuzumab + bendamustin velmi atraktivní pro pacienty s WM, kteří netolerují rituximab. Výsledky první klinické studie, v níž byl použit pro léčbu WM obinutuzumab v kombinaci s dalším lékem, byly publikovány až v roce 2021 [53].
Monoklonální protilátka rituximab přispěla ke zlepšení léčby WM. Novější alternativa obinutuzumab dosáhla v případech folikulárního lymfomu a CLL větší počet odpovědí i delšího PFS. Spekuluje se, že určitý vliv na to bude mít vyšší kumulativní dávka obinutuzumabu ve srovnání s kumulativní dávkou rituximabu. Klasické schéma léčby obinutuzumabu má v prvním cyklu tři aplikace po 1 000 mg v týdenních intervalech a teprve v dalších cyklech následuje jedna aplikace obinutuzumabu na cyklus. Rituximab se podává 1× za cyklus ve standardní dávce 375 mg/m2, vyjma studie CLL-11, kdy byla použita dávka 500 mg/m2 [54].
Každopádně v uvedeném dávkování je obinutuzumab velmi účinným lékem pro low grade CD20 pozitivní lymfoproliferace.
Na našem pracovišti jsme použili obinutuzumab se souhlasem plátce zdravotní péče u pěti pacientů s WM, kteří netolerovali rituximab. Pozitivním překvapením bylo, že u všech pěti pacientů bylo dosaženo hlubší léčebné odpovědi než v předchozích liniích léčby. Předchozí léčebné linie, jejich efekt a efekt léčby obinutuzumabem a bendamustinem ilustruje tab. 7 a sledované laboratorní výsledky pak tab. 8.
Tab. 7. Pacienti, kteří netolerovali rituximab a byla pro ně použita kombinace obinutuzumab + bendamustin. 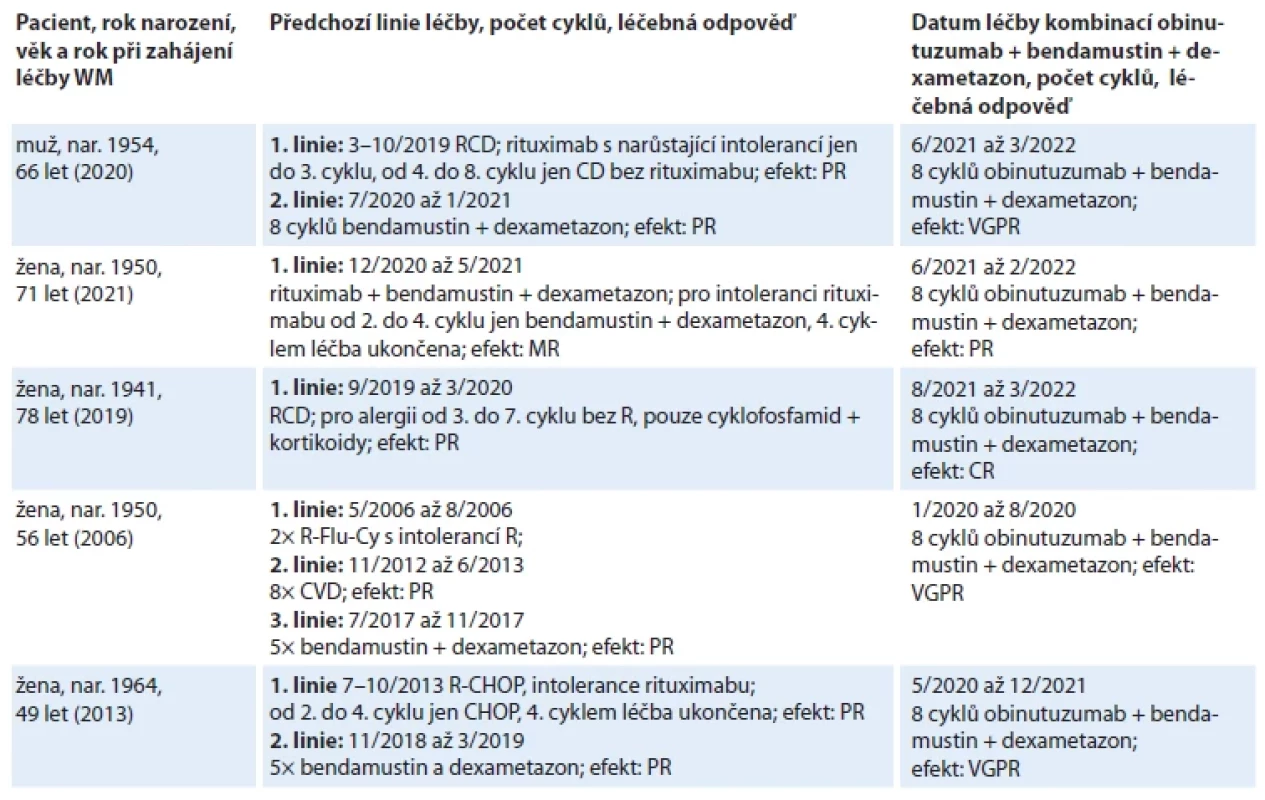
CR – kompletní remise, MR – minimální odpověď, PR – parciální remise, RCD – rituximab, cyklofosfamid, dexametazon, R-CHOP – rituximab, cyklofosfamid, adriamycin, vinkristin, prednison, R-Flu-Cy – rituximab, fl udarabin, cyklofosfamid, VGPR – velmi dobrá parciální remise, WM – Waldenströmova makroglobulinemie Tab. 8. Vývoj laboratorních parametrů při léčbě kombinací obinutuzumab + bendamustin + dexametazon. Uvedené laboratorní hodnoty byly změřeny před zahájením této léčby a po jejím ukončení. 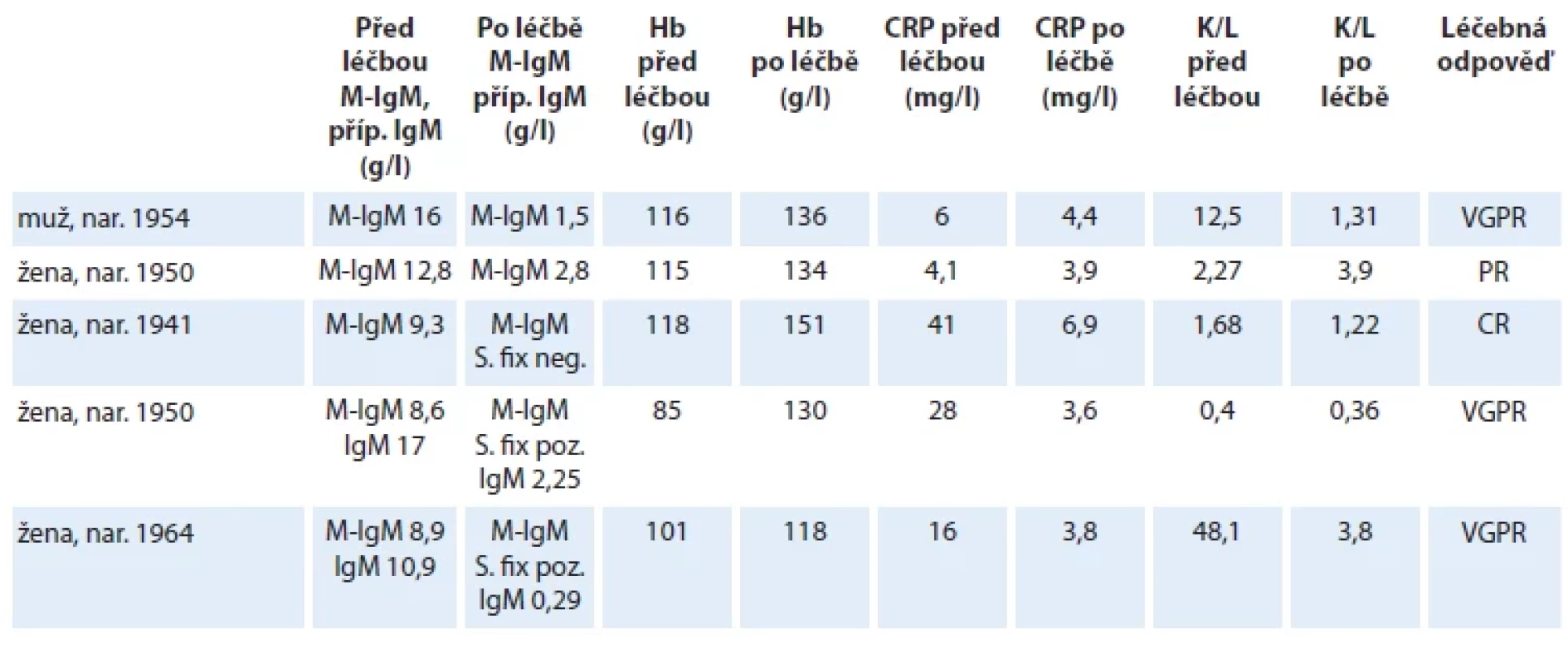
CR – kompletní remise, CRP – C-reaktivní protein, Hb – hemoglobin, IgM –celková koncentrace všech imunoglobulinů IgM (monoklonálního i nemonoklonálního) stanovená metodou nefelometrie, K/L – poměr koncentrace volnych lehkych řetězců kappa/lambda v seru, M-IgM – monoklonální imunoglobulin typu IgM stanovený elektroforézou a denzitometrií, neg. – negativní, poz. – pozitivní, PR – parciální remise, S. fi x – imunofi xační elektroforéza v séru, VGPR –velmi dobrá parciální remise Obinutuzumab tedy představuje užitečnou alternativu rituximabu v případě intolerance rituximabu nebo je alternativou při časné progresi po režimu obsahujícím rituximab.
Bendamustin
Zlatým standardem je trojkombinace antiCD20 protilátka (rituximab) + alkylační cytostatikum + dexametazon. Výsledky klinických studií z posledních let prokázaly, že použití bendamustinu místo klasického alkylačního cytostatika cyklofosfamidu u pacientů s WM prodlouží PFS, a tím i OS.
Tento fakt chceme doložit výčtem klinických studií, které k tomuto závěru vedly, protože bendamustin je možné podat pacientům s WM jen se schválením revizního lékaře.
Bendamustin u dříve léčených pacientů
První zkušenosti s léčbou WM bendamustinem byly publikovány již v roce 2011. Šlo o 24 pacientů s relapsem WM či onemocněním refrakterním na iniciální léčbu. Všichni tito již dříve léčení pacienti dostávali 2 dny po sobě bendamustin (90 mg/m2) a rituximab podávaný ve 4týdenních intervalech. Medián podaných cyklů byl 5. Celková ORR u této předléčené populace byla 83 % (20/24). Medián PFS byl 13,2 měsíce. Prolongovaná myelosuprese byla častější u těch pacientů, kteří byli v rámci předchozí léčby vystaveni fludarabinu nebo kladribinu. Treon et al. prokázali, že bendamustinem v kombinaci s rituximabem lze získat vysoký počet léčebných odpovědí i u předléčených nemocných [55].
K podobným závěrům o vysokém počtu odpovědí u předléčených nemocných dospěla italská studie z roku 2015. Zahrnula 71 pacientů s mediánem věku 72 let, s relabovaným či refrakterním WM (medián dvě linie předchozí léčby). Kombinace rituximab + bendamustin dosáhla PR u 74,6 % pacientů a podíl pacientů s PR + MR byl 80,2 %. Roční a 3leté PFS bylo 80 % a 60 %. Autoři této studie prokázali, že bendamustin je vhodným lékem i pro starší pacienty [56].
Bendamustin u dříve neléčených pacientů
U nově diagnostikovaných pacientů se začal bendamustin testovat v rámci klinických studií o něco později. Závěry francouzské studie byly zveřejněny v roce 2019. Celkem 69 dříve neléčených pacientů s WM bylo léčeno kombinací bendamustin + rituximab. ORR po 18 měsících od léčby byla 97 % a 2leté PFS dosáhlo 87 %. Jak mutace MYD 88, tak CXCR4 neměly vliv na počet léčebných odpovědí [57].
Ve stejném roce 2019 potvrdila vysoký počet léčebných odpovědí také skupina East German Lymphoma Study Group. Šlo velkou studii, do níž bylo zařazeno 293 pacientů s WM léčených rituximabem a bendamustinem. ORR byla 91,4 % a 5leté přežití 78 %. Medián PFS byl 65,3 měsíce [58].
Srovnávací studie kombinace rituximab + bendamustin s jinými režimy
Základem pro rozhodování o léčbě jsou srovnávací studie. První zprávy o excelentním výsledku kombinace rituximab + bendamustin vyplynuly v roce 2013 (tedy před 9 lety) z německé studie. V prospektivní randomizované studii byla léčba bendamustinem a rituximabem srovnávána s režimem rituximab + cyklofosfamid, doxorubicin, vinkristin a prednison (R-CHOP) ve skupině pacientů s low grade lymfomy. Jednu podskupinu tvořilo 41 pacientů s WM, z nichž 22 dostalo bendamustin a 19 pacientů dostalo R-CHOP. V obou podskupinách počet léčebných odpovědí dosáhl 95 %, ale medián PFS byl signifikantně delší ve skupině léčené bendamustinem. Medián PFS ve skupině léčené R-CHOP byl 36 měsíců, zatímco ve skupině léčené bendamustinem nebyl v době hodnocení dosažen (p < 0,001). V době analýzy byly prokázány jen čtyři (18 %) relapsy ve skupině léčené rituximabem + bendamustinem, zatímco ve skupině léčené R-CHOP bylo v té době již prokázáno 11 relapsů (58 %). To jsou výsledky jen pro jednu podskupinu WM, ale lepší výsledky měli všichni pacienti této studie léčení rituximabem s bendamustinem. Pacienti léčení bendamustinem měli nejen lepší léčebnou odpověď a menší počet relapsů, ale i tolerance léčby byla v této skupině podstatně lepší. Po bendamustinu není alopecie, byla menší hematologická toxicita a méně infekcí, ale i menší počet neuropatií [59]. Tato práce iniciovala další ověřování.
O pár let později, v roce 2017, bylo z Dana-Farber Cancer institutu v USA zveřejněno závěrečné hodnocení studie, která u pacientů s WM srovnávala tři režimy – rituximab s bendamustinem vs. rituximab, cyklofosfamid a dexametazon, příp. rituximab, bortezomib a dexametazon. Všechny režimy měly vysoký počet léčebných odpovědí, ale riziko progrese po léčbě bylo menší u pacientů léčených kombinací bendamustin + rituximab nebo bortezomib + dexametazon + rituximab ve srovnání s léčbou rituximabem a cyklofosfamidem neboli v režimu bendamustin s rituximabem bylo dosaženo delší léčebné odpovědi než při léčbě rituximabem s cyklofosfamidem a dexametazonem [60].
Největší srovnávací analýza je z Mayo Clinic, její výsledky shrnuje tab. 9.
Tab. 9. Srovnávací studie kombinace rituximab + cyklofosfamid + dexametazon vs. rituximab + bendamustin. Léčené výsledky jsou lepší jak u dříve neléčených pacientů, tak u pacientů s relapsem nemoci. Celkem bylo léčeno 60 pacientů bendamustinem a rituximabem a 100 pacientů kombinací cyklofosfamid + rituximab + bendamustin [61]. ![Srovnávací studie kombinace rituximab + cyklofosfamid + dexametazon
vs. rituximab + bendamustin. Léčené výsledky jsou lepší jak u dříve neléčených
pacientů, tak u pacientů s relapsem nemoci. Celkem bylo léčeno 60 pacientů bendamustinem
a rituximabem a 100 pacientů kombinací cyklofosfamid + rituximab
+ bendamustin [61].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/a46cdbceab85da3b6e1539faf32d0603.png)
BR – bendamustin + rituximab, PFS – přežití bez progrese, RCD – rituximab + cyklofosfamid + dexametazon Do této studie bylo zařazeno 160 pacientů, z nichž 60 bylo léčeno kombinací rituximab + bendamustin, z toho 43 pacientů mělo relabující nemoc a jen 17 mělo rituximab s bendamustinem jako iniciální léčbu. Celkem 100 pacientů bylo léčeno kombinací rituximab + cyklofosfamid + dexametazon, 50 z nich v rámci iniciální léčby a 50 v rámci léčby relabující nemoci.
U pacientů dříve neléčených dosáhla léčba kombinací rituximab + bendamustin ORR 93 %, zatímco léčba kombinací rituximab + cyklofosfamid + dexametazon dosáhla ORR 96 %. Dvouletého PFS dosáhlo z dříve neléčené skupiny pacientů 88 % po kombinaci s bendamustinem vs. 61 % po kombinaci s cyklofosfamidem (p = 0,07).
U podskupin již dříve léčebných pacientů byla ORR 95 % po bendamustinu s rituximabem vs. 87 % po kombinaci rituximabu s cyklofosfamidem a dexametazonem (p = 0,45). Medián PFS ve skupině s bendamustinem byl 58 měsíců, zatímco ve skupině s cyklofosfamidem jen 32 měsíců. Dvouleté PFS bylo 66 % po bendamustinu vs. 53 % po režimu s cyklofosfamidem (p = 0,08). Tyto výsledky byly nezávislé na statusu MYD88 [61]. A tato fakta doplnila metaanalýza používaných režimů z roku 2016 [62]. Proto byl v letech 2021 a 2022 pro pacienty s WM preferován režim bendamustin + rituximab.
Pouze v případě infiltrace centrálního nervového systému a výskytu Bing Neel syndromu je preferována léčba pronikající přes hematocefalickou bariéru [19]. Dle prvních zpráv překonává hematocefalickou bariéru ibrutinib. Při léčbě ibrutinibem byl při zobrazovacích vyšetřeních prokázán rychlý ústup symptomů a infiltrace nervového systému [63].
Účinek kombinace bendamustin + rituximab lze zvýšit ještě přidáním bortezomibu, ale zvýší se tak i toxicita léčby [64,65].
Použití léků u WM, které se standardně používají pro léčbu MM
Thalidomid a lenalidomid
Nové léky, které v klinických studiích prokázaly přínos pro pacienty s MM, jsou také účinné u WM. Při léčbě kombinací rituximab + thalidomid byla ORR 72 %, ale závažnou komplikací této léčby byla neuropatie [66], a proto další studie testovaly lenalidomid.
Ve studii prováděné v USA s kombinací rituximab + lenalidomid byla ORR 50 %, ale PR byla dosažena jen u 25 % [67]. Ve studii z Francie dosáhl lenalidomid v monoterapii ORR pouze 29 % a taktéž k nežádoucím účinkům patřila anemie [68].
Imidy thalidomid a lenalidomid mají potenciál u části pacientů přinést v kombinaci s rituximabem léčebnou odpověď. Mají však potenciál zhoršit subklinickou neuropatii, která nebývá u pacientů s WM zřídkavá, a prohlubují anemii. Imidy určitý efekt u WM mají, ale jiné léky jsou účinnější.
Bortezomib
Bortezomib má potenciál dosáhnout léčebné odpovědi nejen u MM, ale také u WM. Téměř před 12 lety na to poukázali Dimopouloset et al. [69,70]. Klinické studie, které s tímto lékem proběhly, prokázaly ORR v rozmezí 81–96 %. Bortezomib byl použit jak ve schématu s aplikací 2× týdně první 2 týdny ve 3týdenním intervalu, tak i s aplikací 1× týdně [71–73]. Při léčbě bortezomibem mutace CXCR4 nesnižuje počet léčebných odpovědí [74].
Kombinace rituximab + bortezomib podávaná 1× týdně u dříve neléčených nemocných vedla k parciální remisi u 23 z 26 pacientů a roční PFS bylo 79 % [75]. Skupina The European Myeloma Network použila podobný protokol (kombinace bortezomib + rituximab + dexametazon) taktéž u dříve neléčených nemocných. První cyklus proběhl bez rituximabu s cílem snížit riziko IgM-flare. ORR byla 85 %, medián PFS byl 42 měsíců a 3leté OS bylo 81 % [76].
Periferní neuropatie byla v průběhu léčby diagnostikována u 46 %. Kombinace bortezomib + rituximab + dexametazon je tedy také alternativou pro léčbu relapsu, ale je třeba pečlivého sledování a vyhodnocování míry neuropatie, která po zahájení léčby nastupuje docela časně [76].
Kombinace s bortezomibem byla taktéž testována u pacientů s nemocí chladových aglutininů, počet léčebných odpovědí zde však byl jen 32 % [77], a to je podstatně slabší výsledek než při léčbě nemoci chladových aglutininů kombinací rituximab + bendamustin s ORR 78 %, PR 53 % a dobou trvání léčebné odpovědi > 88 měsíců [78]. Bortezomibový režim se ale osvědčil u pacientů se získaným von Willebrandovým syndromem [79,80].
Bortezomib je tedy účinný, ale u pacientů s WM je provázen nepřehlédnutelnou neuropatií. Jeho účinnost byla potvrzena již ve velkém počtu publikací (z důvodu místa je nelze všechny citovat). Spolu s okolností, že generické preparáty zlevnily léčbu, tyto kombinace představují reálnou možnost i pro naše pacienty.
Karfilzomib
Dalším z této skupiny je karfilzomib. Na rozdíl od bortezomibu nepatří do spektra jeho nežádoucích účinků neuropatie, a přitom má u WM docela vysokou účinnost. Při léčbě kombinací karfilzomib + dexametazon + rituximab bylo u dříve neléčených pacientů dosaženo ORR 87 %, PR 10 % a velmi dobré parciální remise (very good partial remission – VGPR) 10 %. Po 2 letech 65 % léčených zůstávalo bez progrese nemoci. Periferní neuropatie nebo kardiomyopatie při léčbě postihly jen 3 % léčených [81].
V další retrospektivní analýze profitovalo z karfilzomibu šest ze šesti pacientů s WM [82]. Karfilzomib v kombinaci s antiCD20 monoklonální protilátkou je tedy také účinný režim pro pacienty s WM [83], ale pro naše pacienty je hůře dostupný než bortezomib.
Ixazomib
Nejmladší zástupce této skupiny léků si ponechává stejnou výhodu jako karfilzomib (absence neurotoxicity), navíc k jeho přednostem patří perorální podávání. A tak není divu, že v souvislosti s WM je mu věnováno hodně pozornosti. Perorální inhibitor proteazomu ixazomib při kombinaci s dexametazonem a rituximabem v souboru 26 pacientů dosáhl ORR 96 %, PR 77 % a VGPR 19 %. Medián PFS byl 40 měsíců. Medián intervalu k dosažení léčebné odpovědi byl jenom 8 týdnů. Tato studie ukazuje, že u WM by ixazomib v budoucnu mohl být často používaným lékem [84].
V roce 2022 byly zveřejněny první výsledky evropské studie s ixazomibem a rituximabem, tentokrát u relabujících pacientů. Pacienti dostali osm cyklů kombinace rituximab + ixazomib. ORR dosáhla 71 %, což je u předléčených pacientů dobrý výsledek, a ve 14 % případů se jednalo o VGPR. Medián trvání léčebné odpovědi byl 36 měsíců [85] a u pacienta s nemožností dojíždět na infuzní léčbu byl účinný i ixazomib v monoterapii. Citované publikace naznačují, že pro pacienty s WM může být ixazomib optimálním inhibitorem proteazomu s dobrou účinností, ale i tolerancí a že bychom jej měli zvažovat i u našich pacientů [86].
Ibrutinib
Dalším lékem, který přinesl pokrok pro léčbu MR, je ibrutinib. Farmakodynamiku a farmakokinetiku velmi podrobně popsali Mihályová a Ďuraš [87]. Pro naše pacienty s WM sice nepředstavuje lék první volby, ale při recidivě nemoci může být účinnou zbraní. Uvedeme několik dat o jeho účinnosti.
V rámci klinické studie dostávalo ibrutinib 63 relabujících či refrakterních pacientů. U této skupiny pacientů bylo dosaženo PR 73 % a ORR činila 90,5 %. Dvouleté PFS a OS bylo 69,1 a 95,2 %. Medián do dosažení léčebné odpovědi byl jen 4 týdny [88]. Nejčastější nehematologické toxicity byly průjem, krvácení a fibrilace síní (10,7 %) [89]. Ibrutinib je však třeba podávat dlouhodobě, protože po jeho přerušení dochází k rychlému vzestupu M-IgM [90]. Pacienti s nemutovaným genem MYXD mají nižší počet ORR [91].
V multicentrické studii, která zahrnovala 31 pacientů refrakterních na režim s rituximabem, byla v rámci druhé linie použita léčba ibrutinibem. ORR byla 90 % a parciální remise dosáhlo 71 %. Osmnáctiměsíční PFS dosáhlo 86 % a po 18 měsících od zahájení léčby žilo 97 % léčených [92]. Z této studie vyplývá, že právě pacienti refrakterní na iniciální léčbu či s relapsem v krátkém intervalu od ukončení léčby první linie jsou vhodnými kandidáty této léčby.
U dříve neléčených 30 nemocných dosáhl ibrutinib v monoterapii PR 80 % a přitom nebyl zjištěn rozdíl mezi pacienty s „wild-type“ nebo mutovaným MYD 88. Fibrilace síní byla popsána u 10 % léčených [93].
U dříve neléčených nemocných jiní autoři popsali ORR 100 % a PR 83 % [94].
Další informace o účinnosti ibrutinibu jsou z registrů, tedy informací přicházejících ne z klinických studií, ale z reálného života. Při hodnocení 80 pacientů léčených ibrutinibem bylo dosaženo ORR 91 % a 18měsíčního PFS u 82 % léčených. Ovšem 21 pacientů přerušilo léčbu pro její toxicitu, opět dominovala fibrilace síní (11 % léčených). Vzestup M-IgM po ukončení léčby byl pozorován u 36 pacientů [95].
Zatím jsou zveřejněny výsledky první studie, do níž byli pozváni dříve neléčení pacienti, kteří byli randomizováni mezi skupinami léčenými kombinací rituximab + ibrutinib nebo rituximab + placebo.
Při hodnocení po 30 měsících léčby bylo PFS ve skupině rituximab + ibrutinib 82 % a ve skupině rituximab + placebo jen 28 % (p < 0,001). Benefit kombinace ibrutinib + rituximab oproti kombinaci rituximab + placebo byl nezávislý na genotypu MYD88 nebo CXCR4. Pacienti s kombinací rituximab + ibrutinib měli oproti druhé skupině signifikantní vzestup hemoglobinu (73 vs. 41 %; p < 0,001) [96].
Pochopitelně toxicita byla vyšší ve skupině na ibrutinibu s rituximabem než ve skupině léčené kombinací placebo + rituximabem a opět zahrnovala fibrilaci síní (12 vs. 1 %) a hypertenzi (13 vs. 4 %).
Účinnost ibrutinibu souvisí s dávkou – pacienti s dávkou < 97 % plánované dávky měli kratší PFS [97]. Přerušení léčby ibrutinibem na > 1 týden je spojeno se čtyřnásobným rizikem progrese. Pokud již jednou léčba ibrutinibem začne, je třeba ji podávat dlouhodobě a předpokladem léčebného úspěchu je compliance. Přerušení podávání ibrutinibu je spojeno i s dalšími nežádoucími reakcemi – horečka, noční poty, bolesti kloubů a bolesti hlavy. A proto i když je při malé efektivitě ibrutinibu plánována jiná léčba, tak by podávání ibrutinibu mělo pokračovat do zahájení další linie léčby, aby nedošlo k „rebound“ fenoménu [98]. Léčba ibrutinibem v monoterapii nebo v kombinaci s rituximabem byla prověřena i dalšími velkými studiemi a byla shledána účinnou.
Lékaři, kteří jej indikují, si ale musí být vědomi jeho nežádoucích účinků. Ibrutinib může způsobovat krvácivé komplikace, a tak je nutno pečlivě zvažovat, zda může současně probíhat antiagregační či antikoagulační léčba. Antitrombotickou léčbu je možné ponechat, ale za přísného sledování tolerance. V případě, že by pacienti brali warfarin, doporučuje se přechod na nízkomolekulární heparin nebo přímá antikoagulancia.
Dále je nutno respektovat interakce mezi ibrutinibem a dalšími léky (digoxin, dabigatran, verapamil a amiodaron). Interakce byly popsány taktéž s některými antibiotiky (makrolidy, rifampicin) a antiepileptiky. Tyto interakce mohou zvýšit toxicitu či snížit účinnost. V případě operace má být ibrutinib vysazen 3–7 dní před výkonem a zásadně nemá být podáván pacientům vyžadujícím duální či intenzivnější antikoagulační a antitrombotickou léčbu [99].
Další inhibitory Brutonovy kinázy
Ibrutinib je prvním, ale ne posledním lékem této řady. Podobně jako u jiných lékových skupin, i zde se objevují další a další generace inhibitorů Brutonovy kinázy. První z nich je akalabrutinib (ACP-196). Tento lék byl ověřen v klinických studiích u vybraných lymfoproliferací, zatím však není pro naše pacienty dostupný, i když má již schválení pro chronickou lymfatickou leukemii a „mantle cell“ lymfom. Ve studii bylo zaznamenáno 1 % fibrilace síní, závažné krvácivé komplikace měla 3 % pacientů. Jeden pacient zemřel na intrakraniální hematom. Zda bude fibrilace síní opravdu méně častá, prokáží až další studie [100,101].
Zanubrutinib je další z inhibitorů Brutonovy kinázy druhé generace. V randomizované studii ve srovnání s ibrutinibem neprokázal vyšší účinnost, pouze tendence k lepšímu účinku a k nižší toxicitě, hlavně kardiovaskulární [102,103]. Z uvedených publikací je zřejmé, že v budoucnu bude používáno více preparátů z této skupiny, podobně jako jsme toho byli svědky u inhibitorů proteazomu [104,105].
Venetoklax
A protože makroglobulinemie také výrazně exprimuje BCL-1, testuje se zde také venetoklax. Opět zde ale platí, že u WM je tento lék teprve na počátku zkoušení [107].
V této indikaci je také testován idelalisib a čeští autoři po terapii tímto lékem popsali M-IgM-flare podobně jako u rituximabu [108,109].
Transplantace
U WM se používá již léta vysokodávkovaná chemoterapie s autologní transplantací. Tato léčebná alternativa má stále své místo u vhodných pacientů s WM podobně jako u vhodných pacientů s MM a měla by být stále zvažována v léčebném plánu těchto pacientů, jak přehledně uvedli Kyriakou [110] a Kaš - čák et al [111].
Závěr
Waldenströmova makroglobulinemie je relativně vzácná nemoc, a proto i její časné rozpoznání občas činí problém. Nemoc je méně agresivní než mnohočetný myelom. V současnosti, v roce 2022, je pro iniciální léčbu upřednostňována kombinace rituximab + bendamustin před kombinací rituximab + cyklofosfamid. Na našem pracovišti používáme bendamustin v dávce 70 mg/m2 a podáváme jej 1. a 15. den cyklu, což považujeme za vhodnější než 1. a 2. den cyklu. Dle počtu trombocytů a neutrofilů pak můžeme dávku 15. den upravit a vyhnout se kritické cytopenii.
V případě neúčinnosti této kombinace podáváme kombinaci rituximab + bortezomib, ale rádi bychom místo něj vyzkoušeli ixazomib či karfilzomib, protože tyto léky nejsou tak neurotoxické. Rituximab, protilátka proti antigenu CD20, je standardní součástí léčby. V textu však upozorňujeme na řešení problému při intoleranci rituximabu. Prokázali jsme velmi dobrý efekt kombinace obinutuzumab + bendamustin. Ve všech pěti případech tato kombinace dosáhla hlubší léčebné odpovědi než odpovědi v předchozích liniích.
Inhibitory Brutonovy kinázy jsou novou skupinou léků. Zatím jsme je použili jen u několika pacientů refrakterních k některé z výše uvedených terapií, protože přece jen mají své nevýhody (rebound fenomén při náhlém přerušení jejich podávání a známé nehematologické toxicity).
Nové preparáty ze skupiny inhibitorů Brutonovy kinázy měly v klinických studiích nižší toxicitu. Snad tomu bude také tak, až se dostanou do naší klinické praxe.
Dedikace
Publikace byla vytvořena na podporu těchto aktivit: MZ ČR – RVO (FNBr, 65269705) a MOÚ: MZ ČR – RVO (MOÚ, 00209805).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare that they have no potential confl icts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.
prof. MUDr. Zdeněk Adam, CSc.
Interní hematologická a onkologická klinika
FN Brno
Jihlavská 20
625 00 Brno
e-mail: adam.zdenek@fnbrno.cz
Obdrženo/Submitted: 26. 3. 2022
Přijato/Accepted: 18. 5. 2022Klin Onkol 2023; 36(3): 177 – 191
Zdroje
1. Ščudla V, Minařík J, Pika T et al. Diferenciální diagnostika monoklonálních gamapatií z pohledu klinické praxe. I. maligní monoklonální gamapatie. Int Med Praxi 2017; 19 (5): 274–278. doi: 10.36290/int.2017.060.
2. Kyle RA, Larson DR, Therneau TM et al. Long-term follow-up of monoclonal gammopathy of undetermined significance. N Engl J Med 2018; 378 (3): 241–249. doi: 10.1056/NEJMoa1709974.
3. Varettoni M, Zibellini S, Boveri E et al. A risk-stratification model based on the initial concentration of the serum monoclonal protein and MYD88 mutation status identifies a subset of patients with IgM monoclonal gammopathy of undetermined significance at high risk of progression to Waldenstrom macroglobulinaemia or other lymphoproliferative disorders. Br J Haematol 2019; 187 (4): 441–446. doi: 10.1111/bjh.16086.
4. Sandecká V, Adam Z, Krejčí M et al. Diagnostic relevance of 18F-FDG PET/CT in newly diagnosed patients with monoclonal gammopathy of undetermined significance (MGUS): Single-center experience. Neoplasma 2020; 67 (4): 939–945. doi: 10.4149/neo_2020_191104N1137.
5. Wang H, Chen Y, Li F et al. Temporal and geographic variations of Waldenstrom macroglobulinemia incidence: a large population-based study. Cancer 2012; 118 (15): 3793–3800. doi: 10.1002/cncr.26627.
6. Castillo JJ, Olszewski AJ, Kanan S et al. Overall survival and competing risks of death in patients with Waldenström macroglobulinaemia: an analysis of the Surveillance, Epidemiology and End Results database. Br J Haematol 2015; 169 (1): 81–89. doi: 10.1111/bjh.13264.
7. Nanah A, Al Hadidi S. Bing-Neel syndrome: update on the diagnosis and treatment. Clin Lymphoma Myeloma Leuk 2022; 22 (3): e213–e219. doi: 10.1016/j.clml.2021.09.014.
8. Pika T, Kosatíková Z, Juráňová J et al. Nekorpuskulární hyperviskózní syndromy v klinické praxi. Int Med Praxi 2014; 16 (4): 156–158.
9. Jonsson V, Kierkegaard A, Salling S et al. Autoimunity in Waldenström’s macroglobulinemia. Leuk Lymphoma 1999; 34 (3–4): 373–379. doi: 10.3109/10428199909050962.
10. Pika T, Flodr P, Novák M et al. Klinická problematika IgM noklonálních gamapatií. Klin Biochem Metab 2014; 22 (2): 61–64.
11. Owen RG, Treon SP, Al-Katib A et al. Clinicopathological definition of Waldenstrom’s macroglobulinemia: consensus panel recommendations from the Second International Workshop on Waldenstrom’s Macroglobulinemia. Semin Oncol 2003; 30 (2): 110–115. doi: 10.1053/sonc.2003.50082.
12. Gerz MA. Waldenström macroglobulinemia: 2021 update on diagnosis, risk stratification, and management. Am J Hematol 2021; 96 (2): 258–269. doi: 10.1002/ajh.26 082.
13. Gavriatopoulou M, Musto P, Caers J et al. European myeloma network recommendations on diagnosis and management of patients with rare plasma cell dyscrasias. Leukemia 2018; 32 (9): 1883–1898. doi: 10.1038/s41375-018-0209-7.
14. Elba S, Castellino A, Soriasio R et al. Immunoglobulin M (IgM) multiple myeloma versus Waldenström macroglobulinemia: diagnostic challenges and therapeutic options: two case reports. J Med Case Rep 2020; 14 (1): 75. doi: 10.1186/s13256-020-02380-2.
15. Jelínek T, Bezděkova R, Zátopková M et al. Current applications of multiparameter flow cytometry in plasma cell disorders. Blood Cancer J 2017; 7 (10): e617. doi: 10.1038/bcj.2017.90.
16. Baďurová K, Gregorová J, Vlachová M et al. Waldenström macroglobulinemia. Klin Onkol 2021; 34 (6): 428–433. doi: 10.48095/ccko2021428.
17. Sedlaříková L, Sadílková K, Bešše L et al. Cytokine profiles of multiple myeloma and Waldenström macroglobulinemia. Klin Onkol 2014; 27 (1): 18–23. doi: 10.14735/amko201418.
18. Banwait R, O’Regan K, Campigotto F et al. The role of 18F-FDG PET/CT imaging in Waldenstrom macroglobulinemia. Am J Hematol 2011; 86 (7): 567–572. doi: 10.1002/ajh.22044.
19. Kaščák M, Hájek R, Minařík J et al. Diagnostika a léčba Waldenströmovy makroglobulinémie. Trans Hematol Dnes 2022; 28 (Suppl 1): S44–S74. doi: 10.48095/cctahd2022S42.
20. Leleu X, Xie W, Bagshaw M et al. The role of serum immunoglobulin free light chain in response and progression in waldenstrom macroglobulinemia. Clin Cancer Res 2011; 17 (9): 3013–3018. doi: 10.1158/1078-0432.CCR-10-2954.
21. Castillo JJ, Advani RH, Branagan AR et al. Consensus treatment recommendations from the tenth International Workshop for Waldenström Macroglobulinaemia. Lancet Haematol 2020; 7 (11): e827–e837. doi: 10.1016/S2352-3026 (20) 30224-6.
22. Kyle RA, Greipp PR, Gertz MA et al. Waldenstrom‘s macroglobulinaemia: a prospective study comparing daily with intermittent oral chlorambucil. Br J Haematol 2000; 108 (4): 737–742. doi: 10.1046/j.1365-2141.2000.01 918.x.
23. Souchet L, Levy V, Ouzegdouh M et al. Efficacy and long-term toxicity of the rituximab-fludarabine-cyclophosphamide combination therapy in Waldenstrom‘s macroglobulinemia. Am J Hematol 2016; 91 (8): 782–786. doi: 10.1002/ajh.24405.
24. Santos-Lozano A, Morales-Gonzalez A, Sanchis-Gomar F et al. Response rate to the treatment of Waldenstrom macroglobulinemia: a meta-analysis of the results of clinical trials. Crit Rev Oncol Hematol 2016; 105 : 118–126. doi: 10.1016/j.critrevonc.2016.06.004.
25. Lunn MP. Neuropathies and paraproteins. Curr Opin Neurol 2019; 32 (5): 658–665. doi: 10.1097/WCO.0000 000000000726.
26. Ghobrial IM, Fonseca R, Greipp PR et al. Initial immunoglobulin M ‚flare‘ after rituximab therapy in patients diagnosed with Waldenstrom macroglobulinemia: an Eastern Cooperative Oncology Group Study. Cancer 2004; 101 (11): 2593–2598. doi: 10.1002/cncr.20658.
27. Rummel MJ, Lerchenmüller C, Hensel M et al. Two years rituximab maintenance vs. observation after first line treatment with Bendamustine Plus Rituximab (B-R) in patients with Waldenström‘s Macroglobulinemia (MW): results of a prospective, randomized, multicenter phase 3 study. Blood 2019; 134 (Suppl 1): 343. doi: 10.1182/blood-2019-121909.
28. Dimopoulos MA, Anagnostopoulos A, Kyrtsonis MC et al. Primary treatment of Waldenstrom macroglobulinemia with dexamethasone, rituximab, and cyclophosphamide. J Clin Oncol 2007; 25 (22): 3344–3349. doi: 10.1200/JCO.2007.10.9926.
29. Kastritis E, Gavriatopoulou M, Kyrtsonis MC et al. Dexamethasone, rituximab, and cyclophosphamide as primary treatment of Waldenstrom macroglobulinemia: final analysis of a phase 2 study. Blood 2015; 126 (11): 1392–1394. doi: 10.1182/blood-2015-05-647420.
30. Mössner E, Brünker P, Moser P et al. Increasing the efficacy of CD20 antibody therapy through the engineering of a new type II anti-CD20 antibody with enhanced direct and immune effector cell mediated B cell cytotoxicity. Blood 2010; 115 (22): 4393–4402. doi: 10.1182/blood-2009-06-225979.
31. Leblond V, Kastritis E, Advani R et al. Treatment recommendations from the Eighth International Workshop on Waldenström‘s Macroglobulinemia. Blood 2016; 128 (10): 1321–1328. doi: 10.1182/blood-2016-04-711234.
32. Gavriatopoulou M, Kastritis E, Kyrtsonis MC et al. Phase 2 study of ofatumumab, fludarabine and cyclophosphamide in relapsed/refraktory Waldenström‘s macroglobulinemia. Leuk Lymphoma 2017; 58 (6): 1506–1508. doi: 10.1080/10428194.2016.1233541.
33. Furman RR, Eradat HA, DiRienzo CG et al. Once-weekly ofatumumab in untreated or relapsed Waldenström‘s macroglobulinaemia: an open-label, single-arm, phase 2 study. Lancet Haematol 2017; 4 (1): e24–e34. doi: 10.1016/S2352-3026 (16) 30166-1.
34. Sehn LH, Chua N, Mayer J et al. Obinutuzumab plus bendamustine versus bendamustine monotherapy in patients with rituximab-refractory indolent non-Hodgkin lymphoma (GADOLIN): a randomised, controlled, open-label, multicentre, phase 3 trial. Lancet Oncol 2016; 17 (8): 1081–1093. doi: 10.1016/S1470-2045 (16) 30097-3.
35. García-Muñoz R, López-Díaz-de-Cerio A, Feliu J et al. Follicular lymphoma: in vitro effects of combining lymphokine-activated killer (LAK) cell-induced cytotoxicity and rituximab - and obinutuzumab-dependent cellular cytotoxicity (ADCC) activity. Immunol Res 2016; 64 (2): 548–557. doi: 10.1007/s12026-015-8747-9.
36. Herter S, Herting F, Mundigl O et al. Preclinical activity of the type II CD20 antibody GA101 (obinutuzumab) compared with rituximab and ofatumumab in vitro and in xenograft models. Mol Cancer Ther 2013; 12 (10): 2031–2042. doi: 10.1158/1535-7163.MCT-12-1182.
37. Sehn LH, Goy A, Offner FC et al. Randomized phase II trial comparing obinutuzumab (GA101) with rituximab in patients with relapsed CD20+ indolent B cell non-Hodgkin lymphoma: final analysis of the GAUSS study. J Clin Oncol 2015; 33 (30): 3467–3474. doi: 10.1200/JCO.2014.59.2139.
38. Marcus RE, Davies AJ, Ando K et al. Obinutuzumab-based induction and maintenance prolongs progression-free survival (PFS) in patients with previously untreated follicular lymphoma: primary results of the randomized phase 3 GALLIUM study. Blood 2016; 128 : 6.
39. Hiddemann W, Barbui AM, Canales MA et al. Immunochemotherapy with obinutuzumab or rituximab for previously untreated follicular lymphoma in the GALLIUM study: influence of chemotherapy on efficacy and safety. J Clin Oncol 2018; 36 (23): 2395–2404. doi: 10.1200/JCO.2017.76.8960.
40. Seymour JF, Marcus R, Davies A et al. Association of early disease progression and very poor survival in the GALLIUM study in follicular lymphoma: benefit of obinutuzumab in reducing the rate of early progression. Haematologica 2019; 104 (6): 1202–1208. doi: 10.3324/haematol.2018.209015.
41. Jamois C, Gibiansky E, Gibiansky L et al. Role of obinutuzumab exposure on clinical outcome of follicular lymphoma treated with first-line immunochemotherapy. Br J Clin Pharmacol 2019; 85 (7): 1495–1506. doi: 10.1111/bcp.13920.
42. Salles GA, Morschhauser F, Solal-Céligny P et al. Obinutuzumab (GA101) in patients with relapsed/refractory indolent non-Hodgkin lymphoma: results from the Phase II GAUGUIN study. J Clin Oncol 2013; 31 (23): 2920–2926. doi: 10.1200/JCO.2012.46.9718.
43. Cheson BD, Chua N, Mayer J et al. Overall survival benefit in patients with rituximab-refractory indolent non--Hodgkin lymphoma who received obinutuzumab plus bendamustine induction and obinutuzumab maintenance in the GADOLIN study. J Clin Oncol 2018; 36 (22): 2259–2266. doi: 10.1200/JCO.2017.76.3656.
44. Marcus R, Devies A, Ando K et al. Obinutuzumab for the first-line treatment of Follicular lymphoma. N Eng J Med 2017; 377 (14): 1331–1344. doi: 10.1056/NEJMoa1614598.
45. Goede V, Fischer K, Engelke A et al. Obinutuzumab as frontline treatment of chronic lymphocytic leukemia: updated results of the CLL11 study. Leukemia 2015; 29 (7): 1602–1604. doi: 10.1038/leu.2015.14.
46. Vitolo U, Trněný M, Belada D et al. Obinutuzumab or rituximab plus CHOP in patients with previously untreated diffuse large B-cell lymphoma: final results from an open-label, randomized phase 3 study (GOYA). Blood 2016; 128 (22): 470. doi: 10.1182/blood.V128.22.470.470.
47. Sehn LH, Martelli M, Trněný M et al. A randomized, open-label, Phase III study of obinutuzumab or rituximab plus CHOP in patients with previously untreated diffuse large B-Cell lymphoma: final analysis of GOYA. J Hematol Oncol 2020; 13 (1): 71. doi: 10.1186/s13045-020-00900-7.
48. Casasnovas RO, Salles GA, Oberic L et al. Obinutuzumab versus rituximab in combination with ACVBP-14 or CHOP-14 following a PET-driven strategy in Aa-IPI 1–3 DLBCL patients (< 60 years): third planned interim and final analyses of the gained trial. Blood 2017; 130 (Suppl 1): 190. doi: 10.1182/blood.V130.Suppl_1.190.190.
49. Herold M, Hoster E, Janssens A et al. Immunochemotherapy and maintenance with obinutuzumab or rituximab in patients with previously untreated marginal zone lymphoma in the randomized GALLIUM trial. Hemasphere 2022; 6 (3): e699. doi: 10.1097/HS9.0000000000000699.
50. Luo C, Wu G, Huang X et al. Efficacy and safety of new anti-CD20 monoclonal antibodies versus rituximab for induction therapy of CD20+ B-cell non-Hodgkin lymphomas: a systematic review and meta-analysis. Sci Rep 2021; 11 (1): 3255. doi: 10.1038/s41598-021-82841-w.
51. Guzauskas GF, Masaquel A, Thuresson PO et al. Obinutuzumab plus chemotherapy followed by obinutuzumab monotherapy is cost-effective vs. rituximab plus chemotherapy followed by rituximab monotherapy for previously untreated follicular lymphoma patients in the United States. Leuk Lymphoma 2019; 60 (7): 1668–1676. doi: 10.1080/10428194.2018.1551532.
52. Adam Z, Krejčí M, Pour L et al. Obinutuzumab v léčbě pacientky s Waldenströmovou makroglobulinémií netolerující rituximab – popis případu. Transfuze Hematol Dnes 2021; 27 (2): 160–165. doi: 10.48095/cctahd2021160.
53. Tomowiak C, Poulain S, Herbaux C et al. Obinutuzumab and idelalisib in symptomatic patients with relapsed/refractory Waldenström macroglobulinemia. Blood Adv 2021; 5 (9): 2438–2446. doi: 10.1182/bloodadvances.2020003895.
54. Freeman CL, Sehn LH. A tale of two antibodies: obinutuzumab versus rituximab. Br J Haematol 2018; 182 (1): 29–45. doi: 10.1111/bjh.15232.
55. Treon SP, Hanzis C, Tripsas C et al. Bendamustine therapy in patients with relapsed or refractory Waldenstrom‘s macroglobulinemia. Clin Lymphoma Myeloma Leuk 2011; 11 (1): 133–135. doi: 10.3816/CLML.2011.n.030.
56. Tedeschi A, Picardi P, Ferrero S et al. Bendamustine and rituximab combination is safe and effective as salvage regimen in Waldenstrom macroglobulinemia. Leuk Lymphoma 2015; 56 (9): 2637–2642. doi: 10.3109/10428194.2015.1012714.
57. Laribi K, Poulain S, Willems L et al. Bendamustine plus rituximab in newly-diagnosed Waldenstrom macroglobulinaemia patients. A study on behalf of the French Innovative Leukaemia Organization (FILO). Br J Haematol 2019; 186 (1): 146–149. doi: 10.1111/bjh.15718.
58. Rummel MJ, Lerchenmüller C, Hensel M et al. Two years rituximab maintenance vs. observation after first line treatment with Bendamustine Plus Rituximab (B-R) in patients with Waldenström‘s Macroglobulinemia (MW): results of a prospective, randomized, multicenter phase 3 study (the StiL NHL7-2008 MAINTAIN trial). Blood 2019; 134 (8): 343.
59. Rummel MJ, Niederle N, Maschmeyer G et al. Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet 2013; 381 (9873): 1203–1210. doi: 10.1016/S0140-6736 (12) 61763-2.
60. Castillo JJ, Gustine J, Meid K et al. Bendamustine and bortezomib-containing regimens produce higher response rates and more durable responses versus cyclophosphamide-based therapy in frontline Waldenstrom macroglobulinemia. Blood 2017; 130 (Suppl 1): 1488–1489.
61. Paludo J, Abeykoon JP, Shreders A et al. Bendamustine and rituximab (BR) versus dexamethasone, rituximab, and cyclophosphamide (DRC) in patients with Waldenstrom macroglobulinemia. Ann Hematol 2018; 97 (8): 1417–1425. doi: 10.1007/s00277-018-3311-z.
62. Santos-Lozano A, Morales-Gonzalez A, Sanchis-Gomar F et al. Response rate to the treatment of Waldenström macroglobulinemia: a meta-analysis of the results of clinical trials. Crit Rev Oncol Hematol 2016; 105 : 118–126. doi: 10.1016/j.critrevonc.2016.06.004.
63. Castillo JJ, Itchaki G, Paludo J et al. Ibrutinib for the treatment of Bing-Neel syndrome: a multicenter study. Blood 2019; 133 (4): 299–305. doi: 10.1182/blood-2018-10-879593.
64. Benevolo G, Ferrero S, Villivà N et al. Treatment of relapsed/refractory Waldenström macroglobulinemia patients: final clinical and molecular results of the phase II Brb (Bendamustine, Rituximab and Bortezomib) trial of the Fondazione Italiana Linfomi (FIL). Blood 2021; 138 (Suppl 1): 48. doi: 10.1182/blood-2021-148424.
65. Chan WLW, Chong VCL, Wee IJY et al. Evaluating front line treatment regimens for Waldenstrom macroglobulinaemia: a systematic review and meta-analysis. Blood 2021; 138 (Suppl 1): 1358. doi: 10.1182/blood-2021-150678.
66. Treon SP, Soumerai JD, Branagan AR et al. Thalidomide and rituximab in Waldenstrom macroglobulinemia. Blood 2008; 112 (12): 4452–4457. doi: 10.1182/blood-2008-04-150854.
67. Treon SP, Soumerai JD, Branagan AR et al. Lenalidomide and rituximab in Waldenstrom‘s macroglobulinemia. Clin Cancer Res 2009; 15 (1): 355–360. doi: 10.1158/1078-0432.CCR-08-0862.
68. Fouquet G, Guidez S, Petillon MO et al. Lenalidomide is safe and active in Waldenström macroglobulinemia. Am J Hematol 2015; 90 (11): 1055–1059. doi: 10.1002/ajh.24175.
69. Dimopoulos MA, Chen C, Kastritis E et al. Bortezomib as a treatment option in patients with Waldenstrom macroglobulinemia. Clin Lymphoma Myeloma Leuk 2010; 10 (2): 110–117. doi: 10.3816/CLML.2010.n.015.
70. Dimopoulos MA, Terpos E, Kastritis E. Proteasome inhibitor therapy for Waldenström‘s macroglobulinemia. Clin Lymphoma Myeloma Leuk 2013; 13 (2): 235–237. doi: 10.1016/j.clml.2013.02.014.
71. Treon SP, Ioakimidis L, Soumerai JD et al. Primary therapy of Waldenstrom macroglobulinemia with bortezomib, dexamethasone, and rituximab: WMCTG clinical trial 05-180. J Clin Oncol 2009; 27 (23): 3830–3835. doi: 10.1200/JCO.2008.20.4677.
72. Chen C, Kouroukis CT, White D et al. Bortezomib in relapsed or refractory Waldenstrom‘s macroglobulinemia. Clin Lymphoma Myeloma 2009; 9 (1): 74–76. doi: 10.3816/CLM.2009.n.019.
73. Ghobrial IM, Xie W, Padmanabhan S et al. Phase II trial of weekly bortezomib in combination with rituximab in untreated patients with Waldenstrom macroglobulinemia. Am J Hematol 2010; 85 (9): 670–674. doi: 10.1002/ajh.21788.
74. Sklavenitis-Pistofidis R, Capelletti M, Liu CJ et al. Bortezomib overcomes the negative impact of CXCR4 mutations on survival of Waldenstrom macroglobulinemia patients. Blood 2018; 132 (24): 2608–2612. doi: 10.1182/blood-2018-07-863241.
75. Gavriatopoulou M, Garcia-Sanz R, Kastritis E et al. BDR in newly diagnosed patients with WM: final analysis of a phase 2 study after a minimum follow-up of 6 years. Blood 2017; 129 (4): 456–459. doi: 10.1182/blood-2016-09-742411.
76. Dimopoulos MA, Garcia-Sanz R, Gavriatopoulou M et al. Primary therapy of Waldenstrom macroglobulinemia (WM) with weekly bortezomib, low-dose dexamethasone, and rituximab (BDR): long-termresults of a phase 2 study of the European Myeloma Network (EMN). Blood 2013; 122 (19): 3276–3782. doi: 10.1182/blood-2013-05-503862.
77. Rossi G, Gramegna D, Paoloni F et al. Short course of bortezomib in anemic patients with relapsed cold agglutinin disease: a phase 2 prospective GIMEMA study. Blood 2018; 132 (5): 547–550. doi: 10.1182/blood-2018-03-835413.
78. Berentsen S, Barcellini W, D’Sa S et al. Cold agglutinin disease revisited: a multinational observational study of 232 pacients. Blood 2022; 136 (4): 480–488. doi: 10.1182/blood.2020005674.
79. Kong D, Li Y, Fu C et al. Bortezomib provides favorable efficacy in type 3 acquired von willebrand syndrome related to lymphoplasmacytic lymphoma/Waldenstrom‘s macroglobulinemia. Leuk Lymphoma 2022; 63 (2): 491–494. doi: 10.1080/10428194.2021.1992766.
80. Ojeda-Uribe M, Rimelen V, Marzullo C. Good profile of efficacy/tolerance of bortezomib or idelalisib in Waldenström macroglobulinemia associated with acquired Von Willebrand syndrome. J Blood Med 2020; 11 : 67–72. doi: 10.2147/JBM.S233059.
81. Treon SP, Tripsas CK, Meid K et al. Carfilzomib, rituximab, and dexamethasone (CaRD) treatment offers a neuropathy-sparing approach for treating Waldenström‘s macroglobulinemia. Blood 2014; 124 (4): 503–510. doi: 10.1182/blood-2014-03-566273.
82. Vesole DH, Richter J, Biran N et al. Carfilzomib as salvage therapy in Waldenstrom macroglobulinemia: a case series. Leuk Lymphoma 2018; 59 (1): 259–261. doi: 10.1080/10428194.2017.1321749.
83. Chaudhry M, Steiner R, Claussen C et al. Carfilzomib-based combination regimens are highly effective frontline therapies for multiple myeloma and Waldenstrom‘s macroglobulinemia. Leuk Lymphoma 2019; 60 (4): 964–970. doi: 10.1080/10428194.2018.1508668.
84. Castillo JJ, Meid K, Catherine A et al. Ixazomib, dexamethasone, and rituximab in treatment-naive patients with Waldenström macroglobulinemia: long-term follow--up. Blood Adv 2020; 4 (16): 3952–3959. doi: 10.1182/bloodadvances.2020001963.
85. Kersten MJ, Amaador K, Minnema MC et al. Combining ixazomib with subcutaneous rituximab and dexamethasone in relapsed or refractory Waldenström’s macroglobulinemia: final analysis of the phase I/II HOVON124/ECWM-R2 study. J Clin Oncol 2022; 40 (1): 40–51. doi: 10.1200/JCO.21.00105.
86. Kastritis E, Dimopoulos MA. Proteasome inhibitors in Waldenström macroglobulinemia. Hematol Oncol Clin North Am 2018; 32 (5): 829–840. doi: 10.1016/j.hoc.2018.05.011.
87. Fečková-Mihályová J, Ďuraš J, Zuchnická J et al. Ibrutinib v hematoonkologii. Klin Farmakol Farm 2016; 30 (3): 8–14. doi: 10.36290/far.2016.022.
88. Treon SP, Tripsas CK, Meid K et al. Ibrutinib in previously treated Waldenstrom‘s macroglobulinemia. N Engl J Med 2015; 372 (15): 1430–1440. doi: 10.1056/NEJMoa1501548.
89. Yun S, Vincelette ND, Acharya U et al. Risk of atrial fibrillation and bleeding diathesis associated with Ibrutinib treatment: a systematic review and pooled analysis of four randomized controlled trials. Clin Lymphoma Myeloma Leuk 2017; 17 (1): 31–37. doi: 10.1016/j.clml.2016.09.010.
90. Gustine JN, Meid K, Dubeau T et al. Ibrutinib discontinuation in Waldenstrom macroglobulinemia: etiologies, outcomes, and IgM rebound. Am J Hematol 2018; 93 (4): 511–517. doi: 10.1002/ajh.25023.
91. Treon SP, Xu L, Hunter Z. MYD88 mutations and response to ibrutinib in Waldenstrom’s macroglobulinemia. N Engl J Med 2015; 373 (6): 584–586. doi: 10.1056/NEJMc1506192.
92. Dimopoulos MA, Trotman J, Tedeschi A et al. Ibrutinib for patients with rituximab-refractory Waldenstrom‘s macroglobulinaemia (iNNOVATE): an open-label substudy of an international, multicentre, phase 3 trial. Lancet Oncol 2017; 18 (2): 241–250. doi: 10.1016/S1470-2045 (16) 30632-5.
93. Treon SP, Gustine J, Meid K et al. Ibrutinib is highly active as first line therapy in symptomatic Waldenstrom‘s macroglobulinemia. Blood 2017; 130 (Suppl 1): 2767. doi: 10.1182/BLOOD.V130.SUPPL_1.2767.2767.
94. Treon SP, Gustine J, Meid K et al. Ibrutinib monotherapy in symptomatic, treatment-naive patients with Waldenstrom macroglobulinemia. J Clin Oncol 2018; 36 (27): 2755–2761. doi: 10.1200/JCO.2018.78.6426.
95. Abeykoon JP, Zanwar S, Ansell SM et al. Ibrutinib monotherapy outside of clinical trial setting in Waldenstrom macroglobulinaemia: practice patterns, toxicities and outcomes. Br J Haematol 2020; 188 (3): 394–403. doi: 10.1111/bjh.16168.
96. Buske C, Tedeschi A, Trotman J et al. Ibrutinib plus rituximab versus placebo plus rituximab for Waldenström’s macroglobulinemia: final analysis from the randomized phase III iNNOVATE study. J Clin Oncol 2022; 40 (1): 52–62. doi: 10.1200/JCO.21.00838.
97. Castillo JJ, Gustine JN, Meid K et al. Impact of ibrutinib dose intensity on patient outcomes in previously treated Waldenstrom macroglobulinemia. Haematologica 2018; 103 (10): e466–e468. doi: 10.3324/haematol.2018.191 999.
98. Castillo JJ, Gustine JN, Meid K et al. Ibrutinib withdrawal symptoms in patients with Waldenström macroglobulinemia. Haematologica 2018; 103 (7): e307–e310. doi: 10.3324/haematol.2017.186908.
99. Paydas S. Management of adverse effects/toxicity of ibrutinib. Crit Rev Oncol Hematol 2019; 136 : 56–63. doi: 10.1016/j.critrevonc.2019.02.001.
100. Abbas HA, Wierda WG. Acalabrutinib: a selective bruton tyrosine kinase inhibitor for the treatment of B-cell malignancies. Front Oncol 2021; 11 : 668162. doi: 10.3389/fonc.2021.668162.
101. Owen RG, McCarthy H, Rule S et al. Acalabrutinib monotherapy in patients with Waldenström macroglobulinemia: a single-arm, multicentre, phase 2 study. Lancet Haematol 2020; 7 (2): e112–e121. doi: 10.1016/S2352-3026 (19) 30210-8.
102. Tam CS, Opat S, D’Sa S et al. A randomized phase 3 trial of zanubrutinib vs ibrutinib in symptomatic Waldenström macroglobulinemia: the ASPEN study. Blood 2020; 136 (18): 2038–2050. doi: 10.1182/blood.2020006844.
103. Tam CS, LeBlond V, Novotny W et al. A head-to-head Phase III study comparing zanubrutinib versus ibrutinib in patients with Waldenström macroglobulinemia. Future Oncol 2018; 14 (22): 2229–2237. doi: 10.2217/fon-2018-0163.
104. Dimopoulos M, Sanz RG, Lee HP et al. Zanubrutinib for the treatment of MYD88 wild-type Waldenström macroglobulinemia: a substudy of the phase 3 ASPEN trial. Blood Adv 2020; 4 (23): 6009–6018. doi: 10.1182/bloodadvances.2020003010.
105. Argyropoulos KV, Palomba ML. First-generation and second-generation bruton tyrosine kinase inhibitors in Waldenström macroglobulinemia. Hematol Oncol Clin North Am 2018; 32 (5): 853–864. doi: 10.1016/j.hoc.2018.05.012.
106. Munakata W, Tobinai K. Tirabrutinib hydrochloride for B-cell lymphomas. Drugs Today (Barc) 2021; 57 (4): 277–289. doi: 10.1358/dot.2021.57.4.3264113.
107. Castillo JJ, Allan JN, Siddiqi T et al. Venetoclax in previously treated Waldenström macroglobulinemia. J Clin Oncol 2022; 40 (1): 63–71. doi: 10.1200/JCO.21.01194.
108. Novák J, Havrda M, Gahérová Ľ et al. Clinical case: idelalisib-induced immunoglobulin flare. Immunopharmacol Immunotoxicol 2017; 39 (4): 251–255. doi: 10.1080/08923973.2017.1318912.
109. Belada D. Idelalisib v léčbě pacientů s folikulárním lymfomem. Farmakoterapie 2015; 11 (3): 292–296.
110. Kyriakou C. High-dose therapy and hematopoietic stem cell transplantation in Waldenström macroglobulinemia. Hematol Oncol Clin North Am 2018; 32 (5): 865–874. doi: 10.1016/j.hoc.2018.05.013.
111. Kaščák M, Ďuraš J, Navrátil M et al. Autologní transplantace kmenových buněk u Waldenströmovy makroglobulinemie. Transfuze Hematol Dnes 2016; 22 (1): 28–38.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2023 Číslo 3- Spasmolytický účinek metamizolu
- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
-
Všetky články tohto čísla
- Waldenströmova makroglobulinemie, monoklonální gamapatie a Dr. Kyle
- Waldenströmova makroglobulinemie – klinické projevy a přehled léčby včera, dnes a zítra
- Etnické rozdiely v incidencii zhubných nádorov detí
- Skóre polygenního rizika (PRS) a jeho potenciál pro stratifikaci rizika karcinomu prsu
- Hypoplastická forma myelodysplastické neoplazie
- Kvantitatívne profilovanie génov asociovaných s dráhami vzniku mozgových nádorov
- Molekulární testování karcinomu endometria – analýza prvních zkušeností z klinické praxe
- Psychological care reflecting the specifics of the course of viral infection in SARS-CoV-2 oncological patients with oxygenation disorder – a case series
- Efekt imunoterapie u mladého pacienta s mismatch repair deficientním karcinomem rekta – kazuistika
- Hepatosplenic T-cell lymphoma presented with massive splenomegaly and pancytopenia – a case report
- Nová naděje pro pacienty s metastatickým uveálním melanomem
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Waldenströmova makroglobulinemie – klinické projevy a přehled léčby včera, dnes a zítra
- Skóre polygenního rizika (PRS) a jeho potenciál pro stratifikaci rizika karcinomu prsu
- Molekulární testování karcinomu endometria – analýza prvních zkušeností z klinické praxe
- Hypoplastická forma myelodysplastické neoplazie
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



