-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Výsledky rozšířeného novorozeneckého screeningu v České republice
The results of expanded newborn screening in the Czech Republic
The nationwide newborn screening (NBS) using dried blood spots (DBS) was started in 1975 for phenylketonuria//hyperphenylalaninemia (PKU/HPA); in 1985 for congenital hypothyroidism (CH); in 2006 for congenital adrenal hyperplasia (CAH) and in X/2009 screening for cystic fibrosis (CF) and 9 inherited metabolic diseases – maple syrup urine disease (MSUD), glutaric aciduria type I (GA I), isovaleric aciduria (IVA), medium chain acyl-CoA, long chain 3-hydroxyacyl-CoA and very long chain acyl-CoA dehydrogenase deficiency (MCADD, LCHADD and VLCADD), carnitine palmitoyltransferase I and II deficiency (CPTD I and II) and carnitine-acylcarnitine translocase deficiency (CACTD) was mandated.
Methods:
From 1st January 2002 through 31st December 2012 a total of 1 179,136 newborns were screened for PKU//HPA and CH; phenylalanine was measured by different methods, since X/2009 solely by tandem mass spectrometry (MS/MS); the levels of thyreotropin were measured by fluoroimmunoassay (FIA). The of 17-hydroxyprogesterone concentrations were determined in 752,922 newborns by FIA. The level of immunoreactive trypsinogen (IRT) was measured in 367,114 newborns by FIA and the CFTR gene (at first 32, later 50 most common mutations) was analysed in original DBS in 1.05% of newborns with the highest IRT levels to minimize false positive results. The spectrum of metabolites for 9 expanded inborn errors of metabolism was analysed in 362,653 newborns by MS/MS.Results:
NS detected in total 646 patients with subsequently confirmed diagnosis. Screening prevalence were as follows PKU/HPA 1 : 7,234; CH 1 : 3,562; CAH 1 : 12,343; CF 1 : 7,060; MCADD 1 : 17,269; LCHADD 1 : 51,808; VLCADD 1 : 90,663; GA I 1 : 120,884; MSUD and IVA both 1 : 181,327. No case of CPTD I and CPTDII/CACTD was detected. Efficacy of NBS increased with the expansion of diseases in the programme: detection rate rose from 1 : 2,701 in 2002–2005 over 1 : 2,072 in 2007–2008 to 1 : 1,138 after last expansion of NBS in 2009. False positive rate (FPR) was 0.540%, of which 74% represent results of CAH screening.Conclusion:
NBS is an effective approach for presymptomatic detection of serious rare diseases. Further optimization is a subject of current research including the introduction of additional analytical tests (second tiers) to reduce FPR and by further expanding of screened disorders.Key words:
newborn screening, dried blood spot, prevalence, rare diseases, congenital hypothyroidism, congenital adrenal hyperplasia, cystic fibrosis, phenylketonuria, inherited metabolic disorders
Autoři: F. Votava 1; V. Kožich 2; P. Chrastina 2; K. Pešková 2; T. Adam 3; D. Friedecký 3; E. Hlídková 3; H. Vinohradská 4; P. Dejmek 1; V. Krulišová 5; A. Holubová 5; M. Balaščaková 5; T. Piskáčková 5; M. Macek 5; R. Gaillyová 6; I. Valášková 6; V. Skalická 7
Působiště autorů: Klinika dětí a dorostu, UK 3. lékařská fakulta a FN Královské Vinohrady, Prahapřednosta doc. MUDr. F. Votava, Ph. D. 1; Ústav dědičných metabolických poruch, UK 1. lékařská fakulta a Všeobecná fakultní nemocnice, Prahapřednosta prof. MUDr. V. Kožich, CSc. 2; Laboratoř dědičných metabolických poruch OKBI, UP Lékařská fakulta a FN Olomoucvedoucí doc. RNDr. T. Adam, Ph. D. 3; Oddělení klinické biochemie, pracoviště Dětská nemocnice, MU Lékařská fakulta a FN, Brnoprimář doc. MUDr. M. Dastych, CSc. 4; Ústav biologie a lékařské genetiky, UK 2. lékařská fakulta a FN Motol, Prahapřednosta prof. MUDr. M. Macek, DrSc. 5; Oddělení lékařské genetiky, MU Lékařská fakulta a FN, Brnoprimářka MUDr. R. Gaillyová, Ph. D. 6; Pediatrická klinika, UK 2. lékařská fakulta a FN Motol, Prahapřednosta prof. MUDr. J. Lebl, CSc. 7
Vyšlo v časopise: Čes-slov Pediat 2014; 69 (2): 77-86.
Kategorie: Původní práce
Souhrn
Pomocí celoplošného novorozeneckého laboratorního screeningu ze suché kapky krve (SKK) na filtračním papírku jsou od roku 1975 vyhledáváni pacienti s fenylketonurií/hyperfenylalaninemií (PKU/HPA); od roku 1985 s vrozenou hypotyreózou (CH); od roku 2006 s kongenitální adrenální hyperplazií (CAH) a od X/2009 pacienti s cystickou fibrózou (CF) a 9 dalšími dědičnými poruchami metabolismu – leucinózou (MSUD), glutarovou acidurií typu I (GA I), izovalerovou acidurií (IVA), deficitem dehydrogenázy acyl-CoA se středně dlouhým, 3-hydroxyacyl-CoA s dlouhým a acyl-CoA s velmi dlouhým řetězcem (MCADD, LCHADD a VLCADD), deficitem karnitinpalmitoyltransferázy I a II (CPTD I a II) a deficitem karnitinacylkarnitintranslokázy (CACTD).
Metodika:
V období od 1. ledna 2002 až do 31. prosince 2012 bylo vyšetřeno 1 179 136 novorozenců na PKU//HPA a CH; koncentrace fenylalaninu byla měřena různými metodami a od X/2009 jednotně tandemovou hmotnostní spektrometrií (MS/MS); koncentrace tyreotropinu byla zjišťována pomocí fluoroimunoeseje (FIA). U 752 922 novorozenců byla změřena koncentrace 17-hydroxyprogesteronu pomocí FIA. U 367 114 dětí byl změřen imunoreaktivní trypsin (IRT) pomocí FIA a u 1,05 % novorozenců s nejvyšším IRT bylo vyšetřeno v prvotních SKK 32 a později 50 nejčastějších mutací v genu CFTR s cílem minimalizovat falešnou pozitivitu. U 362 653 novorozenců byly analyzovány metabolity pro záchyt dalších 9 dědičných metabolických poruch pomocí MS/MS.Výsledky:
Celkem bylo novorozeneckým screeningem zachyceno 646 pacientů s následně potvrzenou diagnózou. Screeningové prevalence jednotlivých nemocí byly následující CH 1 : 3562; CAH 1 : 12 343; CF 1 : 7060; PKU/HPA 1 : 7234; MCADD 1 : 17 269; LCHADD 1 : 51 808; VLCADD 1 : 90 663; GA I 1 : 120 884; MSUD a IVA shodně 1 : 181 327. Screeningem dosud nebyl zachycen žádný novorozenec s CPTD I, II a CACTD. Efektivita screeningového programu v ČR se zvyšovala, kumulativní četnost záchytů narůstala z 1 : 2701 v letech 2002–2005 přes 1 : 2072 v letech 2007–2008 až na 1 : 1138 po zásadním rozšíření novorozeneckého screeningu (NS) v roce 2009. Četnost falešné pozitivity (FPR) činila 0,540 % , z toho 74 % reprezentuje NS CAH.Závěr:
NS je účinný nástroj sekundární prevence vzácných onemocnění s účinnou léčbou. Pro optimalizaci programu se zavádějí druhostupňová vyšetření u malého množství vzorků s cílem snížit falešnou pozitivitu a hledají se možnosti rozšíření spektra screenovaných chorob.Klíčová slova:
novorozenecký screening, suchá kapka krve, prevalence, vzácná onemocnění, kongenitální hypotyreóza, kongenitální adrenální hyperplazie, cystická fibróza, fenylketonurie, dědičné metabolické poruchyÚVOD
Pod pojem novorozenecký screening (NS) lze v širším smyslu zahrnout jakékoliv preventivní vyšetření novorozence, v užším smyslu se tímto pojmem myslí systematické vyhledávání léčebně ovlivnitelných chorob v jejich preklinickém stadiu. Laboratorní novorozenecký screening je založen na odběru kapilární krve na filtrační papírek (tzv. suché kapky krve, SKK) podle přesně dohodnutých pravidel všem novorozencům na definovaném území (většinou celostátně). SKK se následně vyšetřují v centrálních laboratořích. Tento typ NS je předmětem předkládaného sdělení.
Zakladatelem NS je profesor Robert Guthrie z univerzity v Buffalu ve státě New York, USA. V roce 1963 vyvinul a následně i zavedl do praxe jednoduchou, levnou a spolehlivou semikvantitativní metodu měření koncentrace fenylalaninu (založenou na principu inhibice růstu bakterií) pro NS fenylketonurie [1]. Od té doby se spektrum vyhledávaných chorob stále rozšiřuje. Tabulka 1 uvádí poslední známá data z let 2010/2011 o NS prováděných v Evropě [2]. V jednotlivých státech USA je počet screenovaných chorob v současné době mnohem vyšší, ve většině států mezi 40–50 s maximem 54 nemocí v Minnesotě [3]. Odborné zastřešení NS poskytuje mezinárodní společnost ISNS, International Society for Neonatal Screening, http://www.isns-neoscreening.org/, která organizuje pravidelné celosvětové a regionální (kontinentální) kongresy. Např. 6. evropský kongres této organizace se konal v roce 2009 v Praze a bylo mu věnováno samostatné číslo Česko-slovenské pediatrie [4].
Tab. 1. Přehled novorozeneckých screeningových programů v 36 evropských státech. 
Vysvětlivky: PKU/HPA = fenylketonurie nebo hyperfenylalaninemie; CH = kongenitální hypotyreóza; MCADD = deficit acyl-CoA dehydrogenázy mastných kyselin se středně dlouhým řetězcem; CAH = kongenitální adrenální hyperplazie, resp. deficit 21-hydroxylázy; CF = cystická fibróza; GAL = galaktosémie; BD = deficit biotinidázy; rozšířené DMP = další dědičné metabolické poruchy (kromě PKU a MCADD), spektra a počty vyšetřovaných rozšířených DMP se v jednotlivých státech liší. Upraveno podle [2], 28 členských států Evropské unie + Bosna a Hercegovina, Černá Hora, FYROM (bývalá jugoslávská republika Makedonie), Island, Norsko, Srbsko, Švýcarsko vč. Lichtenštejnska, Turecko). V Albánii není NS prováděn. Nedostupné údaje: Bělorusko, Kosovo, Moldavsko, Rusko a Ukrajina. Od počátku 70. let minulého století se datují pilotní studie NS fenylketonurie (PKU) v naší republice [5, 6], který se v roce 1975 stal naším prvním, pravidelně prováděným celostátním screeningovým programem. Jako druhý v pořadí byl v roce 1985 zaveden NS kongenitální hypotyreózy (CH) [7]. Dalším rozšířením bylo přidání kongenitální adrenální hyperplazie (CAH) v roce 2006 [8]. K poslednímu významnému rozšíření NS v ČR došlo v říjnu 2009, kdy do spektra vyhledávaných onemocnění byla přidána cystická fibróza (CF) [9] a 9 dalších dědičných metabolických poruch [10, 11, 12]. Tabulka 2 shrnuje v současnosti vyhledávaná onemocnění v ČR a hlavní důvod, proč je potřebná jejich včasná detekce. Všechna onemocnění vyhledávaná pomocí NS splňují definici vzácných onemocnění („rare disease“, RD, prevalence <1 : 2000), proto se NS stává modelovým nástrojem diagnostiky a léčby RD a zásadním způsobem může pomoci naplňovat směrnice Evropské unie a usnesení Vlády ČR pro RD [13, 14].
Tab. 2. Onemocnění vyhledávaná novorozeneckým screeningem v ČR. 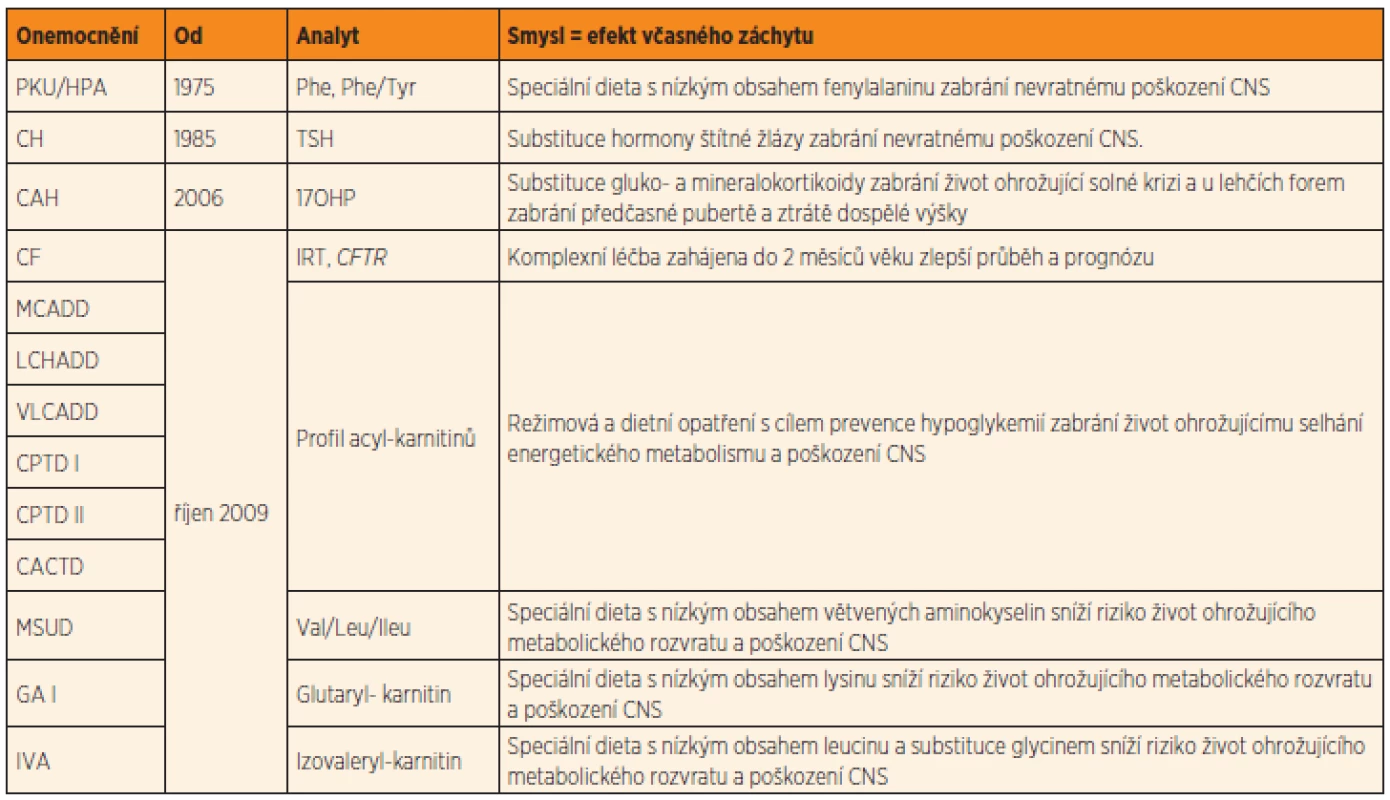
Vysvětlivky: PKU/HPA = fenylketonurie nebo hyperfenylalaninemie; CH = kongenitální hypotyreóza; CAH = kongenitální adrenální hyperplazie, resp. deficit 21-hydroxylázy; CF = cystická fibróza; MCADD = deficit acyl-CoA dehydrogenázy mastných kyselin se středně dlouhým řetězcem; LCHADD = deficit 3-hydroxyacyl-CoA dehydrogenázy mastných kyselin s dlouhým řetězcem; VLCADD = deficit acyl-CoA dehydrogenázy mastných kyselin s velmi dlouhým řetězcem; CPTD I a II = deficit karnitinpalmitoyltransferázy I a II; CACTD = deficit karnitinacylkarnitintranslokázy; MSUD = leucinóza (nemoc javorového sirupu); GA I = glutarová acidurie typ I; IVA = izovalerová acidurie; Phe = fenylalanin, Tyr = tyrosin; TSH = tyreotropin; 17OHP = 17-hydroxyprogesteron; IRT = imunoreaktivní trypsinogen; CFTR = gen pro cystickou fibrózu; Val = valin; Leu = leucin; Ileu = isoleucin Systém NS nespočívá pouze v laboratorní analýze, ale musí zajišťovat i bezchybnou logistiku preanalytické části (informovaný souhlas rodičů; způsob, podmínky, časování a event. opakování odběrů suché kapky krve), navazující analytické části (jaké analyty, jakým způsobem a kde jsou měřeny, nastavení hranice mezi negativitou a pozitivitou – „cut-off“) a konečně postanalytické části (postupy screeningových laboratoří při pozitivním či nejasném nálezu, návaznost na klinická pracoviště ověřující podezření na nemoc podle obecně přijatých definic a konečně i zabezpečení dlouhodobé léčby a sledování pacientů). Celý program se periodicky hodnotí, průběžně se zpracovávají data ze screeningu a nastavují či upravují se pravidla. Sběr dat a hodnocení programu zajišťuje Koordinační centrum pro novorozenecký screening ve Všeobecné fakultní nemocnici v Praze (KCNS) ustanovené Ministerstvem zdravotnictví ČR, které sdružuje všechny laboratoře provádějící NS a zástupce MZ ČR. Způsob provádění NS v ČR je podrobně definován „Metodickým návodem k zajištění celoplošného novorozeneckého laboratorního screeningu a následné péče“, který se v několikaletých intervalech aktualizuje podle dosaženého stupně medicínského poznání, rozvoje NS a celospolečenských podmínek. Metodický návod se publikuje ve Věstníku Ministerstva zdravotnictví ČR. Poslední aktualizace byla zveřejněna v srpnu 2009 [15]. Přesné znění Metodického návodu a řadu dalších informací, sdělení a odpovědí KCNS pro odbornou i laickou veřejnost lze nalézt na webových stránkách http://www.novorozeneckyscreening.cz.
Smyslem tohoto sdělení je vyhodnotit výsledky NS v ČR ve vztahu k jeho postupnému rozšiřování.
SOUBOR, METODIKA
Sledované období 11 let mezi 1. 1. 2002 až 31. 12. 2012 zahrnuje všechny fáze postupného rozšiřování NS, tak, aby bylo možno porovnat kumulativní četnost zachycených pacientů (tzv. „detection rate“) v jednotlivých fázích rozšiřování. Celkem bylo vyšetřeno 1 179 136 novorozenců na hyperfenylalaninemii (PKU//HPA) a CH; koncentrace fenylalaninu byla měřena původní „Guthrieho“ bakteriálně inhibiční metodou, později enzymoimunoesejí (Quantase®, firmy Biorad) či chromatograficky; od X/2009 se vyšetřuje jednotně tandemovou hmotnostní spektrometrií (kity MassChrom® Reagent firmy Chromsystems; MS/MS přístroje API 2000TM, API 3200TM a API 4000TM firmy AB Sciex); koncentrace tyreotropinu byla stanovena pomocí fluoroimunoeseje (FIA; Delfia® a AutoDelfia® firmy Perkin--Elmer). U 752 922 novorozenců byla změřena koncentrace 17-hydroxyprogesteronu v SKK pomocí FIA. U 367 114 dětí byl změřen imunoreaktivní trypsin (IRT) pomocí FIA a u 3859 (1,05 %) z nich s nejvyšším IRT byla provedena analýza CFTR genu (bylo vyšetřováno 32, později 50 nejčastějších mutací pomocí esejí Elucigene CF-EU1TM/Elucigene CF-EU2TM firmy Gen-Probe) v originálních SKK, ve kterých byla zjištěna vysoká koncentrace IRT. Analýza CFTR genu ve druhém stupni NS CF má jediný cíl a výstup – minimalizaci falešně pozitivních výsledků. U 362 653 novorozenců byly analyzovány metabolity pro záchyt dalších 9 dědičných metabolických poruch pomocí výše uvedené MS/MS techniky.
V případě zjištění hodnoty analytu pod „cut-off“ hodnotou byl výsledek NS považován za negativní a proband nebyl dále vyšetřován. Při pozitivní hodnotě analytu byl proband předán ke konfirmaci diagnózy, léčbě a dalšímu sledování příslušnému klinickému pracovišti. Při nejasném výsledku v tzv. „šedé zóně“, kdy hodnota analytu byla mezi „cut-off“ a jasnou pozitivitou, byl odběr SKK na filtračním papíře opakován. Počet opakovaných odběrů SKK s konečným negativním výsledkem v opakovaném odběru, tj. s poklesem hodnoty analytu pod „cut-off“ se vyjadřuje v procentech jako četnost falešné pozitivity („false positivity rate“ – FPR). Zdrojem dat o počtu detekovaných i nedetekovaných pacientů byla hlášení klinických pracovišť screeningovým laboratořím. Diagnóza byla opřena o diagnostický standard platný v dané době. Uvedení konkrétních hodnot analytů pro „cut-off“ a pozitivitu, konfirmaci diagnóz podle domluvených definic a i uvedení léčby a follow-up přesahuje rozsah a smysl tohoto sdělení, zájemce odkazujeme na sekci „Pro odbornou veřejnost“ webových stránek http://www.novorozeneckyscreening.cz.
VÝSLEDKY A DISKUSE
Výsledky NS v ČR v průběhu postupného rozšiřování spektra vyhledávaných onemocnění ve sledovaném období ukazuje tabulka 3.
Tab. 3. Výsledky novorozeneckého screeningu v ČR v období 1. 1. 2002 – 31. 12. 2012. 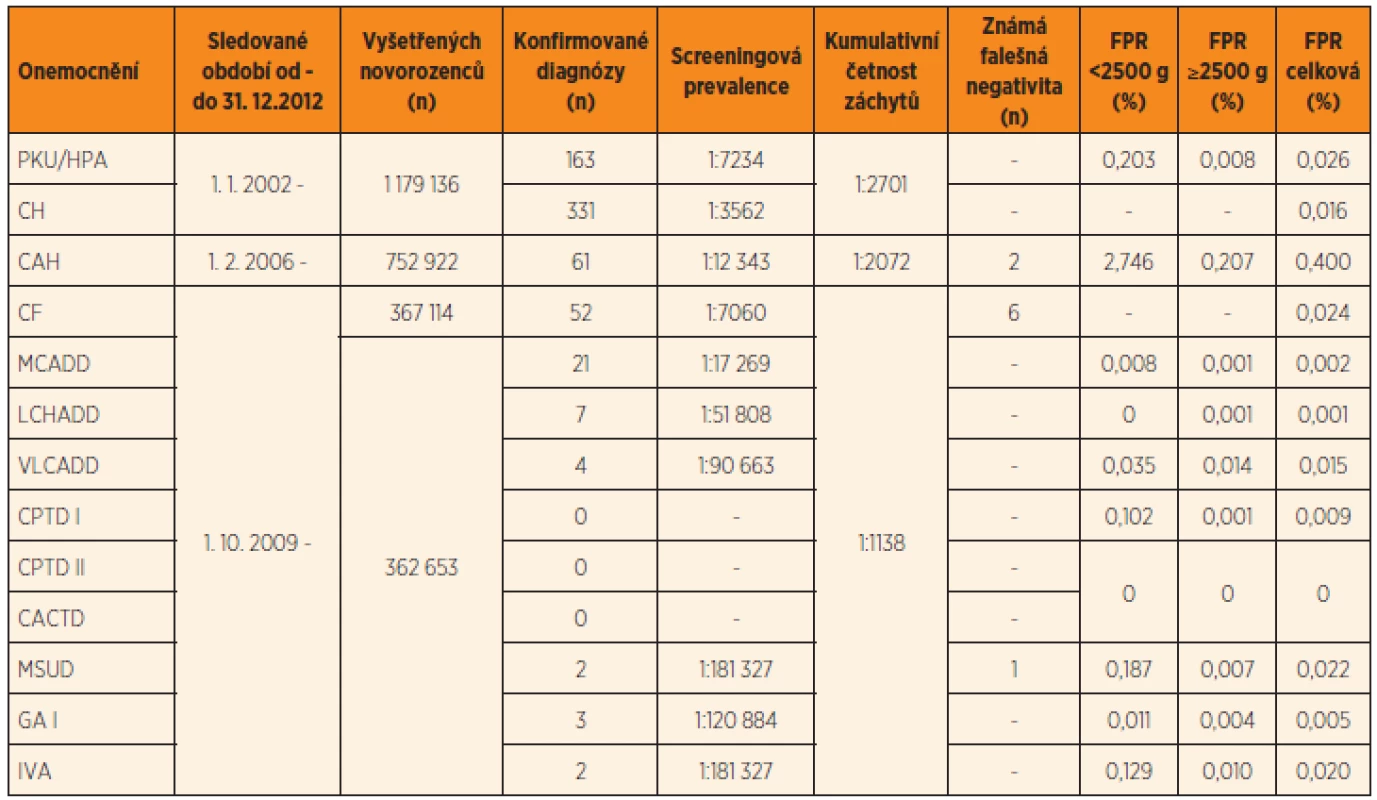
Vysvětlivky: PKU/HPA = fenylketonurie nebo hyperfenylalaninemie; CH = kongenitální hypotyreóza; CAH = kongenitální adrenální hyperplazie resp. deficit 21-hydroxylázy; CF = cystická fibróza; MCADD = deficit acyl-CoA dehydrogenázy mastných kyselin se středně dlouhým řetězcem; LCHADD = deficit 3-hydroxyacyl-CoA dehydrogenázy mastných kyselin s dlouhým řetězcem; VLCADD = deficit acyl-CoA dehydrogenázy mastných kyselin s velmi dlouhým řetězcem; CPTD I a II = deficit karnitinpalmitoyltransferázy I a II; CACTD = deficit karnitinacylkarnitintranslokázy; MSUD = leucinóza (nemoc javorového sirupu); GA I = glutarová acidurie typ I; IVA = izovalerová acidurie; FPR = „false positivity rate“, četnost opakování odběru screeningu s konečným negativním výsledkem pro předchozí nejasný nález v prvním pravidelném odběru mezi 48. a 72. hodinou života, počítáno v období 1. 1. 2010 – 31. 12. 2012 Zlepšující se schopnost celého systému NS v ČR detekovat pacienty s vrozeným či dědičným vzácným onemocněním dokládá kumulativní četnost záchytů, která narůstala z 1 : 2701 v letech 2002–2005 přes 1 : 2072 v letech 2007–2008 po rozšíření o CAH až na 1 : 1138 po posledním rozšíření NS v roce 2009 o CF a dalších 9 DMP. Efektivita screeningového programu se tak mezi lety 2005 a 2012 zvýšila více než 2,5krát a dosahuje parametrů srovnatelných s jinými evropskými zeměmi.
Odvrácenou stranou dosažené vysoké detekční schopnosti systému s větším počtem vyhledávaných nemocí je však nárůst počtu opakování odběru SKK na filtrační papírek pro nejasný první výsledek. U většiny novorozenců se při opakovaném odběru zjistí fyziologické koncentrace analytů a původní abnormální nález se tak stává falešně pozitivním. Kumulativní hodnota FPR v období mezi 1. 1. 2010 až 31. 12. 2012 dosáhla 0,540 % pro všechny vyšetřené novorozence bez rozdílu porodní hmotnosti. Ve skupině novorozenců s porodní hmotností 2500 g a více činila 0,253 % a u novorozenců s nízkou porodní hmotností 3,421 %. Falešná pozitivita přináší jistou zátěž pro zdravou část populace a podle některých studií může zvyšovat stres u rodičů (viz článek Franková a kol. v tomto čísle, s. 87-94). FPR vzrůstá s klesající porodní hmotností (resp. zralostí). Je pravdou, že ve skupině nezralých novorozenců je zátěž a stigmatizace opakovaným odběrem SKK významně menší, protože se většinou jedná o děti na intenzivní péči, které jsou vyšetřovány i z jiných důvodů, ale snižování FPR je pro systém NS výzvou a cílem. Z tabulky 3 je zřejmě, že na falešné pozitivitě se z největší části (74 %) podílí NS CAH. Ostatní screenovaná onemocnění mají FPR významně nižší (např. všech 10 DMP jen okolo 0,1 %). Efektivní cestou ke snižování FPR je zavádění druhostupňových analytických metod, které se provádějí přímo v těch originálních SKK, ve kterých byl zjištěn zvýšený primární analyt. V případě CAH byl zkoušen průkaz alespoň jedné funkční kopie genu CYP21A2 pro 21-hydroxylázu. Tento přístup se nejeví použitelný pro běžnou praxi z důvodu velké pracnosti a finančních nákladů [16]. Slibné je profilování steroidů pomocí kapalinové chromatografie s následnou analýzou pomocí tandemové hmotnostní spektrometrie (LC--MS/MS), pilotní studie probíhají ve světě [17] i v ČR, zavedení této metody jako druhostupňové metody by mohlo podle pilotní studie v ČR snížit FPR pro CAH o cca 80–90 %.
V každém screeningovém programu existují také případy falešné negativity (FN), kdy pa-cienti (většinou s mírnějšími formami nemoci) nejsou screeningem zachyceni. Při NS CAH byly v průběhu sledovaného období zaznamenány dva případy, které unikly detekci NS. V jednom případě se jednalo o probanda s klinickým podezřením na CAH a léčeného kortikoidy již před odběrem SKK, tento případ tedy není faktickou FN, ale ve druhém případě se jednalo o skutečnou „biologickou“ FN u dívky s genotypem svědčícím pro solnou poruchu. Kauza byla podrobně analyzována a publikována [8]. Skutečná novorozenecká prevalence CAH po započítání FN činila 1 : 11 951. Detekci NS unikl i jeden pacient s MSUD, protože při konfirmačním vyšetření standardními technikami nebyly zjištěny zvýšené koncentrace diagnosticky významného analytu – alloisoleucinu, reálná novorozenecká prevalence pak vzroste na 1 : 120 884. Během NS CF bylo ve sledovaném období zaznamenáno 6 dětí, které unikly záchytu. Ve 3 případech se jednalo o pacienty, kteří se v novorozeneckém věku demonstrovali mekoniovým ileem (MI). Nejednalo se tedy o faktický únik diagnóze a nižší koncentrace IRT v případě MI jsou známé [18]. V dalším jednom případě se jednalo o skutečnou „biologickou“ FN s IRT pod „cut-off“ a u dvou novorozenců se jednalo o „analytickou“ FN, protože probandi měli dvě vzácné mutace, které nejsou ve spektru vyšetřovaných. Skutečná prevalence CF v naší kohortě novorozenců po započítání FN činila 1 : 6330. Populační riziko CF po započítání preimplantační a prenatální diagnostiky je však vyšší – cca 1 : 4500. NS CF lze významně zefektivnit pomocí dalšího analytického mezistupně – měření proteinu asociovaného s pankreatitidou [19].
Ze sledovaného období nemáme informaci o FN PKU/HPA. Screeningová prevalence PKU/HPA v období 1. 1. 2010 – 31. 12. 2012 byla vyšší (1 : 5867) než za celé sledované období (1 : 7234). Důvodem může být jednak fluktuace v důsledku relativně malého počtu vyšetřených novorozenců, ale také snížení hranice „cut-off“ pro fenylalanin z 240 na 120 µmol/l a zvýšenému záchytu lehčích forem HPA.
Sekundární non-PKU hyperfenylalaninemie způsobené poruchami metabolismu pterinů nejsou zahrnuty – v celém sledovaném období byl detekován 1 pacient s deficitem tetrahydrobiopterinu.
S technologickým pokrokem se rozšiřují analytické možnosti detekce stále většího počtu onemocnění ze SKK. Rozhodování, která onemocnění zahrnout do novorozeneckého screeningového programu, se stává stále složitější. V historických počátcích NS Wilson a Jungner stanovili rozhodovací kritéria o zařazování onemocnění do NS [20, 21]. Tato kritéria nebyla zpochybněna, ale jsou relativizována, např. hranice prevalence nebo ekonomická hranice (v ČR jsou náklady zdravotní pojišťovny na současný NS u jednoho novorozence 750 Kč). V diskusích se objevují i nová kritéria, jako např. ušetření jedince diagnostickému martyriu u vzácných chorob nebo informovaná reprodukce s možností prenatálního vyšetření či preimplantační diagnostiky u neléčitelných chorob.
S rozšiřováním NS se rozšiřují problémy nejen odborné, ale i etické, ekonomické a politické. Autoritativní stanovisko zaujala Americká společnost lékařské genetiky (ACMG), která po rozsáhlé studii a diskusi publikovala [22] seznam 55 chorob vhodných pro NS, které rozdělila na skupinu základní a na skupinu doplňkovou. Seznam, v USA chápán jako závazný, je uveden v tabulce 4 a postupně se v jednotlivých státech zavádí. Evropská síť odborníků v novorozeneckém screeningu (EUNENBS, European Network of Experts on Newborn Screening) provedla v letech 2010/2011 dotazníkovou studii a vydala [23] podobný seznam 26 onemocnění, které považuje za vhodné k zařazení do spektra NS v evropských státech. Seznam rozdělila na skupinu základní (potřebnou) s vysokou prevalencí, základní s nízkou prevalencí a skupinu kandidátní – viz tabulku 5.
Tab. 4. Onemocnění doporučená k vyhledávání pomocí novorozeneckého screeningu v USA, podle [22]. ![Onemocnění doporučená k vyhledávání pomocí novorozeneckého screeningu v USA, podle [22].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/59bb71f588ceb3f6181a6e56cc6663d0.png)
Vysvětlivky: IVA = izovalerová acidurie; GA I = glutarová acidurie I. typu; HMG = deficit lyázy 3-hydroxy 3-methylglutaryl-CoA; MCD = mnohočetný deficit karboxyláz; MUT = deficit metylmalonyl-CoA mutázy; Cb1 A ,B = metylmalonová acidémie forma Cb1A a B; 3MCC = deficit karboxylázy 3-methylcrotonyl-CoA; PROP = propionová acidurie; BKT = deficit β-ketothiolázy; MCADD = deficit acyl-CoA dehydrogenázy mastných kyselin se středně dlouhým řetězcem; VLCADD = deficit acyl-CoA dehydrogenázy mastných kyselin s velmi dlouhým řetězcem; LCAHDD = deficit acyl-CoA dehydrogenázy mastných kyselin s dlouhým řetězcem; TFP = deficit trifunkčního mitochondriálního proteinu; CUD = defekt vychytávání karnitinu; PKU = fenylketonurie; MSUD = leucinóza (nemoc javorového sirupu); HCY = homocystinurie; TYR I = tyrosinémie I. typu; ASA = arginisukcinátová acidurie; CIT = citrulinemie I. typu; SCA = srpkovitá anemie; Hb S/Th = S-β thalasémie; Hb S/C = kombinovaná hemoglobinopatie S a C; CH = kongenitální hypotyreóza; BD = deficit biotinidázy; CAH = kongenitální adrenální hyperplazie resp. deficit 21-hydroxylázy; GAL = galaktosémie; HEAR = poruchy sluchu; CF = cystická fibróza; SCID = syndrom těžké kombinované imunodeficience (přidán do panelu až v roce 2010); Cb1 C, D = metylmalonová acidemie forma Cb1 C a D; 2M3HBA = 2-metyl-3hydroxybutyrátová acidurie; IBG = deficit dehydrogenázy izobutyryl-CoA; 2MBG = deficit dehydrogenázy 2-metylbutyryl-CoA; 3MGA = 3-metylglutakonová acidurie; MAL = malonová acidemie; M/SCHADD = deficit dehydrogenázy hydroxyacyl- CoA mastných kyselin se středně dlouhým a krátkým řetězcem; SCADD = deficit acyl-CoA dehydrogenázy mastných kyselin s krátkým řetězcem; MCKATD = deficit thiolázy 3-ketoacyl-CoA mastných kyselin se středně dlouhým řetězcem; GA II = glutarová acidurie II. typu; CPTD I = deficit karnitin palmitoyltransferázy I; CPTD II = deficit karnitin palmitoyltransferázy II; CACTD = deficit karnitinacylkarnitintranslokázy; DE REDUCT = deficit reduktázy dienoyl-CoA; HPA = non PKU hyperfenylalaninemie; TYR II = tyrosinémie II. typu; BIOPT (BS) = defekt syntézy biopterinu; TYR III = tyrosinémie III. typu; ARG = argininémie; BIOPT (REG) = defekt regenerace biopterinu; MET = hypermethioninemie; CIT II = citrulinemie II. typu; GALE = deficit epimerázy galaktózy; GALK = deficit galaktokinázy Tab. 5. Onemocnění doporučená k vyhledávání pomocí novorozeneckého screeningu v Evropě, podle [23]. ![Onemocnění doporučená k vyhledávání pomocí novorozeneckého screeningu v Evropě, podle [23].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/0af4088cc073b0eebf613bd2036d5c32.png)
Vysvětlivky: PKU = fenylketonurie resp.hyperfenylalaninemie; CH = kongenitální hypotyreóza; CAH = kongenitální adrenální hyperplazie resp. deficit 21-hydroxylázy; CF = cystická fibróza; MCADD = deficit acyl-CoA dehydrogenázy mastných kyselin se středně dlouhým řetězcem; Hb S/Th = S-β thalasémie; Hb S/C = kombinovaná hemoglobinopatie S a C; MSUD = leucinóza (nemoc javorového sirupu); GA I = glutarová acidurie I. typu; GAL = galaktosémie; BD = deficit biotinidázy; CPTD II = deficit karnitin palmitoyltransferázy II; CACTD = deficit karnitinacylkarnitintranslokázy; GA II = glutarová acidurie II. typu; HMGD = deficit lyázy 3-hydroxy-3-methylglutaryl-CoA; HCSD = deficit syntetázy holokarboxylázy; HCY = homocystinurie; IVA = izovalerová acidurie; BKT = deficit β-ketothiolázy; LCAHDD = deficit acyl-CoA dehydrogenázy mastných kyselin s dlouhým řetězcem; LSD = lyzozomální střádavé choroby (několik jednotek, např. Pompe, Krabbe, Fabry); 3MCC = deficit karboxylázy 3-methylcrotonyl-CoA; TYR I = tyrosinémie I. typu; TYR II a III = tyrosinémie II. a III. typu; VLCADD = deficit acyl-CoA dehydrogenázy mastných kyselin s velmi dlouhým řetězcem; SCID = syndrom těžké kombinované imunodeficience; CMV = vrozená infekce virem CMV Evropský panel je v současnosti vnímán méně závazně než americký a má charakter spíše „doporučení ke zvážení“. V ČR v současné době probíhá pilotní studie k rozšíření spektra dědičných metabolických poruch pomocí MS/MS a metodicky se připravuje studie NS těžké kombinované imunodeficience (SCID) [24].
ZÁVĚR
Rozšíření novorozeneckého screeningového programu v ČR zásadním způsobem zvýšilo efektivitu presymptomatického vyhledávání pacientů, neboť téměř dvaapůlkrát zvýšilo záchyt novorozenců s některou z vyhledávaných nemocí. Úroveň novorozeneckého screeningu v ČR odpovídá nyní standardu vyspělých států Evropské unie. NS v ČR je účinným nástrojem zkvalitnění péče o pacienty se vzácnými onemocněními a je vzorovým příkladem zlepšení přístupu zdravotnického systému k těmto pacientům. Další optimalizace systému NS jsou potřebné a jsou předmětem výzkumu – v současné době jsou vyvíjené druhostupňové metody s cílem snížit falešnou pozitivitu a hledají se možnosti k rozšíření spektra screenovaných chorob.
Práce vznikla za podpory: PRVOUK P31 pro FV1 a P24 pro VK2; IGA MZ ČR NT/12213-3 a MZ ČR RVO-VFN64165/2012 pro VK2; MZOFNM2005, CZ.2.16/3.1.00/24022 a 00064203 pro MM5.
Došlo: 8. 1. 2014
Přijato: 14. 2. 2014
doc. MUDr. Felix Votava, Ph.D.
Klinika dětí a dorostu UK 3. lékařské fakulty
a FN Královské Vinohrady
Šrobárova 50
100 34 Praha 10
e-mail: votava@fnkv.cz
Zdroje
1. Guthrie R, Susi A. A simple phenylalanine method for detecting phenylketonuria in large populations of newborn infants. Pediatrics 1963; 32 : 338–343.
2. Loeber JG, Burgard P, Cornel MC, et al. Newborn screening programmes in Europe; arguments and efforts regarding harmonization. Part 1 – From blood spot to screening result. J Inherit Metab Dis 2012; 35 (4): 603–611.
3. Webové stránky NNSGRC (National Newborn Screeenig and Genetics Resource Center), http://genes-r-us.uthscsa.edu/sites/genes-r-us/files/.
4. Abstracts of the 6th European Regional Meeting in Neonatal Screening. Čes-slov Pediat 2009; 4 : 159–220.
5. Hyánek J, Hoza J, Vinsová N, et al. Výsledky hromadného screeningu vrozených metabolických poruch u novorozenců. Čs Gynek 1972; 4 : 208–209.
6. Blehová B, Pažoutová M, Bloudková D, et al. Zhodnocení screeningu fenylketonurie za šest let trvání laboratoře. Čes-slov Pediat 1976; 7 : 399–400.
7. Hníková O, Kračmar P, Zelenka Z, et al. Screening of congenital hypothyroidism in newborns in Bohemia and Moravia. Endocrinologia Experimentalis 1989; 2 : 117–123.
8. Votava F, Novotna D, Kracmar P, et al. Lessons learned from 5 years of newborn screening for congenital adrenal hyperplasia in the Czech Republic: 17-hydroxyprogesterone, genotypes, and screening performance. Eur J Pediatr 2012; 171 (6): 935–940.
9. Balascakova M, Holubova A, Skalicka V, et al. Pilot newborn screening project for cystic fibrosis in the Czech Republic: defining role of the delay in its symptomatic diagnosis and influence of ultrasound-based prenatal diagnosis on the incidence of the disease. J Cyst Fibros 2009; 8 (3): 224–227.
10. Chrastina P, Šťastná S, Myšková H, et al. Tandemová hmotnostní spektrometrie – budoucnost novorozeneckého screeningu dědičných metabolických poruch. Čes-slov Pediat 2003; 7 : 464–467.
11. Chrastina P, Kostalova E, Paulova H, et al. Experience with screening by tandem mass spectrometry in the Czech Republic. The 5th European ISNS Congresss in Newborn Screening, June 10–12th 2007, Reykjavík, Island, Abstracts book, p.41.
12. Chrastina P, Bártl J, Horník P, et al. LCHAD deficiency – the most frequent fatty acid oxidation disorder in newborn screening in the Czech Republic. Čes-slov Pediat 2009; 4 : 175–176.
13. Doporučení Rady Evropské unie o akci v oblasti vzácných onemocnění ze dne 8.6.2009. http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=OJ:C:2009 : 151 : 0007 : 0010:CS:PDF.
14. Usnesení Vlády ČR č. 466 ze dne 14. 6. 2010 o Národní strategii pro vzácná onemocnění na léta 2010–2020. http://www.vlada.cz/.
15. Metodický návod k zajištění celoplošného novorozeneckého laboratorního screeningu a následné péče. Věstník Ministerstva zdravotnictví ČR 2009; 6 : 7–14.
16. Malikova J, Votava F, Vrzalova Z, et al. Genetic analysis of the CYP21A2 gene in neonatal dried blood spots from children with transiently elevated 17-hydroxyprogesterone. Clin Endocrinol 2012; 77 (2): 187–194.
17. Dhillon K, Ho T, Rich P, et al. An automated method on analysis of blood steroids using liquid chromatography tandem mass spectrometry: application to population screening for congenital adrenal hyperplasia in newborns. Clin Chim Acta 2011; 412 (23–24): 2076–2084.
18. Calvin J, Hogg SL, McShane D, et al. Thirty-years of screening for cystic fibrosis in East Anglia. Arch Dis Child 2012; 97 (12): 1043–1047.
19. Krulisova V, Balascakova M, Skalicka V, et al. Prospective and parallel assessments of cystic fibrosis newborn screening protocols in the Czech Republic: IRT/DNA/IRT versus IRT/PAP and IRT/PAP/DNA. Eur J Pediatr 2012; 1 (8): 1223–1229.
20. Wilson JMG, Jungner G. Principles and practice of screening for dinase. World Health Organisation. Public Health Papers 1968; 34 : 11.
21. Votava F, Strnadová KA. Novorozenecký screening v České republice a v Evropě. Čes-slov Pediat 2008; 63 (2): 96–105.
22. American College of Medical Genetics Newborn Screening Expert Group.Newborn screening: toward a uniform screening panel and systém – executive sum-mary. Pediatrics 2006; 117 (5 Pt 2): S296–S307.
23. Burgard P, Rupp K, Linder M, et al. Newborn screening programmes in Europe; arguments and efforts regarding harmonization. Part 2 – From screening laboratoř results to treatment, follow-up and quality assurance. J Inherit Metab Dis 2012; 35 (4): 613–625.
24. Svaton M, Sediva A, Mejstrikova E, et al. Differential diagnostics of immunodeficiency using antigen receptor excision circles in neonatal screening cards and in postnatal peripheral blood. The 8th European Regional Meeting of International Society of Neonatal Screening, Hungary, Budapest. Orvosi Hetilap 2012; 42.
Štítky
Neonatológia Pediatria Praktické lekárstvo pre deti a dorast
Článek MikropenisČlánek Antonín Mrskoš
Článok vyšiel v časopiseČesko-slovenská pediatrie
Najčítanejšie tento týždeň
2014 Číslo 2- Léčba bolesti a horečky u dětí
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Gastroezofageální reflux a gastroezofageální refluxní onemocnění u kojenců a batolat
- Očkování nejvíc potřebuje ten, kdo sám být očkován nemůže − kazuistika
- Pokrok v boji s malárií − první vakcína poskytující přijatelnou ochranu proti nemoci
-
Všetky články tohto čísla
- Antropometrické, hormonálne a metabolické zmeny u prepubertálnych detí, narodených ako SGA, so zníženým rastom, liečených rastovým hormónom, po prvom roku liečby
- Osteogenesis imperfecta asociovaná s izolovaným deficitom rastového hormónu
- Polohové anomálie varlat a kryptorchismus v prvním roce života
- Mikropenis
- 11. Český pediatrický kongres s mezinárodní účastí
- „EVIDENCE BASED PHARMACOTHERAPY IN NEWBORNS AND CHILDREN“
- Odešel prof. Dr. med. Dr. med. h. c. mult. Theodor Hellbrügge
- Antonín Mrskoš
- Vzťah medzi obezitou a závažnosťou hypertenzie u detí a adolescentov
- Výsledky rozšířeného novorozeneckého screeningu v České republice
- Etické aspekty rozšiřování novorozeneckého screeningu dědičných metabolických poruch
- Chirurgická liečba hydrocefalu a jej komplikácie
- Česko-slovenská pediatrie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Mikropenis
- Chirurgická liečba hydrocefalu a jej komplikácie
- Polohové anomálie varlat a kryptorchismus v prvním roce života
- Výsledky rozšířeného novorozeneckého screeningu v České republice
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



