-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Hyperkapnické respirační selhání
Hypercapnic respiratory failure – review
This review summarizes the issue of acute hypercapnic respiratory failure. Acute respiratory failure is a condition in which the respiratory system is unable to fulfill its basic function, i.e. enriching the blood with oxygen and excreting carbon dioxide. Chronologically, we divide it into acute and chronic, and according to the manifestation into hypoxemic or hypoxemic with hypercapnia. Multiple factors, such as reduced ventilation and increased dead space, contribute to the development of hypoxemic-hypercapnic (global) respiratory failure. Both the patient's clinical presentation and laboratory examination of blood gases and acid-base balance (preferably from arterial blood) are used for diagnosis. In the absence of contraindications, non-invasive ventilation is used to establish normocapnia.
Keywords:
Respiratory failure – hypercapnia – noninvasive ventilation
Autori: Martin Vykopal 1; Jan Mizera 1; Petr Jakubec 1; Samuel Genzor 1,2; Pavol Pobeha 3
Pôsobisko autorov: Klinika plicních nemocí a tuberkulózy LF UP a FN Olomouc 1; Centrum digitálního zdravotnictví LF UP a FN Olomouc 2; Klinika pneumológie a ftizeológie LF UPJŠ a UNLP Košice 3
Vyšlo v časopise: Čas. Lék. čes. 2023; 162: 13-18
Kategória: Přehledový článek
Súhrn
Tento přehledový článek shrnuje problematiku akutního hyperkapnického respiračního selhání. Akutní respirační selhání je stav, kdy respirační ústrojí není schopno plnit svoji základní funkci, tedy obohacování krve kyslíkem a vylučování oxidu uhličitého. Respirační selhání dělíme podle trvání na akutní a chronické, podle manifestace na hypoxemické nebo hypoxemické s hyperkapnií. Při vzniku hypoxemicko-hyperkapnického (globálního) respiračního selhání se uplatňují vícečetné faktory, například snížení ventilace a navýšení mrtvého prostoru různé etiologie. K diagnostice se využívá klinický obraz pacienta, ale definitivním potvrzením diagnózy je laboratorní vyšetření krevních plynů a acidobazické rovnováhy (nejlépe z arteriální krve). K nastolení normokapnie je v nepřítomnosti kontraindikací využívána neinvazivní ventilace.
Klíčová slova:
neinvazivní ventilace – respirační insuficience – hyperkapnie – respirační selhání
ÚVOD
Akutní hyperkapnické respirační selhání (AHRS) je definováno jako náhle vzniklá hypoxémie (parciální tlak kyslíku [PaO2] v arteriální krvi < 8 kPa) a hyperkapnie (parciální tlak oxidu uhličitého [PaCO2] > 6 kPa). Přesné časové hledisko, které by dělilo akutní selhání od chronického, stanoveno není (1). V praxi se často setkáváme se situací, kdy chronické respirační selhání navazuje na akutní (ať už dříve známé či do té doby nediagnostikované). Pak mluvíme o acute-on-chronic hyperkapnickém respiračním selhání.
Hyperkapnie vzniká na podkladě selhání ventilační pumpy, která vede retenci CO2 a současně i poklesu oxygenace (2). AHRS může vzniknout de novo z akutní příčiny – typicky například při akutním městnavém srdečním selhání či akutní exacerbaci chronické obstrukční plicní nemoci (CHOPN) (3). Překvapivě se méně často vyskytuje při syndromu akutní respirační tísně (ARDS – acute respiratory distress syndrome), kde je ovšem respirační selhání spojeno s vyšší celkovou mortalitou pacientů (2). Menší výskyt u ARDS je důsledkem dominance postižení plicního parenchymu. Předávkování látkami suprimujícími dechové centrum a náhlá progrese neuromuskulárních onemocnění tvoří příčiny spíše raritní (4).
Odlišení akutního respiračního selhání od chronického není vždy snadné. Pokud je známo závažné preexistující onemocnění (obvykle neuromuskulární anebo respirační), nabízí se možnost jeho dekompenzace. Jako AHRS se může manifestovat již preexistující chronické hyperkapnické respirační selhání (latentní) při selhání jeho kompenzace (5). Z laboratorních markerů se lze orientačně řídit koncentrací bikarbonátů, která je v prvních hodinách AHRS obvykle v normálním rozmezí anebo pouze lehce zvýšená. Její elevace je projevem metabolické kompenzace respiračního selhání ve snaze o udržení pH krve ve fyziologickém rozmezí (6). Stanovení přesné příčiny AHRS může být problematické, velmi důležité jsou precizní diagnostika a sledování pacientů v období rekonvalescence (7).
Prognóza je velmi často závažná, u neselektovaných pacientů po AHRS činí mortalita v prvním roce až 32 % (1). U nemocných s chronickým respiračním selháním je důležité zahájení domácí neinvazivní ventilační podpory, která snižuje mortalitu i počet hospitalizací a zlepšuje kvalitu života (8).
Tento přehled shrnuje aktuální poznatky o AHRS se zaměřením na jeho etiologii a léčbu.
DEFINICE POJMŮ
Respirační insuficience znamená selhávání hlavních funkcí dýchací soustavy, kterými jsou dodávka kyslíku do tepenné krve a eliminace CO2 z krve žilní. Základní funkce dýchací soustavy můžeme rozdělit na respiraci (výměnu plynů na úrovni alveolokapilární membrány) a ventilaci (dechovou pumpu) zajišťující výměnu plynů mezi zevním prostředím a alveoly (9). K adekvátní funkci ventilační pumpy a respirace je nutný fyziologický stav alveolokapilární membrány, dostatečný alveolární objem a správné fungování neuromuskulární složky.
Z časového hlediska lze respirační insuficienci rozdělit na akutní v případě náhlého vzniku (například aspirace cizího tělesa), chronickou, kdy bývají již rozvinuty kompenzační mechanismy (např. pomalá postupná progrese CHOPN), a chronickou s akutním zhoršením (např. akutní exacerbace CHOPN či astmatu). O latentní respirační insuficienci hovoříme po jejím demaskování zátěží či spánkem (9).
Podle naměřených hodnot krevních plynů dělíme respirační nedostatečnost na hypoxemickou (I. typu) a hyperkapnickou (II. typu) (9). Při hypoxemickém selhání dochází k poklesu arteriálního PaO2 pod jeho fyziologickou hranici, tehdy hovoříme o hypoxémii (PaO2 < 8,0 kPa). Jedná se o selhání oxygenace na úrovni alveolokapilární membrány, etiologicky způsobenou poruchou difúze plynů, ventilačně perfuzním nepoměrem, zkratovou cirkulací či alveolární hypoventilací.
Při hyperkapnickém selhání dochází k nárůstu PaCO2 v krvi nad fyziologickou hranici, hovoříme o hyperkapnii (PaCO2 > 6 kPa). V tomto případě se jedná o selhání na úrovni ventilace (pump failure) (9), kdy je prakticky vždy přítomna i hypoxémie pro současné selhávání oxygenace.
Vznik hyperkapnického respiračního selhání je důsledkem nerovnováhy mezi produkcí a eliminací CO2. Hyperkapnie je přímo úměrná produkci CO2 v organismu (v důsledku látkové přeměny) a nepřímo úměrná alveolární ventilaci.
Na mechanismech vzniku hyperkapnického respiračního selhání se podílí snížení minutové ventilace (útlum dechového centra, poruchy neuromuskulárního přenosu, postižení svalové funkce, deformity hrudního koše, fluidothorax, plicní edém, aspirace cizího tělesa), zvýšení mrtvého prostoru (hyperinflace – emfyzematické změny plicního parenchymu, závažná pulmonální embolizace), zvýšení produkce CO2 (febrilní stavy, katabolismus) a ostatní (OSAS, intoxikace) (9). Přehled základních příčin hyperkapnického respiračního selhání uvádí tab. 1.
Tab. 1. Základní příčiny akutního hyperkapnického respiračního selhání 
Pozn.: OSAS – syndrom obstrukční spánkové apnoe Dekompenzovaná hyperkapnie vede k poruchám acidobazické rovnováhy ve směru acidifikace. Při akutně vzniklé hyperkapnii dochází k respirační acidóze. V případě chronického hyperkapnického selhávání dochází k rozvoji kompenzačních mechanismů (retence bikarbonátů) a pH zůstává obvykle ve fyziologickém rozmezí, pokud nedojde k překročení kritické meze (10).
S akutním hyperkapnickým respiračním selháním se lze setkat jak na urgentních příjmech, standardních odděleních, jednotkách intenzivní péče, tak i na odděleních postoperačních. Hyperkapnie se vyskytuje při přijetí či v průběhu hospitalizace přibližně u 20 % pacientů hospitalizovaných pro exacerbaci CHOPN (11). Nejčastěji se jedná o pacienty s CHOPN či hypoventilačními syndromy, jako je syndrom obezity a hypoventilace (OHS) (12).
KLINICKÝ OBRAZ
Hyperkapnie se projevuje především spavostí, která může být vystřídána neklidem, dušností, třesem až křečemi a bolestmi hlavy. U těžší hyperkapnie vzniká nitrolební hypertenze. Vazodilatace navozená vysokým PaCO2 vyvolává syndrom modré masky (lesklé oči, nastříknuté spojivky, otok obličeje, cyanóza). Cyanóza centrálního typu bývá vyznačena hlavně u nemocných s polycytémií.
Veškeré příznaky se objevují v překryvu se symptomy základního onemocnění (při exacerbaci CHOPN např. kašlem, spastickým poslechovým nálezem; při srdečním selhání otoky, nepřízvučnými chrůpky). Při dalším vzestupu CO2 stav progreduje do hypotenze, bradykardie, soporu, kómatu až smrti (13).
DIAGNOSTIKA
V diagnostice se uplatňuje jak posouzení klinického stavu, tak laboratorní vyšetření. Základní vyšetřovací metodou pro klasifikaci a posouzení závažnosti respirační insuficience je stanovení parciálních tlaků arteriálních krevních plynů (PaO2, PaCO2) a acidobazické rovnováhy (pH) včetně vyjádření kompenzačních metabolických změn (BE – base excess a hydrogenuhličitany [HCO3–]). Base excess je hodnota vyjadřující takové množství kyseliny, které je nutno přidat do vyšetřované tekutiny, aby se její pH upravilo na hodnotu 7,4 (za předpokladu normokapnie a teploty 37 °C). Hydrogenuhličitany v séru pacienta představují jeden z hlavních pufrovacích systému krve, který tvoří součást acidobazické rovnováhy. Vyšetření se doporučuje provádět metodou odběru arteriální krve, z arterializované kapilární krve (obvykle z ušního lalůčku) je méně spolehlivé. Pro základní monitorování oxygenace má význam i sledování saturace hemoglobinu kyslíkem pomocí pulzního oxymetru (13).
CHOPN A HYPERKAPNIE
Chronická obstrukční plicní nemoc je komplexní a heterogenní onemocnění charakterizované zánětlivou reakcí na chronickou expozici vdechovaných toxických částic, která u vnímavých jedinců způsobuje poškození průdušek a plicní tkáně. Vykazuje vysokou heterogenitu z hlediska patologie, imunitní odpovědi, klinických příznaků a fenotypu. Vlivem zánětu dochází v průduškách k hypersekreci hlenu, hyperplazii pohárkových buněk a ztluštění stěn bronchů, v přilehlém parenchymu pak v různé míře k destrukci alveolárních sept se vznikem emfyzému (14).
Přítomnost alveolární hypoventilace, a tedy rozvoj následné hyperkapnie, je častější u těžkých forem CHOPN, ačkoli hyperkapnie je přítomna i u části pacientů se středně těžkým onemocněním (15, 16). Prevalence hyperkapnie u pacientů s velmi těžkou CHOPN činí 30–50 % (16). Hyperkapnie způsobuje strukturální i funkční dysfunkci alveolárního epitelu, což vede k tvorbě edému alveolokapilární membrány a dalšímu zhoršení výměny plynů (17).
Nezávislé prediktory hyperkapnie tvoří FEV1, emfyzematózní změny, již prodělané AHRS a případně současná potřeba oxygenoterapie (18).
Evropská respirační společnost (ERS) doporučuje použití neinvazivní ventilace (NIV) u pacientů s CHOPN a AHRS v případě rozvinuté acidózy (pH ≤ 7,35, PaCO2 > 45 mmHg) způsobené akutní exacerbací CHOPN (19).
Použití NIV při AHRS v rámci exacerbace CHOPN významně snižuje nutnost endotracheální intubace, je s ní spojen pokles mortality a zkrácení doby hospitalizace (20, 21). Úspěšnost terapie velmi závisí na závažnosti hyperkapnie a/nebo acidózy (22).
NIV v paliativní péči u pacientů s CHOPN v terminálním stadiu nejenže zmírňuje dušnost a snižuje počet hospitalizací, ale také zvyšuje pravděpodobnost dlouhodobého přežití (23).
OHS A HYPERKAPNIE
Syndrom obezity a hypoventilace je definován jako kombinace obezity při BMI (body mass index) > 30 kg/m2, denní hyperkapnie, poruch dechu ve spánku a nepřítomnosti ostatních (např. neurologických) příčin, které mohou vyvolat alveolární hypoventilaci. Prevalence je odhadována na 0,4 % dospělé populace. Podezření na OHS je obvykle při akutním hyperkapnickém respiračním selhání, a to buď na podkladě zhoršení chronické hyperkapnie nebo de novo při vyšetření na základě přítomnosti symptomů. K potvrzení diagnózy následuje vyšetření ve spánkové laboratoři s odběry krevních plynů (24).
Terapeuticky je metodou volby, krom režimových opatření a redukce váhy, neinvazivní ventilace. Jak režim CPAP (kontinuální pozitivní přetlak dýchacích cest), tak i BiPAP (dvouúrovňový pozitivní přetlak v dýchacích cestách) vede ke zlepšení výměny plynů, a tím k redukci symptomů a zlepšení kvality života. Režim CPAP je primárně indikován u pacientů s průkazem OHS a diagnózou obstrukční spánkové apnoe (OSAS). Při průkazu hypoventilace je indikováno použití režimu BiPAP (25).
Akutní hyperkapnické respirační selhání pacientů s OHS bylo úspěšně terapeuticky ovlivněno použitím NIV. Tito pacienti však často trpěli městnavým srdečním selháním (26). Při použití NIV měli lepší odpověď a prognózu než pacienti s AHRS jiné etiologie. Vyžadovali však nastavení vyšších hodnot tlaků a normalizace krevních plynů trvala delší dobu (24, 27).
AKUTNÍ RESPIRAČNÍ SELHÁNÍ NEUROMUSKULÁRNÍ ETIOLOGIE
Mnohá z neurologických onemocnění mohou vést k akutnímu respiračnímu selhání, ať už z důvodu postižení samotného bulbárního dechového centra, míchy, motoneuronů, periferních nervů, nervosvalových plotének či dýchacích svalů. Většina pacientů se primárně dostane do stadia AHRS z důvodu poruchy ventilace. V případě selhání ventilační pumpy vedoucí k AHRS je NIV terapeutickou metodou zásadního významu (28). V tomto případě nejsou dostupná data srovnávající invazivní a neinvazivní ventilaci.
SRDEČNÍ SELHÁNÍ
Při levostranném srdečním selhání dochází na podkladě porušené rovnováhy intravaskulární a intersticiální tekutiny k zvýšení kapilárního tlaku v malém oběhu. Hydrostatický tlak krve roste, a tím se i přes působení koloidně osmotických tlaků tekutina dostává z vaskulárního přes intersticiální prostor až do plicních alveolů. Tento proces vede ke vzniku plicního kardiogenního edému (29).
U pacientů s akutním kardiálním plicním edémem NIV snižuje i mortalitu, redukuje nutnost intubace a subjektivně zmírňuje pocity respirační tísně. U pacientů s již rozvinutým šokovým stavem je použití NIV doporučeno až po stabilizaci oběhu (30). Vhodným režimem volby je CPAP (primárně nebyl pozorován rozdíl ve ventilačních režimech, tím spíše je doporučován CPAP pro větší dostupnost a toleranci). V případě již rozvinuté hyperkapnie, a tím spíše u pacientů s CHOPN, je doporučován režim BiPAP (31). Použití vysokoprůtokové nazální oxygenoterapie je vhodnou alternativou při nemožnosti použití NIV (30).
POLÉKOVÉ POSTIŽENÍ
Z léků přímo negativně ovlivňují dechové centrum v prodloužené míše zejména opiáty, benzodiazepiny a barbituráty. Dechové centrum dále tlumí i řada psychofarmak, bezpečný se jeví v tomto ohledu haloperidol. Při abúzu či předávkování dochází k poklesu dechových objemů, snížení ventilačního úsilí a dechové frekvence, což vede v závažnějších případech až ke globálnímu respiračnímu selhání. U náchylných osob (např. pacienti s těžší CHOPN, výraznou obezitou, onemocněním motorického neuronu) může být již prosté podání vyšších průtoků oxygenoterapie rizikovým faktorem pro vznik a progresi hyperkapnie. Rozvíjí se kompenzační tachypnoe k zajištění ventilace a oxygenace se snahou o eliminaci CO2, a tím alkalizaci krve.
Zvýšení dechové frekvence však může vést k depleci glykogenu dýchacích svalů a anaerobnímu metabolismu s produkcí laktátu, a tím k další acidifikaci krve. Klinicky se objevují zmatenost, delirantní stavy až bezvědomí. Obranné reflexy dýchacích cest, jako je kašel, jsou utlumeny.
V časných fázích intoxikace, co se zajištění ventilační podpory týká, by mělo být zváženo použití NIV k redukci práce dýchacích svalů. V případě již rozvinuté mentální deteriorace či vysokého rizika aspirace je však metodou volby ventilace invazivní (32).
LÉČBA
V případě akutního hyperkapnického respiračního selhání je terapeutickou metodou volby neinvazivní přetlaková ventilace, s výjimkou stavů, u kterých je již indikovaná invazivní ventilace (tab. 2) (33). Podle dostupných dat NIV redukuje mortalitu a počet pacientů, u kterých progrese stavu ústí v nutnost orotracheální intubace (OTI) (34). Vždy je však potřeba bedlivé sledování vývoje pro případnou eskalaci terapie na invazivní ventilaci. V případě, že NIV nemá žádoucí efekt na stav pacienta, by se neměla zbytečně oddalovat intubace a invazivní mechanická ventilace. Cílem je eliminovat nadbytečné množství CO2, avšak je třeba sledovat metabolickou kompenzační složku (spíše v rámci chronické hyperkapnie), kdy zrušením respirační acidózy dojde k posunu acidobazické rovnováhy do metabolické alkalózy (přetrvává nadbytek HCO3–). Tím může dojít k přesunu kalia do buněk, hypokalémii a vzniku závažných arytmií (13).
Tab. 2. Možnosti terapie 2. a 3. linie u aktivní střední až těžké EO ve specializovaném centru 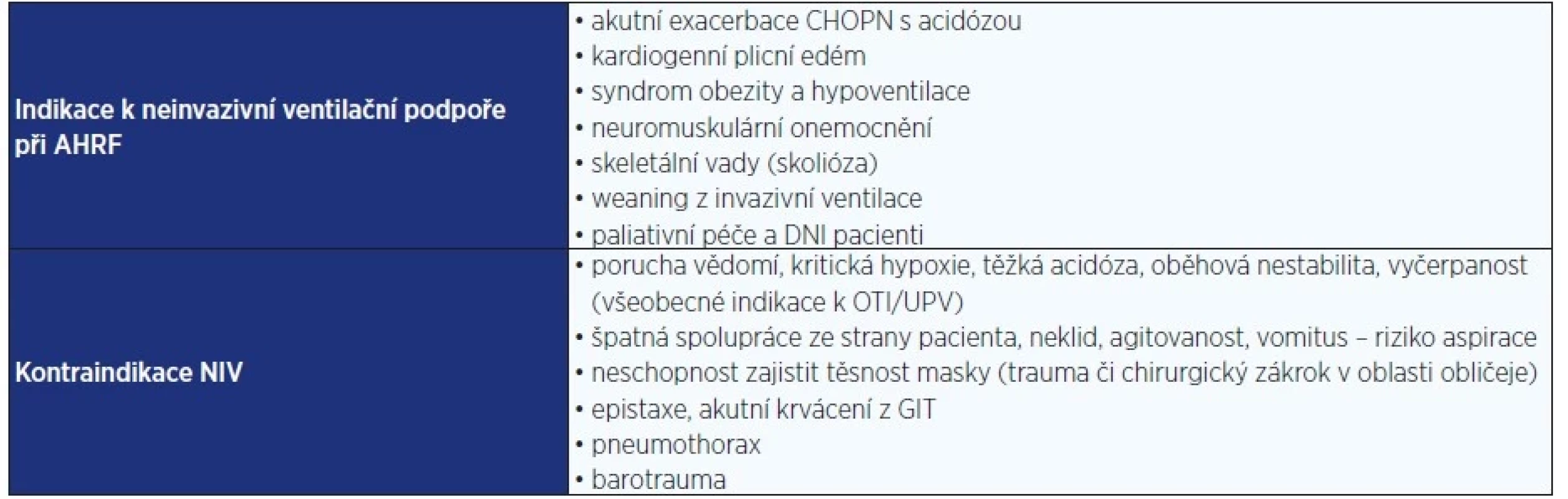
Pozn.: DNI – neintubovat (do not intubate); OTI – orotracheální intubace; UPV – umělá plicní ventilace; GIT – gastrointestinální trakt. Tab. 3. Doporučené iniciální nastavení terapie u nejčastějších indikací k NIV (39) 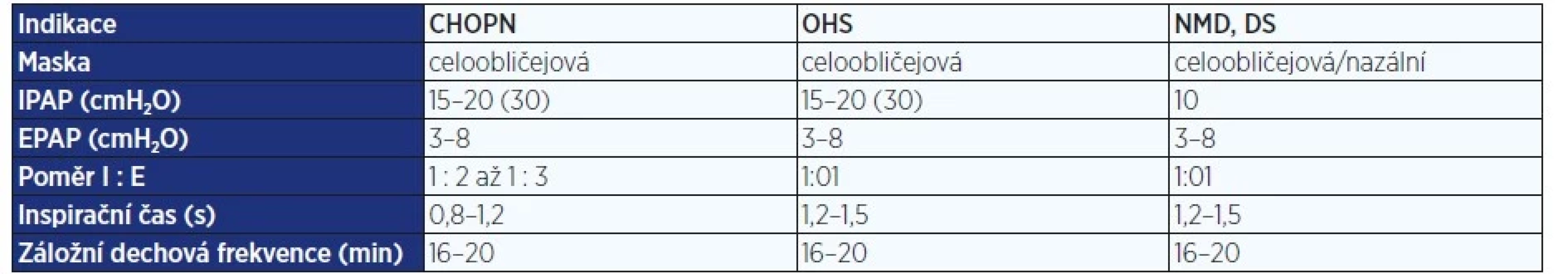
Pozn.: CHOPN – chronická obstrukční plicní nemoc; OHS – syndrom obezity a hypoventilace; NMD – neuromuskulární onemocnění; DS – deformity skeletu; IPAP – inspirační pozitivní přetlak; EPAP – exspirační pozitivní přetlak; I – inspirium; E – exspirium. Podle doporučení ERS je použití NIV jednoznačně indikované v případě hyperkapnie při exacerbaci CHOPN s již rozvinutou acidózou a při terapii kardiogenního plicního edému (19). S nižší váhou doporučení lze NIV použít při respiračním selhání u imunokompromitovaných pacientů, v pooperační péči, u traumat hrudníku, dále profylakticky po extubaci v rámci odvykání (weaning).
Rovněž je NIV doporučena u pacientů s hyperkapnií v terminálních stadiích (terminální CHOPN, onkologičtí pacienti), při kontraindikaci OTI a UPV nebo nesouhlasu pacienta s intubací.
K terapii hyperkapnického respiračního selhání neuromuskulární etiologie je NIV indikována i bez přítomné acidózy, indikací zde je výskyt ortopnoe, tachypnoe či zapojení pomocných dýchacích svalů. V případě bulbárních forem často bývá tolerována problematicky (například při hypersalivaci či netěsnosti masky při ochablém obličejovém svalstvu) – pak je ke zvážení provedení akutní tracheostomie (35). Obvykle používaným režimem bývá objemově řízená ventilace, přičemž postačuje použití nízkých exspiračních tlaků. Výjimku tvoří pacienti s obezitou, kde je vyšší pravděpodobnost přítomnosti či rozvoje komorbidního syndromu spánkové apnoe a těžké hyperkapnie.
Režim objemově řízené ventilační podpory na odděleních urgentního příjmu byl ve studii stejnou účinný i bezpečný jako BiPAP/ST (ST – spontánní a triggerované dechy) bez volumové podpory (36).
U pacientů s hyperkapnickým respiračním selháním na podkladě akutního kardiogenního plicního edému pacienti profitovali ekvivalentně z CPAP i BiPAP.
V recentních studiích autoři porovnávají vysokoprůtokou kyslíkovou terapii (HFNOT) s neinvazivní přetlakovou ventilací. Výsledky svědčí o noninferioritě HFNOT a menších komplikacích, jako jsou např. poranění kůže tlakem masky při NIV. HFNOT je tedy metodou volby při kontraindikacích NIV (např. netolerance NIV ze strany pacienta). Uplatňuje se efekt vysokého průtoku vzduchu a jeho wash out efekt v dýchacích cestách, dále také zmenšení mrtvého prostoru a vytvoření mírného pozitivního end-exspiračního tlaku (PEEP) (37, 38).
NASTAVENÍ VENTILAČNÍCH REŽIMŮ
Použití NIV při AHRS je doporučováno v režimu BiPAP s využitím celoobličejové masky. Počáteční nastavení tlaků se různí podle jednotlivých klinických praxí, například v německém prostředí jsou častěji používány vyšší tlaky, čímž je rychleji a efektivněji dosahováno normalizace krevních plynů, zatímco v Itálii jsou v oblibě nižší tlaky, u kterých lze očekávat lepší toleranci léčby. V naší klinické praxi používáme obvykle iniciálně inspirační tlak 15 cmH2O a exspirační tlak 3–5 cmH2O. Následně by měl být stav evaluován každých 10–30 minut a nastavení upraveno podle tolerance ze strany pacienta a přinášeného efektu. Cílová saturace hemoglobinu kyslíkem při kontinuálním měření by měla dosahovat hodnot 88–92 %, přičemž je vhodné nejprve optimalizovat ventilaci nastavením hodnot tlaků, a až následně přikročit k navyšování frakce kyslíku. Dále by měl být monitorován efekt terapie na zlepšení hodnot pH, PaCO2 a dechové frekvence. První kontrolní odběr tepenné krve ke stanovení krevních plynů provádíme za 20–30 minut po zahájení NIV.
Použití vyšších hodnot IPAP (20–30 cmH2O) může být nutné u pacientů s akutní exacerbací CHOPN či OHS. U neuromuskulárních postižení bez strukturálního postižení plic může být dostatečné použití nižších tlaků. Vyšší hodnoty EPAP mohou být potřeba u pacientů s obstrukcí horních dýchacích cest (OSAS, OHS).
Oxygenoterapie při NIV je řízena cestou vnitřního okruhu přístroje po napojení na zdroj kyslíku, lze zadat požadovanou frakci. U vyšších hodnot IPAP může být nutné zvýšení frakce (28, 39).
Doporučena je co nejdelší doba využití NIV v průběhu prvních 24 hodin, dále podle tolerance a laboratorních kontrol. Pokud neinvazivní ventilační podpora selhává a respirační selhání progreduje, je indikováno zvážení OTI.
PROGNÓZA
Značná část (až 20 %) pacientů po akutní exacerbaci CHOPN s hyperkapnickým respiračním selháním má prolongovanou hyperkapnii. V těchto případech je nutné zvážit léčbu dlouhodobou domácí NIV (40).
Hyperkapnie je téměř vždy známkou vyčerpání ventilačního úsilí. Byly pozorovány rozdíly v roční mortalitě mezi skupinami pacientů přijímaných do nemocniční péče pro dušnost a různá plicní postižení. Roční mortalita pacientů s respiračním onemocněním a vstupně stanovenou akutní hyperkapnií činí přibližně 32 %, u neselektovaných pacientů s chronickým hyperkapnickým respiračním selháním asi 20 % (1). Účinná domácí neinvazivní ventilační podpora u pacientů s přetrvávající chronickou hyperkapnií výrazně zvyšuje pravděpodobnost dlouhodobého přežití. Mortalita zůstává zvýšená u pacientů s normalizací hyperkapnie při dimisi, přičemž podle dostupných dat až přibližně 14 % pacientů umírá v prvním roce po odeznělém AHRS (1).
Pacienti s neuromuskulárními nemocemi představují samostatnou skupinu, přičemž například u amyotrofické laterální sklerózy je AHRS spojeno s výrazně horší prognózou a medián přežití po jeho vzniku nepřesahuje 2 roky (35).
ZÁVĚR
Akutní hyperkapnické respirační selhání je indikátor selhání ventilace. Může být manifestací pokročilého stadia chronické obstrukční plicní nemoci, kde se vyskytuje v rámci exacerbací, nebo chronicky v rámci progrese základního onemocnění. Dále se může jednat o první projev do té doby nediagnostikovaného neuromuskulárního onemocnění, hypoventilačního syndromu při obezitě nebo deformit skeletu. Bývá typickým projevem kardiogenního plicního edému. U těchto pacientů by mělo být na hyperkapnii primárně pomýšleno. Terapeuticky je poté metodou volby neinvazivní ventilace.
Seznam použitých zkratek
AHRS akutní hyperkapnické respirační selhání
ARDS syndrom akutní respirační tísně (acute respiratory distress syndrome)
BiPAP dvouúrovňová terapie positivním přetlakem dýchacích cest (bi-level positive airway pressure)
EPAP exspirační positivní tlak dýchacích cest (expiratory positive airway pressure)
ERS Evropská respirační společnost
FEV1 jednosekundová vitální kapacita
HFNOT vysokoprůtoková nosní oxygenoterapie (high-flow nasal oxygen therapy)
CHOPN chronická obstrukční plicní nemoc
IPAP inspirační pozitivní tlak dýchacích cest (inspiratory positive airway pressure)
NIV neinvazivní ventilace
OHS hypoventilační syndrom při obezitě (obesity-hypoventilation syndrome)
OSAS syndrom obstrukční spánkové apnoe (obstructive sleep apnoea syndrome)
OTI orotracheální intubace
PEEP pozitivní tlak na konci výdechu (positive end-expiratory pressure)
ST spontánní a triggerované dechy
UPV umělá plicní ventilace
Adresa pro korespondenci:
MUDr. Samuel Genzor, Ph.D.
Klinika plicních nemocí a tuberkulózy LF UP a FN Olomouc
Zdravotníků 248/7, 779 00 Olomouc
Tel.: 588 443 561
e-mail: samuel.genzor@fnol.cz
Zdroje
- Vonderbank S, Gibis N, Schulz A et al. Hypercapnia at hospital admission as a predictor of mortality. Open Access Emerg Med 2020; 12 : 173–180.
- Gendreau S, Geri G, Pham T et al. The role of acute hypercapnia on mortality and short-term physiology in patients mechanically ventilated for ARDS: a systematic review and meta-analysis. Intensive Care Med 2022; 48 : 517–534.
- Chung Y, Garden FL, Marks GB, Vedam H. Causes of hypercapnic respiratory failure and associated in‐hospital mortality. Respirology 2023; 28 : 176–182.
- Caruso ALG, Bouillon TW, Schumacher PM et al. Drug-induced respiratory depression: an integrated model of drug effects on the hypercapnic and hypoxic drive. Annu Int Conf IEEE Eng Med Biol Soc 2007; 2007 : 4259–4263.
- Vadász I, Hubmayr RD, Nin N et al. Hypercapnia: a nonpermissive environment for the lung. Am J Respir Cell Mol Biol 2012; 46 : 417–421.
- Patel S, Sharma S. Respiratory acidosis. StatPearls, Treasure Island, 2022.
- Fox BD, Bondarenco M, Shpirer I et al. Transitioning from hospital to home with non-invasive ventilation: who benefits? Results of a cohort study. BMJ Open Respir Res 2022; 9: e001267.
- Blankenburg T, Benthin C, Pohl S et al. Survival of hypercapnic patients with copd and obesity hypoventilation syndrome treated with high intensity noninvasive ventilation in the daily routine care. Open Respir Med J 2017; 11 : 31–40.
- Lněnička J. Respirační insuficience, chronická hyperkapnie a domácí neinvazivní ventilace z pohledu pneumologa. Vnitřní lékařství 2021; 67 : 323–327.
- Tucker AM, Johnson TN. Acid‐base disorders: a primer for clinicians. Nutr Clin Pract 2022; 37 : 980–989.
- Plant PK. One year period prevalence study of respiratory acidosis in acute exacerbations of COPD: Implications for the provision of non-invasive ventilation and oxygen administration. Thorax 2000; 55 : 550–554.
- Resta O, Barbaro MPF, Brindicci C et al. Hypercapnia in overlap syndrome: Possible determinant factors. Sleep Breath 2002; 6(1): 11–17.
- Kolek V, Kašák V, Koziar Vašková M. Pneumologie (3., rozšířené vyd.). Maxdorf, Praha, 2017.
- Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. Global Initiative for Chronic Obstructive Lung Disease, 2023. Dostupné na: https://goldcopd.org/wp-content/uploads/2023/03/GOLD-2023-ver-1.3-17Feb2023_WMV.pdf
- Saure EW, Eagan TML, Jensen RL et al. Explained variance for blood gases in a population with COPD. Clin Respir J 2012; 6 : 72–80.
- Rodríguez-Roisin R, Drakulovic M, Rodríguez DA et al. Ventilation-perfusion imbalance and chronic obstructive pulmonary disease staging severity. J Appl Physiol 2009; 106 : 1902–1908.
- Briva A, Vadász I, Lecuona E et al. High co2 levels impair alveolar epithelial function independently of pH. PLoS One 2007; 2: e1238.
- Dave C, Wharton S, Mukherjee R et al. Development and relevance of hypercapnia in COPD. Can Respir J 2021 : 6623093.
- Rochwerg B, Brochard L, Elliott MW et al. Official ERS/ATS clinical practice guidelines: noninvasive ventilation for acute respiratory failure. Eur Respir J 2017; 50 : 1602426.
- Brochard L, Isabey D, Piquet J et al. Reversal of acute exacerbations of chronic obstructive lung disease by inspiratory assistance with a face mask. N Engl J Med 1990; 323 : 1523–1530.
- Brochard L, Mancebo J, Wysocki M et al. Noninvasive ventilation for acute exacerbations of chronic obstructive pulmonary disease. N Engl J Med 1995; 333 : 817–822.
- Ambrosino N, Foglio K, Rubini F et al. Non-invasive mechanical ventilation in acute respiratory failure due to chronic obstructive pulmonary disease: correlates for success. Thorax 1995; 50 : 755–757.
- Wang S, Singh B, Tian L et al. Epidemiology of noninvasive mechanical ventilation in acute respiratory failure-a retrospective population-based study. BMC Emerg Med 2014; 13 : 6.
- Masa JF, Pépin JL, Borel JC et al. Obesity hypoventilation syndrome. Eur Respir Rev 2019; 28 : 180097.
- Lněnička J, Dostálová S, Doušová T a kol. Doporučený postup pro domácí neinvazivní ventilaci. Stud Pneumol Phtiseol 2022; 82 : 168–184.
- Chebib N, Nesme P, Freymond N et al. Acute respiratory failure in obesity-hypoventilation syndrome managed in the ICU. Respir Care 2019; 64 : 1545–1554.
- Nicolini A, Ferrando M, Solidoro P et al. Non-invasive ventilation in acute respiratory failure of patients with obesity hypoventilation syndrome. Minerva Med 2018; 109 (6 Suppl. 1): 1–5.
- Comellini V, Pacilli AMG, Nava S. Benefits of non‐invasive ventilation in acute hypercapnic respiratory failure. Respirology 2019; 24 : 308–317.
- Iqbal MA, Gupta M. Cardiogenic pulmonary edema. StatPearls, Treasure Island, 2022.
- Masip J. Noninvasive ventilation in acute heart failure. Curr Heart Fail Rep 2019; 16 : 89–97.
- Faqihi BM, Trethewey SP, Morlet J et al. Bilevel positive airway pressure ventilation for non-COPD acute hypercapnic respiratory failure patients: A systematic review and meta-analysis. Ann Thorac Med 2021; 16 : 306–322.
- Wilson KC, Saukkonen JJ. Acute respiratory failure from abused substances. J Intensive Care Med 2004; 19 : 183–193.
- Kreppein U, Litterst P, Westhoff M. Hyperkapnisches Atemversagen. Med Klin Intensivmed Notfmed 2016; 111 : 196–201.
- Osadnik CR, Tee VS, Carson-Chahhoud KV et al. Non-invasive ventilation for the management of acute hypercapnic respiratory failure due to exacerbation of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2017; 7: CD004104.
- Bourke SC, Bullock RE, Williams TL et al. Noninvasive ventilation in ALS: Indications and effect on quality of life. Neurology 2003; 61 : 171–177.
- Gören NZ, Şancı E, Ercan Coşkun FF et al. Comparison of BPAP S/T and average volume-assured pressure support modes for hypercapnic respiratory failure in the emergency department: A randomized controlled trial. Balkan Med J 2021; 38 : 265–271.
- Papachatzakis Y, Nikolaidis PT, Kontogiannis S. High-flow oxygen through nasal cannula vs. non-invasive ventilation in hypercapnic respiratory failure: A randomized clinical trial. Int J Environ Res Public Health 2020; 17 : 5994.
- Sun J, Li Y, Ling B et al. High flow nasal cannula oxygen therapy versus non-invasive ventilation for chronic obstructive pulmonary disease with acute-moderate hypercapnic respiratory failure: an observational cohort study. Int J Chron Obstruct Pulmon Dis 2019; 14 : 1229–1237.
- Ghosh D, Elliott MW. Acute non-invasive ventilation – getting it right on the acute medical take. Clin Med 2019; 19 : 237–242.
- Bräunlich J, Turba K, Wirtz H. Reversibility of hypercapnia after an acute exacerbation of COPD. Respiration 2022; 101 : 816–822.
Štítky
Adiktológia Alergológia a imunológia Angiológia Audiológia a foniatria Biochémia Dermatológia Detská gastroenterológia Detská chirurgia Detská kardiológia Detská neurológia Detská otorinolaryngológia Detská psychiatria Detská reumatológia Diabetológia Farmácia Chirurgia cievna Algeziológia Dentální hygienistka
Článek ÚVODEMČlánek Syndrom křehkostiČlánek Zemřel profesor Karel MaršálČlánek Odešel docent Jiří Ramba
Článok vyšiel v časopiseČasopis lékařů českých
Najčítanejšie tento týždeň
2023 Číslo 1- Spasmolytický účinek metamizolu
- Měření plicního věku pomocí spirometrie – orientační screening plicních funkcí
- Na český trh přichází biosimilar adalimumabu s prokázanou terapeutickou ekvivalencí
- Nech brouka žít… Ať žije astma!
- Screening malignit u pacientů s dermatomyozitidou
-
Všetky články tohto čísla
- ÚVODEM
- Současné možnosti a rizika darování některých tkání, buněk a orgánů od živých dárců
- Tuková tkáň v léčbě androgenní alopecie
- Hyperkapnické respirační selhání
- Farmakoterapie obezity – update 2023
- Syndrom křehkosti
- Léčebný efekt lymfografie u pooperačního chylothoraxu – kazuistiky a přehled literatury
- Protilátky získané po infekci koronavirem nás dlouhodobě chrání před opakovanou infekcí, pravil už i Lancet
- MUDr. Otakar Tardy, významný žák prof. Ningera, zakladatel ORL oddělení v Litomyšli – připomínka při příležitosti 45. výročí jeho úmrtí
- Zemřel profesor Karel Maršál
- Odešel docent Jiří Ramba
- Zemřel docent Petr Brandejský
- Přednáškové večery Spolku českých lékařů v Praze (duben – květen 2023)
- Sjezd České lékařské společnosti JEP
- Časopis lékařů českých
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Farmakoterapie obezity – update 2023
- Hyperkapnické respirační selhání
- Současné možnosti a rizika darování některých tkání, buněk a orgánů od živých dárců
- Protilátky získané po infekci koronavirem nás dlouhodobě chrání před opakovanou infekcí, pravil už i Lancet
Kurzy
Zvýšte si kvalifikáciu online z pohodlia domova
Autori: MUDr. Petr Výborný, CSc., FEBO
Všetky kurzyPrihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



