-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Alveolárny sarkóm mäkkých tkanív u dieťaťa – opis prípadu
Alveolar soft part sarcoma in a child – a case report
Background: Alveolar soft part sarcoma (ASPS) is a very rare mesenchymal malignancy of uncertain origin. It mostly affects young people, with about a quarter of cases being diagnosed in children.
Case: An 11-year-old girl had a painless subcutaneous “lump” in the left elbow area. Imaging exams revealed a solid soft-tissue intramuscular mass of suspicious appearance. A surgical excision of lesion was performed. The biopsy consisted of a lobular tumor measuring 35 × 20 × 12 mm. Histology revealed an epithelioid-cell population arranged in organoid pseudoalveolar pattern. It immunohistochemically expressed TFE3 and harbored the ASPSCR1:: TFE3 gene fusion. A diagnosis of ASPS was established. Subsequently, a wide re-excision of the scar was performed without microscopic residual tumor. The patient is currently without evidence of local recurrence or metastasis.
Conclusion: ASPS is considered an aggressive and prognostically unfavorable chemoresistant neoplasm. Children have a better prognosis compared to adults. Early detection of tumor in a localized stage with complete surgical removal remains a mainstay therapeutic option. Due to its tendency to late metastases, a long-term thorough follow-up of the patient is necessary.
Keywords:
alveolar soft part sarcoma – ASPSCR1:: TFE3
Autori: V. Bartoš 1; D. Sejnová 2; A. Skálová 3,4; I. Béder 5
Pôsobisko autorov: Martinské bioptické centrum, s. r. o., Martin, Slovenská republika 1; Klinika detskej hematológie a onkológie, Národný ústav detských chorôb, Bratislava, Slovenská republika 2; Šiklův patologický ústav LF v Plzni UK a FN Plzeň, Česká republika 3; Bioptická laboratoř s. r. o., Plzeň, Česká Republika 4; Klinika detskej chirurgie, Národný ústav detských chorôb, Bratislava, Slovenská republika 5
Vyšlo v časopise: Klin Onkol 2023; 36(5): 396-400
Kategória: Kazuistika
doi: https://doi.org/10.48095/ccko2023396Súhrn
Východiska: Alveolárny sarkóm mäkkých tkanív (alveolar soft part sarcoma – ASPS) je veľmi zriedkavá mezenchýmová malignita nejasného pôvodu. Väčšinou postihuje mladých ľudí, pričom približne štvrtina prípadov sa diagnostikuje v detskom veku.
Prípad: Jedenásťročné dievča pozorovalo nebolestivú podkožnú „hrčku“ v oblasti ľavého lakťa. Zobrazovacie vyšetrenia potvrdili solídnu mäkkotkanivovú intramuskulárnu rezistenciu suspektného vzhľadu. Vykonaná bola jej chirurgická excízia. Resekát pozostával z laločnatého nádoru rozmerov 35 × 20 × 12 mm. Histologicky bol tvorený organoidne rastúcou epiteloidnobunkovou populáciou s vyznačenou pseudoalveolárnou mikroarchitektonikou. Imunohistochemicky exprimoval TFE3 a geneticko-molekulová analýza preukázala fúziu génu ASPSCR1:: TFE3. Spektrum nálezov potvrdzovalo diagnózu ASPS. Následne bola vykonaná široká reexcízia jazvy bez mikroskopického dôkazu nádorových reziduí. Pacientka je v súčasnosti bez známok lokálnej recidívy či metastáz.
Záver: ASPS sa považuje za agresívny a prognosticky nepriaznivý chemorezistentný nádor. U detí má lepšiu prognózu v porovnaní s dospelými. Z terapeutického hľadiska je kľúčové včasné rozpoznanie tumoru v lokalizovanom štádiu a jeho kompletné chirurgické odstránenie. Vzhľadom na tendenciu vzniku neskorých metastáz je nutný dlhodobý dôkladný follow-up pacienta.
Klíčová slova:
alveolárny sarkóm mäkkých tkanív – ASPSCR1:: TFE3
Úvod
Sarkómy mäkkých tkanív (soft tissue sarcomas – STS) sú zriedkavé nádory, ktorých odhadovaná ročná incidencia sa pohybuje v rozpätí 3–4,5 pacientov na 100 000 obyvateľov [1,2]. V ČR predstavujú 0,78 % zo všetkých zhubných nádorov [2]. STS tvoria veľmi heterogénnu skupinu neoplázií mezenchýmového pôvodu zahrňujúcu > 80 histopatologických jednotiek, ktoré sa významne odlišujú vekovou distribúciou, miestom vzniku, biologickým správaním a prognózou [1,3]. V onkologickej praxi sú vždy vnímané ako ochorenia závažné, často sprevádzané diagnostickými a terapeutickými rozpakmi [3]. Samostatnú a komplexnú problematiku predstavuje dedičná predispozícia k vzniku sarkómom [4].
Alveolárny sarkóm mäkkých tkanív (alveolar soft part sarcoma – ASPS) je veľmi zriedkavý a z viacerých aspektov špecifický typ malígnej neoplázie, ktorá predstavuje < 1 % všetkých STS [5–8]. Charakteristický je chromozómovou translokáciou der (17) t (X: 17) (p11: q25) zapríčiňujúcu fúziu génu ASPSCR1:: TFE3 [5,6,8]. Väčšinou postihuje mladých ľudí medzi 15–35 rokom života (priemerný vek 25 rokov) s prevalenciou ženského pohlavia [5–7]. Približne štvrtina prípadov sa diagnostikuje v detskom veku [9]. U dospelých postihuje najmä hlboké mäkké tkanivové štruktúry dolných končatín a trupu, u detí má väčšiu predilekciu v oblasti hlavy a krku [5–7]. ASPS je nádor s agresívnym biologickým správaním a nepriaznivým klinickým priebehom [6–8]. V prezentovanom príspevku opisujeme prípad ASPS u dieťaťa, s ktorým sme sa stretli v našej praxi.
Obr. 1. Solídne rastúca epiteloidnobunková nádorová populácia, na periférii lemovaná tenkým väzivovým puzdrom (hematoxylín & eozín, zväčšenie 20×). 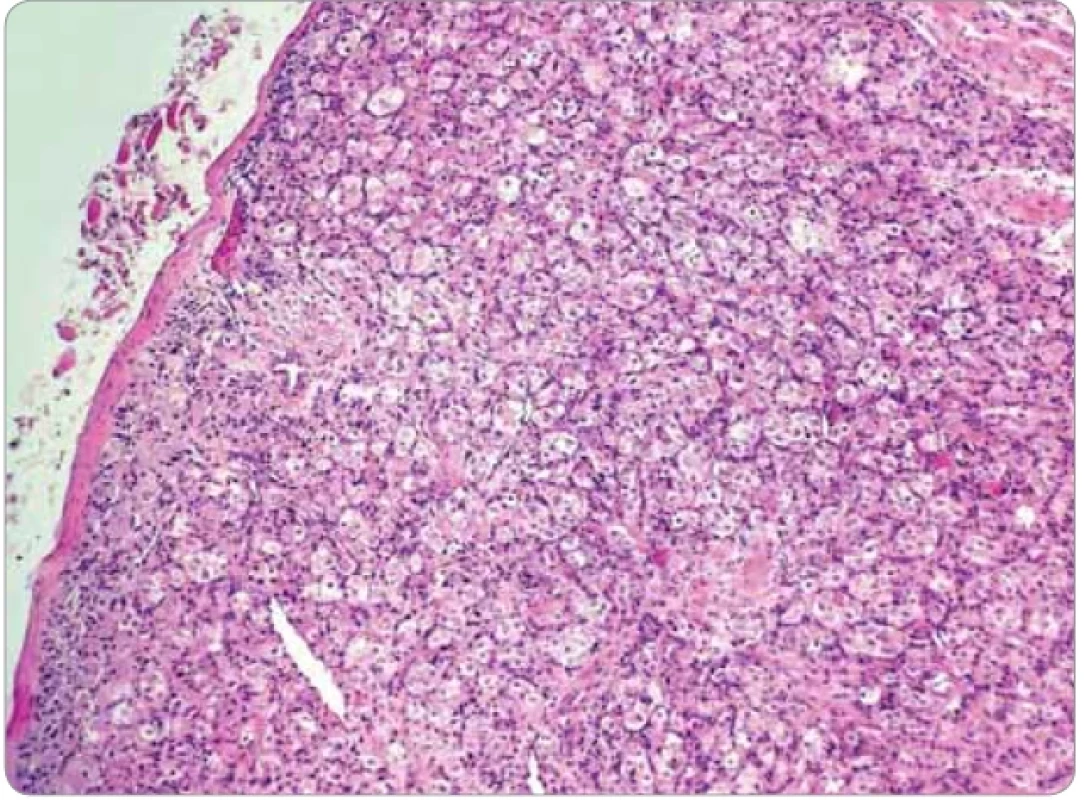
Obr. 2. Typická pseudoalveolárna mikroarchitektonika nádoru (hematoxylín & eozín, zväčšenie 20×). 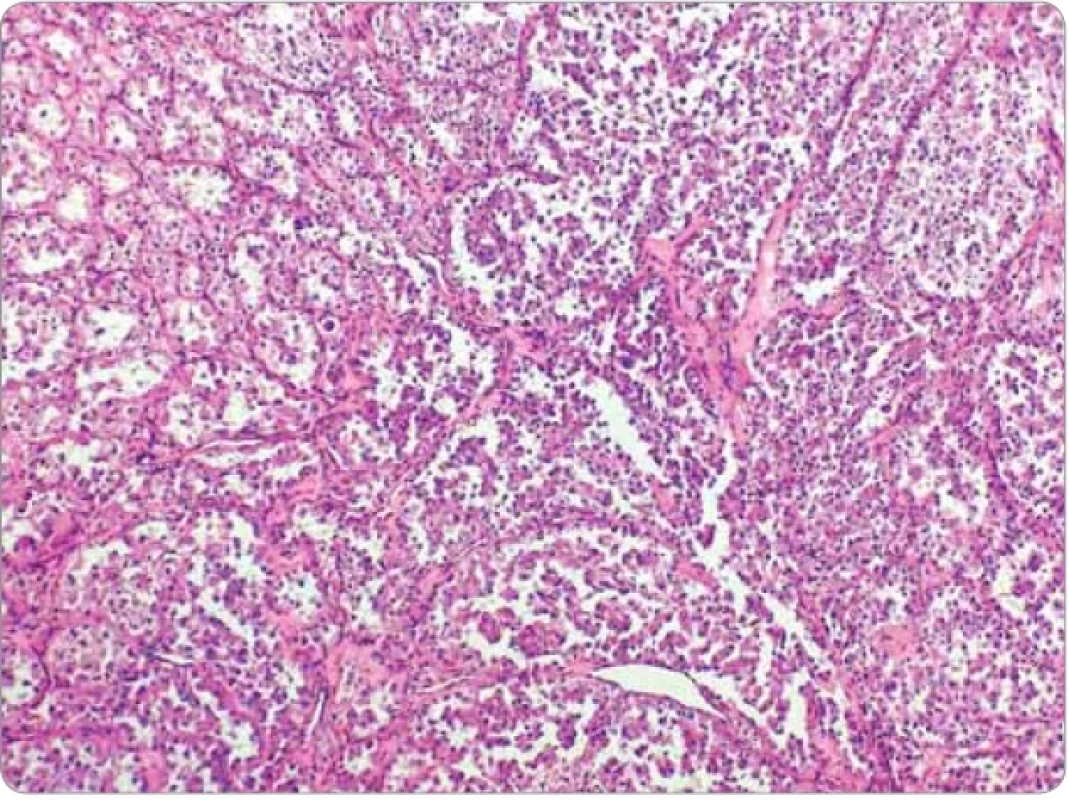
Opis prípadu
Jedenásťročné dievča bez významnejšej rodinnej a osobnej anamnézy (sledovaná u endokrinológa pre obezitu) odoslal pediater na konzílium na traumatologicko-chirurgickú ambulanciu v rajóne pre pretrvávajúcu podkožnú „hrčku“ v oblasti ľavého lakťa. Klinicky mala v danej lokalite hmatateľnú subkutánnu nebolestivú rezistenciu. Predchádzajúci úraz rodičia vylúčili. Nález imponoval ako lipóm. Ultrasonografické (USG) vyšetrenie zobrazilo pod kožou ohraničený solídny vaskularizovaný útvar rozmerov 25 × 19 × 34 mm suspektného vzhľadu. MR potvrdila na rozhraní m. flexor carpi ulnaris a m. flexor digitorum superficialis mäkkotkanivovú expanzívnu intramuskulárnu léziu rozmerov 24 × 42 × 21 mm. Diferenciálno-diagnosticky sa uvažovalo o synoviálnom sarkóme alebo atypickej myxoidnej nádorovej lézii. S týmto nálezom bola pacientka odoslaná na kliniku detskej chirurgie Národného ústavu detských chorôb na exstirpáciu. Predoperačné CT hrudníka zobrazilo pľúcny parenchým bez ložiskových zmien, bez metastáz, lymfatické uzliny v mediastíne, pľúcnych hiloch a obidvoch axilách neboli zväčšené. USG brušných orgánov a dostupnej časti retroperitonea taktiež bez dokázateľných ložiskových zmien, bez lymfadenopatie. V celkovej anestézii sa realizovala radikálna chirurgická excízia tumoru. Resekát pozostával z laločnatého nádorového tkaniva rozmerov 35 × 20 × 12 mm, hnedonažltlej farby, elastickej konzistencie. Histologicky pozostával z organoidne rastúcej epiteloidnobunkovej populácie s vyznačenou pseudoalveolárnou mikroarchitektonikou (obr. 1, 2). Relatívne uniformné bunky mali voluminóznu, prevažne eozinofilnú cytoplazmu, v ktorej sa vyskytoval jemne granulárny kryštaloidný materiál pozitívny pri farbení PAS (periodická kyselina a Shiffovo reagens) a PAS po natrávení diastázou. Centrálne jadrá buniek obsahovali prominujúce jadierka. Imunohistochemicky nádor vykazoval difúznu jadrovú pozitivitu na TFE3 (obr. 3), bol nepravidelne pozitívny na a-hladkosvalový aktín a minoritne aj na vimentín a dezmín (obr. 4). Dôkaz ostatných markerov (polyklonálne cytokeratíny AE1/AE3, CD34, S100, myoD1, kalretinín, chromogranín A) bol negatívny. Proliferačná aktivita (Ki-67 index) fokálne dosahovala 15 %, mitózy sa vyskytovali len sporadicky. Geneticko-molekulová analýza realizovaná na špecializovanom konzultačnom pracovisku preukázala fúziu génu ASPSCR1:: TFE3. Spektrum uvedených nálezov potvrdzovalo diagnózu ASPS. Na periférii resekátu bolo nádorové tkanivo zväčša lemované tenkým väzivovým puzdrom a miestami aj tenkou vrstvou tuku a kostrovej svaloviny, avšak v niektorých úsekoch puzdro absentovalo a nádorové štruktúry zasahovali do okrajov resekátu. Patológ preto považoval excíziu za nedostatočnú.
Po stanovení diagnózy boli u pacientky doplnené vyšetrenia v rámci stagingu: PET/CT vyšetrenie bez nálezu hypermetabolických reziduí v mieste exstirpácie, v lymfatických uzlinách, skelete ani v parenchýmových orgánoch. MR mozgu nepreukázalo štrukturálne zmeny.
Kontrolné pooperačné MR vyšetrenie ľavého predlaktia zobrazilo v mieste pôvodnej expanzie plošné ložiskové signálové zmeny imponujúce ako reziduálne nádorové tkanivo v kombinácii s granulačným zápalovým tkanivom. Následne bola vykonaná široká reexcízia kože a podkožia v mieste jazvy, ktorej histologické vyšetrenie nepotvrdilo nádorové reziduá.
Vzhľadom na operačný výkon (bez mikroskopického rezidua) a staging (bez metastáz) bola pacientka zaradená do onkodispenzárnej starostlivosti s dôkladným follow-up v nasledovnej schéme: sledovanie minimálne 10 rokov s realizovanými zobrazovacími vyšetreniami každé 3 mesiace počas prvých 2 rokov, každé 4 mesiace tretí rok, každých 6 mesiacov počas 4. a 5. roku a následne 1× ročne po dobu 10 rokov. V čase spracovania tohto príspevku (10 mesiacov po operácii) bola pacientka bez známok lokálnej recidívy či metastáz.
Obr. 3. Imunohistochemická jadrová pozitivita nádorových buniek na TFE3 (zväčšenie 20×). 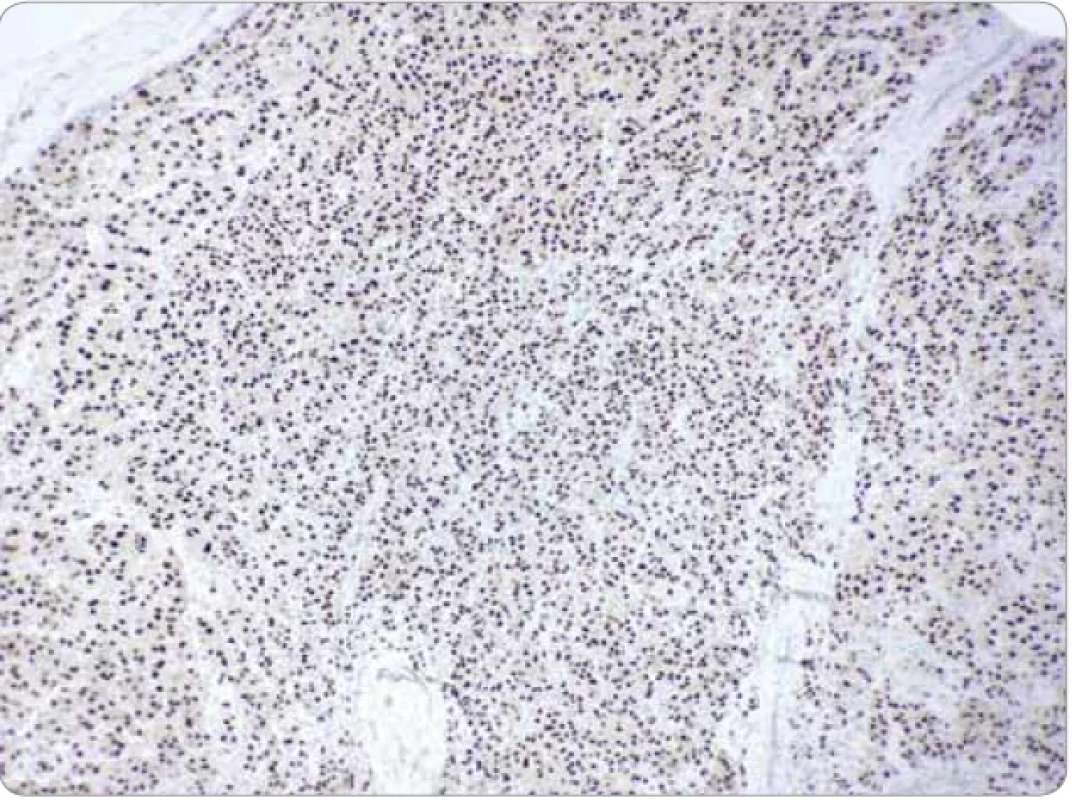
Obr. 4. Imunohistochemická cytoplazmatická pozitivita nádorových buniek na dezmín (zväčšenie 20×). 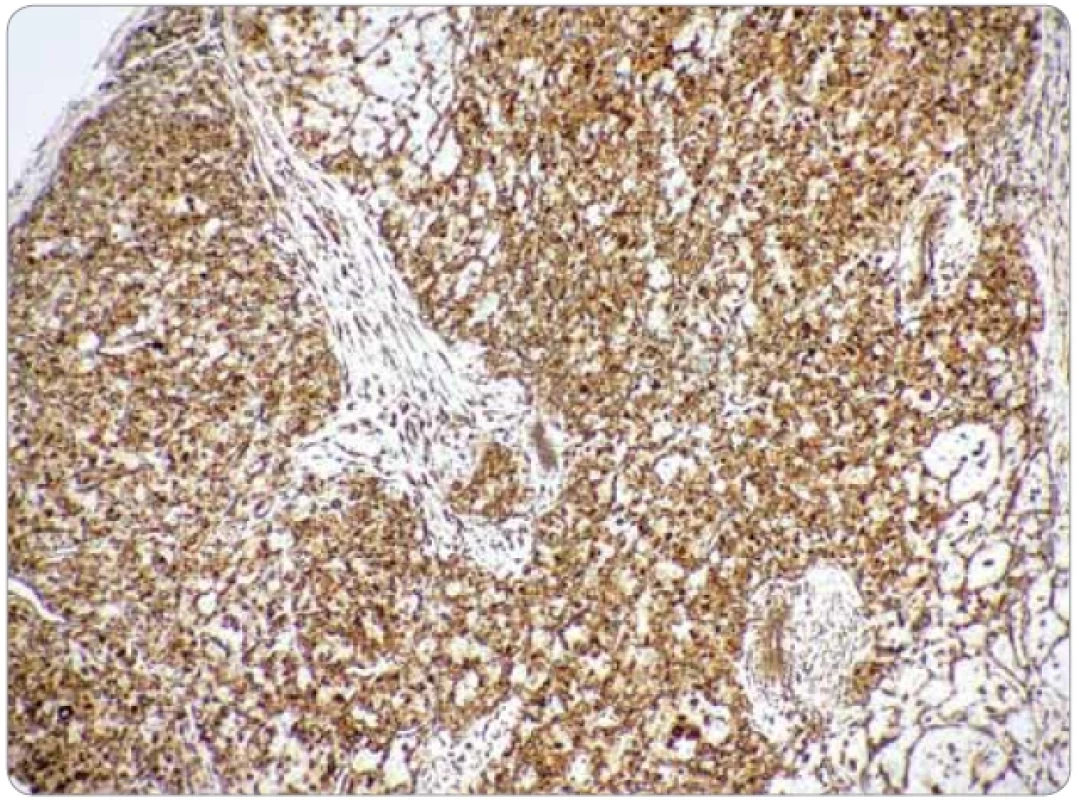
Tab. 1. Prehľad základných klinicko-patologických nálezov u pacientov s alveolárnym sarkómom mäkkých tkanív získaných z doteraz publikovaných väčších štúdií [8–21]. ![Prehľad základných klinicko-patologických nálezov u pacientov s alveolárnym sarkómom mäkkých tkanív získaných z doteraz publikovaných väčších štúdií [8–21].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/8c9e78a00e4ba937b98bfc14ac119515.png)
* follow-up ani u jedného pacienta nedosahoval 5 rokov, ** zahrnutí iba pacienti s vykonanou primárnou resekciou nádoru, M0 – metastázy neprítomné, M1 – metastázy prítomné Diskusia
ASPS je malígny mezenchýmový nádor nejasnej histogenézy, ktorý vzniká najmä u mladých ľudí a predominantne postihuje hlboké mäkké tkanivá končatín [6,9]. Klinicky sa zvyčajne prejavuje ako indolentná, pomaly rastúca nebolestivá tumorózna masa, v závislosti od lokalizácie s rôznorodou symptomatológiou [5,6]. Histomorfologicky má veľmi zaujímavý obraz. Nádorovobunková populácia epiteloidného vzhľadu rastie v organoidných „hniezdovitých“ (angl. nested) formáciách separovaných delikátnymi zväzkami kolagénových vlákien so sínusoidami. V dôsledku centrálnych nekróz často vzniká pseudoalveolárny vzor, z čoho pochádza aj samotný názov tumoru [5,6]. Pri imunohistochemickom vyšetrení je dôležitým znakom nukleárna pozitivita na transkripčný faktor TFE3 [5,6,8]. Okrem toho je nádor pozitívny na katepsín K a zvyčajne aspoň fokálne exprimuje dezmín a svalovo-špecifický aktín [5]. Detekcia fúzneho transkriptu ASPSCR1:: TFE3 metodikou polymerázovej reťazovej reakcie) alebo fluorescenčnej in situ hybridizácie je pre diagnózu významná, nie však úplne špecifická pre toto onkologické ochorenie [5,6,8].
ASPS sa tradične považuje za prognosticky nepriaznivú malígnu neopláziu [5,6]. V prehľadnej tab. 1 sú sumarizované základné klinicko-patologické parametre ochorenia získané z doteraz publikovaných súborných prác analyzujúcich väčší počet pacientov [8–21]. V približne tretine prípadov sa vzdialené metastázy potvrdia už v čase prvotnej diagnostiky ochorenia [8–21]. ASPS má zároveň tendenciu k vzniku neskorých metastáz do viscerálnych orgánov, najmä do pľúc, mozgu a kostí, a to aj bez predchádzajúcej lokoregionálnej recidívy. V jednej staršej štúdii [10] zo 69 pacientov bez prítomných metastáz v čase iniciálnej diagnózy došlo k ich vzniku v 23 % prípadov v priebehu 2 rokov, v 40 % prípadov v priebehu 5 rokoch, v 62 % prípadov v priebehu 10 rokoch a v 85 % prípadov v priebehu 20 rokov. Zaujímavé je, že deti majú v porovnaní s dospelými lepšiu prognózu. Pokým v celkovej populácii je priemerné 5-ročné prežívanie 63 % [9,10,12,13,20,21], u detí do 18 rokov je to takmer 90 % [8,9,13–15,18]. Prognózu ovplyvňuje najmä klinické štádium ochorenia. Pri absencii vzdialených metastáz je priemerné 5-ročné prežívanie 87 %, ale pri generalizovanom štádiu ochorenia len 42 % [8,9,11–13,20,21]. Lepšia prognóza u detí a mladistvých môže súvisieť práve s tým, že sa u nich častejšie diagnostikuje ochorenie v lokalizovanom (resekabilnom) štádiu. Lieberman et al. [10] uvádzajú, že u pacientov do 19 rokov sa metastázy v čase diagnostiky vyskytovali v 17 %, ale vo veku ≥ 30 rokov až v 32 % prípadov. Uvažuje sa aj o biologických rozdieloch nádorového tkaniva sprevádzaných indolentnejším rastom a nižším metastatickým potenciálom u detí v porovnaní s dospelou populáciou [15].
Základnou a najefektívnejšou terapeutickou modalitou je kompletná chirurgická exstirpácia tumoru so širokými resekčnými okrajmi [7]. Pri zasahovaní nádorových reziduí do resekčných línií, nejednoznačných resekčných okrajoch, príp. nemožnom kompletnom odstránení lézie je vhodná lokálna rádioterapia [7]. ASPS je nádor rezistentný na konvenčnú cytotoxickú chemoterapiu, ktorá vo väčšine štúdií preukázala len minimálny alebo žiadny terapeutický efekt [7]. Celková miera odpovede je < 10 % [6]. Z toho dôvodu sa adjuvantná chemoterapia bežne neodporúča, s výnimkou špecifických prípadov [7]. U pacientov s pokročilým štádiom ochorenia je perspektívou cielená liečba inhibítormi tyrozínkinázy a imunitných kontrolných bodov (anti PD-1/PDL-1, anti-CTLA4), vrátane ich kombinácie [7]. Recentné práce [22,23] preukázali klinický benefit kombinovanej liečby zahrňujúcej axitinib + pembrolizumab u 73 % pacientov a liečby anlotinib + TQB2450 (nová protilátka proti PD-L1) u 75 % pacientov s ASPS. Podľa jednej štúdie [19] je u detí imunoterapia menej efektívna v porovnaní s dospelými (iba 16,7 % detí s ASPS benefitovalo z liečby PD-1 inhibítormi), potrebné je to však overiť na väčšom súbore pacientov. Aktuálne rastie potreba kompletizácie výsledkov zo systematických analýz a klinických štúdií, ktoré by sa stali základom pre zavedenie univerzálnych terapeutických postupov pri tomto onkologickom ochorení.
Záver
Alveolárny sarkóm mäkkých tkanív sa považuje za agresívny a prognosticky nepriaznivý chemorezistentný nádor postihujúci najmä mladých ľudí. Deti majú lepšiu prognózu v porovnaní s dospelými. Z terapeutického hľadiska je najdôležitejšie včasné rozpoznanie tumoru v lokalizovanom štádiu a jeho kompletná chirurgická exstirpácia. Vzhľadom na tendenciu vzniku neskorých metastáz je nutné dlhodobé dôkladné sledovanie pacienta.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare that they have no potential conflicts of interest concerning drugs, products, or services used in the study.Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.MUDr., PhDr. Vladimír Bartoš, PhD., MPH
Martinské bioptické centrum, s.r.o.
Prieložtek 1
036 01 Martin
Slovenská republika
e-mail: vladim.bartos@gmail.comObdržané/Submitted: 5. 4. 2023
Prijaté/Accepted: 2. 6. 2023
Zdroje
1. Scepanovic D, Masarykova A, Pobijakova M et al. Multiple metachronous malignant fibrous histiocytomas of the upper limbs – a case report. Klin Onkol 2014; 27 (6): 438–441.
2. Šimůnek R, Adámková-Krákorová D, Šefr R et al. Resekce sarkomu dutiny břišní, pánve a retroperitonea. Klin Onkol 2018; 31 (3): 230–234. doi: 10.14735/amko2018230.
3. Žaloudík J, Talač R, Vagunda V et al. Sarkomy měkkých tkání – přehled novějších diagnostických a léčebných postupů. Klin Onkol 2000; 13 (5): 143–150.
4. Houfková K, Hatina J. Novinky z genetiky, molekulární biologie a klinické onkologie sarkomů. Klin Onkol 2020; 33 (1): 66–78. doi: 10.14735/amko202066.
5. Jaber OI, Kirby PA. Alveolar soft part sarcoma. Arch Pathol Lab Med 2015; 139 (11): 1459–1462. doi: 10.5858/arpa.2014-0385-RS.
6. Palouzzi L, Maki RG. Diagnosis, prognosis, and treatment of alveolar soft-part sarcoma: a review. JAMA Oncol 2019; 5 (2): 254–260. doi: 10.1001/jamaoncol.2018.4490.
7. Chang X, Li Y, Xue X et al. The current management of alveolar soft part sarcomas. Medicine (Baltimore) 2021; 100 (31): e26805. doi: 10.1097/MD.0000000000026 805.
8. Flores RJ, Harrison DJ, Federman NC et al. Alveolar soft part sarcoma in children and young adults: a report of 69 cases. Pediatr Blood Cancer 2018; 65 (5): e26953. doi: 10.1002/pbc.26953.
9. Wang H, Jacobson A, Harmon DC et al. Prognostic factors in alveolar soft part sarcoma: a SEER analysis. J Surg Oncol 2016; 113 (5): 581–586. doi: 10.1002/jso.24183.
10. Lieberman PH, Brennan MF, Kimmel M et al. Alveolar soft-part sarcoma. A clinico-pathologic study of half a century. Cancer 1989; 63 (1): 1–13. doi: 10.1002/ 1097-0142 (19890101) 63 : 1<1:: aid-cncr2820630102>3. 0.co; 2-e.
11. Portera CA Jr, Ho V, Patel SR et al. Alveolar soft part sarcoma: clinical course and patterns of metastasis in 70 patients treated at a single institution. Cancer 2001; 91 (3): 585–591. doi: 10.1002/1097-0142 (20010201) 91 : 3<585:: aid-cncr1038>3.0.co; 2-0.
12. Ogose A, Yazawa Y, Ueda T et al. Alveolar soft part sarcoma in Japan: multi-institutional study of 57 patients from the Japanese Musculoskeletal Oncology Group Oncology 2003; 65 (1): 7–13. doi: 10.1159/000071199.
13. Ogura K, Beppu Y, Chuman H et al. Alveolar soft part sarcoma: a single-center 26-patient case series and review of the literature. Sarcoma 2012; 2012 : 907179. doi: 10.1155/2012/907179.
14. Pappo AS, Parham DM, Cain A et al. Alveolar soft part sarcoma in children and adolescents: clinical features and outcome of 11 patients. Med Pediatr Oncol 1996; 26 (2): 81–84. doi: 10.1002/ (SICI) 1096-911X (199602) 26 : 2<81:: AID-MPO2>3.0.CO; 2-Q.
15. Casanova M, Ferrari A, Bisogno G et al. Alveolar soft part sarcoma in children and adolescents: a report from the Soft-Tissue Sarcoma Italian Cooperative Group. Ann Oncol 2000; 11 (11): 1445–1449. doi: 10.1023/a: 1026579623136.
16. Kayton ML, Meyers P, Wexler LH et al. Clinical presentation, treatment, and outcome of alveolar soft part sarcoma in children, adolescents, and young adults. J Pediatr Surg 2006; 41 (1): 187–193. doi: 10.1016/j.jpedsurg.2005.10.023.
17. Orbach D, Brennan B, Casanova M et al. Paediatric and adolescent alveolar soft part sarcoma: a joint series from European cooperative groups. Pediatr Blood Cancer 2013; 60 (11): 1826–1832. doi: 10.1002/pbc.24683.
18. Brennan B, Zanetti I, Orbach D et al. Alveolar soft part sarcoma in children and adolescents: The European Paediatric Soft Tissue Sarcoma study group prospective trial (EpSSG NRSTS 2005). Pediatr Blood Cancer 2018; 65 (4). doi: 10.1002/pbc.26942.
19. Tan Z, Liu J, Xue R et al. Clinical features and therapeutic outcomes of alveolar soft part sarcoma in children: a single-center, retrospective study. Front Oncol 2022; 12 : 1019911. doi: 10.3389/fonc.2022.1019911.
20. Fujiwara T, Nakata E, Kunisada T et al. Alveolar soft part sarcoma: progress toward improvement in survival? A population-based study. BMC Cancer 2022; 22 (1): 891. doi: 10.1186/s12885-022-09968-5.
21. Hagerty BL, Aversa J, Diggs LP et al. Characterization of alveolar soft part sarcoma using a large national database. Surgery 2020; 168 (5): 825–830. doi: 10.1016/j.surg.2020.06.007.
22. Wilky BA, Trucco MM, Subhawong TK et al. Axitinib plus pembrolizumab in patients with advanced sarcomas including alveolar soft-part sarcoma: a single-centre, single-arm, phase 2 trial. Lancet Oncol 2019; 20 (6): 837–848. doi: 10.1016/S1470-2045 (19) 30153-6.
23. Liu J, Gao T, Tan Z et al. Phase II study of TQB2450, a novel PD-L1 antibody, in combination with anlotinib in patients with locally advanced or metastatic soft tissue sarcoma. Clin Cancer Res 2022; 28 (16): 3473–3479. doi: 10.1158/1078-0432.CCR-22-0871.
Štítky
Detská onkológia Chirurgia všeobecná Onkológia
Článok vyšiel v časopiseKlinická onkologie
Najčítanejšie tento týždeň
2023 Číslo 5- Spasmolytický účinek metamizolu
- Brno opět přivítá onkology a nelékařské zdravotnické pracovníky
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
-
Všetky články tohto čísla
- Editorial
- Využití botulotoxinu při léčbě nežádoucích účinků radioterapie
- Transformace indolentního folikulární lymfomu v difuzní velkobuněčný B-lymfom – molekulární podstata „nádorové agresivity“
- Jak neznámý je karcinom neznámého primárního zdroje metastazující do krčních uzlin?
- Stereotaktická radioterapie v léčbě časného stadia nemalobuněčného karcinomu plic
- Cirkulární RNA hsa-circ-0006203 – hsa-circ-0004872 jako nové biomarkery detekce karcinomu dutiny ústní
- Léčba dospělých pacientů s akutní lymfoblastovou leukemií v České republice v letech 2007–2020
- Alveolárny sarkóm mäkkých tkanív u dieťaťa – opis prípadu
- Raritní případ uroteliálního karcinomu metastazujícího do stěny žlučníku s projevy akutní cholecystitidy
- Aktuality z odborného tisku
- Nová možnost kombinované léčby pro pacienty s metastatickým renální karcinomem v 1. linii léčby: lenvatinib s pembrolizumabem – výsledky studie CLEAR
- Jubilant doc. MUDr. Bohuslav Konopásek, CSc.
- Životní jubileum první dámy české onkologie
- Spomienka na akademika MUDr. Viliama Ujházyho, DrSc. (1926–2023)
- Klinická onkologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Transformace indolentního folikulární lymfomu v difuzní velkobuněčný B-lymfom – molekulární podstata „nádorové agresivity“
- Léčba dospělých pacientů s akutní lymfoblastovou leukemií v České republice v letech 2007–2020
- Stereotaktická radioterapie v léčbě časného stadia nemalobuněčného karcinomu plic
- Využití botulotoxinu při léčbě nežádoucích účinků radioterapie
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



