-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Vybrané choroby ledvin v těhotenství
Selected renal diseases in pregnancy
Kidney disease and pregnancy may exist in two general settings:
acute kidney injury that develops during pregnancy, and chronic kidney disease that predates conception. In the first trimester of pregnancy, acute kidney injury is most often the result of hyperemesis gravidarum, ectopic pregnancy, or miscarriage. In the second and third trimesters, the common causes of acute kidney injury are severe preeclampsia; haemolysis, elevated liver enzymes and low platelets syndrome; acute fatty liver of pregnancy; and thrombotic microangiopathies, which may pose diagnostic challenges to the clinician. Cortical necrosis and obstructive uropathy are other conditions that may lead to acute kidney injury in these trimesters. Early recognition of these disorders is essential to timely treatment and can improve both maternal and foetal outcomes. In women with preexisting kidney disease, mainly including chronic glomerulonephritis diabetic nephropathy and lupus nephritis, pregnancy‑related outcomes depend upon the degree of renal impairment, the amount of proteinuria, and the severity of hypertension. In the majority of patients with mild renal function impairment, and well‑controlled blood pressure, pregnancy is usually successful and does not alter the natural course of maternal renal disease. Conversely, fetal outcome and long‑term maternal renal function might be seriously threatened by pregnancy in women with moderate or severe renal function impairment. During the last few years, advances in our knowledge about the interaction of pregnancy and renal function has resulted in the improvement of foetal outcome in patients with chronic renal failure and also in the management of pregnant women with end‑stage renal disease (ESRD) maintained on dialysis. Neonatal and maternal outcomes in pregnancies among renal transplant patients are generally good if the mother has normal baseline allograft function. Common renally active drugs and immunosuppressant medications must be prescribed, with special considerations in pregnant patients.Keywords:
chronic kidney disease – acute renal injury – pregnancy – preeclampsia – dialysis – transplantation – proteinuria – hypertension
Autoři: O. Zakiyanov 1,2; J. Vachek 1,3; V. Tesař 1
Působiště autorů: Klinika nefrologie VFN a 1. LF UK v Praze 1; Ústav lékařské biochemie a laboratorní diagnostiky VFN a 1. LF UK v Praze 2; Farmakologický ústav 1. LF UK v Praze 3
Vyšlo v časopise: Kardiol Rev Int Med 2014, 16(1): 67-73
Kategorie: Interní medicína
Souhrn
Nemoci ledvin mohou graviditě předcházet nebo se manifestují až v jejím průběhu. V prvním trimestru vzniká akutní poškození ledvin nejčastěji následkem hyperemesis gravidarum, ektopické gravidity nebo potratu. Ve druhém a třetím trimestru jsou nejčastějšími příčinami akutního poškození ledvin těžké formy preeklampsie, HELLP syndrom, akutní těhotenská steatóza a trombotická mikroangiopatie. Stanovení diagnózy u těchto stavů je často problematické. Kortikální nekróza a obstrukční uropatie mohou též vést k akutnímu poškození ledvin. Včasné rozpoznání těchto poruch je nezbytnou podmínkou včasného zahájení léčby a zlepšení prognózy těhotné ženy i plodu. U žen s preexistujícím onemocněním ledvin, zejména chronickou glomerulonefritidou, diabetickou nefropatií a lupusovou nefritidou, závisí výsledky těhotenství i na stupni stupni poškození ledvin, tíži proteinurie a závažnosti hypertenze. U většiny pacientek s mírnou poruchou funkce ledvin a dobrou korekcí hypertenze je prognóza těhotenství i renálních funkcí pacientky dobrá. U nemocných se středně těžkou nebo těžkou poruchou funkce ledvin jsou však výsledky těhotenství horší. V posledních letech naše znalosti v problematice interakce renálních funkcí a gravidity výrazně pokročily, což umožnilo zlepšení výsledků těhotenství u nefrologických pacientek. Přibývají případy úspěšných těhotenství u pacientek v konečném stadiu selhání ledvin, na dialyzační léčbě a po transplantaci ledviny. U těhotných pacientek po transplantaci ledviny je nutné speciální plánování farmakoterapie.
Klíčová slova:
chronické onemocnění ledvin – akutní poškození ledvin – těhotenství – preeklampsie – dialýza – transplantace – proteinurie – hypertenzeÚvod
V těhotenství dochází k očekávaným anatomickým a fyziologickým změnám ledvin. Mezi nejdůležitější komplikace, které se mohou manifestovat v těhotenství, patří hypertenze a proteinurie. Tyto komplikace mohou předcházet rozvoji preeklampsie a jiných závažných onemocnění. Ženy s onemocněním ledvin mohou mít o něco vyšší riziko komplikací jak pro matku, tak i pro plod, ale ve většině případů jsou těhotenství úspěšná. Závažnější onemocnění ledvin je spojováno s nižší fertilitou a vyšším výskytem zdravotních komplikací.
Fyziologické změny ledvin během těhotenství
Anatomické změny
- patrné již v I. trimestru
- do 4. měsíce po porodu
Velikost ledvin se zvětšuje o 1 – 1,5 cm během těhotenství jako odpověď na zvýšení průtoku krve ledvinami a též nárůstu objemu intersticia. Dilatace ureteru, ledvinných kalichů a ledvinných pánviček jsou na vrub hormonálních účinků progesteronu během gravidity a zároveň mechanické obstrukce zvětšenou dělohou. Tato fyziologická hydronefróza ztěžuje správné odlišení od patologické obstrukce močových cest a bývá více vyjádřena na pravé straně. Takto zvětšená kapacitní schopnost kalichopánvičkového systému hromadí o 200 – 300 ml moči více, což pak může mít dopad na nepřesný údaj o množství moči během 24hodinového sběru a navíc predisponovat ascendentním infekcím močovýchcest.
Fyziologické a hemodynamické změny
Pro těhotenství jsou charakteristické podstatné změny systémové a ledvinné hemodynamiky. Srdeční výdej se k 24. týdnu gravidity zvyšuje o 50 % v důsledku 10 – 20% zvýšení srdeční frekvence a vypuzeného systolického objemu. Objem plazmy se zvyšuje v průměru o 1,25 litru. Systémový krevní tlak se však obvykle snižuje v průměru o 10 mm Hg kvůli systémové vazodilataci. Průtok plazmy ledvinou se zvyšuje o 70 % a glomerulární filtrace (GFR) o 50 % (s maximem v 36. týdnu) v důsledku zvětšení srdečního výdeje a objemu plazmy ve spojení s renální vazodilatací. Hladiny sérového kreatininu posléze klesají z hodnot před těhotenstvím. Zvýšení GFR a zvýšený metabolizmus vazopresinu při graviditě vedou k častému močení. Během těhotenství narůstá množství celkové vody v organizmu z 6 na 8 litrů (s maximem ve III. trimestru), což vede k retenci více než 900 mmol/ l soli. Tento nárůst objemu plazmy je odpovědný za „fyziologickou anemii těhotenství“. U těhotných žen pozorujeme pokles osmolality přibližně o10 mOsm/ kg, tj. cca na 270 – 275 mOsm/ kg. Nepřiměřená sekrece ADH má za následek pokles koncentrace sodíku v průměru o 5 mmol/ l. Hladina aldosteronu se významně zvyšuje, což pomáhá udržet arteriální tlak a stimuluje retenci sodíku v terénu systémové vazodilatace. Snížená zpětná tubulární resorpce glukózy může u některých žen způsobovat glykosurii. Stimulace centrálních respiračních receptorů progesteronem způsobuje mírnou respiratorní alkalózu (průměrná parciální tenze CO2 je kolem 30 mm Hg a kompenzační pokles sérového bikarbonátu je na 20 – 22 mmol/ l). Exkrece proteinu moči je během těhotenství zvýšena, ale proteinurie nad 300 mg je pokládána za patologickou. Renální exkrece vápníku, kyseliny močové a glukózy je také zvýšena, ale nedosahuje patologických hodnot [1].
Hypertenzní nemoci v těhotenství
S hypertenzí se setkáváme u 8 – 10 % všech těhotenství a představuje nejčastější patologický nález. Těhotenství komplikovaná hypertenzí mají zvýšené riziko pre/ eklampsie, abrupce placenty, předčasného porodu, nitroděložní růstové retardace a odumření plodu v druhém trimestru gravidity.
Hypertenze v těhotenství se diferenciálně diagnosticky rozlišuje:
- chronická hypertenze – hypertenze známá již v době před početím diagnostikována před 20. týdnem gestace nebo která trvá více než 12 týdnů po porodu
- preeklampsie – hypertenze a proteinurie po 20. týdnu gestace
- gestační hypertenze – hypertenze, která se objevila po 20. týdnu gestace, bez proteinurie
- preeklampsie superponována na chronickou hypertenzi – obvykle zhoršuje již přítomnou hypertenzi a novou proteinurii. Tento typ hypertenze lze někdy obtížně odlišit od chronické hypertenze
Chronická hypertenze v těhotenství
Většina těhotných žen s chronickou hypertenzí má primární hypertenzi, průběh těhotenství je obvykle nekomplikovaný a těhotenství končí úspěšně. Zřídka je ale zvýšení krevního tlaku sekundární. Příčinou může být feochromocytom, Cushingův syndrom, stenóza renálních arterií a primární onemocnění ledvin [2]. Feochromocytom se velmi vzácně může projevit poprvé během těhotenství a může vyústit letálně, zvláště není‑li včas rozpoznán. Pokud je diagnostikován, může být úspěšně léčen chirurgicky nebo i medikamentózně (léčba alfa‑blokátory), v závislosti na stadiu těhotenství [2]. Cushingův syndrom je spojován s exacerbací hypertenze během těhotenství a vyšším zdravotním rizikem pro plod. Angioplastika i implantace stentů byly úspěšně použity pro léčbu stenózy renální arterie u gravidních žen [3].
Cílový krevní tlak pro těhotnou ženu je v případě nekomplikované hypertenze 130 – 150 mm Hg systolického tlaku a 80 – 100 mg Hg diastolického tlaku. Těsná kontrola tlaku pacientek s hypertenzí nezlepšuje celkovou prognózu a je spojována se zpomalením intrauterinního růstu plodu. Léčba těžké hypertenze (systolický tlak > 160 mm Hg nebo diastolického > 105 mm Hg) je nutná vzhledem ke zvýšenému riziku orgánového postižení včetně intracerebrálního krvácení. Ženy se zdravotním rizikem chronického onemocnění jako diabetes mellitus, hyperlipidemie, chronické onemocnění ledvin, městnavé kardiální selhávání, dále pak s anamnézou prodělaného iktu a spontánních potratů či ženy ve věku > 40 let mohou profitovat z těsné kontroly krevního tlaku. U žen s chronickým onemocněním již v časném těhotenství je nutné provést screeningová vyšetření včetně močového sedimentu, kultivace moči, biochemického vyšetření séra a EKG. Dále jsou nutné časté kontroly specialistů s cílem těsné kontroly tenze, proteinurie a sonografické kontroly vývoje plodu. Většina těhotenství žen s hypertenzí prosperuje – hypertoničky by měly porodit do termínu porodu.
Léčba těžké hypertenze při těhotenství
Léčbu obvykle zahájíme centrálně působícími alfa - 2 - agonisty adrenergních receptorů (alfa - methyldopa), dále je možné užít beta‑blokátory a stále častěji se užívají blokátory kalciového kanálu (např. nitrendipin, amlodipin). V léčbě hypertenzní krize se uplatňuje zejména labetalol, diuretika, urapidil [4].
Použití thiazidových diuretik se nedoporučuje z důvodu rizika volumové deplece, ale v léčbě lze pokračovat, pokud byla zahájena již před těhotenstvím. ACEI a sartany by se neměly v těhotenství používat [4].
Gestační hypertenze
Těhotné ženy s krevním tlakem rovným nebo vyšším než 140/ 90 mm Hg bez proteinurie po 20. týdnu, jejichž tlak byl před otěhotněním normální, splňují kritéria gestační hypertenze. Příčiny mohou být různé. Ženy s rodinnou anamnézou těžké hypertenze jsou v prvním a druhém trimestru obvykle normotenzní, ale ke konci třetího trimestru se krevní tlak zvyšuje a dosahuje vyšších hodnot ve srovnání s obdobím před těhotenstvím. Zvýšení tlaku není u gestační hypertenze doprovázeno proteinurií a hladina kyseliny močové nebývá zvýšena. Existují doklady o tom, že přechodná hypertenze během těhotenství predisponuje ke vzniku hypertenze v pozdějším věku, podobně jako vyšší glykemie během gestace může vést k rozvoji diabetu v pozdějším věku.
Určitá část žen (přibližně 30 %) s gestační hypertenzí má časné stadium preeklampsie bez objevení se proteinurie. Tato skupina pacientek jeví určité známky glomerulární endoteliózy v renální biopsii [5]. Někdy může být zvýšení tlaku zapříčiněno psychiatrickým onemocněním – anxiózní poruchou nebo panickou atakou. Velmi vzácně je přítomna mutace vedoucí k aktivaci mineralokortikoidního receptoru, který je aktivován slabým mineralokortikoidním účinkem progesteronu [6]. Tento stav se projeví jako tzv. salt ‑ sensitive hypertension, je provázenen hypokalemií při prakticky neměřitelných hladinách aldosteronu, zvláště při maximálním nárůstu hladin progesteronu. Podávání většího množství fyziologického roztoku během císařského řezu může někdy vyústit v poporodní hypertenzi a otoky, které vymizí během několika dnů po vyloučení solní nálože. Vyšší hodnoty krevního tlaku se ve většině případů upraví do 42. dne po porodu.
Preeklampsie
Preeklampsie komplikuje 3 – 5 % těhotenství a je hlavní příčinou nemocnosti a úmrtnosti plodu a matky a také vyšší maternální mortality. Hlavní projevy preeklampsie zahrnují hypertenzi s tlaky 140/ 90 mm Hg a výše a proteinurii po 20. týdnu gravidity obvykle spojovanou s otoky a hyperurikemií (ACOG practice bulletin). Pokud tento syndrom progreduje k epileptickým záchvatům, nazývá se eklampsie [7]. Rizikové faktory eklampsie uvádí tab. 1.
Tab. 1. Rizikové faktory eklampsie. 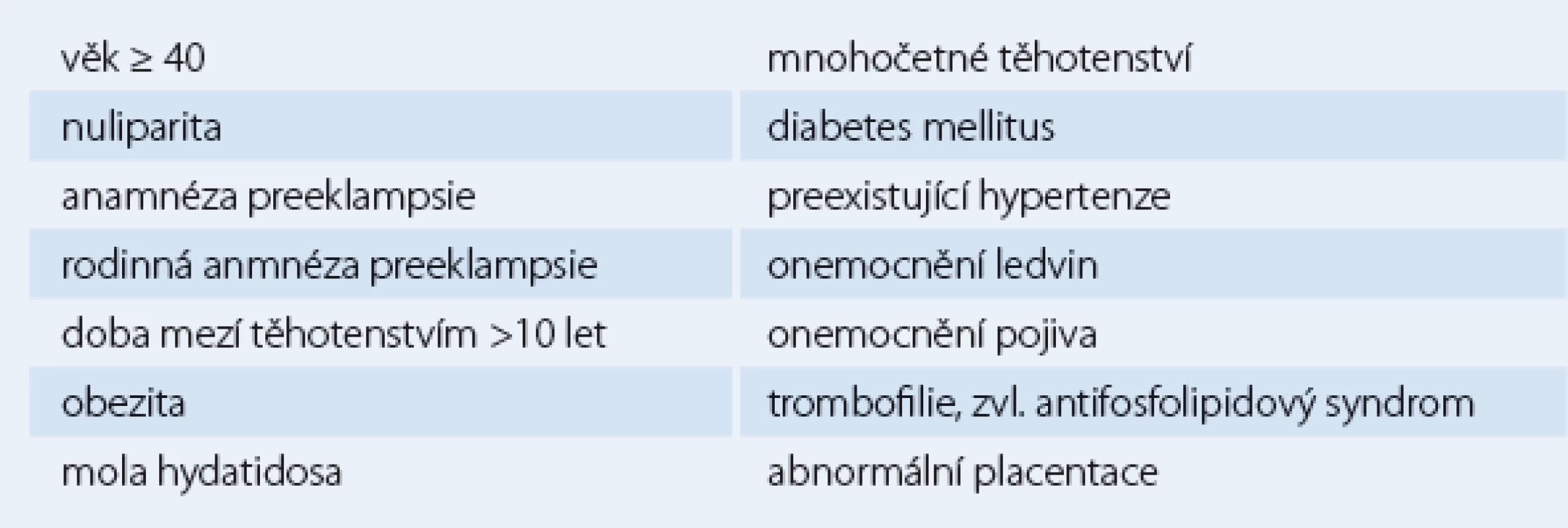
Preeklampsie vzniká jako důsledek abnormální placentace, která vede k endoteliální dysfunkci. Placentace zahrnuje invazi erytroblastů do myometria a spirálních arterií, což vede k dilatovaným, rozvětveným arteriím a sdílené materno ‑ fetální cirkulaci. Při preeklampsii není invaze cytotrofoblastů kompletní, spirální arterie zůstávají v konstrikci a uteroplacentární cirkulace je snížena. V patogenezi se u preeklamptických žen zřejmě uplatňuje zvýšená produkce sFlt ‑ 1 (solubilní fms‑like tyrosine kinasy 1) v placentě [8]. sFlt ‑ 1 je potentním cirkulujícím antagonistou vaskulárního růstového faktoru (VEGF) a placentálního růstového faktoru (PlGF), které jsou důležité pro normální funkci placenty.
Při preeklampsii dochází k:
- systémové vazokonstrikci vedoucí k hypertenzi a orgánové hypoperfuzi
- zvýšené vaskulární propustnosti vedoucí k proteinurii a otoku plic
- aktivaci krevních destiček a koagulační kaskády, což vede ke koagulopatii
- primárním nálezem v ledvinách jsou oteklé, hypertrofované endoteliální buňky, tzv. glomerulární kapilární endotelióza
- v játrech se vyskytují periportální hemoragie, infarkty a trombózy
Klinický obraz
Preeklampsie se obvykle projeví po 32. týdnu gestace, může se však objevit dříve u žen s preexistující hypertenzí nebo s renálním onemocněním. Vzácně se může vyvinout během porodu nebo časně po porodu. Iniciální symptomy preeklampsie mohou být nespecifické. Zvýšení krevního tlaku může být prvním příznakem preeklampsie. Elevace krevního tlaku může začít v druhém trimestru, hodnoty převyšující 140/ 90 mm Hg se typicky vyskytují ve třetím trimestru. S progresí nemoci u mnoha pacientek dochází k náhlému nárůstu tělesné hmotnosti a rozvoji otoků končetin a obličeje (tab. 2). Při bolesti v epigastriu v druhé polovině gravidity musí být vždy pomyšleno na počínající HELLP syndrom.
Tab. 2. Typy nálezů při preklampsii. 
Glomerulární filtrace během těhotenství roste, ale vazokonstrikce při preeklampsii způsobuje pokles clearance kreatininu. Nízká hladina kyseliny močové se při preeklampsii v těhotenství zvyšuje. Proteinurie se pohybuje od mírné až po nefrotickou. Dysfunkce jater se může projevit mírnou elevací jaterních enzymů až po steatózu jater.
HELLP syndrom
Některé hematologické a hepatické abnormality při preeklampsii se sdružují v HELLP syndrom: hemolýza, elevace jaterních enzymů a nízká hladina trombocytů. HELLP syndrom je závažná komplikace s významnou mortalitou a morbiditou. Preeklampsie může postihnout nervovou soustavu s bolestmi hlavy, nervozitou a zvýšenými hlubokými reflexy. Tyto nálezy mohou být následovány záchvaty, které dále prohlubují závažný stav. Nejzávažnější komplikací je intracerebrální hemoragie, která je hlavní příčinou mateřské úmrtnosti při preeklampsii [7].
Léčba
Praktický postup při terapii hypertenze v graviditě: nefarmakologická opatření zahrnují přiměřené omezení fyzické zátěže, pravidelné kontroly TK, selfmonitoring těhotné. Farmakoterapie je indikována při diastolickém TK 95 – 100 mm Hg. Cílovou diastolickou hodnotou je u lehké preeklampsie 90 mm Hg, u těžké 100 mm Hg (ne méně než 95 mm Hg). Při dalším poklesu diastolického TK dochází ke snížené perfuzi v uteroplacentárním řečišti a k následné hypoxii plodu. Terapie se začíná s metyldopou, pokud nedojde k dostatečnému snížení TK, přidává se do kombinace amlodipin, možný je i dříve více používaný metoprolol. K i.v. terapii se užívá labetalol, který je dostupný v rámci specifického léčebného programu, možno je užít i dihydralazin nebo urapidil [4].
U žen s nově diagnostikovanou hypertenzí a proteinurií po 20. týdnu stanovujeme dg. preeklampsie. Ženy s mírnou preeklampsií (TK 140/ 90 – 159/ 109 mm Hg, proteinurie 0,3 – 5,0 g za 24 hodin) je nutné pozorně sledovat s častými kontrolami laboratoře a stavu plodu. Pacientky lze sledovat ambulantně, ale často při objevení se neurologických příznaků, renálního selhávání, nekontrolované hypertenze, známkách HELLP syndromu nebo při ohrožení plodu je nutná hospitalizace. Ženy s těžkou preeklampsií (TK nad 160/ 110 mm Hg, proteinurie nad 5 g za 24 hodin, oligurie pod 400 m/ 24 hodin a typické klinické příznaky) vyžadují okamžitou hospitalizaci. Obvykle je léčba zahájena akutní antihypertenzní terapií (hydrazinoftalaziny, labetalol), kortikosteroidy (betamethasonum 7 mg, v dávce 14 mg i. m./ 24 hodin, ve dvou následujících dávkách během 24 hodin) ke snížení rizika syndromu dechové tísně u novorozence (mezi 24 + 0 až 34 + 6 týdnem gestace), magnesium sulfuricum a benzodiazepiny k prevenci křečí. Pacientky v ukončeném 34. týdnu gestace je nutné připravit k porodu. Několik studií [9] ukázalo, že předčasné ukončení těhotenství pro preeklampsii v 30. – 34. týdnu je spojováno s lepším perinatálním přežíváním, snížením nutnosti hospitalizace na jednotkách intenzivní péče, snížením neonatálních komplikací a zvýšením porodní hmotnosti bez rozdílu v mateřské úmrtnosti. Při těžkém a progresivním průběhu preeklampsie je jediným východiskem porod, a tím i definitivní vyléčení [10].
Některé z absolutních indikací neodkladného porodu jsou:
- těžká preeklampsie při adekvátní léčbě
- hrozící eklampsie
- HELLP syndrom
- abrupce placenty
- akutní či chronická hypoxie plodu
- prohlubující se známky intrauterinní retardace plodu
Akutní renální selhání v těhotenství
Akutní renální selhání během těhotenství, ačkoli je vzácné, je zcela zásadní z hlediska stanovení diagnózy i pro léčbu. Na začátku těhotenství je akutní renální selhání nejčastěji prerenální etiologie z důvodu hyperemesis gravidarum nebo v důsledku akutní tubulární nekrózy po septickém potratu. Při pokročilém těhotenství jsou nejčastějšími příčinami akutního renálního selhání trombotická trombocytopenická purpura, hemolyticko‑uremický syndrom, akutní těhotenská steatóza, renální kortikální nekróza a obstrukční uropatie [11]. Tab. 3 ukazuje klíčové diagnostické postupy v diferenciální diagnostice některých příčin akutního renálního selhání.
Tab. 3. Diferenciální diagnostika akutního renálního selhání. 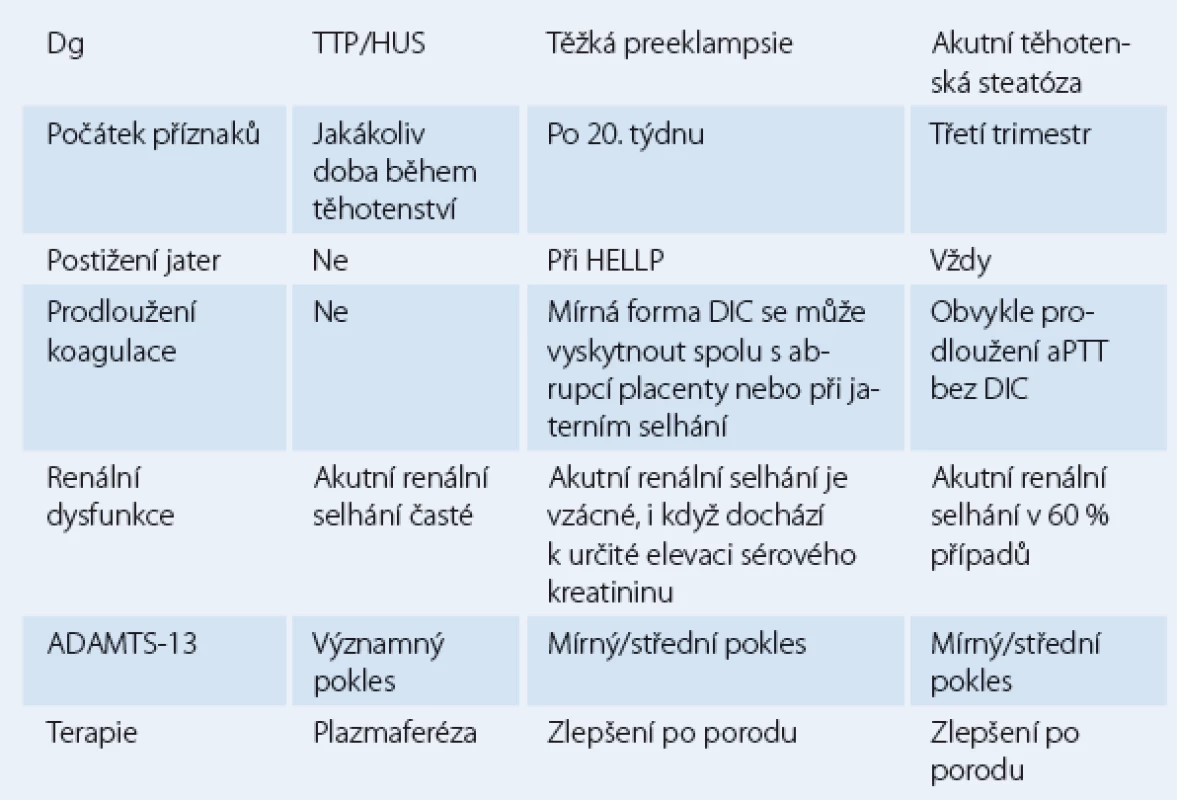
Akutní těhotenská steatóza
Akutní těhotenská steatóza je vzácné onemocnění charakterizované nechutenstvím, žloutenkou, bolestmi břicha, nevolností a zvracením. Pacientky jsou často hypotenzní. V patogenezi se uplatňuje mikrovezikulární tuková infiltrace hepatocytů, která může souviset s mitochondriální poruchou beta ‑ oxidace mastných kyselin. V laboratoři pozorujeme hyperbilirubinemii, mírnou elevaci aspartátaminotransferázy (AST) a alaninaminotransferázy (ALT), často doprovázené hypoglykemií, hypofibrinemií a prodloužením aPTT. Akutní poškození ledvin se vyskytuje v 60 % případů. Přibližně 50 % nemocných v předchorobí má preeklampsii, což může ztěžovat stanovení správné diagnózy. Léčba spočívá v ukončení gravidity dle závažnosti stavu a podpůrné terapii. Těžké postižení jater, někdy i fulminantní selhání, lze zvládnout jen transplantací jater [12].
Renální kortikální nekróza
Renální kortikální nekróza je příčinou akutního renálního selhání jen zřídka a je spíše spojována s komplikacemi těhotenství jako abrupce placenty, embolie plodovou vodou, placenta praevia, těžká preeklampsie nebo retence mrtvého plodu. Hlavními spouštěči tohoto onemocnění jsou diseminovaná intravaskulární koagulopatie a těžká renální ischemie. Pozorujeme bolesti v boku, makrohematurii, oligo/ anurii a hypotenzi. O kortikální nekróze je nutno uvažovat, pokud je obnova renálních funkcí opožděná a pomalá. Sono obraz a CT prokáží hypoechogenní hypodenzní kortex ledvin. Někdy je nutné diagnózu potvrdit renální biopsií nebo arteriografií. Prognóza je špatná. Přibližně 20 – 40 % nemocných, u kterých bylo zahájeno dialyzační léčení, se zotaví, ale s trvající závislostí na dialýze [13,14].
Obstrukční uropatie
Vzhledem k relaxaci ureterů s následnou hydronefrózou v těhotenství je neobvyklé, aby obstrukční uropatie způsobila renální selhání. Určitým vodítkem je postižení levé ledviny obstrukcí, protože ledvina na pravé straně je více ovlivněna fyziologickou hydronefrózou, a dále nález oligurie nebo anurie. Příčinou obstrukce může být zvětšená děloha, polyhydramnion, močový konkrement nebo myomatóza dělohy. Funkce ledvin se může zlepšit při poloze na boku. Obstrukční uropatie se zlepší po porodu, někdy je nutno zavést ureterální stenty k zajištění derivace moči [13].
Proteinurie v těhotenství
Během těhotenství dochází ke zvýšení GFR a permeability kapilár, což vede k mírné proteinurii (~ 200 mg/ den). Pokud proteinurie přesáhne tuto hodnotu, existují tři důležité eventuality vysvětlení – zhoršení preexistujícího chronického renálního onemocnění, hrozící preeklampsie nebo de novo onemocnění ledvin během těhotenství. Léčba proteinurie závisí na příčině a množství proteinurie. Nejčastější příčiny onemocnění ledvin zahrnují stavy, které se často vyskytují u netěhotných žen stejného věku včetně fokálně segmentální glomerulosklerózy (FSGS), membranózní nefropatie, IgA nefropatie a vrozené příčiny [15,16]. Diagnóza je obvykle stanovena od momentu prvního vyšetření moči až po 20. týden gestace. Pacientky se systémovým lupus erythematodes obvykle mají další symptomy celkového onemocnění. Některé diagnózy nelze přesně určit v poporodním období. Samotná proteinurie neovlivňuje prognózu těhotenství a vývoj plodu [17,18].
Léčba
Léčba otoků by měla začít omezením soli v dietě a klidem na lůžku. Při rezistentních otocích lze zvážit opatrné použití diuretik s pečlivou monitorací diurézy (furosemid se nedoporučuje pro nepříznivý vliv na placentární perfuzi; indikován je pouze u hrozícího či vyvinutého plicního edému nebo u edému mozku a je využíván především postnatálně). Biopsii ledvin lze zvážit při náhlém zhoršení funkce ledvin bez jiného vysvětlení (zvláště při aktivním močovém sedimentu) a také v případech, kdy diagnóza preeklampsie je pochybná nebo při symptomatickém nefrotickém syndromu. Biopsie by neměla být prováděna po 32. týdnu gestace [19,20].
Nefrolitiáza v těhotenství
Incidence nefrolitiázy u těhotných je častější než u netěhotných žen. Konkrementy obvykle obsahují vápník. Litiáza obvykle postihuje uretery, většinou distální ureter. Klinické příznaky zahrnují bolesti v bocích, hematurii a dysurii. Léčba je symptomatická, většina konkrementů odejde spontánně. Je indikována hydratace a spasmolyticko‑analgetická terapie.
I když většina konkrementů odejde spontánně, obstrukce může vyústit v hydronefrózu nebo i pyonefros a může se komplikovat renálním selháním. V těchto případech je indikována instrumentální extrakce konkrementů. Litotrypse se obvykle neprovádí. Cystoskopické nebo ureteroskopické odstranění konkrementů je metodou volby. Někdy je nutné založení nefrostomie k zajištění derivace moči.
Preexistující chronické onemocnění ledvin
Dříve se chronické onemocnění ledvin (CKD) považovalo za neslučitelné s úspěšným těhotenstvím, prognóza žen s CKD se však neustále zlepšuje – jak pro matku, tak i pro dítě. Těhotenství u žen se zhoršující se funkcí ledvin je méně časté než v běžné populaci z důvodu vyššího výskytu amenorhey, anovulačního cyklu, sníženého libida z důvodu hyperprolaktinemie a změn v regulaci osy hypotalamus ‑ hypofýza. Z těchto důvodů se týká většina početí žen s mírnou renální insuficiencí s GFR > 50 ml/ min a hladinou kreatininu < 130 µmol/ l. Vývoj plodu není ovlivněn typem onemocnění ledvin. Hlavními příčinami horší prognózy jsou výrazné snížení renálních funkcí, nekontrolovaná hypertenze a velká proteinurie [21].
Jak lze očekávat, těhotenství u žen s mírnou renální insuficiencí (sérový kreatinin < 130 µmol/ l) prosperují lépe než u pacientek s vyšším stupněm renální insuficience. U většiny pacientek s mírnou renální insuficiencí můžeme pozorovat mírný pokles funkce s úpravou po porodu. U pacientek se střední renální insuficiencí (kreatinin 130 – 230 µmol/ l) nebo s pokročilou insuficiencí (kreatinin > 230 µmol/ l) může dojít ke značnému zhoršení renálních funkcí. Pacientky se střední významnou renální insuficiencí ve 2 – 33 % dospějí do konečného stadia renální insuficience. Pacientky s hladinou sérového kreatininu nad 180 µmol/ l mají horší prognózu. Relativně málo dat je k dispozici o těhotenství při pokročilé renální insuficienci z důvodu horší fertility. Renální funkce s GFR < 40 ml/ min a proteinurie > 1 g mají významně vyšší riziko komplikací během těhotenství a riziko deteriorace renálních funkcí.
Jak matka, tak i dítě nesou následky onemocnění ledvin. Mateřské komplikace zahrnují chronickou hypertenzi, zvýšené riziko preeklampsie, trvalé zhoršení renálních funkcí a zvýšení proteinurie. Fetální komplikace mohou vyústit v předčasný porod, retardaci růstu a celkové zvýšení mortality. Pacientky se střední a pokročilou renální insuficiencí mají mnohem vyšší procento předčasných porodů a retardace růstu, ale zachovávají příznivou pravděpodobnost narození živého dítěte. U žen s renálním onemocněním lze pravděpodobnost narození živého dítěte považovat za příznivou, v případě onemocnění ledvin s progresivním zhoršováním jejich funkce je však žádoucí těhotenství neodkládat.
Pro vedení žen s chronickým onemocněním ledvin jsou nutné:
- dobrá kontrola systémového krevního tlaku < 130/ 80 mm Hg
- časná detekce a léčba bakteriurie
- měsíční kontrola renálních funkcí těhotné ženy
- pečlivé sledování a časná diagnóza preeklampsie
- frekventní sledování viability plodu včetně častých ultrazvukových a jiných vyšetření
Systémový lupus erythematosus a těhotenství
Otázka vlivu těhotenství na flares (reaktivace) lupus je stále kontroverzní. Ženy v remisi trvající alespoň šest měsíců mají stejnou frekvenci relapsu během těhotenství jako netěhotné ženy. Riziko pro horší prognózu se zvyšuje při významné proteinurii, hypertenzi a renální dysfunkci a je srovnatelné s jinými onemocněními ledvin. Přítomnost antifosfolipidového syndromu je spojena s vyšším rizikem potratu, těžké hypertenze, retardace růstu plodu a trombotických komplikací pro matku. Všechny těhotné ženy s lupusem by měly být vyšetřeny na přítomnost antifosfolipidových protilátek a pokud jsou protilátky pozitivní, je indikováno preventivní podávání kyseliny acetylsalicylové. U žen s anamnézou trombóz je nutné zahájit léčbu heparinem, resp. LMWH. Děti žen s lupusem jsou ve vyšším riziku neonatálního lupusu, který je primární příčinou srdečních arytmií, resp. blokád. Ženy by měly být vyšetřeny i na přítomnost SSA a SSB protilátek. Ženám s lupusem, které si přejí otěhotnět, je doporučeno odložit početí alespoň šest měsíců od poslední aktivity (flare) choroby. V udržovací léčbě lze pokračovat nízkými dávkami steroidů. Jiné léky, které lze považovat za relativně bezpečné během těhotenství, jsou NSAID (cave vliv na fetální hemodynamiku v třetím trimestru!), antimalarika, glukokortikoidy, azathioprin, cyklosporin A [22].
Diagnóza a léčba
Lupusová nefritida se může objevit během těhotenství a mít stejné rysy jako u netěhotných žen. Je nutno odlišit ji od preeklampsie, jelikož obě onemocnění se mohou prezentovat trombocytopenií a též obě nemoci se mohou vyskytnout současně. Některými důležitými vodítky u lupusu jsou pozitivita antinukleárních protilátek, nízké hladiny komplementu a aktivního močového sedimentu. Medikamentózní terapie SLE v těhotenství zahrnuje glukokortikoidy (prednison nebo methylprednisolon), ze specifických imunosupresiv lze užít s opatrností azathioprin nebo – při normální renální funkci – cyklosporin A, kontraindikována nejsou ani antimalarika (chlorochin), různými studiemi nebylo poškození plodu po expozici chlorochinu prokázáno. Ostatní imunosupresíva jsou v době těhotenství problematická. Součástí celkové terapie jsou i další všeobecná opatření jako kompenzace arteriální hypertenze, ochrana před sluncem atd. [23].
Diabetická nefropatie
Diabetická nefropatie je frekventní příčinou onemocnění ledvin během těhotenství. Stejně jako u jiných onemocnění ledvin mají ženy s mírnou renální dysfunkcí nižší výskyt komplikací a nižší riziko progrese onemocnění. Albuminurie je spojována s větším výskytem komplikací. Obecně terapie spočívá v těsné kontrole systémového krevního tlaku < 140/ 90 mm Hg, je nutné ukončit terapii ACEI nebo sartany, nutná je dobrá kontrola glykemie ke snížení vzniku vrozených defektů [24,25].
Těhotenství a dialýza
Těhotenství u dialyzovaných pacientek je vzácné, vyskytuje se u 1,5 % dialyzovaných žen ve fertilním věku. Pravděpodobnost narození živého dítěte je kolem 50 %. Je doloženo již mnoho úspěšných těhotenství jak při peritoneální dialýze, tak i při hemodialýze. Velkou pozornost je nutné věnovat adekvátnosti dialyzační léčby a další terapie (tab. 4). Časné těhotenství je obtížné rozpoznat, protože beta hCG je u dialyzovaných nemocných arteficiálně zvýšené [26 – 28].
Tab. 4. Obecné principy léčby těhotných dialyzovaných žen. 
Těhotenství po transplantaci ledviny
K prevenci neplánované gravidity je nutné ženy fertilního věku poučit, že může dojít k obnovení menstruačního cyklu již cca jeden měsíc po transplantaci ledviny. Obecně je doporučováno počkat s početím cca jeden, lépe dva roky po transplantaci. Tato doba dovoluje provádět odpovídající potransplantační monitoraci a úpravu léčby a snižuje riziko cytomegalovirové infekce během gravidity. Všechna těhotenství u transplantovaných žen jsou považována za riziková a je nutné je pečlivě monitorovat. Před plánovaným těhotenstvím by hodnoty sérového kreatininu měly být stabilní mezi 130 – 180 µmol/ l, krevní tlak kontrolován s minimálním množstvím léků, proteinurii stabilně < 1 g/ den a neměly by být přítomny epizody rejekce nebo jiných komplikaci v souvislosti s transplantací. Riziko zhoršení funkce štěpu se zvětšuje při hodnotách kreatinu před početím > 130 µmol/ l [29,30].
Imunosupresiva
Obecně nesou kalcineurinové inhibitory a azathioprin riziko růstové retardace, ale v těhotenství jsou považovány za přijatelné stejně jako udržovací dávka prednisonu. Hladiny kalcineurinových inhibitorů klesají během těhotenství z důvodu zvýšení distribučního objemu bez nutnosti zvyšování dávek léku. Léčba mykofenolátem a sirolimem by měla být ukončena 6 – 8 týdnu před početím. Dále je nutné přerušit podávání ACEI a kotrimoxazolu. Kojení je při určitých pravidlech možné [4].
Komplikace
Při přijatelné renální funkci klesá sérový kreatinin zpočátku o 20 – 30 %, v pokročilém těhotenství opět mírně vzroste. Proteinurie se může zvýšit, ale většinou se navrátí na předchozí úroveň při stabilní funkci štěpu. Hodnoty krevního tlaku by měly být srovnatelné s hodnotami v obecné populaci, je nutné brát v potaz též hodnoty tlaku před těhotenstvím. Dysfunkci graftu je nutné okamžitě přešetřit, event. i provést biopsii štěpu. Předčasný porod a nízká porodní hmotnost při těhotenství u transplantovaných je častější. Vliv dlouhodobé expozice imunosupresivních léků na dělohu není zcela znám. Přesto těhotenství jsou i u transplantovaných úspěšná a komplikace jsou srovnatelné s výskytem u netransplantované zdravé populace. Proto je nutné při příznivých podmínkách usilovat o udržení těhotenství [31].
Doručeno do redakce 25. 1. 2014
Přijato po recenzi 4. 2. 2014
MU Dr. PhDr. Oskar Zakiyanov
www.vfn.cz
zoskar@post.cz
Zdroje
1. Lindheimer MD, August P. Aldosterone, maternal volume status and healthy pregnancies: a cycle of differing views. Nephrol Dial Transplant 2009; 24 : 1712 – 1714. doi: 10.1093/ ndt/ gfp093.
2. Lindheimer MD, Katz AI. Hypertension in pregnancy: advances and controversies. Clin Nephrol 1991; 36 : 166 – 173.
3. Lindheimer MD, Davison JM, Katz Al. The kidney and hypertension in pregnancy: twenty exciting years. Semin Nephrol 2001; 21 : 173 – 189.
4. Vachek J, Tesař V, Zakiyanov O et al. Farmakoterapie v těhotenství a při kojení. Praha: Maxdorf; 2013.
5. Strevens H, Wide ‑ Swensson D, Hansen A et al. Glomerular endotheliosis in normal pregnancy and pre‑eclampsia. BJOG 2003; 110 : 831 – 836.
6. Geller DS, Farhi A, Pinkerton N et al. Activating mineralocorticoid receptor mutation in hypertension exacerbated by pregnancy. Science 2000; 289 : 119 – 123.
7. Lindheimer MD, Katz AI. Preeclampsia: pathophysiology, diagnosis, and management. Annu Rev Med 1989; 40 : 233 – 250.
8. Maynard SE, Min JY, Merchan J et al. Excess placental soluble fms‑like tyrosine kinase 1 (sFlt1) may contribute to endothelial dysfunction, hypertension, and proteinuria in preeclampsia. J Clin Invest 2003; 111 : 649 – 658.
9. Odendaal HJ, Pattinson RC, Bam R et al. Aggressive or expectant management for patients with severe preeclampsia between 28 – 34 weeks' gestation: a randomized controlled trial. Obstet Gynecol 1990; 76 : 1070 – 1075.
10. Doporučené postupy v perinatologii. Dostupné z: http:/ / lekari.porodnice.cz/ doporucene ‑ postupy ‑ v ‑ perinatologii. [online].
11. Davison JM, Katz AI, Lindheimer MD. Kidney disease and pregnancy: obstetric outcome and long‑term renal prognosis. Clin Perinatol 1985; 12 : 497 – 519.
12. Minakami H, Morikawa M, Yamada T et al. Differentiation of acute fatty liver of pregnancy from syndrome of hemolysis, elevated liver enzymes and low platelet counts. J Obstet Gynaecol Res 2014. doi: 10.1111/ jog.12282.
13. Gyamlani G, Geraci SA. Kidney disease in pregnancy: (Women's Health Series). South Med J 2013; 106 : 519 – 525.
14. Nwoko R, Plecas D, Garovic VD. Acute kidney injury in the pregnant patient. Clin Nephrol 2012; 78 : 478 – 486.
15. Lo JO, Kerns E, Rueda J et al. Minimal change disease in pregnancy. J Matern Fetal Neonatal Med 2013.
16. Aoshima Y, Iyoda M, Nakazawa A et al. Membranous nephropathy that first presented in pregnancy. Intern Med 2013; 52 : 1949 – 1952.
17. Saxena I, Kapoor S, Gupta RC. Detection of proteinuria in pregnancy: comparison of qualitative tests for proteins and dipsticks with urinary protein creatinine index. J Clin Diagn Res 2013; 7 : 1846 – 1848.
18. Yamada T, Kojima T, Akaishi R et al. Problems in methods for the detection of significant proteinuria in pregnancy. J Obstet Gynaecol Res 2014; 40 : 161 – 166. doi: 10.1111/ jog.12148.
19. Kandukurti K, Sun J, Venuto R. Multiple pathologies in the kidney biopsy of a recently pregnant woman. Case Rep Nephrol Urol 2013; 3 : 9 – 15. doi: 10.1159/ 000346862.
20. Piccoli GB, Daidola G, Attini R et al. Kidney biopsy in pregnancy: evidence for counselling? A systematic narrative review. BJOG 2013; 120 : 412 – 427. doi: 10.1111/ 1471 – 0528.12111.
21. Vellanki K. Pregnancy in chronic kidney disease. Adv Chronic Kidney Dis 2013; 20 : 223 – 228. doi: 10.1053/ j.ackd.2013.02.001.
22. Peart E, Clowse ME. Systemic lupus erythematosus and pregnancy outcomes: an update and review of the literature. Curr Opin Rheumatol 2014; 26 : 118 – 123. doi: 10.1097/ BOR.0000000000000030.
23. Lateef A, Petri M. Managing lupus patients during pregnancy. Best Pract Res Clin Rheumatol 2013; 27 : 435 – 447. doi: 10.1016/ j.berh.2013.07.005.
24. Piccoli GB, Clari R, Ghiotto S et al. Type 1 diabetes, diabetic nephropathy, and pregnancy: a systematic review and meta‑study. Rev Diabet Stud 2013; 10 : 6 – 26. doi: 10.1900/ RDS.2013.10.6.
25. Damm JA, Asbjörnsdóttir B, Callesen NF et al. Diabetic nephropathy and microalbuminuria in pregnant women with type 1 and type 2 diabetes: prevalence, antihypertensive strategy, and pregnancy outcome. Diabetes Care 2013; 36 : 3489 – 3494. doi: 10.2337/ dc13 – 1031.
26. Bili E, Tsolakidis D, Stangou S et al. Pregnancy management and outcome in women with chronic kidney disease. Hippokratia 2013; 17 : 163 – 168.
27. Sivasuthan G, Dahwa R, John GT et al. Dialysis and pregnancy in end stage kidney disease associated with lupus nephritis. Case Rep Med 2013; 2013 : 923581. doi: 10.1155/ 2013/ 923581.
28. Jesudason S, Grace BS, McDonald SP. Pregnancy outcomes according to dialysis commencing before or after conception in women with ESRD. Clin J Am Soc Nephrol 2014; 9 : 143 – 149. doi: 10.2215/ CJN.03560413.
29. El Minshawy O, Ghabrah T, El Bassuoni E. End‑stage renal disease in Tabuk Area, Saudi Arabia: An epidemiological study. Saudi J Kidney Dis Transpl 2014; 25 : 192 – 195.
30. Wyld ML, Clayton PA, Jesudason S et al. Pregnancy outcomes for kidney transplant recipients. Am J Transplant 2013; 13 : 3173 – 3182. doi: 10.1111/ ajt.12452.
31. French VA, Davis JS, Sayles HS et al. Contraception and fertility awareness among women with solid organ transplants. Obstet Gynecol 2013; 122 : 809 – 814. doi: 10.1097/ AOG.0b013e3182a5eda9.
Štítky
Detská kardiológia Interné lekárstvo Kardiochirurgia Kardiológia
Článok vyšiel v časopiseKardiologická revue – Interní medicína
Najčítanejšie tento týždeň
2014 Číslo 1- e-Konzilium.cz — Masivní plicní embolie při tromboembolické nemoci
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Familiární hypercholesterolemie: zaslouženě v centru pozornosti
- Projekt MedPed: péče o nemocné s familiární hypercholesterolémií v České republice
- Mutace v genu PCSK9 zodpovědné za rozvoj familiární hypercholesterolémie
-
Všetky články tohto čísla
- Invazivní léčba karotických stenóz a možnosti její optimalizace transkraniální dopplerovskou ultrasonografií
- Trvalá kardiostimulace z pohledu nových evropských doporučení roku 2013
- Kardiohepatální syndrom u chronického srdečního selhání
- Prognostický význam elevace funkčních jaterních testů u akutních koronárních syndromů s manifestním srdečním selháním
- Vývoj renálních parametrů u pacientů s pokročilým srdečním selháním léčených levosimendanem – retrospektivní analýza
- Hluboká žilní trombóza a plicní embolie při užívání hormonální antikoncepce
- Argumenty pro konzervativní léčbu chronické formy ischemické choroby srdeční přibývají
- Komplexní ošetřovatelská dokumentace při krátkodobé hospitalizaci pacientů indikovaných k trvalé kardiostimulaci
- XXVII. ročník „Šamánkových“ Poděbrad
- XVII. Kardiovaskulární dny v Lázních Teplice nad Bečvou
- Interní medicína
- Chronické onemocnění ledvin – novinky v klasifikaci a terapii
- Farmakoterapie při chronickém onemocnění ledvin
- Akutní poškození ledvin
- Rychle progredující glomerulonefritidy (srpkovité glomerulonefritidy)
- Vybrané choroby ledvin v těhotenství
- Infekce dolních a horních močových cest
- Editorial 2014
- Hluboká žilní trombóza a plicní embolie při užívání hormonální antikoncepce. Kardiol Rev Int Med 2014; 16(1): 36–38
- Kardiologická revue – Interní medicína
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Akutní poškození ledvin
- Vybrané choroby ledvin v těhotenství
- Rychle progredující glomerulonefritidy (srpkovité glomerulonefritidy)
- Farmakoterapie při chronickém onemocnění ledvin
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy




