-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Výsledky endokrinních funkcí hypofýzy po transsfenoidálních operacích afunkčních makroadenomů
Results of Endocrine Function after Transsphenoidal Surgery for Non-functional Pituitary Macroadenomas
Aim:
The aim of this study was to assess changes to endocrine pituitary function following pituitary macroadenoma surgery and to compare the microscopic and endoscopic techniques.Methods:
A study group included patients with nonfunctional pituitary macroadenoma undergoing microscopic or endoscopic transnasal transsphenoidal approach at the Department of Neurosurgery of the University Hospital in Olomouc. All patients underwent neurologic, radiologic and endocrinology examination before and after surgery. All data were retrospectively reviewed and both techniques were statistically compared.Results:
A total of 78 patients were included in this study. In patients without preoperative hormonal abnormalities, postoperative deficit occurred more often in the microscope group (47.4%) compared to endoscopic group (40%) but the difference was not statistically significant (p = 0.761). In patients with a preoperative hormonal abnormality, postoperative deterioration of hormonal functions was more frequent again in the microscope-operated (70%) compared to the endoscopic group (21.4%), the difference was statistically significant (p = 0.015).Conclusion:
In our study, endoscopic technique achieves better postoperative results of pituitary hormonal functions compared to microscopic techniques, particularly in patients with preoperative hormonal abnormality.Key words:
hypopituitarism – transsphenoidal surgery – nonfunctional pituitary adenoma – endocrine deficit
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Chinese summary - 摘要
非功能性垂体大细胞瘤的经蝶窦手术后内分泌功能的研究
目标:
本研究的目的是评估垂体大细胞瘤手术后内分泌垂体功能的变化,并比较微观和内窥镜技术。
方法:
研究组包括非功能性垂体大腺瘤患者在奥洛穆茨大学医院神经外科系进行微观或内窥镜经鼻经蝶窦方法。所有患者术前和术后均进行神经,放射学和内分泌学检查。对所有数据进行回顾性分析,并对两项技术进行统计学比较。
结果:
本研究共纳入78例患者。术前激素异常患者术后缺血发生率明显高于内镜组(40%),差异无统计学意义(P = 0.761)。术前激素异常患者术后,与内窥镜组比较(21.4%),显微手术(70%),术后激素功能下降更为频繁,差异有统计学意义(p = 0.015)。
结论:
在我们的研究中,与微观技术相比,内镜技术实现了垂体激素功能的更好的术后结果,特别是术前激素异常患者。
关键词:
垂体功能减退症 - 经蝶窦手术 - 非功能垂体腺瘤 - 内分泌缺陷
Autoři: V. Novák 1; L. Hrabálek 1; Z. Fryšák 2; J. Hoza 3; C. Hučko 3; D. Krahulík 1
; J. Macháč 1; M. Vaverka 1
Působiště autorů: Neurochirurgická klinika LF UP a FN Olomouc 1; III. interní klinika – nefrologická revmatologická a endokrinologická LF UP a FN Olomouc 2; Otolaryngologická klinika FN a LF UP Olomouc 3
Vyšlo v časopise: Cesk Slov Neurol N 2017; 80/113(3): 286-290
Kategorie: Původní práce
prolekare.web.journal.doi_sk: https://doi.org/10.14735/amcsnn2017286Článek nebyl podpořen formou grantu, přístrojového vybavení nebo léků.
Souhrn
Cíl:
Cílem této studie bylo prokázat změny endokrinních funkcí hypofýzy po operaci afunkčních makroadenomů hypofýzy transnazálním transsfenoidálním přístupem a posoudit rozdíly výsledků při použití mikroskopické a endoskopické techniky.Soubor a metodika:
Do studie byli zařazeni pacienti s nesekrečními makroadenomy hypofýzy, kteří byli operováni buď mikroskopickou nebo endoskopickou metodou transnazálním transsfenoidálním přístupem na Neurochirurgické klinice LF UP a FN Olomouc. Všichni pacienti absolvovali neurologické, radiologické a endokrinologické vyšetření před operací a po ní. Soubor byl retrospektivně vyhodnocen a získané výsledky byly statisticky porovnány.Výsledky:
Celkový soubor tvořilo 78 pacientů. U pacientů bez předoperační hormonální abnormality se vyskytoval pooperační deficit častěji ve skupině operované mikroskopem (47,4 %) v porovnání s pacienty operovanými endoskopickou metodou (40 %); rozdíl ale nebyl statisticky významný (p = 0,761). U pacientů s předoperační hormonální abnormalitou bylo pooperační zhoršení hormonálních funkcí častější opět ve skupině operované mikroskopem (70 %) ve srovnání s endoskopickou skupinou (21,4 %); rozdíl byl statisticky významný (p = 0,015).Závěr:
Při hodnocení našeho souboru dosáhla endoskopická technika lepších pooperačních výsledků hormonálních funkcí hypofýzy ve srovnání s mikroskopickou technikou, a to zejména u pacientů s předoperační hormonální abnormalitou.Klíčová slova:
hypopituitarizmus – transsfenoidální operace – afunkční adenom hypofýzy – endokrinní deficitÚvod
Nesekreční adenomy hypofýzy se vyskytují v populaci s prevalencí průměrně 22 případů na 100 000 obyvatel [1]. Maximum výskytu je ve čtvrté a páté dekádě života a častěji jsou postiženi muži [2]. Mezi typické projevy onemocnění řadíme poruchy zraku, zvláště výpadky zorného pole, dále parézy okohybných nervů, bolesti hlavy nebo příznaky spojené s nedostatečnou endokrinní funkcí hypofýzy [3]. Primární léčebná modalita u symptomatických afunkčních adenomů je chirurgická terapie.
Cílem operace je dekomprimovat nervové struktury, zejména oční nervy, dosáhnout co nejradikálnějšího odstranění tumoru ke snížení pravděpodobnosti recidivy a vyhnout se komplikacím. Stejně významným cílem operace je obnovení nebo alespoň zachování zbylé endokrinní funkce hypofýzy a zabránění vzniku nového trvalého deficitu. Je přitom až s podivem, jak málo autorů zajímá výsledek operací afunkčních adenomů z pohledu hormonálních funkcí [4–11]. Přitom celoživotní užívání některých hormonů, zejména kortikosteroidů nebo antidiuretického hormonu, má pro pacienta četná rizika komplikací a vedlejších účinků.
Incidence předoperačního hypopituitarizmu u afunkčních adenomů hypofýzy se odhaduje na 69–85 % [12,13]. Zlepšení endokrinních funkcí hypofýzy po operaci je v literatuře uváděno v rozmezí 20–50 % [4–7], naopak zhoršení se popisuje v rozmezí 5 – 20 % [4,6 – 11]. Srovnání jednotlivých výsledků je obtížné, neboť každý z autorů si stanovuje vlastní parametry k hodnocení pooperačního zlepšení nebo zhoršení funkce hypofýzy.
Cílem této studie bylo prokázat změny endokrinních funkcí hypofýzy po operaci afunkčních makroadenomů hypofýzy transnazálním transsfenoidálním přístupem a posoudit rozdíly výsledků při použití mikroskopické a endoskopické techniky.
Materiál a metodika
Všichni pacienti před operací podstoupili klinické vyšetření spočívající v neurologickém vyšetření, vyšetření oftalmologem vč. provedení vyšetření na počítačovém perimetru. Základem pro stanovení morfologické diagnózy byla kontrastní magnetická rezonance (MR) hypofýzy. Doplněno bylo endokrinologické vyšetření zaměřené na posouzení funkce hypofýzy a vyloučení prolaktinomu. Indikací k operaci byly útlakové projevy, tedy výpadky zorného pole, zhoršení zrakové ostrosti nebo paréza okohybných nervů jako následek expanzivního chování makroadenomu hypofýzy. Před vlastní operací byla vždy doplněna i výpočetní tomografie (CT) spodiny lební a paranazálních dutin a vyšetření dutiny nosní spolupracujícím otorinolaryngologem.
Operace byly provedeny transnazálním transsfenoidálním přístupem. Do roku 2010 byla na Neurochirurgické klinice LF OU a FN Olomouc použita mikroskopická a následně endoskopická technika. V případech mikroskopické metody byl za skiaskopické kontroly vložen retraktor do dutiny nosní s vymezením operačního koridoru až ke sfenoidální dutině. Endoskopický přístup byl ve spolupráci s otorinolaryngologem prováděn endoskopem s 30° optikou (Storz®, Německo) až ke spodině tureckého sedla. Adenom byl následně exstirpován maximálně radikálně jak v případě mikroskopické, tak i endoskopické optiky za použití vždy stejných nástrojů a operačního postupu, při maximální snaze o zachování tkáně normální hypofýzy. K plastice spodiny tureckého sedla byl využíván sval, tuk, fascie, oxycelulóza (Surgicel®) a tkáňové lepidlo (Tissucol®).
V návaznosti na operační výkon zůstávali nemocní na udržovací dávce glukokortikoidů, konkrétně kortizolu, přičemž nejvyšší dávka léku byla podávána ráno (10 mg), poloviční (5 mg) pak v poledne a večer. V prvním týdnu před propuštěním pacientů bylo provedeno orientační kontrolní endokrinologické vyšetření s předáním do ambulantní péče endokrinologického pracoviště. Cílem bylo zhodnotit, zda je nezbytné pokračovat v substituci kortizolem, případně desmoprezinem. Nemocní byli následně zváni s odstupem 3 měsíců ke krátké hospitalizaci za účelem posouzení míry výpadku všech hormonů hypothalamo-hypofyzární osy. Pokud nebyly přítomny kontraindikace, byl metodou volby při podezření na pooperační nedostatečnost inzulinový toleranční test (ITT) kombinovaný s užitím stimulace LHRH (lutropin uvolňující hormon; oblast gonadotropní sekrece, výjimkou byly z pochopitelných důvodů postmenopauzální nemocné) a TRH (thyreotropin uvolňující hormon). V indikovaných případech poskytl ITT informace i o poruchách sekrece růstového hormonu. V případě kontraindikace provedení ITT byl pro zhodnocení poruch sekrece růstového hormonu (GH) zvolen test s infuzí argininu doplněný hormonem stimulujícím sekreci růstového hormonu (GHRH). Překlenutí tranzitorní pooperační poruchy, případně léčba trvalého kraniálního diabetes insipidus (cDI) byla řešena podáváním desmopresinu (Minirin®).
Tři měsíce po operaci absolvovali pacienti také vyšetření perimetrem, MR hypofýzy s kontrastem ke zhodnocení radikality operace a vyšetření dutiny nosní ke zhodnocení hojení endoskopicky operovaných pacientů.
Endokrinní vyšetření
Předoperační vyšetření mělo za cíl posouzení sekreční kapacity hypofýzy. Cíleně bylo pátráno po prolaktinomu, protože prolaktinom, byť by se jednalo o makroprolaktinom, je primárně indikován k medikamentózní léčbě. Problém bývá v některých případech odlišení pseudoprolaktinomu, projev důsledku útlaku stopky hypofýzy makroadenomem jiné povahy než prolaktinomem. Přesný laboratorní test zde chybí a naopak je neocenitelná klinická zkušenost.
Hormonální poměry byly hodnoceny podle referenčních mezí Oddělení biochemie FN Olomouc. Za hormonální deficit bylo považováno:
- nízké fT4 (< 9,1 pmol/l) při normálním nebo nízkém TSH (thyreotropní hormon) (< 0,350 mIU/ l);
- nízké FSH (folikulostimulační hormon) a LH (luteinizační hormon) u žen podle fází cyklu, případně podle toho, zda se jednalo o ženu ve fertilním nebo menopauzálním věku, u mužů při nízkém FSH (< 1,0 IU/ l) a LH (< 0,6 IUl/l), pro metodické nedostatky jsme nehodnotili hladiny volného testosteronu a dali jsme proto přednost celkové hladině testosteronu;
- nízká kortizolemie (< 171 nmol/l) při normálním nebo nízkém ACTH (adrenokortikotropní hormon) (< 5 ng/ l);
- nízké IGF-1 (insulin-like growth factor-1; korigované dle věku pacienta), věk 20–30 let (< 232 µg/l), 30 – 40 let (< 177 µg/l), 40 – 50 let (< 124 µg/l), 50 a více let (< 71 µg/l);
- nízká hladina prolaktinu (< 72 mIU/l) u mužů a (< 109 mIU/l) u žen.
cDI byl charakterizován polydipsií, polyurií (diuréza > 250 ml/hod) a nízkou specifickou hmotností moči (< 1,005 kg/ m3) při osmolaritě moči pod 300 mOsm/ l.
Inkluzivní kritérium pro zařazení pacientů do retrospektivní studie byla diagnóza nesekrečního makroadenomu hypofýzy doložená následně histologickým vyšetřením. Afunkční makroadenom hypofýzy byl definován jako adenom větší než 10 mm, bez prokazatelné klinické i laboratorní hormonální aktivity. Další podmínkou bylo provedení pouze jedné operace transnazální transsfenoidální cestou, dostupnost kompletních výsledků endokrinních funkcí hypofýzy bezprostředně před operací, dále v prvním týdnu po operaci a 3 měsíce po ní. Všechna endokrinologická vyšetření byla provedena jednotným způsobem na III. interní klinice – nefrologické, revmatologické a endokrinologické LF UP a FN Olomouc. Minimální doba sledování nemocných byla stanovena na 1 rok.
Všechna kritéria v průběhu let 2004 – 2014 splnilo 78 pacientů. Soubor pacientů byl vyhodnocen společně a následně rozdělen do dvou skupin: 1. skupina operovaná mikroskopickou a 2. skupina operovaná endoskopickou technikou. Jednotlivé skupiny byly dále rozděleny na podskupiny s předoperační hormonální abnormalitou a bez hormonální abnormality. Do podskupiny s hormonální abnormalitou byli zařazeni pacienti s deficitem jednoho nebo více hypofyzárních hormonů (hormony adenohypofýzy i neurohypofýzy) a/nebo s pseudoprolaktinemií. Pooperačně bylo zhodnoceno, zda došlo ke zlepšení, zhoršení nebo hormonální abnormalita zůstala bez změny. Za zlepšení byla považována normalizace hladin jednotlivých hormonů, které se pooperačně dostaly znovu do rozmezí normálních referenčních hodnot. V případě, že došlo ke zlepšení v jedné nebo více hormonálních osách, ale současně ke zhoršení v jiné, nebylo to považováno za zlepšení a výsledek byl zařazen do skupiny zhoršených. Přechodný pooperační diabetes insipidus nebyl považován za hormonální deficit.
Statistické zpracování
Soubor byl statisticky zpracován pomocí programu IBM SPSS Statistics 23 a všechny testy byly provedeny na hladině významnosti p = 0,05. Kategoriální data byla zapsána do kontingenčních tabulek (Cross tab) a skupiny byly porovnány Fisherovým přesným testem. Normalita zkoumaného statistického výběru byla ověřena Shapirovým-Wilkovým testem a neparametrickým Mannovým-Whitneyho U testem.
Výsledky
Celkový soubor tvořilo 78 pacientů, z toho bylo 46 mužů a 32 žen. Věkové rozmezí bylo 22–85 let (průměrný věk 59,5 let). Předoperační hormonální abnormalita byla prokázána u 34 (43,6 %) pacientů, hormonální léčba probíhala u sedmi nemocných (9 %).
Skupinu operovanou mikroskopicky tvořilo 39 pacientů, z toho bylo 20 mužů a 19 žen. Věkové rozmezí bylo 22–78 let (průměrný věk 57,4 let). Předoperační hormonální abnormalita byla zjištěna u 20 (51,3 %) pacientů, hormonální léčba probíhala u tří nemocných (7,7 %).
Skupinu operovanou endoskopicky tvořilo 39 pacientů, z toho bylo 26 mužů a 13 žen. Věkové rozmezí bylo 28–85 let (průměrný věk 61,6 let). Předoperační hormonální abnormalita byla zjištěna u 14 (35,9 %) pacientů, hormonální léčba probíhala u čtyřech nemocných (10,3 %).
Shapirovým-Wilkovým testem normality bylo prokázáno, že věk nemá normální distribuci, proto byly skupiny porovnány neparametrickým Mannovým-Whitneyho U testem. Tento test neprokázal statisticky významný rozdíl ve věku mezi pacienty operovanými endoskopem a mikroskopem. Nebyl prokázán statisticky významný rozdíl mezi oběma skupinami ani v zastoupení jednotlivých pohlaví, ani v četnosti výskytu předoperační hormonální abnormality a medikamentózní terapie. Obě skupiny byly tedy homogenní a vhodné ke srovnání pooperačních výsledků.
Výsledky jednotlivých hormonálních os hypofýzy u celého souboru a obou skupin před operací a 3 měsíce po operaci jsou uvedeny v tab. 1.
Tab. 1. Výsledky jednotlivých hormonálních abnormalit. 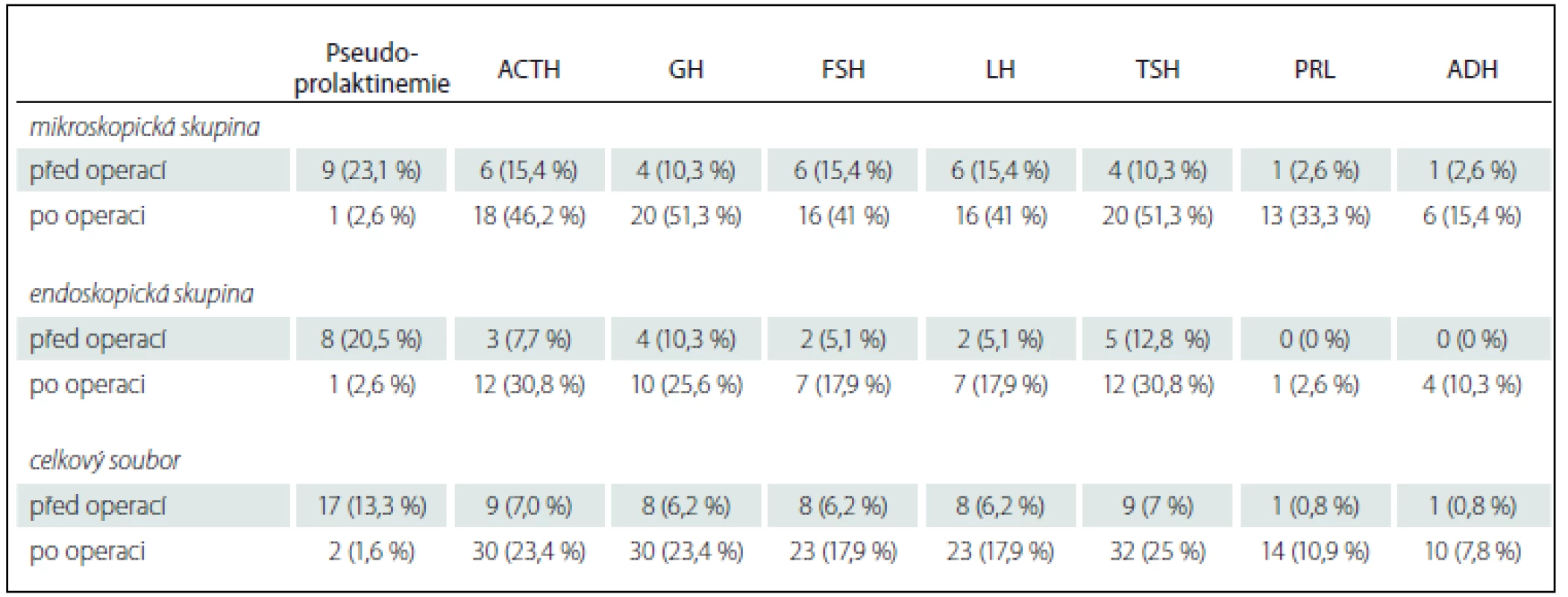
Vysvětlení zkratek naleznete v seznamu použitých zkratek. Výsledné hodnocení změny funkce hypofýzy (zlepšení, zhoršení nebo změna nenastala) v důsledku operace, četnost pooperační medikamentózní terapie a pacientů s reziduem adenomu jsou uvedeny v tab. 2.
Tab. 2. Pooperační výsledky a srovnání skupiny nemocných operovaných mikroskopickou nebo endoskopickou metodou. 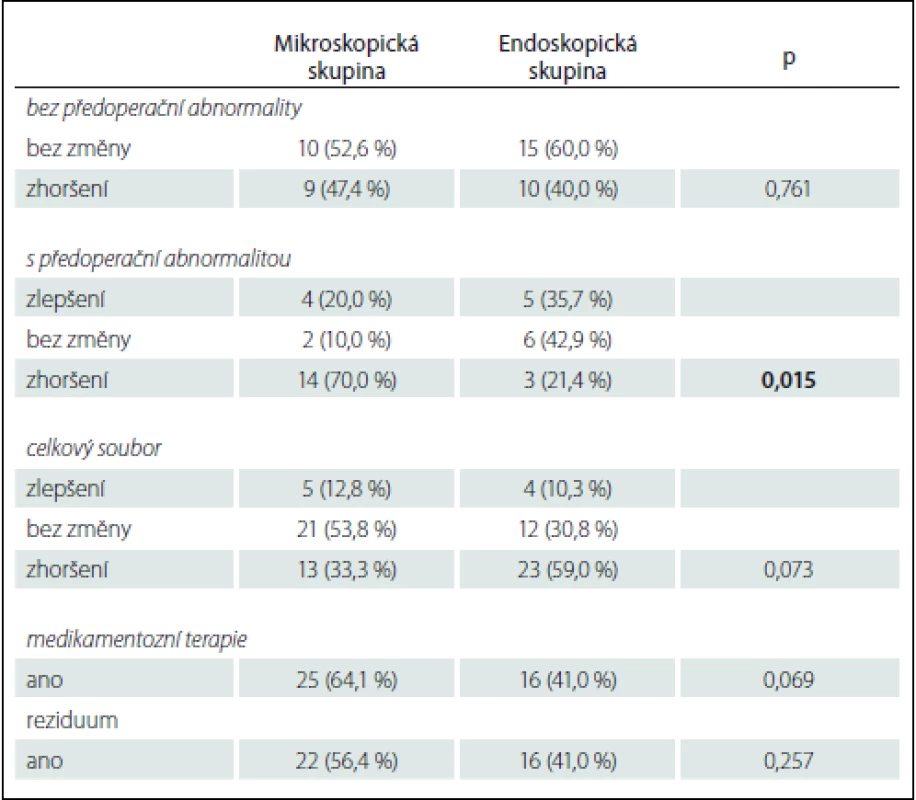
Výsledky pooperačních hormonálních funkcí hypofýzy ve vztahu k přítomnosti rezidua adenomu jsou uvedeny v tab. 3.
Tab. 3. Pooperační výsledky a srovnání skupiny s reziduem a bez rezidua adenomu. 
U pacientů bez předoperační hormonální abnormality se vyskytoval pooperační deficit častěji ve skupině operované mikroskopem (47,4 %) ve srovnání s endoskopickou skupinou (40 %); rozdíl ale nebyl statisticky významný (p = 0,761). U pacientů s předoperační hormonální abnormalitou bylo pooperační zhoršení hormonálních funkcí častější opět ve skupině operované mikroskopem (70 %) ve srovnání s endoskopickou skupinou (21,4 %); rozdíl byl statisticky významný (p = 0,015).
U pacientů operovaných endoskopem, ve srovnání s mikroskopickou operací, byl ve větší míře pooperační stav hormonálních funkcí stejný jako před operací nebo došlo ke zlepšení, rozdíl ale nebyl statisticky významný (p = 0,073).
Častěji byl výskyt rezidua pozorován ve skupině operované mikroskopicky, ale bez statistické významnosti (p = 0,257).
U pacientů bez výskytu pooperačního rezidua, ve srovnání s pacienty s reziduem, byly častěji hormonální funkce zlepšeny, zůstaly stejné nebo nedošlo ke zhoršení, ale bez statistické významnosti (p = 0,309).
Diskuze
Transnazální transsfenoidální mikroskopická operativa adenomů hypofýzy byla na Neurochirurgické klinice v Olomouci prováděna od 90. let minulého století. Endoskopická technika se následně stala rutinně využívanou od roku 2010. První zmínky v českém písemnictví o využití endonazálního transsfenoidálního přístupu v terapii selárních lézí přináší Masopust et al v roce 2008 [14].
Vznik hypopituitarizmu u afunkčních adenomů se patofyziologicky vysvětluje zvýšeným intraselárním tlakem, který vede ke kompresi portálních žil s následkem ischemizace a nekrózou tkáně hypofýzy. Hypofunkce může být také způsobena dlouhodobou kompresí hypofýzy vlastním adenomem [13]. K hypofunkci může dojít i akutně, při apoplexii. Působením zvýšeného intraselárního tlaku na stopku hypofýzy dochází k poruše hypothalamo-hypofyzárního transportu a nedostatečné stimulaci endokrinních buněk adenohypofýzy. Kromě toho nedostatečné působení inhibičního dopaminu na laktotrofní buňky vede k projevům pseudoprolaktinemie.
Schopnost zlepšení endokrinních funkcí po operaci závisí na množství nepoškozených buněk hypofýzy. Mezi pozitivní prediktivní faktory zlepšení patří menší velikost adenomu, absence invazivního chování adenomu, větší reziduální porce tkáně hypofýzy, normální nebo zvýšená sekrece prolaktinu, předoperační elevace TSH po stimulaci TRH, elevace LH po stimulaci GnRH, nízká hladina deficitu IGF-1, první operace, radikální exstirpace nádoru, absence pooperační likvorey, normotenze a mladší věk nemocného [6 – 8,13,15,16]. Na druhou stranu k novému pooperačnímu deficitu dochází častěji u pacientů starších, s hormonálně afunkčními adenomy, po transkraniálních operacích a pituitární apoplexii [6,7]. Fatemi et al navíc uvádí vyšší frekvenci pooperačního zhoršení v případě, kdy nevyužili proplachu operační dutiny peroxidem vodíku [6]. Zda peroxid vodíku skutečně ovlivňuje endokrinní funkci a snižuje riziko recidivy, není zřejmé, ačkoli byl prokázán tumoricidní efekt na buňky adenomu hypofýzy [17]. Zajímavé je, že v námi prezentovaném souboru bylo lepších hormonálních funkcí dosaženo endoskopickou technikou v podskupině pacientů s přítomností předoperační hormonální abnormality. Domníváme se, že endoskopická technika byla šetrnější při exstirpaci adenomu a vedla k menší traumatizaci již funkčně dekompenzované tkáně hypofýzy.
Chabot et al publikovali retrospektivně sledovaný soubor 39 pacientů s makroadenomy většími než 3 cm, operovaných transnazální transsfenoidální endoskopickou technikou. Autoři nehodnotili pouze afunkční adenomy, ale do souboru započítali i dva makroadenomy s nadprodukcí ACTH, dva s nadprodukcí GH a tři prolaktinomy. Endokrinolog zhodnotil stav předoperačního a přítomnost nového pooperačního hypopituitarizmu, metodika hodnocení však nebyla specifikována. Po operaci došlo ke zhoršení stávajícího nebo nového výskytu hypopituitarizmu s nutností hormonální substituce u 12,8 % pacientů [18].
Fatemi at al prezentovali retrospektivně sledovaný soubor 253 pacientů s afunkčními adenomy hypofýzy operovaných transnazální transsfenoidální mikroskopickou technikou. Pacienti absolvovali endokrinní laboratorní vyšetření před operací a 3 měsíce po operaci. Za zlepšení byla považována normalizace laboratorních parametrů pro jednotlivé hypofyzární hormony. Zhoršení bylo definováno nutností hormonální substituce a přítomností nové laboratorní abnormality. Po operaci došlo v 7 % ke vzniku nového endokrinního deficitu, zlepšení bylo popisováno ve 48 %. Zlepšení bylo nejčastěji u pacientů s pseudoprolaktinemií, a to v 78 %, v gonadální ose v 21 % a v adrenokortikotropní ose v 16 %. Nejčastější pooperační deficit byl výpadek růstového hormonu s frekvencí 6 %. Limitací studie byly nejednotné referenční meze pro sledované laboratorní parametry a nekompletnost vyšetřovaných dat [6].
Dallapiazza et al srovnávali pacienty s afunkčními makroadenomy hypofýzy operovanými mikroskopickou a endoskopickou technikou. Skupinu mikroskopicky operovanou tvořilo 43 pacientů a skupinu endoskopicky operovanou tvořilo 56 pacientů. Pooperační výsledek hormonálních funkcí byl hodnocen pouze na základě nutnosti užívání hormonální substituce. V mikroskopické skupině byl zaznamenán pooperační přechodný cDI v šesti případech, trvalý cDI v jednom případě, SIADH v sedmi případech, přechodný hypokortizolizmus ve třech případech a trvalý ve třech případech. V endoskopické skupině byl zaznamenán pooperační přechodný cDI v 10 případech, trvalý cDI nebyl prokázán, SIADH se vyskytlo v pěti případech, přechodný hypokortizolizmus v pěti případech a trvalý ve třech případech. Při srovnání obou skupin nebyl statisticky signifikantní rozdíl. Pooperační likvorea se objevila ve 12 % ve skupině mikroskopicky operovaných a v 7 % ve skupině endoskopicky operovaných, bez statisticky významného rozdílu. Radikality bylo dosaženo v 79 % ve skupině mikroskopicky operované a v 85 % ve skupině endoskopicky operované [19].
Z českých autorů hodnotili výsledky hormonálních funkcí hypofýzy po transnazálních operacích adenomů Masopust et al [20]. Porovnávány byly tři skupiny o identické velikosti 50 pacientů: 1. skupina operována mikroskopickou technikou, 2. skupina operována endoskopickou technikou a 3. skupina operována endoskopicky s využitím peroperační MR. Do studie byli zahrnuti pacienti jak s mikroadenomy, tak s makroadenomy a bez ohledu, zda se jednalo o afunkční nebo hormonálně aktivní adenom. Hormonální funkce byla hodnocena na základě nutnosti dočasné nebo permanentní substituce desmoprezinem. V 1. skupině desmoprezin užívalo pět pacientů a z toho tři chronicky, ve 2. skupině byla dočasná substituce u čtyř pacientů a ve 3. skupině u pěti. Rozvoj nového pooperačního deficitu adenohypofýzy (thyroidní, adrenokortikotropní nebo gonadotroponí osa) byl zaznamenán v 10 případech v 1. skupině, ve čtyřech případech ve 2. skupině a ve třech v 3. skupině [20]. Stejně jako v námi předkládané studii bylo lepších výsledků dosahováno endoskopickou technikou.
Při hodnocení naší studie bylo přesvědčivě lepších výsledků dosaženo ve skupině operovaných endoskopickou metodou, a to zejména u pacientů s předoperačním deficitem. Ve prospěch endoskopické techniky hovořila i menší míra pooperačních reziduí. To vše lze vysvětlit lepším operačním přehledem endoskopu s přesnější, a tedy šetrnější možností zásahu do tumoru, a naopak protekcí zbytku hypofýzy.
Limitací naší a doposud publikovaných studií hodnotící endokrinologické výsledky po operacích afunkčních adenomů hypofýzy je jejich retrospektivní charakter. Nutno přiznat, že v námi prezentované studii nebyla zohledněna jak velikost, tak invazivita adenomu a délka předoperačního hormonálního deficitu ve vztahu k výsledkům hormonálních funkcí.
Závěr
Při hodnocení našeho souboru dosáhla endoskopická technika lepších pooperačních výsledků hormonálních funkcí hypofýzy ve srovnání s mikroskopickou technikou, a to zejména u pacientů s předoperační hormonální abnormalitou.
Seznam použitých zkratek
ACTH – adrenokortikotropní hormon
ADH – antidiuretický hormon
cDI – kraniální diabetes insipidus
CT – počítačová tomografie
FSH – folikulostimulační hormon
fT4 – volný thyroxin
GnRH – gonadotropin uvolňující hormon
GHRH – růstový hormon uvolňující hormon
IGF-1 – insulin-like growth factor-1
ITT – inzulínový toleranční test
LH – luteinizační hormon
LHRH – lutropin uvolňující hormon
MR – magnetická rezonance
PRL – prolaktin
TRH – thyreotropin uvolňující hormon
TSH – thyreotropní hormon
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Vlastimil Novák
Neurochirurgická klinika
LF UP a FN Olomouc
I. P. Pavlova 6
779 00 Olomouc
e-mail: nvlastimil@seznam.cz
Přijato k recenzi: 16. 9. 2016
Přijato do tisku: 6. 12. 2016
Zdroje
1. Fernandez A, Karavitaki N, Wass JA. Prevalence of pituitary adenomas: a community-based, cross-sectional study in Banbury (Oxfordshire, UK). Clin Endocrinol (Oxf) 2010;72(3):377 – 82. doi: 10.1111/ j.1365-2265.2009.03667.x.
2. Thapar K, Kovacs K, Horvath E et al. Classification and Pathology of Pituitary Tumors. In: Wilkins RH, Rengachary SS, eds. Neurosurgery. 2nd ed. New York: McGraw-Hill 1996 : 1273 – 89.
3. Shao S, Li X. Clinical features and analysis in 1,385 Chinese patients with pituitary adenomas. J Neurosurg Sci 2013;57(3):267 – 75.
4. Nomikos P, Ladar C, Fahlbusch R et al. Impact of primary surgery on pituitary function in patients with non--functioning pituitary adenomas – a study on 721 patients. Acta Neurochir (Wien) 2004;146(1):27 – 35.
5. Wichers-Rother M, Hoven S, Kristof RA, et al. Non--functioning pituitary adenomas: endocrinological and clinical outcome after transsphenoidal and transcranial surgery. Exp Clin Endocrinol Diabetes 2004;112(6):323 – 7.
6. Fatemi N, Dusick JR, Mattozo C, et al. Pituitary hormonal loss and recovery after transsphenoidal adenoma removal. Neurosurgery 2008;63(4):709 – 18. doi: 10.1227/ 01.NEU.0000325725.77132.90.
7. Berkmann S, Fandino J, Müller B, et al. Intraoperative MRI and endocrinological outcome of transsphenoidal surgery for non-functioning pituitary adenoma. Acta Neurochir (Wien) 2012;154(4):639 – 47. doi: 10.1007/ s00701-012-1285-5.
8. Jahangiri A, Wagner JR, Han SW, et al. Improved versus worsened endocrine function after transsphenoidal surgery for nonfunctional pituitary adenomas: rate, time course, and radiological analysis. J Neurosurg 2016;124(3):589 – 95. doi: 10.3171/ 2015.1.JNS141543.
9. Brand IR, Dalton GA, Fletcher RF. Long-term follow-up of trans-sphenoidal hypophysectomy for Cushing‘s disease. J R Soc Med 1985;78(4):291 – 3.
10. Hammer GD, Tyrrell JB, Lamborn KR, et al. Transsphenoidal microsurgery for Cushing‘s disease: initial outcome and long-term results. J Clin Endocrinol Metab 2004;89(12):6348 – 57.
11. Nemergut EC, Zuo Z, Jane JA jr, et al. Predictors of diabetes insipidus after transsphenoidal surgery: a review of 881 patients. J Neurosurg 2005;103(3):448 – 54.
12. Marazuela M, Astigarraga B, Vicente A, et al. Recovery of visual and endocrine function following transsphenoidal surgery of large nonfunctioning pituitary adenomas. J Endocrinol Invest 1994;17(9):703 – 7.
13. Arafah BM. Reversible hypopituitarism in patients with large non-functioning pituitary adenomas. J Clin Endocrinol Metab 1986;62(6):1173 – 9.
14. Masopust V, Netuka D, Benes V. Endonazální endoskopická transsfenoidální resekce selárních lézí. Cesk Slov Neurol N 2008;71/ 104(6):704 – 10.
15. Webb SM, Rigla M, Wägner A, et al. Recovery of hypopituitarism after neurosurgical treatment of pituitary adenomas. J Clin Endocrinol Metab 1999;84(10):3696 – 700.
16. Jahangiri A, Wagner J, Han SW, et al. Rate and time course of improvement in endocrine function after more than 1,000 pituitary operations. Neurosurgery 2014;61(Suppl 1):163 – 6. doi: 10.1227/ NEU.0000000000000405.
17. Mesiwala AH, Farrell L, Santiago P, et al. The effects of hydrogen peroxide on brain and brain tumors. Surg Neurol 2003;59(5):398 – 407.
18. Chabot JD, Chakraborty S, Imbarrato G, et al. Evaluation of Outcomes After Endoscopic Endonasal Surgery for Large and Giant Pituitary Macroadenoma: a Retrospective Review of 39 Consecutive Patients. World Neurosurg 2015;84(4):978 – 88. doi: 10.1016/ j.wneu.2015.06.007.
19. Dallapiazza R, Bond AE, Grober Y, et al. Retrospective analysis of a concurrent series of microscopic versus endoscopic transsphenoidal surgeries for Knosp Grades 0 – 2 non-functioning pituitary macroadenomas at a single institution. J Neurosurg 2014;121(3):511 – 7. doi: 10.3171/ 2014.6.JNS131321.
20. Masopust V, Netuka D, Benes V, et al. Endonasal endoscopic pituitary adenoma resection: preservation of neurohypophyseal function. J Neurol Surg A Cent Eur Neurosurg 2014;75(5):336 – 42. doi: 10.1055/ s-0034-1368687.
Štítky
Detská neurológia Neurochirurgia Neurológia
Článok vyšiel v časopiseČeská a slovenská neurologie a neurochirurgie
Najčítanejšie tento týždeň
2017 Číslo 3- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Spasmolytický účinek metamizolu
- I „pouhé“ doporučení znamená velkou pomoc. Nasměrujte své pacienty pod křídla Dobrých andělů
- Realita liečby bolesti v paliatívnej starostlivosti v Nemecku
- MUDr. Lenka Klimešová: Multiodborová vizita je kľúč k efektívnejšej perioperačnej liečbe chronickej bolesti
-
Všetky články tohto čísla
- Myotonická dystrofie – jednota v různosti
- Je třeba léčit premotorické stadium Parkinsonovy nemoci?
- Je potrebné liečiť premotorické štádium Parkinsonovej choroby?
-
Komentář ke kontroverzím
Je potrebné liečiť premotorické štádium Parkinsonovej choroby? - Febrilní křeče – méně je někdy více
- Riziko poškození plodu v důsledku rentgenových výkonů u gravidních žen
- Vertebrogenní algický syndrom – medicína založená na důkazech a běžná klinická praxe. Existuje důvod něco změnit?
- Výsledky endokrinních funkcí hypofýzy po transsfenoidálních operacích afunkčních makroadenomů
- Radiologické nálezy u donošených novorozenců s hypoxicko-ischemickou encefalopatií
- Token test – validační studie české verze u osob vyššího věku a pacientů s neurodegenerativním onemocněním mozku
- Měření simulace – Test mince v ruce
- Efekty cílené orofaciální rehabilitace u pacientů s poruchou řečových funkcí po cévní mozkové příhodě
- Kvalita života u soběstačných pacientů po cévní mozkové příhodě
- Zobrazení difuzních tenzorů u pacientů s idiopatickým normotenzním hydrocefalem
- Anti-NMDAR protilátky u demyelinizačních onemocnění
- Úspěšná léčba meningoencefalitidy vyvolané Cryptococcus gattii Ommaya rezervoárem a intratékální injekcí amfotericinu B – kazuistika
- Diferenciální diagnostika bithalamické a palidální hypointenzity – kazuistika s mutací HEXB
- Pyridoxin dependentní epilepsie – kazuistiky
- Signifikantní edém mozku u neprasklé arteriovenózní malformace – kazuistika
- Klasifikace nádorů centrálního nervového systému – WHO 2016 Update
-
Analýza dat v neurologii
LXIII. Pozor na interpretaci ekologických (korelačních) studií – II. - Profesor MUDr. Karel Urbánek, CSc., slaví 80 let
- Karel Šonka šedesátiletý
- Recenze knih
- Dopis redakci
- Česká neurochirurgie byla nominována mezi 75 vybraných světových center na globální oslavě prof. Spetzlera
- Česká a slovenská neurologie a neurochirurgie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Myotonická dystrofie – jednota v různosti
- Riziko poškození plodu v důsledku rentgenových výkonů u gravidních žen
- Vertebrogenní algický syndrom – medicína založená na důkazech a běžná klinická praxe. Existuje důvod něco změnit?
- Febrilní křeče – méně je někdy více
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



