-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Současné praktické postupy pro vyšetřování a léčbu chronické urtikárie
Aktualizovaný přehled a interpretace doporučených postupů pro praxi
Current Practical Approaches to Investigation and Management of Chronic Urticaria
The introduction of new antihistamines and biologics has renewed the interest in chronic urticaria both in the field of investigation and clinical practice. The updated EAACI, GA(2)LEN, EDF, WAO recommendation for the definition, classification, diagnosis and management of chronic urticaria provide the physicians with evidence based and proved guide in diagnostics and therapy. The most beneficial tool for assessing the type of chronic urticaria is the patient’s history, taken in a stratified algorithm. Non sedating H1 antihistamines are the drug of the first choice, eventually in updosed regimen. Third line therapy is represented by immunosupressant and immunomudulators as add on therapy. Some cases need to be dealed in an individual way, including the use of less common empirical drugs. For the general management of chronic urticaria an adequate patient’s education nad psychosomatic attitude are important. This article with schemes, tables, charts and educational patient’s sheets provides a guide for physicians in daily practice. The board of Czech Dermatovenerological Society has reccomended the EAACI, GA(2)LEN, EDF, WAO guideline to be used in medical practice in Czech Republic.
Key words:
chronic urticaria – guidelines for practice
Autoři: N. Benáková 1,2
Působiště autorů: Dermatovenerologická klinika 1. LF UK Praha přednosta prof. MUDr. Jiří Štork, CSc. 1; Dermatologická ordinace alergoimunologického centra ImmunoFlow Praha vedoucí lékař MUDr. Martin Fuchs 2
Vyšlo v časopise: Čes-slov Derm, 90, 2015, No. 5, p. 198-212
Kategorie: Terapie, farmakologie a klinické studie
Souhrn
Zavádění nových antihistaminik a biologik oživilo zájem o problematiku chronické kopřivky jak na poli výzkumu, tak klinické praxe. Aktualizované Doporučené postupy EAACI, GA(2)LEN, EDF a WAO pro léčbu chronické kopřivky poskytují lékařům objektivně prověřené vodítko v diagnostice i léčbě. Strukturovaná anamnéza je nejpřínosnější diagnostický prostředek ke zjištění typu chronické kopřivky. Léky první volby jsou prověřená nesedativní H1 antihistaminika, a to i ve zvýšeném dávkování. Jako třetí linie se k nim přidávají imunosupresivní a imunomodulační léky. Jednotlivé případy však nadále vyžadují individuální přístup včetně použití méně obvyklých empirických léků. Ke zvládnutí chronické kopřivky je důležitá i přiměřená edukace pacienta a psychosomatický přístup. Článek poskytuje formou praktických šablon, tabulek, schémat a doprovodného textu pomůcku pro vyšetřování a léčbu pacientů s chronickou urtikárií v každodenní praxi, a to jak pro lékaře v běžné ambulanci, tak v klinickém centru. Výbor ČDS ČLS JEP doporučil Doporučené postupy EAACI, GA(2)LEN, EDF a WAO k používání v praxi pro české dermatology a další lékaře.
Klíčová slova:
chronická urtikárie – doporučené postupy pro praxiÚVOD
Chronická urtikárie (CU) tvoří etiopatogeneticky nesourodou skupinu, která se na kůži projevuje výsevy kopřivkových pupenů, angioedémem, případně oběma příznaky. CU je definována jako kopřivka trvající déle než 6 týdnů, která se objevuje denně či téměř denně (respektive více jak 2krát týdně) [17]. Hlavním mediátorem je především histamin a jiné biogenní aminy, ale mohou ji vyvolat i další prozánětlivé mediátory s účinkem na cévy, jako jsou leukotrieny, faktor aktivující destičky (PAF), prostaglandiny, bradykinin, interleukiny, složky komplementu, hemokoagulační faktory aj. [15], kde proto léčba antihistaminiky není účinná.
Prevalence chronické kopřivky se pohybuje okolo 1 %, převažují mladší dospělí, častěji ženy. Kopřivka a angioedém představují spektrum jedné choroby – podkladem je edém v koriu a výsledný klinický obraz je dán hloubkou jeho lokalizace. Typický je náhlý vznik a obvykle prchavý charakter kopřivky – pomfy ustupují v řádu minut až hodin, což je charakteristické pro indukovatelné urtikárie (kromě pozdní tlakové) a kontaktní urtikárie. Pomfy u pozdní tlakové urtikárie se objevují s latencí 4–8 hodin a mohou trvat i déle než 24 hodin. Pomfy u spontánní urtikárie ustupují v řádu více hodin, nepřesahují ale 24 hodin. Pomfy u urtikariální vaskulitidy trvají déle než 24 hodin, obvykle 2–3 dny. Angioedém odeznívá pomaleji, a to do několika dnů [17].
Zavádění nových antihistaminik a biologik oživilo zájem o tuto problematiku jak na poli výzkumu, tak klinické praxe. V České republice bylo dosud jen málo dermatologických pracovišť, respektive dermatologů, kteří se vyšetřováním a léčbou CU soustavně zabývali. Problematika CU má mezioborový charakter, ale díky pokračujícímu pokroku ve výzkumu a především díky praktickému pojetí mezinárodních doporučených postupů [19] se pacientů s CU může primárně ujímat jak dermatolog, tak alergolog. Předpokladem je být odborně schopen, ale i ochoten se chronickému pacientovi věnovat. V listopadu 2014 se v Praze konalo první mezinárodní „Global Urticaria Forum“, které ve dvoudenním maratonu přednášek a interaktivních workshopů seznámilo s novými vědeckými poznatky i používáním doporučených postupů v praxi. Podstatné informace z této konference jsou zahrnuty též do tohoto článku.
Léčba a zvládání CU jsou náročné. V oblasti vyšetřování a léčby je velkým přínosem práce expertní pracovní skupiny odborníků pod vedením prof. Zuberbiera a Maurera z dermatologické kliniky berlínské Charité. Tato skupina iniciovala, tvořila, zpracovávala a koordinovala práce, které vyústily v mezinárodní Doporučené postupy pro definování, klasifikaci, diagnostiku a zvládání urtikárie společností EAACI, GA(2)LEN, EDF a WAO (European Academy of Allergology and Clinical Immunology, Global Allergy and Asthma European Network, European Dermatology Forum, World Allergology Organisation). Tato diagnostická a léčebná doporučení odborných evropských a světových alergologických a dermatologických společností (19) poskytují lékařům objektivně prověřené vodítko v diagnostice i léčbě. Tiskem byly vydány poprvé v roce 2006, pak v 2009 a poslední aktualizace vyšla v roce 2014 [19]. Reprint Doporučení z roku 2006 byl vydán v angličtině jako suplementum časopisu Čs. dermatologie v roce 2007 [18]. Solidní informace z doporučených postupů z roku 2009 mohli naši dermatologové získat v češtině vloni v přehledném článku v časopise Čs. dermatologie [3] a z roku 2014 v časopise Alergie [1].
Text posledních Doporučených postupů z roku 2014 jsme nyní zpracovali ve formě pečlivého českého překladu a vyjednali možnost vytištění, aby byla všem českým dermatologům srozumitelná a dostupná (suplementum Čs. dermatologie).Výbor České dermatovenerologické společnosti ČLS JEP, je doporučil k používání v praxi pro české dermatology a další lékaře. Kromě české verze textu recentních Doporučených postupů jsme ve spolupráci s kolegyní MUDr. Ivou Karlovou (z pracoviště dermatovenerologické kliniky FN Olomouc, které se problematice chronické urtikárie dlouhodobě věnuje) a za podpory společnosti Novartis připravily na základě řady recentních článků, přednášek, workshopů a po odborných diskusích a mnoha úpravách i další praktické materiály, umožňující snadnější orientaci a práci s doporučenými postupy v praxi. Nakonec bylo rozhodlnuto je koncepčně pojmout jako součást výkladového, doprovodného článku, který nyní dostáváte do rukou. Jedná se o šablony pro vyšetření, tabulky klasifikace, diagnostických a vyšetřovacích algoritmů, kalendář pro pacienta, formulář pro hodnocení UAS7 skóre. Pro komplexnost jsme mimo článek připravily též edukační letáček pro pacienty o chronické kopřivce a letáček o dietě s nízkým obsahem histaminu a histaminoliberátorů (budou k dispozici na webové stránce Čs. dermatologie). Zájemce o další a podrobnější informace odkazuji na recentní články – viz Literatura.
KLASIFIKACE A DIAGNOSTIKA
Kopřivky, zejména chronické, se liší průběhem, diagnostikou, prevencí a léčbou. Současná klasifikace vychází z příznaků, které uspořádané v praktickém několikastupňovém algoritmu vedou ke zpřesnění diagnostiky a volby léčby. Rozděluje chronické kopřivky z hlediska vyvolatelnosti projevů do dvou kategorií – na spontánní a indukovatelné (tab. 1). Doporučené postupy přináší kromě klasifikace a návodů pro diagnostiku i praktické prověřené pokyny pro léčbu. V tomto ohledu umožňují mj. i rozlišení, kdy lze a nelze čekat efekt léčby antihistaminiky – chronické kopřivky spontánní i indukovatelné mají při léčbě antihistaminiky šanci na zlepšení, což neplatí pro urtikariální syndromy, protože zde hraje hlavní roli IL-1, a podobně pro angioedémy zprostředkované bradykininem [12]. Navíc lze při jednotné klasifikaci urtikárií srovnávat výsledky studií s pozitivním dopadem pro výzkum i praxi.
Tab. 1. Klasifikace chronických urtikárií a urtikariálních syndromů 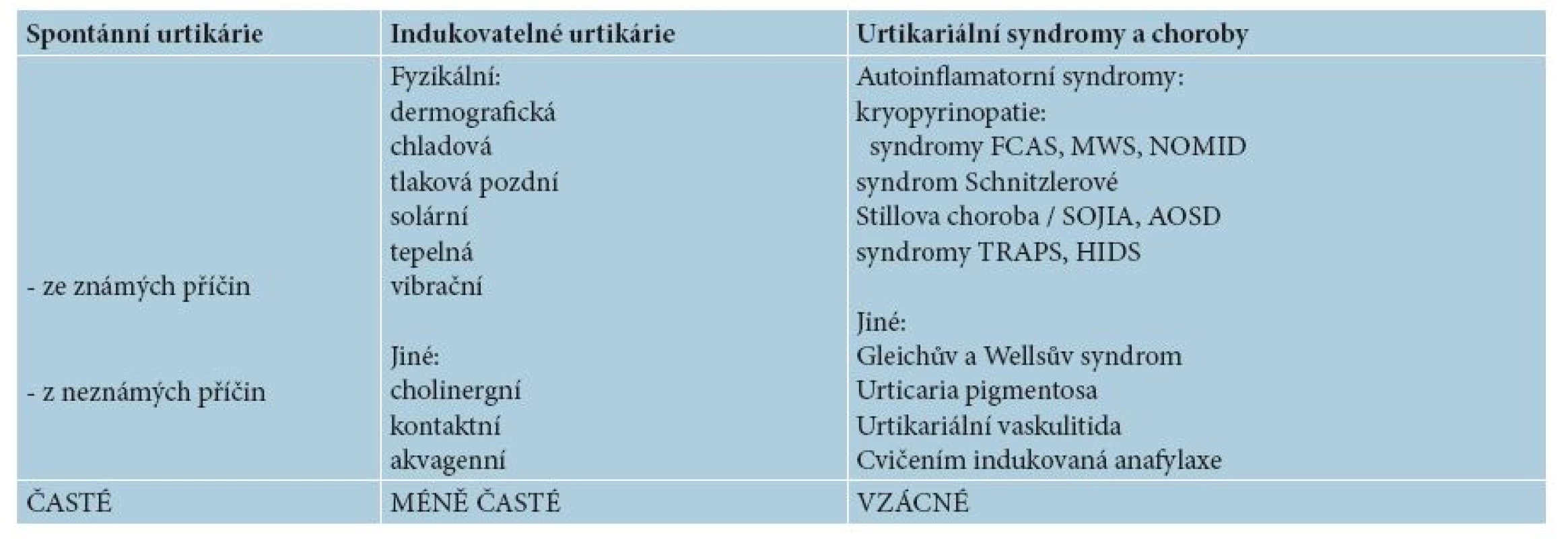
(podle [10, 12, 19, 20]) FCAS = chladová familiární urtikárie, MWS = Muckle-Wellsův syndrom, NOMID = multisystémové zánětlivé onemocnění novorozenců, Stillova choroba v dětství a dospělosti: SOJIA = systémová juvenilní idiopatická artritida a AOSD = adult onset Still disease, TRAPS = syndrom periodické horečky spojovaný s receptorem tumor nekrotizujícího faktoru, HIDS = syndrom hyperimunoglobulinémie D Chronická spontánní urtikárie (CSU), dříve označovaná jako idiopatická [11], patří mezi nejčastější typ chronických urtikárií (> 2/3). Představuje kopřivku, kterou nelze cíleně vyvolat. „Spontánní urtikárie není alergie“ (prof. Maurer), uplatňuje se zde autoreaktivní/autoimunitní etiologie (až v 50 % případů), kdy k uvolnění histaminu dochází především vazbou protilátek proti IgE a proti IgE receptoru na mastocytech a bazofilech, ale též autoaktivací komplementu vzniklými imunokomplexy [14]. K dalším příčinám a spouštěčům patří histaminoliberace/intolerance potravin a léků (snížená funkce či blokování diaminooxidázy, liberátory histaminu, laktózová intolerance, zásah do metabolismu kyseliny arachidonové aj. mechanismy) a infekce [18]. Příčina zůstává nadále neznámá u 50 % CSU. Udává se, že do 1–5 let odezní 50 % CSU, nad 10 let trvá 20 % CSU [12, 13].
Chronické indukovatelné urtikárie (CINDU) tvoří skupinu, kde lze identifikovat fyzikální či jiný spouštěcí faktor a kde lze projevy opakovaně vyprovokovat stejným spouštěčem. Vyskytují se relativně často, ale méně často než CSU. Patří sem klasické fyzikální urtikárie, jako jsou dermografická, pozdní tlaková, vibrační, chladová, tepelná a solární, a jiné, jako jsou akvagenní, cholinergní a kontaktní. Cvičením (námahou) indukovaná kopřivka se již neřadí mezi fyzikální kopřivky, nýbrž k anafylaktickým reakcím („excercize induced anaphylaxis“) [19]. Prognóza fyzikálních kopřivek je velmi variabilní; pokud však nelze spouštěcí faktor dostatečně zmírnit nebo navodit toleranci, s léty obvykle neustupují.
Zvláště se řadí urtikariální syndromy a choroby [12, 19, 20], tedy stavy, kdy je urtikárie jedním z řady příznaků jiné systémové choroby. V pozadí je často autoinflamatorní etiologie, kdy dochází k nekontrolovanému „sterilnímu“ zánětu bez primární účasti mikrobů či autoimunity. Jedná se o řídká multisystémová zánětlivá onemocnění s různými celkovými příznaky, jako periodické febrilie bez zjevné příčiny, nereagující na antibiotickou léčbu, artralgie, myalgie, celková malátnost, únava aj. Patří sem řada syndromů: jednak kryopyrinopatie, jako je chladová familiární urtikárie, Muckle-Wellsův syndrom a multisystémové zánětlivé onemocnění novorozenců, dále syndrom Schnitzlerové, Stillova choroba juvenilní i dospělých, syndrom periodické horečky spojovaný s receptorem tumor nekrotizujícího faktoru, syndrom hyperimunoglobulinémie D, nově označovaný jako syndrom deficience mevalonát kinázy. Tyto urtikárie nesvědí, jsou bez angioedému a histologicky je často přítomný neutrofilní infiltrát (bez leukocytoklázie), proto se též nazývají neutrofilní urtikárie. Tématu autoinflamatorních chorob s kožními příznaky jsme věnovali samostatný článek v Čs. dermatologii [4], kde je možno načerpat podrobnější informace.
Mimo zmíněné se do této zvláštní skupiny kopřivkových syndromů řadí též Gleichův syndrom (epizodický angioedém s eozinofilií) a Wellsův syndrom (granulomatózní dermatitida s eozinofilií), urticaria pigmentosa, cvičením (námahou) indukovaná anafylaxe a konečně i klasická urtikariální vaskulitida. Histologicky se jedná o leukocytoklastickou vaskulitidu (leukocytární infiltrát s rozpadajícím se jádry, fibrinoidní nekróza cévní stěny), kopřivkové projevy trvají déle než 24 hodin, spíše pálí než svědí, často má hemoragický charakter, může zanechávat pozánětlivé erytémy či pigmentace (obr. 1) a angioedém ji doprovází naprosto výjimečně. Může provázet systémový lupus erytematosus, Sjögrenův syndrom, kryoglobulinémii či hypokomplementémii.
Obr. 1. Urtikariální vaskulitida 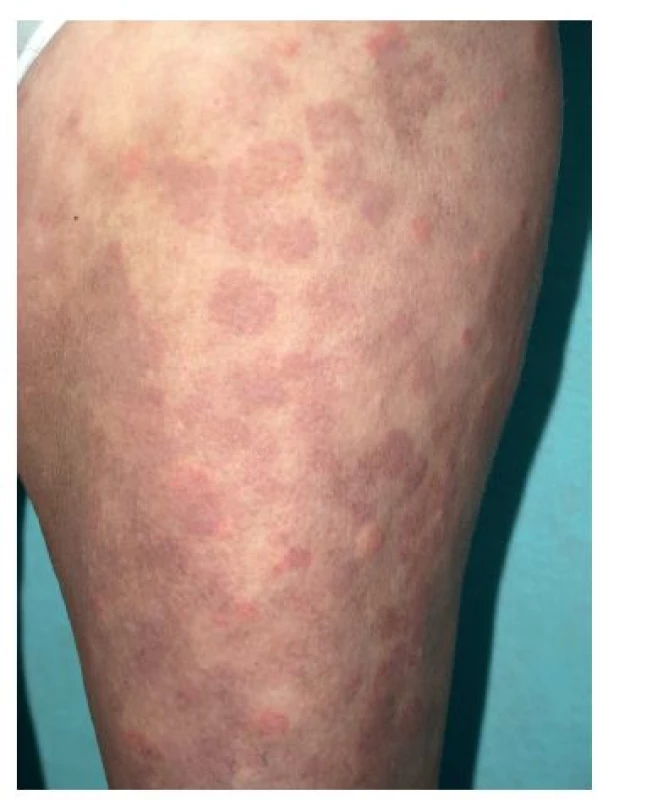
Podobně je zvláště řazen též chronický angioedém bez pomfů. Je jen řídce způsoben výše uvedenými kopřivkami (CSU, CINDU) jako jejich izolovaný projev. Tento „urtikariální angioedém“ [5] se vyskytuje v 10 až 15 % CSU (viz tab. 4). Další histaminem a mediátory mastocytů zprostředkované angioedémy mohou být způsobeny imunologicky cestou IgE, ale i non IgE-alergický angioedém anebo neimunologickou liberací histaminu – pseudoalergický angioedém. Obvykle se objevuje jen nárazově, respektive intermitentně. U chronických angioedémů bez pomfů se ale ve většině případů jedná o jiný mediátor, a to bradykinin. Uplatňuje se nejčastěji u angioedémů po lécích ze skupiny inhibitorů ACE jako tzv. ACEI indukovaný angioedém. Až 30 % angioedémů vyšetřených na lékařské pohotovosti je způsobeno právě ACEI, přičemž 40 % může být život ohrožující. Potenciálně i další nové léky mohou způsobovat bradykininový angioedém [20]. Dále je bradykinin mediátorem u skupiny hereditárních (HAE) a získaných angioedémů (AAE) s abnormitami v oblasti komplementového systému – deficience či dysfunkce inhibitoru C1 složky (HAE I-II) či hemokoagulace – faktoru XII (HAE III). Vrozené HAE I.–III. typu jsou dány mutacemi na 11. chromozomu s autosomálně dominantní dědičností, získané AAE I–II. typu mají v pozadí obvykle vyšší katabolizaci či konzumpci C1 inhibitoru při lymfoproliferativních chorobách. Tento recidivující angioedém postihuje různé partie, nejčastěji horní končetiny, nesvědí, trvá déle než 24 hodin, nemá současně pomfy. Doprovodně mohou být bolesti břicha s nauzeou a zvracením (až imitující náhlou příhodu břišní), rizikový je laryngospasmus s asfyxií. Tento angioedém nereaguje na antihistaminika ani kortikoidy. Příznaky gradují v průběhu 1–3 dnů a odeznívají do 2–5 dnů. Spouštěčem může být malé trauma, rizikové jsou zejména stomatologické výkony, stres, infekce, menstruace, léky jako ACEI či estrogeny. HAE se objevuje před 18. rokem věku, rodinná anamnéza bývá pozitivní, AAE vzniká ve středním věku a bez rodinné anamnézy [5, 10, 12]. Angioedém po lécích ze skupiny nesteroidních antiflogistik (NSAID) je zprostředkován prostaglandiny a leukotrieny [5, 10].
Při vyšetřování pacienta s kopřivkou je žádoucí zachovávat určitý vyšetřovací postup, zaměřený jednak na diferenciální diagnostiku jiných dermatóz a syndromů s pomfy/angioedémem, a jednak na určení typu a závažnosti urtikárie/angioedému [1, 12, 20] – tabulka 2.
Tab. 2. Vyšetřovací postup u chronické urtikárie 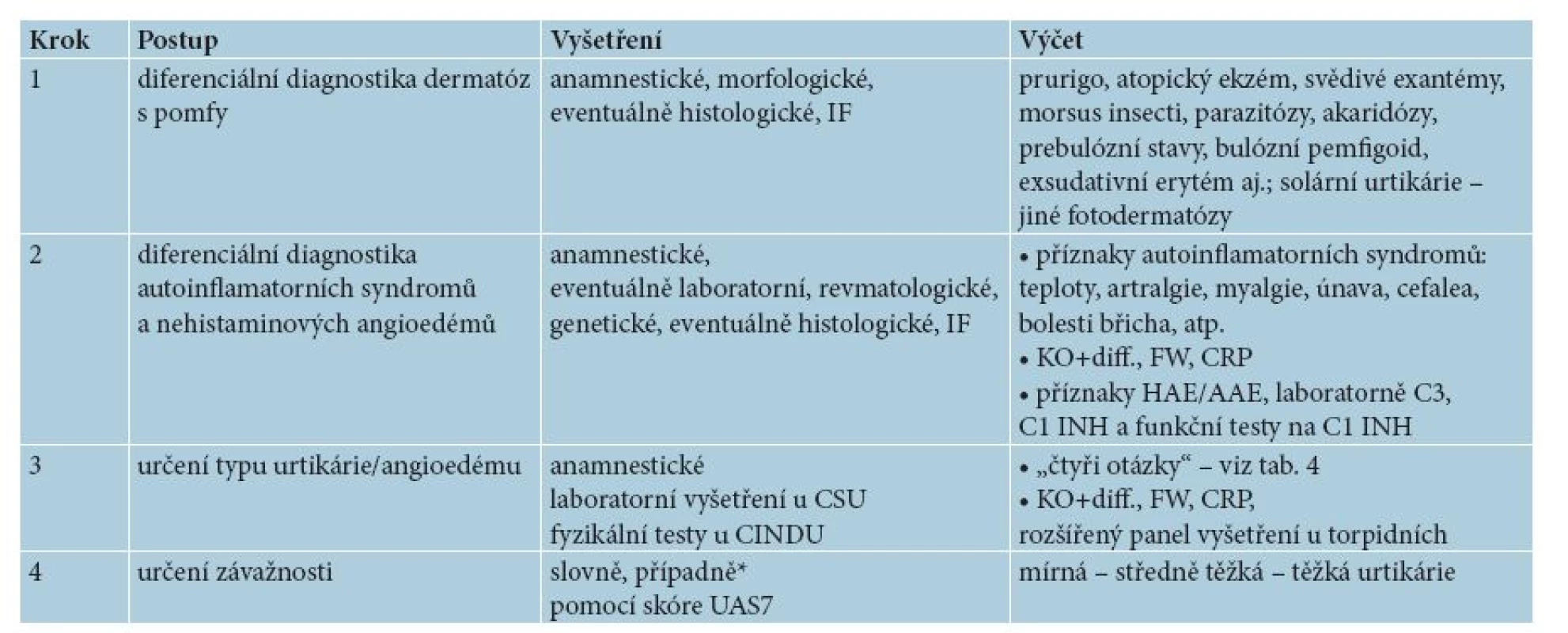
IF = imunofluorescence, KO+diff., FW, CRP = krevní obraz a diferenciální rozpočet leukocytů, sedimentace erytrocytů a C reaktivní protein, CSU = chronická spontánní urtikárie, CINDU = indukovatelné chronické urtikárie, HAE/AAE = hereditární a získaný angioedém, UAS7= týdenní skóre aktivity kopřivky *V centrech biologické léčby je UAS7 obligatorní. Diferenciální diagnostika urtikariálních dermatóz má vyloučit chronické dermatózy, kde se pomfy mohou vyskytnout jako jeden z příznaků, nejsou však hlavní morfou. Je třeba ověřit, zda se skutečně o urtikárii jedná – základem je morfologické vyšetření aspekcí, při pochybnostech i histologické vyšetření, eventuálně imunofluorescenční. Dále je nutno vyloučit urtikariální autoinflamatorní syndromy a nehistaminové angioedémy. Základem je cílená anamnéza na příznaky výše uvedených autoinflamatorních syndromů, u angioedémů je to zejména léková anamnéza, případně i laboratorní vyšetření, zejména při podezření na hereditární a získané angioedémy s abnormitami C1 inhibitoru.
Určení typu urtikárie anebo angioedému vychází z cílené strukturované anamnézy a cílených laboratorních vyšetření, které jsou zaměřeny na nejčastější příčiny, spouštěče a komorbidity. Na tomto základě může lékař určit typ chronické kopřivky, navrhnout plán vyšetření, preventivních opatření a léčby.
Mezi nejčastější příčiny a spouštěče patří léky, zejména nesteroidní antiflogistika (NSAID), především typu COX-1 inhibitorů. Po požití NSAID se kopřivka/angioedém objevuje do 30 minut až šesti hodin. Může se jednat jak o přímý vliv, tj. lékem indukovanou kopřivku, tak o kopřivku, která je prostřednictvím NSAID exacerbována (NECD = NSAID exacerbated cutaneous disease) [13]. Jako analgetika je u pacientů s kopřivkou vhodné použít paracetamol či COX-2 inhibitory, které urtikárii obvykle nezpůsobují. Dále jsou to fokální infekce, potraviny, fyzikální vlivy, tyreopatie, atopie a další – šablona I. a II. pro vyšetřování v ambulancích a centrech.
Základní čtyři dotazy k rozlišení typu chronické urtikárie vyplývající z Doporučených postupů jsou ve schématu 1 a v tabulce 3.
Tab. 3. Základní anamnestický postup a interpretace k určení typu CU [1] ![Základní anamnestický postup a interpretace k určení typu CU [1]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/dfe6f66e6c55564a128341106eb9bcc5.jpg)
*CSU se manifestuje v 50–60 % jen pomfy, ve 30–40 % pomfy a angioedémem a v 10 % pouze angioedémem [12]. Šablona I. Klinické vyšetření pacienta s CU – ambulantní lékař Cíl: diagnostika a diferenciální diagnostika CU, reakce na léčbu 1. a 2. linie, rozvaha, zda je pacient kandidátem léčby 3. linie, respektive biologické léčby 
Šablona II. Klinické vyšetření pacienta s CU – centrum Cíl: ověření diagnózy CSU a posouzení indikace léčby 3. linie, respektive biologické léčby 
Schéma 1. Diagnostický algoritmus u chronické urtikárie (podle [12]) ![Schéma 1. Diagnostický algoritmus u chronické urtikárie
(podle [12])](https://pl-master.mdcdn.cz/media/image/0ff114bdbc5b673f42dd6cb14a1ddd6a.jpg?version=1537792378)
Pokud je na všechny čtyři otázky odpověď negativní, tedy u pacienta se objevuje kopřivka s angioedémem nebo bez něj, nemá doprovodné příznaky autoinflamatorních chorob, projevy nelze opakovaně vyvolat a jednotlivé pomfy netrvají déle než 24 hodin, pak se s velkou pravděpodobností jedná o chronickou spontánní urtikárii.
V praxi může být klasifikace pacienta s chronickou urtikárií komplikována – např. souběh různých typů urtikárie, např. CSU s tlakovou nebo překrývání různých typů fyzikálních kopřivek, anebo souběh kopřivky s jinou chorobou, např. s histaminovou intolerancí, což může vést k atypickému obrazu a průběhu, a tak ztížené diagnostice i odlišné reakci na léčbu.
Základní rozlišovací otázky a postupy ke zjištění typu angioedému bez pomfů, vyplývající z doporučených postupů, jsou uvedeny v tabulce 5. Týkají se vyloučení nebo potvrzení lékové či komplementové etiologie (C1 INH). Žádný bradykininem zprostředkovaný angioedém nezpůsobuje kopřivku; je netypickým a vysloveně vzácným projevem u pacientů s kopřivkou u autoinflamatorních chorob; výjimečně se může vyskytovat u podskupiny pacientů s urtikariální vaskulitidou [12]. Výskyt angioedému u chronické urtikárie ukazují tabulky 3 a 4. Označení „idiopatický“ angioedém přísluší případům bez rodinné a lékové anamnézy, bez abnormit v C1 inhibitoru, nereagující na antihistaminika, kortikoidy či adrenalin. Patogeneze je zde neznámá, mediátorem není ani histamin, ani bradykinin [10, 12, 19, 20].
Tab. 4. Výskyt pomfů/angioedému u různých typů urtikárie a angioedému [12] ![Výskyt pomfů/angioedému u různých typů urtikárie a angioedému [12]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/56c4e85a82d4b9e1f65a89c1fdaa564b.jpg)
*kromě pozdní tlakové, která nemívá klasické pomfy (nýbrž bolestivý edém kůže [17]) **kromě dermografické a cholinergní, které se neprojevují angioedémem Tab. 5. Rozlišovací dotazy u recidivujícího angioedému bez pomfů [1] ![Rozlišovací dotazy u recidivujícího angioedému bez pomfů [1]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/fcfdfafedd00ea50ad392fbd4afc77f3.jpg)
ACEI = inhibitory angiotenzin konvertujícího enzymu, NSAID = nesteroidní antiflogistika, HAE/AAE = vrozený a získaný angioedém s abnormitami inhibitoru C1 složky komplementu *Angioedém se po vysazení ACEI může ještě nějakou dobu tvořit, ne však v řádu měsíců. **Diferenciální diagnostika angioedémů: a) histaminové, respektive způsobené mediátory mastocytů: urtikariální, alergický/pseudoalergický; b) nehistaminové – polékový (ACEI indukovaný, NSAIDS), HAE/AAE, idiopatický. Zhodnocení závažnosti urtikárie vychází v běžné praxi ze slovního popisu intenzity, rozsahu a průběhu kopřivky (frekvence výsevů, délka remise, reakce na léčbu, kvalita života). Urtikárii lze z hlediska závažnosti hodnotit jako jiné kožní choroby ve škále mírná, středně těžká a těžká. K tomu lze i v běžné praxi použít objektivní numerické hodnocení, tzv. UAS skóre (Urticaria Activity Score), nejčastěji v týdenním horizontu jako UAS7, jež nabývá hodnot 0–42 (Kalendář s. 205 a Týdenní hodnocení kopřivky s. 204). Toto hodnocení není formální, protože u CU, na rozdíl od jiných kožních chorob, jsou projevy prchavé a často je pacient při vyšetření v ordinaci asymptomatický. A tak je důležitý záznam průběhu choroby samotným pacientem („patient related outcomes“), což UAS7 umožňuje – sleduje denně počet pomfů a intenzitu pruritu.V klinických studiích a v centrech biologické léčby CU je používání tohoto skórovacího systému obligatorní, podobně jako např. PASI skóre u psoriázy. Skóre UAS7 se používá jak k hodnocení závažnosti (tab. 6), tedy při rozhodování o volbě léčby, ale i k hodnocení léčebného efektu. Toto skóre nelze použít pro indukovatelné urikárie a angioedém [17].
Tab. 6. Hodnocení závažnosti urtikárie podle hodnot UAS7 [17] ![Hodnocení závažnosti urtikárie podle hodnot UAS7 [17]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/bb2c26f81d4504ecfe2e17efa557fe33.jpg)
Laboratorní a další vyšetření
V případech, kde ze samotné anamnézy a klinického vyšetření nelze usoudit na typ urtikárie a při pátrání po spouštěčích, komorbiditách a obecně příčinách těžkého a úporného průběhu, jsou vhodná laboratorní vyšetření a další testy. Doporučené postupy upřednostňují co nejméně vyšetření [19, 20]. Základem je pátrání po zánětlivých chorobách (infekční, autoimunitní, autoinflamatorní) – vyšetřit krevní obraz a diferenciální rozpočet leukocytů, sedimentaci erytrocytů a C reaktivní protein. Z jednoduchých fyzikálních testů lze v běžné ambulanci provést vyšetření dermografismu – u atopiků bývá bílý, u časné tlakové/dermografické urtikárie plastický. Kromě klasického provedení lze též lze použít tzv. FrickTest® (plastová pomůcka s čtyřmi výstupky různé výšky) ke kvalitativní a semikvantitativní diagnostice dermografické urtikárie.
Další vyšetření jsou prováděna cíleně na základě anamnézy, příznaků a s vědomím co a proč chceme zjistit či vyloučit. Týká se pacientů s dlouho trvající anebo těžkou CU. Laboratorní vyšetřování se provádí zejména u CSU. U indukovatelných kopřivek (CINDU) se laboratorní vyšetřování běžně neprovádí [13], neboť příčiny/spouštěče jsou zřejmé z anamnézy a fyzikálních testů. Mediátorem je zde též histamin, ale mechanismy jeho uvolnění jsou jiné než u CSU. Pouze u chladové urtikárie se provádí KO + diff., FW, CRP a fokusy k vyloučení syndromu FCAS a u sekundární chladové urtikárie pak kryoglobuliny [13, 20].
Z hlediska komorbidit a případných spouštěčů CU lze provést základní screening na infekce – fokusy a autoimunitu (tab. 7).
Tab. 7. Základní vyšetření na záněty + základní screening fokusů a komorbidit u CSU 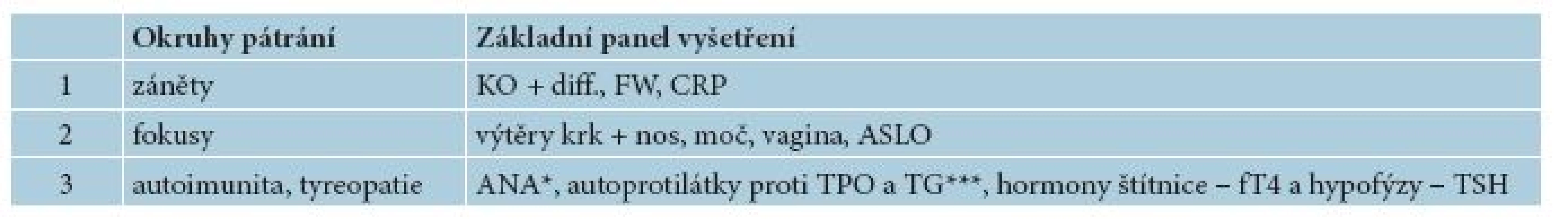
KO + diff. = krevní obraz a diferenciální rozpočet leukocytů, FW = sedimentace erytrocytů, CRP = C reaktivní protein, ANA = antinukleární autoprotilátky, TPO = thyreoperoxidáza, TG = thyreoglobulin *ANA pozitivita koreluje se závažností CU a může predikovat nedostatečnou reakci na antihistaminika [9]. **Výskyt autoprotilátek proti TG a TPO často koreluje s výskytem autoprotilátek proti IgE a IgE receptoru [9]. V rozšířeném provedení lze, ve spolupráci s příslušnými specialisty, doplnit o následující vyšetření [5, 19, 20]:
1. fokusy – stolice na parazity a H. pylori (HP), sérologie hepatitid (HAV, HBV, HCV), stomatologické fokusy.
2. atopie/alergie – k identifikaci alergie 1. typu, tedy alergenů jako spouštěčů: specifické IgE – panel potravin a aeroalergenů, prick testy s aeroalergeny (na specializovaných alergologických pracovištích se provádí i s potravinami). Při podezření na kontaktně alergický původ se provádí i prick a epikutánní testy se suspektním kontaktním alergenem.
3. autoimunita – autoreaktivní urtikárie bývá asociována s autoimunitními chorobami, jako jsou vitiligo, perniciózní anémie, revmatoidní artritida, diabetes mellitus I. typu, autoimunitní tyreoiditida, celiakie a další [14]. Pro screening těchto chorob lze provést další vyšetření, optimálně v koordinaci s imunologem, jako jsou: autoprotilátky EMA, a-tTG, anti gliadin, RF, ENA, dsDNA, SSA, SSB, Scl 70 aj. Případně další vyšetření jako jsou profil imunoglobulinů, kryoglobuliny u sekundární chladové urtikárie, paraproteiny u myelomu a jiné.
Přímý průkaz funkčních autoprotilátek proti IgE a receptoru pro IgE u autoimunitní urtikárie lze provést metodou ELISA či WB, avšak takováto vyšetření nejsou u nás ani v zahraničí zatím běžně dostupná [10, 12]. Pro nepřímý průkaz těchto funkčních protilátek slouží i. d. kožní test s autologním sérem (ASST = autologous serum skin test) anebo test BHRA (basophil histamine release assay) [10, 13, 15, 19, 20], které se u nás též rutinně neprovádějí.
Při podezření na urtikariální vaskulitidu se provádí vyšetření ANA, CIK, C3, C4, C1q, případně protilátky proti C1q a další vyšetření dle imunologie.
4. intolerance – při podezření na účast histaminu a jiných biogenních aminů a jejich liberátorů v potravě zavést jako eliminační test dietu s nízkým obsahem histaminu a jeho liberátorů, minimálně na 3 týdny. Při podezření na histaminovou intoleranci lze provést vyšetření koncentrace a aktivity diaminooxidázy (DAO) [6], při podezření na systémovou mastocytózu vyšetření koncentrace tryptázy [19, 20].
5. fyzikální testy – pokud není dostačující anamnéza, lze při podezření na fyzikální příčiny provést různé fyzikální testy (chladový, tepelný, tlakový a další), jejich provedení ale není standardizované. Orientační popis metodiky je uveden ve zmiňovaných doporučených postupech [19], v české odborné literatuře lze čerpat z práce doc. Viktorinové [16]. U potravin a léků pak lze provést provokační/expoziční testy. Zlatým standardem je dvojitě slepý, placebem kontrolovaný potravinový expoziční test. Všechny provokační testy je třeba provádět obezřetně a mít zajištěn rychle dostupný komplement pro urgentní léčbu.
6. angioedém hereditární (HAE) – při podezření se provádí vyšetření komplementu, jako jsou hladina C4, hladina C1 INH a funkční testy na C1 INH. Pokud jsou hodnoty C4 v normě, měl by být odběr zopakován, a to v době ataky angioedému, kdy je u HAE I a AAE hladina C4 snížená. Hodnoty C1 INH jsou snížené u HAE I a AAE, u HAE II jsou normální, avšak je snížená jeho funkce, u HAE III jsou hladina i funkce C1 INH normální. Při podezření na získaný angioedém (AAE) se provádí též stanovení C1q (proteolytický komplementový enzym) – u HAE je hladina v normě, u AAE snížená. U nejednoznačných předchozí testů lze provést vyšetření protilátek proti C1q (bývají pozitivní u AAE), jsou-li tyto testy dostupné. Hodnoty C3 a CH50 bývají v normě, proto není smysluplné je vyšetřovat. Při pozitivitě rodinné anamnézy na HAE pak genetické vyšetření na mutace – sekvenování genu SERPING 1 (HAE I a II) nebo genů pro faktor XII (HAE III) [5, 10, 20].
Alergický, pseudoalergický, ACEI indukovaný a idiopatický angioedém nemají odchylky v sérových hladinách komplementových proteinů [10]. Vzhledem ke vzácnosti HAE a AAE a nutnosti rutinní znalosti problematiky, je třeba optimální provedení a především interpretaci těchto vyšetření svěřit alergoimunologovi, popř. hematologovi.
7. autoinflamatorní syndromy – při podezření se provádí příslušná konzilia a genetická vyšetření k potvrzení či vyloučení jednotek, jako jsou: syndrom Schnitzlerové, Stillova choroba v dětství (systémová juvenilní idopatická artritida – sJIA) a v dospělosti (AOSD) a kryopyrinopatie, jako je FCAS, Muckle-Wellsův syndrom, NOMID. Méně často pak HIDS a TRAPS [20].
8. histologické vyšetření – včetně imunofluorescence je plně indikováno, pokud jednotlivé pomfy trvají déle než 24 hodin a obecně při podezření na urtikariální vaskulitidu.
Výjimečně se provádí u CU onkologický screening [19].
Jako prognosticky nepříznivé faktory [7] pro průběh chronické urtikárie se uvádí: selhání léčby H1 antihistaminiky v běžném dávkování, trvání nad šest měsíců před návštěvou lékaře, přítomnost angioedému, fyzikální urtikárie, průkaz autoprotilátek – štítnice, IgE, IgER, pozitivita ASST a BHRA, hypertenze, známky aktivace vnější cesty hemokoagulační kaskády (fragmenty protrombinu) nebo fibrinolýzy (D dimery).
LÉČEBNÝ POSTUP
Jako u všech chronických chorob je cílem získat nad onemocněním kontrolu, zmírnit příznaky, zabránit vzniku komplikací a snížit dopad na kvalitu života. Pro celkové zvládání kopřivky je proto významná i nefarmakologická léčba, tedy edukace o chorobě, možnostech a limitacích léčby, latenci nástupu a rozsahu efektu léčby („realistická očekávání“), prognóze, preventivních a režimových opatřeních a psychosomatický přístup lékaře k pacientovi. Ohledně podrobností odkazuji na přehledný článek o terapeutické edukaci [2]. Podle doporučených postupů je cílem léčby u chronické urtikárie kompletní vymizení příznaků [19, 20]. Obecně lze léčebná a preventivní opatření shrnout do tří bodů, podobně jako u jiných chorob s účastí mastocytů [13, 19, 20]:
- pátrání a vyhýbání se příčinám a spouštěčům,
- symptomatická farmakologická léčba snižující uvolňování mediátorů mastocytů nebo jejich působení na cílový orgán,
- eventuální navození tolerance.
Ve farmakoterapii se podle zmíněných doporučených postupů [19] doporučuje třístupňové schéma léčby, a to podle reakce na léčbu nesedativními H1 antihistaminiky, prověřenými pro léčbu CU (schéma 2).
Schéma 2. Terapeutický algoritmus u chronické urtikárie (podle [18]) ![Schéma 2. Terapeutický algoritmus u chronické urtikárie (podle [18])](https://pl-master.mdcdn.cz/media/image/8d9d568b446e2b7a3121a6546b33dcd4.jpg?version=1537795211)
Nesedativní antihistaminika je vhodné podle doporučených postupů podávat kontinuálně (ne pouze intermitentně, nárazově, podle potřeby, při výsevech), protože jen kontinuální podávání vede ke zmírnění průběhu, tedy snížení frekvence výsevů, rozsahu a intenzity. Jako prověřená „moderní“ antihistaminika pro léčbu CU i ve 2–4 vyšších dávkách jsou udávána tato (abecedně): bilastin, cetirizin/levocetirizin, desloratadin/loratadin, fexofenadin a rupatadin [13, 19, 20].
Léčba sedativními antihistaminiky nebo léčba vyššími dávkami neprověřených antihistaminik se z bezpečnostních důvodů u CU nedoporučuje. Léčba celkovými kortikoidy se pro známé nežádoucí účinky dlouhodobě také nedoporučuje; jejich uplatnění je v nárazové léčbě při exacerbaci, po dobu maximálně 10 dnů.
Tato doporučení nejsou v praxi stále ještě dostatečně zažitá, přestože se objevila v odborné literatuře již před osmi lety. Při malém efektu se antihistaminika v běžném dávkování používají spíše jako kombinace různých antihistaminik navzájem, než aby se zvyšovala dávka jednoho antihistaminika. Teoretickým vysvětlením, proč část pacientů s CU nereaguje na standardní dávky antihistaminika, ale reaguje až na dávky vyšší, je fakt, že mohou mít funkční změny v expresi a/nebo afinitě H1 receptorů. Kombinace sice nejsou „zapovězeny“, ale upřednostňuje se zvyšování dávky prověřeného nesedativního antihistaminika, a to zejména pro lepší bezpečnost při stejně dobré, ne-li vyšší účinnosti [8, 13, 19, 20]. Z hlediska farmakokinetiky totiž při kombinaci antihistaminik mezi sebou (různých generací či H1 a H2) nedochází ke kvalitativnímu zvýšení účinnosti, ale častěji pouze k blokování či snížení metabolizace jednoho či druhého antihistaminika. To s sebou nese i otázky tolerance a bezpečnosti takovéto kombinace [1, 8].
U dětí je častější urtikárie akutní než chronická. Nicméně se udává, že u dětí trpících opakovaně na akutní urtikárie se v 20–30 % později vyvine urtikárie chronická [13]. Podle aktuálních Doporučených postupů se má u dětí s CU postupovat obdobně jako u dospělých. Nesedativní H1 antihistaminika 2. generace s prověřeným účinkem u CU jsou ovšem limitována věkem – tabulka 9. Ve studiích a kazuistikách lze najít používání i v nižším věku, rozhodnutí o indikaci a dávce je v takových případech individuální. Bezpečnost vyššího dávkování v pediatrické populaci je prověřena zatím u dvojic loratadin/desloratadin a cetirizin/levocetirizin [13]. Studie jsou prováděny obvykle s originálními preparáty, takže jak dolní věková hranice, tak bezpečnost vyšších dávek u dlouhodobého používání se mohou u generických antihistaminik výrazně lišit (viz SPC).
Tab. 8. Rozšířený panel vyšetření u CU 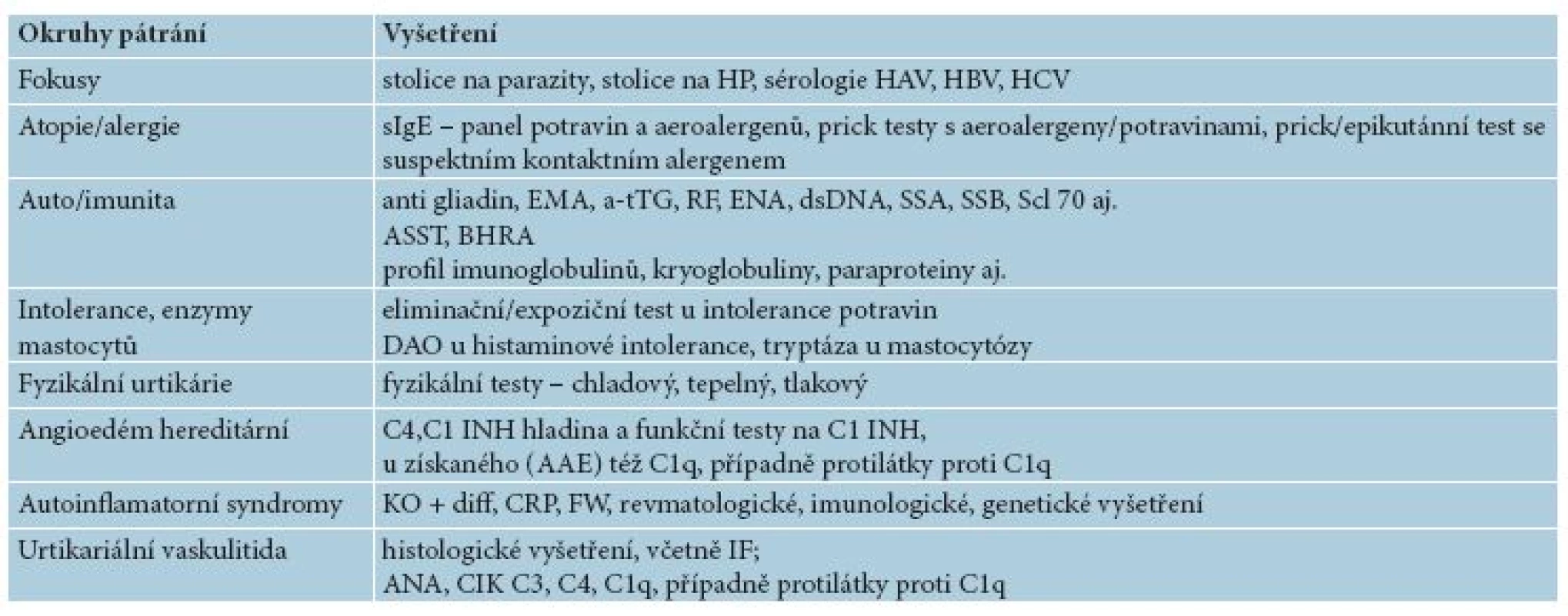
Tab. 9. Nesedativní H1 antihistaminka u CU – originální preparáty v ČR 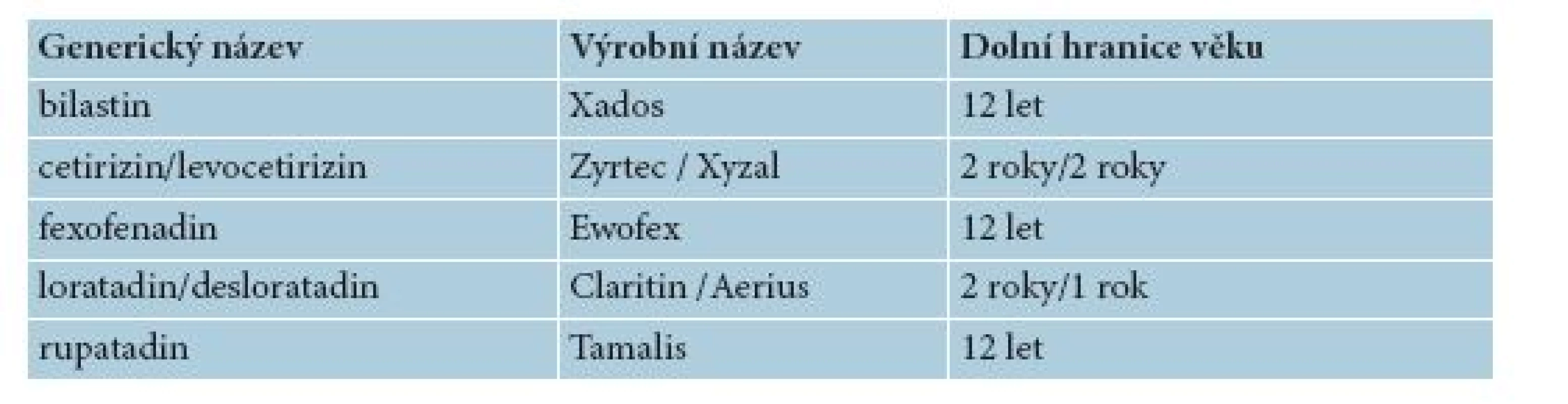
U gravidních a v laktaci se postupuje z hlediska bezpečnosti obdobně jako u dětí, konkrétně se udávají loratadin/desloratadin a cetirizin/levocetirizin. Všechna H1 antihistaminika se ale dostávají v nízkých koncentracích do mateřského mléka. Podle doporučených postupů [19] se mají používat pouze nesedativní H1 antihistaminika – mají přijatelné riziko, patří do kategorie B (studie na zvířatech neprokázaly riziko pro plod, nejsou k dispozici studie u těhotných žen). Při zvažování použití vyšších dávek je třeba postupovat opatrně, protože bezpečnostní studie u této populace dosud nebyly prováděny. U loratadinu je třeba z hlediska bezpečnosti mít na paměti, že se metabolizuje v játrech [13, 19, 20].
U starší populace nejsou žádné studie s antihistaminiky u CU k dispozici, natož s vyšším dávkováním. Základními léky jsou opět nesedativní H1 antihistaminika, ale je třeba je pečlivě a individuálně volit vzhledem ke snížené jaterní metabolizaci a i sníženému vylučování ledvinami ve vyšším věku, což je třeba brát v potaz např. u loratadinu a desloratadinu [13]. Také lékové interakce – tedy antihistaminikum s pacientovou interní medikací – mohou mít nežádoucí vliv jak na účinnost léčby, tak zejména na její bezpečnost. Z tohoto pohledu se jako relativně nejšetrnější pro tuto populaci jeví bilastin, který se nemetabolizuje přes cytochrom P450 (viz SPC).
Biologický lék omalizumab je v ČR schválen jako léčba 3. linie jen pro těžkou CSU, tedy s UAS7 ≥ 28, a to u osob nad 12 let (indikační kritéria viz Šablona II.). Ve studiích byla vstupním kritériem středně těžká až těžká CSU, tedy s nižším UAS7 ≥ 16 (17). Jedná se o monoklonální humanizovanou protilátku proti IgE, podává se pouze parenterálně, a to v intervalu jednoho měsíce v dávce 300 mg s. c. Tento lék je v klinické praxi již od roku 2005, a to v léčbě těžkého astmatu, takže je k dispozici solidní množství bezpečnostních dat o jeho používání. Zatím je schválen pro CSU, ve studiích se ukazují příznivé výsledky i u těžkých CINDU [11, 13, 17].
Antileukotrien montelukast a imunosupresivum cyklosporin A jako další léky 3. linie se v indikaci CU v ČR pohybují v kategorii „off label use“, nicméně doporučené postupy [19] na základě četných studií, kazuistik i denní praxe jejich použití odůvodňují. V dětské populaci je montelukast v ČR schválen od šesti měsíců věku (preskripční limitace na alergologa), cyklosporin A od jednoho roku věku (viz SPC).
Léčebné schéma je doporučováno jak pro CSU, tak pro CINDU, avšak zde s ohledem na nedostatek studií nepanuje pro volbu dalších léků konsenzus. Pacienti s CINDU – fyzikální a další indukovatelné urtikárie – obvykle potřebují vyšší dávky antihistaminik. Pokud mají anafylaktické reakce v anamnéze (chladová kopřivka, námahou indukovaná anafylaxe), je třeba je vybavit pohotovostním balíčkem s adrenalinem v autoinjektoru, nesedativním antihistaminikem, případně i kortikoidem.
U těžkých, refrakterních CINDU se kromě výše uvedené 3. linie léčby uvádějí na základě kazuistik či malých studií pro velmi těžké případy také: etanercept (anti TNF) a anakinra (anti IL-1) u chladové urtikárie, anticholinergika, betablokátory, botulotoxin, danazol u cholinergní urtikárie. U solární urtikárie se kromě indukce tolerance pomocí UVA či NBUVB fototerapie uvádí též plazmaferéza či IVIG, celkové kortikoidy, chlorochin a analoga MSH. Pozdní tlaková urtikárie, zejména při souběhu s CSU a angioedémy, bývá těžko zvladatelná. Pokud nereaguje dostatečně na čtyřnásobné dávky nesedativních H1 antihistaminik, a ani na přidání montelukastu, lze zvážit i celkové kortikoidy, na které reaguje. Vzhledem k jejich dlouhodobým nežádoucím účinkům se volí intermitentní režimy podávání kortikoidů a zkouší se přidat i kortikoidy šetřící léčiva, např. chlorochin, kumariny, anti TNF biologika, sulfony, metotrexát, IVIG [13]. V doporučených postupech [19] nejsou pro nedostatek údajů o účinnosti a bezpečnosti (evidence based medicine) podrobněji zmiňovány výše uvedené další možnosti z odborné literatury, které jsou kromě fototerapie NBUVB či PUVA, v kategorii „off label use“.
Léčba nehistaminových angioedémů [5, 10, 13] doznala též pokroku – u bradykininem zprostředkovaných angioedémů, tedy především u ACEI indukovaného angioedému a HAE/AAE se používá k akutní léčbě i profylaxi před rizikovými výkony koncentrát C1 inhibitoru, dále ikatibant (antagonista receptoru pro bradykinin) a ekalantid (inhibitor kalikreinu). A kde nejsou dostupné, tak se používá dosavadní léčba plazmou. Z akutních intervencí při edému horních cest dýchacích je nutná intubace, při progresi tracheotomie. Kde není dostupný koncentrát C1 INH se z preventivních léčiv nadále používají pro krátkodobou i dlouhodobou profylaxi androgeny jako danazol, které zvyšují syntézu C1 inhibitoru v játrech. Pečlivé klinické a laboratorní monitorování je vzhledem k nežádoucím účinků nutné. Dále se s menší účinností používají antifibrinolytika jako kyselina tranexamová, zejména u případů s kontraindikací androgenů. Pro léčbu případné hypertenze se u těchto pacientů doporučuje zvolit lék ze skupiny antagonistů receptoru pro angiotenzin (ARB), které angioedém prakticky nezpůsobují [13].
Hodnocení účinku a průběhu léčby
Hodnocení léčebné odpovědi, tedy účinnosti léčby včetně preventivních opatření, lze v běžné praxi provádět slovně, např. ve čtyřstupňové škále: zhojeno – zlepšeno – nezlepšeno – zhoršeno. I v ambulantní praxi lze provést hodnocení rovnou pomocí skóre UAS7. K tomu lze využít pacientových záznamů ze strukturovaného kopřivkového kalendáře (s. 205). V klinických studiích a centrech biologické léčby CU je používání skóre UAS7 k hodnocení účinku zkoumaných léčiv včetně biologik obligatorní – týdenní formulář UAS7, vytvořený pro účely dokumentace pro zdravotní pojišťovny (s. 204).
Podle jednání se zdravotními pojišťovnami a po schválení výborem ČDS ČLS JEP budou Centra pro léčbu chronické urtikárie lokalizována na stejných dermatologických klinikách či odděleních, jako jsou dosavadní Centra pro biologickou léčbu psoriázy, personálně budou obsazena lékaři z oblasti dematoalergologie. Do centra může pacienty při splnění požadovaných kritérií (viz Šablona I) posílat ambulantní dermatolog, alergolog, ale i praktický lékař, pediatr, eventuálně i další.
V zahraničí existuje analogicky pro hodnocení angioedému též skóre AAS (Angioedema Activity Score). Pro hodnocení „kontroly nad chorobou“ pak dotazník Urticaria Control Test (UCT) a též dotazník pro hodnocení kvality života u chronické urtikárie (CU-Q2oL), které v ČR nejsou pro český jazyk zatím validovány. Oba ale dobře korelují s UAS7 [17], takže nejsou nezbytné.
Biomarkery pro posouzení aktivity choroby a reakci na léčbu zatím nejsou k dispozici. Perspektivními se zdají být D-diméry a substance P, je však třeba dalšího výzkumu [17].
ZÁVĚR
Léčba a zvládání chronické urtikárie jsou náročné a svízelné, žádný stávající lék není totiž plně uspokojivý. Je to pochopitelné vzhledem k heterogenitě příčin, mediátorů, spouštěcích vlivů a dalších kofaktorů. Oproti předchozím dobám ale již existují doporučené postupy poskytující lékařům objektivně prověřené vodítko v diagnostice i léčbě – zjednodušily anamnézu vytipováním zásadních otázek pro detekci příčin a spouštěcích faktorů a volbu léčby, zakomponovaly do klasifikace a vyšetřovacího algoritmu nové poznatky o urtikariálních syndromech a angioedému, navrhly racionální postup pro laboratorní vyšetřování, v léčbě prověřily třístupňové schéma podle reakce na léčbu antihistaminiky a další pozitiva.
Za základní pilíř lze považovat anamnézu jako nejlepší diagnostický prostředek ke zjištění typu chronické kopřivky; léky první volby jsou nesedativní H1 antihistaminika, a to i ve zvýšeném dávkování. Výzkum na poli farmakoterapie přinesl také velký pokrok – kromě nových antihistaminik došlo k uvedení nového léku biologické povahy do klinické praxe, tedy omalizumabu jako léku 3. volby, což pomůže zlepšit zvládání choroby u nejtěžších případů.
V případech, kde zvolená léčba nevede ke zlepšení průběhu, je třeba hledat rezervy v diagnostice, prevenci i léčbě. Pomýšlet i na souběh s jinými chorobami, problém pojímat v širších souvislostech a využívat mezioborové spolupráce.
Individuální případy však vyžadují individuální přístup. Lékař by proto měl nejen sledovat recentní odbornou literaturu a začlenit tyto poznatky do své praxe, ale také mít na paměti, že edukace pacienta a psychosomatický přístup jsou ke zvládnutí chronické kopřivky téměř stejně důležité jako farmakoterapie. K pacientovi je třeba přistupovat individuálně, spolupracovat s ním, mít partnerský přístup a nezapomínat na opakovanou edukaci a podporu.
Každý lékař je v diagnostice i léčbě individualitou z hlediska znalostí, schopností a přístupu k pacientovi. Tyto materiály vycházejí ze současných doporučení a specializované praxe, lékaři mají sloužit jako pomoc a vodítko v náročné problematice, jako příručka pro vyšetřování a léčbu pacientů s chronickou urtikárií v každodenní praxi – jak v běžné ambulanci, tak v klinickém centru. Vlastní využití a případné modifikace jsou na individuálním rozhodnutí lékaře. Nicméně používání doporučených postupů vede u pacientů s chronickou kopřivkou jednoznačně ke zlepšení péče a léčby.
Poděkování patří všem kolegům, kteří se na konečné podobě těchto materiálů podíleli.
Adresa pro korespondenci:
MUDr. Nina Benáková, Ph.D.
Dermatologická ordinace Immunoflow Praha
e-mail: nina.benakova@email.cz
Zdroje
1. BENÁKOVÁ, N. Chronické urtikarie v teorii a praxi. Alergie, 2014, 2, s. 28–32.
2. BENÁKOVÁ, N. Terapeutická edukace v dermatologii. Čes-Slov. Derm., 2015, 1, s. 1–44.
3. BRODSKÁ, P. Kopřivka, diagnostika, léčba. Čes-Slov. Derm. 2014, 2, s. 55–64.
4. CETKOVSKÁ, P., BENÁKOVÁ, N. Autoinflamatorní syndromy s kožními projevy. Čes-Slov. Derm., 2015, 3, s. 93–104.
5. CRAIG, T. et al. WAO guideline for the management of hereditary angioedema. WAO Journal, 2012, 5, p. 182–199.
6. FUCHS, M. Histaminová intolerance, snížená aktivita diaminooxidázy. Alergie, 2011, 3, s. 229–233.
7. GREENBERGER, P. A. Chronic urticaria – new management options. World Allergy Org. J., 2014, 7, 31.
8. CHURCH, M. K., MAURER, M. H1 antihistamines and urticaria – how can we predict the best drug for our patient? Clin. Exp. Allerg., 2012, 42, p. 1423–1429.
9. MAGEN, E. et al. Clinical laboratory characteristics of ANA-positive chronic idiopathic urticaria. Allergy Astma Proc., 2015, 36, p. 138–134.
10. MAURER, M., PARISH, L. C. The dermatology view of hereditary angio-oedema: practical diagnostic and management considerations, JEADV, 2013, 27, p. 133–141.
11. MAURER, M. et al. Chronic idiopathic urticaria is no longer idiopathic: time for an update. Br. J. Dermatol., 2013, 168, p. 445–456.
12. MAURER, M. et al. Practical algorithm for diagnosing recurent wheals or angioedema. Allergy, 2013, 68, p. 816–819.
13. MAURER, M., CHURCH, M. K. Management and treatment of chronic urticaria. JEADV, 2015, 29, Suppl. 4, p. 16–32.
14. KONSTANTINOU, G. N., ASERO, R., FERER, M. et al. AACI taskforce position paper: evidence for autoimmune urticaria and proposal for defining diagnostic criteria. Allergy, 2013, 68, p. 27–36.
15. MLYNEK, A., MAURER, M., ZALEWSKA, A. Update of chronic urticaria: focusing on mechanism. Curr. Opin. Allergy Clin. Immunol., 2009, 6, p. 1–5.
16. VIKTORÍNOVÁ, M. Fyzikální kopřivky. Ref. výběr z dermatovenerologie, 2012, 1, p. 79–88.
17. WELLER, K., ZUBERBIER, T., MAURER, M. Chronic urticaria: tools to aid the diagnosis and assessment of disease status in daily practice. JEADV, 2015, 29, Suppl. 4, p. 38–44.
18. ZUBERBIER, T. et al. EAACI/GA(2)LEN/EDF/WAO guideline for the definition, classification and diagnosis of urticaria. Čes-Slov.Derm., 2007, 1, Suppl. 1, S1–16.
19. ZUBERBIER, T. et al. EAACI/GA(2)LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria: the 2013 revision and update. Allergy, 2014, 7, p. 868–887.
20. ZUBERBIER, T. et al. GA(2)LEN Pocket guide. EAACI/GA(2)LEN/EDF/WAO Urticaria guidelines. GA(2)LEN e.V., Berlin 2014. DOI:10.111/all.12313.
Štítky
Dermatológia Detská dermatológia
Článok vyšiel v časopiseČesko-slovenská dermatologie
Najčítanejšie tento týždeň
2015 Číslo 5- Na český trh přichází biosimilar adalimumabu s prokázanou terapeutickou ekvivalencí
- Nehoňte nemocné s mMCC od čerta k ďáblu!
- První a jediná schválená imunoterapie vzácného agresivního karcinomu kůže
- Screening malignit u pacientů s dermatomyozitidou
- Jakým způsobem hydroresponzivní krytí napomáhá hojení rány?
-
Všetky články tohto čísla
- Úvodník
- Difuzní řídnutí vlasů u žen v klinické praxi
-
DOŠKOLOVÁNÍ LÉKAŘŮ
KONTROLNÍ TEST - Závislost mezi senzibilizací na inhalační alergeny a výskytem bronchiálního astmatu, alergické rýmy a dalších parametrů u pacientů s atopickým ekzémem
-
Současné praktické postupy pro vyšetřování a léčbu chronické urtikárie
Aktualizovaný přehled a interpretace doporučených postupů pro praxi - Mid-dermální elastolýza
- Klinický případ: svědivý exantém v graviditě
-
Zápis ze schůze výboru ČDS
konané dne 17. září 2015 -
Poznatky ze Specialty Dermatology Academy,
Dublin, 25.-27.6.2015 -
Spomienka na MUDr. Antona Bakytu, CSc.
(1936–2015) - Odborné akce 2015
- Česko-slovenská dermatologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Difuzní řídnutí vlasů u žen v klinické praxi
-
Současné praktické postupy pro vyšetřování a léčbu chronické urtikárie
Aktualizovaný přehled a interpretace doporučených postupů pro praxi - Klinický případ: svědivý exantém v graviditě
- Mid-dermální elastolýza
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy









