-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Prevence a léčba kardiovaskulárních a krvácivých komplikací u nemocných s chronickou lymfocytární leukemií léčených inhibitory Brutonovy kinázy
Managing BTK inhibitor treatment-related adverse events in patients with chronic lymphocytic leukaemia – cardiovascular complications and bleeding
Bruton’s tyrosine kinase (BTK) inhibitors have altered the treatment landscape of chronic lymphocytic leukaemia (CLL). These highly eff ective drugs improve not only the prognosis but also the quality of life of CLL patients. Long-term BTK inhibitor treatment can be limited by specifi c adverse events (AEs) such as cardiovascular (CV) complications or bleeding. Ibrutinib, the fi rst-in-class BTK inhibitor, was discontinued in up to 26% of patients in clinical trials due to AEs. Therefore, there are continuing eff orts to develop BTK inhibitors with the same eff ectivity but better safety profi le, such as covalent BTKi acalabrutinib and zanubrutinib and non-covalent BTKi pirtobrutinib and nemtabrutinib. The pre-treatment workup for all patients should include CV risk level assessment using scoring systems, e. g., Framingham risk score or SCORE. In patients with high CV risk levels, next-generation BTK inhibitors or other targeted drugs (venetoclax or idelalisib) are generally preferred over ibrutinib. Patients who experience CV toxicity, particularly atrial fi brillation or heart failure, should be consulted with a cardiologist to defi ne the best treatment algorithm. In contrast to CV toxicity, the risk of major bleeding events is equal for both ibrutinib and acalabrutinib (2–9% vs. 2–5%) based on data from clinical trials. Regarding prevention of bleeding events, BTK inhibitor treatment should be appropriately held prior to any invasive procedure and cannot be restarted until the risk of bleeding is minimal. Good knowledge of the patient’s current medication and potential interactions is crucial in the prevention of any adverse event. This review describes the mechanisms of pathogenesis of cardiovascular complications and bleeding in BTK inhibitor-treated patients. It summarises their incidence in selected clinical trials and provides recommendations for managing these AEs in clinical practice.
Keywords:
bleeding – ibrutinib – arterial hypertension – chronic lymphocytic leukaemia – acalabrutinib – BTK inhibitor – atrial fi brillation
Autori: A. Panovská 1; T. Arpáš 1; M. Šimkovič 2; M. Špaček 3; T. Papajík 4; D. Lysák 5; L. Bezděková 1; M. Doubek 1
Pôsobisko autorov: Interní hematologická a onkologická klinika LF MU a FN Brno 1; IV. interní hematologická klinika LF UK a FN Hradec Králové 2; I. interní klinika – klinika hematologie I. LF UK a VFN v Praze 3; Hemato-onkologická klinika LF UP a FN Olomouc 4; Hematologicko-onkologické oddělení FN Plzeň 5
Vyšlo v časopise: Transfuze Hematol. dnes,29, 2023, No. 3, p. 177-184.
Kategória: Souhrnné a edukační práce
doi: https://doi.org/10.48095/cctahd2023prolekare.cz12Súhrn
Inhibitory Brutonovy kinázy (BTKi) jsou první skupinou cílených léčiv, která výrazně zlepšila prognózu i kvalitu života nemocných s chronickou lymfocytární leukemií (CLL). Specifické nežádoucí účinky BTKi, zejména kardiovaskulární (KV) a krvácivé, však mohou limitovat jejich dlouhodobé užívání. Ibrutinib, BTKi první generace, byl pro nežádoucí účinky přerušen až u 26 % pacientů léčených v rámci klinických studií. I z těchto důvodů pokračují snahy o vývoj dalších generací BTKi, které by měly bezpečnější profil při zachovaném protinádorovém účinku. Patří mezi ně kovalentně se vázající BTKi akalabrutinib a zanubrutinib a reverzibilní, nekovalentní BTK inhibitory pirtobrutinib a nemtabrutinib. V České republice je v současnosti z veřejného zdravotního pojištění hrazen akalabrutinib. V rámci prevence KV komplikací je zásadní stanovení KV rizika u konkrétního pacienta; pro tyto potřeby lze využít jednoduché skórovací systémy typu Framinghamského skóre nebo tabulky SCORE. U nemocných s vysokým KV rizikem je doporučována léčba BTKi 2. generace nebo léky ze skupiny bcl-2 inhibitorů, případně inhibitorů fosfatidylinositol-3-kinázy. Pokud dojde k rozvoji fibrilace síní nebo srdečního selhání, je nezbytná spolupráce s kardiologem. Riziko závažného krvácení je, na rozdíl od KV komplikací, podobné u obou dostupných preparátů (2–9 % u ibrutinibu vs. 2–5 % u akalabrutinibu). V prevenci klinicky manifestního krvácení je zásadní přerušení léčby BTKi s dostatečným předstihem před každým invazivním výkonem a znovuzahájení terapie až ve chvíli, kdy je riziko krvácení již minimální. Důležitým faktorem pro snížení rizika rozvoje jakékoli komplikace je znalost stávající medikace pacienta a potenciálních lékových interakcí s BTKi. Tato práce shrnuje mechanizmus vniku kardiovaskulárních a krvácivých komplikací, jejich incidenci ve vybraných klinických studiích a doporučení pro prevenci a léčbu těchto nežádoucích účinků v běžné klinické praxi.
Klíčová slova:
krvácení – arteriální hypertenze – srdeční selhání – chronická lymfocytární leukemie – ibrutinib – BTK inhibitor – fi brilace síní – akalabrutinib
ÚVOD
Léčba chronické lymfocytární leukemie (CLL) prochází v posledních letech zásadním vývojem. Široké používání nových cílených léků s sebou přináší nejen zlepšení léčebných výsledků, ale i nové nežádoucí účinky (adverse events – AE). První skupinou cílených léčiv, která významně zlepšila prognózu nemocných s CLL, jsou inhibitory Brutonovy kinázy (BTKi). V České republice jsou indikovány v léčbě relapsu / refrakterní CLL a v první linii terapie u pacientů s přítomností mutace TP53 a/nebo delece 17p [1]. Inhibicí BTK snižují signalizaci přes B buněčný receptor, která je nezbytná pro přežití nádorového B lymfocytu. Dlouhodobá expozice BTKi však může vést k rozvoji komplikací, které u části pacientů limitují pokračování terapie. Specifickými nežádoucími účinky, s kterými se setkáváme při léčbě BTKi, jsou zejména kardiovaskulární komplikace a krvácení. Správný postup při řešení těchto AE je zásadní pro úspěšné pokračování léčby.
V České republice mají schválenou úhradu pro léčbu CLL dva preparáty z této skupiny (stav k 3/2023). Prvním a nejdéle používaným lékem je ibrutinib, který ireverzibilně a neselektivně inhibuje BTK. S různou afinitou se váže i na jiné kinázy, což přímo souvisí s jeho specifickými nežádoucími účinky. Inhibice kináz z rodiny ITK (interleukin-2-inducible T-cell kinase) a TEC (tyrosine kinase expressed in hepatocellular carcinoma) je asociována s trombocytopatií a krvácením, inhibice EGFR (epidermal growth factor receptor) s průjmy a exantémem a inhibice kináz z rodiny CSK (C-terminal Src kinase) s rozvojem fibrilací síní. Tyto specifické a potenciálně závažné AE vedou dle dostupných dat k trvalému přerušení terapie až u 26 % pacientů léčených ibrutinibem [2–4]. Pokračují tedy snahy o vývoj dalších generací BTKi, které by měly bezpečnější profil při zachovaném protinádorovém účinku. Patří mezi ně kovalentně se vázající BTKi akalabrutinib a zanubrutinib a reverzibilní, nekovalentní BTKi pirtobrutinib a nemtabrutinib. V České republice je od roku 2021 z veřejného zdravotního pojištění hrazen akalabrutinib. Akalabrutinib neinhibuje CSK kinázy, méně ovlivňuje kinázy z rodiny TEC a in vitro nevykazuje aktivitu proti EGFR, což odpovídá nižší frekvenci exantému, průjmu a zejména kardiovaskulárním (KV) komplikacím [5]. V současné době probíhají četné klinické studie, které hodnotí účinnost a bezpečnost nových BTK inhibitorů v léčbě CLL. Začátkem roku 2023 byly publikovány výsledky studie ALPINE, která jako první prokázala vyšší účinnost BTKi nové generace – zanubrutinibu ve srovnání s ibrutinibem u pacientů s relapsem / refrakterní CLL (R/R CLL), přičemž výskyt KV komplikací byl také nižší v rameni se zanubrutinibem [6]. První reverzibilně se vázající BTKi pirtobrutinib dosahuje slibných léčebných výsledků i u pacientů, kteří již byli léčeni kovalentními BTK inhibitory a mají přítomnou mutaci BTK C481. Incidence kardiovaskulárních AE na léčbě pirtobrutinibem zůstává nízká [7].
KARDIOVASKULÁRNÍ A KRVÁCIVÉ KOMPLIKACE – DATA Z KLINICKÝCH STUDIÍ
Studie RESONATE srovnávala monoterapii ibrutinibem nebo ofatumumabem v léčbě R/R CLL a stala se přelomovou studií, která prokázala vysokou účinnost BTKi u nemocných s CLL. Při dlouhodobém sledování pacientů léčených ibrutinibem byla fibrilace síní zachycena u 12 % z nich (grade ≥ 3 u 6 % dle CTCAE [common terminology criteria for adverse events]), arteriální hypertenze u 21 % (grade ≥ 3 u 9 %) nemocných. Incidence arteriální hypertenze, na rozdíl od ostatních AE, s časem stále narůstá. Komorová tachykardie byla popsána u 2 (1 %) pacientů, u 5 % se objevilo městnavé srdeční selhání. Závažné krvácení grade ≥ 3 se rozvinulo u 9 % nemocných [8]. Účinnost a bezpečnost ibrutinibu v léčbě první linie nemocných s CLL hodnotila studie RESONATE-2, kontrolní rameno představoval chlorambucil. Při mediánu sledování 57 měsíců se fibrilace síní objevila u 16 % (grade ≥ 3 u 5 %) a arteriální hypertenze u 26 % (grade ≥ 3 u 9 %) léčených. Případy dekompenzace krevního tlaku grade ≥ 3 byly úspěšně řešeny redukcí dávky ibrutinibu. Rozvoj komorové tachykardie u pacienta léčeného ibrutinibem v této studii popsán nebyl. U pacientů léčených ibrutinibem bylo krvácení grade ≥ 3 zachyceno v 7 % [9]. Ve studii ELEVATE-RR srovnávající ibrutinib a akalabrutinib v léčbě R/R CLL byla incidence fibrilace síní vyšší v ibrutinibovém rameni (celkem 16 %, grade ≥ 3 u 3 %) ve srovnání s akalabrutinibem (celkem 9 %; grade ≥ 3 u 4 %). U pacientů léčených akalabrutinibem byl pozorován i nižší výskyt arteriální hypertenze (9 % vs. 23 %). Krvácení se objevilo u 51 % pacientů užívajících ibrutinib a 38 % akalabrutinib, závažné krvácení grade ≥ 3 se v obou ramenech pohybovalo okolo 5 %. Z důvodu AE častěji ukončili terapii pacienti užívající ibrutinib (21 vs. 15 %). Medián sledování činil necelých 41 měsíců [4]. Studie ELEVATE-TN hodnotila akalabrutinib v monoterapii nebo v kombinaci s obinutuzumabem (AO) v první linii terapie CLL; srovnávacím ramenem byla kombinace chlorambucilu s obinutuzumabem. Pacienti s klinicky významným KV onemocněním nemohli být do této studie zařazeni. Při mediánu sledování 46 měsíců se fibrilace síní objevila u 6 % pacientů (žádný grade ≥ 3) léčených akalabrutinibem v monoterapii, resp. u 4 % (grade ≥ 3 u 1 %) léčených kombinací AO. Arteriální hypertenze se rozvinula u 7 % (grade ≥ 3 u 3 %) nemocných léčených akalabrutinibem a 8 % (3 % grade ≥ 3) AO kombinací. Pacienti v akalabrutinibovém rameni zažili krvácivou příhodu ve 42 % (grade ≥ 3 u 3 %), pacienti léčení AO ve 47 % (grade ≥ 3 u 3 %) [10].
Riziko závažného krvácení (grade ≥ 3) je na rozdíl od KV komplikací obdobné u obou dostupných preparátů. U ibrutinibu se pohybuje mezi 2–9 % napříč studiemi, u akalabrutinibu mezi 2–5 % [2–4,6,8–10]. Jones a kolegové analyzovali vliv současného užívání antikoagulační (vyjma antagonistů vitaminů K) nebo antiagregační terapie a ibrutinibu na počet krvácivých příhod u pacientů s CLL ve 2 multicentrických studiích [11]. Ve studii PCYC-1102, která hodnotila účinnost a bezpečnost ibrutinibu u pacientů s R/R CLL i v první linii terapie, bylo závažné krvácení zaznamenáno u 9 % pacientů užívajících ibrutinib spolu s antikoagulační terapií a 4 % při kombinaci ibrutinibu s antiagregačními látkami (při mediánu sledování 22 měsíců) [3]. V již zmiňované studii RESONATE se při mediánu sledování 10 měsíců u pacientů kombinujících ibrutinib a antikoagulační léčbu objevilo krvácení grade ≥ 3 u 2 %, resp. u 1 % nemocných na kombinaci ibrutinibu a antiagregace [8]. Závažné krvácení bylo téměř vždy spojeno s dalšími spouštěcími faktory, např. se současným užíváním CYP3A4 inhibitoru nebo invazivním výkonem [11].
FIBRILACE SÍNÍ
Fibrilace síní patří mezi specifické nežádoucí účinky BTK inhibitorů. Vyšší incidence je popisována u starších pacientů (> 70 let), pacientů s R/R CLL a přidruženými chorobami. Nejdůležitějším faktorem pro prevenci rozvoje fibrilace síní je správná volba cílené terapie u konkrétního pacienta. Před zahájením léčby je nezbytné zhodnotit aktuální zdravotní stav nemocného a medikaci, kterou pravidelně užívá. Důkladná znalost předchorobí nám pomůže zachytit pacienty nevhodné k léčbě BTKi, kterými jsou typicky nemocní s paroxysmem komorové tachykardie v anamnéze. Naopak pacienti s paroxysmální či perzistentní fibrilací síní mohou být k léčbě BTKi indikování a často z ní profitují [12,13]. Pokud je pacient pravidelně sledován u ambulantních specialistů, např. kardiologa nebo internisty, je vhodné požádat o jejich souhrnné zhodnocení před definitivní volbou cílené terapie. V současnosti máme k dispozici několik skórovacích systémů, které nám pomáhají stanovit KV riziko u konkrétního jedince. V zahraničí je nejčastěji používané tzv. Framinghamské skóre, které bylo ve své původní verzi vytvořeno Kannelem a jeho kolektivem v roce 1976. Současná celosvětová podoba vychází z pěti základních rizikových faktorů – věku a pohlaví, kouření cigaret, systolického krevního tlaku a celkového cholesterolu. Na základě těchto parametrů stanovuje míru KV rizika (fatální i nefatální koronární příhody) u konkrétního jedince ve věku 30–70 let. Jako nízké absolutní 10leté riziko bylo arbitrárně stanoveno ≤ 10 %, střední 10–20 % a vysoké KV riziko > 20 % [12,14,15]. Pro rychlý výpočet Framinghamského skóre jsou k dispozici on-line kalkulátory. V České republice je nejčastěji používán systém SCORE, který pracuje s podobnými rizikovými faktory a je adaptován přímo pro českou populaci (obr. 1) [15–17]. Na rozdíl od předchozího skórovacího modelu systém SCORE identifikuje možné fatální KV příhody v následujících 10 letech a ve věku 60 let, což je s ohledem na věkové složení CLL populace méně praktické. U pacientů s vysokým KV rizikem je doporučována léčba BTK inhibitorem 2. generace, bcl-2 mimetikem nebo inhibitorem fosfatidylinositol-3-kinázy (PI3K) [5,12,13].
Pokud i přes správnou indikaci BTKi dojde k rozvoji fibrilace síní, další postup je přísně individuální a měl by probíhat ve spolupráci s kardiologem či internistou. Závisí na možnostech ovlivnění arytmie samotné (elektrická/farmakologická verze), na riziku krvácení na straně jedné (HAS-BLED skóre) a riziku kardioembolizační příhody na straně druhé (CHA2DS2-VASc) [18,19]. Obecně platí, že u pacientů s vyšším rizikem krvácení nebo obtížně řešitelnou arytmií lze zvážit změnu inhibitoru [20,21]. Vhodnou alternativu představuje kombinace založená na bcl-2 inhibitoru venetoklaxu, případně PI3K inhibitoru idelalisibu. Naopak u pacienta s asymptomatickou fibrilací síní a nízkým rizikem dle CHA2DS2-VASc (0–1 bodů) lze v léčbě BTK inhibitorem pokračovat. Pacienti indikovaní k antikoagulační terapii (CHA2DS2-VASc ≥ 2), kteří by profitovali z pokračování léčby BTKi, na ní mohou být ponecháni. Někteří autoři doporučují alespoň přechodné přerušení BTKi a po stabilizaci stavu znovuzahájení léčby buď v původní, nebo redukované dávce. Pokud se fibrilace síní rozvine na léčbě ibrutinibem, lze zvážit záměnu léku za BTKi druhé generace. Z antikoagulancií je doporučována terapie apixabanem v redukované dávce (2,5 mg 2× denně) nebo enoxaparinem (ve standardním dávkování při hodnotě trombocytů > 50×109/l). Souběžná léčba warfarinem je naopak kontraindikována. Pro nízké riziko interakcí jsou v léčbě fibrilace síní preferovány betablokátory před amiodaronem (substrát P-glykoproteinu) a blokátory kalciových kanálů (verapamil, diltiazem – CYP3A4 inhibitory) (tab. 1) [6,12,13].
ARTERIÁLNÍ HYPERTENZE
Nejčastějším KV nežádoucím účinkem BTK inhibitorů je arteriální hypertenze, na rozdíl od fibrilace síní je však méně často příčinou trvalého ukončení léčby. Na základě dlouhodobých dat studie RESONATE vyplývá, že medián vzniku arteriální hypertenze je 14 měsíců, přičemž incidence s délkou užívání léku mírně narůstá. Až 70 % zachycených AE vniká de novo, tedy u pacientů, kteří se dosud s arteriální hypertenzí neléčili [8,13]. Nejdůležitějším faktorem prevence závažné dekompenzace arteriální hypertenze je opět správná volba cílené terapie u konkrétního pacienta. Arteriální hypertenze v anamnéze není kontraindikací léčby BTKi, je však nezbytná pravidelná monitorace krevního tlaku ve spolupráci s pacientem a jeho praktickým lékařem. Po dobu prvních 6 měsíců je doporučováno měření krevního tlaku dvakrát týdně. Antihypertenzní terapii je třeba korigovat časně, přičemž bychom se měli vyhýbat lékům inhibujícím CYP3A4 pro riziko dalšího zvýšení toxicity. Pokud adekvátní úprava hypotenziv nevede k normalizaci hodnot krevního tlaku a dosahuje závažnosti grade ≥ 3, je vhodné přerušení BTK inhibitoru a po stabilizaci stavu znovu zahájení léčby v redukované dávce. U pacientů užívajících ibrutinib lze zvážit změnu preparátu za BTKi druhé generace, případně bcl-2 nebo PI3K inhibitor [5,12,13]. Nesmíme zapomínat i na úpravu/redukci antihypertenziv v případě, že dojde k vysazení BTK inhibitoru z jiných příčin (tab. 1) [12,13].
Obr. 1. Tabulka rizika úmrtí v důsledku srdečně-cévního onemocnění v následujících 10 letech (pro českou populaci) [17]. ![Tabulka rizika úmrtí v důsledku srdečně-cévního onemocnění v následujících 10 letech (pro českou populaci) [17].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/5c3751753a73c9fafe5e1719099bbe25.png)
SRDEČNÍ SELHÁNÍ
Městnavé srdeční selhání patří mezi méně časté KV nežádoucí účinky BTK inhibitorů. Nejdůležitější prevencí rozvoje této komplikace je opět stanovení KV rizika u konkrétního pacienta a následně správná volba cílené terapie. I pacienti s již známým chronickým srdečním selháním (CHSS) stupně NYHA I a II mohou být bezpečně léčeni BTK inhibitory. Preferovány jsou v tomto případě BTKi druhé generace pro nižší riziko rozvoje fibrilace síní [4,5,12,13]. Léčbu BTKi naopak není doporučeno zahajovat u pacientů s akutním srdečním selhání nebo dekompenzací chronického selhání [12,22]. Pro tyto nemocné, pokud nemají restrikci příjmu tekutin, je vhodnou alternativou léčba venetoklaxem, případně idelalisibem.
U nemocných s CHSS léčených BTKi je nezbytná pravidelná spolupráce s kardiologem, který zajistí monitoraci pacienta (krevního tlaku, hmotnosti, bilance tekutin, restrikce sodíku) a adekvátní úpravu medikace a režimových opatření. V posledních letech se v návaznosti na práci onkologických center rozvíjí oblast kardioonkologie, úzké spolupráce mezi onkology a kardiology, kteří se specializují na péči o onkologické pacienty léčené potenciálně kardiotoxickými režimy. Díky tomuto přístupu jsme schopni časně zachytit první známky srdeční nedostatečnosti a zahájit odpovídající léčbu. V roce 2022 byla vydána doporučení Evropské kardiologické společnosti pro oblast kardioonkologie, v kterých jsou diskutovány i komplikace léčby BTK inhibitory [23].
Tab. 1. Kardiovaskulární komplikace – prevence a léčba. 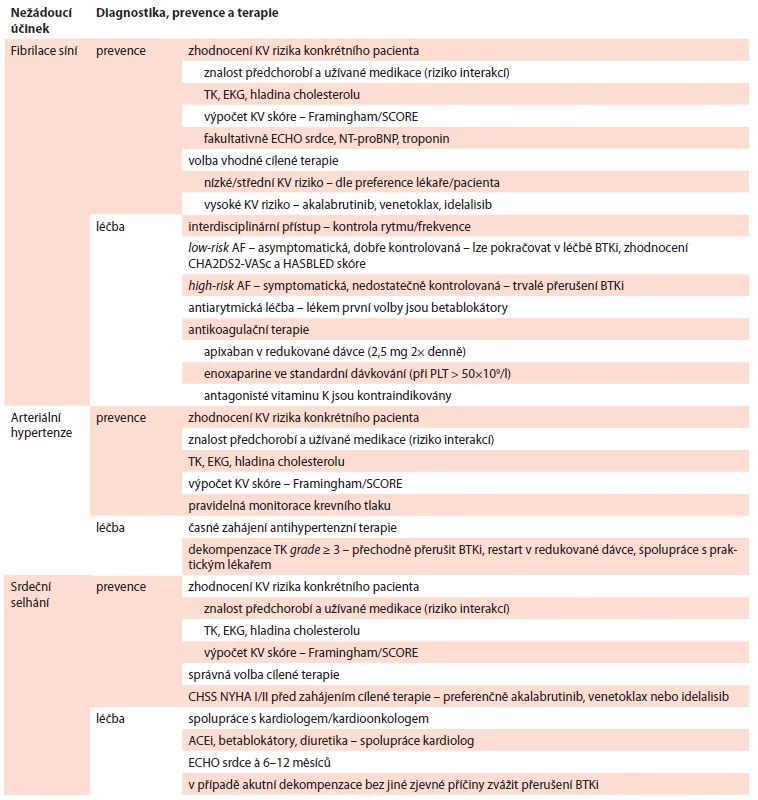
ACEi – inhibitory angiotenzin konvertujícího enzymu; AF – fi brilace síní (atrial fi brillation); BTKi – inhibitor Brutonovy kinázy; ECHO – echokardiografi e; EKG – elektrokardiogram; KV – kardiovaskulární; NT-proBNP – hormonálně neaktivní fragment prohormonu proBNP; PLT – trombocyty (platelets); TK – krevní tlak Tab. 2. Krvácivé komplikace – prevence a léčba. 
BTKi – inhibitor Brutonovy kinázy; DOAC – přímá orální antikoagulancia (direct oral anticoagulation); LMWH – nízkomolekulární heparin (low molecular weight heparine) KRVÁCENÍ
Krvácení patří spolu s KV komplikacemi k specifickým nežádoucím účinkům BTK inhibitorů. Brutonova kináza a kinázy z rodiny TEC jsou součástí signální dráhy receptoru pro glykoprotein VI, který se podílí na vazbě trombocytů na kolagen při poranění cévního řečiště [24]. U pacientů léčených ibrutinibem dochází k méně robustní agregaci krevních destiček než u zdravých jedinců, přičemž významněji je zasaženo právě kolagenem indukované srážení [24–26]. Dobie a kol. popsali také ztrátu komplexu glykoproteinu Ib-IX a integrinu aIIbß3 na povrchu trombocytů u pacientů léčených ibrutinibem, která se mění s délkou užívání a dávkou léku [27]. Rizikovou skupinu pro rozvoj manifestního krvácení představují pacienti, u nichž je přítomna trombocytopenie při aktivitě CLL a nemocní užívající současně antikoagulační nebo antiagregační léčbu [4,5,12,13]. Za vysoce rizikovou se považuje kombinace BTK inhibitoru a duální antiagregace. V případě, že je u pacienta léčeného BTKi indikováno zahájení duální antiagregace, je vhodné BTKi přerušit. V závislosti na aktivitě CLL přerušujeme léčbu buď přechodně po dobu trvání duální antiagregační léčby, nebo trvale za současné změny cílené terapie. V této situaci je doporučována léčba založená na venetoklaxu nebo idelalisibu [5,12,13,28]. Primární prevencí krvácení je nejen správná indikace BTK inhibitoru, ale i pravidelné sledování pacienta v průběhu terapie. Léčbu BTKi přerušujeme s dostatečným předstihem před každým invazivním výkonem (3–7 dní dle závažnosti zákroku) a znovuzahájení terapie je možné až ve chvíli, kdy je riziko krvácení z rány minimální (1–3 dny dle typu zákroku).
Pokud je výkon indikován akutně, léčbu BTKi přerušujeme ihned a ke snížení rizika krvácení substituujeme pacienta trombocyty. In vitro data naznačují, že k úpravě hemostázy dochází při dosažení 50 % čerstvě podaných trombocytů v krvi pacienta [28–30]. V případě samotného přerušení ibrutinibu dosáhneme parciálního snížení protidestičkového efektu za 2,5 dne [28–30]. Nevhodné je současné užívání doplňků stravy obsahujících vitamín E a rybí olej a nesteroidních antiflogistik, které mohou dále nepříznivě ovlivnit srážlivost krve. Vždy je třeba zhodnotit současně užívanou medikaci pacienta. Z antikoagulační terapie je doporučována léčba přímými perorálními antikoagulancii, eventuálně nízkomolekulárním heparinem. Do prvních studií, které hodnotily ibrutinib v léčbě B lymfoproliferací, byli zařazováni i pacienti užívající antagonisty vitamínu K [3,31–33]. Pro signifikantně vyšší incidenci krvácivých příhod u těchto pacientů je v současnosti souběžná léčba BTKi a antagonisty vitamínu K kontraindikována a pacienti užívající tento typ léčby do studií s BTKi nemohou být zařazeni (tab. 2).
Klinicky patrné krvácení se v průběhu terapie BTKi objevuje až u poloviny pacientů, většinou se však jedná o drobné kožní krvácení, které nevyžaduje intervenci ani přerušení terapie. Pokud jsou potíže protrahované a nemocného obtěžují, doporučuje se léčbu BTKi krátkodobě přerušit. V případě klinicky závažného krvácení je nezbytné užívání BTKi přerušit ihned a substituovat trombocyty bez ohledu na jejich hladinu v krvi pacienta obdobně, jak je doporučeno v případě akutního invazivního výkonu. Další postup se odvíjí od typu a zdroje krvácení a probíhá ve spolupráci s příslušnými specialisty. V případě krvácení grade ≥ 3 je ke zvážení trvalé ukončení terapie BTK inhibitorem [12,28,33].
ZÁVĚR
Kardiovaskulární a krvácivé komplikace jsou typické pro léčbu BTK inhibitory a nesetkáváme se s nimi u jiných cílených molekul v terapii CLL. Jsou jednou z nejčastějších příčin přerušení léčby a mnohdy se jedná o život ohrožující komplikace. Správná indikace cílené léčby u konkrétního pacienta a správný postup při řešení AE je zásadní pro možnost pokračování léčby a její výsledný efekt. Díky zhodnocení KV rizika ještě před zahájením terapie CLL jsme schopni zachytit nemocné s vysokým rizikem rozvoje KV komplikací, u nichž preferenčně volíme jiné cílené léky než ibrutinib. Při řešení KV komplikací je výhodná úzká spolupráce hematoonkologa a kardiologa, s čímž souvisí rozvoj kardioonkologie v posledních letech. V rámci prevence krvácivých příhod je důležité respektovat doporučené intervaly pro přerušení léčby BTKi v perioperačním období. Další možností, jak snížit incidenci komplikací při léčbě BTK inhibitory, je jejich časově omezené podávání nejčastěji v kombinaci s venetoklaxem. Výsledky klinických studií hodnotících bezpečnost a účinnost těchto léčebných kombinací potvrzují nižší incidenci zejména AE, jejichž výskyt s časem narůstá. Typickým příkladem je arteriální hypertenze. Pokračují také snahy o vývoj dalších BTKi, které budou mít bezpečnější profil a budou účinné i u pacientů s relapsem / refrakterní CLL na léčbu kovalentními BTK inhibitory.
PODÍL AUTORŮ NA PŘÍPRAVĚ RUKOPISU
AP – příprava a revize rukopisu
MD, TA, MŠi, MŠp, TP, DL, LB – revize a připomínkování textu
KONFLIKTU ZÁJMŮ
AP – přednášková a poradní činnost, cestovní granty: AstraZeneca, Janssen, Gilead
MD – přednášková a poradní činnost, cestovní granty: AbbVie, AstraZeneca, AOP, Janssen, Novartis
TA – cestovní granty: AstraZeneca, AbbVie
MŠi – přednášková a poradní činnost, cestovní granty: AbbVie, AstraZeneca, Janssen
MŠp – přednášková a poradní činnost, cestovní granty: AbbVie, AstraZeneca, Janssen
TP – přednášková a poradní činnost, cestovní granty: AbbVie, AstraZeneca, Janssen
DL – přednášková a poradní činnost, cestovní granty: AbbVie, AstraZeneca, Janssen, Novartis
LB – cestovní granty: Janssen, Gilead
Do redakce doručeno dne: 8. 3. 2023.
Přijato po recenzi dne: 14. 4. 2023.
MUDr. Anna Panovská, Ph.D.
Interní hematologická a onkologická
klinika
LF MU a FN Brno
Jihlavská 20, 62500 Brno
e-mail: panovska.anna@fnbrno.cz
Zdroje
1. Smolej L, Špaček M, Pospíšilová Š, et al. Doporučení pro diagnostiku a léčbu chronické lymfocytární leukemie 2021. Transfuze Hematol Dnes. 2021; 27 (1): 91–106.
2. Burger JA, Tedeschi A, Barr PM, et al. Ibrutinib as initial therapy for patients with chronic lymphocytic leukemia. N Engl J Med. 2015; 373 : 2425–2437.
3. Byrd JC, Furman RR, Coutre SE, et al. Ibrutinib treatment for first-line and relapsed/refractory chronic lymphocytic leukemia: final analysis of the pivotal phase Ib/II PCYC-1102 study. Clin Cancer Res. 2020; 26 : 3918–3927.
4. Byrd JC, Hillmen P, Ghia P, et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial. J Clin Oncol. 2021; 39 (31): 3441–3452.
5. O’Brien SM, Brown JR, Byrd JC, et al. Monitoring and managing BTK inhibitor treatment-related adverse events in clinical practice. Front Oncol. 2021; 11 : 720704.
6. Brown JR, Eichhorst B, Hillmen P, et al. Zanubrutinib or ibrutinib in relapsed or refractory chronic lymphocytic leukemia. N Eng J Med. 2023; 388 : 319–332.
7. Mato AR, Woyach JA, Brown JR, et al. Efficacy of pirtobrutinib in covalent BTK-inhibitor pre-treated relapsed/refractory CLL/SLL: additional patients and extended follow-up from phase 1/2 BRUIN study. Blood. 2022; 140 (Suppl 1): 2316–2320.
8. Munir T, Brown JR, O’Brien S, et al. Final analysis from RESONATE: up to six years of follow-up on ibrutinib patients with previously treated chronic lymphocytic leukemia or small lymphocytic lymphoma. Am J Hematol. 2019; 94 (12): 1353–1363.
9. Burger JA, Barr PM, Robak T, et al. Long-term efficacy and safety of first-line ibrutinib treatment for patients with CLL/SLL: 5 years of follow-up from the phase 3 RESONATE-2 study. Leukemia. 2020; 34 (3): 787–798.
10. Sharman JP, Egyed M, Jurczak W, et al. Efficacy and safety in a 4-year follow-up the ELEVATE-TN study comparing acalabrutinib with or without obinutuzumab versus obinutuzumab plus chlorambucil in treatment-naïve chronic lymphocytic leukemia. Leukemia. 2022; 36 : 1171–1175.
11. Jones JA, Hillmen P, Coutre S, et al. Use of anticoagulants and antiplatelet in patients with chronic lymphocytic leukaemia treated with single-agent ibrutinib. Br J Haematol. 2017; 178 : 286–291.
12. Awan FT, Addison D, Alfraih F, et al. International consensus statement on management of cardiovascular risk of Bruton‘s tyrosine kinase inhibitors in CLL. Bood Adv. 2022; 6 (18): 5516–5524.
13. Lipsky A, Lamanna N. Managing toxicities of Bruton tyrosine kinase inhibitors. Hematology Am Soc Hematol Educ Program. 2020; 1 : 336–345.
14. Bitton A, Gaziano T. The Framigham Hear Study’s impact on global risk assessment. Prog Cardiovasc Dis. 2010; 53 : 6878.
15. Zikmund Galková L, Špinar J, Ludka O. Skórovací systémy preventivní kardiologie. Kardiol Rev Int Med. 2015; 17 (2): 112–116.
16. De Backer G, Ambrosioni E, Borch-Johnsen K, et al. European guidelines on cardiovascular disease prevention in clinical practice. Eur Hear J. 2003; 24 : 1601–1610.
17. Cífková R, Býma S, Češka R, et al. Prevence kardiovaskulárních onemocnění v dospělém věku. Společné doporučení českých odborných společností. Cor Vasa. 2005; 47 (Suppl): 3–14.
18. Lip GY, Nieuwlaat R, Pisters R, et al. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest. 2010; 137 (2): 263–272.
19. Pisters R, Lane DA, Nieuwlaat R, et al. Novel user friendly score (Has-Bled) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the euro heart survey. Chest. 2010; 138 (5): 1093–1100.
20. Brown JR. How I treat CLL patients with ibrutinib. Blood. 2018; 131 (4): 379–386.
21. Stephens DM, Byrd JC. How I manage ibrutinib intolerance and complications in patients with chronic lymphocytic leukemia. Blood. 2019; 133 (12): 1298–1307.
22. Piepoli MF, Hoes AW, Agewall S, et al. European guidelines on cardiovascular disease prevention in clinical practice; the sixth joint task force of the European Society of Cardiology and other societies on cardiovascular disease prevention in clinical practice (constituted by representatives of 10 societies and by invited experts): developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur J Prev Cardiol. 2016; 23 (11): NP1–NP96.
23. Lyon AR, López-Fernandéz T, Couch LS, et al. Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic RAdiology and Oncology (ESTRO) and the International Cardio-Oncology Sociery (IC-OS). Eur Heart J. 2022; 43 : 4229–4361.
24. Quek LS, Bolej J, Watson SP. A role for Bruton’s tyrosine kinase (Btk) in platelet activation by collagen. Curr Biol CB. 1998; 8 (20): 1137–1140.
25. Kamel S, Horton L, Yserbat L, et al. Ibrutinib inhibits collagen-mediated but not ADP-mediated platelet aggregation. Leukemia. 2015; 29 (4): 783–787.
26. Lipsky AH, Farooqui MZH, Tian X, et al. Incidence and risk factors of bleeding-related adverse events in patients with chronic lymphocytic leukemia treated with ibrutinib. Haematologica. 2015; 100 (12): 1571–1578.
27. Dobie G, Kuriri FA, Omar MMA, et al. Ibrutinib, but not zanubrutinib, induces platelet receptor shedding of GPIb-IX-V complex and integrin aIIbß3 in mice and humans. Blood Adv. 2019; 3 (24): 4298–4311.
28. Shatzel JJ, Olson SR, Tao DL, et al. Ibrutinib-associated bleeding; pathogenesis, management, and risk reduction strategies. J Thromb Haemost. 2017; 15 (5): 835–847.
29. Kamel S, Horton L, Ysebaert L, et al. Ibrutinib inhibits collagen-mediated but not ADP-mediated platelet aggregation. Leukemia. 2015; 29 : 783–787.
30. Levade M, David E, Garcia C, et al. Ibrutinib treatment affects collagen and von Willebrand factor-dependent platelet functions. Blood. 2014; 124 : 3991–3995.
31. Byrd JC, Brown JR, O’BrienS, et al. Ibrutinib versus ofatumumab in previously treated chronic lymphocytic leukemia. N Eng J Med. 2014; 371 (3): 213–223.
32. O’Brien S, Jones JA, Coutre SE, et al. Ibrutinib for patients with relapsed or refractory chronic lymphocytic leukaemia with 17 deletion (RESONATE17): a phase 2, open-label, multicentre study. Lancet Oncol. 2016; 17 (10): 1409–1418.
33. Wang ML, Blum KA, Martin P, et al. Long term follow-up of MCL patients treated with single-agent ibrutinib: updated safety and efficacy results. Blood. 2015; 126 : 739–745.
Štítky
Hematológia Interné lekárstvo Onkológia
Článok vyšiel v časopiseTransfuze a hematologie dnes
Najčítanejšie tento týždeň
2023 Číslo 3- Intermitentní hladovění v prevenci a léčbě chorob
- Dentální extrakce u hemofiliků
- Sport nemění u zdravých mužů skóre HJHS
- Rizikové faktory pro rozvoj inhibitorů u dětí s hemofilií – výsledky kohortové studie
- Kazuistika: Neobvyklá příčina prodlouženého APPT u SLE – získaná hemofilie a lupus antikoagulans
-
Všetky články tohto čísla
- Hereditary haemorrhagic teleangiectasia (Rendu-Osler-Weber disease)
- Prevence a léčba kardiovaskulárních a krvácivých komplikací u nemocných s chronickou lymfocytární leukemií léčených inhibitory Brutonovy kinázy
- Covid skóre – přínos v prognostické stratifi kaci nemocných s COVID-19
- Zpráva o programu použití rekonvalescentní plazmy při léčbě pacientů s onemocněním COVID-19 v ČR a výsledky národní multicentrické studie RESCOVID-19
- Životní jubileum paní primářky MUDr. Jarmily Živné
- Boris Bubeník slaví sedmdesátiny
- MUDr. Jaroslava Voglová slaví 70 let
- Teklistamab s nejnovějšími dvouletými daty o účinnosti a bezpečnosti v léčbě RRMM
- Transfuze a hematologie dnes
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Hereditary haemorrhagic teleangiectasia (Rendu-Osler-Weber disease)
- Boris Bubeník slaví sedmdesátiny
- Prevence a léčba kardiovaskulárních a krvácivých komplikací u nemocných s chronickou lymfocytární leukemií léčených inhibitory Brutonovy kinázy
- Teklistamab s nejnovějšími dvouletými daty o účinnosti a bezpečnosti v léčbě RRMM
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



