-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
- Kariéra
Onemocnění plic u novorozenců
Lung disease in newborns
Korček P, Korčeková Z. Lung disease in newborns
A fundamental prerequisite for the successful postnatal adaptation of a newborn is the onset of spontaneous breathing activity, the replacement of fluid in the lungs with air (lung aeration), the establishment of functional residual capacity, and subsequently the remodeling of the circulatory system. Respiratory distress syndrome (RDS) may arise when these adaptive processes are disrupted and is defined as a change in the character and/or frequency of breathing. RDS is one of the most common reasons for admitting newborns to the intensive care unit. For practical and didactic reasons, the causes of respiratory difficulties in newborns can be divided into pulmonary and extrapulmonary. The following overview focuses primarily on pulmonary causes of RDS – lung disease in newborns.
Keywords:
surfactant – oxygen therapy – respiratory distress syndrome of a newborn – ventilation support
Autori: Peter Korček 1,2; Zuzana Korčeková 1
Pôsobisko autorov: Neonatologická klinika, Ústav pro péči o matku a dítě, 3. lékařská fakulta Univerzity Karlovy, Praha 1; 3. lékařská fakulta Univerzity Karlovy, Praha 2
Vyšlo v časopise: Čes-slov Pediat 2025; 80 (5): 244-251.
Kategória:
doi: https://doi.org/10.55095/cspediatrie2025/039Súhrn
Korček P, Korčeková Z. Onemocnění plic u novorozenců
Základním předpokladem úspěšné poporodní adaptace novorozence je nástup spontánní dechové aktivity, nahrazení tekutiny v plicích vzduchem (aerace plic), ustanovení funkční reziduální kapacity a následně přestavba oběhového systému. Syndrom dechové tísně (respiratory distress syndrome – RDS) může vzniknout při narušení těchto adaptačních procesů a je definován jako změna charakteru a/nebo frekvence dýchání. RDS představuje jeden z nejčastějších důvodů příjmu novorozenců na jednotku intenzivní péče. Z praktických a didaktických důvodů můžeme příčiny dechových obtíží u novorozenců rozdělit na plicní (pulmonální) a mimoplicní (extrapulmonální). Následující přehled se věnuje primárně plicním příčinám RDS – onemocnění plic u novorozenců.
Klíčová slova:
surfaktant – oxygenoterapie – syndrom dechové tísně novorozence – ventilační podpora
ÚVOD
Základním předpokladem úspěšné bezprostřední poporodní adaptace novorozence je nástup spontánní dechové aktivity, nahrazení tekutiny v plicích vzduchem (aerace plic) a následně přestavba oběhového systému. Spontánní dechová aktivita (a ustanovení funkční reziduální kapacity plic, FRC) způsobí během několika minut zvýšení parciálního tlaku kyslíku v pulmonálních cévách (PaO2 3 kPa → 10 kPa) a dramaticky sníží plicní vaskulární rezistenci. V kombinaci se změnou pravolevého zkratu přes ductus arteriosus (Botallova dučej) na levopravý se významně zvýší plicní perfuze, preload levé komory a srdeční výdej (obr. 1). Uvedené změny může podpořit provedení oddáleného podvazu pupečníku ≥ 60 sekund (delayed cord clamping, DCC) – navýšení objemu cirkulující krve, zlepšení kontraktility myokardu, a zvýšení dodávky kyslíku tkáním.(1,2)
Obr. 1. Fyziologie postnatální adaptace novorozence 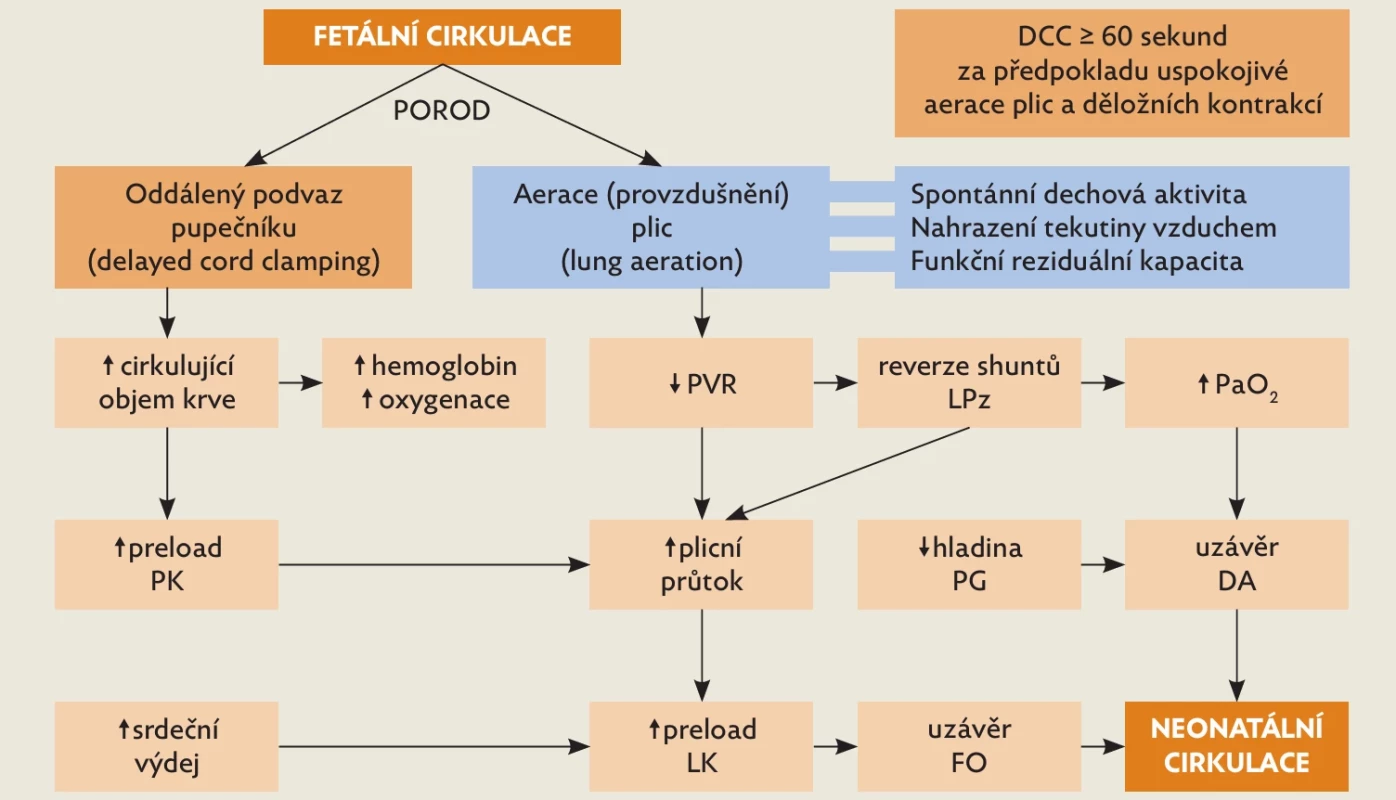
DA – ductus arteriosus; DCC – delayed cord clamping (oddálený podvaz pupečníku); FO – foramen ovale; IK – levá komora; LPz – levopravý zkrat; PG – prostaglandiny;
PK – pravá komora; PVR – plicní vaskulární rezistenceV případě narušené adaptace novorozence (viz Rizikové faktory níže) se rozvíjí syndrom dechové tísně (respiratory distress syndrome, RDS), který je definován jako změna charakteru a/nebo frekvence dýchání. Jedná se o jeden z nejčastějších důvodů příjmu novorozenců na jednotku intenzivní péče.(3–5) Příznaky RDS se ale mohou objevit i v pozdějším průběhu hospitalizace (viz Diferenciální diagnostika RDS). Z praktických a didaktických důvodů můžeme příčiny dechových obtíží u novorozenců rozdělit na plicní (pulmonální) a mimoplicní (extrapulmonální).(3–7)
RIZIKOVÉ FAKTORY VZNIKU RDS
- Nezralost (incidence RDS se zvyšuje s klesajícím gestačním týdnem novorozence vlivem nedostatečné produkce surfaktantu, svalové hypotonie a tendence k apnoe a laryngospasmu).
- Postmaturita.
- Porod císařským řezem (absence přirozených mechanismů k zajištění dostatečné postnatální aerace plic – aktivní resorpce fetální plicní tekutiny do krevních a lymfatických cév vlivem katecholaminů a glukokortikoidů; tlakové změny s pasivním transferem tekutiny do intersticiálního prostoru).
- Diabetes mellitus matky (opožděná zralost plic při fetální hyperinzulinemii).
- Perinatální hypoxie (dysfunkce surfaktantu).
- Zkalená plodová voda (riziko vzniku syndromu aspirace mekonia).
- Prolongovaný odtok plodové vody s oligohydramnion/anhydramnion (riziko hypoplazie plic).
- Infekční komplikace (chorioamnionitida, GBS pozitivní matka s nedostatečnou ATB profylaxí).
- Prenatální zjištění vrozené vývojové vady – VVV (vrozená brániční hernie – plicní hypoplazie, malformace dýchacích cest a plic).
DIAGNOSTIKA RDS
Klinické nálezy
- Tachypnoe (> 60 dechů za minutu).
- Dyspnoe (ztížené dýchání se zatahováním mezižeberních prostorů, jugula a bránice při inspiriu).
- Alární souhyb (zvedání nosních křídel při inspiriu).
- Grunting (patologický zvukový/distanční fenomén během exspiria – výdech proti zavřené glottis ve snaze udržet FRC).
- Centrální cyanóza/desaturace (hypoxemie – měření prostřednictvím pulzní oxymetrie).
- Apnoe (bezdeší).
- Tachykardie, bledost (při respirační nebo smíšené acidóze), zhoršené prokrvení.
- Letargie.
Laboratorní vyšetření
- Acidobazická rovnováha (hyperkapnie, hypoxie, respirační nebo smíšená acidóza – posouzení typu a závažnosti respirační insuficience).
- Biochemické a hematologické vyšetření (nálezy odpovídají vyvolávající příčině RDS – např. elevace parametrů zánětu při sepsi nebo pneumonii).
Zobrazovací metody
- RTG plic (viz Nejčastější plicní příčiny RDS).
- UZ plic (v dnešní době stále více používaná bed-side neinvazivní a relativně rychlá technika vyšetření plic novorozence na jednotce intenzivní péče).
- Echokardiografie (VVV srdce, plicní hypertenze).
DIFERENCIÁLNÍ DIAGNOSTIKA RDS
Plicní (pulmonální) příčiny
- Deficit surfaktantu u nezralých novorozenců (v literatuře můžeme často najít označení RDS pouze pro toto specifické onemocnění – z didaktických a diferenciálně diagnostických důvodů je ale vhodnější označení RDS pro širší skupinu onemocnění, kde společným jmenovatelem je změna charakteru a/nebo frekvence dýchání novorozence).
- Tranzitorní tachypnoe novorozence (TTN).
- Aspirace plodové vody/mekonia (meconium aspiration syndrome, MAS).
- Air-leak syndromy (pneumotorax, pneumomediastinum, plicní intersticiální emfyzém).
- Pneumonie.
- Atelektáza.
- Plicní apoplexie.
- VVV plic a dolních cest dýchacích (congenital pulmonary airway malformation, CPAM).
- Perzistující plicní hypertenze novorozence (PPHN).
- Bronchopulmonální dysplazie (BPD).
- Geneticky podmíněné onemocnění – mutace v genech kódujících proteinové složky surfaktantu (SP-B, SP-C) nebo protein zajišťující transport fosfolipidů do lamelárních tělísek k tvorbě surfaktantu (ABCA3).
Mimoplicní (extrapulmonální) příčiny
- Infekční komplikace (sepse).
- Hypotermie/hypertermie.
- Kardiologické příčiny (VVV srdce, kardiomyopatie, arytmie, hypervolemie).
- VVV gastrointestinálního traktu (atrézie jícnu).
- Vrozená brániční hernie (congenital diaphragmatic hernia, CDH).
- Vrozené deformity hrudníku.
- Obstrukce dýchacích cest (obr. 2).
Obr. 2. Obstrukce dýchacích cest patologickou tkání 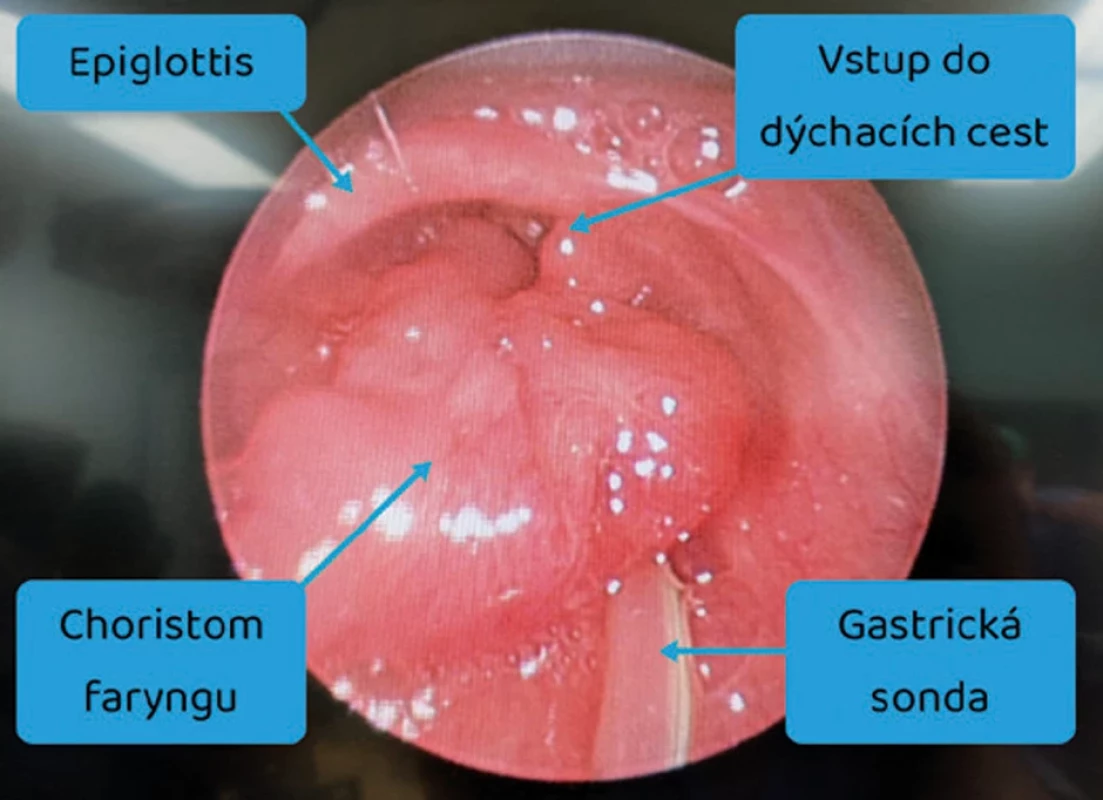
- Fluidotorax (např. chylotorax).
- VVV horních cest dýchacích (atrézie choan, rozštěpové vady).
- Neuromuskulární poruchy (trauma CNS, peri-/intraventrikulární krvácení, paréza n. frenicus, myastenie/myotonie, svalové dystrofie).
- Farmakologický útlum dýchání vlivem medikace (např. opiáty).
- Hematologické příčiny (anemie, polycytemie – hyperviskózní syndrom).
- Metabolické příčiny (hypoglykemie, dědičné poruchy metabolismu – DPM).
V diferenciální diagnostice příčin dechové tísně novorozence nám může pomoct znalost pravděpodobnosti výskytu jednotlivých onemocnění (tab. 1).
Tab. 1. Příčiny dechové tísně z hlediska frekvence výskytu jednotlivých onemocnění 
NEJČASTĚJŠÍ PLICNÍ PŘÍČINY RDS
Deficit surfaktantu u nezralých novorozenců (užší pojetí pojmu RDS)
Původní název nemoc hyalinních membrán (hyaline membrane disease) reflektoval patologicko-anatomický nález v plicních alveolech zemřelých nezralých novorozenců (intraalveolární leak proteinů a tekutiny → depozita amorfní/hyalinní hmoty lemující alveoly). Syndrom je charakterizovaný funkční a anatomickou nezralostí plic (deficit surfaktantu, neschopnost udržet FRC, hypotonie dýchacích svalů) a jeho incidence se zvyšuje s klesajícím gestačním stářím novorozence. Příznaky RDS se rozvíjejí a progredují během prvních hodin po porodu s rizikem život ohrožujících komplikací (respirační selhání, air-leak syndrom). Jedná se o homogenní postižení plic s typickým obrazem na nativním RTG snímku (obr. 3) – symetrická retikulo-granulární kresba (atelektázy obklopené ložisky hyperinflace) a snížená transparence plic (někdy až charakteru „bílé plíce“).(3–7)
Obr. 3. Syndrom dechové tísně (rds) při deficitu surfaktantu u nezralého novorozence – homogenní, symetrické postižení plic s retikulo-granulární kresbou, výrazně sníženou transparencí a setřelými konturami mediastina a bránice 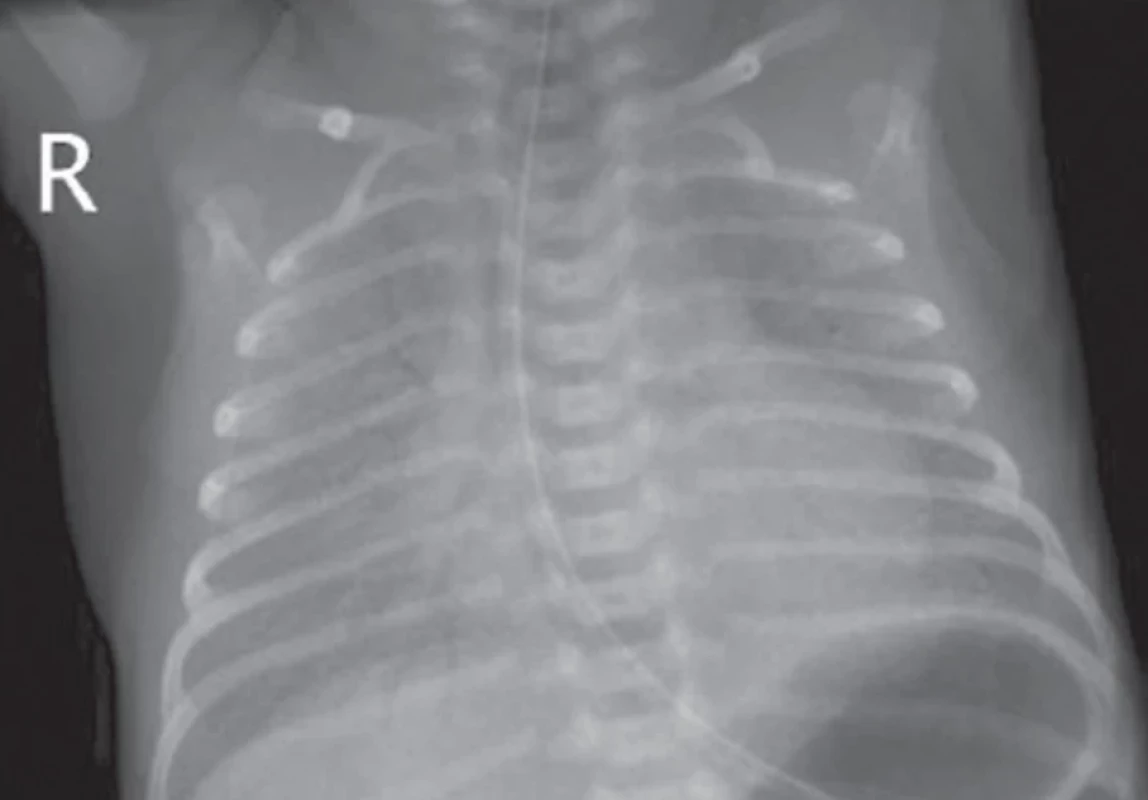
Tato příčina RDS vyžaduje ventilační podporu, oxygenoterapii a jiné terapeutické modality (viz Terapie RDS). Z hlediska ventilační podpory zahajujeme neinvazivní nazální distenční podporu CPAP (continuous positive airway pressure). Při závažnějším průběhu je nutná aplikace surfaktantu a event. umělá plicní ventilace (UPV). Podání surfaktantu lze provést několika způsoby dle rizikových faktorů a individuálního vývoje onemocnění – viz Terapie RDS.(6)
Tranzitorní tachypnoe novorozence (TTN)
Onemocnění je způsobené opožděnou peripartální resorpcí plicní tekutiny do krevních a lymfatických cév, a proto se také někdy označuje jako syndrom vlhké plíce (obr. 4). Snížená efektivita výměny plynů způsobí zvýšenou dechovou práci a vzniká tachypnoe (auskultačně vlhké fenomény bilaterálně). Typicky se vyskytuje u donošených nebo mírně nedonošených novorozenců (late preterm – gestační týden 34 + 0 až 36 + 6) po císařském řezu (zvl. bez předchozí děložní činnosti) a při přítomnosti dalších rizikových faktorů (perinatální hypoxie, diabetes mellitus matky). Prognóza je dobrá a v některých případech stačí jen observace a monitorace novorozence. Mírnější formy TTN vyžadují oxygenoterapii s ústupem obtíží do 24–48 hodin; závažnější formy mohou vyžadovat ventilační podporu a trvají zhruba 3–7 dní. V diferenciální diagnostice je potřeba vyloučit jiné příčiny dechové tísně → sepse/pneumonie, pneumotorax, MAS nebo RDS z deficitu surfaktantu.(3–7)
Obr. 4. Tranzitorní tachypnoe novorozence (TTN) s mírně sníženou transparencí, výraznější perihilózní cévní kresbou, mírným rozšířením srdečního stínu a malým výpotkem v oblasti středního plicního pole vpravo 
Syndrom aspirace mekonia (MAS)
Perinatální hypoxie může způsobit odchod smolky (mekonia) do plodové vody a gasping (hluboké, lapavé, nepravidelné dechy). Následkem může být aspirace zkalené plodové vody nebo mekonia (MAS), která se vyskytuje převážně u donošených a přenášených novorozenců. Bezprostředně po porodu nastupuje tachydyspnoe a rozvíjí se hypoxemie s nutností ventilační podpory / oxygenoterapie. RTG obraz je charakteristický ložiskovým nálezem se sníženou transparencí (obr. 5). Těžší průběh MAS zahrnuje dysfunkci/inaktivaci surfaktantu se závažnějším průběhem RDS, nutností UPV, aplikace surfaktantu a možným rozvojem PPHN.(3–7)
Obr. 5. Syndrom aspirace mekonia (MAS) s heterogenním obou stranným postižením – disperzní zastínění až difuzně splývající infiltráty predominantně v pravé plíci 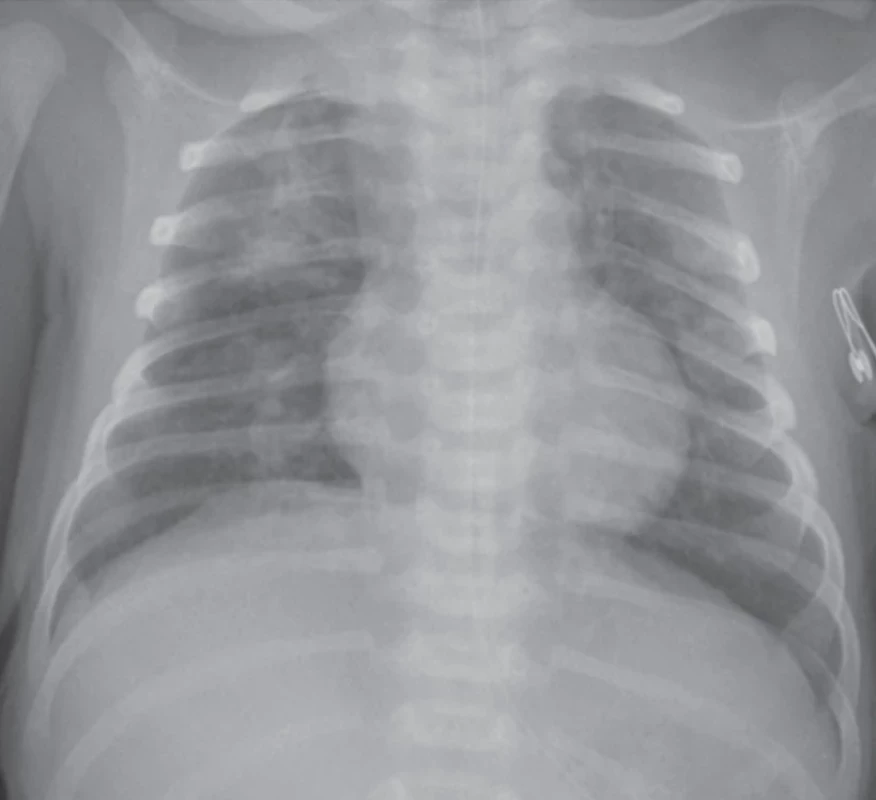
Pneumonie
Infekční komplikace může vzniknout v časném (chorioamnionitida, aspirace infikované plodové vody → adnátní pneumonie) nebo pozdním novorozeneckém období (hematogenně nebo patologickou kolonizací dýchacích cest při dlouhodobé UPV). Mezi etiologická agens patří GBS (Streptococcus agalactiae), gramnegativní bakterie (např. E. coli nebo Klebsiella pneumoniae) a původci atypických pneumonií (Ureaplasma urealyticum/parvum). Klinický a RTG nález bývá podobný jako u MAS. Nedílnou součástí terapie jsou intravenózní antibiotika (např. ampicilin + gentamicin pro adnátní pneumonii) po předchozím odběru materiálů k mikrobiologickým vyšetřením.(3–7)
Air-leak syndrom
Tato skupina zahrnuje několik jednotek – pneumotorax (PNO), plicní intersticiální emfyzém (PIE), pneumomedia-
stinum nebo pneumoperikard. Air-leak syndrom (únik vzduchu mimo dýchací cesty) může komplikovat RDS z plicních příčin (deficit surfaktantu, MAS, pneumonie) nebo se vyskytuje v rámci UPV s nekontrolovanými dechovými objemy (nastavení ventilátoru, resuscitace). Typický je asymetrický auskultační nález a RTG/UZ nález (obr. 6). V případě plášťového pneumotoraxu je možná spontánní úprava, zatímco tenzní pneumotorax vyžaduje urgentní řešení (riziko oběhového selhání a asystolie) → jednorázová punkce (2.–3. mezižeberní prostor v medioklavikulární čáře) a/nebo hrudní drenáž (4.–6. mezižeberní prostor v přední axilární čáře).(3–7)Obr. 6. Tenzní pneumotorax (PNO) – pozitivní transiluminace (prosvícení hrudníku zdrojem silného světla – diafanoskopie) levého hemitoraxu s RTG korelátem (projasnění bez plicního parenchymu s kolapsem levé plíce a přesunem mediastina doprava) 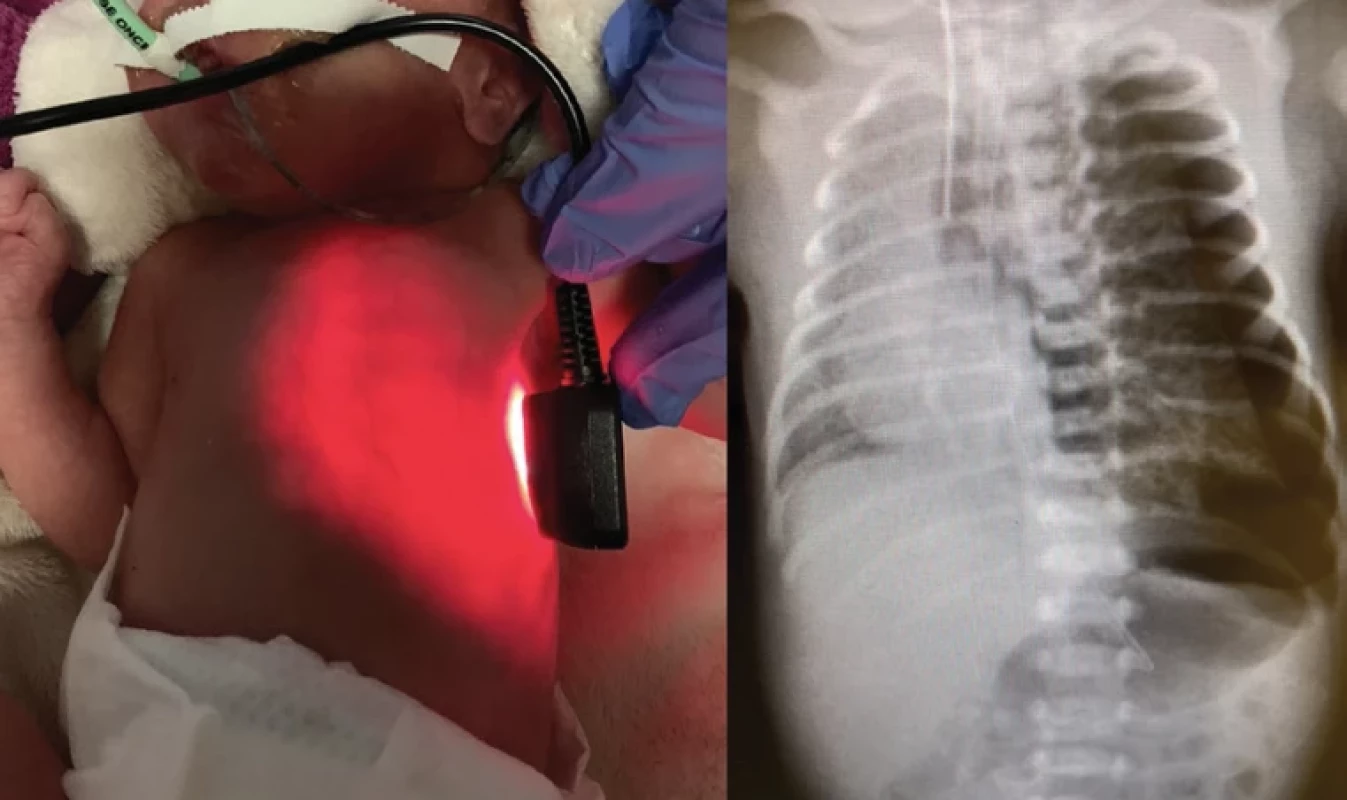
Bronchopulmonální dysplazie (BPD)
BPD představuje multifaktoriální, chronické plicní onemocnění vznikající především u nezralých novorozenců < 32. gestační týden. Působení různých faktorů (infekce, oxygenoterapie, UPV, malnutrice) na nezralou a vulnerabilní plicní tkáň způsobí typický klinický a RTG nález → heterogenní postižení plic s difuzně sníženou transparencí a fokálními změnami ve smyslu emfyzému a atelektázy (obr. 7). Patofyziologicky se jedná o restriktivní plicní onemocnění s fibrotizací (zmnožení intersticiálního vaziva) a poruchou alveolizace a vaskularizace.(3–7) V dnešní době se často používá klasifikace dle Jensena na základě ventilační podpory (bez ohledu na oxygenoterapii) ve 36. postmenstruačním týdnu (tab. 2). Toto rozdělení je nejen relativně jednoduché, ale zároveň nejlépe predikuje úroveň respirační morbidity v časném dětském věku.(8)
Obr. 7. Bronchopulmonální dysplazie (BPD) – heterogenní oboustranné postižení plic s difuzně sníženou transparencí, fokálními atelektázami a emfyzematózně-bulózními změnami 
Tab. 2. Klasifikace bronchopulmonální dysplazie (BPD) dle Jensena ve 36. postmenstruačním týdnu 
Terapie je komplexní a zahrnuje také optimalizaci nutrice (časté je neprospívání), pravidelné kardiologické kontroly (echo k vyloučení závažné plicní hypertenze – riziko cor pulmonale) a u nejzávažnějších forem i domácí oxygenoterapii (propouštění dětí závislých na kyslíku do domácí péče). U dětí s BPD je nutná prevence závažných forem virových respiračních infekcí (respirační syncytiální virus – RSV) prostřednictvím pasivní imunizace (např. palivizumab nebo nirsevimab).(3–8) Interaktivní formulář a indikační kritéria k imunoprofylaxi jsou k dispozici na stránkách České neonatologické společnosti (https://cneos.cz/palivizumab).
TERAPIE RDS
Oxygenoterapie
Kontinuální měření saturace hemoglobinu kyslíkem prostřednictvím pulzní oxymetrie (SpO2) nám umožňuje přesnější dávkování oxygenoterapie (prevence hypoxie a hyperoxie).(3–7)
Ventilační podpora
Neinvazivní ventilační podpora představuje nejčastěji distenční podporu s pozitivním přetlakem (např. PEEP 5–8 cmH2O/mbar) v dýchacích cestách (nazální CPAP – nosní kanyly nebo maska). Invazivní (mechanická) ventilační podpora (UPV) vyžaduje intubaci a zavedení endotracheální kanyly. Používají se konvenční i nekonvenční (vysokofrekvenční) ventilační režimy.(3–8) Nastavení synchronní ventilace (např. SIMV, SIPPV, PSV) a volume guarantee (VG) k dosažení stabilnějších dechových objemů sníží riziko volutraumatu/barotraumatu (air-leak syndrom) a závažných forem peri-/intraventrikulárního krvácení u nezralých novorozenců.(9)
Pro donošené a lehce nedonošené novorozence (≥ 35. gestační týden) se známkami RDS v časném peripartálním období je k dispozici doporučený postup České neonatologické společnosti (https://cneos.cz/wp-content/uploads/2022/08/RDS_Term_LatePreterm_2022.pdf).
Surfaktant
Surfaktant je povrchově aktivní látka (surface active agent), která snižuje povrchové napětí, stabilizuje alveoly proti kolapsu na konci exspiria a zlepšuje poddajnost (compliance) plic (obr. 8). Pneumocyty II. typu začínají produkovat surfaktant ve 22.–24. týdnu těhotenství a jsou zodpovědné i za jeho následnou reabsorpci a recyklaci k dalšímu použití. Zásoby surfaktantu (surfactant storage pool) u donošeného a nedonošeného novorozence se dramaticky liší (100 mg/kg vs. 5 mg/kg). Surfaktant je tvořen z 85 % fosfolipidy (dipalmitoyl fosfatidylcholin, fosfatidylcholin, fosfatidylglycerol) a z 10 % specifickými proteiny (SP-A/B/C/D).(10)
Obr. 8. Pneumocyty I. typu tvoří většinu vnitřního povrchu alveolu (výměna plynů). Pneumocyty II. typu jsou zodpovědné za produkci a recyklaci surfaktantu (snížení povrchového napětí) 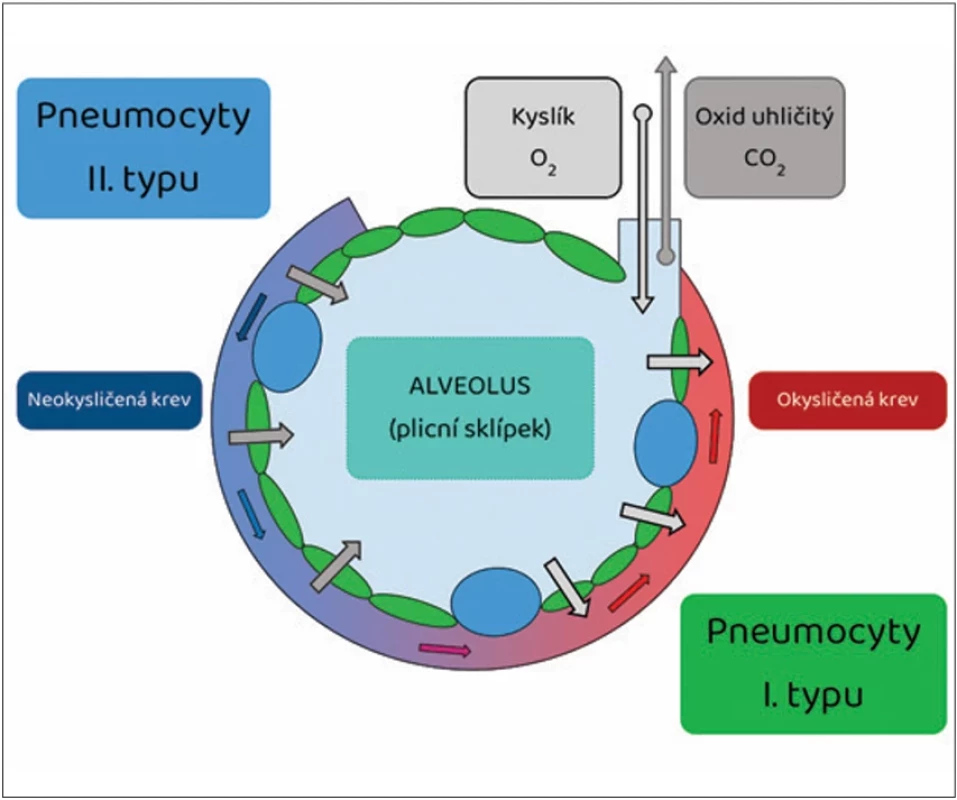
Při závažnějším průběhu RDS na podkladě deficitu surfaktantu je nutná jeho exogenní aplikace do plic (např. poractant alfa / Curosurf® 200 mg/kg – surfaktant získaný z laváže prasečích plic). Léčebnou látku lze aplikovat i v případech sekundární inaktivace/dysfunkce surfaktantu (např. kongenitální/adnátní pneumonie, MAS nebo plicní apoplexie). Administraci surfaktantu lze provést několika způsoby:(3–7)
- Intubace a podání surfaktantu při pokračování v UPV („klasická“ metoda).
- LISA (less invasive surfactant administration) – aplikace surfaktantu pomocí tenkého katétru (např. Vygon Surfcath) za probíhající neinvazivní ventilační podpory (další podrobnosti vč. praktických videozáznamů lze najít na stránkách České neonatologické společnosti https://cneos.cz/manual-surfaktant-metoda-lisa).
- INSURE (intubace, aplikace surfaktantu a následná extubace ihned nebo do 30–60 minut od administrace surfaktantu).
- Jiné metody zkoušené v klinických studiích – aplikace surfaktantu elektrickou nebulizací (studie CURONEB) nebo prostřednictvím laryngeální masky (surfactant administration through laryngeal or supraglottic airways, SALSA).
Další terapeutické možnosti (dle příčiny RDS)
- Oběhová podpora (PPHN, CDH, kardiologické onemocnění).
- Parenterální nutrice (atrézie jícnu, těžký průběh RDS).
- Antibiotická léčba (pneumonie/sepse).
- Analgosedace (PPHN, těžké formy RDS, BPD).
- Plicní vazodilatace (oxid dusnatý, sildenafil, epoprostenol).
- Antiinflamatorní terapie – kortikosteroidy (BPD).
- Bronchodilatace (salbutamol).
- Chirurgická léčba (VVV srdce, atrézie jícnu, CDH).
- Hrudní drenáž (tenzní pneumotorax).
- Extrakorporální membránová oxygenace (ECMO).
- Ošetřovatelská péče (normotermie, toaleta dýchacích cest, polohování).
- Antenatální kortikosteroidy (dexamethason) – snížení incidence závažných forem RDS.
ZÁVĚR
Syndrom dechové tísně (RDS) novorozence lze definovat jako změnu charakteru (dyspnoe, grunting) a/nebo frekvence (tachypnoe) dýchání.
RDS představuje jeden z nejčastějších důvodů příjmu novorozenců na jednotku intenzivní péče (obr. 9).
Obr. 9. Algoritmus péče o novorozence ≥ 35. gestační týden se známkami RDS – doporučený postup České neonatologické společnosti 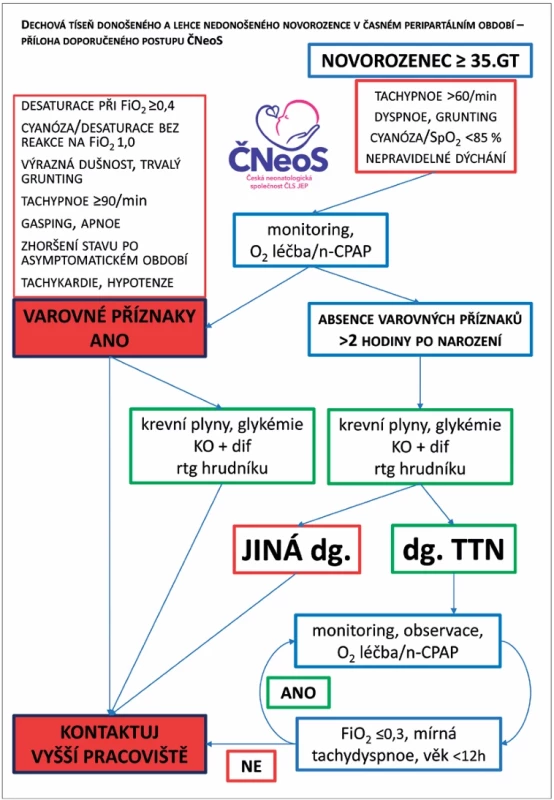
Z praktického, didaktického a diferenciálně diagnostického hlediska můžeme příčiny RDS rozdělit na plicní (pulmonální) a mimoplicní (extrapulmonální).
Plicní příčiny RDS (onemocnění plic) často navazují na narušenou poporodní adaptaci novorozence vlivem různých faktorů (nezralost, císařský řez, diabetes mellitus matky, perinatální hypoxie, zkalená plodová voda, infekční komplikace).
Zhodnocení rizikových faktorů a anamnézy, klinické a laboratorní vyšetření spolu se zobrazovacími metodami (RTG a UZ plic) nám umožňují lépe posoudit závažnost onemocnění, a zvolit tak adekvátní terapii.
Mezi terapeutické modality patří oxygenoterapie, ventilační podpora, aplikace surfaktantu, podpůrná (ošetřovatelská péče, parenterální nutrice) a specifická léčba (antibiotika, operace, hrudní drenáž).
Zdroje
1. Korček P, Straňák Z. Význam placentární transfuze ve vztahu ke kardiopulmonální stabilizaci novorozence a závažné neonatální morbiditě. Čes-slov Neonat 2022; 28(1): 50–54.
2. Madar J, Roehr CC, Ainsworth S, et al. European Resuscitation Council Guidelines 2021: Newborn resuscitation and support of transition of infants at birth. Resuscitation 2021; 161 : 291–326.
3. Straňák Z, Janota J. Neonatologie. EEZY Publishing 2023.
4. Malý J, Juren T. Dechová tíseň (Respiratory distress) donošeného a lehce nedonošeného novorozence v časném peripartálním období. Doporučený postup České neonatologické společnosti 2022.
5. Dort J, Dortová E, Jehlička P. Neonatologie. Učební texty Univerzity Karlovy v Praze. Karolinum 2013.
6. Sweet DG, Carnielli VP, Greisen G, et al. European Consensus Guidelines on the Management of Respiratory Distress Syndrome: 2022 Update. Neonatology 2023; 120(1): 3–23. doi: 10.1159/000528914
7. Yadav S, Lee B. Neonatal respiratory distress syndrome. In: StatPearls. Treasure Island (FL): StatPearls Publishing 2023.
8. Jensen EA, Dysart K, Gantz MG, et al. The diagnosis of bronchopulmonary dysplasia in very preterm infants. An evidence-based approach. Am J Respir Crit Care Med 2019; 200(6): 751–759. doi: 10.1164/rccm.201812-2348OC
9. Korček P, Širc J, Berka I, et al. Does perinatal management have the potential to reduce the risk of intraventricular hemorrhage in preterm infants? Front Pediatr 2024; 12 : 1361074. doi: 10.3389/fped.2024.1361074
10. Sardesai S, Biniwale M, Wertheimer F, et al. Evolution of surfactant therapy for respiratory distress syndrome: past, present, and future. Pediatr Res 2017; 81 : 240–248. doi: 10.1038/pr.2016.203
Štítky
Neonatológia Pediatria Praktické lekárstvo pre deti a dorast
Článok vyšiel v časopiseČesko-slovenská pediatrie
Najčítanejšie tento týždeň
2025 Číslo 5- Léčba bolesti a horečky u dětí
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Gastroezofageální reflux a gastroezofageální refluxní onemocnění u kojenců a batolat
- Očkování nejvíc potřebuje ten, kdo sám být očkován nemůže − kazuistika
- Pokrok v boji s malárií − první vakcína poskytující přijatelnou ochranu proti nemoci
-
Všetky články tohto čísla
- Josef Hubáček: Osamělý dům (1926)
- Odkud jdeme a kam směřujeme? Cestu pediatrie naznačí ohlédnutí prostřednictvím vybraných textů, které uveřejnil náš časopis před 75, 50 a 25 lety.
- Rossum’s Universal Robots (R.U.R.) a Artificial Intelligence (AI)
- Umělá inteligence pro pediatry: jak (ne)bojovat s budoucností
- Umělá inteligence v zobrazovacích metodách
- Využití metod umělé inteligence v patologii
- Pohled na využití umělé inteligence v klinické mikrobiologii
- Sedem aktuálnych trendov umelej inteligencie v pediatrii
- Atypický HUS s mutáciou trombomodulínu – klinický priebeh a odpoveď na inhibíciu komplementu
- Onemocnění plic u novorozenců
- Genderová dysforie a genderový nesoulad u dětí a dospívajících: průvodce pro pediatrickou praxi
- Príspevok k histórii detskej kardiológie na Slovensku
- Laudácia k významnému životnému jubileu
- Cena J. E. Purkyně udělena prof. MUDr. Vladimíru Komárkovi
- Stéla Klostermann
- Česko-slovenská pediatrie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Onemocnění plic u novorozenců
- Genderová dysforie a genderový nesoulad u dětí a dospívajících: průvodce pro pediatrickou praxi
- Atypický HUS s mutáciou trombomodulínu – klinický priebeh a odpoveď na inhibíciu komplementu
- Sedem aktuálnych trendov umelej inteligencie v pediatrii
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



