Ewingův sarkom – současné diagnostické a terapeutické postupy
Ewing sarcoma – current diagnostic and therapeutic approaches
Background: Ewing sarcoma belongs to the family of undifferentiated small round cell sarcomas of bone and soft tissue. It is characterized by a gene fusion involving EWSR1 and an ETS-family transcription factor gene. In 85–96% of cases, a specific chromosomal translocation results in the EWSR1-FLI1 fusion gene, whose product functions as an oncogene essential for tumorigenesis. Ewing sarcoma is most common in adolescents and young adults. It primarily affects the diaphyses of long bones, the pelvis, and the axial skeleton, although extraosseous involvement is not uncommon. This is a highly malignant neoplasm, and in most cases, micrometastases are already present at the time of diagnosis. The treatment is multimodal and includes local therapy (surgery and/or radiotherapy) and systemic chemotherapy. One of the greatest therapeutic challenges remains the long-term systemic control of the disease. To improve overall survival – especially in high-risk patients – innovative treatment strategies are essential, as the potential for intensifying chemotherapy has reached its limit due to treatment-related toxicity. Both diagnostic and therapeutic management should take place in specialized sarcoma centers. Aim: This article aims to provide an up-to-date overview of current diagnostic and therapeutic approaches in Ewing sarcoma.
Keywords:
Chemotherapy – Ewing sarcoma – targeted therapy
Authors:
A. Nohejlová Medková; P. Pacas; K. Kopečková
Authors‘ workplace:
Onkologická klinika 2. LF UK a FN Motol a Homolka, Praha
Published in:
Klin Onkol 2026; 39(2): 99-104
Category:
Review
doi:
https://doi.org/10.48095/ccko202699
Overview
Východiska: Ewingův sarkom se řadí do rodiny tzv. nediferencovaných malých kulatobuněčných sarkomů kostí a měkkých tkání (small round cell sarcomas). Je charakterizován genovou fúzí zahrnující EWSR1 a gen pro transkripční faktor z rodiny ETS. Produktem specifické chromozomální translokace je v 85–96 % vznik fúzního genu EWSR-FLI1, jehož produkt působí jako onkogen zásadní pro tumorigenezi. Nejčastěji se vyskytuje u adolescentů a mladých dospělých. Postihuje primárně diafýzy dlouhých kostí, pánevní a osový skelet, vzácností není ani extraoseální postižení. Jedná se o vysoce maligní nádorové onemocnění, které se, ve většině případů již v době diagnózy, vyznačuje přítomností mikrometastáz. Léčba je multimodální, zahrnuje lokální terapii – chirurgie, radioterapie – i systémovou léčbu chemoterapií. Největší výzvou v terapii zůstává dlouhodobá efektivní systémová kontrola onemocnění. Pro zlepšení celkového přežití, zejména u pacientů s vysokým rizikem, jsou nezbytné inovativní terapeutické strategie, jelikož možnosti podávání chemoterapie dosáhly svého maxima stran toxicity léčby. Management diagnostiky i terapie má probíhat ve specializovaných sarkomových centrech. Cíl: Tento článek by měl poskytnout aktuální přehled o diagnostice a terapii Ewingova sarkomu.
Klíčová slova:
Ewingův sarkom – cílená léčba – chemoterapie
Úvod, epidemiologie
Ewingův sarkom (EwS) je pojmenován po americkém profesorovi Jamesi Ewingovi (1866–1943), který byl ve své době průkopníkem výzkumu a léčby maligních onemocnění (obr. 1). V roce 1920 popsal zhoubný nádor kosti, který po něm byl později pojmenován [1].

Incidence EwS je 0,3/100 000 obyvatel za rok (u kavkazské rasy). Nejčastěji postihuje adolescenty a mladé dospělé, častěji se vyskytuje u chlapců, mužů. Medián věku výskytu je 15 let [2]. V klinické praxi se setkáváme i s pacienty staršího věku.
Nádor může vzniknout prakticky kdekoliv, přičemž nejčastěji postihuje diafýzy dlouhých kostí, zejména femuru, dále pánev, žebra a axiální skelet. Výjimkou však nejsou ani extraoseální manifestace, v ČR je např. popsán případ 15leté pacientky s primárním postižením děložního čípku [3] nebo 54leté nemocné s primárním postižením močového měchýře [4]. Přibližně 20–25 % pacientů má v době diagnózy metastatické onemocnění, přičemž metastázy se nejčastěji nacházejí v plicích (70–80 %), kostech a kostní dřeni (40–45 %). Přítomnost metastáz významně zhoršuje prognózu pacientů [5].
Mezi prognostické faktory se řadí věk (< 15 let vs. ≥ 15 let), objem nádoru (< 200 ml vs. ≥ 200 ml), primární lokalizace (končetiny vs. osový skelet), známá přítomnost vzdálených metastáz, patologická odpověď na neoadjuvantní terapii. Na základě těchto faktorů byly stanoveny prognostické skupiny: pacienti s dobrou prognózou (lokalizované onemocnění < 200 ml, dobrá odpověď na neoadjuvantní léčbu) a nemocní se špatnou prognózou (lokalizované onemocnění ≥ 200 ml, špatná odpověď na neoadjuvantní léčbu). Nejhorší prognózu mají pacienti primárně generalizovaní, prognóza je lepší u těch, kteří mají metastatické onemocnění izolovaně v plicích oproti pacientům s metastázami v jiných lokalizacích [2].
Diagnostika
Základní pilíře diagnostiky jsou klinický obraz, zobrazovací metody a bioptické vyšetření včetně histologického, imunohistochemického a molekulárně-genetického vyšetření.
Tyto diagnostické postupy vyžadují multidisciplinární přístup a jsou klíčové pro včasné zahájení léčby a zlepšení prognózy pacientů.
Klinický obraz
EwS se projevuje lokálně i systémově. Mezi nejčastější lokální příznaky patří: bolest v oblasti postižené kosti nebo končetiny, která často zesiluje v noci nebo při fyzické aktivitě. Otok a zarudnutí v oblasti nádoru. Zvýšená teplota kůže nad postiženým místem.
Mezi celkové příznaky patří: horečky, únava, hubnutí. V laboratoři dochází k vzestupu zánětlivých parametrů a laktátdehydrogenázy (LDH).
Diferenciálně diagnosticky mohou být tyto příznaky zaměněny za osteomyelitidu nebo jiné nádorové onemocnění kostí (osteosarkom, lymfom, Langerhansova histiocytóza či metastázy – neuroblastom) [2].
Zobrazovací metody
Správný výběr zobrazovací metody je klíčový pro stanovení diagnózy, posouzení rozsahu onemocnění a následný terapeutický postup. Základem je MR a pozitronová emisní tomografie (PET/CT) či CT.
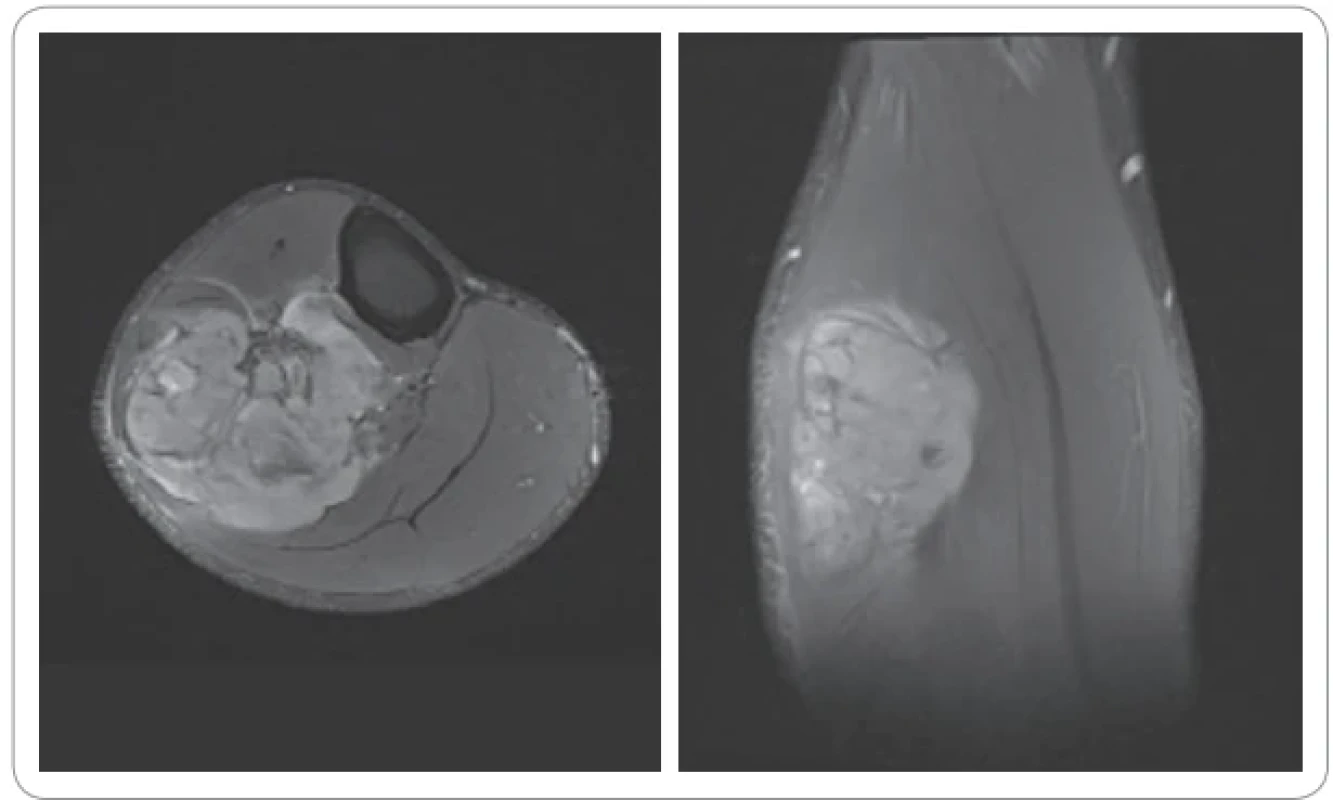
MR je metodou volby při podezření na EwS, neboť poskytuje detailní informace o lokální invazi nádoru a jeho vztahu k okolním strukturám (obr. 2). Používají se sekvence T1 a T2 s kontrastní látkou (gadolinium), které odhalují charakteristické znaky tumoru, jako jsou ostrá přechodová zóna mezi nádorem a zdravou kostní tkání, edém v okolí tumoru, zvýšené vychytávání kontrastní látky (gadolinium enhancement), přítomnost měkkotkáňové složky. Pro vyloučení tzv. skip metastáz je nutné vyšetření celého kompartmentu. MR se také uplatňuje v hodnocení terapeutické odpovědi a sledování nemocných po ukončení léčby.
PET/CT s fluorodeoxyglukózou značenou fluorem-18 (18F-FDG), je další klíčovou metodou k určení rozsahu onemocnění a vyloučení vzdálených metastáz [5].
V rámci zobrazovacích metod provádíme před zahájením terapie i vyšetření srdce pomocí echokardiografie z důvodu aplikace antracyklinů.
Bioptické vyšetření
Diagnostickou biopsii je nutné provádět ve specializovaných centrech zaměřujících se na diagnostiku a terapii sarkomů, po konzultaci s ortopedickým nebo chirurgickým týmem, který bude provádět následnou definitivní operaci tumoru, včetně odstranění kanálu po biopsii. Provádí se na základě magnetické rezonance. Pro správné vyhodnocení je důležitý dostatek materiálu, doporučuje se získat více vzorků z jedné biopsie, proto je nedostačující biopsie pouze tenkou jehlou [2]. Využívá se incizionální biopsie, otevřená biopsie nebo biopsie širokou jehlou. Dostačující je odběr z extraoseální složky tumoru. Kostní biopsii provádíme pouze v případě, že je tumor lokalizován pouze v kosti. Bez ohledu na metodu biopsie je důležité vyvarovat se vzniku hematomu a kontaminace neurovaskulárních struktur a tkání. Veškerá okolní tkáň, která by mohla být kontaminována, musí být následně resekována.
Za určitých okolností se biopsie provádí i v případě recidivy onemocnění, jednak pro potvrzení, že se jedná o recidivu, a také pro případ dalšího genetického testování.
Při negativitě PET/CT neprovádíme odběr kostní dřeně.
Biopsie, nezbytná pro definitivní diagnózu, zahrnuje:
1)
Histologické vyšetření, které potvrdí přítomnost nediferencovaných malých, kulatých nádorových buněk s vysokou mitotickou aktivitou.
2)
Imunohistochemické vyšetření zaměřené na detekci typických markerů, jako jsou CD99 a FLI-1. CD99 je vysoce senzitivní, ale málo specifický znak, objevuje se u 90 % EwS, ale vyskytuje se i v normálních tkáních a u různých dalších nádorových onemocnění, typicky u lymfomů. Dalším senzitivním, ale nespecifickým znakem je exprese FLI1.
3)
Molekulárně patologické a molekulárně genetické vyšetření, která jsou nutná pro definitivní potvrzení diagnózy EwS.
Typické pro EwS jsou translokace t (11; 22) (q24; q12) vedoucí k fúzi genů EWSR1-FLI1 (v 85 %) a t (21; 22) (q22; q12) vedoucí k fúzi genů EWSR1-ERG (v 10 %). Metodou fluorescenční in situ hybridizace (FISH) detekujeme přestavbu genů EWSR1 anebo pomocí polymerázové řetězové reakce v reálném čase (RT-PCR) lze detekovat fúze genu FET-ETS specifických pro EwS. Tato vyšetření jsou používána více než 25 let [6]. Stanovení EWSR1 je důležité pro diferenciální diagnostiku dalších podtypů nesoucích fúze EWSR1 s non-ETS geny (PATZ1, NFATc2) či zcela jiných druhů sarkomů (desmoplastický malobuněčný nádor, světlobuněčný sarkom, extraskeletální myxoidní chondrosarkom). Jako odlišná nozologická jednotka se vyčleňují CIC rearanžované, resp. BCOR alterované sarkomy [7]. V současné době je součástí vyšetření i molekulárně genetické testování (next generation sequencing – NGS). Použití NGS je doporučeno pro malé kulatobuněčné nádory, u kterých metodou FISH ani RT-PCR nemůžeme potvrdit diagnózu EwS [2,5].
Laboratorní vyšetření
Z laboratorních metod vyšetřujeme krevní obraz a biochemii, včetně LDH a CRP [2].
Terapie
V léčbě EwS se uplatňuje lokální i systémová léčba. Primárně se řídíme doporučením multidisciplinárního týmu a doporučenými postupy, které vycházejí z mezinárodních randomizovaných klinických studií. Tyto protokoly jsou určeny především pro dětskou populaci a pacienty mladšího dospělého věku. Ve své praxi se setkáváme i s pacienty staršího věku, kde je nutné terapeutický přístup modifikovat s ohledem na závažnou toxicitu léčby. Veškerá léčba má probíhat ve specializovaných sarkomových centrech, kde je k dispozici tým odborníků na danou problematiku.
Lokální terapie
V lokální léčbě se uplatňuje chirurgie nebo radioterapie (RT). Operační řešení dosahuje lepší lokální kontroly oproti definitivní RT. Při volbě metody zvažujeme riziko lokální recidivy vs. funkční výsledek a pozdní následky obou modalit.
Radikální operační výkon následuje standardně po neoadjuvantní chemoterapii (CHT). Pouze v případě hrozících komplikací, např. míšní komprese, je možná primární operace. Podstatou chirurgického zákroku je široká resekce založená na primární velikosti nádoru. Dle lokalizace primárního tumoru mohou být součástí operačního výkonu i rekonstrukční chirurgické techniky. Primární amputace je prováděna pouze ve vzácných případech.
Histopatologická odpověď má zásadní vliv na riziko lokální recidivy. Za adekvátní odpověď na CHT se považuje přítomnost více než 90 % nekróz. Chirurgická léčba se může zvažovat i u primárně metastatického onemocnění či relabujícího onemocnění a měla by být doplňkem k systémové léčbě [5].
Radioterapie
Radiosenzitivita EwS byla rozpoznána již v době popisu onemocnění Jamesem Ewingem. RT se využívá buď jako definitivní metoda u inoperabilních nádorů, nebo v kombinaci s operací před výkonem nebo po něm. Předoperačně se používá v případě progrese primárního nádoru, v případě předpokládané R1 nebo R2 resekce. Po operaci je indikována při intralezionální či R+ resekci, event. při špatné histologické odpovědi na neoadjuvantní CHT (více než 10 % viabilní tkáně v tumoru). Používají se techniky RT s modulovanou intenzitou (intensity-modulated radiotherapy – IMRT), event. protonové terapie.
U metastatického onemocnění může být RT důležitou součástí multimodální léčby, kdy všechna mimoplicní ložiska mohou být ozářena nižší dávkou, pro oligometastatické onemocnění se využívají techniky stereotaktické RT. RT celých plic (whole-lung irradiation – WLI) je v současné době využívána vzácně, a to spíše u dětí než u dospělých. Zvažuje se u pacientů s izolovaným metastatickým postižením plic a s dobrou odpovědí na CHT. RT má své místo i v paliativní péči [5,8].
Systémová léčba
Systémová léčba je nedílnou součástí terapie EwS. V první linii léčby je standardem aplikace neoadjuvantní a po resekci primárního tumoru adjuvantní CHT. V současné době používáme režim v rámci protokolu EURO EWING 2012 na základě výsledků randomizované studie EE2012 (schéma 1), kde byla prokázána superiorita ve smyslu léčebné odpovědi a nižší toxicity v rameni s kombinovanou terapií VDC/IE (vinkristin, doxorubicin, cyklofosfamid/ifosfamid, etoposid) oproti rameni s CHT režimem VIDE (vinkristin, ifosfamid, doxorubicin, etoposid); tento režim byl dříve standardem v rámci protokolu EURO EWING 99 / EWING 2008. Tříletého přežití bez příhody (event-free survival – EFS) bylo ve skupině s CHT režimem VIDE dosaženo u 61 % pacientů a ve skupině VDC/IE u 67 % pacientů [9]. Mezi nejčastější nežádoucí účinky patří hematologická toxicita, především leukopenie a trombocytopenie, dále nauzea, zvracení a specifická toxicita jednotlivých preparátů. Důležité je profylaktické podávání hematopoetických růstových faktorů, prevence nauzey a zvracení, dostatečná hydratace, prevence hemoragické cystitidy. Standardem je aplikace do permanentního centrálního žilního vstupu. Pro prognózu pacientů je zásadní dodržení dávkové intenzity CHT. Je potřeba držet se protokolu studie, kde jsou jasně daná kritéria k podání léčby. Vzhledem k náročnosti terapie, managementu nežádoucích účinků a průběhu terapie je důležité léčbu podávat ve vybraných národních onkologických centrech, které mají nejvíce zkušeností s takovým postupem. Fungují zde multidisciplinární týmy, proto by měl být pacient na specializovaná pracoviště odeslán již při podezření na toto onemocnění [10].
![Schéma 1. Protokol studie [19].](https://pl-master.mdcdn.cz/media/image/6acbeda6bae9d1cd8c642e2c96de5fd8.png?version=1777026712)
Role vysokodávkové CHT s autologní transplantací kmenových buněk v léčbě nově diagnostikovaného EwS je kontroverzní. V současnosti není standardně doporučována pro léčbu nově diagnostikovaného EwS, zejména v éře intenzivních neoadjuvantních režimů typu VDC/IE. Její využití by mělo být individuálně zváženo, ideálně v rámci prospektivních klinických studií [8].
Relaps onemocnění je pozorován přibližně u 30–40 % pacientů s primárně lokalizovaným onemocněním a až u 60–80 % pacientů s metastatickou formou EwS. Systémový relaps tvoří 71–73 % případů, kombinovaný systémový a lokální relaps se vyskytuje ve 12–18 % a izolovaný lokální relaps je zaznamenán pouze u 11–15 % pacientů.
Volba terapie pro pacienty s recidivou EwS je individuální, prognóza onemocnění je špatná, dlouhodobě přežívá pouze 25 % pacientů.
Nejvýznamnějším prognostickým faktorem je doba do progrese onemocnění. Pacienti, kteří relabují v průběhu prvních 2 let, mají naději na dlouhodobé celkové přežití v méně než 10 %, nemocní s recidivou po více než 2 letech od primární diagnózy kolem 30 %. Dalším prognostickým faktorem je lokalizace recidivy. Lepší prognózu mají pacienti s lokální recidivou oproti pacientům s metastatickým rozsevem. Nejhorší prognózu mají nemocní s lokální i systémovou recidivou. Tyto faktory musí být zohledněny při volbě léčebné strategie.
Většina pacientů s první recidivou je léčena CHT. Nemocní s dobrou odpovědí na systémovou léčbu mohou podstoupit následnou lokální léčbu (chirurgickou, radioterapeutickou) reziduální choroby [5].
Pro pacienty je vhodné zařazení do mezinárodních klinických studií. Od roku 2015 probíhá pro pacienty s recidivou EwS randomizovaná studie rEECur, jejímž cílem je porovnat různé režimy CHT a určit, který z nich má největší efektivitu a nejméně závažných nežádoucích účinků. Nábor pacientů do ramen topotekan a cyklofosfamid, irinotekan a temozolomid a také gemcitabin s docetaxelem byl uzavřen, jelikož se neprokázala superiorita oproti monoterapii s ifosfamidem. V současnosti je možno zařazovat pacienty do ramene s ifosfamidem (nově v kombinaci s lenvatinibem) nebo s karboplatinou a etoposidem [11]. Studie je vedena ve Velké Británii a z regulačních důvodů není t. č. možné v ČR pacienty zařadit. Před odchodem Velké Británie z EU jsme na našem pracovišti zařadili pět pacientů.
Pro pacienty léčené ve vyšších liniích není standardní terapie a jedná se o léčbu s paliativním záměrem. Tito nemocní jsou kandidáti pro zařazení do klinických studií fáze I/II. Existuje nenaplněná potřeba nových terapeutických možností pro tyto pacienty.
Léčba pomocí CHT dosáhla svého maxima, co se týče její intenzity. Pro její toxicitu nelze již dávky navyšovat, proto je v současné době ve fázi klinického testování cílená terapie používaná u jiných typů nádorových onemocnění. Cílem výzkumu je i léčba založená na mechanizmu vzniku nádorového onemocnění [5].
Cílená léčba
Mezi preparáty s určitým pozitivním efektem se řadí kabozantinib či regorafenib.
Kabozantinib je multityrozinkinázový inhibitor (mTKI) a byl testován ve studii CABONE u pacientů s relabovaným EwS. Zařazeno bylo 39 pacientů, 10 z nich (26 %) dosáhlo objektivní odpovědi v 6 měsících. Kabozantinib by mohl být zvažován s ohledem na prokázaný protinádorový efekt a dobrou toleranci jako léčba druhé a vyšší linie u pacientů s předchozí významnou hematologickou toxicitou, jako nechemoterapeutická varianta s benefitem tabletové léčby. Před zavedením do běžné praxe je potřeba další výzkum [5,12].
Regorafenib je dalším TKI, testován proti placebu u pacientů progredujících na standardní terapii ve studii REGOBONE. Medián doby do progrese (progression-free survival – PFS) byl 11,4 týdne v rameni s regorafenibem oproti 3,9 týdne v rameni s placebem. Lze předpokládat, že regorafenib může lehce prodloužit dobu do další progrese onemocnění po selhání předchozích linií CHT [13].
Dále proběhla studie fáze I s talazoparibem + irinotekanem ± temozolomidem, kdy byla prokázána jistá aktivita, ovšem zde je potřeba další výzkum [14]. Další testovanou léčebnou variantou je kombinace inhibice CDK4/6 a IGFR1 [15]. Probíhá (pre) klinický výzkum na terapeutické zacílení na EWSR1-FLI1 [5].
Imunoterapie
Nízká mutační nálož a nedostatek nádorově specifických antigenů (TSAs) řadí EwS mezi tzv. imunologicky „chladné“ nádory, což zásadně omezuje účinnost standardních imunoterapií. Zároveň je u EwS často přítomna nízká exprese MHC I, zvýšená exprese kontrolních bodů a imunosupresivní nádorové mikroprostředí bohaté na M2 makrofágy, které podporují růst nádoru. Současné možnosti imunoterapie (checkpoint inhibitory, onkolytické viry, nádorové vakcíny a adoptivní buněčné terapie (např. CAR T, TCR-transgenní T buňky)), které přinesly zásadní průlom u imunogenních nádorů, jsou u pediatrických sarkomů včetně EwS pro nízkou účinnost omezené. Pro zlepšení účinnosti imunoterapie u EwS je nezbytné cílit jak na nádorové buňky, tak na jejich mikroprostředí [16].
Cíle dalšího výzkumu
Přes trvající výzkum onemocnění a intenzifikaci terapie je ve srovnání s ostatními maligními nádory prognóza pacientů s EwS stále špatná. Další výzkum probíhá na mezinárodní úrovni. Naše pracoviště je zapojeno na úrovni klinických studií do spolupráce s EuroEwing Consortium (EEC). Strategií výzkumu je sjednotit vyšetření vzorků nádorové tkáně, vytvoření biobank a na základě toho identifikovat a validovat molekulární stratifikaci, identifikovat mechanizmy patogeneze, rezistence, analyzovat biomarkery zodpovědné za relaps. Mezi další cíle se řadí i výzkum nádorového mikroprostředí a vývoj vhodných preklinických modelů [17].
V rámci prekliniky je využíván mimo jiné integrovaný přístup zahrnující transkriptomiku, proteomiku a metylomiku ke komplexní analýze primárních nádorů i metastáz EwS vedoucích k identifikaci specifických signálních drah a kandidátních genů, které by mohly hrát roli v progresi a agresivitě onemocnění. Jiné výzkumné skupiny rozšiřují poznání o EwS pomocí jednobuněčné RNA-sekvenování (scRNA-seq), epigenomických profilací a dalších multiomických přístupů. Tyto strategie umožňují detailní porozumění molekulárním mechanizmům regulujícím chování nádorových buněk EwS. Dvě nedávno publikované multiomické studie identifikovaly odlišné dráhy, které EwS buňky pravděpodobně využívají k progresi onemocnění. Jako potenciální regulátory EwS byly identifikovány geny CREB1, LOXHD1 a FGD4, které si zasluhují další funkční charakterizaci. Pozornost si zaslouží imunitní modulace prostřednictvím IFNa nebo TNFa, která může podporovat vznik metastáz změnou mikroprostředí nádoru.
Celkově je preklinický výzkum důležitý k detailnějšímu porozumění biologii EwS a cílem je usnadnit vývoj terapeutických strategií vedoucích ke zlepšení prognózy pacientů s tímto onemocněním [18].
Závěr
Prognóza pacientů s EwS závisí na časné a správné diagnóze a na rychlém zahájení léčby. Tyto podmínky je reálné naplnit ve specializovaných centrech, kam mají být nemocní s podezřením na tuto diagnózu co nejdříve odesláni. EwS není jen onemocněním dětského věku, vyskytuje se i u mladých dospělých a ve výjimečných případech i u starších pacientů. Proto je nutné na tuto diagnózu myslet v každém věku. Současný přístup k léčbě je založen na multimodální strategii kombinující CHT, chirurgickou resekci a RT. Právě tento komplexní přístup významně zlepšuje prognózu pacientů, zejména těch s lokalizovanou formou onemocnění.
Sources
1. AACR. Founder James Ewing. [online]. Available from: https: //www.aacr.org/governance/james-ewing/.
2. Fernández CM, Sebio A, Rincon JO et al., Clinical practice guidelines for the treatment of Ewing sarcoma (Spanish Sarcoma Research Group-GEIS). Clin Transl Oncol 2025; 27 (3): 824–836. doi: 10.1007/s12094-024 - 03602-5.
3. Bílek O, Holánek M, Zvaríková M et al. Extraoseus Ewings sarcoma, primary affection of uterine cervix – case report. Klin Onkol 2015; 28 (4): 284–287. doi: 10.14735/amko2015284.
4. Král M, Kurfürstová D, Hartmann I et al. Ewing’s sarcoma of the urinary bladder – the urologic and pathologic differential diagnosis and current therapeutic options. Klin Onkol 2023; 36 (4): 314–319.
5. Zöllner SK, Amatruda JF, Bauer S et al. Ewing sarcoma – diagnosis, treatment, clinical challenges and future perspectives. J Clin Med 2021; 10 (8): 1685. doi: 10.3390/jcm10081685.
6. Procházka P, Vícha A, Kodet R et al. Nádory ze skupiny Ewingova sarkomu – molekulární biologie a genetika. Klin Onkol 2007; 20 (2): 205–208.
7. Dehner CA, Lazar AJ, Chrisinger JSA. Updates on WHO classification for small round cell tumors: Ewing sarcoma vs. everything else. Hum Pathol 2024; 147 : 101–113. doi: 10.1016/j.humpath.2024.01.007.
8. Gupta A, Riedel RF, Shah C et al. Consensus recommendations in the management of Ewing sarcoma from the National Ewing Sarcoma Tumor Board. Cancer 2023; 129 (21): 3363–3371. doi: 10.1002/cncr.34942.
9. Brennan B, Kirton L, Perrine MB et al. Comparison of two chemotherapy regimens in patients with newly diagnosed Ewing sarcoma (EE2012): an open-label, randomised, phase 3 trial. Lancet 2022; 400 (10362): 1513–1521. doi: 10.1016/S0140-6736 (22) 01 790-1.
10. Krákorová Adámková D, Tuček Š, Tomášek J et al. Léčba Ewingova sarkomu/periferního neuroektodermálního tumoru dospělých. Onkologie 2012; 6 (2): 91–95.
11. UCL. rEECur. [online]. Dostupné z: https: //www.ucl.ac.uk/medical-sciences/divisions/cancer/centres-and-networks/euro-ewing-consortium/clinical-trials/reecur.
12. Italiano A, Mir O, Mathoulin-Pelissier S et al. Cabozantinib in patients with advanced Ewing sarcoma or osteosarcoma (CABONE): a multicentre, single-arm, phase 2 trial. Lancet Oncol 2020; 21 (3): 446–455. doi: 10.1016/S1470-2045 (19) 30825-3.
13. Duffaud F, Blay JY, Le Cesne A et al. Regorafenib in patients with advanced Ewing sarcoma: results of a non-comparative, randomised, double-blind, placebo-controlled, multicentre Phase II study. Br J Cancer 2023; 129 (12): 1940–1948. doi: 10.1038/s41416-023-02 413-9.
14. Federico SM, Pappo AS, Sahr N et al. A phase I trial of talazoparib and irinotecan with and without temozolomide in children and young adults with recurrent or refractory solid malignancies. Eur J Cancer 2020; 137 : 204–213. doi: 10.1016/j.ejca.2020.06.014.
15. Guenther LM, Dharia NV, Ross L et al. A combination CDK4/6 and IGF1R inhibitor strategy for Ewing sarcoma. Clin Cancer Res 2019; 25 (4): 1343–1357. doi: 10.1158/1078-0432.CCR-18-0372.
16. Evdokimova V, Gassmann H, Radvanyi L et al. Current state of immunotherapy and mechanisms of immune evasion in Ewing sarcoma and osteosarcoma. Cancers 2022; 15 (1): 272. doi: 10.3390/cancers15010272.
17. Geen D, van Ewijk R, Tirtei E et al. Biological sample collection to advanced research and treatment: a fight osreosarcoma through European Research and Euro Ewing Consortium Statement. Clin Cancer Res 2024; 30 (16): 3395–3406. doi: 10.1158/1078-0432.CCR-24-0101.
18. Chicón-Bosch M, Sanchéz-Serra S, Rosàs-Lapeña M et al. Multi-omics profiling reveals key factors involved in Ewing sarcoma metastasis. Mol Oncol 2025; 19 (4): 1002–1028. doi: 10.1002/1878-0261.13788.
19. Anderton J, Moroz V, Marec-Bérard P et al. International randomised controlled trial for the treatment of newly diagnosed EWING sarcoma family of tumours – EURO EWING 2012 Protocol. Trials 2020; 21 (1): 96. doi: 10.1186/s13063-019-4026-8.
Labels
Paediatric clinical oncology Surgery Clinical oncologyArticle was published in
Clinical Oncology

2026 Issue 2
- Safety and Tolerance of Metamizole in Postoperative Analgesia in Children
- Metamizole in perioperative treatment in children under 14 years – results of a questionnaire survey from practice
- Obstacle Called Vasospasm: Which Solution Is Most Effective in Microsurgery and How to Pharmacologically Assist It?
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Current Insights into the Antispasmodic and Analgesic Effects of Metamizole on the Gastrointestinal Tract
-
All articles in this issue
- Není ct jako CT
- Léčba Castlemanovy choroby z pohledu roku 2026
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Cirkulující nádorová DNA jako biomarker pro predikci minimální reziduální nemoci a individualizaci adjuvantní léčby kolorektálního karcinomu – přehled současných poznatků a perspektiv
- Intravaskulárna propagácia adenomyózy v krvných cievach myometria a uterinného leiomyómu u pacientky s mutáciou génu fumaráthydratázy – zriedkavý nález imitujúci malígnu neopláziu
- Druhá rekurence karcinomu prsu 36 let po počátečním chirurgickém výkonu a 18 let po první rekurenci – extrémně vzácný případ
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
- Cancer patients admitted to intensive care unit
- Nádory GIT – chemoterapie a precizní léčba se synergicky doplňují
- Snižování škod rizikového chování v onkologické prevenci
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Clinical Oncology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Léčba Castlemanovy choroby z pohledu roku 2026
- FDG-PET/CT: metabolicky aktivní solitární ložisko podkožně gluteálně u pacientky s karcinomem prsu – granulom či metastáza?
- Ewingův sarkom – současné diagnostické a terapeutické postupy
- Intravaskulárna propagácia adenomyózy v krvných cievach myometria a uterinného leiomyómu u pacientky s mutáciou génu fumaráthydratázy – zriedkavý nález imitujúci malígnu neopláziu
