Aplikovatelnost rozšířené reality při jaterní resekci v rámci perioperačního použití
Applicability of augmented reality in perioperative liver resection
Introduction: Liver resection ranks among the most technically demanding abdominal procedures, requiring detailed knowledge of complex three-dimensional anatomy. Augmented reality (AR) represents an innovative technology that overlays digital information on the surgical field and may serve as a tool for perioperative navigation.
Methods: A systematic search of PubMed, MEDLINE, and Cochrane databases was conducted for studies published between January 2022 and August 2025. Only articles in English focusing on human subjects and describing the use of AR during liver resection were included. A total of 133 studies were identified; after removing duplicates, 67 remained. Based on predefined criteria, 10 studies were finally considered relevant for analysis.
Results: The analyzed studies involved 649 patients, of whom 245 underwent liver resection with AR assistance. Five were retrospective with control groups, three were single-arm, and one was prospective. Most studies demonstrated that AR improved intraoperative orientation, facilitated lesion localization, and could reduce blood loss and operative time. In cases of deep-seated lesions, AR was associated with wider resection margins, higher R0 resection rates, and fewer conversions. Conversely, long-term oncologic outcomes and postoperative complication rates were not consistently affected.
Conclusion: AR appears to be a safe technique with the potential to enhance the precision of liver resections and support intraoperative decision-making. Nevertheless, large prospective trials and further technological advances in registration and tissue deformation correction are required before routine clinical implementation.
Keywords:
liver resection – Hepatectomy – liver – augmented reality
Authors:
I. Tomyak; A. Nikov
; M. Oliverius
; R. Novotný
; Z. Šubrt
Authors‘ workplace:
Chirurgická klinika 3. LF UK a FN Královské Vinohrady, Praha
Published in:
Rozhl. Chir., 2026, roč. 105, č. 2, s. 68-74.
Category:
Review
doi:
https://doi.org/10.48095/ccrvch202668
Overview
Úvod: Jaterní resekce patří k technicky nejnáročnějším výkonům břišní chirurgie a vyžaduje detailní znalost komplexní trojrozměrné anatomie. Rozšířená realita (augmented reality – AR) představuje moderní technologii, která umožňuje překrytí digitálních informací s reálným operačním polem a může sloužit jako nástroj pro perioperační navigaci.
Metody: Byla provedena rešerše s využitím databází PubMed, MEDLINE a Cochrane, byly analyzovány studie publikované v období leden 2022 až srpen 2025. Zařazeny byly pouze články publikované v angličtině, které odpovídaly následujícím klíčovým slovům augmented reality, liver surgery, liver resection, hepatectomy, zaměřené na lidské subjekty s využitím technologie rozšířené reality (augmented reality – AR) během jaterní resekce. Celkem bylo identifikováno 133 studií. Po odstranění duplicit zůstalo 67 článků. Na základě stanovených kritérií bylo do finální analýzy zařazeno 10 studií, které byly shledány relevantními k danému tématu.
Výsledky: Analyzované studie zahrnovaly celkem 649 pacientů, z toho u 245 byla během resekce využita AR. Pět studií bylo retrospektivních s kontrolní skupinou, tři single‑arm a jedna prospektivní. Většina prací prokázala, že AR zlepšuje intraoperační orientaci, usnadňuje lokalizaci lézí a může snížit krevní ztrátu i operační čas. U hluboko uložených ložisek vedlo použití AR k širším resekčním okrajům, vyšší míře R0 resekcí a nižší míře konverzí. Naopak dlouhodobé onkologické výsledky a výskyt pooperačních komplikací nebyly jednoznačně ovlivněny.
Závěr: AR je bezpečná metoda, která má potenciál zvýšit přesnost jaterních resekcí a podpořit intraoperační rozhodování. Pro její rutinní zavedení do klinické praxe jsou však nezbytné rozsáhlejší prospektivní studie a další technologický rozvoj v oblasti registrace a korekce deformace tkání.
Klíčová slova:
resekce jater – játra – hepatektomie – rozšířená realita
Úvod
Jaterní chirurgie patří k nejnáročnějším oblastem břišní chirurgie. Chirurgická anatomie jater je velice komplexní, a to především složitou trojrozměrnou architekturou cévního a žlučového systému uvnitř jaterního parenchymu. Výrazná variabilita těchto struktur dále komplikuje orientaci v jaterní anatomii [1]. Jaterní léze jsou často lokalizovány hluboko v parenchymu, a tudíž nejsou během operace makroskopicky patrné. Proto je znalost a orientace v jaterní anatomii jedním z kruciálních faktorů, který ovlivňuje úspěšnost léčby. Jaterní resekci si dnes nelze představit bez využití zobrazovacích metod – jak v předoperační fázi pro stanovení diagnózy a plánování výkonu, např. výpočetní tomografie (CT) nebo magnetická rezonance (MR), tak i v perioperačním období, kde zlatým standardem zůstává intraoperační ultrasonografie [2–4]. Moderní zobrazovací techniky sice umožňují trojrozměrné zobrazení (např. CT/MR), nicméně klasické zobrazovací metody prezentují tato data převážně ve dvourozměrném (2D) formátu. Pro přesné provedení chirurgického zákroku je však nezbytné, aby chirurg správně porozuměl prostorovému uspořádání léze a jejímu vztahu k cévním a biliárním strukturám. Interpretace 2D obrazů je složitá, vyžaduje značné zkušenosti a čas.
V klinické praxi se stále častěji využívají 3D rekonstrukce předoperačních zobrazovacích metod – ať už ve formě virtuálního modelu, nebo fyzického modelu vytvořeného 3D tiskem [5]. Ani tyto metody však zcela neřeší intraoperační problém orientace, zejména u hluboko uložených tumorů. V tomto ohledu zůstává ultrasonografie nenahraditelnou navigační metodou, která umožňuje bezpečné vedení resekční linie a dosažení radikality typu resekce R0. V posledních letech však nabývá na významu rozšířená realita (augmented reality – AR) jak v předoperačním plánování, tak přímo během jaterních operací. Tato technologie má potenciál zjednodušit plánování resekce a zároveň sloužit jako další nástroj pro intraoperační navigaci.
Klíčové je přitom správné vymezení pojmu AR a její odlišení od virtuální reality (VR). AR je definována jako překrytí digitálních informací na reálný svět prostřednictvím obrazovky nebo jiného zobrazovacího zařízení. V jaterní chirurgii to znamená, že chirurg vidí na zobrazovacím zařízení (např. v AR brýlích nebo na monitoru) reálná játra doplněná o virtuální 3D model orgánu vč. léze, cévních struktur či žlučových cest vytvořený z předoperačního CT/MR, s možností použití různých režimů zobrazení a volby jednotlivých struktur. Aby bylo zobrazení co nejpřesnější, systém nejprve provede registraci, tedy přiřazení 3D modelu ke skutečné anatomii pacienta, a poté vytvoří překrytí (overlay), při němž jsou virtuální struktury umístěny na správná místa v reálném obrazu. VR naproti tomu zcela odděluje uživatele od skutečného světa a umožňuje mu ponoření do plně digitálního, simulovaného prostředí [6]. S rostoucím využíváním technologie AR narůstá i počet souvisejících studií. Je proto nezbytné tyto studie správně posuzovat s ohledem na perspektivu implementace této technologie do klinické praxe. V posledních letech se objevují také studie, ve kterých byla technologie AR aplikována přímo v perioperační fázi. Významným problémem však zůstává značná heterogenita publikovaných studií, jež se často liší jak svým zaměřením, tak metodologií. Některé práce se soustředí především na hodnocení přesnosti zobrazení, jiné zkoumají vliv AR na snížení počtu perioperačních komplikací či popisují různé techniky synchronizace obrazu mezi virtuálním a reálným prostředím. Přestože přístupy a metodické rámce jednotlivých studií nejsou jednotné, jejich společným cílem je zhodnotit přínos využití AR během jaterní resekce.
Metodologie
Byla provedena rešerše s využitím databází PubMed, MEDLINE a Cochrane, přičemž byly analyzovány studie publikované v období od ledna 2022 do srpna 2025. Vzhledem k narůstajícímu počtu studií byly do analýzy zařazeny pouze práce z posledních 3 let, které odpovídaly následujícím klíčovým slovům: augmented reality, liver surgery, liver resection, hepatectomy.
Inclusion criteria: originální studie, AR použita během jaterní resekce, studie s více než pěti pacienty, pouze lidské subjekty, publikace v angličtině.
Exclusion criteria: nepopsáno klinické využití AR, jiné operační výkony než jaterní resekce. Přehledové články či sekundární analýzy dříve publikovaných dat, kazuistiky a studie s méně než pěti pacienty.
Cíle
Cílem této přehledové studie je identifikace a kritická analýza dostupných publikací zabývajících se využitím technik AR při jaterních resekcích perioperačně s cílem definovat současný stav poznání a zhodnotit jeho uplatnění v klinické praxi.
Výsledky
Celkem bylo identifikováno 133 studií. Po odstranění duplicit zůstalo 67 článků. Na základě předem stanovených kritérií bylo do finální analýzy zařazeno 10 studií, které byly shledány relevantními k danému tématu (schéma 1). Z celkového počtu 10 studií bylo pět retrospektivních kohortových s kontrolní skupinou, jedna prospektivní bez kontrolní skupiny a čtyři single‑arm kohortové studie. Celkově bylo analyzováno 649 pacientů, z nichž u 245 byla během resekce použita technologie AR. Přestože je většina studií retrospektivních a metodologicky se liší, některé z nich sdílejí společné cíle. Proto mohly být výsledky rozděleny do několika skupin a jsou uvedeny v tab. 1.
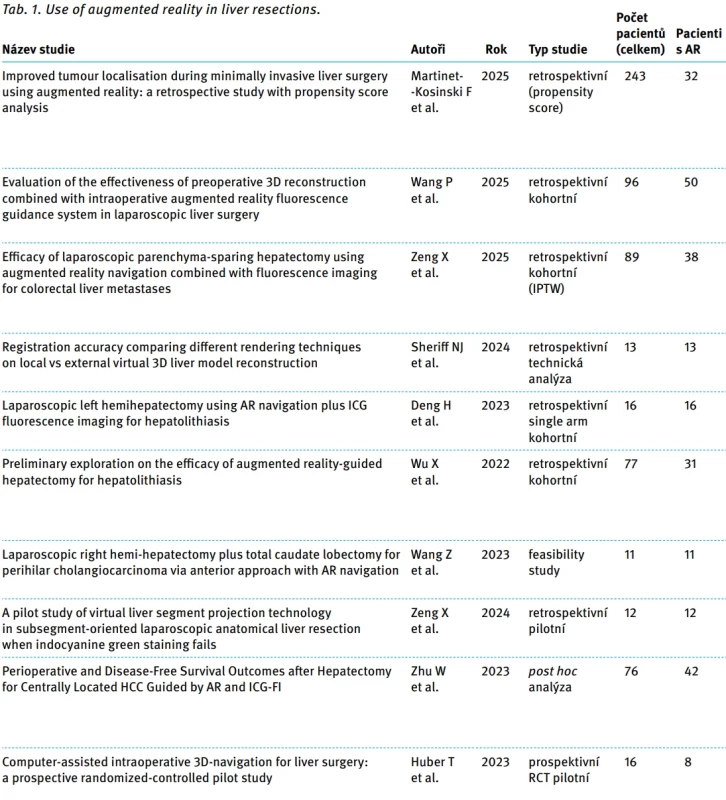
RPV – pravá portální žila, ICG – indocyaninová zeleň, VLSP – virtuální projekce jaterního segmentu,
LLH – laparoskopická levostranná hepatektomie, CCA – cholangiokarcinom, RCT – randomizovaná kontrolovaná klinická studie
Technologická proveditelnost a přesnost
Několik studií se detailně zaměřilo na technické aspekty AR. Single‑arm studie od Wanga et al. a Denga et al. potvrdily technickou proveditelnost AR i u vysoce komplexních výkonů, jako je laparoskopická resekce lobus caudatus nebo levostranná hemihepatektomie. Tyto práce zdůrazňují, že multimodální přístupy, jako je kombinace AR s fluorescenčním zobrazením pomocí indocyaninové zeleně (indocyanine green – ICG) a virtuální projekcí segmentů (virtual liver segment projection – VLSP), dokážou částečně kompenzovat omezenou přesnost samotné AR [7,8]. Sheriff et al. ve své analýze přesnosti registrace ukázali, že spolehlivost AR není ovlivněna metodou tvorby 3D modelu – nebyl nalezen významný rozdíl mezi přesností registrace s lokálními a externími modely (8,76 ± 0,9 mm vs. 7,85 ± 0,9 mm; p = 0,272). (Pro správné pochopení výsledků je třeba uvést, že předoperační 3D model jater může být vytvořen buď lokálně na pracovišti pomocí segmentačního softwaru, nebo externě ve specializovaném centru. Obě varianty vycházejí ze stejných CT/MR dat, liší se však použitými algoritmy a stupněm postprocessingu). Kriticky však závisí na volbě cévního orientačního bodu. Registrace vedené přes levou portální žílu (left portal vein – LPV) měly signifikantně vyšší přesnost než přes pravou portální žílu (right portal vein – RPV) (6,2 ± 0,85 mm vs. 10,41 ± 0,99 mm; p < 0,001). Přesnost do 8 mm byla zaznamenána u více než 70 % měření v rozsahu do 3 cm od RPV. Tato studie ukazuje, že registrace přes LPV vedla k přesnějším překryvům a může být preferovanou volbou pro intraoperační navigaci [9].
Zlepšení perioperačních parametrů a snížení krevní ztráty
Studie Wanga et al. a Zenga et al. prokázaly, že použití AR vede ke zkrácení operačního času a snížení peroperační krevní ztráty [10,11]. Např. Wang et al. zaznamenali u pacientů s AR kratší operační čas při laparoskopické resekci jater (110,8 ± 20,6 min vs. 122,4 ± 20,5 min; p = 0,013) a nižší krevní ztrátu (300,8 ± 32,7 ml vs. 320,8 ± 35,8 ml; p = 0,002), přičemž rozdíly představovaly relativní snížení o cca 9,5 a 6,2 % [10]. Ve studii Zenga et al. byl zaznamenán kratší čas parenchymální transekce (80 vs. 119 min; p < 0,001) [11]. U hluboko uložených lézí navíc AR‑ICG vedla k nižší krevní ztrátě (180 vs. 200 ml; p <0,001) [11]. Podobně Wu et al. u hepatektomií pro hepatikolitiázu uvádí, že skupina, kde byla použita AR, měla nižší peroperační krevní ztrátu (p < 0,001), ale zároveň delší dobu operace (p < 0,001) [12]. Stejně tak Zhu et al. u resekcí centrálně uloženého hepatocelulárního karcinomu potvrdili výrazně nižší krevní ztráty (275 vs. 300 ml; p = 0,013) a sníženou potřebu transfuzí (14,3 vs. 64,7 %; p < 0,01) [13].
Vliv na míru konverze
Martinet‑Kosinski et al. prokázali, že ve skupině s AR nebyla provedena žádná konverze, zatímco ve skupině bez AR dosáhla míra konverze 2,8 % (p = 0,7) [14]. Statisticky zatím technologie AR neovlivňuje míru konverze, ale přitom umožňuje lokalizaci jaterní léze ve všech zaznamenaných případech. Studie Zenga et al. ukazuje, že skupina s AR měla nižší míru konverze (10,2 vs. 31,9 %; p = 0,012), a shodně potvrzuje, že AR umožňuje úspěšnou lokalizaci lézí ve všech případech, což eliminuje konverzi z tohoto důvodu [11].
Dopad na onkologickou radikalitu
Zeng et al. ukázali ve skupině s použitím AR širší resekční okraj u pacientů s kolorektálními jaterními metastázami (8,0 vs. 4,0 mm; p < 0,001) a u hluboko uložených lézí navíc vyšší míru R0 resekcí (81,6 vs. 61,7 %; p = 0,041) [11]. Práce Wanga et al. ukázala, že podíl R0 resekcí u maligních diagnóz (92,3 vs. 89,5 %) se statisticky významně nelišil [10]. Huber et al. neprokázali signifikantní změny v provedení R0 resekcí, kde minimální resekční okraj činil 0,15 vs. 0,40 cm (p = 0,384) [15]. Ve studiích Wanga et al. a Zenga et al. byla ve všech případech dosažena R0 resekce, ale vzhledem k tomu, že se jednalo o retrospektivní single‑arm analýzy bez kontrolní kohorty, nelze posuzovat vliv AR na výsledky [7,16].
Vliv na komplikace
AR se jeví jako nástroj, který může potenciálně vést k bezpečnějšímu provedení výkonu na základě lepší vizualizace. Podívejme se však na data ze studií, zda tomu tak skutečně je. Studie Wanga et al., Martinet‑Kosinskiho et al. a Hubera et al. nezaznamenaly statisticky významný rozdíl ve výskytu pooperačních komplikací mezi skupinami s AR a bez AR [10,14,15]. Zhu et al. pozorovali signifikantně nižší výskyt komplikací ve skupině s AR (35,7 vs. 61,8 %; p = 0,024). Tento nález může souviset s nižší krevní ztrátou, avšak podobnou tendenci nepozorujeme ve studii Wanga et al., kde byla rovněž prokázána nižší krevní ztráta [10,13]. Deng et al. (2024) a Wang et al. (2023) prokázali, že použití AR je technicky bezpečné. Jejich single‑arm design však neumožňuje srovnání s kontrolní skupinou, a proto nelze jednoznačně posoudit snížení komplikací. Nicméně tyto studie potvrzují, že AR nepředstavuje zvýšené riziko [8,7].
Doba hospitalizace
Zhu et al. a Zeng et al. prokázali signifikantní vliv použití AR během operačního výkonu na délku hospitalizace (hospitalizace 8 vs. 9 dní; p = 0,005) a (hospitalizace 6,1 vs. 8,0 dní; p = 0,019) [12,13].
Přežití a celková mortalita
Zeng et al. (p = 0,388) ani Zhu et al. (p = 0,16) nezaznamenali statisticky významný rozdíl v disease free survival. Ani v celkové mortalitě mezi skupinami s AR a bez ní [11,13]. Limitací těchto studií je však krátké sledovací období.
Diskuze
Dostupná data z posledních let ukazují, že využití AR v jaterní chirurgii je bezpečné a ve vybraných případech přináší klinický benefit [10,13]. Většina dostupných studií potvrzuje, že AR zlepšuje intraoperační orientaci chirurga, umožňuje přesnější identifikaci anatomických struktur a patologických ložisek a usnadňuje plánování a vedení resekčních linií [8,10–13]. Tyto faktory jsou obzvláště významné u pacientů s hluboko uloženými nebo špatně přístupnými lézemi, kde může být standardní intraoperační ultrasonografie limitována [8]. V této skupině pacientů byla AR spojena se širšími resekčními okraji, nižší mírou konverzí na laparotomii a vyšším podílem R0 resekcí, což může mít zásadní význam z hlediska onkologické radikality [12].
Pozorovaným benefitem je potenciální redukce peroperačních krevních ztrát a zkrácení délky operace [10,11]. Některé studie uvádějí kratší dobu parenchymální transekce i celkové zkrácení operačního času, což lze vysvětlit přesnější lokalizací cévních struktur a cílenějším vedením resekčních linií [7,10,11,16]. Přesto je nutné zdůraznit, že rozdíly v některých parametrech (např. délka hospitalizace, pooperační morbidita či mortalita) zatím nejsou jednoznačně prokázány a nelze je považovat za konzistentní napříč publikovanými studiemi [10,12,13]. Velkou limitací dostupné literatury je značná heterogenita studií. Jednotlivé práce se liší nejen designem, ale i počtem pacientů, použitými technologiemi AR a sledovanými parametry. Většina publikovaných dat vychází z retrospektivních kohort, často s relativně malými soubory pacientů [8,7,16].
Technickým limitem současných systémů zůstává přesnost registrace, tedy schopnost přesně překrýt předoperační 3D model jater s aktuálním intraoperačním obrazem [9]. Přesnost registrace se může snižovat v průběhu operace vlivem deformace a posunu jaterní tkáně během transekce či manipulace s parenchymem. Tento problém se projevuje zejména u výkonů v zadních a centrálních segmentech, kde je přístup obtížnější. Zeng et al. ukazují, že kombinace AR s fluorescenčním zobrazováním pomocí ICG nebo s VLSP dokáže částečně kompenzovat omezenou přesnost samotné AR a zvýšit spolehlivost intraoperační navigace [11].
Z hlediska klinického využití AR nemusí být vnímána jako náhrada, ale spíše jako doplněk zavedených metod, zejména intraoperační ultrasonografie [16]. V současnosti AR nabízí spíše podpůrnou roli – zvyšuje bezpečnost a přesnost výkonu, zejména v náročných případech. Její plné začlenění do každodenní praxe však bude podmíněno nejen dalším technickým vývojem, ale i validací prostřednictvím kvalitních klinických studií. Souhrnně lze konstatovat, že AR představuje slibnou technologii s vysokým potenciálem v jaterní chirurgii. Přináší především lepší intraoperační orientaci, může zlepšit bezpečnost výkonů a přispět k vyšší míře radikality. Její rutinní implementace však zatím naráží na technologické a metodologické limity a vyžaduje další vědecké ověření [15].
Budoucí vývoj pravděpodobně povede k integraci AR do multimodálních navigačních systémů kombinujících předoperační 3D rekonstrukce, intraoperační ultrasonografii, fluorescenční zobrazování a pokročilé algoritmy pro kompenzaci deformace tkání. Pokročilé algoritmy využívající umělou inteligenci a strojové učení přispějí k automatizaci registrace a k dynamické korekci deformace tkání v reálném čase, což představuje klíčový krok k dosažení rutinní použitelnosti AR v jaterní chirurgii. Tyto komplexní přístupy by mohly v budoucnu zásadně proměnit způsob provádění jaterních resekcí a zvýšit jejich bezpečnost, přesnost i onkologickou efektivitu.
Závěr
AR se jeví jako technologie s výrazným potenciálem pro další rozvoj navigace v jaterní chirurgii. Další pokrok lze očekávat zejména v jejím propojení s vícezdrojovými zobrazovacími metodami, jako jsou detailní 3D rekonstrukce, intraoperační ultrazvuk či fluorescenční zobrazování, a s algoritmy schopnými průběžně korigovat deformaci tkání v průběhu operačního zákroku. Takto integrované systémy mohou v budoucnu zásadně zpřesnit provádění jaterních resekcí a přispět k vyšší bezpečnosti i onkologické radikalitě výkonů. Plné zavedení AR do běžné klinické praxe však bude záviset na dalším technickém vývoji a robustních klinických důkazech.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
Sources
1. Majno P, Mentha G, Toso C et al. Anatomy of the liver: an outline with three levels of complexity – a further step towards tailored territorial liver resections. J Hepatol 2014; 60(3): 654–662. doi: 10.1016/j.jhep.2013.10.026.
2. Parker GA, Lawrence W, Horsley JS et al. Intraoperative ultrasound of the liver affects operative decision making. Ann Surg 1989; 209(5): 569–577. doi: 10.1097/00000658-198905000-00009.
3. Marcal LP. Intraoperative abdominal ultrasound in oncologic imaging. WJR 2013; 5(3): 51–60. doi: 10.4329/wjr.v5.i3.51.
4. Elbanna KY, Kielar AZ. Computed tomography versus magnetic resonance imaging for hepatic lesion characterization/diagnosis. Clin Liver Dis (Hoboken) 2021; 17(3): 159–164. doi: 10.1002/cld.1089.
5. Lang H, Radtke A, Hindennach M et al. Impact of virtual tumor resection and computer-assisted risk analysis on operation planning and intraoperative strategy in major hepatic resection. Arch Surg 2005; 140(7): 629–638. doi: 10.1001/archsurg.140.7.629.
6. Jung C, Wolff G, Wernly B et al. Virtual and augmented reality in cardiovascular care. JACC Cardiovasc Imaging 2022; 15(3): 519–532. doi: 10.1016/j.jcmg.2021.08.017.
7. Wang Z, Tao H, Wang J et al. Laparoscopic right hemi-hepatectomy plus total caudate lobectomy for perihilar cholangiocarcinoma via anterior approach with augmented reality navigation: a feasibility study. Surg Endosc 2023; 37(10): 8156–8164. doi: 10.1007/s00464-023-10397-z.
8. Deng H, Zeng X, Hu H et al. Laparoscopic left hemihepatectomy using augmented reality navigation plus ICG fluorescence imaging for hepatolithiasis: a retrospective single-arm cohort study (with video). Surg Endosc 2024; 38(7): 4048–4056. doi: 10.1007/s00464-024-10922-8.
9. Sheriff NJ, Thomas M, Bunck AC et al. Registration accuracy comparing different rendering techniques on local vs external virtual 3D liver model reconstruction for vascular landmark setting by intraoperative ultrasound in augmented reality navigated liver resection. Langenbecks Arch Surg 2024; 409(1): 268. doi: 10.1007/s00423-024-03456-z.
10. Wang P, Wang S, Luo P. Evaluation of the effectiveness of preoperative 3D reconstruction combined with intraoperative augmented reality fluorescence guidance system in laparoscopic liver surgery: a retrospective cohort study. BMC Surg 2025; 25(1): 288. doi: 10.1186/s12893-025-02989-4.
11. Zeng X, Li X, Lin W et al. Efficacy of laparoscopic parenchyma-sparing hepatectomy using augmented reality navigation combined with fluorescence imaging for colorectal liver metastases: a retrospective cohort study using inverse probability treatment weighting analysis. Int J Surg 2025; 111(2): 1749–1759. doi: 10.1097/JS9.0000000000002193.
12. Wu X, Zeng N, Hu H et al. Preliminary exploration on the efficacy of augmented reality-guided hepatectomy for hepatolithiasis. J Am Coll Surg 2022; 235(4): 677–688. doi: 10.1097/XCS.0000000000000285.
13. Zhu W, Zeng X, Hu H et al. Perioperative and disease-free survival outcomes after hepatectomy for centrally located hepatocellular carcinoma guided by augmented reality and indocyanine green fluorescence imaging: a single - -center experience. J Am Coll Surg 2023; 236(2): 328–337. doi: 10.1097/XCS.0000000000000472.
14. Martinet-Kosinski F, Le Roy B, Lopez YE et al. Improved tumour localisation during minimally invasive liver surgery using augmented reality: a retrospective study with propensity score analysis. Surg Endosc 2025; 39(8): 5027–5034. doi: 10.1007/s00464-025-11672-x.
15. Huber T, Tripke V, Baumgart J et al. Computer-assisted intraoperative 3D-navigation for liver surgery: aprospective randomized-controlled pilot study. Ann Transl Med 2023; 11(10): 346. doi: 10.21037/atm-22-5489.
16. Zeng X, Deng H, Dong Y et al. A pilot study of virtual liver segment projection technology in subsegment-oriented laparoscopic anatomical liver resection when indocyanine green staining fails (with video). Surg Endosc 2024; 38(7): 4057–4066. doi: 10.1007/s00464-024-10912-w.
Labels
Surgery Orthopaedics Trauma surgeryArticle was published in
Perspectives in Surgery

2026 Issue 2
- Safety and Tolerance of Metamizole in Postoperative Analgesia in Children
- Metamizole in perioperative treatment in children under 14 years – results of a questionnaire survey from practice
- Obstacle Called Vasospasm: Which Solution Is Most Effective in Microsurgery and How to Pharmacologically Assist It?
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Current Insights into the Antispasmodic and Analgesic Effects of Metamizole on the Gastrointestinal Tract
-
All articles in this issue
- O čem sní mladí chirurgové
- Prof. MUDr. Jiří Šnajdauf, DrSc. (5. 1. 1949 – 21. 1. 2026)
- Soutěž o nejlepší práce publikované v Rozhledech v chirurgii v roce 2025
- Sekce mladých chirurgů ČCHS ČLS JEP – první rok ve funkci
- Náhlé příhody břišní gynekologického původu
- Sexuální a reprodukční zdraví po chirurgických zákrocích – význam multioborové spolupráce
- Aplikovatelnost rozšířené reality při jaterní resekci v rámci perioperačního použití
- Probiotika a synbiotika v perioperační péči u kolorektální chirurgie – budoucí součást ERAS protokolu?
- Okamžité rekonstrukce prsu implantátem u pacientek podstupujících mastektomii pro karcinom – přehledový článek
- Ruptura serózy žaludku při pankreatické pseudocystě jako příčina hemoperitonea
- Komentář k článku Ruptura serózy žaludku při pankreatické pseudocystě jako příčina hemoperitonea
- Edukace v robotické kolorektální chirurgii
- Perspectives in Surgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Náhlé příhody břišní gynekologického původu
- Sexuální a reprodukční zdraví po chirurgických zákrocích – význam multioborové spolupráce
- Probiotika a synbiotika v perioperační péči u kolorektální chirurgie – budoucí součást ERAS protokolu?
- Okamžité rekonstrukce prsu implantátem u pacientek podstupujících mastektomii pro karcinom – přehledový článek


