Korekce hyperurikemie v jednotlivých stadiích dnavé artritidy. Pohled revmatologa – diskuse pokračuje
Correction of hyperuricemia across stages of gout A rheumatologist‘s perspective – the debate continues
Hyperuricemia (HU) affects up to 15% of the general population; however, the prevalence of gout is estimated at 1–10%, depending on geographic region, socioeconomic status, and ethnic background. According to a comprehensive predictive model based on data from 35 countries collected between 1990 and 2020, the global burden of gout is expected to increase by more than 70% between 2020 and 2050, mainly due to population growth and aging. This article provides an overview of available evidence regarding treatment strategies across the different stages of gout. Particular attention is paid to the controversial issue of whether asymptomatic hyperuricemia should be treated. Published data indicate that approximately 24 patients with asymptomatic HU need to be treated to prevent a single gout flare (number needed to treat, NNT = 24). For this reason, most rheumatology guidelines do not recommend pharmacological treatment of asymptomatic hyperuricemia. A different perspective is emerging from the cardiology literature, where multiple epidemiological studies have suggested that hyperuricemia may represent an independent risk factor for increased cardiovascular risk.
The serum urate (s-UA)/serum creatinine (s-Cr) ratio has been proposed as an index of xanthine oxidase/xanthine dehydrogenase (XO) activity, with values > 3.6 indicating increased enzyme activity; such patients may particularly benefit from urate-lowering therapy. Initiation of urate-lowering treatment during an acute gout flare is generally not recommended and should be postponed until inflammatory symptoms have resolved.
Target serum urate levels are < 360 µmol/L for all patients and < 300 µmol/L for those with tophaceous gout.
As prophylaxis against recurrent gout flares, low-dose colchicine is recommended for approximately three months.
Keywords:
gout – hyperuricemia – xanthine oxidase inhibitors
Authors:
K. Pavelka; B. Stibůrková
Authors‘ workplace:
Revmatologický ústav Praha, Revmatologická klinika 1. LF UK, Praha
Published in:
Čes. Revmatol., 33, 2025, No. 3, p. 107-118.
Category:
Review Article
Overview
Hyperurikemie (HU) se vyskytuje až u 15 % populace, nicméně výskyt dnavé artritidy se odhaduje na 1–10 % v závislosti na regionu, socioekonomickém statusu a etnickém původu. Dle komplexního prediktivního modelu založeného na datech z let 1990–2020 z 35 zemi se očekává, že počet osob trpících dnou vzroste mezi lety 2020 a 2050 o více než 70 %, především v důsledku růstu populace a stárnutí. Předmětem článku je přehled evidence o strategiích léčby v jednotlivých stadiích dny. Obsáhle je diskutován problém, zda léčit asymptomatickou hyperurikemii, či nikoliv – s přihlédnutím k publikovaným datům, která ukazují, že je nutné léčit přibližně 24 pacientů s asymptomatickou HU, aby se zabránilo jednomu dnavému záchvatu (NNT = 24). Z těchto důvodů většina revmatologických doporučení léčbu asymptomatické HU nedoporučuje. Odlišný pohled přichází z kardiologické literatury, kde řada epidemiologických studií ukázala, že hyperurikemie může být samostatným rizikovým faktorem zvýšeného kardiovaskulárního rizika. Byl navržen index s-KM/s-Kr, jehož hodnoty > 3,6 indikují zvýšenou aktivitu xanthinoxidázy/xanthin dehydrogenázy (XO), a právě tito pacienti mohou profitovat z léčby snižující urikemii. V průběhu akutního dnavého záchvatu se obecně nedoporučuje hypourikemickou léčbu zahajovat; vhodné je její nasazení až po odeznění zánětlivých symptomů. Cílové hodnoty urikemie jsou < 360 µmol/l u všech pacientů a < 300 µmol/l u pacientů s tofózní dnou.
Klíčová slova:
DNA – hyperurikemie – inhibitory xanthinoxidázy
ÚVOD
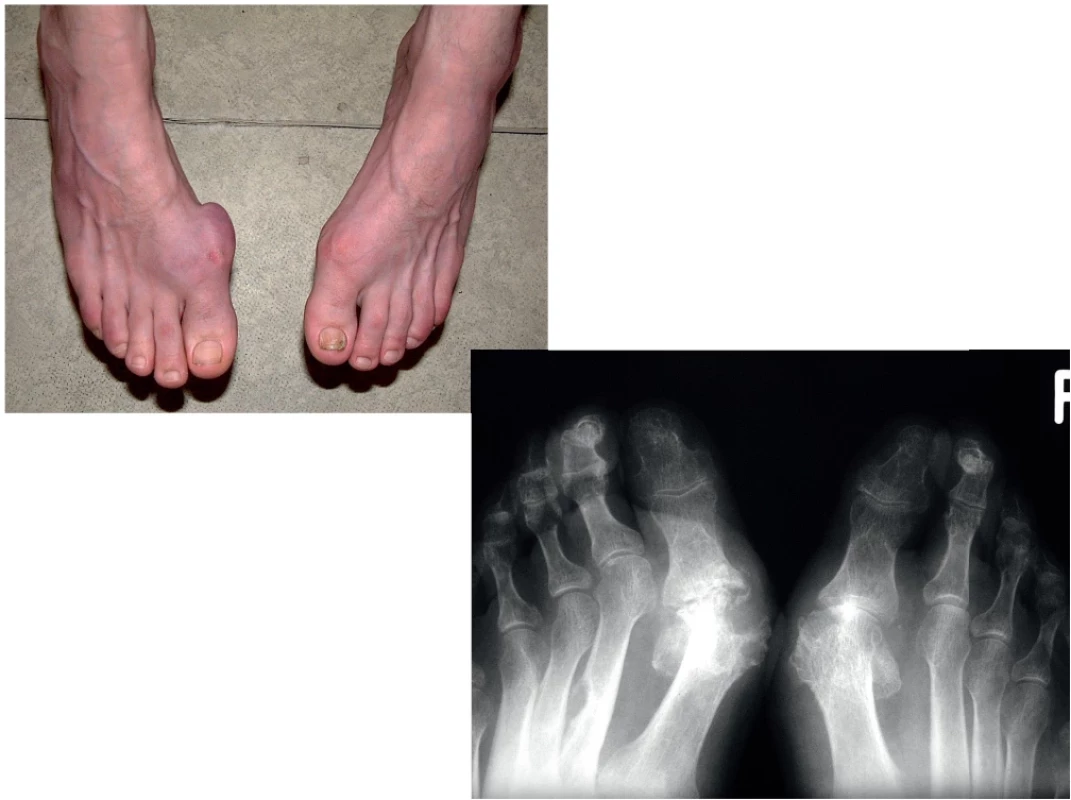
Dna (dnavá artritida) je chronické, zánětlivé onemocnění vyvolané ukládáním krystalů kyseliny močové v kloubech, kolem kloubních tkání a v ledvinách s následnou zánětlivou reakcí (obr. 1). Mechanismus vzniku zánětu po fagocytóze krystalů je komplikovaný, ale řada nových poznatků svědčí o dominantní roli prvků vrozené imunity, jako např. vznik NLRP3 inflamazomu a interleukinu 1 (1). Dna patří v širším kontextu mezi metabolicky podmíněná revmatická onemocnění, protože je známa kauzální metabolická příčina vzniku dny, a to je zvýšena hladina kyseliny močové.
V posledních 20 letech byla publikována řada epidemiologických studií ze zemí vyspělého západního světa, ale i z Číny a Koreje, která ukazují zvyšující se incidenci a prevalenci dnavé artritidy (2). Aktuálně se v USA a jiných západních zemích uvádí výskyt dnavé artritidy 4% (3), a dna se tak stala nejčastější zánětlivou artropatií. Důvodem zvýšené prevalence dnavé artritidy jsou především změny životního stylu. Patří mezi ně jednak faktory dietologické, jednak nedostatek pohybu a sedavý způsob života. Z dietologických faktorů jde o především zvyšující se příjem potravin bohatých na puriny, především červeného masa, ale i metabolizace fruktózy (především slazené nápoje, slazené cereálie a cukrovinky) a příjem alkoholu s následným vznikem obezity. Nálož puriny a inzulinové rezistence jsou také klíčové ovlivnitelné faktory prevence vzniku dny.
Dna je systémové onemocnění a kromě postižení kloubů jsou velmi často přítomná další onemocnění, někdy nazývaná jako asociovaná nebo nověji komorbiditami. Nejdůležitější je metabolický syndrom a jeho jednotlivé složky a postižení ledvin. Prakticky všechny studie potvrzují zvýšené kardiovaskulární riziko u pacientů s dnou, včetně zvýšené mortality (4).
HYPERURIKEMIE
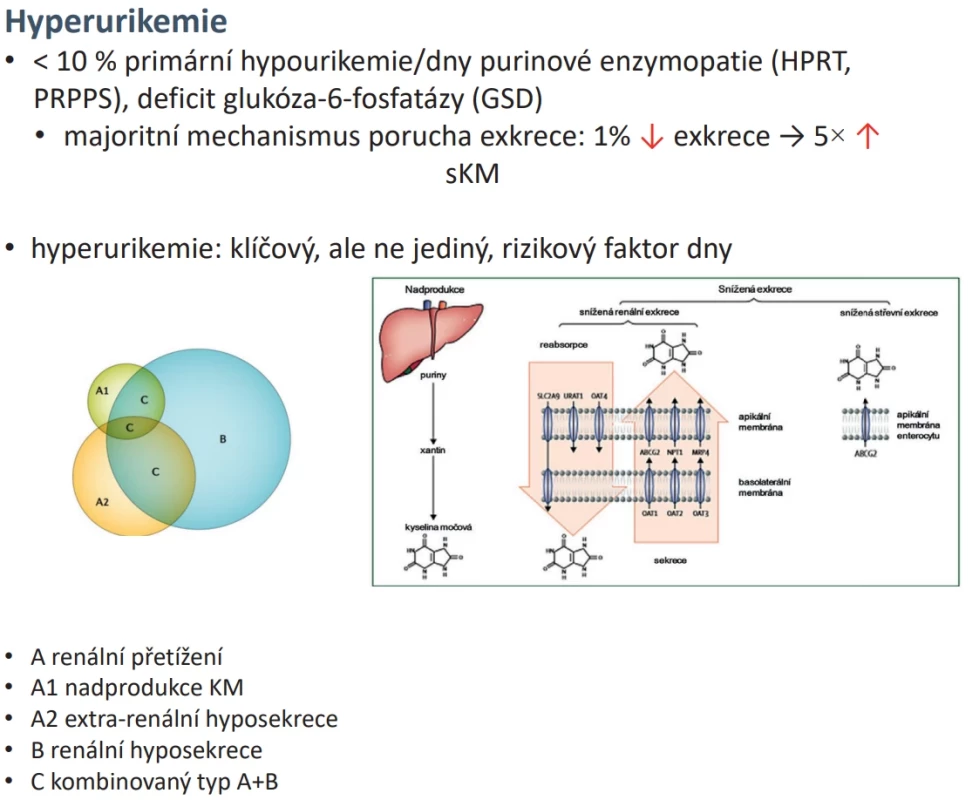
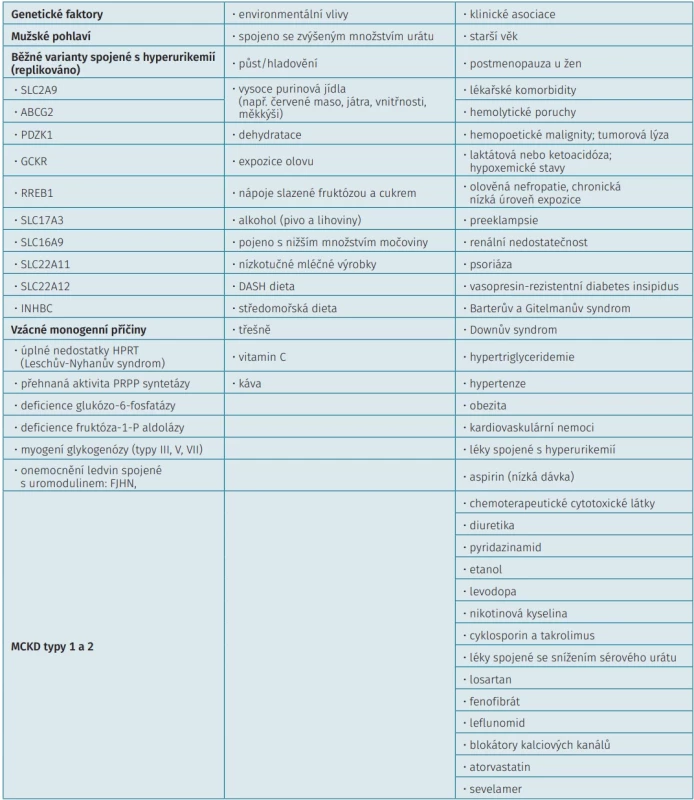
Hladiny urátů v séru jsou udržovány delikátní rovnováhou mezi produkcí urátů a jejich vylučováním. Tato rovnováha může být porušena mnoha faktory, včetně genetických predispozic, vlivů zevního prostředí, přidružených onemocnění či užívaných léků (obr. 2). Za normálních podmínek je udržována dynamická rovnováha mezi endogenní syntézou, exogenním příjmem a recyklací purinů na jedné straně a jejich exkrecí v ledvinách a gastrointestinálním traktu, s dominantním vlivem transportéru ABCG2 na straně druhé (5). Faktory, které mohou ovlivňovat hladiny urátů, jsou uvedeny v tabulce 1.
Je několik hledisek, jak se má praktikující revmatolog dívat na přítomnost HU u pacienta. Ve starších pracích se někdy uvádělo dělení HU na primární a sekundární, které se používá méně, ale je praktické. Sekundární HU či dna mohou být příznakem dalších chorob, a to jak na straně zvýšené novotvorby, kde je zvýšený buněčný obrat (malignity, psoriáza, hematologická onemocnění), tak na straně vylučování (onemocnění ledvin). Tato onemocnění je nutné aktivně vyhledávat, HU může být někdy i prvním klinickým příznakem. Řada příčin sekundární HU může být léčitelná.
Důležitá je analýza léků, které nemocný užívá, z nichž nejčastějšími jsou diuretika a malé dávky kyseliny acetylsalicylové. Z imunosupresiv používaných v revmatologii je možné jmenovat cyklosporin.
U primární HU může být z hlediska výběru optimálního léčebného postupu užitečné určit, zda je primárně u pacienta příčinou vzniku HU nadprodukce KM či porucha vylučování. Dříve doporučované vyšetření tzv. odpadu urátů v moči se v praxi moc neužívá, protože sběr moči za 24 hodin je nepřesný a pro pacienty nekomfortní. Nově navrhuje pracovní skupina kardiologů používat index sérové hladiny kyseliny močové a kreatininu (s-KM/s-Kr) jako indikátor zvýšené aktivity xanthinoxidázy/xanthin dehydrogenázy (XO), a tudíž nadprodukce kyseliny močové (viz dále kardiovaskulární riziko) (6).
KLINICKÁ STADIA DNY A JEJICH LÉČBA
Dna je fenotypicky pestré onemocnění, avšak její průběh je možné rozdělit na čtyři stadia: 1. asymptomatická hyperurikemie, 2. akutní dnavý záchvat, 3. intermitentní dna a 4. chronická tofózní dna.
Cílem léčby je při záchvatu dny ukončit ataku co nejrychleji a bezpečně. Dlouhodobými cíli je pak zabránění vzniku dalších záchvatů a především vzniku destruktivních kloubních změn. Zásadním faktorem, který umožňuje dosáhnout těchto cílů, je dlouhodobé dosažení požadované hladiny kyseliny močové v séru. Normalizace hladiny KM u dnavých pacientů též snižuje KV riziko. Je také nutné monitorovat a léčit tzv. asociovaná onemocnění, především metabolický syndrom a ledvinná onemocnění. Data ukazují, že pouze jedna třetina až polovina pacientů s dnou dostává účinnou, kurativní hypourikemickou léčbu, a méně než polovina pacientů dodržuje předepsaný léčebný režim. Novější údaje naznačují, že počet pacientů s dnou s raným nástupem (< 40 let) roste, přičemž tito pacienti mohou vykazovat odlišné klinické projevy a komorbidity než pacienti s pozdějším nástupem onemocnění (7).
TERAPIE ASYMPTOMATICKÉ HYPERURIKEMIE
Asymptomatická hyperurikemie není nemoc, ačkoliv je conditio sine qua non vzniku dnavé artritidy. HU sama o sobě není schopna vyvolat klinickou dnu. Většina pacientů s HU klinickou dnu nikdy nevyvine. Mechanismy, které jsou zodpovědné za vznik artritických projevů u menšiny pacientů HU, nejsou známy, ale výzkum se soustřeďuje především do genetiky mechanismů vrozené imunitní reakce. Jisté ale je, že existuje asociace výšky HU a vzniku dnavých záchvatů. Například při hodnotách KM více než 600 μmol/l vyvine již 50 % pacientů klinickou dnu. K dnešnímu dni neexistuje univerzálně uznávaná defi nice hyperurikemie. Pro účely související s ukládáním urátových krystalů odpovídá fyzikálně-chemická defi nice hyperurikemie, založená na rozpustnostním limitu urátu v tělních tekutinách koncentracím, hodnotám s-KM přesahujícím přibližně 420 µmol/l (7 mg/dl). Jako praktická a klinicky relevantní defi nice hyperurikemie je některými odborníky navrhována alternativa, kdy s-KM přesahuje 360 µmol/l (6 mg/dl); tato hodnota by zahrnovala odhadovaný práh pro celoživotní riziko klinických následků hyperurikemie spolu s široce doporučovaným cílovým rozmezím < 360 µmol/l pro klinicky úspěšné snižování urátu při dně. To, zda a jak se rozlišuje hyperurikemie mezi muži a ženami (> 420 µmol/l pro muže a > 360 µmol/l pro ženy a děti do 15 let), se rovněž značně liší.
Období asymptomatické HU končí vznikem prvního dnavého záchvatu. Nové zobrazovací metody jako specializovaný ultrazvuk a DECT prokazují, že synoviální mikrotofy a klinicky němé mikrotofy urátů v měkkých tkáních jsou přítomné u většiny pacientů s asymptomatickou HU.
Není jistě bez zajímavosti, že až banálně znějící otázka – zda léčit, či neléčit asymptomatickou HU, stále není jednoznačně odpovězena. Mohou být i rozdílné pohledy specialistů, jako např. revmatologů a kardiologů. A co říkají odborná doporučení? Respektovaná Kolej amerických revmatologů (ACR) asymptomatickou hyperurikemii léčit nedoporučuje. Uvádí randomizovanou studii v trvání 3 let, kdy byli srovnáváni pacienti léčení preparáty snižujícími HU a placebem. Výskyt dnavých záchvatů byl v obou skupinách nízký (≤ 1 % vs. 5 %) (8). Jinými slovy počet pacientů, které je nutné léčit 3 roky hypourikemickou terapií, aby se zabránilo jednomu dnavému záchvatu, byl 24. Panel expertů se domnívá, že benefity podávání hypourikemické léčby nepřevažují její rizika a náklady, protože většina pacientů dnu nikdy nevyvine. Týká se to i pacientů se zvýšeným KV rizikem a dokonce i pacientů s ukládáním krystalů urátů patrným na zobrazovacích metodách. Doporučení Čínské revmatologické společnosti uvádí, že léčba asymptomatické HU by mělo být prováděna pouze u pacientů s HU > 540 μmol/l nebo u pacientů s komorbiditami, jako je zvýšené KV riziko (10). Doporučuje také hypourikemickou léčbu ukončit, pokud je HU při třech následujících kontrolách nižší než 360 μmol/l nebo nižší než 240 μmol/l při dvou následujících kontrolách. EULAR se ve svých doporučeních z roku 2017 terapii asymptomatické HU vůbec nezmiňuje (11) (obr. 3).
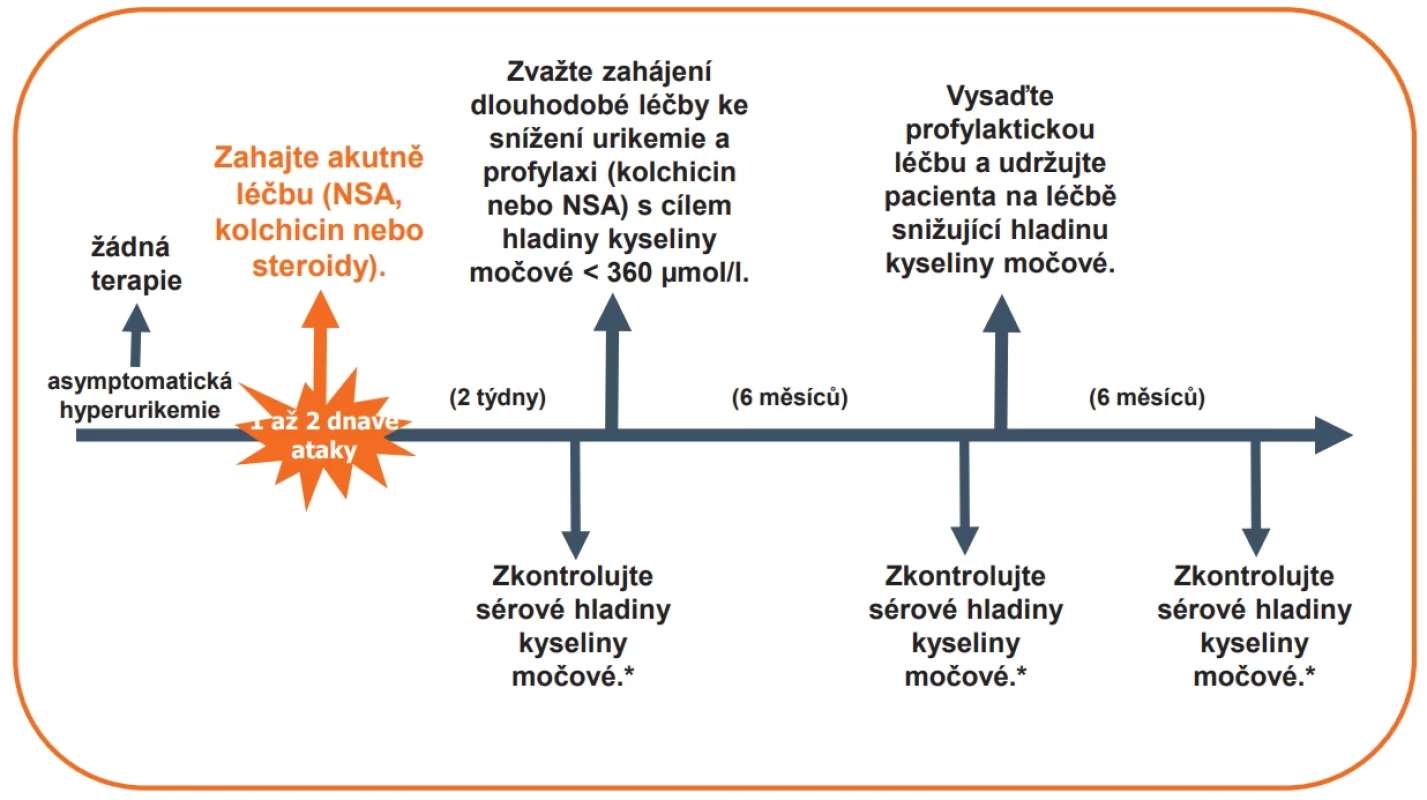
Odlišný pohled na asymptomatickou hyperurikemii mají kardiologové, kteří zdůrazňují možné zvýšené KV riziko (5), jak bude diskutováno v dalším textu (6). Vyšší hladina s-KM je významným rizikovým faktorem pro rozvoj dny. V rámci Normative Aging Study byla roční incidence dny 4,9 % u pacientů s předchozí hladinou s-KM ≥ 540 µmol/l, ve srovnání s 0,1 % u pacientů s předchozí hladinou s-KM < 420 µmol/l. Období asymptomatické hyperurikemie ukončuje vznik akutní artritidy, která bývá pro svou intenzitu označovaná jako akutní dnavý záchvat. Postihuje v 70 % I. metatarzofalangeální (MTP) kloub na noze (podagra), dalšími postiženými klouby bývají kotníky nebo kolenní klouby. Typická je monoartritida, ale u části pacientů se může jednat o oligoartritidu nebo méně často o polyartritidu. Frekvence a délka záchvatů je obtížně predikovatelná, rizikoví jsou pacienti s iniciálně vysokou a obtížně korigovatelnou HU. Diagnóza akutního záchvatu není obtížná v typických formách, může být obtížnější u atypických forem např. u žen nebo ve stáří. Zlatým diagnostickým standardem je průkaz krystalů natrium urátu v polarizačním mikroskopu. Syno - viální výpotek bývá silně zánětlivý. Ze zobrazovacích metod lze doporučit sonografii nebo MR. Klasický rentgen je většinou na začátku nemoci negativní.
Pro léčbu akutního dnavého záchvatu lze použít ne - steroidní antirevmatika (NSA), kolchicin, systémově nebo lokálně podávané glukokortikoidy, nebo u těžkých prolongovaných záchvatů inhibitory IL-1. U zvláště závažných lze užít i kombinaci více modalit. Otázkou zůstává, jaký přístup zvolit k přítomné HU během probíhajícího záchvatu. Historicky se uváděl princip neměnit hladiny kyseliny močové nebo nezačínat podávání hypourikemické léčby během záchvatu. Nicméně dvě randomizované a jedna observační studie prokázaly, že zahájení hypourikemické terapie během záchvatu neprodlužuje ani délku ani závažnost záchvatu (12). Panel expertů proto zahájení hypourikemické léčby během dnavého záchvatu podmíněně doporučuje. V každém případě je ale doporučeno při zahajování hypourikemické léčby podávat 3–6 měsíců jako prevenci dalších záchvatů malé dávky kolchicinu (1 až 2 tablety à 0,5 mg denně) nebo malé dávky NSA. Při zahajování hypourikemické léčby je silně doporučován princip go low, go slow, jinými slovy zahájit nižšími dávkami a titrovat dávky podle potřeby výše. Například u pacientů s chronickým selháním ledvin se doporučuje zahajovat léčbu denní dávkou 50 mg allopurinolu a nižšími. Otázkou zůstává také, jak dlouho po první atace dny hypourikemickou léčbu podávat. Byla diskutována alternativa ukončení hypourikemické léčby po nejméně 12 měsících léčby u pacientů, kteří neměli dnavý záchvat a nemají tofy. Panel se nicméně přiklonil k doporučení hypourikemickou léčbu neukončovat, a to především u pacientů, kteří ji dobře tolerují, kolchicin může u pacientů s dnou zahajujících hypourikemickou terapii snižovat kardiovaskulární riziko jak omezením vaskulárního zánětu, tak i prevencí dnavých záchvatů.
Účinnost canakinumabu při snižování jak kardiovaskulárních příhod, tak dnavých záchvatů poskytuje navíc další důkaz pro koncept, že kontrola zánětu předchází kardiovaskulárním příhodám.
Předepisování profylaxe dnavých záchvatů kolchicinem tedy může vést k lepším celkovým výsledkům u pacientů s dnou tím, že současně předchází záchvatům dny i kardiovaskulárním příhodám.
Dle recentní studie práce Cipoletta (9) byla u pacientů s dnou zahajujících hypourikemickou léčbu profylaxe dnavých záchvatů kolchicinem spojena s nižší mírou kardiovaskulárních příhod během následujících až 180 dnů ve srovnání s pacienty bez profylaxe.
TERAPIE V INTERMITENTNÍ OBDOBÍ A CHRONICKÁ DNAVÁ ARTRITIDA
Většina pacientů v ordinaci lékaře je ve stadiu tzv. intermitentní dny, tzn., že již prodělala jeden nebo více dnavých záchvatů. Frekvence dnavých záchvatů je velmi individuální. Na jedné straně jsou pacienti s vysokou frekvencí i několika záchvatů ročně a na druhé straně pacienti s jedním záchvatem za život. Rizikem větší frekvence záchvatů může
být nedosažení cílové hodnoty hladiny kyseliny močové a přetrvávající HU, dále známky nedobré adherence pacienta k léčbě, slabá ochota k úpravě životního způsobu (dieta, alkohol, absence pohybu, obezita), přítomnost komorbidit a užívání některých léků. Téměř všechna doporučení se přiklonila k používání strategie léčba k cíli (T2T – treat to target) (tab. 2). Princip T2T má dvě komponenty, a to pravidelné monitorování hladiny kyseliny močové a dále adjustace dávek hypourikemické terapie při nedosažení cíle léčby. Cílem léčby je hladina v séru ≤ 360 μmol/l u všech pacientů s dnou, u pacientů s tofy pak ≤ 300 μmol. Kontrolovaná studie prokázala, že při používání principů T2T oproti běžnému postupu byl nižší výskyt nedostatečné adherence k léčbě, nižší hladiny KM, redukce tofů a nižší výskyt pacientů s častými dnavými atakami (dvě a více za rok) (13).

Část pacientů (5–10 %) přechází do stadia chronické dny, a protože mívají velmi často tofy, hovoříme o stadiu tzv. chronické, tofózní dny. Tofy můžeme diagnostikovat klinicky nebo zobrazovacími metodami. Na RTG snímku se tofy představují jakoby průbojníkem vyražená cystoidní projasnění. Typickou lokalizací je I. MTP, ale mohou být i v jiných kloubních lokalizacích. Důležitou novější zobrazovací metodou je sonografie a průkaz tzv. dvojité kontury, DECT, MR nebo low dose CT. Pacienti mohou vyvinout destrukce kloubů. Klinický průběh je variabilní, většinou je přítomna chronická oligo - či polyartritida s kolísavým průběhem. Monitorování těchto pacientů vyžaduje pravidelné hodnocení KM, reaktantů akutní fáze a asociovaných metabolických onemocnění. Sledování strukturální progrese pomocí zobrazovacích metod lze doporučit v ročních intervalech. Cílem terapie HU je dlouhodobé dosažení hladin KM ≤ 300 μmol/l. Přítomnost artritidy může vyžadovat podávání protizánětlivé léčby, jako jsou glukokortikoidy, NSA nebo u refrakterních pacientů se závažnou dnou inhibitorů IL-1. Léčba HU je trvalá, většinou celoživotní.
LÉKY SNIŽUJÍCÍ HLADINU KYSELINY MOČOVÉ
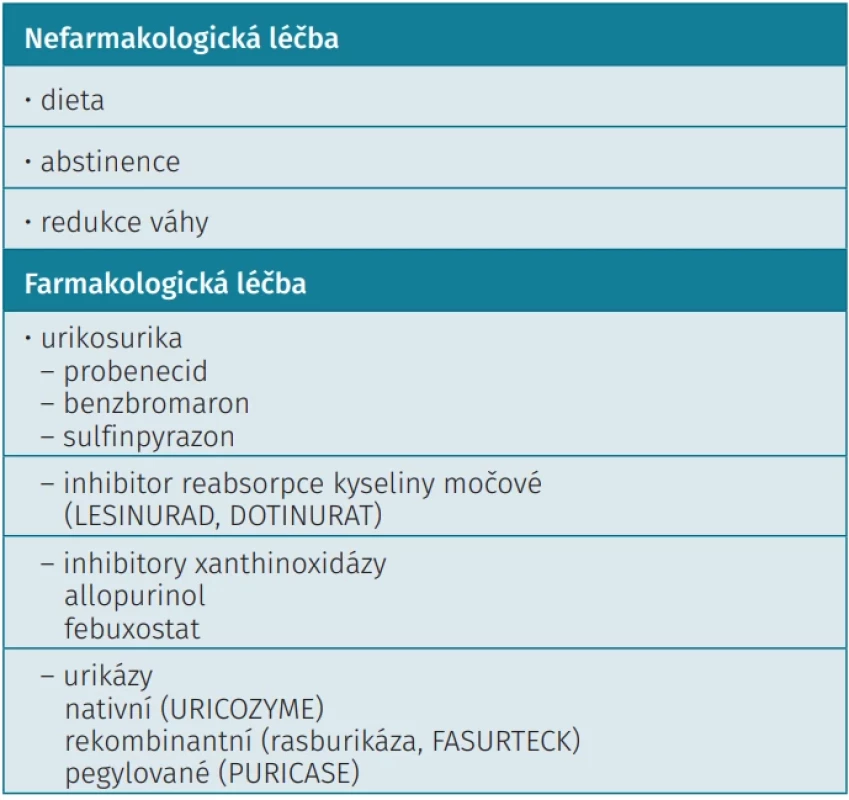
Léky snižující hladinu kyseliny močové lze rozdělit podle mechanismu účinku na léky snižující syntézu kyseliny močové a na léky, které zvyšují exkreci kyseliny močové ledvinami (urikosurika) (tab. 3).
Urikostatika (např. allopurinol, febuxostat, topiroxostat) snižují tvorbu kyseliny močové prostřednictvím kompetitivní inhibice enzymů degradace purinů.
Urikosurika (např. sulfinpyrazon, probenecid, benzbromaron) zvyšují vylučování kyseliny močové močí blokováním renální tubulární reabsorpce urátu.
V současné době je preferována dlouhodobá léčba hyperurikemie zaměřena na modulaci aktivity klíčových enzymů zapojených do metabolismu kyseliny močové, jako jsou xanthinoxidáza, xanthin dehydrogenáza a aldehydoxidáza. Jako lék první linie je doporučován purinový inhibitor allopurinol.
Inhibitory xanthin oxidázy
Allopurinol je purinový inhibitor xanthin oxidázy a xanthin dehydrogenázy, který efektivně snižuje hladinu KM. Používá se v širokém dávkovém rozmezí 100–900 mg denně. U každého pacienta je nutné vytitrovat účinnou dávku, která vede k dosažení stanovené cílové hodnoty pro individuálního pacienta. Není proto správná strategie 300 mg pro každého pacienta. Doporučuje se ale začínat s nižšími dávkami, např. 100 mg denně. Používání ještě nižších dávek (méně než 100 mg denně) u pacientů s rizikem alergických reakcí (tzv. desenzitizační protokol) není rutinně dopo - ručováno (14). Prodloužená renální eliminace aktivního metabolitu oxypurinolu vyžaduje redukci dávky allopurinolu u onemocnění s poškozenou renální funkcí. Allopurinol je také kontraindikován u pacientů léčených azathioprinem a 6 merkaptopurinem. Léčba allopurinolem je ekonomicky efektivní a většinou je dobře tolerována. Nicméně kožní vyrážky se vyskytují asi u 2 % pacientů, další intolerance (hepatotoxicita, gastrointestinální intolerance, CNS projevy) se vyskytují až v 10 %. Allopurinolový hypersenzitivní syndrom je vzácný a vyskytuje se ve frekvenci nižší než 1/1000 pacientů. Nicméně může být závažný s udávanou fatální prognózou až ve 20 %. Rizikovými faktory vzniku tohoto syndromu je přítomnost alely HLA B 5801 (u pacientů asijského původu), současné podávání thiazidů, chronické onemocnění ledvin a vyšší startovní dávka. Kritéria pro stanovení diagnózy allopurinolového hypersenzitivního syndromu jsou uvedena v tabulce 4. Velkými kritérii jsou kožní vyrážka, zhoršení renálních funkcí a poškození jater.

Novější febuxostat (originál uvedený na trh v ČR pod názvem Adenuric) je nepurinový, selektivní inhibitor XO. Je metabolizován na rozdíl od allopurinolu duálně, a proto není nutná adjustace jeho dávky u pacientů s parciální ledvinou insuficiencí (clearance > 30 ml/min). Nemá vliv na jiné enzymy purinového a pyrimidinového metabolismu. Ve studii FACT byl febuxostat 80 mg denně účinnější než allopurinol 300 mg. Febuxostat je indikován a hrazen ve druhé linii hypourikemické léčby při nedostatečné účinnosti nebo intoleranci allopurinolu. Doporučovaná dávka febuxostatu je v USA 40 mg denně, v Evropě pak 80 mg denně. Z klinické praxe je však známo, že u řady pacientů je dávka 40 mg denně nebo 80 mg ob den dostatečná. Febuxostat se většinou dobře snáší, elevace jaterních testů se vyskytují u 3–5 % pacientů. Diskutována je ovšem kardiovaskulární bezpečnost febuxostatu. V randomizované, kontrolované studii CARES byla srovnávána kardiovaskulární bezpečnost allopurinolu a febuxostatu a bylo zjištěno zvýšené riziko celkové úmrtnosti a úmrtnosti z KV příčin po febuxostatu než po allopurinolu (15). Odlišné výsledky byly získány ve studii FAST, která srovnávala dlouhodobou KV bezpečnost febuxostatu a allopurinolu, a mezi oběma léky nebyl zjištěn žádný rozdíl v kardiovaskulární bezpečnosti (16). V největší populační dlouhodobé studii v Koreji bylo hodnoceno celkem 1 260 930 pacientů a při srovnávání skupin na febuxostatu a allopurinolu byli pacienti adjustováni na 60 kovariant. Primárním cílem byl kompozitní index složený z infarktu myokardu, koronární revaskularizace a mozkové příhody (17). Nebyl zjištěn žádný signifikantní rozdíl v primárním ukazateli (febuxostat vs. allopurinol, 2,06 a 2,27 na 100 paciento-roků (95% CI 1,03/0,95–1,12). Celková mortalita byla po febuxostatu o 16 % nižší než po allopurinolu.
Urikosurika
Urikosurika ovlivňují metabolismus aniontu kyseliny močové tím, že inhibují postsekreční renální reabsorpci kyseliny močové a zvyšují renální eliminaci kyseliny močové. V posledních letech byl pozorován určitý odklon od používání urikosurik. Například v doporučeních ACR bylo hlasováno proti používání urikosurik (8). Důvodem bylo zjištění v jedné studii, která ukazovala zvýšený výskyt urolitiázy. Bylo také diskutováno, zda nejprve nestanovit u pacienta vylučování urátů za 24 hodin a urikosurika volit až u pacientů se sníženým vylučováním, nepoužít je jako lék první volby a při léčbě zajistit u těchto pacientů dostatečnou diurézu, eventuálně alkalizaci moči jako prevenci urolitiázy.
Panel ACR však zdůraznil obtíže při 24hodinovém sběru moči a doporučuje použít jako lék první volby u všech dnavých pacientů nezávisle na patofyziologických příčinách HU k léčbě blokátory XO. Připouští však u malého počtu pacientů s nedostatečnou odpovědí na inhibitory XO kombinovanou léčbu s urikosurikem. Kombinace inhibitoru XO s urikosurikem je také jako možnost u refrakterních pa - cientů uvedena v doporučeních EULAR (11). Z urikosurik jsou v klinické praxi k dispozici pouze benzbromaron a probenecid, z novějších urikosurik lesinurad (v ČR však není registrován). Nežádoucí účinky spojené s benzbromaronem jsou relativně vzácné, ale mohou být závažné – benzbromaron je silný inhibitor cytochromu CYP2C9 a zvyšuje riziko hepatotoxicity, zejména u pacientů s genotypem CYP2C9*3/*3. Žádné urikosurikum není t.č. v České republice komerčně dostupné a v případě jeho indikace je nutné požádat o individuální dovoz.
Pegylovaná urikáza
Pegylovaná urikáza katalyzuje oxidaci KM na alantoin, který je více rozpustný. Podává se v dávce 8 mg intravenózně v intervalu 2 týdnů. EULAR doporučuje použití pegylované urikázy u pacientů s chronickou, destruktivní dnou a špatnou kvalitou života, u kterých není možné docílit žádoucího snížení urikemie žádným dostupným lékem v maximální dávce, a to včetně kombinací (11).
Nové léky
Výzkumy ukazují, že inhibitory SGLT2 mohou snižovat riziko vzniku dnavých atak u pacientů s diabetem 2. typu. Například studie publikovaná v JAMA Network Open zjistila, že zahájení léčby inhibitory SGLT2 bylo spojeno s nižším výskytem opakovaných dnavých atak ve srovnání s jinými antidiabetiky, jako jsou DPP-4 inhibitory nebo GLP-1 agonisté (18).
HYPERURIKEMIE JAKO RIZIKOVÝ FAKTOR KARDIOVASKULÁRNÍHO RIZIKA U PACIENTŮ S DNOU A ASYMPTOMATICKOU HYPERURIKEMIÍ
Hyperurikemii jako rizikový kardiovaskulární faktor popsali skvěle ve své konsenzuální práci a doporučení Vrablík a spolupracovníci (5). Zdůraznili také heterogenitu sledovaných populací a také metody sledování. Citovali také často zmiňovanou studii NHANES, která prokázala souvislost HU s řadou chorob, včetně renálních kardiovaskulárních a metabolických (19). Korelace HU a zvýšeného rizika však byla signifikantní pouze u pacientů s HU a klinicky manifestní dnou, nikoliv u asymptomatické HU. Ve studii CARDIA, která zahrnovala 4725 pacientů a sledovala je 20 let, bylo prokázáno, že riziko hypertenze roste s narůstající urikemií (20). Mechanismů, jakými může HU zvyšovat KV riziko, byla popsána celá řada: souvislost s dysfunkcí cévního endotelu (21), remodelací a hypertrofií levé srdeční komory (22) a snížením tvorby NO endotelem (23). Ukázalo se, že zvýšená hladina KM zvyšuje riziko v systému SCORE 2, kde byla nezávislým prediktorem závažných kardiovaskulárních příhod (MACE) v průběhu 6,7 let sledování (24).
V kardiologické literatuře lze nalézt řadu studií, které se věnovaly problematice vlivu hypourikemické léčby na KV riziko. Například metaanalýza randomizovaných studií s inhibitory XO, která hodnotila více než 10 000 pa - cientů, sice prokázala snížení jakýchkoliv KV příhod a závažných KV příhod v porovnání s placebem, nikoliv však MACE (25). V další studii bylo snížení rizika průkazné jen u pacientů s preexistujícím KV rizikem, při analýze všech studií bylo snížení tohoto rizika nevýznamné (26). Recentní rozsáhlá randomizovaná intervenční studie ALL-HEART žádný protektivní benefit allopurinolu u starších pacientů se zvýšeným KV rizikem (bez ohledu na vstupní hodnotu s-KM) neprokázala (27). V retrospektivní studii u pacientů s asymptomatickou hyperurikemií hypourikemická léčba febuxostatem neprokázala žádný kardiovaskulární klinický benefit (28). Evidence o tom, že hypourikemická léčba je přínosem pro všechny pacienty s HU, tedy není dostupná. Vrablík a spol. charakterizují dosavadní sledované kohorty jako heterogenní a neselektované (5). Na základě dostupných studií (29) a určitého konsenzu expertů se doporučuje u každého pacienta s hyperurikemií stanovit index s-KM/s-Kr. Vyšší hodnota může ukazovat na hyper - urikemii z nadprodukce urátů v důsledku zvýšené aktivity xanthinoxidázy, což je teoreticky spojeno s vyšším kardiovaskulárním rizikem. Hyperurikemie z renálních příčin je považována za z hlediska KV rizika za méně rizikovou. Za rizikové hodnoty indexu se považují hodnoty > 3,6. Navrhují tedy léčit pacienty s asymptomatickou hyperurikemií a indexem > 3,6 a kardiovaskulárním rizikem. Nepatří sem například pacienti s HU po používání léků, kteří mají index zpravidla nižší.
Vráblík a spol. reprezentují pohled kardiologů na asymptomatickou HU a opírají se o řadu velmi kvalitních experimentálních i klinických studií (6). Poněkud odlišný je přehled literatury revmatologické. Určité pochybnosti přinesla již často citovaná populační studie NHANES (30). Zde vedla HU jednoznačně k řadě klinických komplikací, včetně kardiologických, ale signifikantní korelace byly průkazné u pacientů s HU a klinicky manifestní dnou a nikoliv u pacientů s asymptomatickou HU. Zatím nebyla provedena studie, která by jednoznačně KV riziko podle přítomnosti či nepřítomnosti klinické manifestaci (dny) stratifikovala. Není pohled na HU poněkud mechanistický?
A jakou roli hraje přítomnost chronického zánětu?
Dna je charakterizována zánětem nízké intenzity se zvýšenou koncentrací prozánětlivých cytokinů a reaktivních kyslíkatých radikálů, formováním extracelulárních pastí, endoteliální dysfunkcí a destičkovou hyperaktivitou, což může významně přispívat k rozvoji aterosklerózy (31). Dnavé záchvaty jsou charakterizovány zánětem, který vzniká aktivací NALP3 inflamazomu. V randomizovaných klinických studiích blokování NALP3 působilo redukci opakovaných kardiovaskulárních příhod (32). Velmi zajímavý pohled na KV riziko u dny přinesly dvě nové studie. V populační studii v Anglii bylo sledováno 62 574 pacientů s dnou a adjustovaných kontrol bez dny v průběhu 23 let (33, 34). Prokázali, že riziko velké KV příhody je přechodně zvýšeno v prvních 30 dnech po dnavém záchvatu. K podobným závěrům dospěli i autoři australské studie, kteří sledovali asociaci mezi přijetím na hospitalizaci pro MACE a dnavým záchvatem. Sledovali výskyt MACE 365 dní před dnavým záchvatem a 365 po dnavém záchvatu. Regresní analýza ukázala zvýšené riziko MACE po záchvatu (RR 1,67, 95% CI 1,38–2,03). Obě citované studie mohou podporovat hypotézu, že KV riziko je zvýšené především u pacientů s klinickou dnou a zvláště v období 30 dnů po akutním záchvatu, kdy je intenzita zánětu mnohem vyšší než u asymptomatické HU.
ZÁVĚR
Cílem práce bylo diskutovat současné názory na léčbu HU v jednotlivých stadiích dny u fenotypově odlišných pa - cientů. Navrhované indikace po léčbu HU jsou uvedené v tabulce 5. Ve starších doporučeních EULAR byli k hypourikemické léčbě indikováni pacienti s dnou, častými záchvaty, tofy a destrukcemi kloubů a renálními komplikacemi. Byl diskutován fakt, zda zahájit hypourikemickou léčbu až po druhém či dalším záchvatu, nebo ji zahájit již po prvním záchvatu. V současné době je výrazná tendence k časnějšímu zahájení hypourikemické terapie, tzn. již po prvním záchvatu u všech pacientů.
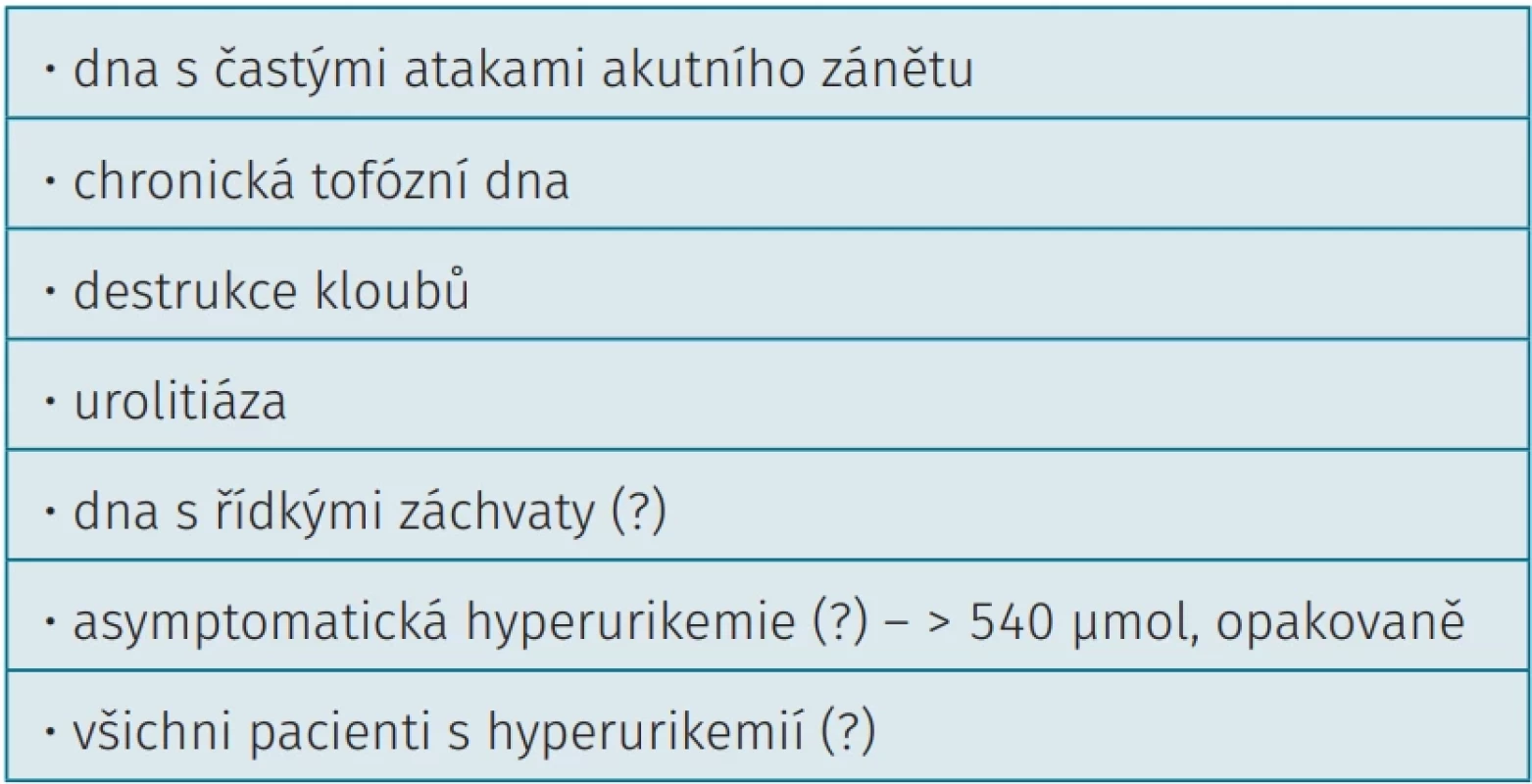
Jedním z důvodů pro časné zahájení hypourikemické terapie je také pravděpodobné snížení KV rizika u pacientů s dnou. Diskutovanou otázkou je také časový faktor nasazení hypourikemické léčby v průběhu dnavého záchvatu. Randomizovaná, kontrolovaná studie neprokázala, že by nasazení hypourikemické léčby prodlužovalo nebo zhoršovalo zánět, takže je s ním možné souhlasit (35). Část konzervativnějších revmatologů, ke kterým se také řadím, však poukazuje na určité limitace výše zmíněné studie a doporučuje se zahájením hypourikemické terapie počkat 2 týdny po odeznění záchvatu, což je uvedeno i v Doporučeních České revmatologické společnosti ČLS JEP pro léčbu dny (36). Cílové hodnoty sérové KM jsou ≤ 360 μmol/l u pacientů s dnou a ≤ 300 μmol/l u pacientů s tofy nebo destrukcemi na RTG snímku.
V čem se ale jednotlivá doporučení shodují, je princip go low, go slow, což v praxi znamená zahájit malou dávkou allopurinolu (100 mg denně) a postupně ji titrovat výše na nejnižší účinnou dávku, při které je dosaženo cílových hodnot, jak je uvedeno výše. Shoda panuje také v uplatňování strategie léčba k cíli, která znamená pravidelné kontroly KM v séru a úpravu léčby. Otázkou zůstává interval kontrol. Lze předpokládat, že postačuje 6 nebo 12 měsíců.
Lze také předpokládat uplatnění telemedicíny.
Při zahajování hypourikemické léčby by měla být také podávána jako profylaxe vzniku nových záchvatů léčba kolchicinem v dávce 0,5 mg denně nebo malé dávky NSA. Lékem první volby je allopurinol, při jeho nedostatečném efektu nebo intoleranci febuxostat, který může být lékem první volby u nemocných částečnou renální insuficiencí. U refrakterních pacientů lze výjimečně uvažovat kombinaci inhibitoru XO a benzbromaronu. Jako ultimativní řešení pro nejvíce refrakterní pacienty může být aplikována pegylovaná urikáza.
Problematice HU jako samostatnému rizikovému kardiovaskulárnímu faktoru u pacientů s dnou je věnována celá řada studií a zde je nutné souhlasit s četnými pracemi kardiologů, že po odfiltrování vlivu dalších rizikových faktorů aterosklerózy je možné najít evidenci o škodlivém vlivu HU. U pacientů s asymptomatickou HU jednoznačný průkaz podán nebyl, a proto se přikláníme k názoru expertů American College of Rheumatology, že asymptomatická HU by neměla být léčena (9). ACR také zmiňuje náklady na léčbu velké množství nutných pacientů k léčbě (NNT) a možné i výrazné nežádoucí účinky allopurinolu, včetně fatálních reakcí (toxická epidermální nekrolýza). Sérová hladina kyseliny močové je uznávána nejen jako biomarker, ale i jako kauzální rizikový faktor pro kardiovaskulární onemocnění, protože podporuje zánět a oxidační stres v endoteliálních a hladkých svalových buňkách cév, což vede k endoteliální dysfunkci a zvyšuje riziko aterosklerózy. Zvýšené hladiny KM spouštějí zánětlivé dráhy, například NF-κB a MAP-kinázy, a jejich klinický význam je potvrzen klinickými studiemi.
Pacienti s hyperurikemií a dnou tvoří etiologicky heterogenní populaci. Někteří mají genetickou predispozici na základě genetických variant kódujících majoritní urátové transportéry (ABCG2, SLC2A9, SLC22A12) se sníženou renální či extrarenální exkrecí, zatímco u pacientů s nadprodukčním typem hyperurikemie je zvýšená aktivita xanthinoxidázy/xanthin dehydrogenázy.
Návrh Vráblíka a spol. (6) na stratifikaci pacientů s asymptomatickou HU podle indexu s-KM/s-Kr a léčbu podávat pouze u pacientů se zvýšenou aktivitou xanthinoxidázy je nutné považovat za velmi zajímavý, ale bude nutné ho ověřit v klinické studii, která bude nesmírně náročná, počtem sledovaných pacientů, délkou sledování a interpretací. Bude také vyžadovat výrazně interdisciplinární přístup za účasti revmatologů, kardiologů a epidemiologů.
Dna byla popsána již ve starobylém Řecku a některé tzv. Hippokratovy aforismy platí dodnes. Na druhé straně přes obrovský pokrok zůstává stále řada otázek otevřená. B.W. Coburn to vystihl v názvu se publikace: The problem with gout is that its still such a problem (37).
Sources
1. Mikuls TR. Gout. N Engl J Med. 2022; 387(20): 1877–1887.
2. Yokose C, McCormick N, Lu N, et al. Trends in prevalence of gout among US Asian adults, 2011–2018. JAMA Netw Open 2023; 6(4): e239501.
3. Kuo CF, Grainge MJ, Zhang W, Doherty M. Global epidemiology of gout: prevalence, incidence and risk factors. Nat Rev Rheumatol. 2015; 11(11): 649–662.
4. Ferguson LD, Molenberghs G, Verbeke G, et al. Gout and inci-dence of 12 cardiovascular diseases: a case-control study including 152 663 individuals with gout and 709 981 matched controls. Lancet Rheumatol. 2024; 6(3): e156–e167.
5. Kvasnička A, Friedecký D, Piskláková B, et al. Ceramide-based risk score: A novel laboratory tool for cardiovascular risk stratification in hyperuricemia and gout. Vascul Pharmacol. 2025; 159 : 107495.
6. Vrablík M, Borghi C, Rosolova8 H, et al. Diagnostika a léčba hyperurikemie v kardiovaskulární prevenci na základě patofyziologického mechanismu jejího vzniku: expertní konsensus českých a slovenských odborníků 2024. AtheroRev. 2024; 9(2): 61–71.
7. Pascart T, Norberciak L, Ea H-K, et al. Patients with earlyonset gout and development of earlier severe joint involvement and metabolic comorbid conditions: Results from a cross-sectional epidemiologic survey. Arthritis Care Res. 2019; 71 : 986–992.
8. FitzGerald JD, Dalbeth N, Mikuls T, et al. 2020 American College of Rheumatology Guideline for the Management of Gout. Arthritis Care Res. (Hoboken) 2020; 72(6): 744–760.
9. Cipolletta E, Tata LJ, Abhishek A. Colchicine and cardiovascular protection in gout: unresolved questions – Authors’ reply. Lancet Rheumatol. 2025; 7(3): e161.
10. Sun M, Lyu Z, Wang C, et al. 2024 Update of Chinese Guidelines for Diagnosis and Treatment of Hyperuricemia and Gout Part I: Recommendations for General Patients. Int J Rheum Dis. 2025; 28(7): e70375.
11. Richette P, Doherty M, Pascual E, et al. 2018 updated European League Against Rheumatism evidence-based recommendations for the diagnosis of gout. Ann Rheum Dis. 2020; 79(1): 31–38.
12. Hill EM, Sky K, Sit M, wt al. Does starting allopurinol prolong acute treated gout? A randomized clinical trial. J Clin Rheumatol. 2015; 21(3): 120–125.
13. Mikuls TR, Cheetham TC, Levy GD, et al. Adherence and outcomes with urate-lowering therapy: A site-randomized trial. Am J Med. 2019; 132(3): 354–361.
14. Becker MA, Schumacher HR Jr, Wortmann RL, et al. Febuxostat compared with allopurinol in patients with hyperuricemia and gout. N Engl J Med. 2005; 353(23): 2450–2461. 15. White WB, Saag KG, Becker MA, et al.; CARES Investigators. Cardiovascular safety of febuxostat or allopurinol in patients with gout. N Engl J Med. 2018; 378(13): 1200–1210.
16. Mackenzie IS, Ford I, Nuki G, et al.; FAST Study Group. Long-term cardiovascular safety of febuxostat compared with allopurinol in patients with gout (FAST): a multicentre, prospective, randomised, open-label, non-inferiority trial. Lancet 2020; 396(10264): 1745–1757.
17. Shin A, Choi SR, Han M, et al. Cardiovascular safety asso-ciated with febuxostat versus allopurinol among patients with gout: Update with accumulated use of febuxostat. Semin Arthritis Rheum. 2022; 56 : 152080.
18. Yang S, Hu Q, Liu K, et al. Serum uric acid reduction through SGLT2 inhibitors: evidence from a systematic review and meta-analysis. Front Pharmacol. 2025; 16 : 1551390.
19. Zhu Y, Pandya BJ, Choi HK. Comorbidities of gout and hyperuricemia in the US general population: NHANES 2007–2008. Am J Med. 2012; 125(7): 679–687.
20. Gaffo AL, Jacobs DR Jr, Sijtsma F, et al. Serum urate association with hypertension in young adults: analysis from the Coronary Artery Risk Development in Young Adults cohort. Ann Rheum Dis. 2013; 72(8): 1321–1327.
21. Zoccali C, Maio R, Mallamaci F, et al. Uric acid and endothelial dysfunction in essential hypertension. J Am Soc Nephrol. 2006; 17(5): 1466–1471.
22. Kuo CF, Yu KH, Luo SF, et al. Role of uric acid in the link between arterial stiffness and cardiac hypertrophy: a cross-sectional study. Rheumatology (Oxford) 2010; 49(6): 1189–1896.
23. Kang DH, Park SK, Lee IK, et al. Uric acid-induced C-reactive protein expression: implication on cell proliferation and nitric oxide production of human vascular cells. J Am Soc Nephrol. 2005; 16(12): 3553–3562.
24. Moshkovits Y, Tiosano S, Kaplan A, et al. Serum uric acid sig-nificantly improves the accuracy of cardiovascular risk score models. Eur J Prev Cardiol. 2023; 30(7): 524–532.
25. Bredemeier M, Lopes LM, Eisenreich MA, et al. Xanthine oxida-se inhibitors for prevention of cardiovascular events: a systematic review and meta-analysis of randomized controlled trials. BMC Cardiovasc Disord. 2018; 18(1): 24.
26. Gill D, Cameron AC, Burgess S, et al. Urate, blood pressure, and cardiovascular disease: Evidence from mendelian randomization and meta-analysis of clinical trials. Hypertension 2021; 77(2): 383–392.
27. Mackenzie IS, Hawkey CJ, Ford I, et al.; ALL-HEART Study Group. Allopurinol versus usual care in UK patients with ischaemic heart disease (ALL-HEART): a multicentre, prospective, randomised, open-label, blinded-endpoint trial. Lancet 2022; 400(10359): 1195–1205.
28. Long X, Wang Z, Yuan W. Effects of febuxostat on heart failure patients with asymptomatic hyperuricaemia: a retrospective cohort study. BMJ Open 2025; 15(7): e099442.
29. Kotozaki Y, Satoh M, Tanno K, et al. Plasma xanthine oxidore-ductase activity is associated with a high risk of cardiovascular disease in a general Japanese population. Int J Environ Res Public Health 2021; 18(4): 1894.
30. Zhu Y, Pandya BJ, Choi HK. Comorbidities of gout and hyperuricemia in the US general population: NHANES 2007-2008. Am J Med. 2012; 125(7): 679–87.e1.
31. Hansildaar R, Vedder D, Baniaamam M, et al. Cardiovascular risk in inflammatory arthritis: rheumatoid arthritis and gout. Lancet Rheumatol. 2021; 3(1): e58–e70.
32. Ridker PM, Everett BM, Thuren T, et al.; CANTOS Trial Group. Antiinflammatory therapy with canakinumab for atherosclerotic disease. N Engl J Med. 2017; 377(12): 1119–1131.
33. Cipolletta E, Tata LJ, Nakafero G, et al. Association between gout flare and subsequent cardiovascular events among patients with gout. JAMA 2022; 328(5): 440–450.
34. Lopez D, Dwivedi G, Nossent J, et al. Risk of major adverse cardiovascular event following incident hospitalization for acute gout: A western Australian population-level linked data study. ACR Open Rheumatol. 2023; 5(6): 298–304.
35. Hill EM, Sky K, Sit M, et al. Does starting allopurinol prolong acute treated gout? A randomized clinical trial. J Clin Rheumatol. 2015; 21(3): 120–125.
36. Pavelka K. Doporučení České revmatologické společnosti pro léčbu dny. Čes. Revmatol. 2019; 27(4): 166–176.
37. Coburn BW, Mikuls TR. The problem with gout is that it’s still such a problem. J Rheumatol. 2016; 43(8): 1453–1455.
Labels
Dermatology & STDs Paediatric rheumatology RheumatologyArticle was published in
Czech Rheumatology

2025 Issue 3
-
All articles in this issue
- MUDr. Olga Kryštůfková, Ph.D
- Correction of hyperuricemia across stages of gout A rheumatologist‘s perspective – the debate continues
- Rheumatology care in the Czech Republic: A cross-sectional analysis of care providers in 2024
- EULAR points to consider on the initiation of targeted therapies in patients with inflammatory arthritis and a history of cancer
- EULAR recommendations for use of antirheumatic drugs in reproduction, pregnancy, and lactation: 2024 update
- Czech Rheumatology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Correction of hyperuricemia across stages of gout A rheumatologist‘s perspective – the debate continues
- Rheumatology care in the Czech Republic: A cross-sectional analysis of care providers in 2024
- MUDr. Olga Kryštůfková, Ph.D
- EULAR points to consider on the initiation of targeted therapies in patients with inflammatory arthritis and a history of cancer