Pramipexol v léčbě farmakorezistentní deprese
Treatment-resistant depression (TRD) presents a complex therapeutic challenge. A significant proportion of patients with depressive symptomatology fail to achieve remission with standard treatment. TRD is most commonly defined as an insufficient clinical response to at least two antidepressant regimens, each administered in adequate dosages and sufficient duration. Although electroconvulsive therapy (ECT) is considered the gold standard in the treatment of TRD, it does not always lead to a satisfactory therapeutic outcome. Therefore, exploring alternative treatment options is essential. One promising direction involves the use of pharmacological agents originally developed for other indications – ketamine being a notable example, with its antidepressant effects repeatedly confirmed in clinical studies. Another potential strategy includes drugs that modulate dopaminergic neurotransmission. Dopamine plays a crucial role in the regulation of motivation, emotion, reward, and cognitive functions. However, most conventional antidepressants do not directly affect dopaminergic transmission, which may contribute to persistent residual symptoms such as impaired motivation, concentration, and the ability to experience pleasure and joy. Pramipexole, a dopamine agonist indicated for the treatment of Parkinson’s disease and restless legs syndrome, has been investigated for its potential effects on depressive symptoms – particularly in light of dopamine’s involvement in the pathogenesis of certain depressive symptoms. Several studies have already demonstrated its efficacy and safety in the treatment of both unipolar and bipolar forms of treatment--resistant depression. This article summarizes findings from selected studies evaluating the use of pramipexole in the treatment of a depressive episode and compares them with clinical experience from off-label pramipexole administration in patients hospitalized at the Department of Psychiatry, University Hospital and the Faculty of Medicine. Current research, along with our clinical observations, suggests that pramipexole is an effective and well-tolerated option in the therapy of treatment-resistant depression, with a low incidence of adverse effects.
Keywords:
dopamine agonists – bipolar depression –treatment-resistant depression – pramipexole – unipolar depression
Authors:
Zuzana Timková; Jana Hořínková; Eliška Bartečková
Authors‘ workplace:
Psychiatrická klinika LF MU a FN Brno
Published in:
Čes. a slov. Psychiat., 122, 2026, No. 2, pp. 59-66.
Category:
Review
doi:
https://doi.org/10.48095/cccsp202604
Overview
Farmakorezistentní deprese a její léčba představují komplikovanou terapeutickou výzvu. Významná část pacientů s depresivní symptomatologií není schopna při standardní léčbě dosáhnout remise. Farmakorezistence je nejčastěji definována jako nedostatečná klinická odpověď na dvě léčebné kúry, které trvaly dostatečně dlouho a byly podávány v dostatečných dávkách. Zlatým standardem léčby farmakorezistentní deprese je elektrokonvulzivní terapie, ale ani ta někdy nevede k uspokojivé terapeutické odpovědi. Hledání dalších možností léčby se proto jeví jako nezbytné. Zajímavou alternativou je využití léčiv původně určených pro jiné indikace – jak se stalo např. v případě ketaminu, jehož účinek již byl opakovaně prokázán v klinických studiích. Další terapeutickou možnost tak představují léčiva, která ovlivňují dopaminergní neurotransmisi. Dopamin hraje klíčovou roli v regulaci motivace, emocí, odměny a kognitivních funkcí, nicméně většina konvenčních antidepresiv neurotransmisi dopaminu přímo neovlivňuje, což může přispět k reziduálním příznakům, jako je porucha motivace, koncentrace a schopnosti prožívat radost a potěšení. Pramipexol, dopaminový agonista indikovaný k léčbě Parkinsonovy nemoci a syndromu neklidných nohou, je zkoumán i pro svůj možný efekt na depresivní symptomatologii – zejména s ohledem na roli dopaminu v patogenezi některých příznaků deprese. Řada studií již doložila jeho účinnost a bezpečnost v léčbě farmakorezistentní bipolární i unipolární deprese. Tento článek shrnuje výsledky vybraných studií hodnotících využití pramipexolu v léčbě depresivního syndromu a porovnává je s klinickými zkušenostmi s off--label podáváním pramipexolu u pacientů hospitalizovaných na Psychiatrické klinice Fakultní nemocnice Brno a Lékařské fakulty Masarykovy univerzity. Dosavadní výzkum i naše klinické zkušenosti naznačují, že pramipexol je účinným a bezpečným lékem v léčbě farmakorezistentní deprese. Zároveň se jedná o léčivo dobře snášené, s nízkou frekvencí výskytu nežádoucích účinků.
Klíčová slova:
agonisté dopaminu – bipolární deprese – farmakorezistentní deprese – pramipexol – unipolární deprese
Úvod
Významná část pacientů s depresivní symptomatologií není schopna při standardní léčbě dosáhnout remise. To se týká jak pacientů s depresivní poruchou, tak pacientů s bipolární afektivní poruchou. Navíc se s rostoucím počtem léčebných režimů pravděpodobnost, že pacient dosáhne remise, snižuje [1]. U pacientů s depresivním syndromem nereagujícím v dostatečné míře na léčbu farmaky hovoříme o farmakorezistentní depresi (treatment-resistant depression – TRD). Různí autoři definují farmakorezistenci různými způsoby. V naší literatuře je nejvíce rozšířená následující definice: nedostatečná klinická odpověď na dvě léčebné kúry, které trvaly dostatečně dlouho a byly podávány v dostatečných dávkách. Za dostatečnou délku terapeutického pokusu lze z konzervativního pohledu považovat 4 týdny obvyklých účinných dávek a další 1–2 týdny maximálních ještě tolerovaných dávek [2]. Ve všech případech je nutné vyloučit pseudofarmakorezistenci, která může být způsobena nonadherencí pacienta k medikaci nebo dávkou léčiva, která pro daného pacienta není dostatečná (např. v důsledku rychlé metabolizace léčiva). Za tímto účelem lze využít tzv. terapeutické monitorování léčiv (therapeutic drug monitoring – TDM), tedy měření plazmatické koncentrace léčiva, popřípadě jeho aktivních metabolitů [2].
Zlatým standardem v léčbě farmakorezistentní deprese je elektrokonvulzivní terapie (ECT). ECT je nejstarší stále využívaná neurostimulační metoda s rychlým nástupem účinku a vysokou mírou účinnosti v akutní i udržovací léčbě farmakorezistentní deprese [3]. Nicméně existují pacienti, u kterých ani ECT nevede ke zmírnění příznaků nebo tato terapie musí být ukončena pro rozvoj nežádoucích účinků.
Zajímavou alternativou je využití léčiv původně určených pro jiné indikace – jak se stalo např. v případě ketaminu, antagonisty NMDA (N-metyl-D-aspartát) glutamátergních receptorů, jehož antidepresivní efekt byl opakovaně prokázán [2].
Další možností mohou být léčiva modulující dopaminergní transmisi, která má význam v rozvoji některých příznaků depresivního syndromu, např. anhedonie, abulie nebo snížené schopnosti koncentrace [4].
Dopamin a deprese
Dopamin hraje, společně se serotoninem a noradrenalinem, důležitou roli v patofyziologii deprese. Nicméně, většina konvenčních antidepresiv neurotransmisi dopaminu přímo neovlivňuje, což může přispět k reziduálním příznakům, jako je porucha motivace, koncentrace a schopnosti prožívat radost a potěšení (anhedonie) [5].
Roli dopaminu v patofyziologii a léčbě depresivních příznaků podporuje několik pozorování.
V randomizované, dvojitě zaslepené, placebem kontrolované studii byla zjištěna vysoká korelace mezi závažností deprese a pozitivní odpovědí na orální podání d-amfetaminu, látky, která zvyšuje koncentraci synaptického dopaminu [6]. Pacienti s těžkou depresí, kteří současně neužívali žádnou další medikaci, vykazovali po podání d-amfetaminu výraznější pocit odměny a potěšení. Nicméně podobný účinek u pacientů s mírnějšími formami deprese nebyl patrný. Jedno z vysvětlení pro tato zjištění je, že u těžké deprese dochází k deficitu v uvolňování dopaminu, což má za následek rozvoj kompenzačních mechanizmů jako upregulace postsynaptických dopaminových receptorů a snížení hustoty dopaminového transportéru (DAT). Tyto změny mohou být normalizovány po zvýšení koncentrace dopaminu např. právě d-amfetaminem [6].
Zvýšená odpověď po podání amfetaminu u pacientů s těžkou depresí byla zjištěna i ve studii s využitím funkční magnetické rezonance (fMRI), a to ve formě změny signálu v oblasti ventrolaterálního prefrontálního kortexu, orbitofrontálního kortexu, ncl. caudatus a putamen [7].
Někteří pacienti s farmakorezistentní depresí vykazují určitý typ hypodopaminergní deprese charakterizovaný převahou příznaků spojených s nedostatkem dopaminu, tj. zpomalené psychomotorické tempo, snížená schopnost koncentrace (hypoprosexie), nedostatečná motivace (abulie), neschopnost prožívat radost a potěšení (anhedonie). Z toho vyplývá, že tito pacienti by mohli profitovat více z terapie dopaminergními agonisty, inhibitory monoaminooxidázy nebo inhibitory zpětného vychytávání dopaminu než z terapie selektivními inhibitory zpětného vychytávání serotoninu (SSRI) nebo inhibitory zpětného vychytávání serotoninu a noradrenalinu (SNRI) [8].
Pramipexol
Pramipexol je dopaminergní léčivo původně určené pro léčbu Parkinsonovy nemoci. Byl vyvinut firmou Pharmacia & Upjohn v roce 1997 pod firemním názvem Mirapex [9]. V současnosti je v České republice dostupný pod několika názvy. Je indikován k léčbě Parkinsonovy nemoci, a to jak v monoterapii, tak v kombinaci s levodopou, a k symptomatické léčbě středně těžkého až těžkého idiopatického syndromu neklidných nohou [10]. Nicméně vzhledem k farmakodynamickému profilu bylo zkoumáno také jeho využití v léčbě jiných poruch, mimo jiné také unipolární a bipolární deprese.
Farmakodynamika
Pramipexol je dopaminergní agonista s minimální aktivitou na jiných receptorech. Nejvyšší afinitu vykazuje k D3 receptorům, následuje afinita k D2 pre - i postsynaptickým receptorům a D4 receptorům. Dále bývá uváděna nízká afinita k serotoninovým 5-HT1A, 5-HT1B, 5-HT1D a adrenergním a2 receptorům. K ostatním receptorům je afinita zanedbatelná [11–13]. Afinita pramipexolu k receptorům je shrnuta v tab. 1.
![Afinita pramipexolu k receptorům. Afinita je hodnocena jako Inhibiční konstanta (Ki) v nanomolech na litr (nmol/l) [11–13].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/3e5892fac9eeb8def94825376d484f8b.png)
Farmakokinetika
Pramipexol se po orálním podání dobře absorbuje a vykazuje biologickou dostupnost více než 90 % [14]. Maximální plazmatickou koncentraci dosahuje 6 h od podání v případě tablet s prodlouženým uvolňováním. Má vysoký distribuční objem (500 l) a nízkou vazbu na bílkoviny (< 15 %). Z 90 % je vylučován ledvinami v nezměněné podobě. Eliminační poločas je 8–12 h v závislosti na funkci ledvin [15].
Nežádoucí účinky
Nežádoucí účinky pramipexolu jsou obdobné jako u jiných dopaminergních agonistů a většina z nich se vyskytuje v počátku léčby a při pokračovací léčbě vymizí. Mezi nejčastější patří nauzea, zácpa, závratě, nespavost, halucinace, dyskineze a bolest hlavy. Výskyt somnolence je pravděpodobnější při dávkách vyšších než 1,5 mg soli pramipexolu denně. Při kombinaci pramipexolu se sedativními léčivy je nutná opatrnost. Na počátku léčby se může vyskytnout hypotenze, zvláště pokud je pramipexol titrován příliš rychle. Dávky vyšší než 4,5 mg/den byly asociovány s rozvojem psychotických příznaků, zejména zrakových halucinací. Četnost těchto příznaků je závislá na dávce. Poruchy kontroly impulzivity se většinou objevují v prvních dvou letech léčby a mohou se projevovat ve formě patologického hráčství, hypersexuality, záchvatovitého přejídání, nutkavého utrácení a nakupování [15].
Pramipexol v léčbě depresivního syndromu
Skutečnost, že pramipexol může vykazovat antidepresivní aktivitu, vychází z jeho farmakodynamiky. Tuto hypotézu dále podporuje např. zjištění, že subakutní administrace pramipexolu v délce 12–15 dní v dávce 1 mg denně vyvolávala u zdravých dobrovolníků podobnou neuronální odpověď jako konvenční monoaminergní antidepresiva [16].
Dostupná literatura nabízí poměrně rozsáhlý soubor údajů týkajících se účinnosti a snášenlivosti pramipexolu.
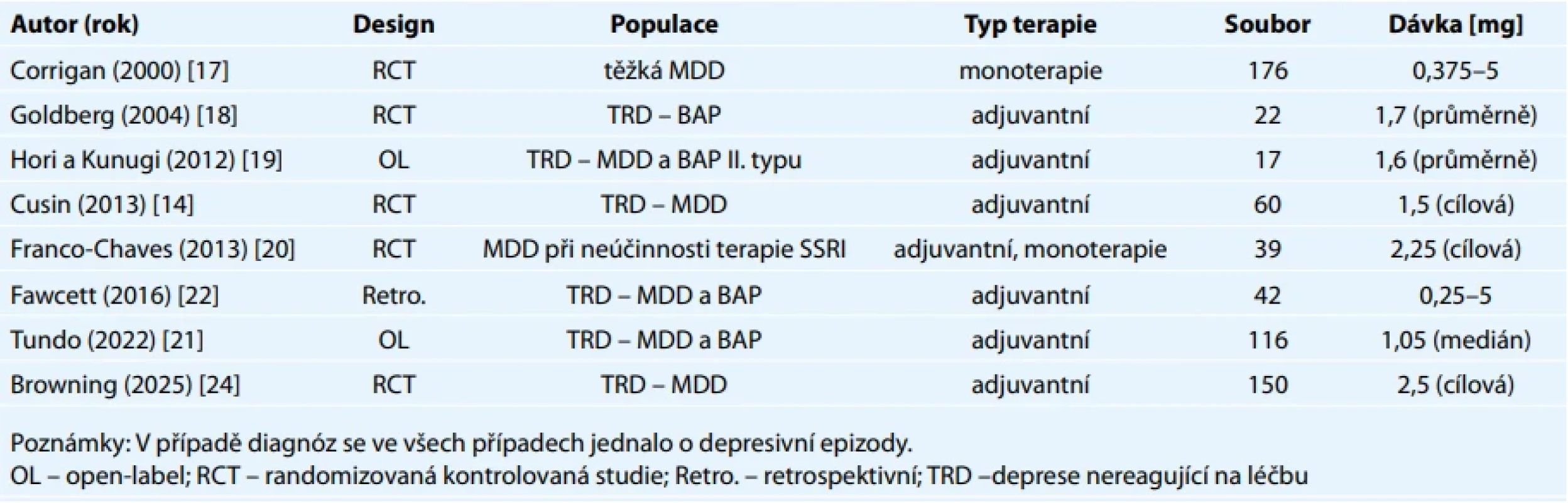
Jedna z prvních studií je z roku 2000 a zkoumala účinnost pramipexolu ve srovnání s fluoxetinem a placebem v randomizované, dvojitě zaslepené studii (randomized clinical trial – RCT) [17]. Do studie bylo zařazeno 176 pacientů s těžkou depresivní poruchou (major depressive disorder [MDD] podle DSM-IV), rozdělených do pěti skupin – pramipexol 0,375 mg, 1 mg a 5 mg, fluoxetin 20 mg a placebo. Studie samotná trvala 8 týdnů a za dalších 9 týdnů následoval follow-up. Klinické hodnocení probíhalo škálou MADRS (Montgomery-Asberg Depression Scale), HAM-D (Hamilton Depression Rating Scale) a CGI-S (Clinical Global Impression Severity Scale). Nejvýraznější zlepšení bylo pozorováno ve skupině, která dostávala pramipexol 5 mg/den (titrace v průběhu 14 dní), avšak tato skupina měla i nejvyšší výskyt nežádoucích účinků, zejména nevolnosti, zvracení, a nejvyšší drop-out. Hned po ní následovala skupina pacientů s pramipexolem v dávce 1 mg/den.
Goldberg et al. se v roce 2004 zaměřili na účinnost pramipexolu jako adjuvantní terapie depresivní fáze bipolární afektivní poruchy při současné léčbě stabilizátory nálady [18]. Do této menší dvojitě zaslepené RCT bylo zařazeno 22 pacientů s farmakorezistentní bipolární depresí. Studie trvala 6 týdnů, průměrná dávka pramipexolu byla 1,7 mg/den. Za odpověď na léčbu byl považován pokles HAM-D o polovinu. Celkem 60 % pacientů vykazovalo responzi při adjuvantní léčbě pramipexolem ve srovnání s 20 % pacientů léčených placebem, u pacientů léčených pramipexolem bylo pozorováno výraznější zlepšení v škále HAM-D i CGI-S oproti placebu. Studii dokončilo 83 % pacientů ze skupiny léčené pramipexolem oproti 50 % pacientů ze skupiny léčené placebem. U jednoho pacienta došlo k rozvoji hypománie.
V open-label studii autorů Hori a Kunugi z roku 2012 byla zkoumaná účinnost pramipexolu jako přídatné medikace u pacientů s farmakorezistentní depresí [19]. Do studie bylo zařazeno 17 pacientů, z toho 12 mělo diagnózu těžké depresivní poruchy (MDD podle DSM-IV) a 5 pacientů diagnózu bipolární afektivní poruchy II. typu. Jednalo se o ambulantní farmakorezistentní pacienty. Pramipexol byl přidán ke stávající medikaci a pacienti byli sledováni po dobu 12 týdnů každé dva týdny; klinicky byli hodnoceni škálou HDRS-21 (Hamilton depression rating scale 21 – item version). Průměrná maximální dávka pramipexolu byla 1,6 mg. U 12 pacientů (71 %) došlo k redukci HDRS-21 o polovinu, z toho 10 pacientů (21 %) dosáhlo remisi (HDRS-21 < 8 na konci studie). Nevyskytly se žádné závažné nežádoucí účinky.
Randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie z roku 2013 od Cusin et al. zkoumala efektivitu a bezpečnost augmentace SSRI nebo SNRI pramipexolem u farmakorezistentní depresivní poruchy [14]. Do studie bylo zařazeno 60 pacientů ve věku 18–75 let s diagnózou těžké depresivní epizody bez psychotických příznaků (MDD podle DSM-IV). Polovině pacientů bylo podáno placebo a druhé polovině pramipexol. Farmakorezistence byla v této studii definována jako přetrvávající deprese (MADRS ≥ 18) navzdory léčbě minimálně jedním antidepresivem v dostatečné dávce po dostatečně dlouhou dobu při aktuální depresivní fázi. Počáteční dávka pramipexolu byla 0,25 mg, cílová dávka při dobré toleranci byla 1,5 mg. Studie trvala 8 týdnů. Za odpověď na léčbu byl považován pokles MADRS o polovinu, za remisi hodnota MADRS ≤ 10 na konci studie. Během studie se nevyskytly žádné žávažné nežádoucí účinky. Při analýze lineárním smíšeným modelem v této studii vychází efektivita pramipexolu statisticky významná oproti placebu (p = 0,038).
Z dalších studií lze zmínit malou randomizovanou studii na pacientech s depresivní poruchou, u nichž selhala léčba SSRI. V ní bylo 39 pacientů randomizováno do tří ramen: monoterapie pramipexolem, kombinace citalopramu a pramipexolu a monoterapie citalopramem. Pacienti léčení pouze pramipexolem vykazovali signifikantně vyšší redukci symptomatologie měřené škálou MADRS než pacienti s kombinovanou terapií; jiné porovnání nebylo statisticky významné. Zajímavým pozorováním bylo, že pacienti s kombinovanou terapií tolerovali přírůstky dávky pramipexolu při jeho titraci hůře než pacienti s monoterapií (pouze 15 % oproti 45 % v rameni monoterapie) a v tomto rameni byl pozorován také největší drop-out (69 % oproti 15 % v obou zbývajících ramenech) [20].
Nejen klinické, ale i funkční zlepšení při augmentaci léčby pramipexolem popisuje observační studie z roku 2022 na 116 pacientech s farmakorezistentní depresivní epizodou u MDD (32 %) a BAP (62 %). Celkem 24 týdnů po zahájení léčby dosahovala míra responze 74,1 % a remise 66,4 %. Dále bylo sledováno signifikantní funkční zlepšení sledované škálou GAF (Global Assessment of Functioning) průměrně z 53 na 80 bodů [21].
Retrospektivní práce z roku 2016 zahrnuje 42 pacientů s farmakorezistentní depresivní epizodou (24 s depresivní poruchou, 18 s bipolární afektivní poruchou), vč. 8 pacientů, u nichž selhala terapie ECT. Celkem 20 (47,6 %) pacientů dosáhlo remise (vč. 4 pacientů, u kterých byla neúčinná ECT), 12 odpovědělo na léčbu (28,6 %). Těchto 32 respondérů bylo dále sledováno až 15,8 měsíce při trvající terapii pramipexolem, přičemž pouze u dvou byl popsán relaps depresivní poruchy. Autoři dále vyzdvihují nutnost úpravy titračních schémat podle individuální snášenlivosti a doplňují pozorování, že intolerance se nejčastěji vyskytuje v úvodu léčby (3–10 den) [22].
Údaje k těmto prvním studiím jsou shrnuty v tab. 2.
Metaanalýza z roku 2017 provedená Szmulewiczem et al. se zaměřila na bezpečnost a efektivitu dopaminergních látek v léčbě bipolární deprese. Jednalo se o modafinil, armodafinil, pramipexol, methylfenidát a amfetamin [20]. Do metaanalýzy bylo zařazeno devět randomizovaných, dvojitě zaslepených studií, celkově se jednalo o 1 716 pacientů. Léčba těmito látkami byla asociována s vyšší mírou terapeutické odpovědi a s vyšší mírou dosažení remise, zároveň nebyla spojena s vyšším rizikem přesmyku do mánie.
Metaanalýza z roku 2023 od italských autorů Tundo et al. se zaměřila na výsledky observačních studií, které zkoumaly efektivitu a bezpečnost pramipexolu jako augmentaci u farmakorezistentní bipolární a unipolární deprese. Studie hodnotící účinnost monoterapie pramipexolem do této metaanalýzy nebyly zařazeny. Do analýzy bylo zahrnuto 8 studií, celkově 281 pacientů, 60 % mělo diagnózu MDD, ostatní diagnózu bipolární deprese. Celková odpověď na léčbu byla 62,5 %, remise dosáhlo 48,1 % pacientů bez významného rozdílu mezi pacienty s unipolární a bipolární depresí. Nejčastějšími nežádoucími účinky byla nauzea a ospalost. K rozvoji mánie došlo u celkově 1,1 % pacientů [23].
V zatím poslední randomizované kontrolované studii u pacientů s farmakorezistentní depresí na 150 pacientech randomizovaných do dvou ramen (stávající medikace s pramipexolem oproti stávající medikaci s placebem), byla prokázána signifikantní redukce depresivní symptomatologie na škále QIDS-SR16 (16položková sebehodnoticí verze škály Quick Inventory of Depressive symptomatology) po 12 týdnech léčby (Cohenovo d = 0,78, což odpovídá horní hranici střední velikosti účinku). 20 % pacientů v aktivní větvi studii ukončilo předčasně pro nežádoucí účinky konzistentní se známými nežádoucími účinky pramipexolu (nauzea, bolest hlavy, narušení spánku a somnolence) [24].
Kazuistiky
V následující části bude popsána čtveřice pacientů hospitalizovaných pro depresivní epizodu, u kterých byla využita off-label léčba pramipexolem.
Ve všech případech se jednalo o pacienty, u nichž byla přítomna těžká depresivní epizoda bez psychotických příznaků a u kterých byla konstatována farmakorezistence. Titrace pramipexolu probíhala dle SPC [10]. Případné nežádoucí účinky byly monitorovány v rámci pravidelných vizit při standardním režimu uzavřeného oddělení. Všichni pacienti udělili písemný souhlas s využitím anonymizovaných údajů pro publikační účely.
Základní informace o pacientech a terapii pramipexolem jsou shrnuty v tab. 3.
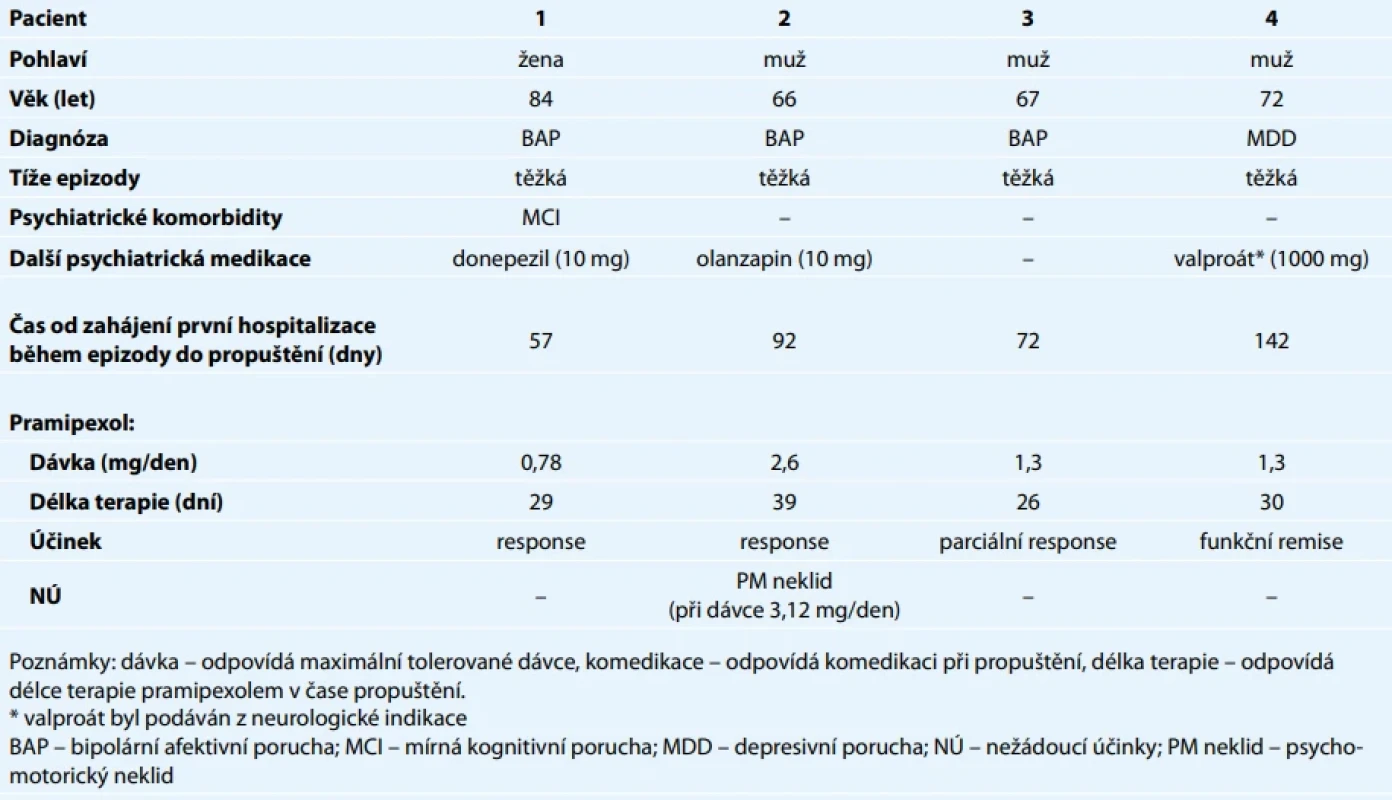
Kazuistika 1
První pacientkou byla 84letá žena s diagnózou bipolární afektivní poruchy. Jednalo se o polymorbidní pacientku. Nejvýznamnější diagnózy zahrnovaly chronické srdeční selhání, ischemickou chorobu srdeční, chronickou renální insuficienci a metabolický syndrom. Pacientka měla také onkologickou anamnézu: v 55 letech absolvovala thyreoidektomii pro karcinom štítné žlázy a v 71 a 75 letech také operační zákroky a chemoterapii pro karcinom ovaria. Při došetřování možných metastáz byly na magnetické rezonanci (MR) mozku zachyceny dva meningeomy, byla popsána difuzní mozková atrofie a postischemická leukoencefalopatie.
Pacientka byla vyučená pekařka, v minulosti pracovala jako vedoucí prodejny. V čase hospitalizace byla ve starobním důchodu. Byla již téměř 60 let vdaná a měla dospělého syna.
Pacientka byla psychiatricky léčena od svých 30 let. Hospitalizovaná byla více než 20×, vesměs pod obrazem těžké depresivní fáze s apaticko-abulickým syndromem. V průběhu let byla léčena kombinací antidepresiv augmentovanou antipsychotiky i stabilizátory nálady. V posledních 20 letech medikace zahrnovala různé kombinace léčiv: tricyklická antidepresiva (dosulepin, nortriptylin), SSRI, venlafaxin, mirtazapin, quetiapin a pregabalin. Pro farmakorezistenci byla opakovaně použita také elektrokonvulzivní terapie, a to jak v rámci akutní léčby, tak ve formě udržovací ECT. Délky remise se zprvu pohybovaly v rozsahu 5 let, postupně se ale zkracovaly. Jako závažné precipitující faktory relapsů byly zvažovány recidivy tumoru ovaria. Poslední předchozí hospitalizace proběhla před 4 lety a byla komplikována rozvojem mikromanické bludné produkce s restrikcí stravy a tekutin.
Popisovaná hospitalizace byla indikována pro relaps depresivní symptomatologie. Při příjmu byl v klinickém obraze patrný plně vyjádřený depresivní syndrom s apatií, abulií a psychomotorickou retardací. Stávající medikace – kombinace quetiapinu, vortioxetinu a valproátu – byla změněna na off-label lurasidon v kombinaci s bupropionem a agomelatinem, avšak bez zjevného klinického účinku. Dále byl podáván donepezil, a to pro kognitivní deficit popisovaný již před hospitalizací. ECT bylo zamítnuto pro riziko komplikací při četných komorbiditách.
Jako terapeutický pokus byl tedy nasazen off-label pramipexol, postupně v dávce až 0,78 mg/den, ostatní psychiatrická medikace, vyjma donepezilu, byla vysazena. Nežádoucí účinky pramipexolu nebyly pozorovány. Na této medikaci došlo ke klinicky významnému ústupu depresivní symptomatologie, i když nadále přetrvávala subdepresivní nálada. Z psychiatrického hlediska mohla být pacientka propuštěna, nicméně pro subkompenzaci chronického srdečního selhání a renální insuficience přítomné po celou dobu hospitalizace byla pacientka přeložena do zařízení následné péče.
Kazuistika 2
Druhým pacientem byl 66letý muž v dlouhodobé psychiatrické péči pro bipolární afektivní poruchu. Somaticky se léčil s hypertenzí, v minulosti prodělal hlubokou žilní trombózu dolní končetiny. Stran psychiatrické heredity se jeho dcera léčila se schizofrenií. Pacient byl v invalidním důchodu z psychiatrické indikace, v minulosti pracoval jako sazeč. Byl ženatý a bydlel v rodinném domě s manželkou a dětmi.
Psychiatricky byl léčen od svých 44 let, kdy se u něj rozvinula depresivní a následně hypomanická symptomatologie. V průběhu následujících let pacient absolvoval čtyři hospitalizace se zkracujícími se obdobími uspokojivého stavu (7 let, 5 let, 3 roky a 1 rok). Medikace zahrnovala mirtazapin, venlafaxin, amitriptylin a valproát. Pro farmakorezistentní depresivní epizody byl opakovaně léčen ECT, obvykle s dobrým efektem, ale také s mnestickými poruchami.
Při popisované hospitalizaci po dalším roce byl pacient opět přijat pro rozvoj těžké depresivní epizody. V klinickém obraze dominovalo zpomalené psychomotorické tempo, apatie, anhedonie, abulie. Neúspěšné terapeutické pokusy zahrnovaly postupně venlafaxin, vortioxetin, vortioxetin augmentovaný quetiapinem a posléze olanzapinem. Pro farmakorezistenci byla provedena vyšetření v rámci diferenciální diagnostiky – EEG, MR mozku (s nálezem mnohočetných hyperintenzit v bílé hmotě paraventrikulárně a subkortikálně) a Addenbrookský kognitivní test (87/100 bodů).
Pacient odmítal doporučované ECT, a tak bylo přistoupeno k off-label medikaci pramipexolem při pokračující léčbě olanzapinem. Při titraci bylo dosaženo dávky 3,12 mg/den, na které došlo k rozvoji psychomotorického neklidu, proto byla dávka snížena na 2,6 mg/den. Na této dávce byl pozorován uspokojivý klinický účinek a po 3 měsících mohl být pacient propuštěn do ambulantní péče.
Kazuistika 3
V tomto případě se jednalo o 67letého muže, který byl od mládí v invalidním důchodu pro bipolární afektivní poruchu. Po somatické stránce se léčil s hypertenzí, hyperlipidemií a hypertrofií prostaty. Neměl žádnou známou psychiatrickou hereditu. V minulosti krátce pracoval jako sazeč. Bydlel v bytě v manželkou, děti neměl.
Na psychiatrickou kliniku byl pacient přijat s těžkou depresivní fází bez psychotických příznaků. V klinickém obraze bylo vedle depresivní nálady přítomno inhibované psychomotorické tempo, dále abulie, anhedonie, anxieta, hypoprosexie, autoakuzace, vágní suicidální myšlenky. Dále byla zaznamenána svalová rigidita na horních i dolních končetinách. EEG, MR mozku byly bez patologického nálezu.
V medikaci byl vysazen bupropion a fluoxetin, byl navýšen aripiprazol a přiordinován quetiapin, avšak bez zjevného klinického účinku. Pro zajímavost lze uvést, že i při standardních dávkách obou léčiv byly u pacienta zachyceny jejich vysoké plazmatické koncentrace. Dextrometorfanovým a kofeinovým testem bylo prokázáno, že pacient byl pomalý metabolizátor cytochromu CYP 2D6 a CYP 3A4.
Pacientovi byla navržena ECT, kterou ale odmítal. Dvacet sezení repetitivní transkraniální magnetické stimulace mělo pouze minimální efekt.
Dále byl tedy nasazen off-label pramipexol, postupně v dávce až 1,3 mg/den, který vedl ke zlepšení depresivní symptomatologie. Nežádoucí účinky nebyly sledovány. Po stránce somatické byla hospitalizace komplikována parciální flebotrombózou v. femoralis vpravo. Pacient si následně přál být propuštěn do domácího prostředí, čemuž bylo vyhověno.
Kazuistika 4
Posledním pacientem byl 72letý muž léčený pro periodickou depresivní epizodu.
Po somatické stránce se léčil s hypertenzí, hyperlipidemií, hyperplazií prostaty, prodělal hlubokou žilní trombózu v. fibularis vpravo. V rodinné anamnéze figurovala informace o suicidiu jeho strýce. Pacient měl vystudovanou teologickou fakultu a působil jako kněz.
První epizodu depresivní poruchy prodělal v 52 letech, byl hospitalizován a jeho stav se zlepšil na terapii venlafaxinem.
K relapsu došlo až po 20 letech. Následovala série hospitalizací, která byla komplikována psychiatricky i somaticky. V úvodu v klinickém obraze dominoval výrazný celkový bradypsychizmus. V medikaci byly učiněny pokusy s mirtazapinem, vortioxetinem, quetiapinem, aripiprazolem, lamotriginem a agomelatinem. Pro extrapyramidové nežádoucí účinky byl podáván biperiden. Hospitalizace však vyvrcholila výrazným zhoršením stavu – rozvojem mutizmu, negativizmu a desorientace. Na MR mozku provedené z diferenciálně-diagnostických důvodů byl nález starších postischemických změn mozkové kůry vpravo bazálně temporálně.
Dále byla zahájena ECT, která byla komplikována rozvojem dezorientace, restrikce stravy a tekutin při bilaterálním umístění elektrod (osm aplikací), což si vyžádalo změnu strategie na pravé unilaterální umístění (dalších 11 aplikací). V udržovací terapii byl podáván citalopram a off-label brexpiprazol a bylo rozhodnuto o zahájení pokračovací ECT. Nicméně již po následující hospitalizaci a další sérii devíti ECT bylo zjevné, že tato terapie má pouze částečný a přechodný efekt. Po dimisi navíc došlo k rozvoji epileptického paroxyzmu, proto byla ECT na doporučení neurologů ukončena.
Vzhledem k progresi hypokineticko-rigidního syndromu byl proveden DaT scan (scan dopaminového transportéru), kde byl lehce abnormální nález v oblasti levého striata, nicméně nález se nejevil jako typický pro Parkinsonovu nemoc. Pro neúčinnost byla veškerá psychiatrická medikace vysazena, byl ponechán jen valproát, který byl nasazen z neurologické indikace.
Vzhledem k vyčerpání ostatních terapeutických modalit byl do medikace zaveden pramipexol, který byl titrován do dávky 1,3 mg/den. Na této dávce nebyly pozorovány žádné nežádoucí účinky. Postupně došlo ke zlepšení hypokineticko-rigidního syndromu a k ústupu depresivní symptomatologie a pacient mohl být propuštěn.
Několik měsíců po hospitalizaci byl pacient v uspokojivém stavu po symptomatické i funkční stránce. Vrátil se např. ke svým pracovním povinnostem, vč. bohoslužeb.
Diskuze
V této práci bylo využití pramipexolu v léčbě depresivního syndromu demonstrováno na čtyřech pacientech, třech s bipolární afektivní poruchou (kazuistika 1–3) a jednom s periodickou depresivní poruchou (kazuistika 4). Ve všech případech se jednalo o seniory ve věku 66–84 let s těžkou depresivní epizodou a několika somatickými komorbiditami. Stav všech pacientů vyžadoval hospitalizaci na uzavřeném psychiatrickém oddělení a u všech byla v průběhu léčby konstatována farmakorezistence. Vzhledem k selhání jiných terapeutických modalit byla u těchto pacientů zahájena off-label léčba pramipexolem.
V našem souboru se toto léčivo jevilo jako relativně dobře účinné. Míra účinku se pohybovala od symptomatické i funkční remise (pacient 4) ke klinicky výraznému zlepšení při reziduální symptomatologii. Pramipexol byl až na jednu výjimku (pacient 2), podáván jako jediné léčivo s cílem ovlivnit depresivní symptomatologii: u pacientky 1 byl dále podáván donepezil a u pacienta 4 valproát, nicméně se v tomto případě jednalo o pacienta s unipolární depresí a antikonvulzivum bylo indikováno neurologem.
Vzhledem ke konstatované farmakorezistenci byla u pacientů před podáváním off-label medikace zvažována elektrokonvulzivní terapie. V prvním případě byla ECT zamítnuta vzhledem k věku a četným somatickým komorbiditám, pacienti z druhé a třetí kazuistiky ECT opakovaně odmítali a v posledním případě byla udržovací ECT ukončena pro výskyt epileptického paroxyzmu. Lze tedy usuzovat, že pramipexol může nalézt využití jako vhodná alternativa u pacientů, u kterých není ECT z různých příčin možná.
Ze symptomatického hlediska je vhodné zmínit, že všichni čtyři pacienti vykazovali příznaky odpovídající hypodopaminergnímu stavu – anhedonie, apatie, abulie, hypoprosexie, inhibované psychomotorické tempo. Toto pozorování je v souladu s hypotézou, že dopaminergní dysfunkce může hrát důležitou roli v patofyziologii některých příznaků deprese [4–8]. Potvrzuje tak i vhodnost individualizace terapie s ohledem na pozorované příznaky.
Dávkování pramipexolu se u našich pacientů pohybovalo v rozmezí 0,78–3,12 mg/den v tabletách s prodlouženým uvolňováním. To odpovídá dávkování v dostupných studiích, kde byla průměrná denní dávka pramipexolu 1,6 mg/den [14,18,19]. K dosažení dávky bylo použito obdobné schéma, jaké je doporučováno pro jiné diagnózy, tedy zahájit podávání na dávce 0,26 mg báze denně a každých 5–7 dní dávku zvyšovat až do dosažení účinku nebo nežádoucích účinků, při kterých má být dávka snížena na poslední tolerovanou dávku [25].
Většina pacientů z našeho souboru nevykazovala žádné nežádoucí účinky, u jednoho pacienta se při dávce 3,12 mg/den rozvinul psychomotorický neklid, který odezněl po snížení dávky. Opět je naše pozorování v souladu s dostupnými údaji z literatury, podle kterých pramipexol vykazuje dobrou snášenlivost. Podle metaanalýzy z roku 2023 byly nejčastějšími nežádoucími účinky nauzea a ospalost, k rozvoji mánie došlo celkem u 1,1 % pacientů [23].
Z hlediska farmakokinetického je vhodné zmínit pacienta 3, u kterého byla fenotypizací (dextromethophanovým a kofeinovým testem) zjištěna pomalá metabolizace přes CYP2D6 a 3A4. V tomto kontextu je výhodou pramipexolu skutečnost, že jeho metabolizmus na těchto cytochromových systémech nezávisí, a jeho farmakokinetika je tak u těchto pacientů stabilní a předvídatelná [15].
Hospitalizace byly protrahované, trvaly 2–3 měsíce a před nasazením pramipexolu pacienti užívali kombinaci tří až čtyř psychofarmak. U všech pacientů vedla terapie pramipexolem ke snížení počtu užívaných léků a zlepšení stavu, které umožnilo dimisi. U dvou pacientů sice přetrvávala subdepresivní nálada, oproti situaci před nasazením pramipexolu byly ale reziduální příznaky pouze mírné. U pacienta s periodickou depresivní poruchou dokonce došlo k natolik výraznému zlepšení stavu, že byl schopen se po dlouhé době opět zapojit do pracovního procesu. Vysoká míra účinnosti pramipexolu je zmiňována jak v dostupných studiích, tak v metaanalýzách [23,26]. V recentní open-label studii dokonce augmentace pramipexolem překonala augmentaci aripiprazolem v krátkodobé i dlouhodobé účinnosti, vč. funkčního zlepšení [27].
Závěr
Dosavadní výzkum i naše klinické zkušenosti naznačují, že pramipexol je účinným a bezpečným lékem v léčbě farmakorezistentní deprese. Zároveň se jedná o léčivo dobře snášené a s nízkou frekvencí výskytu nežádoucích účinků. I když jsou výsledky dosavadních prací slibné, je potřeba dalších randomizovaných, dvojitě zaslepených studií s větším počtem pacientů různých věkových skupin a s delší dobou ambulantního sledování, které potvrdí dlouhodobu účinnost a bezpečnost pramipexolu v léčbě deprese. Nicméně u pacientů s rezistentní depresí, obzvlášť s dominujícími symptomy hypodopaminergního typu, u kterých jiné léčebné režimy selhaly, je pramipexol slibná volba augmentace – za předpokladu pečlivého sledování nežádoucích účinků a individualizovaného dávkování.
Dedikace
Podpořeno projektem č. LX22NPO5107 (MŠMT): Financováno Evropskou unií – Next Generation EU a MZ ČR – RVO (FNBr, 65269705).
Sources
1. Rush JA, Trivedi MH, Wisniewski SR et al. Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report. Am J Psychiatry 2006; 163 (11): 1905–1917. doi: 10.1176/ajp.2006.163.11.1905.
2. Češková E, Šilhán P. Treatment options for pharmacoresistant depression in routine clinical practice. Psychiatr praxi 2020; 21 (3): 124–127.
3. Kellner CH, Greenberg RM, Murrough JW et al. ECT in treatment-resistant depression. Am J Psychiatry 2012; 169 (12): 1238–1244. doi: 10.1176/appi.ajp.2012.12050648.
4. Gold MS, Blum K, Febo M et al. Molecular role of dopamine in anhedonia linked to reward deficiency syndrome (RDS) and anti - reward systems. Front Biosci (Schol Ed) 2018; 10 (2): 309–325. doi: 10.2741/s514.
5. Dunlop BW, Nemeroff CB. The role of dopamine in the pathophysiology of depression. Arch Gen Psychiatry 2007; 64 (3): 327–337. doi: 10.1001/archpsyc.64.3.327.
6. Tremblay LK, Naranjo CA, Cardenas L et al. Probing brain reward system function in major depressive disorder: altered response to dextroamphetamine. Arch Gen Psychiatry 2002; 59 (5): 409–416. doi: 10.1001/archpsyc.59.5.409.
7. Tremblay LK, Naranjo CA, Graham SJ et al. Functional neuroanatomical substrates of altered reward processing in major depressive disorder revealed by a dopaminergic probe. Arch Gen Psychiatry 2005; 62 (11): 1228–1236. doi: 10.1001/archpsyc.62.11.1228.
8. Hori H, Kunugi H. Dopamine agonist-responsive depression. Psychogeriatrics 2013; 13 (3): 189–195. doi: 10.1111/psyg.12024.
9. Wilson SM, Wurst MG, Whatley MF, Daniels NR. Classics in Chemical Neuroscience: Pramipexole. ACS Chem Neurosci 2020; 11 (17): 2506–2512. doi: 10.1021/acschemneuro.0c00390.
10. Evropská léková agentura. Mirapexin: Souhrn údajů o přípravku. [online]. Dostupné z: https: //www.ema.europa.eu/en/documents/product-information/mirapexin-epar-product-information_en.pdf.
11. Kvernmo T, Härtter S, Burger E. A review of the receptor-binding and pharmacokinetic properties of dopamine agonists. Clin Ther 2006; 28 (8): 1065–1078. doi: 10.1016/j.clinthera.2006.08.004.
12. Newman-Tancredi A, Cussac D, Audinot V et al. Differential actions of antiparkinson agents at multiple classes of monoaminergic receptor. II. Agonist and antagonist properties at subtypes of dopamine D (2) -like receptor and alpha (1) /alpha (2) -adrenoceptor. J Pharmacol Exp Ther 2002; 303 (2): 805–814. doi: 10.1124/jpet.102.039867.
13. Drugbank. Pramipexole [online]. Dostupné z: https: //go.drugbank.com/drugs/DB00413.
14. Cusin C, Iovieno N, Iosifescu DV et al. A Randomized, double-blind, placebo-controlled trial of pramipexole augmentation in treatment-resistant major depressive disorder. J Clin Psychiatry 2013; 74 (7): 636–641. doi: 10.4088/JCP.12m08034.
15. Bennett, JP, Piercey MF. Pramipexole – a new dopamine agonist for the treatment of Parkinson’s disease. J Neurol Sci 1999; 163 (1): 25–31. doi: 10.1016/S0022-510X (98) 00316-8.
16. Martens MAG, Kaltenboeck A, Halahakoon DC et al. An experimental medicine investigation of the effects of subacute pramipexole treatment on emotional information processing in healthy volunteers. Pharmaceuticals (Basel) 2021; 14 (8): 800.
17. Corrigan MH, Denahan AQ, Wright CE et al. Comparison of pramipexole, fluoxetine, and placebo in patients with major depression. Depress Anxiety 2000; 11 (2): 58–65. doi: 10.1002/ (SICI) 1520-6394 (2000) 11 : 2<58:: AID-DA3>3.0.CO; 2-H.
18. Goldberg JF, Burdick KE, Endick CJ. Preliminary randomized, double-blind, placebo-controlled trial of pramipexole added to mood stabilizers for treatment-resistant bipolar depression. Am J Psychiatry 2004; 161 (3): 564–566. doi: 10.1176/appi.ajp.161.3.564.
19. Hori H, Kunugi H. The efficacy of pramipexole, a dopamine receptor agonist, as an adjunctive treatment in treatment-resistant depression: an open-label trial. ScientificWorldJournal 2012; 2012 (6): 372474. doi: 10.1100/2012/372474.
20. Franco-Chaves JA, Mateus CF, Luckenbaugh DA et al. Combining a dopamine agonist and selective serotonin reuptake inhibitor for the treatment of depression: a double-blind, randomized pilot study. J Affect Disord 2013; 149 (1–3): 319–325. doi: 10.1016/j.jad.2013.01.040.
21. Tundo A, Betró S, Iommi M, de Filippis R. Efficacy and safety of 24-week pramipexole augmentation in patients with treatment resistant depression. A retrospective cohort study. Prog Neuropsychopharmacol Biol Psychiatry 2022; 10 (112): 110425. doi: 10.1016/j.pnpbp.2021.110425.
22. Fawcett J, Rush AJ, Vukelich J et al. Clinical experience with high-dosage pramipexole in patients with treatment-resistant depressive episodes in unipolar and bipolar depression. Am J Psychiatry 2016; 173 (2): 107–111. doi: 10.1176/appi.ajp.2015.15060788.
23. Tundo A, Betro S, De Filippis R et al. Pramipexole augmentation for treatment-resistant unipolar and bipolar depression in the real world: a systematic review and meta-analysis. Life 2023; 13 (4): 1043. doi: 10.3390/life13041043.
24. Browning M, Cowen PJ, Galal U et al. Pramipexole augmentation for the acute phase of treatment-resistant, unipolar depression: a placebo-controlled, double-blind, randomised trial in the UK. Lancet Psychiatry 2025; 12 (8): 579–589. doi: 10.1016/S2215-0366 (25) 00152-5.
25. Lindhani J, Asp M, Ståhl D et al. Add-on pramipexole for anhedonic depression: study protocol for a randomised controlled trial and open-label follow-up in Lund, Sweden. BMJ Open 2023; 13: e076900. doi: 10.1136/bmjopen-2023-076900.
26. Szmulewicz AG, Angriman F, Samamé C et al. Dopaminergic agents in the treatment of bipolar depression: a systematic review and meta-analysis. Acta Psychiatr Scand 2017; 135 (6): 527–538. doi: 10.1111/acps.12723.
27. Tundo A, Betrò S, de Filippis R et al. Comparative short - and long-term effectiveness and safety of pramipexole and aripiprazole augmentation in treatment-resistant unipolar depression: an observational study. Biomedicines 2024; 12 : 2064. doi: 10.3390/biomedicines12092064.
Labels
Addictology Paediatric psychiatry PsychiatryArticle was published in
Czech and Slovak Psychiatry

2026 Issue 2
- Hope Awakens with Early Diagnosis of Parkinson's Disease Based on Skin Odor
- Deep stimulation of the globus pallidus improved clinical symptoms in a patient with refractory parkinsonism and genetic mutation
- Memantine Eases Daily Life for Patients and Caregivers
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
-
All articles in this issue
- Příliš otevřené dveře? Proč jsou naše ambulance přeplněny klienty, kterým neumíme správně pomoci
- Smoking as a determinant of psychopharmacotherapy effectiveness
- Pramipexol v léčbě farmakorezistentní deprese
- Diagnosis and otherness – Emmanuel Lévinas’s thinking as an inspiration for contemporary psychiatric practice
- Psychiatrická klinika 1. LF UK a VFN v Praze otevřela nové Centrum denních stacionářů pro adolescenty a dospělé
- EPA 2026
- Když standardní léčba nestačí – ambulantní terapie depresivní poruchy přípravkem SPRAVATO®
- Czech and Slovak Psychiatry
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Příliš otevřené dveře? Proč jsou naše ambulance přeplněny klienty, kterým neumíme správně pomoci
- Když standardní léčba nestačí – ambulantní terapie depresivní poruchy přípravkem SPRAVATO®
- Smoking as a determinant of psychopharmacotherapy effectiveness
- Psychiatrická klinika 1. LF UK a VFN v Praze otevřela nové Centrum denních stacionářů pro adolescenty a dospělé
