-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Hyperbarická oxygenoterapie při léčbě dětí s neuroblastomem nejvyššího rizika – zkušenosti z období let 1997–2000
Hyperbaric Oxygenotherapy in Treatment of Children with Neuroblastoma of Highest Risk: Experience in 1997–2000
Treatment of highest risk neuroblastoma is problematic. 5 years overall survival is about 20%. Prognosis can be improved by administration of 131I MIBG. The advantage of this targeted tumour specific radiotherapy is the possibility of achievement 5–10 fold higher dose in comparison with external irradiation with less organ toxicity. 14 131I MIBG treatment applications were done in 7 patients with highest risk neuroblastoma in this period. Four children were given one administration, three children were given repetitive administrations. Out of these seven patients, three survived longer. 5.5 GBq was given within the first administration, 3.7 GBq in subsequent courses, irrespective of body weight, always followed by four days 100 minutes lasting hyperbaric oxygen therapy. Immediate tolerance of treatment was good. 131I MIBG treatment is well tolerated targeted irradiation enhanced by hyperbaric oxygen therapy.
Key words:
neuroblastoma, MIBG, hyperbaric oxygen therapy
Autori: P. Došel 1; M. Sázel 1; J. Staňková 2; P. Kavan 2; H. Křížová 2; P. Gajdoš 3
Pôsobisko autorov: Ústav leteckého zdravotnictví Praha, ředitel MUDr. Dušan Bartoš, CSc. 1; Klinika dětské onkologie FN Motol a 2. LF UK v Praze, přednosta Prof. MUDr. Jan Starý, DrSc. 2; Klinika nukleární medicíny FN Motol a 2. LF UK v Praze, přednosta Doc. MUDr. Petr Vlček, CSc. 3
Vyšlo v časopise: Pracov. Lék., 59, 2007, No. 1-2, s. 5-8.
Kategória: Původní práce
Súhrn
Terapie neuroblastomu nejvyššího rizika je přes široký léčebný přístup stále svízelná a pětileté přežití se pohybuje kolem 20 %. Prognózu je možné zlepšit terapeutickou aplikací metaiodobenzylguanidinu (131I MIBG). Výhodou této téměř cílené nádorově specifické radioterapie je možnost dosažení zhruba 5–10násobně vyšší dávky záření ve srovnání s externí radioterapií při nižší orgánové toxicitě. Terapeutická aplikace 131I MIBG byla provedena celkem čtrtnáctkrát sedmi nemocným s relapsem neuroblastomu vysokého rizika. U tří dětí byla aplikace opakována, čtyři ji podstoupily jedenkrát. Z těchto sedmi pacientů dlouhodobě žili tři. Poprvé bylo aplikováno 5,5 GBq, při opakované terapii 3,7 GBq 131I MIBG bez ohledu na hmotnost pacienta vždy s následnou hyperbarickou oxygenoterapií (4 dny po dobu 100 minut). Bezprostřední tolerance radiofarmaka byla dobrá. Terapeutická aplikace 131I MIBG je dobře tolerovatelná léčebná metoda, která představuje v podstatě cílenou radioterapii ve své účinnosti posílenou hyperbarickou oxygenoterapií.
Klíčová slova:
neuroblastom, MIBG, hyperbarická oxygenoterapieÚvod
Terapie neuroblastomu nejvyššího rizika je přes komplexní léčebný přístup stále problematická. Pouze 20 % nemocných přežívá 5 let. Pacienti s kombinací prognosticky nepříznivých biologických faktorů a relapsem onemocnění jsou prakticky nevyléčitelní. Neuroblastom je embryonální neurogenní nádor. Nádor je biologicky velmi variabilní – od spontánní regrese, benigního typu až po mimořádně agresivní typ. U dětí do 15 let se vyskytuje v 8 %. Prognosticky jsou nejvýznamnější faktory klinické (věk v době stanovení diagnózy, lokalizace primárního tumoru), biochemické (LDH, ferritin, NSE) a cytogenetické (obsah DNA, počet kopií genu MYCN a další). Kombinace prognosticky nepříznivých faktorů má za následek, že perspektiva vyléčení je mizivá. Průběh onemocnění je možné zlepšit terapeutickou aplikací 131I MIBG (metaiodobenzylguadinin). Literární údaje, publikované v pracích zejména holandských, italských a severoamerických autorů, prokazují úspěšnost této paliativní metody a byly podnětem k využití této metody i na našich pracovištích. Účinnost metody je zvýšena současným využitím hyperbarické oxygenoterapie (dále HBO).
Metodika a soubor pacientů
K terapii byli indikováni pacienti splňující následující kritéria:
- reziduální choroba po ukončení indukční a konsolidační fáze léčby,
- relaps nebo progrese choroby po myeoloablativní léčbě s autologní transplantací hematopoetických kmenových buněk,
- nedostatečná odpověď nebo progrese onemocnění v indukční fázi léčby neumožňující zařadit myeoloablativní režim,
- předpokládaná doba života delší 9 týdnů, odstup od předchozí chemoterapie a radioterapie delší 4 týdnů, počet trombocytů nad l00 x l09/l (při nižším počtu trombocytů je nutná redukce aplikované aktivity),
- pozitivní 123I/131I MIBG diagnostická scintigrafie,
- souhlas rodičů,
- věk nad 1 rok.
V období od dubna 1997 do dubna 2000 byl 131I MIBG terapeuticky podán celkem čtrnáctkrát sedmi nemocným: Čtyřem dívkám a třem chlapcům ve věkovém rozmezí 57–167 měsíců. Tři děti byly léčeny opakovaně, u čtyř šlo o jednorázovou aplikaci radiofarmaka. Primární tumor byl většinou retroperitoneálně lokalizovaný. U všech pacientů šlo o generalizované onemocnění (u 86 % metastázy ve skeletu). Mimo jednoho pacienta se ve všech případech jednalo o remisi onemocnění.
Léčebná strategie
Po stanovení diagnózy a prognostických faktorů byla zahájena intenzivní indukční kombinovaná chemoterapie a primární reziduum bylo po dosažení dřeňové remise nabídnuto k chirurgickému řešení nebo ošetřeno lokálním ozářením (25–30 Gy). Při následném relapsu nebo progresi choroby byl aplikován 131I MIBG a transplantovány hematopoetické kmenové buňky. Léčba byla kombinována s HBO.
Léčebná odpověď byla posuzována podle mezinárodních kritérií (INRC) stupnicí: kompletní remise (CR), velmi dobrá parciální remise (VGPR), parciální remise (PR), progrese onemocnění (DP). Detaily jsou uvedeny v tabulce 1.
Tab. 1. Klasifikace léčebné odpovědi (podle mezinárodních kritérií INRC) 
Terapie131I MIBG
Metaiodobenzylguanidin je syntetický analog norepinefrinu připravený v r. 1980 pro zobrazení tkání a nádoru neuroektodermového původu. MIBG má silnou afinitu ke dřeni nadledvin a adrenergní nervové tkáni. Fyziologicky se akumuluje ve slinných žlázách, myokardu, játrech a mírně v obsahu močového měchýře. Patologická distribuce MIBG znamená jeho akumulaci v místech výše uvedené fyziologické lokality. Difuzní akumulace v kostech je odrazem generalizované infiltrace kostní dřeně, ložisková je suspektní z metastatického postižení skeletu. MIBG akumuluje více než 90 % neuroblastomů. Specificita MIBG v detekci neuroblastomu se blíží 100 %.
131I MIBG je užíván k terapii neuroblastomu a feochromocytomu (méně často medulárního karcinomu štítné žlázy a karcinoidu). Užívá se 131I o vysoké specifické aktivitě (až 1,48 GBq . mg-1). Při první aplikaci se u dětí s neuroblastomem podává 5,55 GBq/150mCi/131I MIBG. Při dobré toleranci se dávka při druhé terapii nemění. Je-li hematologická toxicita významná (zejména trombocytopenie), je aktivita další léčby redukována na 3,7 GBq/150mCi/131I MIBG.
Hyperbarická oxygenoterapie
Třetí den po aplikaci 131I MIBG je zahajována hyperbarická oxygenoterapie(HBO) – obrázek 1. Léčebné schéma představují čtyři expozice v po sobě následujících dnech. Parametry expozice:
- Komprese na tlak 0,28 MPa v průběhu cca 12 min.
- Izokomprese s inhalací kyslíku po dobu 100 min.
- Dekomprese se zastávkami na 6 m a 3 m po dobu 5 min. a 10 min.
- Kyslík je podáván obličejovou maskou v množství 5–8 l. min-1, u nespolupracujících dětí kyslíkovou sprchou.
Obr. 1. Přetlaková komora Ústavu leteckého zdravotnictví 
V průběhu HBO jsme se u dětí ani rodičovského doprovodu nesetkali s žádnými obtížemi. Výjimkou byly mírné baroobtíže ve fázi komprese na počátcích léčby, kdy bylo nutno naučit děti vyrovnávat změny tlaku ve středoušní dutině. Kontaminace komory byla pravidelně monitorována.
Kombinovaná terapie: 131I MIBG + HBO
Na účinku kombinované terapie se podílejí následující faktory:
a) Defekt endogenních obranných mechanismů nádorových buněk proti účinkům kyslíkem derivovaných volných radikálů:
- redukce katalázové aktivity vedoucí k intracelulární akumulaci peroxidu vodíku,
- dvoj - až trojnásobné zvýšení intracelulární hladiny ferritinu. Ferritin je redukován superoxidovými radikály a dále reaguje s peroxidem vodíku na toxické hydroxylové radikály, které se podílejí na peroxidaci proteinů, lipidů a DNA.
b) HBO indukovaná zvýšená produkce intracelulárních volných kyslíkových radikálů.
c) Vyšší množství molekulárního kyslíku (navozené HBO) dostupného nádorovým buňkám v době iradiace zvyšuje jejich radiosenzitivitu.
d) MIBG indukovaná inhibice komplexu I. Tento komplex je situovaný na mitochondriálním respiračním řetězci. Důsledkem je opět zvýšená hladina intracelulárních volných superoxidových a hydroxylových radikálů.
e) Vlastní radioaktivní efekt beta složky 131I MIBG.
Výsledky
V období od dubna 1997 do ledna 2000 byl 131I MIBG terapeuticky podán celkem čtrnáctkrát sedmi nemocným, 4 dívkám a 3 chlapcům ve věkovém rozmezí 57–167měsíců, medián 89 měsíců, průměr 105 měsíců. Tři děti byly takto léčeny opakovaně, u čtyřech šlo o jednorázovou aplikaci radiofarmaka. Většina z nich byla v době terapie 131I MIBG v progresi choroby, pouze jedno přicházelo se stabilizovaným onemocněním ve velmi dobré parciální remisi. Dvě děti byly přijaty s vyloženě infaustní prognózou. V jednom případě bylo naším cílem dosahnout analgetického účinku terapie a ve druhém bylo vyhověno přání rodičů. U pacientky s mnohočetnými kostními metastázami bylo možno již během hospitalizace snížit dávky opiátu a zlepšila se hybnost končetin. Přesto však, obdobně jako u dalšího pacienta s difuzní infiltrací kostní dřeně, nastala další progrese onemocnění za 3, respektive 4 měsíce po terapii. Třetí, značně předléčený nemocný zemřel 10 měsíců po terapeutické aplikaci MIBG komplikacemi vysokodávkované chemoterapie, která byla indikována pro další relaps onemocnění. Opakovaná aplikace 131I MIBG radiofarmaka nebyla v jeho případě možná pro nízkou hodnotu glomerulární filtrace. Dvě děti žily bez známek aktivity onemocnění, z toho jedna pacientka v dlouhodobě kompletní remisi (47 měsíců po 1. terapii, celkem 5) a druhý nemocný 41 měsíců po 1. terapii. U další pacientky byl efekt terapeutické aplikace velmi dobrý, umožnila operabilitu primárního tumoru, celkem bylo možné uskutečnit 3 terapie, ale další podání MIBG bylo kontraindikováno vzhledem k renální insuficienci a dítě žilo s progresí choroby 38 měsíců od 1. aplikace. Rozsah onemocnění a prognostické faktory léčeného souboru jsou uspořádány v tabulce 2. Tabulka 3 přináší charakteristiku zdravotního stavu před aplikací radiofarmaka a důvody kontraindikace opakování terapie. Přehled výsledků léčby a charakteristika klinického stavu pacientů uvádí v tabulka 4.
Tab. 2. Rozsah onemocnění a prognostické faktory 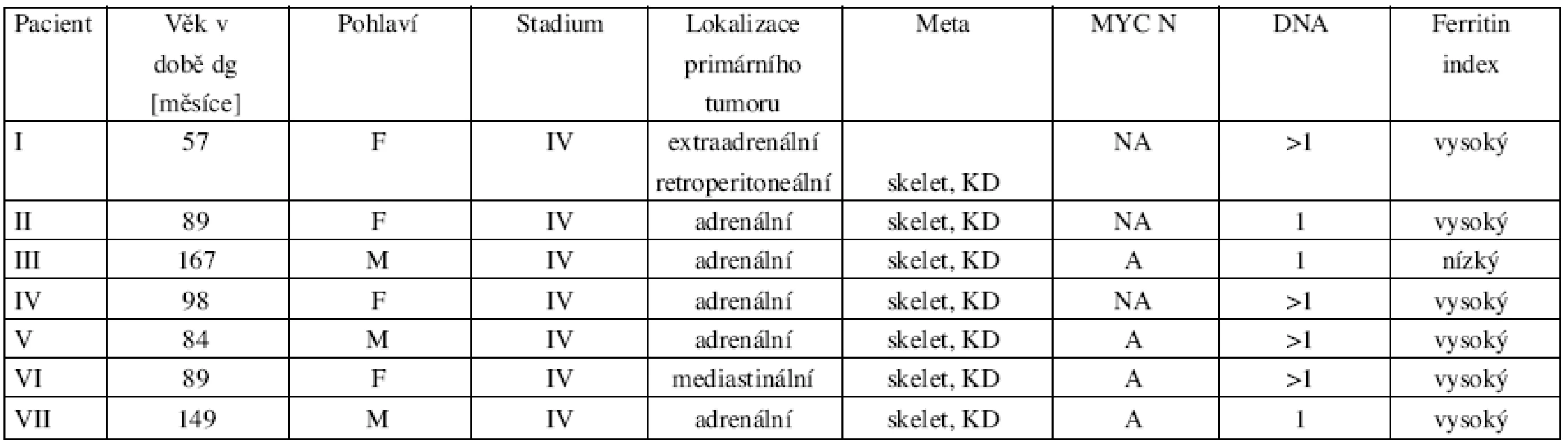
Tab. 3. Charakteristika souboru pacientů před a po MIBG terapii a důvodů kontraindikace další léčby radioizotopem 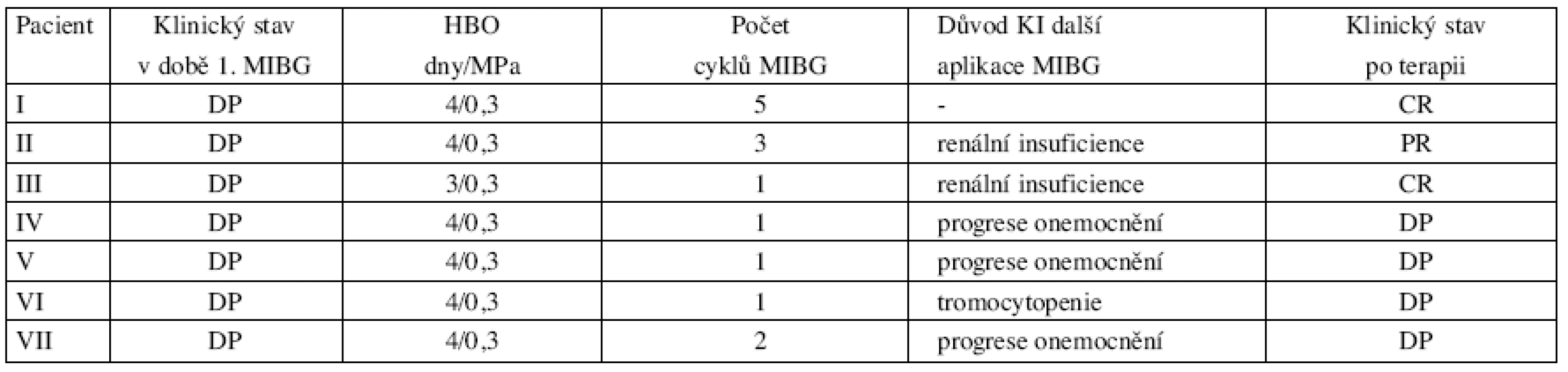
MIBG – metaiodbenzylguanidin Tab. 4. Přehled klinického stavu po aplikací jednotlivých terapeutických aktivit 
DP – disease progression; PR – partial regression; VGPR – very good partial regression; CR – complete regression Bezprostřední tolerance 131I MIBG terapie byla velmi dobrá. Během infuze radiofarmaka byl zaznamenán pouze u jedné pacientky vzestup krevního tlaku. Únava, nechutenství byly obvyklé nežádoucí účinky většinou 2. a 3. den po aplikaci. Ojediněle se vyskytla nauzea a zvracení. Nejzávažnějšími časnými nežádoucími účinky byl dřeňový útlum dosahující nejvýraznějšího stupně u pacientů s infiltrací kostní dřeně v době terapie či s rozsáhlou masou akumulující nádorové tkáně, zejména ve skeletu. Dominovala trombocytopenie. Leukopenie a anémie byly méně závažné. Infekční komplikace při neutropenii byly důvodem podávání baktericidních širokospektrých antibiotik u třech nemocných.
Závěr
- a) Ze sedmi pacientů postižených neuroblastomem dlouhodobě přežívaly tři děti, u kterých bylo dosaženo kompletní regrese nebo významné dílčí regrese. Tento terapeutický výsledek je vzhledem k závažnosti onemocnění velmi významný.
- b) Děti tolerují kombinovanou léčbu (respektive HBO) velmi dobře a ve srovnání s izolovanou aplikací 131I MIBG není vyšší časná ani pozdní toxicita.
- c) Dlouhodobé léčebné výsledky kombinované terapie: 131I MIBG + HBO (literární údaje) jsou statisticky významně lepší oproti samotné aplikaci radioizotopu.
- d) Soubor léčených dětí není doposud dostatečný k zobecnění výsledků terapie.
- e) Kombinovaná terapie 131I MIBG + HBO je dobře tolerovatelná paliativní léčebná metoda pro terapii dětí s neuroblastomem nejvyššího rizika. V této indikaci představuje vhodnou metodu k optimalizaci léčebné strategie a dává naději ke zlepšení prognózy onemocnění.
Poznámka: Odchodem Doc. Kavana, CSc., do zahraničí byla spolupráce přerušena a další terapie nepokračovala. Účelem článku je připomenout možný přínos HBO při léčbě onkologicky nemocných dětských pacientů. V současnosti již pracoviště přetlakové komory ÚLZ nemá oprávnění k práci s radioaktivními látkami.
Kontaktní adresa:
MUDr. Petr Došel
Ústav leteckého zdravotnictví
Gen. Píky 1
160 00 Praha 6
e-mail: petrdosel@atlas.cz
Zdroje
1. VOUTE, P. A., KRAKER DE, J., HOEFNAGEL, C. A. Tumours of the Sympathetic Nervous System: Neuroblastoma, Ganglioneuroma and Phacochromocytoma. In Cancer in Children. Clinical Management. 3rd edition. Eds. P. A. Voute, A. Barrett, J. Lemerle. Heidelberg : Spinger Verlag 1992.
2. BRODCUR, G. M., PRITCHARD, J., BERTOLD, F., CARLSEN, N. L., CASTEL, V. CASTLEBERRY, R. P. et al. Revisions of international criteria for neuroblastoma diagnosis, staging and response to treatment. J. Clin. Oncol., 1993, 11, s. 1466–1477.
3. GRAY, L. H., CONGER, A. D., EBERT, M., HORNSEY S., SCOTT O. C. A. The concentration of oxygen dissolved in tissues at the time of irradiation as a factor in radiotherapy. B. J. Radiol., 1953, 26, s. 638–648.
4. FUJIMURA, F. Experimental studies on radiations effects under high oxygen pressure. J. Osaka Dent. Univ., 1974, 19, s. 100–108.
5. HENK, J. H., SMITH, C., W. Radiotherapy and hyperbaric oxygen in head and neck cancer. Lancet, 1977, 2, 4, s.105.
6. NIAS, A., H., W. The oxygen problem in radiotherapy. In Colin, B. Seymour, Carmel, Mothersill (eds.) New Developments in Fundamental and Applied Radiobiology. Taylor & Francis Ltd. 4 Fohn St. London WCIN 2ET, 1991 s. 318–327.
Štítky
Hygiena a epidemiológia Hyperbarická medicína Pracovné lekárstvo
Článek Transkutánní oxymetrieČlánek Zdravotní prohlídky potápěčů
Článok vyšiel v časopisePracovní lékařství
Najčítanejšie tento týždeň
2007 Číslo 1-2- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- V ČR chybí specializovaná péče o pacienty s nervosvalovým onemocněním
-
Všetky články tohto čísla
- Přínos hyperbarické oxygenoterapie v komplexní terapii hypoxických postižení mozku nejrůznější etiologie u dětí a dospělých
- Monitorování srdeční frekvence při výcviku potápěčů
- Vznik oboru hyperbarická medicína a oxygenoterapie v České republice a jeho význam v současné humánní medicíně
- Pracovní lékařství a hyperbarická medicína
- Hyperbarický kyslík a diabetická noha
- K problematice Sudeckova syndromu
- Transkutánní oxymetrie
- Význam hyperbarické oxygenoterapie v léčbě nehojících se defektů
- Hyperbarická oxygenoterapie při léčbě dětí s neuroblastomem nejvyššího rizika – zkušenosti z období let 1997–2000
- Zdravotnická problematika potápění
- Zdravotní prohlídky potápěčů
- Perzistentní foramen ovale a potápění
- Životní jubilea MUDr. Vladimíra Doležala, CSc., a Doc. MUDr. Rudolfa Barcala, CSc.
- Osobnosti oboru hyperbarická medicína a oxygenoterapie
- Vzdělávací program v oboru hyperbarická medicína a oxygenoterapie
- Využití hyperbarické oxygenoterapie v traumatologii – výsledky léčby v roce 2005
- Pracovní lékařství
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- K problematice Sudeckova syndromu
- Přínos hyperbarické oxygenoterapie v komplexní terapii hypoxických postižení mozku nejrůznější etiologie u dětí a dospělých
- Zdravotní prohlídky potápěčů
- Transkutánní oxymetrie
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy


